ABSTRAK
IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA MERAH DALAM SAMPEL MINUMAN MENGGUNAKAN DETEKTOR EMISSION
SPECTROMETER DAN COLORIMETER
Telah dilakukan penelitian untuk identifikasi dan pengukuran konsentrasi jenis pewarna merah dalam sampel minuman menggunakan Detektor Emission Spectrometer dan Colorimeter buatan Vernier. Pewarna merah Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720, Carmoisine CI 14720, dan Ponceau 4R CI 16255 digunakan sebagai acuan. Identifikasi dilakukan berdasarkan pola serapan. Pola serapan sampel dibandingkan dengan pola serapan larutan standar pewarna merah. Pola serapan diperoleh menggunakan Detektor Emission Spectrometer. Detektor Emission Spectrometer merupakan detektor yang dirancang untuk mengukur intensitas dari berbagai sumber cahaya. Detektor bekerja pada panjang gelombang mulai dari 320 nm sampai dengan 900 nm dengan interval 1 nm. Pengukuran absorbansi dilakukan menggunakan Detektor Colorimeter. Detektor Colorimeter memiliki kemampuan untuk mengukur absorbansi dengan range 0,05 sampai 1,0 dan transmittans sampel dengan range 10% sampai 90%. Detektor Colorimeter bekerja dengan panjang gelombang cahaya 430 nm, 470 nm, 565 nm, dan 635 nm. Konsentrasi pewarna merah sampel diperoleh dari hasil analisa absorbansi sampel menggunakan persamaan grafik absorbansi pewarna merah standar terhadap kosentrasi pada panjang gelombang selektif dan sensitifnya.
ABSTRACT
THE IDENTIFICATION AND MEASUREMENT OF THE CONCENTRATION RED DYE IN SAMPLE USING EMISSION SPECTROMETER AND
COLORIMETER DETECTOR
The identification and measurement of the concentration red dye in sample using Emission Spectrometer and Colorimeter detector has been invetigated. Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720, Carmoisine CI 14720, dan Ponceau 4R CI 16255 red dye is used a reference. The identification is based on spectrum of absorbance. The absorbance spectrum is compared with the red dye standart absorbance spectrum. The absorbance spectrum is analyzed using spectrometer detector. The Emission Spectrometer is a portable spectrometer designed to measure the intensity of variety light sources. The Emission Spectrometer can work on 320–900 nm wavelength range with interval 1 nm. The absorbance is measured using Colorimeter detector. The Colorimeter has the ability to measure absorbance with 0,05-1,0 range absorbance and 10% - 90% range transmittance. The Colorimeter measures the amount of light transmitted through a sample at a user-selectable wavelength; 430 nm, 470 nm, 565 nm, 635 nm. The concentration of red dye samples is obtained from the analysis of the sample absorbance using graphing equations absorbance to concentration of standard red dye at the wavelength selective and sensitive.
i
IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA MERAH DALAM SAMPEL MINUMAN MENGGUNAKAN DETEKTOR
EMISSION SPECTROMETER DAN COLORIMETER SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Pendidikan
Program Studi Pendidikan Fisika
Oleh :
Cosmas Jerry Anggoro NIM: 121424016
PROGRAM STUDI PENDIDIKAN FISIKA
JURUSAN PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM
FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN UNIVERSITAS SANATA DHARMA
ii
iii
iv
LEMBAR PERSEMBAHAN
v
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Cosmas Jerry Anggoro
Nim : 121424016
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
“IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA MERAH DALAM SAMPEL MINUMAN MENGGUNAKAN DETEKTOR
EMISSION SPECTROMETER DAN COLORIMETER”
Dengan demikian saya memberikan kepada perpustakaan hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengolahnya dalam bentuk pangkalan data, mendistribusikannya secara terbatas dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya. Dilihat di Yogyakarta
Pada tanggal: 26 Agustus 2016 Yang menyatakan,
vii ABSTRAK
IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA MERAH DALAM SAMPEL MINUMAN MENGGUNAKAN DETEKTOR
EMISSION SPECTROMETER DAN COLORIMETER
Telah dilakukan penelitian untuk identifikasi dan pengukuran konsentrasi jenis pewarna merah dalam sampel minuman menggunakan Detektor Emission Spectrometer dan Colorimeter buatan Vernier. Pewarna merah Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720, Carmoisine CI 14720, dan Ponceau 4R CI 16255 digunakan sebagai acuan. Identifikasi dilakukan berdasarkan pola serapan. Pola serapan sampel dibandingkan dengan pola serapan larutan standar pewarna merah. Pola serapan diperoleh menggunakan Detektor Emission Spectrometer. Detektor Emission Spectrometer merupakan detektor yang dirancang untuk mengukur intensitas dari berbagai sumber cahaya. Detektor bekerja pada panjang gelombang mulai dari 320 nm sampai dengan 900 nm dengan interval 1 nm. Pengukuran absorbansi dilakukan menggunakan Detektor Colorimeter. Detektor Colorimeter memiliki kemampuan untuk mengukur absorbansi dengan range 0,05 sampai 1,0 dan transmittans sampel dengan range 10% sampai 90%. Detektor Colorimeter bekerja dengan panjang gelombang cahaya 430 nm, 470 nm, 565 nm, dan 635 nm. Konsentrasi pewarna merah sampel diperoleh dari hasil analisa absorbansi sampel menggunakan persamaan grafik absorbansi pewarna merah standar terhadap kosentrasi pada panjang gelombang selektif dan sensitifnya.
viii ABSTRACT
THE IDENTIFICATION AND MEASUREMENT OF THE CONCENTRATION RED DYE IN SAMPLE USING EMISSION
SPECTROMETER AND COLORIMETER DETECTOR
The identification and measurement of the concentration red dye in sample using Emission Spectrometer and Colorimeter detector has been invetigated. Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720, Carmoisine CI 14720, dan Ponceau 4R CI 16255 red dye is used a reference. The identification is based on spectrum of absorbance. The absorbance spectrum is compared with the red dye standart absorbance spectrum. The absorbance spectrum is analyzed using spectrometer detector. The Emission Spectrometer is a portable spectrometer designed to measure the intensity of variety light sources. The Emission Spectrometer can work on 320–900 nm wavelength range with interval 1 nm. The absorbance is measured using Colorimeter detector. The Colorimeter has the ability to measure absorbance with 0,05-1,0 range absorbance and 10% - 90% range transmittance. The Colorimeter measures the amount of light transmitted through a sample at a user-selectable wavelength; 430 nm, 470 nm, 565 nm, 635 nm. The concentration of red dye samples is obtained from the analysis of the sample absorbance using graphing equations absorbance to concentration of standard red dye at the wavelength selective and sensitive.
ix
KATA PENGANTAR
Puji syukur kepada Tuhan Yesus Kristus atas rahmat dan berkatNya yang begitu melimpah dan cinta yang begitu luar biasa. Berkat kasihNya yang luar biasa melimpah, penyusunan skripsi ini dapat terselesaikan dengan baik. Karena
cintanya pula skripsi yang berjudul “IDENTIFIKASI DAN PENGUKURAN
KONSENTRASI PEWARNA MERAH DALAM SAMPEL MINUMAN MENGGUNAKAN DETEKTOR EMISSION SPECTROMETER DAN COLORIMETER” dapat berjalan dengan baik dan terselesaikan dengan baik. Penelitian skripsi ini merupakan salah satu syarat guna memperoleh gelar sarjana pendidikan untuk Program Studi Pendidikan Fisika Fakultas Keguruan dan Ilmu pendidikan.
Penulisan dan penelitian ini bisa terselesaikan dengan baik bukan hanya karena penulis saja, melainkan banyak pihak yang senantiasa membantu serta memberi dukungan kepada penulis. Ucapan terimakasih yang begitu dalam diucapkan kepada :
1. Dr. Ign. Edi Santosa, M.S, selaku dosen pembimbing yang senantiasa dengan tulus hati membimbing, meluangkan waktu, memotivasi, mengarahkan, mendengarkan kesulitan yang dialami tentang penelitian ini serta memberikan solusi terbaiknya.
2. Petrus Ngadiono selaku laboran yang selalu membantu dalam pengadaan alat, memberi saran terhadap kesulitan dalam pemilihan alat.
3. Ibu Sri Agustini dan bapak Severinus Domi selaku DPA yang selalu membimbing dan memantau perkembangan skripsi mahasiswanya serta ucapan terimakasih untuk dosen-dosen Pendidikan Fisika atas segala bimbingannya dalam membantu kelancaran penelitian.
4. Dosen-dosen Pendidikan Fisika yang telah membantu saya dalam
perkuliahan selama 4 tahun ini.
5. Bapak dan Ibu tercinta dirumah, Ambrosius Sarjono dan Lusia Luveniasmi
yang selalu mendoakan serta memberikan kasih sayangnya dalam memberikan semangat dan dukungan kepada penulis.
6. Kakaku tercinta Dimas Adi Setiawan yang selalu mengingatkanku untuk pantang menyerah, memberikan pengalaman, dan memberikan dukungan serta motivasi.
7. Veronika Adventa Dewi yang telah memberi semangat untuk berjuang
menyelesaikan tugas akhir ini.
8. Sahabatku Gregorius Agung Rendra Prasastyo yang membantu memberi
x
9. Ignatius Mayo Aquino Pang dan Edward Arung, orang yang telah
menyediakan waktu untuk berdiskusi tentang penelitian.
10.Anastasia Susi Murwaningsih dan Timotius Vivid Nugroho sahabat
terbaik selama kuliah, memberi saran satu sama lain untuk memperbaiki penelitian ini maupun penelitian yang mereka kerjakan.
11.Blasius Trisna Hermawan, Bartolomius Delfian Wicaksono, Paskalis
seggrafiare, Fransiskus lima yang selalu menyemangati saya dan menjadi teman sekaligus sahabat terbaik saya.
12.
13.Teman Seperjuanganku yang selalu membantuku saat bimbingan yaitu
Natalia Peni Suharyanti dan Lusia Sandra Oey.
14.Teman-teman Pendidikan Fisika 2012 yang selalu saling mendukung,
mengingatkan serta memberikan semangat.
15.Angeline yang telah membantu dalam penyusunan abstrak dalam bahasa Inggris.
Penulis menyadari bahwa penulisan skripsi ini belum mencapai tahap yang sempurna. Untuk itu, kritik dan saran yang membangun akan diterima dengan senang hati penulis berharap skripsi ini bermanfaat bagi pembaca.
Yogyakarta, 26 Agustus 2016 Penulis
xi DAFTAR ISI
IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA MERAH DALAM SAMPEL MINUMAN MENGGUNAKAN DETEKTOR EMISSION SPECTROMETER DAN COLORIMETER . i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
LEMBAR PERSEMBAHAN ...iv
PERNYATAAN KEASLIAN KARYA ... v
... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ...vi
ABSTRAK ... vii
ABSTRACT ... viii
KATA PENGANTAR... ix
DAFTAR ISI ... xi
HALAMAN DAFTAR TABEL... xiii
HALAMAN DAFTAR GAMBAR ... xiv
HALAMAN DAFTAR LAMPIRAN ... xviii
BAB I ... 1
PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Rumusan Masalah ... 6
C. Batasan Masalah ... 7
D. Tujuan penelitian ... 7
E. Manfaat penelitian ... 8
F. Sistematika penulisan ... 9
BAB II ... 10
DASAR TEORI ... 10
A. Teori Atom ... 10
B. Teori Molekul ... 17
C. Hukum Beer-Lambert ... 18
xii
E. Colorimeter ... 22
F. Pewarna Merah ... 23
G. Teknik Pengenceran ... 25
BAB III ... 26
EKSPERIMEN ... 26
A. Persiapan Alat ... 26
B. Persiapan Bahan ... 31
C. Prosedur percobaan ... 34
D. Analisa Data ... 35
BAB IV ... 37
HASIL EKSPERIMEN DAN PEMBAHASAN ... 37
A. Hasil Eksperimen ... 37
1. Penentuan Pola Serapan Standar Pewarna Merah Eritrosine, Eritrosine-Carmoisine, Eritrosine-Carmoisine, dan Ponceau 4R. ... 37
2. Pengukuran Absorbansi Larutan Standar Perwana Merah Eritrosine, Eritrosine-Carmoisine, Eritrosine-Carmoisine, dan Ponceau 4R dengan Variasi Konsentrasi. ... 43
3. Hasil pengukuran sampel. ... 50
B. Pembahasan ... 58
BAB V ... 63
PENUTUP ... 63
A. Kesimpulan ... 63
B. Saran ... 64
DAFTAR PUSTAKA ... 65
xiii
HALAMAN DAFTAR TABEL
Tabel 4.1: Hubungan Absorbansi A terhadap konsentrasi C ( ml/L ) larutan
standar Carmoisine CI 14720 pada panjang gelombang 470 nm ... 44 Tabel 4.2 : Persamaan garis pada panjang gelombang 430 nm, 470 nm,
565 nm, dan 635 nm untuk pewarna merah Carmoisine CI 14720 ... 45 Tabel 4.3 : Persamaan garis pada panjang gelombang 430 nm, 470 nm,
565 nm, dan 635 nm untuk pewarna merah Eritrosine CI 16035 ... 48 Tabel 4.4 : Persamaan garis pada panjang gelombang 430 nm, 470 nm,
565 nm, dan 635 nm untuk pewarna merah Eritrosine CI
16035-Carmoisine CI 14720 ... 49 Tabel 4.5 : Persamaan garis pada panjang gelombang 430 nm, 470 nm,
565 nm, dan 635 nm untuk pewarna merah Ponceau 4R CI 16255 ... 49 Tabel 4.6 : Besar konsentrasi pewarna merah dalam sampel yang mengandung
Carmosine CI 14720. ... 58 Tabel 4.7 : Besar kosentrasi pewarna merah dalam sampel yang mengandung
xiv
HALAMAN DAFTAR GAMBAR
Gambar 2.1 : Interaksi inti dengan elektron ... 11
Gambar 2.2 : Peristiwa Deeksitasi ... 15
Gambar 2.3 : Peristiwa Eksitasi ... 16
Gambar 2.4 : Sketsa tingkat tenaga molekul : tingkat tenaga elektronik, tingkat
tenaga vibrasi, dan tingkat tenaga rotasi ... 17
Gambar 2.5 : Proses serapan yang terjadi ketika cahaya datang menuju suatu
sampel ... 19
Gambar 2.6 : Bagan analisa kualitatif menggunakan detektor Emission Spectrometer .. 21
Gambar 2.7 : Struktur kimia pewarna Eritrosine CI 16035 ... 24
Gambar 2.8 : Struktur kimia pewarna Carmoisine CL 14720 ... 24
Gambar 2.9 : Struktur kimia pewarna Ponceau 4R CI 16255 ... 24
Gambar 3.1 : Susunan alat eksperimen untuk mengidentifikasi pewarna merah
dalam sampel ... 27
Gambar 3.2 : Susunan alat eksperimen untuk menentukan konsentrasi pewarna
merah minuman dalam sampel ... 30
Gambar 4.1 : Grafik hubungan Intensitas terhadap panjang gelombang (nm)
larutan standar Eritrosine CI 16035 pada konsentrasi 10 ml/l,
8 ml/l, 6 ml/l, 4 ml/l, dan 2 ml/l ... 38
Gambar 4.2 : Grafik hubungan Intensitas terhadap panjang gelombang (nm)
larutan standar Eritrosine CI 16035-Carmoisine CI 14720 pada
xv
Gambar 4.3: Grafik hubungan Intensitas terhadap panjang gelombang (nm)
larutan standar Carmoisine CI 14720 pada konsentrasi 10 ml/l,
8 ml/l, 6 ml/l, 4 ml/l, dan 2 ml/l ... 39
Gambar 4.4 : Grafik hubungan Intensitas terhadap panjang gelombang (nm)
larutan standar Ponceau 4R CI 16255 pada konsentrasi 10 ml/l,
8 ml/l, 6 ml/l, 4 ml/l, dan 2 ml/l ... 40
Gambar 4.5 : Grafik hubungan Intensitas terhadap panjang gelombang (nm)
larutan standar Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine
CI 14720, Carmoisine CI 14720, dan Ponceau 4R CI 16255 pada konsentrasi 8ml/l. ... 41
Gambar 4.6 : Grafik hubungan Intensitas terhadap panjang gelombang (nm)
larutan standar Tartrasine CI 19410 pada konsentrasi 8 ml/l. ... 42
Gambar 4.7 : Grafik hubungan Intensitas terhadap panjang gelombang (nm)
larutan standar Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine
CI 14720, Carmoisine CI 14720, dan Ponceau 4R CI 16255 pada konsentrasi 8 ml/l dan larutan standar Tartrasine CI 19410 pada
konsentrasi 8 ml/l ... 42
Gambar 4.8 : Grafik Hubungan Absorbansi terhadap konsentrasi (ml/l) pada
panjang gelombang 470 nm untuk larutan standar Carmoisine
CI 14720 ... 44
Gambar 4.9 : Grafik Hubungan Absorbansi terhadap konsentrasi (ml/l) pada
xvi
larutan standar Carmoisine CI 14720 ... 45
Gambar 4.10 : Grafik Hubungan Absorbansi terhadap konsentrasi (ml/l) pada
panjang gelombang 430 nm, 470 nm, 565 nm, dan 635 nm untuk
larutan standar Eritrosine CI 16035 ... 47
Gambar 4.11 : Grafik Hubungan Absorbansi terhadap konsentrasi (ml/l) pada
panjang gelombang 430 nm, 470 nm, 565 nm, dan 635 nm untuk larutan standar Eritrosine CI 16035-Carmoisine CI ... 47
Gambar 4.12 : Grafik Hubungan Absorbansi terhadap konsentrasi (ml/l) pada
panjang gelombang 430 nm, 470 nm, 565 nm, dan 635 nm untuk larutan standar Ponceau 4R CI ... 48
Gambar 4.13 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
sampel minuman Panter pada konsentrasi x ml/l ... 50
Gambar 4.14 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
sampel minuman Panter pada konsentrasi x ml/l, 8/10x ml/l ... 51
Gambar 4.15 : Grafik Perbandingan Hubungan Intensitas terhadap panjang gelombang (nm) larutan standar Carmoisine CI 14720dengan konsentrasi 10 ml/L, 8 ml/L, 6 ml/L, 4 ml/L, dan 2 ml/L dengan sampel minuman panter pada konsentrasi x ml/l, 8/10x ml/ l ... 52
Gambar 4.16 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
sampel minuman Fanta pada konsentrasi x ml/l, 8/10x ml/l ... 54
Gambar 4.17 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
sampel minuman Sirup Freiss pada konsentrasi x ml/l, 8/10x ml/l .... 54
xvii
sampel minuman sirup Nikisari pada konsentrasi x ml/l, 8/10x ml/l . 55
Gambar 4.19 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
sampel Pamela 1 pada konsentrasi x ml/l, 8/10x ml/l ... 55
Gambar 4.20 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
sampel Pamela 2 pada konsentrasi x ml/l, 8/10x ml/l ... 56
Gambar 4.21 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
sampel USD 1 pada konsentrasi x ml/l, 8/10x ml/l ... 56
Gambar 4.22 : Grafik Hubungan Intensitas terhadap panjang gelombang (nm)
xviii
HALAMAN DAFTAR LAMPIRAN
Lampiran 1 : Tabel hubungan Intensitas terhadap panjang gelombang (nm) untuk larutan standar pewarna merah Carmoisine CI 14720 pada konsentrasi 10 ml/L, 8 ml/L, 6ml/L, 4 ml/L, dan 2 ml/L.
Lampiran 2 : Tabel hubungan Intensitas terhadap panjang gelombang (nm) larutan standar Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720, Carmoisine CI 14720, dan Ponceau 4R CI 16255 pada konsentrasi 8 ml/l dan larutan standar Tartrasine CI 19410pada konsentrasi 8 ml/l.
Lampiran 3 : Tabel Perbandingan Hubungan Intensitas terhadap panjang gelombang (nm) larutan standar Carmoisine CI 14720 dengan konsentrasi 10 ml/L, 8 ml/L dengan sampel minuman panter pada konsentrasi x ml/l, 8/10x ml/l.
1 BAB I PENDAHULUAN A. Latar Belakang
Fisika adalah ilmu yang mempelajari tentang gejala alam. Fisika
berhubungan dengan pengamatan, pemahaman, dan dugaan fenomena
alam termasuk sifat-sifat sistem buatan manusia [Gadgrave, 2009]. Fisika
mempelajari perilaku dan sifat materi atau benda dalam bidang yang
sangat beragam, mulai dari partikel submikroskopis hingga perilaku materi
alam semesta sebagai satu kesatuan kosmos. Fisika merupakan ilmu dasar
atau fundamental karena hukum fisika diterapkan di cabang ilmu lain
seperti kimia yang mempelajari jenis materi tertentu. Suatu zat kimia yang
ditentukan oleh sifat molekul penyusunnya dapat dijelaskan dengan ilmu
fisika. Salah satu contohnya adalah keberadaan molekul dalam pewarna
makanan dan minuman.
Warna minuman tergantung molekul-molekul penyusun dari pewarna
yang digunakan. Minuman berwarna hijau dapat dihasilkan dengan
menggunakan pewarna Tartrazine CI 19140, kuning menggunakan Kuning
kuinolin CI 47005, biru menggunakan Biru berlian FCF CI 42090,
sedangkan untuk warna merah dapat menggunakan Citrus Red CI 12156,
Rhodamine B 45170, Eritrosine CI 16035, Eritrosine CI
16035-Carmoisine CI 14720, 16035-Carmoisine CI 14720, Ponceau 3R 16155, Ponceau
SX 14700, dan Ponceau 4R CI 16255 [Menkes RI, 1998]. Pewarna
minuman beredar luas di pasar, namun masyarakat tidak bisa mengetahui
2
pewarna tersebut bisa saja membahayakan kesehatan, misalnya alergi,
asma, kerusakan sistem urin, bahkan memicu kanker. Pemerintah telah
menetapkan pewarna minuman merah yang diperbolehkan terbuat dari
Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720,
Carmoisine CI 14720, dan Ponceau 4R CI 16255 [Wenninger et all, 2000;
Menkes RI, 1998].
Pewarna merah dalam minuman dapat diketahui jenis dan
konsentrasinya dengan melakukan penelitian. Penelitian dikatakan ideal
bila alat yang digunakan mampu membedakan molekul pewarna merah
satu dengan lainnya. Alat dapat memastikan bahwa molekul yang diteliti
merupakan pewarna merah jenis tertentu, bukan molekul lain. Selain itu,
alat memiliki kepekaan dan tidak mengubah kondisi sampel yang diukur.
Hal ini mempengaruhi ketepatan hasil pengukuran pewarna merah yang
diperoleh. Oleh karena itu, dibutuhkan instrumen yang selektif dan sensitif
agar mengurangi gangguan saat pengukuran [Doebelin, 1992].
Penelitian untuk mengetahui jenis larutan dalam suatu sampel telah
dilakukan sebelumnya, yaitu pengukuran rotasi optik spesifikasi larutan
glukosa, fruktosa, dan laktosa dengan menggunakan polarimeter.
Polarimeter merupakan alat yang bekerja berdasarkan prinsip polarisasi
cahaya. Laser HeNe digunakan sebagai sumber cahaya. Beam Spliter
merupakan pemecah berkas untuk menghasilkan dua berkas cahaya dari
satu sumber cahaya. Penelitian ini menunjukkan bahwa besarnya
3
[Atmajati, 2014]. Pengukuran acuan dan sampel dilakukan secara
bersamaan. Penelitian ini terbatas pada larutan yang berifat optis aktif.
Pengukuran sudut rotasi optik sangat tergantung pada keadaan lingkungan
seperti suhu dan cahaya yang digunakan. Selain itu, pengaruh panjang
gelombang cahaya terhadap sudut rotasi optik belum dilakukan penelitian
lebih lanjut.
Penelitian untuk pengukuran konsentrasi Carmosine CI 14720 dalam
minuman menggunakan UV-Vis Spektrofotometer SP8-400 telah
dilakukan. Panjang gelombang selektif optimal yang digunakan untuk
mengukur nilai konsentrasi carmoisine dalam sampel adalah 515 nm.
Analisa kualitatif penelitian ini membandingkan grafik absorbansi sampel
terhadap panjang gelombang dengan grafik absorbansi carmoisine
terhadap panjang gelombang. Analisa kuantitatif berdasarkan persamaan
grafik absorbansi terhadap kosentrasi carmoisine untuk menentukan nilai
konsentrasi sampel. Penelitian ini menggunakan detektor PMT (Photo
Multiplyer Tube). Detektor PMT merupakan tabung pengganda fotoelektron yang terlepas dari katoda hasil penembakan dengan cahaya
monokromatis. Amplifier memperkuat dan mengubah elektron yang
sampai ke anoda menjadi arus listrik [Sasmoko, 2001]. Penelitian ini
terbatas pada pewarna merah carmoisine. Analisa kualitatif pada penelitian
ini berdasarkan grafik hubungan absorbansi terhadap konsentrasi
4
Penelitian berbasis komputer telah banyak dilakukan, antara lain
pengukuran konstanta dielektrikum kertas menggunakan bantuan Software
LogerPro [Murwaningsih dan Santosa, 2015], pengukuran gaya interaksi antar dipol magnet dengan Software LogerPro [Arung dan Santosa, 2015],
dan pengukuran medan magnet di sekitar kumparan berarus listrik
menggunakan Software LogerPro [Anggoro dan Santosa, 2015]. Software
Loger Pro dilengkapi dengan berbagai program terkait dengan hukum-hukum fisika bahkan pada bidang ilmu yang lain seperti kimia dan biologi.
Software LogerPro juga dilengkapi dengan fasilitas fitting data yang mempermudah peneliti dalam pengambilan dan analisa data.
Detektor Vernier Colorimeter adalah detektor yang digunakan untuk
menentukan konsentrasi dengan analisis intensitas cahaya buatan vernier.
Detektor Colorimeter dilengkapi sumber cahaya dengan empat panjang
gelombang. Panjang gelombang cahaya yang digunakan adalah 430 nm,
470 nm, 565 nm, dan 635 nm. Colorimeter memiliki kemampuan untuk
mengukur absorbansi sampel dengan range 0,05 sampai 1,0 dan
transmittans sampel dengan range 10% sampai 90%. Fitur seperti
identifikasi sensor otomatis dan kalibrasi hanya dengan satu langkah
menjadikan sensor mudah untuk digunakan. Detektor terhubung dengan
komputer menggunakan interface LabPro. Pengambilan dan perekaman
data menggunakan Software LogerPro [www.vernier.com]. Detektor
5
mengetahui senyawa dalam sampel yang akan diukur. Detektor
Colorimeter dapat digunakan jika senyawa dalam sampel yang akan diukur telah diketahui.
Detektor Emission Spectrometer adalah detektor yang dirancang untuk
mengukur intensitas dari berbagai sumber cahaya. Intensitas yang terukur
ditampilkan mulai dari 0 sampai dengan 1. Detektor bekerja pada panjang
gelombang mulai dari 320 nm sampai dengan 900 nm dengan interval 1
nm [www.vernier.com]. Detektor Emission Spectrometer dapat digunakan
untuk analisa kualitatif. Analisa kualitatif yaitu mengidentifikasi senyawa
yang terkandung dalam sampel.
Berdasarkan uraian di atas, penelitian yang akan dilakukan adalah
mengidentifikasi jenis pewarna merah dan mengetahui berapa konsentrasi
pewarna merah dalam sampel minuman. Penelitian secara garis besar
dilakukan menjadi dua tahap. Tahap pertama mengidentifikasi keberadaan
pewarna merah jenis tertentu dengan menggunakan detektor Emission
Spectrometer. Tahap kedua yaitu menentukan besar konsentrasi pewarna merah menggunakan Colorimeter. Detektor ini dapat mengukur absorbansi
dan transmittans yang dihasilkan oleh suatu larutan secara bersamaan.
Software Logger Pro digunakan untuk membantu dan mempermudah menganalisa data.
Penelitian ini menunjukkan adanya peristiwa serapan tenaga pada
panjang gelombang tertentu oleh molekul-molekul penyusun suatu
6
materi fisika atom dan molekul. Hal ini dikarenakan penjelasan materi
fisika atom kurang mendalam dan jarang dilakukan praktikum pada
pembelajaran di SMA.
Penelitian ini juga memberikan informasi kepada masyarakat terkait
pewarna yang diperbolehkan untuk digunakan pada minuman dan
makanan. Eksperimen menunjukkan jenis pewarna merah yang digunakan
dan besar konsentrasi pewarna merah dalam sampel minuman yang
diambil dari beberapa jenis minuman di beberapa tempat.
B. Rumusan Masalah
Berdasarkan uraian yang terdapat pada latar belakang maka dapat
dirumuskan menjadi beberapa masalah sebagai berikut:
1. Bagaimana cara mengidentifikasi keberadaan pewarna merah jenis
tertentu dalam sampel minuman menggunakan Detektor Emission
Spectrometer?
2. Bagaimana cara mengukur konsentrasi pewarna merah dalam sampel
minuman menggunakan Detektor Colorimeter?
3. Berapa konsentrasi pewarna merah minuman dalam sampel diukur
7 C. Batasan Masalah
Penelitian ini terbatas pada mengidentifikasi keberadaan jenis
pewarna merah dan pengukuran konsentrasi pewarna merah yang
terkandung dari suatu sampel minuman berwarna merah mencolok.
Standar yang digunakan merupakan pewarna merah Eritrosine CI 16035,
Eritrosine CI 16035-Carmoisine CI 14720, Carmoisine CI 14720, dan
Ponceau 4R CI 16255. Sampel merupakan minuman berwarna merah
mencolok yang dijual dipasaran dalam bentuk cairan. Pewarna makanan
berwana hijau Tartazine CI 19140 digunakan sebagai pembanding untuk
menunjukkan pola serapan pewarna merah dengan pewarna selain merah.
D. Tujuan penelitian
Tujuan penelitian ini adalah:
1. Mengetahui cara mengidentifikasi keberadaan pewarna merah jenis
tertentu dalam sampel minuman menggunakan Detektor Emission
Spectrometer.
2. Mengetahui cara mengukur konsentrasi pewarna merah dalam sampel
minuman menggunakan Detektor Colorimeter.
3. Dapat menentukan konsentrasi pewarna merah dalam sampel minuman
8 E. Manfaat penelitian
Manfaat penelitian ini adalah sebagai berikut:
Bagi peneliti:
1. Mengetahui cara mengidentifikasi keberadaan jenis pewarna merah
dalam sampel minuman menggunakan Detektor Emission
Spectrometer.
2. Mengetahui cara mengukur konsetrasi pewarna merah menggunakan
Detektor Colorimeter.
3. Menunjukkan bahwa spektrum tenaga yang dihasilkan oleh setiap
senyawa berbeda tergantung dari molekul penyusunnya.
4. Mengembangkan kemampuan dalam menggunakan software
LoggerPro untuk menganalisa data sehingga mendapatkan hasil yang
maksimal.
5. Meningkatkan pengetahuan tentang metode untuk mengidentifikasi
keberadaan jenis pewarna merah dalam sampel.
Bagi pembaca:
1. Memberikan informasi penerapan konsep exitasi dan deexitasi
(serapan) molekul mengikuti peristiwa yang dialami oleh elektron
dalam suatu atom tertentu.
2. Memberi informasi penggunaan Detektor Emission Spectrometer dan
9
3. Mengembangkan metode eksperimen dalam pembelajaran tentang
materi fisika atom dan molekul di SMA.
4. Meningkatkan pengetahuan terkait jenis pewarna merah yang
digunakan pada sirup, minuman dalam kemasan, dan minuman yang
dijual pedagang kaki lima.
5. Mengetahui konsentrasi pewarna merah yang digunakan dalam
beberapa sampel yang diperoleh dari beberapa sampel minuman dan
beberapa daerah di sekitar kampus Universitas Sanata Dharma.
F. Sistematika penulisan
Sistematika penulisan hasil penelitian ditulis sebagai berikut:
1. BAB I Pendahuluan
Bab ini menguraikan tentang latar belakang masalah, rumusan
masalah, batasan masalah, tujuan, manfaat, dan sistematika penulisan.
2. BAB II Dasar Teori
Bab ini menguraikan dasar teori seperti teori atom, teori molekul,
hukum lambert Berr, Emission Spectrometer, Colorimeter, pewarna
merah, dan teknik pengenceran.
3. BAB III Metode Penelitian
Bab ini menguraikan alat dan bahan yang digunakan selama penelitian,
prosedur penelitian, dan analisa data.
4. BAB IV Hasil dan Pembahasan
Bab ini menguraikan hasil penelitian dan pembahasan.
10 BAB II DASAR TEORI A. Teori Atom
Nama atom berasal dari bahasa Yunani Atomos yang artinya tidak dapat
dipotong atau dibagi lagi. Atom merupakan bagian terkecil dari suatu materi
yang tidak dapat dibagi lagi. Teori tentang atom mulai berkembang pesat
sejak abad ke-19. Model struktur atom pertama dikemukaan oleh J.J
Thomson pada tahun 1897 dengan keberhasilannya mencirikan elektron dan
mengukur nisbah muatan terhadap massa (e/m) elektron. Menurut J.J
Thomson elektron bermuatan negatif dan berada dalam atom, namun secara
keseluruhan atom bermuatan netral. J.J Thomson mengusulkan bahwa atom
merupakan bola pejal yang terdiri dari elektron dan materi bermuatan positif
tersebar secara merata. Model ini disebut model atom plum pudding [Krane,
1992].
Pada tahun 1911, Rutherford bersama kedua muridnya Hans Geiger dan
Ernest Marsden melakukan eksperimen tentang “Hamburan Sinar Alfa”.
Percobaan hamburan tersebut dilakukan dengan menembakan seberkas
pertikel menuju selembar emas tipis. Hasil eksperimen menunjukkan
adanya ketidaksesuaian dengan model atom J.J Thomson. Partikel (
bermuatan positif) tidak bergerak lurus menembus lempeng emas, namun
terhambur dengan berbagai sudut. Rutherford mengoreksi model Thomson
dengan mengungkapkan bahwa atom terdiri dari partikel bermuatan positif
yang terkonsentrasi pada suatu daerah kecil yang disebut inti dan dikelilingi
11
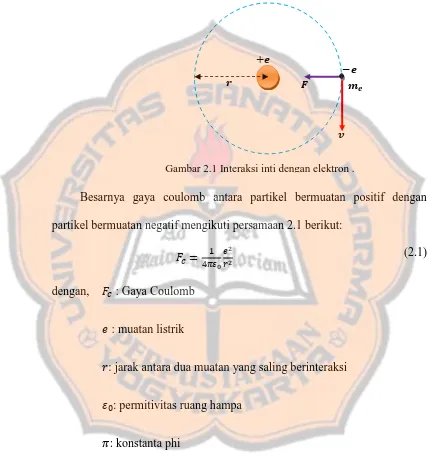
coulomb. Interaksi antara inti dan tiap elektron ditunjukan pada gambar 2.1
berikut [Krane, 1992].
Besarnya gaya coulomb antara partikel bermuatan positif dengan
partikel bermuatan negatif mengikuti persamaan 2.1 berikut:
= �� 0
2
2 (2.1)
dengan, : Gaya Coulomb
: muatan listrik
�: jarak antara dua muatan yang saling berinteraksi
� : permitivitas ruang hampa
�: konstanta phi
Elektron dapat bergerak mengelilingi inti karena mengalami gaya
sentripetal. Besar gaya sentripetal mengikuti persamaan 2.2 berikut:
= �2 (2.2)
�
−� ��
�
+�
[image:31.595.83.513.180.636.2]�
12 dengan, : Gaya sentripetal.
: massa elektron.
� : kecepatan elektron.
�: jarak antara elektron terhadap inti.
Berdasarkan persamaan 2.1 dan persamaan 2.2 diperoleh persamaan 2.3
sebagai berikut:
� = �� 0
2
(2.3)
Model atom Rutherford masih mempunyai kelemahan seperti:
1. Muatan yang dipercepat akan memancarkan radiasi elektromagnetik.
Pada gerak melingkar kecepatannya tidak tetap sehingga elektron akan
mengalami percepatan. Elektron akan memancarkan tenaga dalam bentuk
gelombang eletromagnetik. Elektron kehilangan tenaga dan jari-jari orbit
akan mengecil hingga akhirnya akan bersatu kembali dengan inti. Pada
kenyataannya atom tetap utuh, elektron dan inti terpisah.
2. Frekuensi radiasi sama dengan frekuensi orbitnya. Jika jari-jari orbit
mengecil secara kontinyu maka frekuensi radiasi juga berubah secara
kontinyu. Pada kenyataannya frekuensi radiasi atom diskrit tidak
kontinyu.
Pada tahun 1913, Niels Bohr mengemukakan bahwa atom mirip sistem
13
halnya planet-planet beredar mengelilingi matahari. Bohr memecahkan
persoalan sebelumnya dengan mempostulatkan bahwa elektron hanya dapat
bergerak dalam orbit yang diperkenankan. Orbit stabil ini disebut sebagai
keadaan stasioner. Elektron bergerak pada orbit yang diperkenankan tanpa
memancarkan radiasi elektromagnetik. Atom dapat meradiasi tenaga dalam
bentuk gelombang elektromagnetik jika elektron berpindah dari keadaan
stasioner ke keadaan stasioner lain yang lebih rendah.
Untuk atom Hidrogen dengan jari-jari orbit r dan massa elektron m,
tenaga total sistem merupakan tenaga kinetik elektron ditambah tenaga
potensial Coloumb [Halliday,1978]. Tenaga total sistem sebesar:
= + (2.4)
Dengan tenaga kinetik elektron mengikuti persamaan 2.5 berikut:
=8��2 0
(2.5)
Tenaga potensial sistem proton-elektron sebesar,
= − ��2 0
(2.6)
Sehingga tenaga total elektron menjadi:
= −8��2 0
(2.7)
14
inti atom bernilai bilangan bulat dikalikan konstanta Planck dibagi dengan 2�
yang ditunjukkan dengan persamaan 2.8.
�� = ℎ� = ħ (2.8)
Berdasarkan persamaan 2.8 dan persamaan 2.5 diperoleh persamaan
2.9. Elektron hanya berada pada orbit yang diperkenankan, dimana jari-jari
orbit menurut Bohr [Krane,1992]:
� = ��0ħ2
2 = (2.9)
dengan, � : jari-jari orbit elektron
ħ : tetapan Planck tereduksi = ℎ
�
: merupakan bilangan bulat 1,2,3, ...
∶ ,
Berdasarkan persamaan 2.9 dan persamaan 2.7 diperoleh
= − �2�4
02ħ2 2
(2.10)
Bilangan bulat n merupakan bilangan kuantum utama. Persamaan 2.10
dapat disederhanakan mengikuti persamaan 2.11 berikut.
= − 2,6 eV (2.11)
Elektron dapat berpindah dari suatu orbit ke orbit yang lain. Bila
elektron berpindah dari orbit awal ( tingkat tenaga � ) ke orbit akhir (tingkat
15
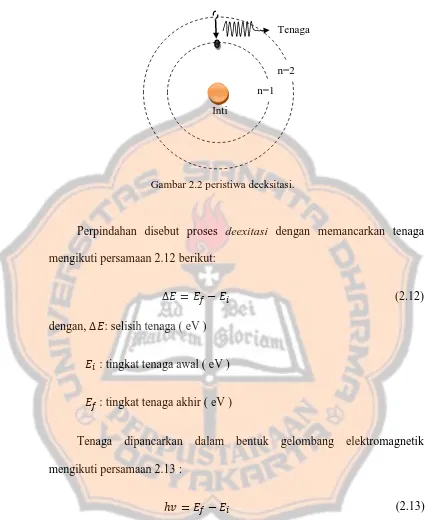
Perpindahan disebut proses deexitasi dengan memancarkan tenaga
mengikuti persamaan 2.12 berikut:
∆ = − � (2.12)
dengan, ∆ : selisih tenaga ( eV )
� : tingkat tenaga awal ( eV )
: tingkat tenaga akhir ( eV )
Tenaga dipancarkan dalam bentuk gelombang elektromagnetik
mengikuti persamaan 2.13 :
ℎ� = − � (2.13)
dengan, h : tetapan Planck sebesar 6,63 x 10-34 J.s
[image:35.595.86.515.103.623.2]v : frekuensi gelombang elektromagnetik s-1 ( Hz ) Gambar 2.2 peristiwa deeksitasi.
Inti
16
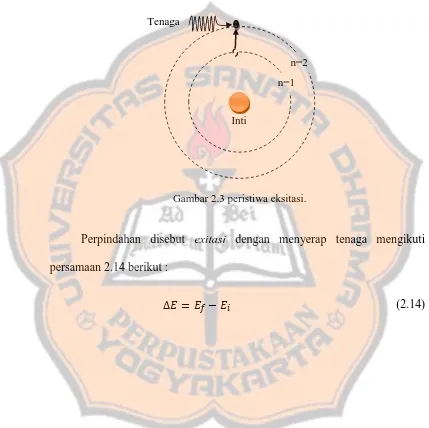
Sebaliknya, elektron berpindah dari orbit awal ( tingkat tenaga � ) ke
orbit akhir (tingkat tenaga ) dengan � < seperti ditunjukkan pada
gambar 2.3.
Perpindahan disebut exitasi dengan menyerap tenaga mengikuti
persamaan 2.14 berikut :
[image:36.595.85.514.198.626.2]∆ = − � (2.14)
Gambar 2.3 peristiwa eksitasi. Inti
17 B. Teori Molekul
Molekul dapat menyerap dan memancarkan tenaga seperti pada atom.
Molekul memiliki tiga tingkat tenaga yaitu tenaga elektronik, tenaga rotasi,
dan tenaga vibrasi mengikuti persamaan 2.15 berikut ini [Beiser,1982]:
= � + �� �+ � (2.15)
Molekul selalu berusaha mencapai keadaan ke tingkat tenaga yang
stabil dengan menyerap dan melepaskan tenaga sebesar [Krane,1992]:
∆ = ℎ� = ℎ� (2.16)
Dengan, ∆ : tenaga yang diserap ( eV )
c : kelajuan cahaya sebesar 3 x 108 m.s-1
� : panjang gelombang ( m )
Karena setiap molekul memiliki tingkat tenaga molekuler yang berbeda,
maka spektrum yang dihasilkan berbeda dari masing-masing molekul. Hal ini
dapat dimanfaatkan dalam menentukan molekul yang terkandung dalam suatu
[image:37.595.84.513.202.636.2]sampel.
Gambar 2.4 Sketsa tingkat tenaga molekul : tingkat tenaga elektronik, tingkat tenaga vibrasi, dan tingkat tenaga rotasi
Tingkat tenaga rotasi Tingkat tenaga vibrasi
Tingkat tenaga elektronik keadaan eksitasi
Tingkat tenaga rotasi Tingkat tenaga vibrasi
18 C. Hukum Beer-Lambert
Seberkas cahaya dengan Intensitas awal memiliki panjang
gelombang �. Berkas cahaya ditembakkan menuju sampel. Sebagian cahaya
akan diteruskan atau ditransmisikan , sebagian dipantulkan r , dan
sebagian lagi diserap . [Skoog et al,1965].
Transmitans � didefinisikan sebagai perbandingan antara intensitas
cahaya yang keluar dari larutan dengan intensitas cahaya datang. Besarnya
transmitans adalah [Skoog et al,1965] :
� =�� 0
(2.17)
Berdasarkan nilai � dapat diperoleh besaran baru yang disebut
absorbansi �, sebesar [Skoog et al,1965]:
� = � �0
� = − log � (2.18)
Hukum Beer dan Lambert menyatakan bahwa absorbansi dari sebuah
sampel berbanding lurus dengan konsentrasi senyawa yang menyerap.
Hubungan antara sebagian cahaya yang melewati sampel (Transmitans)
dengan konsentrasi sampel ternyata tidak linear. Proses berkurangnya
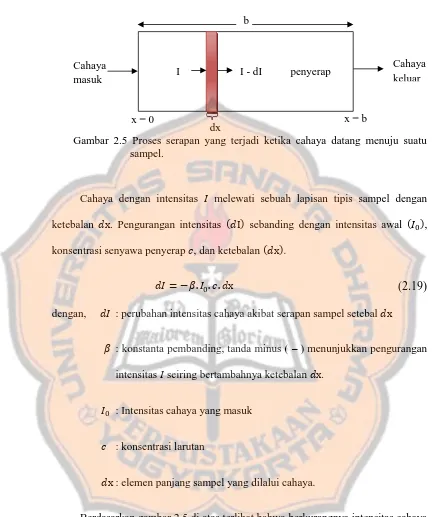
intensitas cahaya ketika melewati sampel ditunjukkan oleh gambar 2.5
19
Cahaya dengan intensitas melewati sebuah lapisan tipis sampel dengan
ketebalan x. Pengurangan intensitas I sebanding dengan intensitas awal ,
konsentrasi senyawa penyerap , dan ketebalan x .
= − . . . x (2.19)
dengan, : perubahan intensitas cahaya akibat serapan sampel setebal x
: konstanta pembanding, tanda minus ( – ) menunjukkan pengurangan
intensitas seiring bertambahnya ketebalan x.
: Intensitas cahaya yang masuk
: konsentrasi larutan
x : elemen panjang sampel yang dilalui cahaya.
Berdasarkan gambar 2.5 di atas terlihat bahwa berkurangnya intensitas cahaya
akibat proses serapan setiap lapisan tipis sampel sepanjang x mulai dari x =
sampai x = b. Sehingga total serapan cahaya (pengurangan intensitas cahaya)
merupakan jumlah dari serapan masing-masing lapisan tipis sampel. Intensitas
cahaya pada saat x = dan intensitas cahaya pada saat x = b. Sehingga
persamaan 2.19 dapat diintegrasikan menjadi [Skoog et al,1965]:
Gambar 2.5 Proses serapan yang terjadi ketika cahaya datang menuju suatu sampel.
Cahaya masuk
x = 0 x = b
I Cahaya
keluar
dx b
[image:39.595.83.515.103.620.2]20 − ��= . . x
− ∫��0 ��= ∫ x
− ln��
0=
ln�0
� =
Berdasarkan hubungan ln � = ln log � maka persamaan tersebut menjadi:
ln log�0
� =
log�0
� = ⏟ ln
= �
−log � =� (2.20)
Dari persamaan 2.18 dan persamaan 2.20 diperoleh hubungan sebagai berikut
[Skoog et al,1965]:
� = � (2.21)
Dengan, � : Absorbansi larutan
: kosentrasi larutan
: tebal larutan
� : merupakan absortivitas molar.
D. Emission Spectrometer
Detektor Emission Spectrometer adalah detektor yang dirancang untuk
mengukur intensitas dari berabagai sumber cahaya. Detektor bekerja pada
panjang gelombang mulai dari 320 nm sampai dengan 900 nm dengan
interval 1 nm [www.vernier.com]. Detektor Emission Spectrometer
21
mengetahui senyawa yang terkandung dalam sampel yang akan diteliti.
Analisa kualitatif dilakukan berdasarkan pola serapan sampel. Analisa
kualitatif dilakukan dengan menyusun detektor Emission Spectrometer
mengikuti gambar 2.6 berikut:
Analisa kualitatif menggunakan Detektor Emission Spectrometer
Setiap molekul memerlukan tenaga untuk melakukan transisi dari
tingkat awal ( �) ke tingkat tenaga akhir ( ) yang lebih tinggi. Tenaga ini
disebut tenaga exitasi. Tenaga exitasi sama dengan tenaga untuk melakukan
deexitasi. Tenaga deexitasi merupakan tenaga untuk melakukan transisi dari tingkat awal ( �) ke tingkat tenaga akhir ( ) yang lebih rendah.
Sinar datang dari sumber radiasi memiliki berbagai panjang
gelombang. Hal ini menunjukkan tenaga yang dibawa oleh sinar datang juga
bervariasi. Jika tenaga yang dibawa oleh sinar datang sama dengan tenaga
yang diperlukan oleh molekul untuk melakukan exitasi maka akan terjadi
proses serah terima tenaga. Tenaga yang dibawa oleh sinar datang akan
diserahkan kepada molekul untuk melakukan exitasi. Misalnya untuk
transisi, molekul memerlukan cahaya dengan panjang gelombang �, maka
cahaya dari sumber dengan panjang gelombang � inilah yang akan diserap
Sumber Radiasi
[image:41.595.86.508.201.617.2]Kuvet Dektektor Perekam dan penampil data
22
oleh molekul. Hal ini merupakan peristiwa serapan tenaga. Karena dalam
larutan terdapat banyak molekul dengan jenis yang sama, maka serapan
ditunjukkan dengan berkurangnya intensitas pada panjang gelombang
tertentu. Berkurangnya intensitas pada panjang gelombang cahaya akan
menghasilkan pola tertentu. Pola inilah yang disebut sebagai pola serapan.
Pola serapan tergantung molekul penyerapnya. Pola serapan menjadi dasar
untuk mengidentifikasi molekul yang terkandung dalam sampel. Setelah
sampel dipastikan mengandung molekul yang diinginkan, proses analisa
dilanjutkan dengan analisa kuantitatif yaitu menentukan konsentrasi
molekul yang terkandung dalam sampel.
E. Colorimeter
Detektor Colorimeter adalah detektor yang digunakan untuk
menentukan konsentrasi dengan analisis intensitas cahaya yang diteruskan
oleh larutan. Detektor memiliki kemampuan untuk mengukur absorbansi
sampel dengan range 0,05 sampai 1,0. Detektor dilengkapi sumber cahaya
dengan empat panjang gelombang. Panjang gelombang cahaya yang
digunakan adalah 430 nm, 470 nm, 565 nm, dan 635 nm. Detektor dilengkapi
dengan fitur seperti identifikasi sensor otomatis dan kalibrasi hanya dengan
satu langkah menjadikan sensor dapat secara langsung digunakan
[www.vernier.com]. Sampel yang sudah diidentifikasi dan diyakini
mengandung senyawa yang diinginkan maka analisa dilakukan secara
kuantitatif. Analisa kuantitatif dilakukan menggunakan detektor Colorimeter.
23
Detektor Colorimeter bekerja berdasarkan Hukum Beer-Lambert yang
dijelaskan pada dasar teori. Sinar datang dengan panjang gelombang �
memiliki intensitas , setelah melewati molekul penyerap maka intensitasnya
menjadi . Intensitas cahaya berkurang menunjukkan adanya cahaya yang
diserap oleh molekul penyerap. Serapan dapat ditunjukkan dengan absorbansi
yang dihasilkan oleh sampel mengikuti persamaan 2.21. Dengan mengetahui
absorbansi akibat proses serapan oleh molekul penyerap, maka konsentrasi
molekul penyerap dapat diketahui.
F. Pewarna Merah
Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720,
Carmoisine CI 14720, dan Ponceau 4R CI 16255 merupakan pewarna sintetis
yang memberikan warna merah muda hingga marun. CI merupakan indeks
warna yang tertera pada kemasan. Rumus empiris Eritrosin adalah
C20H6I4Na2O5. Struktur kimia Eritrosine ditunjukkan oleh gambar 2.7
[www.scribd.com]. Carmoisine mempunyai rumus empiris kimia
C20H12N2Na2O7S2. Struktur kimia Carmoisine ditunjukan seperti pada gambar 2.8. Ponceau 4R mempunyai rumus empiris kimia C20H11N2Na3O10S3. Struktur kimia Ponceau 4R ditunjukkan seperti pada gambar 2.9 [Turak et all,
[image:43.595.84.517.235.726.2]2014].
24
Penggunaan pewarna merah pada makanan dan minuman diatur dalam
Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia
(BPOMRI) no 37 Tahun 2013 tentang batas maksimum penggunaan bahan
tambahan pangan pewarna. Menurut BPOMRI batas penggunaan carmoisine
pada beberapa minuman seperti sirup, minuman beralkohol, dan larutan gula
[image:44.595.84.517.205.635.2]memiliki batas maksimum 70 mg/kg yang setara dengan 70 ml/L.
Gambar 2.8. Struktur kimia pewarna Carmoisine CL 14720 [Turak et all, 2004].
25 G. Teknik Pengenceran
Pengenceran dilakukan untuk mendapatkan variasi konsentrasi dari
suatu pewarna minuman. Larutan diencerkan dengan menggunakan
persamaan 2.22 berikut [Brady, 1994]:
. � = . � (2.22)
dengan, = konsentrasi larutan induk ( ml / L )
� = volume larutan induk yang diambil ( ml )
= konsentrasi larutan yang diinginkan ( ml/L )
26 BAB III EKSPERIMEN
Penelitian ini bertujuan untuk identifikasi keberadaan jenis pewarna merah
dan menentukan konsentrasi pewarna merah dari sampel minuman. Penelitian ini
dilakukan berdasarkan beberapa tahapan. Tahap pertama adalah persiapan alat dan
bahan. Tahap kedua adalah pengambilan data.
A. Persiapan Alat
Alat yang digunakan dalam penelitian ini secara garis besar dibagi
menjadi dua bagian.
1. Alat untuk mengidentifikasi jenis pewarna merah dalam suatu sampel
Alat yang digunakan untuk mengindentifikasi keberadaan
pewarna minuman terdiri dari beberapa komponen. Alat yang digunakan
antara lain:
a. Sumber cahaya.
Sumber cahaya yang digunakan merupakan lampu pijar dengan
daya sebesar 40 watt.
b. Kuvet
Kuvet digunakan untuk meletakan sampel. Kuvet bersifat
transparan dan dapat tembus sinar. Bahan pembuat kuvet tidak
berinteraksi dengan larutan. Kuvet yang digunakan dapat
menampung sampel dengan ketebalan 10 mm. Kuvet berisi larutan
standar sebagai acuan dan larutan sampel.
27
Detektor yang digunakan adalah Emissions Spectrometer buatan
Vernier. Detektor Emissions Spectrometer bekerja pada panjang
gelombang 320 nm sampai 900 nm dengan interval 1 nm. Detektor
menggunakan kabel penghubung USB menuju komputer.
d. Komputer
Komputer digunakan untuk merekam, menampilkan, dan
menganalisa data. Komputer dilengkapi dengan Software Logger Pro
version 3.8.6.2.
Alat kemudian dirangkai seperti gambar 3.1 berikut.
Keterangan gambar
A : sumber cahaya lampu pijar D : Komputer
B : kuvet E : Ruang gelap
A
C
B
[image:47.595.89.514.205.597.2]PC E
28 C : detekor Emission Spectrometer
Sebuah lampu pijar A dengan daya 40 watt, kuvet B, dan detektor
Emission Spectrometer D disusun seperti pada gambar 3.1. Ruang gelap E digunakan untuk mengatasi gangguan cahaya luar. Sehingga berkas
cahaya yang sampai ke detektor merupakan berkas cahaya dari sumber
cahaya. Cahaya dengan panjang gelombang � memiliki intensitas awal
. Berkas cahaya ditembakkan menuju kuvet yang berisi larutan standar
dan sampel. Jika tenaga yang dibawa oleh cahaya sama dengan tenaga
molekul untuk melakukan transisi, maka akan terjadi serah terima tenaga.
Tenaga yang dibawa oleh cahaya digunakan molekul untuk melakukan
transisi mengikuti persamaan 2.16. Serah terima tenaga ini merupakan
peristiwa serapan. Setelah melewati larutan, berkas cahaya ini langsung
menuju detektor. Detektor mengukur intensitas cahaya setelah melewati
larutan. Serapan ditunjukkan dengan berkurangnya intensitas cahaya
setelah melewati larutan pada panjang gelombang �. Berkurangnya
intensitas cahaya pada panjang gelombang � akan menghasilkan pola
serapan. Pola serapan digunakan untuk mengidentifikasi keberadaan jenis
pewarna merah dalam sampel. Detektor dihubungkan ke komputer PC
dengan menggunakan kabel penghubung USB. Untuk pengambilan dan
perekaman data digunakan Software LogerPro.
29
Alat yang digunakan untuk menentukan konsentrasi pewarna
minuman suatu sampel terdiri dari beberapa komponen, yaitu:
a. Kuvet
Kuvet digunakan untuk meletakan sampel.
b. Detektor
Detektor yang digunakan adalah Colorimeter buatan Vernier.
Colorimeter bekerja berdasarkan prinsip hukum Beer Lambert. Pada Colorimeter terdapat sumber cahaya dengan empat panjang gelombang, yaitu 430 nm, 470 nm, 565 nm, dan 635 nm.
Colorimeter menggunakan interface LabPro untuk menghubungkan ke komputer.
c. Interface
Interface merupakan alat yang digunakan untuk menghubungkan
detektor Colorimeter menuju komputer. Interface yang digunakan
dalam penelitian ini adalah LabPro.
d. Komputer
Komputer digunakan untuk merekam, menampilkan, dan
menganalisa data.
30
Kuvet A diletakkan ke dalam Detektor Colorimeter B. Detektor
bekerja berdasarkan Hukum Beer-Lambert yang dijelaskan pada dasar
teori. Detektor dihubungkan ke komputer PC menggunakan interface
LabPro C. Sinar datang dengan panjang gelombang � memiliki intensitas
, setelah melewati molekul penyerap maka intensitanya menjadi . Hal
ini menunjukkan bahwa serapan akan sebanding dengan jumlah molekul
yang menyerap. Serapan dapat ditunjukkan dengan absorbansi yang
dihasilkan oleh sampel mengikuti persamaan 2.21. Untuk pengambilan
dan perakaman data digunakan Software LogerPro. Dengan mengetahui
serapan molekul cahaya yang melewati molekul, maka konsentrasi
[image:50.595.85.509.101.625.2]molekul penyerap dapat diketahui. A
Gambar 3.2 Susunan alat eksperimen untuk menentukan konsentrasi pewarna merah minuman dalam sampel.
B
C
31 B. Persiapan Bahan
Persiapan bahan dilakukan dengan dua tahap yaitu pengenceran larutan
standar dan pembuatan standar kalibrasi.
1. Pengenceran
Larutan standar yang digunakan dihasilkan dari beberapa pewarna
merah. Pewarna merah Carmoisine CL 14720, Carmoisin 14720 –
Eritrosine CL 16035, Eritrosine CL 16035, dan Ponceau 4R CL 16255
diencerkan menggunakan aquades. Pola serapan pewarna merah standar
merupakan dasar untuk mengidentifikasi keberadaan pewarna merah
dalam sampel. Pewarna hijau Tartrasine CL 19140 diencerkan dengan
aquades digunakan sebagai pembanding. Sampel yang dipilih adalah
minuman cair, dalam kemasan, dan berwarna merah mencolok.
Alat yang digunakan dalam pengenceran adalah pipet, gelas ukur,
dan labu ukur. Pengenceran dilakukan berdasarkan persamaan 2.22.
Pengenceran dilakukan berdasarkan dua tahap, yaitu:
a. Larutan Induk
Larutan induk Carmoisine dengan konsentrasi 10 ml/L didapatkan
dengan cara mengambil standar Carmoisine 100% sebanyak 1 ml
ditambah aquadest sebagai pelarut sampai larutan menjadi 100 ml.
Larutan induk standar untuk pewarna merah lain Carmoisin 14720 –
Eritrosine CL 16035, Eritrosine CL 16035, serta Ponceau 4R CL
16255 dibuat dengan cara yang sama.
32
Larutan standar dibuat dengan konsentrasi yang berbeda yaitu 10
ml/L, 8 ml/L, 6 ml/L, 4 ml/L, dan 2 ml/L. Larutan standar carmoisine
dengan konsentrasi 8 ml/L sebanyak 10 ml diperoleh dengan cara
mengambil larutan induk carmoisine dengan konsentrasi 10 ml/L
sebanyak 8 ml kemudian ditambah aquadest hingga volume menjadi
10 ml. Larutan standar carmoisine dengan konsentrasi 6 ml/L
seebanyak 10 ml diperoleh dengan cara mengambil larutan induk
carmoisine dengan konsentrasi 10 ml/L sebanyak 6 ml kemudian
ditambah aquadest hingga volume menjadi 10 ml dan seterusnya.
Larutan standar dengan konsentrasi berbeda untuk pewarna merah lain
dapat diperoleh dengan cara yang sama.
2. Kalibrasi Larutan Standar
a. Pola Serapan Laturan Standar yang Diperoleh Menggunakan Detektor Emission Spectrometer
Pola serapan digunakan untuk mengidentifikasi keberadaan jenis
pewarna merah tertentu dalam sampel minuman. Pola serapan
diperoleh dengan menggunakan Detektor Emission Spectrometer.
Minuman berwarna merah dapat dihasilkan dari pewarna minuman
yang mengandung Carmoisin 14720, Carmoisin 14720 – Eritrosine
CL 16035, Eritrosine CL 16035, dan Ponceau 4R CL 16255. Pola
serapan ditunjukkan dengan grafik hubungan antara intensitas
terhadap panjang gelombang. Konsistensi pola serapan
33
terhadap panjang gelombang pada berberapa konsentrasi pewarna
merah standar. Hal ini digunakan untuk mengidentifikasi keberadaan
jenis pewarna merah tertentu dalam sampel minuman.
b. Pengukuran Absorbansi Larutan Standar menggunakan Detektor Colorimeter pada berbagai konsentrasi
Nilai absorbansi larutan standar pewarna merah Carmoisine CL
14720, Carmoisin 14720 – Eritrosine CL 16035, Eritrosine CL 16035,
dan Ponceau 4R CL 16255 diukur dengan menggunakan detektor
Colorimeter. Nilai absorbansi yang diperoleh dari larutan standar digunakan sebagai acuan. Nilai absorbansi yang diperoleh tergantung
dengan konsentrasi larutan standar. Hubungan antara nilai absorbansi
terhadap konsentrasi menghasilkan persamaan grafik linear mengikuti
persamaan 2.21. Pengukuran dilakukan dengan menyinari larutan
standar dengan menggunakan cahaya pada panjang gelombang 430
nm, 470 nm, 565 nm, dan 635 nm. Berdasarkan pengukuran nilai
absorbansi menggunakan detektor Colorimeter diperoleh empat grafik
hubungan antara absorbansi terhadap konsentrasi untuk masing –
masing pewarna merah standar. Hal inilah yang digunakan sebagai
dasar pengukuran konsentrasi pewarna merah dalam sampel. Nilai
absorbansi sampel dimasukkan ke dalam persamaan grafik hubungan
antara absorbansi terhadap konsentrasi larutan pewarna merah standar
34 C. Prosedur percobaan
Eksperimen dilakukan secara garis besar menjadi dua tahap berikut:
a. Penentuan pola serapan Sampel menggunakan detektor Emission Spectrometer.
1) Menuangkan sampel ke dalam kuvet
2) Meletakkan kuvet yang berisi sampel di antara sumber cahaya dan
detektor Emission Spetrometer.
3) Mengatur posisi lampu pijar, kuvet, dan detektor menjadi satu garis
lurus.
4) Menekan tombol collect untuk memulai pengukuran.
5) Membandingkan pola serapan sampel dengan pola serapan larutan
standar pewarna merah. Pola serapan ditunjukkan dengan nilai
intensitas yang melewati larutan sampel pada panjang gelombang
320 nm sampai 900 nm dengan interval panjang gelombang 1 nm.
b. Pengukuran absorbansi Sampel menggunakan detektor Colorimeter.
1) Memilih sumber cahaya dengan panjang gelombang yang
diinginkan.
2) Menekan tombol kalibrasi pada detektor Colorimeter.
3) Setelah proses kalibrasi selesai, meletakkan kuvet berisi larutan
sampel yang telah diukur menggunakan detektor Emssion
Spectrometer ke dalam detektor Colorimeter.
4) Mengukur absorbansi sampel dengan panjang gelombang 430 nm,
35
5) Menganalisis hasil eksperimen.
D. Analisa Data
Analisa data secara garis besar dilakukan melalui dua tahap. Tahap
pertama yaitu analisa kualitatif. Analisa kualitatif dilakukan dengan
mengidentifikasi senyawa yang terkandung dalam sampel pewarna merah jenis
tertentu. Tahap ini dilakukan dengan cara membandingkan pola serapan yang
dihasilkan oleh sampel terhadap pola serapan larutan standar pewarna merah.
Sampel dikatakan mengandung pewarna merah jenis tertentu jika pola
serapannya sama dan mengikuti pola serapan yang dihasilkan oleh salah satu
pewarna merah standar. Intensitas cahaya setelah melewati larutan akan
berkurang dibandingkan dengan intensitas cahaya awal. Pengurangan intensitas
pada grafik hubungan intensitas terhadap panjang gelombang menunjukkan
absorbansi larutan.
Tahap kedua yaitu analisa kuantitatif. Analisa kuantitatif dilakukan dengan
membandingkan absorbansi larutan standar dengan absorbansi larutan sampel
menggunakan persamaan 2.21. Persamaan tersebut merupakan dasar
perhitungan untuk mendapatkan grafik hubungan antara absorbansi terhadap
konsentrasi larutan standar pewarna merah. Grafik hubungan antara absorbansi
terhadap konsentrasi tersebut akan menghasilkan persamaan grafik linear.
Persamaan grafik yang diperoleh adalah
� = + (3.1)
36
m : merupakan gradien(sensitifitas alat)
c : konsentrasi larutan
b : konstanta
Konsentrasi sampel dapat dihitung dengan memasukan nilai-nilai
absorbansi sampel yang diukur menggunakan panjang gelombang yang telah
37 BAB IV
HASIL EKSPERIMEN DAN PEMBAHASAN A. Hasil Eksperimen
Standar pewarna merah yang digunakan dalam penelitian ini adalah
eritrosin, eritrosin-carmoisine, carmoisine, dan ponceau 4R. Penelitian ini
dilakukan dengan menentukan pola serapan standar pewarna merah dan
sampel. Kedua mengukur nilai absorbansi larutan standar dan sampel. Setelah
diperoleh data kemudian dilakukan analisa.
1. Penentuan Pola Serapan Standar Pewarna Merah Eritrosine, Eritrosine-Carmoisine, Carmoisine, dan Ponceau 4R.
Jenis pewarna merah tergantung dari molekul penyusunnya. Setiap
molekul memiliki tingkat tenaga molekuler yang berbeda. Tenaga
molekul dapat diamati berdasarkan spektrum yang dihasilkan. Spektrum
tenaga menunjukkan pola serapan tertentu.
Penelitian ini dilakukan berdasarkan pola serapan pewarna merah.
Serapan yang dihasilkan oleh masing-masing pewarna merah memiliki
pola berbeda. Pola serapan ditunjukkan dengan grafik hubungan antara
intensitas cahaya setelah melewati larutan terhadap panjang gelombang.
Pengukuran intensitas cahaya setelah melewati larutan dilakukan pada
panjang gelombang 320 nm sampai dengan 900 nm. Hasil pengukuran
intensitas larutan standar pewarna merah eritrosin, eritrosin-carmoisine,
carmoisine, dan ponceau 4R dengan konsentrasi 10 ml/L, 8 ml/L, 6 ml/L,
4 ml/L, dan 2 ml/L terdapat pada tabel lampiran 1. Nilai intensitas cahaya
38
eritrosine ditunjukkan oleh grafik 4.1, nilai intensitas cahaya pada panjang
gelombang 320 nm sampai 900 nm untuk pewarna eritrosine-carmoisine
ditunjukkan oleh grafik 4.2, nilai intensitas cahaya pada panjang
gelombang 320 nm sampai 900 nm untuk pewarna carmoisine
ditunjukkan oleh grafik 4.3, dan nilai intensitas cahaya pada panjang
gelombang 320 nm sampai 900 nm untuk pewarna ponceau 4R
ditunjukkan oleh grafik 4.4.
[image:58.595.84.518.198.629.2]39
Grafik 4.2. Hubungan Intensitas terhadap panjang gelombang (nm) larutan standar Eritrosine CI 16035-Carmoisine CI 14720 pada konsentrasi 10 ml/l ( ), 8 ml/l ( ), 6 ml/l ( ), 4 ml/l ( ), dan 2 ml/l ( ).
[image:59.595.89.514.114.668.2]40
Grafik intensitas terhadap panjang gelombang pewarna eritrosine,
eritrosine-carmoisine, carmoisine, dan ponceau 4R menunjukkan pola
serapan yang berbeda. Grafik intensitas terhadap panjang gelombang
pewarna eritrosine, eritrosine-carmoisine, carmoisine, dan ponceau 4R
merupakan dasar untuk melakukan identifikasi sampel. Sampel dikatakan
mengandung salah satu jenis pewarna merah standar jika pola serapan
yang dihasilkan oleh sampel sama dan mengikuti salah satu pola dari
pewana standar eritrosine, eritrosine-carmoisine, carmoisine, dan
ponceau 4R.
Sampel merupakan senyawa yang terdiri dari berbagai molekul
penyusunnya. Molekul penyusun pewarna merah inilah yang diharapkan
memberi sumbangan serapan, bukan molekul pewarna lain. Dasar Grafik 4.4. Hubungan Intensitas terhadap panjang gelombang (nm) larutan standar
[image:60.595.85.516.111.662.2]41
penelitian yang digunakan adalah konsep selektifitas. Panjang gelombang
terjadi serapan maksimum untuk molekul-molekul penyusun pewarna
merah dapat ditunjukkan dengan membandingkan pola serapan pewarna
merah standar dengan pewarna lain. Pewarna hijau Tartrasine CI 19410
digunakan sebagai pembanding.
Hasil pengukuran nilai intensitas larutan standar pewarna merah
Eritrosine CI 16035, Eritrosine CI 16035-Carmoisine CI 14720,
Carmoisine CI 14720, dan Ponceau 4R CI 16255 dengan konsentrasi 8
ml/l ditunjukkan dengan grafik 4.5 berikut.
Hasil pengukuran nilai intensitas untuk larutan standar Tartrasine
CI 19410 dengan konsentrasi 8 ml/l ditunjukkan oleh grafik 4.6 berikut. Grafik 4.5. Hubungan Intensitas terhadap panjang gelombang (nm) larutan
42
Berdasarkan grafik 4.5 dan 4.6 diperoleh grafik 4.7 berikut ini. Grafik 4.6. Hubungan Intensitas terhadap panjang gelombang (nm) larutan
standar Tartrasine CI 19410 pada konsentrasi 8 ml/l.
43
Berdasarkan grafik 4.7 dapat ditentukan panjang gelombang paling
selektif untuk larutan standar pewarna merah. Panjang gelombang
selektif optimal ditentukan dengan cara memilih panjang gelombang
yang mempunyai serapan paling maksimal untuk pewarna merah dan
paling minimal untuk Tartrasine CI 19410. Serapan maksimal
ditunjukkan dengan intensitas yang rendah, sedangkan serapan minimal
ditunjukkan dengan intensitas tinggi. Panjang gelombang selektif untuk
larutan standar pewarna merah berkisar 430 nm sampai 500 nm. Karena
panjang gelombang ini membawa tenaga yang sama dengan tenaga
molekul pewarna merah untuk melakukan transisi, maka pada panjang
gelombang ini yang mempengaruhi serapan hanya pewarna merah
standar.
2. Pengukuran Absorbansi Larutan Standar Perwana Merah Eritrosine, Eritrosine-Carmoisine, Carmoisine, dan Ponceau 4R dengan Variasi Konsentrasi.
Analisa secara kuantitatif dilakukan jika telah dilakukan analisa
secara kualitatif. Detektor Colorimeter dapat mengukur absorbansi dan
transmittans secara bersamaan. Detektor Colorimeter dilengkapi sumber
cahaya dengan empat panjang gelombang. Hal ini dilakukan dengan
melihat pengaruh konsetrasi pewarna merah standar terhadap absorbansi
pada panjang gelombang tertentu. Berdasarkan pengaruh konsentrasi
larutan standar Carmoisine CI 14720 terhadap absorbansi dapat diperoleh
persamaan grafik hubungan Absorbansi terhadap konsentrasi. Hasilnya
44
Dari tabel 4.1 diperoleh grafik hubungan absorbansi terhadap
konsentrasi yang ditunjukkan grafik 4.8 berikut ini.
Hubungan absorbansi terhadap kosentrasi larutan Carmoisine CI
14720 p

![Gambar 2.7. Struktur kimia pewarna Eritrosine CI 16035 [www.scribd.com].](https://thumb-ap.123doks.com/thumbv2/123dok/899678.597716/43.595.84.517.235.726/gambar-struktur-kimia-pewarna-eritrosine-ci-www-scribd.webp)
![Gambar 2.8. Struktur kimia pewarna Carmoisine CL 14720 [Turak et all, 2004].](https://thumb-ap.123doks.com/thumbv2/123dok/899678.597716/44.595.84.517.205.635/gambar-struktur-kimia-pewarna-carmoisine-cl-turak-all.webp)

