SIFAT DAN STRUKTUR LIPID
1Syifa Khaerani, 2Muhammad Fahrul Nugraha, 3Puspa Julistia P 1Mahasiswa, 2Asisten Praktikum, 3Penanggung Jawab Praktikum
Departemen Biokimia
Fakultas Matematika dan Ilmu Pengetahuan Alam Program Sarjana
Institut Pertanian Bogor 2018
ABSTRAK
lipid didefinisikan sebagai senyawa yang tak larut dalam air tapi larut dalam pelarut organik yang kepolarannya rendah atau non polar. Lipid dibedakan menjadi triasilgliserol, gliserofosfolipid, sfingolipid, kolesterol dan hormon steroid. Berdasarkan sumber, lipid atau lemak dibedakan menjadi lemak nabati dan hewani. Sifat dan struktur lipid dapat diidentifikasi dan dipelajari melalui pengujian pada lipid. Uji lipid yang dilakukan pada praktikum ini adalah uji kelarutan lipid, uji arkoelin, uji ketidakjenuhan, uji ketengikan, uji Salkowski, dan uji Lieberman Buchard untuk kolesterol. Sampel lipid yang digunakan yaitu minyak kelapa, minyak kelapa tengik, margarin, mentega, blue band, asam palmitat, asam oleat, asam stearat, gliserol, dan pati.
Kata Kunci: Lipid, uji akrolein, uji ketidakjenuhan, uji ketengikan, uji kolesterol.
PENDAHULUAN
Lipid didefinisikan sebagai senyawa yang tak larut dalam air yang diekstrak dari organisme hidup menggunakan pelarut yang kepolarannya lemah atau pelarut non polar. Definisi ini berdasarkan sifat fisik, berlawanan dengan definisi protein, karbohidrat, maupun asam nukleat yang berdasarkan atas struktur kimianya (Ngili Y 2009). Jika diklasifikasikan berdasarkan sifat kimianya, lipid dibagi menjadi dua kelompok, yaitu: 1). Kelompok pertama terdiri dari senyawa rantai terbuka dengan gugus kepala bersifat polar serta ekor bersifat non polar. Contoh senyawa kelompok ini adalah asam lemak, trigliserida, sphingolipid, fosfoasilgliserol, dan glikolipid. 2). Kelompok uatama kaedua terdiri dari senyawa
fusedring, steroid. Contoh kelompok ini adalah kolesterol (Marks et.al 2000). Kolesterol meruapakan komponen umum membran sel hewan dan juga merupakan prekursor (senyawa pendahulu) yang mana dari prekursor ini steroid akan disintesis. Banyak hormon termasuk hormon termasuk hormone seks vertebrata merupakan steroid yang dihasilkan dari kolesterol (Campbell et al.
2002).
struktur lipid melalui uji-uji kualitatif dan menunjukkan sifat-sifat lipid melalui beberapa reaksi uji kualitatif untuk lipid.
METODE
Waktu dan Tempat
Praktikum dilaksanakan Senin, 13 Maret 2018 pukul 13.00-16.00 WIB di Laboratorium Pendidikan Biokimia, Gedung Fakultas Peternakan, Institut Pertanian Bogor.
Alat dan Bahan
Alat yang digunakan adalah tabung reaksi, pipet mohr 5ml dan 10 ml, batang pengaduk, pipet tetes, bunsen, Erlenmeyer, kertas saring, bulb, dan karet penyumbat.
Bahan yang digunakan.adalah air, eter, kloroform, alkohol, alkali, asam encer, minyak kelapa, lemak hewan, mentega, margarin, gliserol, asam palmitat, asam stearat, pati, KHSO4, Iod Hubl, HCl pekat, florogusinol, serbk CaCO3,
kolesterol, asam sulfat pekat, dan asam asetat anhidrat.
Prosedur
Uji Kelarutan
Sebanyak 2 ml pelarut dimasukkan ke dalam tabung reaksi bersih. Setelah itu, sedikit bahan percobaan dibubuhkan ke dalam tabung yang sudah berisi pelarut. Isi tabung dikocok kuat-kuat, lalu diamati kelarutannya.
Uji Akrolein
Sedikit kristal KHSO4 dimasukkan ke dalam tabung yang bersih dan
kering. Setelah itu 3-4 tetes bahan percobaan yakni minyak kelapa, lemak hewan, gliserol, asam palmitate, asam stearate dan pati dibubuhkan. Tabung dipanaskan di atas api langsung, dan bau akrolein yang terbentuk berupa asap putih diamati. Bau akrolein dibandingkan dengan bau SO2 yang terbang dari karbohidrat.
Uji Ketidakjenuhan
Sebanyak 1 ml bahan percobaan, yaitu minyak kelapa, minyak kelapa yang tengik, lemak hewan, mentega, blue band, asam palmitate, dan asam oleat dimasukkan ke dalam tabung bersih. Setelah itu kloroform sebanyak 1 ml ditambahkan, lalu kocok sampai bahan larut. Tetes demi tetes pereaksi Iod Hubl dibubuhkan sambil dikocok, lalu diamati perubahannya.
Uji Ketengikan
Erlenmeyer 100 ml disediakan. Sebanyak 5 ml bahan percobaan dimasukkan. Setelah itu, sebanyak 5 ml HCl pekat ditambahkan dan dicampurkan secara hati-hati. Kertas saring yang telah dicelupkan ke dalam floroglusinol dan sumbat karet disediakan. Setelah itu serbuk CaCO3 dimasukkan ke dalam
yang terjadi diamati pada kertas saring tersebut. Perubahan warna menjadi warna merah muda menandakan bahan tersebut tengik.
Uji Salkowski untuk Kolesterol
Dalam tabung reaksi bersih dan kering dilarutkan beberapa miligram kolesterol di dalam 3 ml kolesterol anhidrat, setelah itu asam sulfat dengan volume yang sama ditambahkan dan dikocok secara perlahan-lahan. Lapisan cairan dibiarkan terpisah dan warna yang terjadi diamati.
Uji Liberman Buchard untuk Kolesterol
Ke dalam larutan-larutan kolesterol dan kloroform (dari percobaan Salkowski) ditambahkan 10 tetes asam asset anhidrat dan 2 tetes asam sulfat pekat. Larutan dikocok perlahan dan dibiarkan beberapa menit.
HASIL DAN PEMBAHASAN
Uji Kelarutan
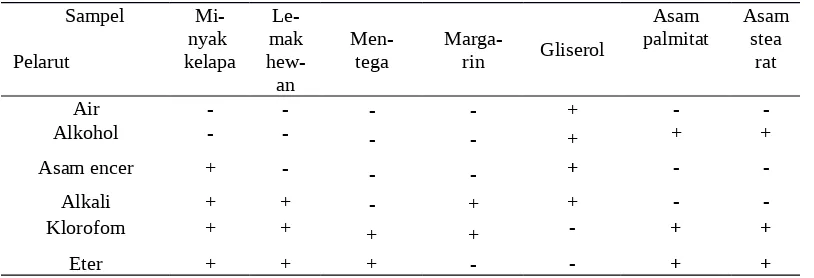
Suatu pelarut dikatakan polar jika pelarut tersebut memiliki indeks polaritas yang besar, contohnya air yang memiliki indeks polaritas sebesar 10.2. Pelarut semi polar memiliki indeks polaritas pertengahan sekitar 4.1 untuk kloroform dan 5.1 untuk senyawa alkohol. Adapun pelarut non polar yaitu pelarut yang memiliki indeks bias kecil seperti heksana, yaitu sebesar 0.1 (Rais 2014).
Pada tabel 1 dapat dilihat bahwa semua lipid tidak dapat larut dalam air melainkan larut dalam pelarut organik. Hal ini dikarenakan lipid disusun oleh karbon dan hidrogen dengan proporsi tinggi sehingga tidak larut dalam air (Ngili 2009). Adapun gliserol bukan termasuk ke dalam lemak melainkan termasuk golongan alkohol yang memiliki 3 gugus hidroksil sehingga dapat larut dalam air dan tidak dapat larut dalam pelarut organik, seperti kloroform dan eter (Ngili 2009). Alkohol merupakan pelarut oraganik yang bersifat polar (saifudin 2012) Hal ini dapat menjadi penyebab kelarutan lipid dalam alkohol sangat rendah. Eter dan kloroform merupakan pelarut organik yang bersifat non polar (Cairns 2004). Lipid larut dalam pelarut eter dan kloroform, hal ini dikarenakan lipid tersusun atas asam lemak yang bersifat non polar.
Pada tabel 1 dapat dilihat bahwa mentega tidak larut dalam eter dan kloroform, begipun dengan lemak hewan tidak larut dalam kloroform, hal ini dapat disebabkan oleh mentega dan lemak hewan yang memiliki kadar air di dalamnya. Dalam asam maupun basa lemak ada yang larut dan ada pula yang tidak larut. Gliserol larut dalam asam dan basa karena bersifat polar, tetapi asam lemak tidak larut dalam asam dan basa karena asam lemak berbeda polaritas dengan asam basa.
Uji Arkoelin
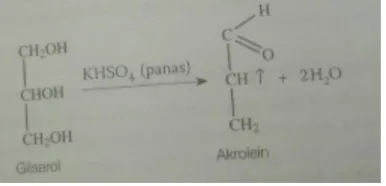
Bintang (2010) menyatakan, suatu gliserol akan terdehidrasi dan membentuk akrolein aldehida yang berbau menyengat jika direaksikan dengan kalium bisulfit (KHSO4). Tabel 2 menunjukkan bahwa lemak pada sampel, yaitu
minyak kelapa, lemak hewan, dan mentega mengandung gliserol. Hal ini dapat dilihat dari hasil yang positif pada uji akrolein. Sesuai dengan pendapat Makfoeld et.al (2002) bahwa lemak (Triasilgliserol) tersusun atas tiga asam lemak dan gliserol, sehingga ketika keduanya terpisah akan menghasilkan gliserol dan asam lemak. Tetapi, hasil negatif akan didapat pada uji asam lemak, hal ini dikarenakan asam lemak tidak tersusun atas gliserol.
Tabel 2 Uji Akrolein
Sampel Bau Asap
Minyak kelapa ++ Ada
Lemak hewan + Ada
Gliserol +++ Ada
Asam palmitat - Tidak ada
Mentega - Tidak ada
Asam stearat - Tidak ada
Keterangan: + = Mengandung gliserol - = Tidak mengandung gliserol Reaksi yang terjadi adalah sebagai berikut:
Uji ketidakjenuhan
Uji ketidakjenuhan digunakan untuk menentukan lipid yang mengandung asam lemak tak jenuh. Asam lemak tak jenuh adalah asam lemak yang mengandung satu atau lebih ikatan rangkap, wujudnya cair dalam suhu kamar bahkan suhu dingin. Asam lemak jenuh adalah asam lemak yang hanya memiliki ikatan tunggal saja sebagai penyusunnya (Sartika 2008). Secara umum, lemak tak jenuh dapat menguntungkan kolesterol darah dari pada asam lemak jenuh. Uji ketidakjenuhan menggunakan Iod Hubl sebagai perekasinya, sedangkan penggunaan kloroform untuk melarutkan lipid. Banyaknya ikatan rangkap di dalam asam lemak ditnjukkan oleh sebuah angka yang disebut angka iodium (Prihandana et.al 2006).
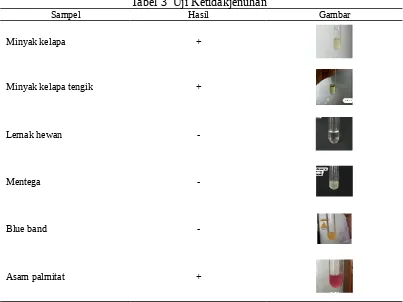
Tabel 3 juga menunjukkan bahwa sampel yang positif mengandung asam lemak tak jenuh yaitu minyak kelapa, minyak kelapa tengik, dan asam palmitat. Menurut Campbel (2002) minyak yang berasal dari tumbuhan seperti minyak kelapa merupakan lipid yang tersusun atas asam lemak jenuh, sedangkan lemak yang didapat dari hewan bukan ikan biasanya tersusun atas asam lemak yang jenuh. Mentega juga termasuk ke dalam lemak jenuh (Campbel 2002). Menurut Silalahi (2006) palmitat termasuk ke dalam golongan asam lemak jenuh. Hasil potisif asam palmitat pada uji ini dapat disebabkan oleh pencemar pada asam palmitat, sehingga ada rekasi dengan iod yang terjadi di dalam asam palmitat tersebut.
Tabel 3 Uji Ketidakjenuhan
Sampel Hasil Gambar
Minyak kelapa +
Minyak kelapa tengik +
Lemak hewan
-Mentega
-Blue band
-Asam palmitat +
Tabel 3 menunjukkan beberapa lipid dan asam lemak bebas yang mengandung ikatan ganda pada penyusun asam lemaknya. Hal ini ditandai dengan munculnya perubahan warna setelah penambahan Iod Hubl. Iod hubl akan mengadisi ikatan rangkap, sehingga warna pereaksi tidak terlihat (Bintang 2010). Reaksi yang terjadi adalah sebagai berikut:
Gambar 2 Rekasi adisi iod (Bintang 2010)
Uji Ketengikan
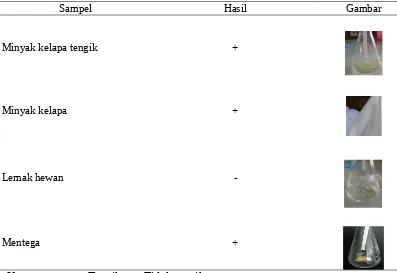
Proses ketengikan (rancidity) merupakan problem utama yang dijumpai pada minyak, lemak dan bahan pangan mengandung lemak. Ketengikan dapat disebabkan oleh aktivitas enzim, proses hidrolisis, maupun proses oksidasi (Chen 2003). Tabel 4 menunjukkan ketengikan dari suatu sampel. Sampel yang positif tengik, yaitu minyak kelapa tengik, minyak kelapa, dan mentega, ditandai dengan munculnya warna merah muda pada kertas saring yang telah dicelupkan pada florogusinol. Lemak hewan dan mentega tersusun atas asam lemak jenuh. Asam lemak jenuh tidak mudah teroksidasi, sehingga menghasilkan hasil yang negatif pada uji ketengikan
Tabel 4 Hasil uji ketengikan
Sampel Hasil Gambar
Minyak kelapa tengik +
Minyak kelapa +
Lemak hewan
-Mentega +
Uji Salkowski
Sterol dengan konfigurasi tidak jenuh direaksikan dengan asam kuat dalam kondisi bebas air, maka akan terbentuk kompleks warna bervariasi sesuai dengan kondisi percobaan. Mula-mula warna yang timbul adalah biru menjadi merah di bagian kloroform, sedangkan dibagian asam berwarna kuning dengan floresensi biru bila melalui sinar refleksi (Bintang 2010).
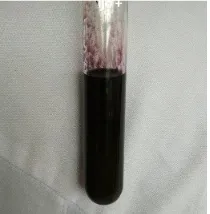
Gambar 3 Uji Salkowski
Gambar 3 menujukkan pengujian kolestrol dengan uji Salkowski. Hasil pada uji ini positif. Warna merah dan hijau kekuningan terlihat pada gambar ini yang menunjukkan adanya kolesterol pada sampel. Fungsi kloroform pada uji ini adalah untuk melarutkan kolesterol, selanjutnya kolesterol membentuk kompleks warna akibat bereaksi dengan asam pekat.
Uji Lieberman Buchard
Prinsip dari uji Lieberman Buchard sama seperti Salkowski, bedanya adalah uji Lieberman Buchard digunakan untuk analisis kualitatif dan kuantitaf, yang memperhatikan jumlah bahan yang dipakai pada percobaan.
Gambar 4 Uji Lieberman Buchard
Aplikasi dari uji kolesterol dalam kehidupan sehari-hari yaitu pengujian kolesterol daging dengan metode Lieberman Buchard. Hal ini dilakukan untuk mengetahui kadar kolesterol yang ada pada daging. Kadar kolesterol yang didapatkan merupakan jumlah kandungan lipid dari daging tersebut (Dwiloka
SIMPULAN
Sifat dan struktur lipid dapat ditentukan oleh uji kualitatif pada lipid. Lipid tidak dapat larut dalam air, melainkan larut dalam pelarut organik. Lipid tersusun atas asam lemak jenuh dan ada juga yang tersusun atas asam lemak tak jenuh. Ketidakjenuhan suatu lipid dapat ditentukan oleh reaksi denga Iod Hubl, yakni lipid yang bereaksi dengan Iod Hubl termasuk ke dalam lemak tak jenuh. Lipid juga dapat mengalami oksidasi yang disebut dengan ketengikan. Kolesterol dalam lipid dapat ditunjukan oleh uji Salkowski dan Lieberman Buchard.
DAFTAR PUSTAKA
Cairns D. 2004. Intisari Kimia Farmasi. Jakarta(ID): Buku Kedokteran EGC. Campbell NA, Reece JB, dan Mitchell LG. 2002. Bologi Jl. 1 Ed. 5 Jakarta(ID):
Erlangga.
Chen BK and Diosady LL. 2003. Enzymatic Aqueous Processing of Coconut.
International Journal of Applied Science and Engineering. 1:55-51.
Dwiloka B, Meliandasari D, dan Suprijatna E. 2015. Optimasi daun kayambang untuk penurunan kolesterol daging dan peningkatan kualitas asam lemak esensial. Jurnal Aplikasi Teknologi Pangan. 4(1): 23-26
Makfoeld D at.al. 2002. Kamus Istilah Pangan dan Nutrisi. Yogtakarta(ID): Kanisius
Marks DB, Marks AD, dan Smith CM. 2000. Biokimia Kedokteran Dasar. Jakarta(ID): Buku Kedokteran EGC.
Ngili Y. 2009. Biokimia: Metabolisme dan Bioenergetika. Yogyakarta(ID): Graha Ilmu
Prihandana R, Hendroko R, dan Nuramin M. 2006. Menghasilkan Biodiesel Murah: Mengatasi Polusi & kelangkaan BBM. Tangerang(ID): Agromedia Pustaka.
Rais IR. 2014. Ekstraksi andrografolid dari Andrographis paniculata (Burm,.f.) Nees manggunakan eksraktor soxhlet. Pharmaciana. 4(1):85-92.
Saifudin A. 2012. Senyawa Alam Metabolit Sekunder. Yogyakarta(ID): Deepublish.