BAB I PENDAHULUAN
Selenium merupakan salah satu trace elemen esensial bagi tubuh. Mikronutrien ini menjadi bagian yang penting dari enzim yang tergantung selenium, yang disebut selenoprotein. Terdapat 11 selenoprotein yang telah teridentifikasi, yaitu enzim glutathione peroksidase (4 jenis), iodothyronine deiodinase (3 jenis), thioredoksin reduktase, selenofosfat sintetase, selenoprotein P dan selenoprotein W. Tinjauan kepustakaan ini hanya akan membahas selenium yang berfungsi sebagai komponen dari enzim glutathione peroksidase.1-4
Selenium tubuh berasal dari makanan dan minuman. Daging dan makanan laut mempunyai kandungan selenium yang tinggi. Kandungan total selenium dalam tubuh bervariasi antara 3mg sampai 20,3 mg. Distribusi selenium pada tubuh paling banyak terdapat di hepar, ginjal, otot dan plasma. Absorbsi selenium terjadi di duodenum dengan besar penyerapan 50% sampai 100% dan diekskresikan melalui urine, feses dan pernafasan. Kebutuhan selenium (berdasarkan RDA) untuk anak sebesar 20 mcgr/hari sedangkan untuk dewasa sebesar 55 mcg/hari.5-7
Enzim glutathione peroksidase terdiri dari 4 atom selenium yang terikat sebagai selenocystein. Enzim ini terdiri dari 4 tipe, yaitu seluler glutathione peroksidase (cGPx), ekstraseluler glutathione peroksidase (eGPx), gastrointestinal glutathione peroksidase (GPx-GI) dan fosfolipid glutathione peroksidase (PhGPx). Enzim glutathione peroksidase mencegah kerusakan sel dengan cara mengkatalisa peroksida menjadi air dan oksigen. Karena kemampuannya inilah maka enzim ini disebut sebagai enzim antioksidan.1-4
Oksidan (radikal bebas) adalah molekul dimana elektron yang terletak pada lintasan paling luar tidak mempunyai pasangan. Di dalam tubuh, radikal bebas yang paling banyak terbentuk adalah superokside. Superokside dapat dirubah menjadi hydrogen peroksida. Hidrogen peroksida kemudian diubah menjadi radikal hidroksil. Radikal hidroksil inilah yang dapat menyebabkan peroksidasi lipid pada membran sel sehingga terjadi kerusakan sel.8-10
Dalam keadaan normal, oksidan yang terbentuk dapat dinetralisir oleh antioksidan. Antioksidan dalam tubuh terdiri dari antioksidan enzimatik dan non enzimatik. Glutathione peroksidase adalah antioksidan enzimatik.8-10
Sebagai komponen dari enzim yang berfungsi sebagai antioksidan, selenium telah dihubungkan dengan berbagai penyakit, seperti penyakit kardiovaskuler (aterosklerosis, miokard infark dan kardiomiopati), penyakit paru-paru (asma, kistik fibrosis), penyakit gastrointestinal (penyakit Crohn’s), penyakit virus (penyakit Keshan, influenza dan HIV), kanker, sistem imun, penyakit sendi (penyakit Kashin-Beck) dan infertilitas pada laki-laki.
Keracunan selenium dapat terjadi akut maupun kronis. Keracunan akut dan fatal terjadi karena kecelakaan atau usaha bunuh diri dengan menelan sejumlah besar selenium. Keracunan kronis selenium terjadi dengan menelan dosis yang lebih kecil dalam waktu lama. Gejala-gejala yang umum ditemukan pada selenosis adalah rambut rontok, kuku yang rapuh, gangguan pencernaan, dermatitis, bau nafas seperti bau bawang, rasa metalik, kelemahan dan bahkan kematian.1-4
Tujuan penulisan sari pustaka ini adalah membicarakan selenium sebagai komponen enzim glutathione peroksidase yang berperan sebagai antioksidan dan merupakan salah satu syarat untuk menyelesaikan program pendidikan dokter spesialis anak.
BAB II SELENIUM
2.1 Batasan
Selenium adalah trace elemen esensial dalam tubuh manusia. Mikronutrien ini merupakan bagian dari enzim yang tergantung selenium yang disebut selenoprotein. Terdapat 11 selenoprotein yang telah teridentifikasi, yaitu enzim glutathione peroksidase (4 jenis), iodothyronine deiodinase (3 jenis), thioredoksin reduktase, selenofosfat sintetase, selenoprotein P dan selenoprotein W.1-4
2.2 Sejarah
Selenium ditemukan pertama kali pada tahun 1817 oleh Jons Jakob Berzelius, seorang ahli kimia yang berasal dari Swedia. Kata selenium berasal dari nama Dewi Bulan, Selene.11,12
Pada tahun 1957 Dr. Klaus Schwarz dan Fultz melaporkan bahwa selenium dapat mencegah nekrosis hepar pada tikus yang mengalami defisiensi vitamin E. Pada manusia, fungsi selenium baru ditemukan pada tahun 1973. Dr. John Rottuck dari Universitas Wisconsin menemukan bahwa selenium dapat bergabung dalam molekul suatu enzim yang disebut glutathione peroksidase (GPx).12 Sejak itu, terutama tahun 1980-an informasi mengenai selenium meningkat dengan cepat.
2.3 Sifat Fisik dan Kimia
Selenium adalah elemen kimia non metalik pada group VI A, pada tabel periodik dengan symbol Se, nomor atom 34, berat atom 78,96 A. Titik beku 217,0
0C, titik didih 684,9 0C. Ada 4 tingkat oksidasi, yaitu elemental Se (0), selenate (+6),
selenite (+4) dan selenide (-2). Selenium memiliki 3 bentuk, yaitu kristal berwarna merah, bubuk berwarna merah dan kristal heksagonal warna abu-abu.
Di alam, terdapat berbagai senyawa yang mengandung selenium, yaitu elemental selenium, garam inorganik (selenite dan selenate), organik (selemomethionine, selenocystein dan selenocystine), gas (hydrogen selenide) dan cair (selenium oksiklorid, selenium dioksid dan asam selenius).11,13
Dalam kehidupan sehari-hari, kita mendapat asupan selenium dari makanan dalam bentuk organik dan dari minuman dalam bentuk garam inorganik. 3,4,12,13 Rumus kimia selenomethioine dan selenocystein dapat dilihat pada gambar 1.4
H H H2 N--C--COOH H2N---C---COOH CH2 CH2 SeH CH2 Se Selenocystein CH3 Selenomethionine
Gambar.1. Rumus kimia selenomethionine dan selenocystein. Gambar didapat dari Burk RF, Levander OA. Selenium. In: Modern Nutrition in Health and Disease; edisi ke-7. Philadelphia, 1988;265-74.
Selenomethionine adalah selenium murni yang berikatan dengan asam amino methionine. Selenomethionine terdapat secara alami pada makanan. Selenomethionine mempunyai 2 bentuk, yaitu selenomethionine dengan isomer L dan isomer D. Bentuk yang digunakan tubuh adalah selenomethionine dengan isomer L.12
2.4 Fisiologi
2.4.1 Distribusi selenium dalam tubuh
Kandungan selenium dalam tubuh manusia bervariasi antara 3 mg sampai 20,3 mg, tergantung dari kandungan selenium pada tanah di daerah tersebut. Tanah dengan kandungan selenium rendah menyebabkan kandungan selenium pada tanaman juga rendah sehingga ambilan selenium juga rendah, begitu pula sebaliknya. Di Amerika Serikat kadar selenium pada orang dewasa berkisar antara 13 mg sampai 20,3 mg tetapi di German berkisar 6,6 mg, di Polandia 5,2 mg dan 3 mg sampai 6,1 mg di New Zealand.6 Sedangkan konsentrasi selenium pada air susu berkisar antara 15 sampai 20 mcg/L.
Dengan diet yang normal, konsentrasi selenium terbanyak terdapat di hepar dan otot masing-masing sebesar 30%. Selain itu dapat juga ditemukan di ginjal (15%), plasma (10%), lien, pankreas, jantung, otak, paru-paru, tulang, rambut dan kuku.5,7 Konsentrasi serum selenium pada orang dewasa >4x dibandingkan pada fetus dan neonatus, tetapi sebaliknya konsentrasi selenium pada serebrum fetus dan neonatus lebih besar dibandingkan pada orang dewasa. Tetapi penyebab fenomena ini belum diketahui.
Distribusi selenium di dalam tubuh dapat berubah sesuai dengan kebutuhan organ vital, sebagai contoh, pada penelitian yang dilakukan oleh Behne,dkk tahun 2000,6 dilakukan pengurangan selenium dalam jangka panjang, terjadi penurunan secara drastis kadar selenium di hepar, otot dan darah sampai <1% dari normal, tetapi di otak kadar selenium masih terdapat 60%.
2.4.2 Absorbsi dan Transport
Absorbsi selenium terjadi di duodenum melalui Na+-dependent neutral amino acid transport sistem.15 Selenomethionine diabsorbsi hampir 100%.16,17 Sedangkan absorbsi selenium inorganik bervariasi tergantung dengan faktor luminal.4,17 Selenium bentuk organik, terutama L-selenomethionine lebih mudah diserap oleh tubuh daripada bentuk inorganik, hal ini disebabkan karena selenium bentuk organik mengandung asam amino, sehingga dapat bergabung dengan protein tubuh dan memungkinkan untuk disimpan dan dilepaskan kembali jika diperlukan. D-selenomethionine didegradasi menjadi selenium inorganik. Oleh karena itu bioavailabilitinya hanya 1/5 dari L-selenomethionine. Sedangkan selenium inorganik langsung didegradasi sehingga tidak dapat disimpan.12
Absorbsi selenium tidak dipengaruhi oleh status selenium dalam tubuh.4 Absorbsi selenium tergantung kepada beberapa nutrisi yang lain. Vitamin A, C dan E meningkatkan absorbsi. Sedangkan merkuri menurunkan absorbsi selenium karena terbentuk endapan.17 Selenomethionine yang tidak langsung dimetabolisme akan bergabung dengan protein tubuh dalam otot rangka, eritrosit, pankreas, hati, ginjal, lambung dan mukosa gastrointestinal.15
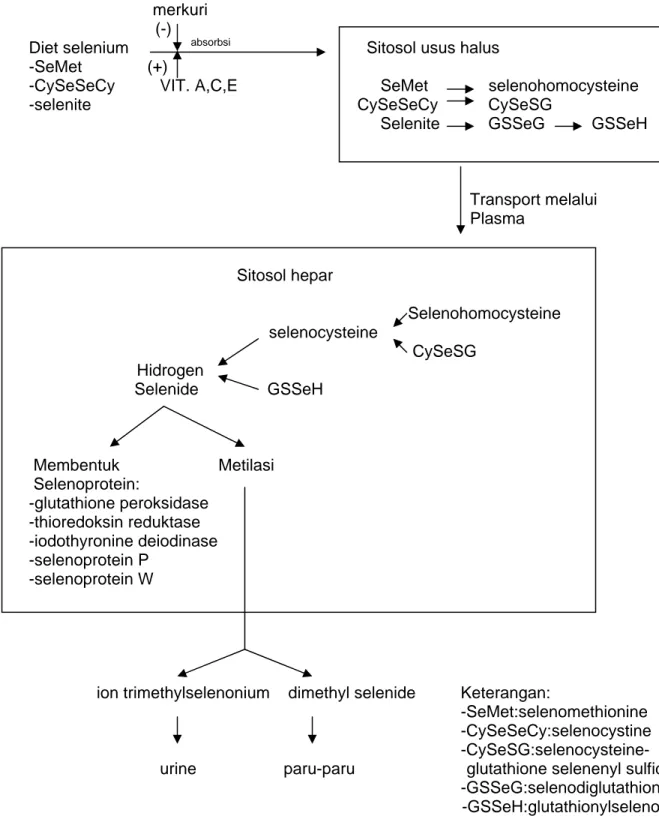
Seperti yang terlihat pada gambar 2, di dalam sel usus halus, senyawa selenium akan dimetabolisme menjadi selenocysteine. Selenomethionine (SeMet) diubah menjadi selenocysteine (CySeH) melalui selenohomocystein dan
selenocsystathionine. Di hepar selenocysteine akan mengalami dekomposisi menjadi serine dan hydrogen selenide (H2S) oleh enzim β-lyase. H2S akan
digunakan untuk sintesa selenoprotein atau mengalami metilasi menjadi mono-, di-, dan trimethyl oleh S-adenosylmethionine (SAM). Di hepar, selenomethionine juga dapat mengalami pemotongan oleh enzim γ-lyase menjadi monomethyl selenol.3
Di dalam sitosol usus halus, selenocystine bereaksi dengan glutathione tereduksi (GSH) membentuk selenocysteine-glutathione selenenyl sulfide (CySeSG). CySeSG kemudian direduksi oleh GSH menjadi selenocysteine. CySeSG juga direduksi oleh enzim glutathione reduktase menjadi selenocysteine dan NADPH. Selenocystein selanjutnya akan mengalami proses yang sama seperti selenomethionine.3
Selenite dimetabolisme oleh glutathione (GSH) atau glutathione reduktase menjadi hydrogen selenide melalui selenodiglutathione dan glutathyonylselenol. Hydrogen selenide selanjutnya mengalami proses proses yang sama seperti di atas.3
Mekanisme transport sejauh ini masih belum jelas. Tetapi ada hipotesis yang mengatakan bahwa selenium masuk ke sel darah merah melalui proses difusi dan kemudian dibawa ke seluruh tubuh. Di dalam darah selenium terikat pada lipoprotein, seperti VLDL atau LDL. Mekanisme transport kedua diduga adalah selenoprotein P.17
2.4.3 Ekskresi
Homeostasis selenium dalam tubuh dilakukan melalui ekskresi, baik melalui urine, feses atau pernafasan. Sebagian besar selenium diekskresi melalui urine (60-80%).18 Sebagian besar metabolit selenium diekskresi dalam bentuk metilasi yaitu methylselenol. Selenium dalam bentuk ion trimethylselenonium (TMSe) diekskresi melalui urine dan bentuk volatile yaitu dimethylselenide (DMSe) diekskresi melalui paru-paru. Ekskresi melalui paru-paru ditandai dengan bau nafas seperti bawang putih.3,4,17
merkuri
(-)
Diet selenium absorbsi Sitosol usus halus -SeMet (+)
-CySeSeCy VIT. A,C,E SeMet selenohomocysteine -selenite CySeSeCy CySeSG
Selenite GSSeG GSSeH
Transport melalui Plasma Sitosol hepar Selenohomocysteine selenocysteine CySeSG Hidrogen Selenide GSSeH Membentuk Metilasi Selenoprotein: -glutathione peroksidase -thioredoksin reduktase -iodothyronine deiodinase -selenoprotein P -selenoprotein W
ion trimethylselenonium dimethyl selenide Keterangan:
-SeMet:selenomethionine
-CySeSeCy:selenocystine
-CySeSG:selenocysteine-
urine paru-paru glutathione selenenyl sulfide
-GSSeG:selenodiglutathione
-GSSeH:glutathionylselenol
2.5 Sumber Selenium
Selenium dalam tubuh berasal dari makanan dan minuman. Daging dan makanan laut mempunyai kandungan selenium yang tinggi.1 Sumber makanan yang lain, seperti sereal dan padi memiliki kandungan selenium yang bervariasi, tergantung dengan kadar selenium pada tanah. Sebagai contoh, kandungan selenium orang Inggris menurun dari 65 ke 31 μg/hari setelah sumber gandum yang semula berasal dari Amerika Utara diganti dari Eropa. Makanan yang berasal dari binatang mempunyai variasi yang lebih kecil karena binatang mempunyai kontrol homeostatik.4
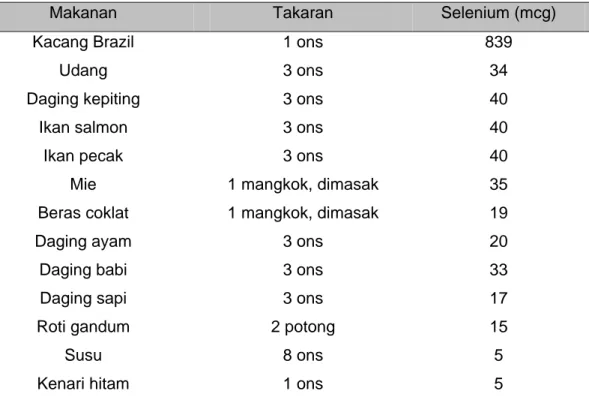
Air minum tidak mengandung selenium dalam jumlah yang cukup. ASI mengandung selenium lebih banyak daripada susu sapi. Tabel di bawah ini memperlihatkan sumber makanan yang kaya selenium berdasarkan USDA (United State Dietary Allowences).
Tabel 1. Sumber makanan yang kaya selenium
Makanan Takaran Selenium (mcg)
Kacang Brazil Udang Daging kepiting Ikan salmon Ikan pecak Mie Beras coklat Daging ayam Daging babi Daging sapi Roti gandum Susu Kenari hitam 1 ons 3 ons 3 ons 3 ons 3 ons 1 mangkok, dimasak 1 mangkok, dimasak 3 ons 3 ons 3 ons 2 potong 8 ons 1 ons 839 34 40 40 40 35 19 20 33 17 15 5 5 Dikutip dari Whanger,PD, Dept.of Environmental and Molecular Toxicology, Linus Pauling Institute, 20021
2.6 Kebutuhan selenium
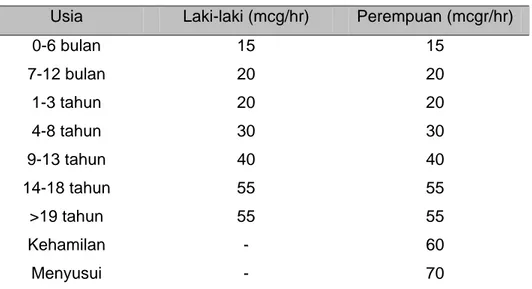
Kebutuhan selenium berdasarkan RDA (recommended dietary allowance) yang dibuat oleh Badan Nutrisi dan Makanan Amerika Serikat tahun 2000 seperti terlihat pada tabel di bawah ini. RDA ini berdasarkan jumlah selenium yang dibutuhkan untuk memaksimalkan aktifitas enzim glutathione peroksidase di dalam plasma.1
Tabel 2. Recommended Dietary Allowance (RDA) untuk selenium Usia Laki-laki (mcg/hr) Perempuan (mcgr/hr) 0-6 bulan 7-12 bulan 1-3 tahun 4-8 tahun 9-13 tahun 14-18 tahun >19 tahun Kehamilan Menyusui 15 20 20 30 40 55 55 - - 15 20 20 30 40 55 55 60 70
Dikutip dari Whanger,PD, Dept.of Environmental and Molecular Toxicology, The Linus Pauling Institute, 20021
2.7 Fungsi Selenium
Selenium berfungsi sebagai komponen dari sejumlah enzim. Enzim yang mengandung selenium disebut selenoprotein. Terdapat 11 selenoprotein yang telah diidentifikasi, yaitu kelompok glutathione peroksidase (4 jenis), kelompok iodothyronine deiodinase (3 jenis), thioredoksin reduktase, selenophosphate synthetase, selenoprotein P dan selenoprotein W.1-4
2.7.1 Iodothyronine deiodinase
Kelenjar tiroid melepaskan sejumlah kecil triiodo thyronine (T3) dan sejumlah besar thyroxine (T4) ke dalam sirkulasi. Sebagian besar T3 yang terdapat di dalam sirkulasi dan sel dibentuk dari T4 dengan membuang satu atom iodine. Reaksi ini dikatalisa oleh enzim iodothyronine deiodinase, yaitu enzim yang mengandung selenium. 1,4,19,20
Iodothyronine deiodinase terdiri dari 3 tipe yaitu tipe 1 (D1), tipe 2 (D2) dan tipe 3 (D3). D1 dapat ditemukan terutama di hepar, ginjal dan thyroid. D2 dapat ditemukan di otak, kelenjar pituitary dan jaringan lemak coklat. D3 ditemukan di kortek serebri dan kulit, dan kandungan tertinggi ditemui pada plasenta dan uterus wanita hamil.19
Ketiga enzim deiodinase ini mengandung selenium dalam bentuk selenocystein. Adanya defisiensi selenium akan mengakibatkan perubahan aktivitas deiodinase secara bermakna. Pada tikus dengan kadar selenium yang turun hampir 80% (0,01-1,1 ppm) jaringan masih dapat mempertahankan kadar aktivitas deiodinase. Tetapi jika kadar selenium turun >80% terlihat penurunan aktivitas deiodinase pada hepar, kulit dan non pregnant uterus. Sedangkan pada otak, kelenjar pituitary, thyroid, ovarium, testis dan pada jaringan lemak coklat tidak terjadi penurunan aktivitas deiodinase. Namun, anehnya walaupun terjadi penurunan aktivitas deiodinase kadar plasma T3 masih dapat dipertahankan. Bagaimana mekanisme ini terjadi masih belum diketahui.19
2.7.2 Thioredoksin reduktase
Thioredoksin reduktase adalah suatu flavoenzim yang menggunakan NADPH untuk mereduksi thioredoksin. Thioredoksin adalah protein dengan berat molekul 12 kD yang mengandung 5 molekul cysteine. Thioredoksin dan thioredoksin reduktase berperan sebagai antioksidan yang mengubah peroksida menjadi air.21,22
2.7.3 Selenoprotein P
Selenoprotein P adalah glikoprotein ekstra seluler yang ditemukan di dalam plasma. Enzim ini berhubungan dengan sel endothelial dinding bagian dalam pembuluh darah.1,4 Fungsi selenoprotein ini belum diketahui tetapi diperkirakan sebagai transport protein. Juga diperkirakan sebagai antioksidan yang melindungi sel-sel endothelial dari kerusakan oleh peroxynitrite.1
2.7.4 Selenoprotein W
Selenoprotein W ditemukan pada otot. Fungsi selenoprotein ini belum jelas tetapi diperkirakan berfungsi dalam metabolisme otot.1,4
2.7.5 Selenophosphate synthetase
Enzim ini dibutuhkan dalam penggabungan selenocystein dengan protein. Selenophosphate synthetase juga berfungsi mengkatalisa sintesa monoselenium phosphate, yang merupakan prekusor dari selenocystein.1,4
2.7.6 Glutathione peroksidase
Glutathione peroksidase adalah enzim yang berfungsi mengkatabolisme hydroperoksidase (H2O2). Terdisi dari 4 jenis enzim yang mengandung selenium,
yaitu cellular glutathioneperoksidase (GPx-1), gastrointestinal glutathione peroksidase (GPx-2), ekstra selular glutathione peroksidase (GPx-3) dan phospholipid hydroperoxide (GPx-4). Lebih jauh lagi mengenai glutathione ini akan dibahas pada bab berikutnya.1,3,4,16
2.8 Penilaian Status Selenium
Penilaian status selenium dapat dilakukan dengan dua cara: (1) Menghitung komposisi makanan yang masuk dan (2) Biokimia.23
Pemeriksaan laboratorium untuk menilai status selenium dapat dilakukan pada plasma, serum, darah, urin, rambut dan kuku. Pengukuran kadar selenium dalam urin tidak dapat memberikan hasil yang tepat karena dipengaruhi oleh pengenceran dan kadar selenium pada makanan yang dimakan sebelumnya. Pengukuran kadar selenium pada rambut telah digunakan di Cina, tetapi cara ini tidak dapat digunakan di negara-negara Barat, karena di daerah tersebut banyak menggunakan shampoo yang mengandung selenium. Pengukuran kadar selenium pada kuku telah banyak digunakan sebagai metode noninvasif. Di Amerika Serikat pada Survey Kesehatan dan Nutrisi Ketiga tahun 1988-1994 dilakukan pengukuran kadar selenium plasma, serum atau darah dengan menggunakan metode spektometri.23
Penilaian status selenium dengan mengkalkulasi asupan makanan dilakukan dengan melihat tabel komposisi makanan. Tetapi metode ini sangat riskan, karena kandungan selenium pada makanan mempunyai variasi yang luas.23
Tabel 3. Nilai konsentrasi selenium dalam jaringan/cairan tubuh pada manusia dewasa
Jaringan/cairan tubuh Konsentrasi selenium (μg/kg)
Hepar 250-400 Darah 90-130 Plasma 75-120 Urine 25-50 ASI 10-25 Rambut 500-1000 Dikutip dari: WHO. Selenium.In:Trace Elements in Human Nutrition and Health
Geneva.1996
2.9 Defisiensi Selenium 2.9.1 Etiologi
Defisiensi selenium dapat disebabkan karena: 1. Intake selenium yang tidak adekuat
Defisiensi selenium yang disebabkan intake yang tidak adekuat biasanya terdapat di daerah dimana kandungan selenium pada tanah sangat rendah, contohnya di Cina dimana intake selenium <19 mcg/hari pada laki-laki dan <13 mcg/hari pada perempuan.18 Defisiensi selenium di Cina yang berhubungan dengan penyakit jantung disebut Penyakit Keshan. Penyakit Keshan adalah kardiomiopati yang terdapat pada anak dan wanita muda yang ditandai dengan pembesaran jantung dan penurunan fungsi jantung.
Kemungkinan defisiensi selenium harus dipikirkan pada semua pasien malnutrisi yang mendapat Nutrisi Parenteral Total (NPT). Pada pasien ini defisiensi dapat terjadi karena nutrisi yang diberikan tidak mengandung selenium.18
2. Gangguan absorbsi
Gangguan gastrointestinal berat, misalnya pada penyakit Crohn’s dapat menurunkan absorbsi selenium.2
3. Peningkatan penggunaan selenium.
Kebutuhan selenium meningkat pada masa kehamilan, menyusui dan masa penyembuhan penyakit.2
2.9.2 Gejala klinik
Defisiensi selenium telah dihubungkan dengan berbagai penyakit seperti yang akan dijelaskan pada bab V.
2.10 Kelebihan selenium
Kadar selenium yang tinggi masih dapat ditoleransi untuk jangka waktu yang pendek. Keracunan akut dan fatal terjadi karena kecelakaan atau usaha bunuh diri dengan menelan sejumlah besar selenium. Keracunan kronis selenium terjadi dengan menelan dosis yang lebih kecil dalam waktu lama. Gejala-gejala yang umum ditemukan pada kelebihan selenium adalah rambut rontok, kuku yang rapuh, gangguan pencernaan, dermatitis, bau nafas seperti bau bawang, rasa metalik, kelemahan dan bahkan kematian.1,4
Badan Nutrisi dan Makanan Amerika Serikat menetapkan batas atas untuk selenium yaitu 400 mcg/hr pada dewasa, 150 mcg/hr pada anak dan 45 mcg/hr pada bayi.1
BAB III
ENZIM GLUTATHIONE PEROKSIDASE
3.1 Fisiologi
Glutathione peroksidase (GPx) adalah protein dengan bentuk tetramer. Mempunyai berat molekul sebesar 85.000 D. Enzim ini mengandung 4 atom selenium yang terikat sebagai selenocysteine. Struktur enzim ini dapat dilihat pada gambar 3.24,25,26
Gambar. 3 Struktur Glutathione peroksidase. Didapat dari
Anonim. Glutathione peroksidase. 2000. Didapat dari: www.wikipedia/thefreeencyclopedia.
Enzim glutathione peroksidase membantu mencegah kerusakan sel yang disebabkan oleh radikal bebas dengan cara mengkatalisa berbagai hidroperoksida. Glutathione peroksidase mereduksi H2O2 menjadi H2O dan glutathione disulfide
(GSSG) dengan bantuan glutathione tereduksi (GSH). Reaksi enzim tersebut seperti di bawah ini.24
H2O2 + 2GSH GPX GSSG + 2H2O
Selenium yang mengandung enzim glutathione peroksidase terdiri dari empat jenis, yaitu seluler glutathione peroksidase (GPx-1), gastrointestinal glutathione peroksidase (GPx-2), ekstraseluler glutathione peroksidase (GPx-3) dan phospholipid hydroperoksidase (GPx-4).1,3,4,16
Persamaan dari keempatnya adalah:27 1. Aktifitas enzim tergantung selenium
3. Adanya reaksi enzimatik bolak-balik pada proses reduksi peroksida 4. Oksidasi selenium yang diikuti oleh reduksi yang diperantarai glutathione
3.1.1 Seluler Glutathione Peroksidase (GPx-1/cGPx)
Seluler glutathione peroksidase adalah enzim yang mengandung selenium yang pertama kali ditemukan. Terdiri dari homotetramer dengan subunit yang berukuran 22 kDa dan terdapat di seluruh jaringan tubuh. GPx-1 memegang peranan penting dalam melindungi sel dari kerusakan yang disebabkan oleh paraquat, yaitu suatu radikal bebas yang dapat menghasilkan lipid peroksidase. Garberg dan Thullberg, 199628 telah menunjukkan bahwa GPx-1 merupakan bentuk metabolik selenium tubuh yang utama yang melindungi sel dari oksidatif stress akut yang disebabkan oleh kadar paraquat yang tinggi tetapi tidak begitu penting pada oksidatif stress dengan kadar yang relatif rendah. Tetapi menurut penelitian oleh Wen-Hsing Cheng, 199828,29, peranan antioksidan cGPx secara in vivo belum jelas, sebab tidak terdapat hubungan langsung antara rendahnya GPx dan gejala-gejala penyakit yang berhubungan dengan selenium.
Bermano, dkk (1995), Lei, dkk (1995), menyatakan bahwa GPx-1 merupakan bentuk penyimpanan selenium dalam tubuh untuk menjaga fungsi homeostasis selenium.28
3.1.2 Gastrointestinal Glutathione Peroksidase (GPx-2/GPx-GI)
GPx-GI merupakan selenium yang mengandung enzim glutathione peroksidase yang terdapat di dalam sel. Ditemukan dari isolasi GPx-GI cDNA sel hepar manusia (HepG2). Paling banyak ditemukan di mukosa epitel traktus gastrointestinal. GPx-GI dibedakan dengan GPx-1 berdasarkan komposisi DNA, dimana pada GPx-GI terdapat 1.9 kilobase GPx-GI mRNA. GPx-GI juga tidak bereaksi dengan antisera manusia yang mengandung GPx-1 dan GPx plasma.30 Aktifitas GPx-GI dan GPx-1 dapat ditemukan pada traktus gastrointestinal bagian tengah dan bawah, terutama pada kripta dan villi usus.31 GPx-GI pada villi berfungsi untuk melindungi epitel villi, sedangkan villinya sendiri dilindungi oleh eGPx.32
GPx-1 dan 2 mempunyai persamaan dalam hal antioksidan yaitu sama-sama mereduksi H2O2, terbutyl hydroperoxide, cumene hydroperoxide dan linoleic acid
gastrointestinal menunjukkan bahwa enzim ini melindungi tubuh dari lipid hydroperoxide yang tertelan.30
3.1.3 Ekstraseluler Glutathione Peroksidase (GPx-3/eGPx)
Ekstraseluler glutathione peroksidase adalah selenoprotein yang dapat mereduksi hydrogen peroxide, organik hydroperoxide, free fatty acid hydroperoxide dan phosphatidylcholine hydroperoxide. eGPx dapat ditemukan di dalam plasma dan cairan ekstraseluler lainnya, seperti pada ASI , cairan amnion, cairan eksoselom dan cairan yang berasal dari bilasan paru.27,32
Sumber utama eGPx berasal dari ginjal dan dalam jumlah kecil juga disintesa di paru, jantung dan usus.27,32 Orang yang tidak mempunyai ginjal menunjukkan aktifitas eGPx yang rendah, yaitu hanya sebesar 5-25% normal.27 Hal ini mengindikasikan bahwa ginjal merupakan sumber utama eGPx. eGPx disintesa di tubulus proksimal dan disekresikan melalui membran basolateral epitel tubulus proksimal. Selain disintesa di ginjal eGPx juga disintesa di paru, jantung dan intestinal, terutama di epitel villi caecum.27,32
eGPx berbentuk homotetramer dengan ukuran subunit 23 kDa. Konsentrasi glutathione plasma lebih rendah bila dibandingkan dengan konsentrasi di dalam sel, yaitu 1-5 μM di plasma dan 1-10 mM di dalam sel. Sedangkan konsentrasi glutathione di cairan interstitial ginjal tidak diketahui.27 eGPx berbeda dengan cGPx berdasarkan imunologi dan karakteristik biokimia. Asam amino eGPx dan cGPx hanya identik sebesar 45%.
3.1.4 Phospholipid-hydroperoxide Glutathione Peroksidase (PhGPx)
PhGPx adalah selenoenzim yang dapat mereduksi phospholipid hydroperoxide, cholesterol dan cholesteryl ester melalui glutathione. PhGPx juga dapat mereduksi 7-hidroksikolesterol yang merupakan sitotoksin utama dari lipoprotein yang teroksidasi. Lipid-lipid ini tidak dapat direduksi oleh GPx-1.33
PhGPx telah diisolasi dari jantung babi, hepar dan otak, sitosol dan mitokondria testis tikus dan hepar manusia. Berdasarkan analisa biokimia PhGPx adalah protein yang terdiri dari 170 asam amino dengan ukuran 20 kDa. cDNA yang mengkode PhGPx telah diisolasi dari jantung babi, blastokista dan testis manusia.33
PhGPx mempunyai 2 bentuk, yaitu L-form dengan berat molekul 23 kDa dan S-form dengan berat molekul 20 kDa. L-form adalah PhGPx yang terdapat di mitokondria sedangkan S-form disebut PhGPx non mitokondria.34
Kadar tertinggi PhGPx terdapat pada daerah antara membran luar dan dalam mitokondria testis tikus dimana regulasinya diatur oleh gonadotropin. PhGPx dapat dideteksi di dalam sitoplasma, mitokondria, membran plasma dan nuclear, tetapi struktur dasar PhGPx pada lokasi ini belum diketahui.35
PhGPx mitokondria mencegah kematian sel yang disebabkan oleh kalium sianida (KCN). KCN adalah inhibitor pada rantai respirasi mitokondria yang dapat menyebabkan pembentukan reactive oxygen spesies (ROS).35 PhGPx mitokondria mencegah perubahan fungsi mitokondria dan kematian sel dengan cara mengurangi pembentukan seluler hidroperokside.34
BAB IV OKSIDAN (RADIKAL BEBAS)
4.1 Definisi
Radikal bebas adalah suatu molekul dimana elektron yang terletak pada lapisan paling luar tidak mempunyai pasangan (Greenwald, 1991; Halliwell, 1995). Adanya molekul dengan elektron yang tidak berpasangan ini membuat mereka sangat reaktif.8-10 Reaktif artinya mereka mempunyai spesifisitas yang rendah sehingga mereka mampu bereaksi dengan molekul-molekul yang berada disekitarnya. Molekul-molekul tersebut termasuk protein, lipid, karbohidrat dan DNA. Reaktif juga berarti mereka tidak bertahan lama dalam bentuk “asli” karena untuk mempertahankan kestabilan molekul, mereka harus mengambil satu elektron dari molekul yang lain. Artinya, radikal bebas menyerang molekul stabil yang berada di dekatnya dan mengambil elektron dari molekul tersebut. Molekul yang diambil elektronnya kemudian juga menjadi radikal bebas dan mengambil elektron dari molekul lain, begitulah seterusnya sampai terjadi kerusakan sel. Karena molekul-molekul yang sangat reaktif ini sebagian besar berasal dari oksigen maka secara umum molekul-molekul tersebut disebut reactive oxygen species (ROS).8
Gambar 4. Molekul stabil dan radikal bebas. Didapat dari Fouad T. Free Radical, Types, Source and Damaging Reactions. Didapat dari: www. thedoctorslounge.net /medlounge/articles/antioxidant.
4.2 Fisiologi
Radikal bebas dapat ditimbulkan baik secara in vitro maupun invivo dengan mekanisme sebagai berikut:8
1. Pemecahan ikatan kovalen. Cara ini tidak lazim pada sistem biologi karena memerlukan energi yang tinggi, seperti sinar ultra violet atau radiasi ion.
2. Molekul normal yang kehilangan satu elektron
3. Penambahan satu elektron pada molekul yang normal.
Radikal bebas dapat bermuatan positif, negatif atau netral. Elektron yang tidak berpasangan dapat menambah molekul yang bersifat netral sehingga molekul tersebut menjadi bermuatan negatif. Molekul bermuatan negatif juga dapat terbentuk dari molekul bermuatan positif yang kehilangan elektron. Molekul yang asalnya tidak netral dengan penambahan atau pengurangan elektron dapat menjadi netral.8
Sebagian besar radikal bebas terbentuk di dalam sel melalui transfer elektron di mitokondria dan retikulum endoplasmik. Transfer elektron tersebut dapat diperantarai secara enzimatik atau non enzimatik.8
4.3 Patofisiologi
Dalam keadaan normal radikal bebas yang terbentuk dapat dinetralisir oleh antioksidan tetapi bila kadar reactive oxygen species (ROS) yang toksik melebihi pertahanan antioksidan endogen maka akan terjadi suatu keadaan yang disebut stres oksidatif. Pada tahap ini kelebihan radikal bebas dapat bereaksi dengan sel lipid, protein dan asam nukleat, sehingga menyebabkan kerusakan lokal bahkan dapat sampai terjadi disfungsi organ. Lemak adalah molekul yang paling rentan untuk diserang radikal bebas.8
4.3.1 Peroksidasi Lipid
Membran sel terdiri dari 2 lapisan yang kaya akan sumber asam lemak tak jenuh ganda (Poly Unsaturated Fatty Acid/PUFA). Pada lapisan luar membran sel bersifat hidrofilik sedangkan lapisan dalam bersifat lipofilik (gb. 5A). Dibagian dalam membran sel terdapat protein yang merupakan bagian yang paling penting dari sel. Protein tersebut berfungsi mengontrol pergerakan ion atau berfungsi sebagai reseptor sel.
Radikal bebas dapat mengambil elektron dari lipid yang berada di membran sel. Reaksi ini disebut peroksidasi lipid. Sasaran reactive oxygen species (ROS) adalah karbon-karbon dengan ikatan ganda dari molekul PUFA. Adanya ikatan ganda ini menyebabkan ikatan antara karbon dan hydrogen menjadi lemah dan mudah terdisosiasi menjadi radikal bebas. Radikal bebas akan mengambil satu elektron dari hydrogen yang berikatan ganda dengan karbon. Molekul yang terbentuk kemudian bereaksi dengan oksigen membentuk radikal peroksil. Radikal peroksil kemudian mengambil satu elektron dari molekul lipid yang lain, begitulah seterusnya (gb. 5B).
Antioksidan dapat menetralisir dengan cara bereaksi dengan radikal peroksil. Vitamin E (tokoferol) dapat mereduksi radikal peroksil menjadi lipid yang teroksidasi. Lipid yang teroksidasi ini kemudian dikonversi oleh glutathione peroksidase menjadi lipid alkohol yang tidak berbahaya.10,36
4.3.2 Kerusakan Protein
Adanya peroksidasi lipid dapat mengubah struktur dan fungsi protein. Perubahan struktur dan fungsi ini menyebabkan hilangnya regulasi intra seluler Ca2+ oleh Ca2+ ATPase. Hilangnya regulasi ini dapat menyebabkan kematian sel (Thomas & Reed, 1989).36
Gb. 5A. Membran sel dengan 2 lapis lipid
Gb. 5B. 1. Radikal bebas menarik electron dari molekul lipid 2. Radikal lipid menarik electron dari lipid disebelahnya 3&4. Fungsi protein mengalami kerusakan
5. Pembentukan radikal dapat merusak struktur yang berjauhan
Didapat dari Bottje W, Enkvetchakul B, Wideman RF. Antioxidant, Hypoxia and Lipid Peroxidation Involvement in Pulmonary Hypertension Syndrome (Ascites). Didapat dari: www.yahoo.com.
4.3.3 Kerusakan DNA
Kromatin dapat melindungi DNA dari proses oksidasi oleh radikal bebas. Tetapi jumlah radikal bebas yang melebihi pertahanan ini dapat menyebabkan mutasi gen. Adanya paparan yang lama dari stress oksidatif dapat menimbulkan proses karsinogenesis.
Kemampuan radikal bebas untuk menyebabkan mutasi disebabkan oleh interaksi langsung radikal hidroksil (OH) dengan semua komponen molekul DNA. Yang selanjutnya dapat menyebabkan kerusakan genetik. Kerusakan genetik yang disebabkan oleh radikal bebas dapat berupa modifikasi rantai, penembahan rantai, delesi, pemutusan rantai, pergantian rantai, pertukaran protein DNA atau penyusunan kembali kromosom.37
4.4 Sumber Oksidan
Radikal bebas dapat bersumber dari dua tempat, yaitu (1) endogen dan (2) eksogen.8
4.4.1 Sumber Endogen a. Organella Subseluler
Organella subseluler seperti mitokondria, kloroplas, mikrosome, peroksisome dan nuklei dapat menghasilkan superokside (O2-).8
Mitokondria merupakan penghasil utama energi dalam sel sehingga disebut the powerhouse of the cell. Energi yang dihasilkan berbentuk adenosine trifosfat (ATP) melalui suatu rantai transpor elektron dan oksigen merupakan rantai terakhir penerima elektron.8,36
Proses metabolisme ini tidak 100% efisien, terdapat sejumlah besar energi yang hilang berupa panas. Lebih kurang 2-4% oksigen yang
dikonsumsi oleh mitokondria tidak direduksi menjadi air tetapi direduksi menjadi superokside atau hydrogen peroksida.36
Adanya kerusakan pada sistem transport elektron pada mitokondria memungkinkan O2 untuk menerima satu elektron sehingga terbentuk O2
-(Halliwell,1995). Pembentukan superoksida oleh mitokondria dapat terjadi pada 2 keadaan, (1) jika konsentrasi oksigen meningkat atau (2) jika terjadi iskemia (gb. 6).8
Gb 6. Metabolisme mitokondria. Didapat dari Didapat dari Bottje W, Enkvetchakul B, Wideman RF. Antioxidant, Hypoxia and Lipid Peroxidation Involvement in Pulmonary Hypertension Syndrome (Ascites). Didapat dari: www.yahoo.com.
Mikrosome sitokrom P450 dapat menghasilkan H2O2 sebesar 80% in
vivo jika terjadi hiperoksia. (Jamieson, dkk, 1986).8
Peroksisome diketahui dapat membentuk H2O2 tetapi tidak
membentuk O2- pada keadaan fisiologis (Chance, dkk, 1979).32 Pada
kondisi kelaparan yang lama, peroksisome dapat mengoksidasi asam lemak menjadi H2O2.
b. Inflamasi
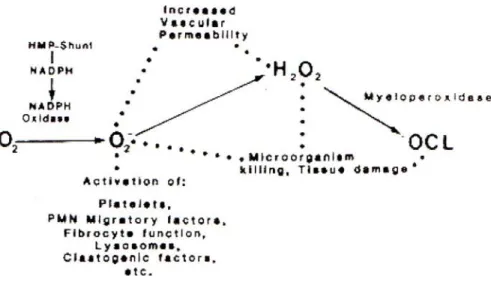
Selama inflamasi terjadi proses fagositosis oleh makrofag dan neutrofil36. Makrofag dan neutrofil harus membentuk radikal bebas agar dapat memfagositosis bakteri. Pada tahap pertama bakteri akan masuk ke dalam fagosome dan berdifusi ke dalam lisosome. Pada membran lisosome terdapat enzim NADPH (Nikotinamide Adenine Dinukleotide Phosphate) oksidase yang berfungsi mengkatalisa pembentukan superokside. Reaksi ini membutuhkan oksigen dalam jumlah besar sehingga disebut respiratory burst.
Selanjutnya enzim superokside dismutase (SOD) akan mengubah superokside menjadi hydrogen peroksida. Hydrogen peroksida selanjutnya akan menghancurkan bakteri.
Neutrofil menghancurkan bakteri menggunakan enzim myeloperoksidase. Enzim ini mengkatalisa reaksi antara hydrogen peroksida dengan ion kloride untuk menghasilkan antiseptik ion hipokloride.36,38
Gambar 7. Terbentuknya reactive oxygen species selama inflamasi. Didapat dari Proctor PH. Free Radicals and Human Disease. Dalam: CRC Handbook of Free Radicals and Antioxidants. Volume 1. 1989, hal. 209-21.
c. Ion Metal Transisi
Ion metal transisi adalah elemen dimana salah satu bentuk ionnya pada orbital d tidak terisi penuh. Di alam terdapat 30 elemen yang disebut ion metal transisi. Besi dan tembaga merupakan ion metal transisi yang terdapat di dalam tubuh manusia.40
Besi dan tembaga memegang peranan utama dalam membentuk radikal bebas dan menimbulkan peroksidasi lipid. Ion metal transisi ikut dalam reaksi Haber-Weiss, dimana reaksi ini dapat menghasilkan radikal hidroksil (.OH).8
O2- + Fe3+ Æ Fe2+ + O2
H2O2 + Fe2+ Æ Fe3+ + OH- + .OH
d. Oksidasi enzimatik
Beberapa enzim dapat membentuk radikal bebas dalam jumlah yang cukup bermakna. Enzim-enzim tersebut adalah xantin oksidase, prostaglandin sintase, lipoksigenase, aldehide oksidase dan asam amino oksidase. Enzim mieloperoksidase menggunakan hydrogen peroksida untuk mengoksidasi ion klorid, sehingga menghasilkan oksidan yang kuat, yaitu asam hipoklorus (HOCl).8
e. Auto-oksidasi
Auto-oksidasi adalah suatu proses yang terjadi di dalam lingkungan aerobik. Molekul yang mengalami proses auto-oksidasi adalah katekolamin, hemoglobin, mioglobin, sitokrom C dan thiol. Auto-oksidasi dari molekul-molekul tersebut akan menghasilkan radikal bebas yang mengandung oksigen. Superoksida adalah radikal bebas utama yang terbentuk pada proses ini.8
f. Reperfusi pada Iskemia
Dalam keadaan normal, xantine oksidase mengkatalisis reaksi hipoxantine menjadi xantine dan selanjutnya xantine diubah menjadi asam urat. Reaksi ini membutuhkan penerima elektron sebagai kofaktor. Selama periode iskemia terdapat 2 keadaan, (1) meningkatnya produksi
xantine dan xantine oksidase (2) tidak adanya antioksidan superoksid dismutase dan glutathione peroksidase. Molekul oksigen yang disuplai selama proses reperfusi bertindak sebagai penerima elektron dan kofaktor bagi xantine oksidase. Hal ini menimbulkan pembentukan O2
-dan H2O2. Latihan yang berat juga dapat mencetuskan reaksi xantine
oksidase dan membentuk radikal bebas pada otot rangka dan jantung.8
4.4.2 Sumber Eksogen a. Obat-obatan
Sejumlah obat-obatan dapat membentuk radikal bebas. Mekanismenya diperkirakan bahwa obat-obatan tersebut memperkuat hiperoksia yang sudah terjadi. Obat-obatan tersebut adalah antibiotik golongan quinolon atau antibiotik yang berikatan dengan metal untuk aktifitasnya (nitrofurantoin), antineoplastik (bleomisin), adriamisin (Fisher, 1988) dan metotreksat (Gressier dkk,1994). Obat-obatan seperti penisilamin, fenilbutazon, asam mefenamat dan aminosalisilat (komponen sulfasalazin) dapat menambah pembentukan radikal bebas dengan cara menurunkan kerja asam askorbat.
b. Radiasi
Radioterapi dapat menyebabkan kerusakan jaringan melalui pembentukan radikal bebas. Radiasi elektromagnetik (sinar X, sinar gamma) dan radiasi partikel (elektron, proton, neutron dan partikel alfa dan beta) menghasilkan radikal bebas melalui transfer energi ke komponen seluler.
c. Tembakau (Rokok)
Oksidan yang dihasilkan oleh tembakau memegang peranan penting dalam terjadinya kerusakan saluran nafas. Oksidan yang dihasilkan tembakau menurunkan jumlah antioksidan intraseluler yang terdapat di dalam sel paru-paru. Satu kali isapan rokok menghasilkan oksidan dalam jumlah yang besar, yaitu aldehide, epokside, perokside. nitrik okside, radikal peroksil dan karbon dapat terbentuk selama fase “gas”. Oksidan yang lebih stabil dihasilkan pada fase “tar”, yaitu semiquinone.
d. Partikel Inorganik
Partikel inorganik, yang terinhalasi, seperti asbes, silika dapat merusak paru-paru melalui pembentukan radikal bebas. Inhalasi asbes telah dihubungkan dengan peningkatan risiko terjadinya fibrosis pulmonal (asbestosis), mesotelioma dan karsinoma bronkogenik. Partikel silika dan asbes difagositosis oleh makrofag paru-paru. Sel ini kemudian pecah, melepaskan enzim proteolitik dan kemotaktik mediator yang menyebabkan infiltrasi sel-sel lain, seperti neutrofil. Maka dimulailah proses inflamasi. (Kehrer dkk, 1988). Serat asbes yang mengandung besi juga dapat menstimulasi pembentukan radikal hidroksil.
e. Gas
Ozon bukanlah radikal bebas tetapi merupakan agen pengoksidasi yang sangat kuat. Ozon (O3) memiliki dua elektron yang tidak
berpasangan dan bereaksi dengan substrat biologik membentuk radikal bebas. Secara in vitro ozon dapat menghasilkan lipid peroksidase, tetapi in vivo belum dapat dibuktikan.8
4.5 Tipe Oksidan
Radikal bebas yang paling penting di dalam tubuh adalah radikal yang berasal dari oksigen yang disebut reactive oxygen species. Radikal bebas tersebut adalah oksigen dalam bentuk triplet singlet (1O2), anion superokside (O2-), radikal
hidroksil (.OH), nitrik okside (NO), peroksinitrit (ONOO-), hypochlorous acid (HOCl), hydrogen peroksida (H2O2), dan radikal peroksil (LO2).8-10
4.5.1 Superokside (O2-)
Anion superokside terbentuk jika oksigen direduksi melalui transfer satu elektron. Secara invivo, sumber utama superokside berasal dari rantai transport elektron pada mitokondria. Superokside sebenarnya tidak merusak, tetapi anion ini dapat bereaksi dengan ion metal transisi membentuk radikal hidroksil yang sangat merusak.
Sumber utama lainnya adalah melalui enzim NADPH oksidase yang terdapat pada makrofag.
4.5.2 Hidrogen Peroksida (H2O2)
Hidrogen peroksida merupakan agen pengoksidasi untuk membentuk radikal hidroksil dalam reaksi dengan ion metal transisi. Hidrogen peroksida terbentuk dari oksigen yang mengalami reduksi dua elektron. Pada sistem biologi, hydrogen peroksida terbentuk dari superokside. Dua molekul superokside dapat bereaksi membentuk hydrogen peroksida dan oksigen, seperti terlihat pada reaksi di bawah ini.
2O2- + 2H Æ H2O2 + O2
4.5.3 Radikal hidroksil (.OH)
Radikal hidroksil adalah radikal yang sangat reaktif. Radikal ini dapat bereaksi dengan hampir seluruh biomolekul, artinya, reaksi akan segera timbul pada molekul biologis.
Pada tahun 1933 Fritz Haber dan Joseph Weiss menemukan bahwa radikal bebas hidroksil terbentuk oleh superokside dan hydrogen peroksida (reaksi Haber-Weiss).
O2- + H2O2 Æ O2 + .OH + OH
-Henty Fenton telah meneliti agen pereduksi, ion ferro (Fe2+) bersama dengan hydrogen peroksida dapat mengoksidasi senyawa organik. Mekanismenya melibatkan radikal hidroksil.
H2O2 + Fe2+ Æ .OH + OH- + Fe3+
4.5.4 Singlet oksigen (O2)
Singlet oksigen merupakan agen pengoksidasi yang sangat kuat. Singlet oksigen dapat terbentuk dari reaksi enzimatik, seperti peroksidase, atau oleh reaksi hydrogen peroksidase dengan peroksinitrit.
4.5.5 Nitrik okside (NO.)
Merupakan radikal bebas dalam bentuk gas. Dikenal mempunyai peranan dalam fisiologi vaskuler sebagai faktor perelaksasi endothelium. Endotelium vaskuler menghasilkan nitrik okside dari arginine menggunakan enzim nitrik okside sintetase. Reaksi ini dapat distimulasi oleh sitokin, faktor nekrosis tumor atau interleukin.
4.5.6 Peroksinitrite (ONOO-)
Terbentuk dari reaksi nitrik okside dengan superokside.
4.5.7 Hypochlorous acid (HOCl)
Sebagai agen bakterisidal, sel PMN menghasilkan HOCl. Terbentuk oleh reaksi dari ion kloride dengan hydrogen peroksida yang dikatalisa oleh enzim myeloperoksidase.
H2O2 + Cl- ÆHOCl + OH
-Reaksi ini timbul pada vakuole neutrofil setelah berfusi dengan vesikel lisosome yang mengandung mieloperoksidase.
Hypochlorous acid dapat melewati membran sel, dan jika bereaksi dengan ion metal transisi dapat membentuk radikal hidroksil. HOCl dapat memulai peoksidasi lipid dan selanjutnya merusak sel.
HOCl +O2- Æ .OH + Cl- + O2
BAB V ANTIOKSIDAN
5.1 Definisi
Antioksidan adalah zat kimia dengan konsentrasi rendah, secara signifikan dapat mencegah atau mereduksi suatu zat yang teroksidasi (Halliwell, 1995).41
Disebut antioksidan karena zat tersebut dapat melawan proses oksidasi. Zat-zat ini melindungi bahan kimia lain dari reaksi oksidasi yang dapat merusak sel. Antioksidan bekerja dengan cara bereaksi dengan radikal bebas yang ada di dalam tubuh.
5.2 Klasifikasi Antioksidan Utama
Antioksidan dibagi menjadi dua golongan besar, yaitu antioksidan non-enzimatik dan antioksidan non-enzimatik. Klasifikasi selengkapnya dapat dilihat pada tabel 4.41
Tabel. 4 Klasifikasi antioksidan
Enzim Antioksidan Peranan Ciri-ciri
Superokside dismutase (SOD): mitokondrial, sitoplasmik, ekstraseluler MengubahO2 -menjadi H2O2 Mengandung mangan (MnSOD) Mengandung
tembaga dan seng (CuZnSOD)
Mengandung tembaga (CuSOD) Katalase Mengubah H2O2 menjadi H2O Hemoprotein
berbentuk tetramer Glutathione peroksidase
(GPx)
Mengubah H2O2 dan lipid
perokside Selenoprotein Terutama berada di sitosol dan mitokondria Menggunakan GSH Vitamin Alpha tokoferol Memutus peroksidase lipid
Scavenge lipid perokside,
O2
dan .OH
Vitamin yang larut dalam lemak
Beta karotene scavenge O2
-, bereaksi langsung dengan peroksil
Vitamin larut dalam lemak
Asam askorbat scavenge secara langsung
OH,O2
-Menetralkan oksidan dari stimulasi neutrofil
Berperan dalam regenerasi vit.E
Vitamin larut dalam air
Dikutip dari: Fouad T. Antioxidant system
5.2.1 Antioksidan Non-enzimatik 5.2.1.1 Alfa tokoferol (Vitamin E)
Alfa tokoferol adalah antioksidan yang larut dalam lemak yang terdapat di dalam sel. Alfa tokoferol ditemukan sekitar awal 1920-an. Nama tokoferol pertama kali digunakan oleh Evans. Tokoferol berasal dari kata Yunani, tokos berarti kelahiran bayi, phero berarti membawa kemajuan dan ol menunjukkan bahwa molekulnya mengandung alkohol. Vitamin E adalah istilah umum untuk menunjukkan semua aktifitas biologi vitamin E alami, yaitu d-alfa-tokoferol. Di alam, terdapat 8 substansi yang memiliki aktifitas vitamin E, yaitu kelompok tokoferol (alfa, beta, gamma dan delta-tokoferol) dan kelompok tokotrienol ((alfa, d-beta, d-gamma, dan d-delta-tokotrienol). Kedua kelompok ini berbeda dalam hal metilasi dan rantainya. Dari semuanya, d-alfa-tokoferol mempunyai aktifitas biologik yang paling tinggi sehinga dijadikan sebagai standard bagi yang lain.
Vitamin E adalah nutrisi esensial yang berfungsi sebagai antioksidan di dalam tubuh manusia. Disebut esensial karena tubuh tidak dapat membuat sendiri, sehingga harus disediakan dari makanan. Tokoferol terdapat dalam minyak, kacang, gandum dan padi. Absorbsi tokoferol didalam usus berhubungan dengan absorbsi lemak. Lebih kurang 40% tokoferol yang dimakan akan diabsorbsi. Tokoferol masuk ke dalam darah melalui pembuluh limfe sebagai kilomikron. Vitamin E disimpan di jaringan lemak dan terkonsentrasi di mitokondria, retikulum endoplasmik dan membran plasma.
Vitamin E lebih tepat disebut sebagai antioksidan daripada vitamin. Karena tidak seperti vitamin yang lain, vitamin E tidak bertindak sebagai ko-faktor bagi reaksi enzimatik. Vitamin E juga tidak menimbulkan suatu penyakit yang khas seperti vitamin yang lain. Defisiensi vitamin E dapat terjadi jika terdapat malabsorbsi lemak, bayi prematur dan penderita yang mendapat nutrisi parenteral total. Efek dari intake vitamin E yang inadekuat biasanya baru tampak dalam jangka panjang dan biasanya berhubungan dengan penyakit kronis, seperti kanker dan atherosklerosis.
Fungsi utama vitamin E adalah mencegah peroksidasi membran fosfolipid. Karakteristik vitamin E yang lipofilik memungkinkan tokoferol berada di lapisan dalam sel membran (Halliway dan Getteridge, 1992).Tokoferol OH dapat memindahkan atom hidrogen dengan satu elektron ke radikal bebas dan membersihkan radikal bebas sebelum radikal bebas bereaksi dengan protein
membran sel atau bereaksi membentuk lipid peroksidasi. Tokoferol-OH yang bereaksi dengan radikal bebas membentuk tokoferol-O. Tokoferol-O sendiri adalah radikal bebas juga. Tokoferol-O akan bereaksi lagi dengan vitamin C membentuk semidehidroaskorbat, suatu radikal bebas yang lemah.
5.2.1.2 Beta karoten
Karotenoid adalah mikronutrien yang memberi warna pada buah dan sayuran. Karotenoid adalah prekursor vitamin A dan mempunyai efek antioksidan. Ada lebih dari 600 karotenoid telah ditemukan di dalam makanan. Yang paling sering adalah alfa-karoten, beta-karoten, likopen, krosetin, santaantin dan fukosantin. Beta-karoten adalah jenis yang paling banyak diteliti. Beta karoten terdiri dari dua molekul vitamin A (retinol). Beta karoten yang berasal dari diet diubah menjadi retinol di mukosa intestinal.
Fungsi beta karoten sebagai antioksidan adalah kemampuannya untuk bereaksi dengan radikal bebas. Tetapi kemampuan beta karoten bereaksi dengan radikal bebas juga terbatas karena karotenoid sendiri dapat mengalami oksidasi (auto-oksidasi).
5.2.1.3 Asam askorbat (vitamin C)
Asam askorbat adalah vitamin yang larut dalam air. Antioksidan yang terdapat dalam buah jeruk, kentang, tomat dan sayuran yang berwarna hijau. Manusia tidak mampu mensintesa l-askorbic acid dari d-glukosa karena tidak mempunyai enzim l-gulakolakton oksidase. Oleh sebab itu manusia memperoleh asam askorbat dari diet.
Fungsi antioksidan vitamin C adalah kemampuannya sebagai agen pereduksi (donor elektron) radikal bebas. Pemberian satu elektron yang berasal dari asam askorbat membentuk radikal semi-dehidroaskorbat (DHA). Askorbat bereaksi dengan O2- dan OH untuk membentuk DHA. Menurut penelitian Jialal,1990, askorbat
mempunyai kemampuan yang lebih kuat daripada tokoferol dalam menghambat oksidasi LDL. Konsentrasi askorbat yang digunakan untuk menghambat oksidasi LDL adalah sebesar 40-60 ppm. 41
5.2.2 Antioksidan Enzimatik
5.2.2.1 Superoksid dismutase (SOD)
SOD adalah enzim intraseluler. SOD terdapat dalam tiga bentuk: (1) Cu-Zn SOD yang terdiri dari dua sub unit dan terdapat di dalam sitoplasma (2) Mn-SOD di dalam mitokondria dan (3) Cu-SOD yang terdapat di ekstraseluler.
SOD bereaksi dengan radikal bebas sebagai pereduksi superoksid untuk membentuk H2O2. Enzim katalase dan glutathione peroksidase mereduksi H2O2
menjadi H2O. Masing-masing enzim tersebut bekerja dengan sistem umpan balik.
Peningkatan superoksid akan menghambat glutathione peroksidase dan katalase. Peningkatan H2O2 akan menurunkan aktifitas CuZn-SOD. Sementara katalase dan
glutathione peroksidase dengan mereduksi H2O2 akan menghemat SOD. SOD
dengan mereduksi superoksid akan menghemat katalase dan glutathione peroksidase. Melalui sistem umpan balik ini tercapailah keadaan SOD, katalase, glutathione peroksidase, superoksid dan H2O2 dalam keadaan seimbang.
5.2.2.2 Enzim Katalase
Enzim ini adalah protein yang terdapat di semua sel aerob pada jaringan tubuh. Katalase terutama terkonsentrasi pada hati dan eritrosit. Otak, otot rangka, jantung hanya mengandung katalase dalam jumlah sedikit.
Katalase dan glutathione peroksidase mengubah hidrogen peroksida menjadi air dan oksigen. Peningkatan produksi hidrogen peroksida oleh enzim SOD tanpa diikuti peningkatan katalase atau glutathione peroksidase akan menyebabkan penumpukan hidrogen peroksida.41
5.2.2.3 Enzim Glutathione peroksidase
Enzim ini sudah dijelaskan di dalam bab sebelumnya.
Interaksi enzim-enzim tersebut terhadap radikal bebas dapat dilihat pada reaksi di bawah ini.
SOD
1. 2O2- + 2H+ H2 O2 + O2
GPx
5.3 Fisiologi
Tubuh manusia mempunyai beberapa sistem antioksidan endogen. Sistem ini dibagi menjadi dua bagian, yaitu kelompok enzimatik dan non enzimatik. Antioksidan bekerja dalam 3 cara yaitu: (1) Pemutusan rantai reaksi (2) Mengurangi pembentukan radikal bebas dan (3) “Memakan” (scavenge) radikal bebas
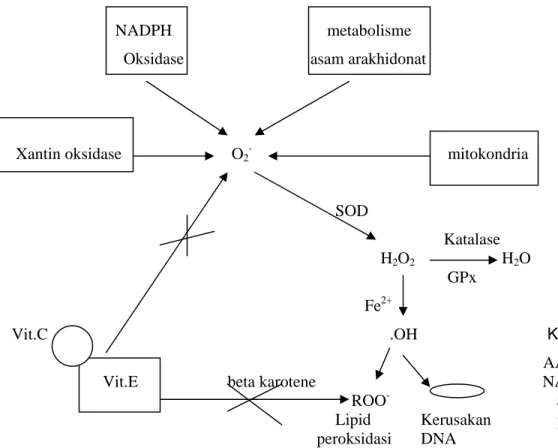
Gambar 5 memperlihatkan sumber radikal bebas dan tempat kerja dari berbagai antioksidan. Radikal superokside (O2-) merupakan bentuk yang paling
reaktif yang paling banyak dihasilkan oleh berbagai mekanisme di dalam tubuh antara lain, mitokondria, sistem enzim NADPH oksidase, reaksi dari xantine oksidase dan metabolisme asam arakidonat. Radikal superokside kemudian dapat langsung di “makan” oleh antioksidan vitamin E atau diubah menjadi H2O2 yang
kemudian diubah lagi menjadi air oleh enzim glutathione peroksidase. H2O2 yang
terbentuk juga dapat diubah menjadi radikal hidroksil (.OH). Jika tidak dinetralisir, .OH akan merusak lipid dan DNA.
NADPH metabolisme Oksidase asam arakhidonat
Xantin oksidase O2 mitokondria SOD Katalase H2O2 H2O GPx Fe2+
Vit.C .OH Ket:
AA:asam arakhidonat
Vit.E beta karotene NADPH:Nikotinamide ROO- adenine dinukleotide
Lipid Kerusakan phosphate peroksidasi DNA
Gambar 8. Sumber radikal bebas dan tempat kerja antioksidan Fouad T. Antioxidant system www. thedoctorslounge.net /medlounge/articles/antioxidant.
BAB VI
SELENIUM SEBAGAI ANTIOKSIDAN DAN HUBUNGANNYA DENGAN PENYAKIT
6.1 Penyakit kardiovaskuler
Reactive oxygen species (ROS) berperan dalam terjadinya vaskulopati, seperti aterosklerosis, hipertensi dan stenosis. Radikal bebas yang banyak berperan dalam fisiologi dan patofisiologi vaskuler adalah nitric okside (NO.), superokside (O2 -), hydrogen peroksida (H2O2) dan peroksinitrit (ONOO-). Masing-masing radikal
bebas ini dihasilkan oleh reaksi enzimatik dan kimiawi yang spesifik. Pada pembuluh darah, dalam keadaan normal NO dihasilkan oleh endothelial nitrik okside sintetase (eNOS), tetapi jika terjadi peradangan NOS juga terdapat pada makrofag dan sel otot polos yang kemudian menghasilkan NO. Sedangkan O2- dan H2O2 dapat
dihasilkan oleh semua sel pembuluh darah. Pada pembuluh darah normal kedua radikal bebas tersebut dapat dihasilkan di oleh dua enzim, yaitu sitokrom P450 yang telah teridentifikasi di arteri koronaria dan NADPH oksidase.42,43
Nitrik okside merupakan mediator vasodilatasi pembuluh darah dan berperan dalam agregasi trombosit, sedangkan O2- dan H2O2 merupakan mediator
pertumbuhan, difrensiasi dan apoptosis sel otot polos pembuluh darah. O2- dan NO
dapat bereaksi membentuk radikal yang sangat reaktif yaitu peroksinitrit (ONOO-). Peroksinitrit merupakan mediator terjadinya peroksidasi lipid, termasuk oksidasi LDL. Banyak peneliti berpendapat bahwa oksidasi LDL pada pembuluh darah yang mengalami peradangan menyebabkan atherogenesis.42,43
Seluler glutathione peroksidase (GPx-1) merupakan bentuk yang paling banyak terdapat di hampir seluruh sel, termasuk di endothelium pembuluh darah. Pada sel endotel, 70% H2O2 yang terbentuk oleh lekosit PMN didetoksifikasi oleh
GPx-1.43 Glutathione peroksidase berfungsi untuk mereduksi hydrogen peroksida menjadi air dan lipid peroksida menjadi alkohol. Marc A Forgione berpendapat bahwa defisiensi GPx-1 berhubungan langsung dengan meningkatnya stress oksidatif pada pembuluh darah sehingga terjadi disfungsi endotel.44
Pada tikus, defisiensi GPx-1 mengakibatkan kelainan fungsi dan struktur vaskuler dan jantung, seperti peningkatan inflamasi dari periadventitial pembuluh
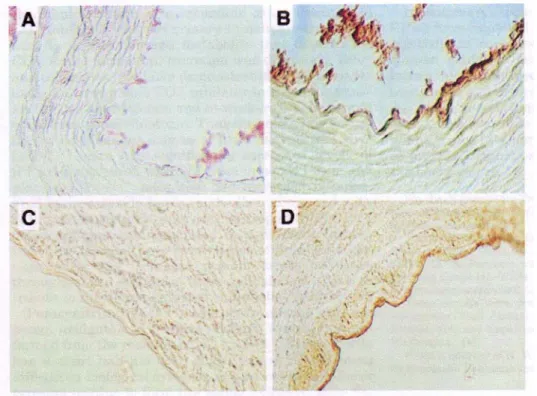
darah, pembentukkan tunika intima baru dan penimbunan kolagen di sekitar arteri koronaria. Pada jaringan aorta yang menggunakan pewarnaan 3-nitrotyrosine, tikus dengan defisiensi mempunyai pewarnaan yang lebih banyak dibanding tikus normal (gambar 9). 43 Hal ini menunjukkan peningkatan pembentukan radikal bebas di bagian tersebut. Pada manusia, penurunan aktifitas GPx-1 pada lesi aterosklerosis menyebabkan penyakit berkembang ke arah yang lebih berat.44
Gambar 9. Potongan melintang aorta pada binatang usia 10 minggu. A: tikus Dengan jaringan normal; B: tikus dengan peroksinitrite; C: tikus dengan defisiensi GPx-1; D:tikus dengan defisiensi GPx-1setelah terapi. Gambar di- dapat dari Forgione MA, Weiss N, Heydrick S, Cap A, Kling ES, Bierl C, dkk. Celluler Glutathione Peroxidase Deficiency and Endothelial dysfunction. Am J Physiol Heart Circ Physiol 2002;282:1255-61.
Pada tikus, GPx-1 dapat menghambat 5-lipoksigenase pada sel monositik. Lima lipoksigenase dalam sel monosit dan makrofag menyebabkan progresifitas penyakit aterosklerosis. Jadi adanya GPx-1 dapat mencegah perburukan aterosklerosis.44
Aktifitas GPx-1 antara individu bervariasi, tetapi penyebab adanya variasi tersebut belum diketahui. Pada penelitian didapatkan aktifitas GPx-1 lebih tinggi
pada wanita daripada laki-laki. Rokok sangat berpengaruh, dimana kadar GPx-1 pada perokok lebih rendah dibandingkan dengan bukan perokok.44
Studi epidemiologi mengenai suplementasi selenium pada penyakit kardiovaskuler masih kontroversial. Suplementasi selenium dapat mencegah terjadinya penyakit karena defisiensi selenium, tetapi tidak bisa mengembalikan otot jantung yang sudah mengalami kerusakan. Walaupun begitu identifikasi mengenai kadar aktifitas GPx-1 pada pasien dengan penyakit kardiovaskuler berguna untuk mengetahui besarnya risiko penyakit jantung.44
6.2 Penyakit Paru-paru
Paru-paru mempunyai permukaan epitel yang luas, yang berisiko dirusak oleh oksidan. Trakhea, bronchus dan alveoli dapat terekspos oleh radikal bebas yang berasal dari polutan yang terinhalasi, asap rokok dan produk-produk inflamasi. Oleh sebab itu paru-paru membutuhkan antioksidan untuk mencegah kerusakan jaringan. Paru-paru mempunyai enzim antioksidan intraseluler yang menjaga keseimbangan reduksi-oksidasi. Alveoli dapat menambah antioksidan dari cairan epithelial (epithelial lining fluid/ELF). 45,46 Cairan ini mengandung sejumlah besar (90%) glutathione tereduksi (GSH).45
Beberapa studi menunjukkan bahwa oksidan memegang peranan penting pada timbulnya penyakit dan progresifitas penyakit. Penyakit paru yang berhubungan dengan oksidatif stress adalah asma, kistik fibrosis dan penyakit interstitial paru.
Pada kondisi paru-paru yang mengalami peradangan, sistem glutathione dapat berubah-ubah. Contohnya, kadar GSH meningkat di ELF pada perokok kronis dan pada penyakit berillium kronik. Kadar GSH di ELF menurun dengan cepat pada pasien asma ringan selama eksaserbasi. Kadar GSH di dalam ELF juga menurun pada fibrosis pulmonal idiopatik, asbestosis dan sindrom gawat nafas. Beberapa studi juga menunjukkan peningkatan aktifitas GPx di ELF pada perokok dibandingkan dengan bukan perokok.
Kelompok glutathione peroksidase merupakan komponen enzim yang penting pada mekanisme detoksifikasi radikal bebas pada paru-paru. eGPx dapat ditemukan di sel epitel brush border yang mengandung lipid. eGPx terdapat pada sel epitel bronkhial dan ELF sebagai reaksi terhadap oksidatif stress pada pasien asma
atau penyakit beryllium kronik dan pada individu yang terekspos oksidan dari luar seperti asap rokok. Ekstra selular glutathione peroksidase timbul lebih lambat setelah eksposur (setelah 24 jam), hal ini menjelaskan mengapa eGPx tidak timbul setelah 12 jam hiperoksia.46
6.2.1 Asma
Bukti epidemiologi menunjukkan bahwa perubahan diet, terutama pengurangan asupan antioksidan dapat meningkatkan prevalensi dan beratnya penyakit. Hal ini memungkinkan adanya interfensi diet pada penatalaksanaan penyakit asma.
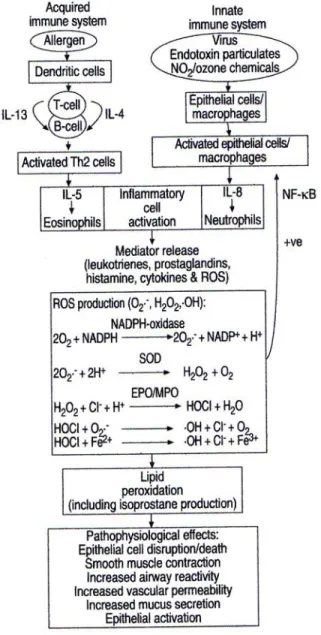
Stres oksidatif memegang peranan penting dalam patofisiologi asma.47,48 Gambar memperlihatkan bagaimana terjadinya peradangan saluran nafas yang disebabkan oleh paparan berbagai allergen, seperti gas, bahan kimia, obat, bakteri dan virus. Reaksi spesifik dari allergen dapat merangsang sistim immune didapat dan sistim immune alamiah. Sistim immune didapat memproduksi interleukin (IL)-5 dan selanjutnya mengaktifkan eosinofil. Sedangkan rangsangan terhadap sistim immune alamiah memproduksi IL-8 yang selanjutnya mengaktifasi neutrofil. Selanjutnya kedua sistem ini mengaktifkan sel-sel inflamatori dalam proses yang disebut respiratory burst (ledakan respirasi). Pengaktifan sel-sel inflamatori membutuhkan oksigen dan selanjutnya melepaskan reactive oxygen species (ROS) disekitar sel. Selama ledakan respirasi, NADPH teraktifasi dan melepaskan superokside (O2-) ke dalam sel. Superokside dismutase (SOD) kemudian
mengkatalisa superokside menjadi hydrogen peroksida (H2O2). Hidrogen peroksida
kemudian bereaksi dengan ion halide (I-, Cl-, Br-) membentuk asam hipohalous (HOCl/HOBr). Di dalam eosinofil reaksi ini dikatalisa oleh eosinofil peroksidase (EPO) sedangkan di netrofil dikatalisa oleh nyeloperoksidase. Selanjutnya, asam hipohalous akan bereaksi dengan O2- membentuk oksidan yang kuat yaitu radikal
hidroksil (.OH). Radikal bebas selanjutnya menyebabka peroksidasi lipid. Selama ledakan respirasi jumlah radikal bebas yang dibentuk dapat melebihi pertahanan antioksidan dan menyebabkan stres oksidatif.47
Stres oksidatif menyebabkan berbagai efek pada saluran nafas, yaitu kontraksi otot polos, peningkatan reaktifitas, hipersekresi mukus dan eksudasi vaskuler.
Gambar 10. Mekanisme peroksidasi lipid pada asma. Gambar didapat dari Wood LG, Gibson PG, Garg ML. Biomarkers of Lipid Peroxidation, Airway Inflammation and Asthma. Eur Respir J 2003;21:177-86.
Defisiensi antioksidan telah sering dilaporkan terdapat pada pasien asma. Antioksidan enzimatik yang paling berperan adalah superokside dismutase (SOD) dan glutathione peroksidase (GPx). Pada pasien asma aktifitas glutathione peroksidase menurun. Selenium yang merupakan komponen dari enzim glutathione peroksidase juga menurun. Terdapat peningkatan risiko terjadinya asma 1,9 sampai
5,8 kali pada subjek dengan kadar selenium dan glutathione peroksidase yang rendah.49,50,51
Walaupun telah banyak bukti bahwa peningkatan stress oksidatif dan penurunan aktifitas antioksidan berperan dalam terjadinya asma, namun penelitian mengenai suplementasi antioksidan masih sangat sedikit. Salah satu percobaan mengenai suplementasi selenium selama 1 minggu memberikan hasil yang positif. Namun karena studi mengenai suplementasi selenium ini masih sangat terbatas maka masih dianjurkan untuk memberikan suplementasi antioksidan kombinasi.47
6.2.2 Kistik Fibrosis
Stress oksidatif telah terbukti memegang peranan pada patofisiologi terjadinya kistik fibrosis. Pada kistik fibrosis terjadi peradangan jalan nafas yang berulang-ulang. Adanya koloni bakteri pada paru-paru menarik neutrofil untuk memusnahkan bakteri tersebut. Proses memusnahkan bakteri ini melepaskan ROS dalam jumlah besar. Terbentuknya radikal bebas pada kistik fibrosis juga disebabkan oleh meningkatnya kebutuhan oksigen yang dapat mencapai 120-150% dari normal.52,53
Pada penderita kistik fibrosis juga didapatkan penurunan aktifitas enzim glutathione peroxidase.52,53
Penelitian yang dilakukan oleh Lisa G Wood menunjukkan bahwa dengan suplementasi selenium sebesar 90 mikrogram selama 8 minggu dapat meningkatkan aktifitas glutathione peroksidase dan memperbaiki gejala klinis penyakit.53
6.3 Penyakit Gastrointestinal
Radikal bebas telah diindikasikan berperan dalam penyakit kolon, seperti radang usus (inflammatory bowel syndrome/IBD), seperti Crohn disease dan kolitis ulseratif. Kadar oksigen reaktif juga meningkat pada mukosa traktus gastrointestinal yang mengalami peradangan, dibandingkan dengan mukosa normal. Bahan toksik pada mukosa epitelium dapat menyebabkan peradangan. Beberapa penelitian telah melaporkan bahwa kolon pasien sindroma radang usus (SRU)/inflammatory bowel syndrome (IBD) memproduksi lebih banyak radikal bebas.54
Pada penyakit Crohn, ROS dibentuk oleh neutrofil sebagai akibat proses peradangan. ROS menyerang hampir seluruh komponen sel yang berada disekitarnya, sehingga terjadi kerusakan sel. ROS dapat merusak ikatan asam lemak tak jenuh ganda sehingga menyebabkan peroksidasi lipid, akibatnya kerusakan jaringan bertambah banyak. Selama peradangan kronik ROS dibentuk terus-menerus sehingga antioksidan tidak mampu lagi menetralisir. Pada usus halus dan usus besar ROS dapat ditimbulkan oleh sel fagosit, sel endotel mikrovaskuler dan sel epitel mukosa. Telah dilaporkan bahwa onset peyakit Crohn dimulai dari adanya pengurangan enzim antioksidan dan mikronutrien pada mukosa usus dan plasma.55
Pada anak-anak yang menderita sindroma radang usus terlihat peningkatan aktifitas GPx pada plasma (eGPx). Sedangkan percobaan yang dilakukan pada tikus menunjukkan peningkatan GPx plasma sebesar 61% pada distal kolon setelah diterapi selama 7 hari dibanding kontrol.54
Glutathione peroksidase pada traktus gastrointestinal terdiri dari GPx-1 dan Gpx-GI. Keduanya dapat mereduksi H2O2 dan hidroperoksida asam lemak dengan
baik. Pada epitelium kripta, aktifitas glutathione peroksidase sangat penting dalam mencegah inflamasi. Aktifitas kedua jenis GPx ini bekerja pada tempat yang berbeda. GPx-1 lebih banyak pada villi sedangkan GPx-GI lebih banyak terdapat di kripta. Hal ini menunjukkan bahwa keduanya bekerja saling melengkapi.56
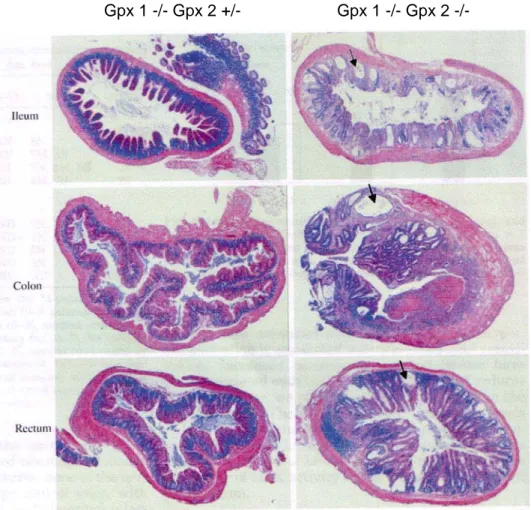
Pada percobaan dengan menggunakan tikus, pada tikus yang mengalami defisiensi, pada pemeriksaan histologi usus terlihat peradangan yang terbatas pada mukosa, yaitu infiltrasi sel-sel radang, deplesi mucin dan distorsi kripta. Gambaran ini sesuai dengan gambaran colitis yang terjadi pada manusia. Abses pada kripta lebih sering ditemukan pada ileum. kolon dan rektum (gambar 11). 56
Gpx 1 -/- Gpx 2 +/- Gpx 1 -/- Gpx 2 -/-
Gambar 11. Histologi ileum, kolon dan rektum tikus. Gambar sebelah kiri memperlihatkan jaringan normal, gambar sebelah kanan jaringan pada tikus dengan defisiensi. Tanda panah menunjukkan letak abses kripta. Gambar didapat dari Esworthy, Steven R, Aranda R, Martin MG, Doroshow JH, Binder SW, dkk. Mice with combined disruption of Gpx1 and Gpx2 genes have colitis. Am J Physiol Gastrointest Liver Physiol 2001;281:848-55.
Pada penderita sindroma radang usus sering ditemukan defisiensi selenium oleh karena itu dianjurkan untuk memberikan suplementasi selenium pada pasien dengan sindroma radang usus.56
6.4 Penyakit Virus 6.4.1 Penyakit Keshan
Penyakit Keshan adalah kardiomiopati yang terdapat pada wanita dan anak-anak pada daerah di China dimana kandungan seleniumnya rendah. Penyakit Keshan dicirikan dengan lesi nekrotik pada seluruh miokardium dengan derajat
infiltrasi seluler dan kalsifikasi yang berbeda-beda. Bentuk akut penyakit ini ditandai dengan terjadinya insufisiensi jantung yang tiba-tiba, sedangkan bentuk kronik ditandai dengan pembesaran jantung yang berat dengan berbagai derajat insufisiensi. Insiden penyakit ini berhubungan dengan rendahnya intake selenium dan suplementasi selenium dapat mencegah terjadinya penyakit ini.1,57
Adanya variasi musiman pada penyakit ini menunjukkan bahwa ada agen infeksius lain yang berperan dalam timbulnya penyakit Keshan selain selenium. Virus coxsackie telah diisolasi dari penderita Keshan dan virus ini mampu menyebabkan peradangan pada jantung yang disebut miokarditis.
Defisiensi selenium dapat meningkatkan virulensi atau progresifitas virus coxsackie. Meningkatnya stress oksidatif akibat defisiensi selenium dapat menimbulkan mutasi atau perubahan gen virus. Hal ini diperlihatkan pada penelitian yang dilakukan oleh Melinda A.Beck pada tikus yang diinokulasi dengan virus Coxsackie B3. Pada penelitian ini, tikus yang mengalami defisiensi selenium dan tikus dengan diet selenium yang cukup, diinokulasi dengan strain virus coxsackie yang amiokarditik (CVB3/0). Pada tikus dengan defisiensi selenium timbul miokarditis sedangkan pada tikus dengan diet selenium cukup tidak terjadi miokarditis. Hasil ini menunjukkan bahwa telah terjadi perubahan genome virus pada tikus dengan defisiensi selenium. Untuk mengkonfirmasi perubahan genome ini dilakukan penguraian gen, dan ditemukan ada 6 tempat mutasi pada virus tersebut.57-59
Perubahan genome virus coxsackie pada defisiensi selenium juga berhubungan dengan rendahnya aktivitas seluler glutathione peroksidase (GPx-1). Pada tikus dengan aktifitas seluler GPx yang rendah didapatkan perubahan nucleotide virus sebanyak 7 buah dibandingkan dengan tikus biasa.57-59
Selain faktor nutrisi dan virus, adanya perubahan respons immune pada defisiensi selenium juga mempermudah timbulnya miokarditis. Percobaan pada tikus menunjukkan bahwa pada tikus dengan defisiensi selenium terjadi hambatan dalam proliferasi sel limfosit T.57-59
6.4.2 Influenza
Virus influenza mempunyai kemampuan untuk mengubah protein permukaanya (hemaglutinin/HA dan neurominidase/NA) untuk menghindar dari deteksi sistem immune. Perubahan sedikit saja dari HA dan NA membuat virus tersebut dapat terhindar dari deteksi.
Efek ini telah dibuktikan oleh peneliti di University of North Carolina. Mereka membandingkan tikus yang mengalami defisiensi selenium dengan yang tidak, semua tikus terekspos human influenza virus. Tikus dengan defisiensi selenium yang diinfeksi dengan strain virus influenza yang ringan (A/Bangkok/1/29) mengalami radang paru (pneumonitis) berat. Penelitian pada mRNA virus yang mengkode protein permukaan (HA dan NA) menunjukkan adanya perubahan pada matrix protein sebanyak 29 nukleotide. Perubahan nucleotide ini menyebabkan perubahan 6 asam amino.57
6.4.3 Human Immunodefisiensi Virus (HIV)
Penurunan kadar selenium pada individu yang terinfeksi HIV merupakan tanda yang sensitive untuk progresifitas penyakit. Rendahnya kadar selenium juga berhubungan dengan meningkatnya risiko kematian karena HIV. Status nutrisi selenium yang adekuat dapat meningkatkan resistensi terhadap infeksi virus HIV dengan cara memperkuat sistem immune. Pada infeksi HIV, stress oksidatif dapat mempengaruhi replikasi virus. Sebagai komponen dari glutathione peroksidase, selenium berperan dalam menurunkan stres oksidatif pada sel yang terinfeksi HIV dan menurunkan kecepatan replikasi virus.1,60,61
Defisiensi selenium juga berhubungan dengan progresifitas virus dan kematian pada infeksi HIV dibandingkan dengan mikronutrien lain. Pada observasi selama 5 tahun terhadap 24 anak dengan HIV, mereka yang mempunyai kadar selenium yang rendah meninggal dalam umur yang lebih muda, hal ini mengindikasikan perjalanan penyakit yang lebih cepat.
Pada penderita HIV dengan suplementasi selenium, sel-T menghambat replikasi virus HIV dan menurunkan pembentukan sitokin, yang berperan dalam proses peradangan. Suplementasi dengan jamur yang diperkaya selenium pada individu dengan HIV dengan dosis 400 mcg/hari memperlihatkan perbaikan. Studi
lainnya yang mengikuti 15 penderita HIV yang disuplementasi dengan sodium selenit 100 mcg/hari selama 1 tahun, memperlihatkan penurunan stress oksidatif.1
6.5 Kanker
Studi geografi secara konsisten memperlihatkan bahwa populasi yang tinggal di daerah dengan kadar selenium pada tanah yang rendah menyebabkan intake selenium relatif rendah dan mempunyai angka mortalitas kanker yang lebih tinggi. Studi epidemiologi menunjukkan individu dengan kadar selenium yang rendah (pada darah dan kuku) mempunyai insiden kanker yang lebih tinggi. Tetapi kecenderungan ini tidak begitu nyata pada perempuan, contohnya, studi prosfektif pada 60.000 perawat perempuan di U.S menunjukkan tidak terdapat hubungan antara kadar selenium dengan risiko kanker. Infeksi kronis virus hepatitis B dan C secara signifikan meningkatkan risiko kanker hepar, contohnya, studi yang dilakukan pada orang laki-laki di Taiwan menunjukkan penurunan kadar selenium berhubungan dengan meningkatnya risiko kanker hepar. Kadar selenium yang rendah juga berhubungan dengan meningkatnya risiko mendapat kanker paru-paru, terutama pada perokok. Individu dengan intake selenium sebesar 159 mcg/hari risiko untuk mendapat kanker prostat hanya 35% dibandingkan dengan individu dengan intake selenium 86 mcg/hari.1,62,63
Beberapa mekanisme telah diketahui dalam mencegah kanker, yaitu:1
1. Maksimalisasi aktifitas antioksidan selenoenzim dan memperbaiki status antioksidan.
2. Memperbaiki sistem imun.
3. Mempengaruhi metabolisme karsinogen.
4. Meningkatnya kadar metabolit selenium yang dapat menghambat pertumbuhan sel tumor
Walaupun peranan selenium dalam kehidupan sel telah terbukti, tetapi mekanisme protektif masih terbatas. Studi yang dilakukan pada sel Jurkat, suatu sel lymphoma, dalam 24 jam terlihat penurunan viabilitas sel pada media bebas selenium. Pada penelitian ini terlihat kematian sel terjadi setelah pembelahan pertama kali. Penelitian ini memberikan spekulasi bahwa pembelahan sel tergantung dengan selenium. Pada studi ini juga terlihat bahwa kematian sel disebabkan karena