PENGARUH VARIASI JUMLAH CMC-Na SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS FISIK SEDIAAN SABUN CUCI TANGAN ANTIBAKTERI EKSTRAK ETANOL DAUN BELUNTAS
(Pluchea indica (L.) Less)
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh :
Marcelina Widani Amanda Rompas NIM : 108114163
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH VARIASI JUMLAH CMC-Na SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS FISIK SEDIAAN SABUN CUCI TANGAN ANTIBAKTERI EKSTRAK ETANOL DAUN BELUNTAS
(Pluchea indica (L.) Less)
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh :
Marcelina Widani Amanda Rompas NIM : 108114163
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Don’t feel pressured to know what your life purpose is.
Just chill out and enjoy the peace.
The idea will come.
– Josh Langley -
Kupersembahkan karyaku ini untuk:
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas berkat,
rahmat dan karunia-Nya selama penelitian dan penyusunan skripsi ini sehingga
dapat diselesaikan dengan baik. Skripsi berjudul PENGARUH VARIASI
JUMLAH CMC-Na SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK
DAN STABILITAS FISIK SEDIAAN SABUN CUCI TANGAN EKSTRAK
ETANOL DAUN BELUNTAS (Pluchea indica (L.) Less) ini disusun untuk
memenuhi salah satu syarat untuk memperoleh gelar Sarjana Strata Satu Program
Studi Ilmu Farmasi (S. Farm.). Penyusunan laporan ini tidak lepas dari bantuan
dan dorongan dari berbagai pihak. Oleh karena itu, pada kesempatan ini penulis
menyampaikan terima kasih yang sebesar-besarnya kepada:
1. Bapak Septimawanto Dwi Prasetyo, M.Si., Apt., selaku Dosen Pembimbing
yang telah memberikan bimbingan dan pengarahan kepada penulis selama
penelitian maupun penyusunan skripsi.
2. Bapak Prof. Dr. C. J. Soegihardjo, Apt., selaku Dosen Penguji yang telah
memberikan masukan, kritik dan saran kepada penulis.
3. Bapak Enade Perdana Istyastono, Ph.D., Apt., selaku Dosen Penguji yang telah
memberikan masukan, kritik dan saran kepada penulis.
4. Ibu Aris Widayati, M.Si., Ph.D., Apt., selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
5. Seluruh Dosen Fakultas Farmasi Universitas Sanata Dharma atas ilmu yang
viii
6. Pak Musrifin, Pak Mukmin, Mas Agung serta laboran-laboran lainnya atas
bantuan selama penulis menyelesaikan penelitian.
7. Kedua orang tua penulis, Abraham Sonny Rompas dan Cornelia Tri Widayati
atas doa dan dukungan yang selalu diberikan kepada penulis selama penelitian
dan penyusunan skripsi.
8. Bernadette Sonya Anindita Rompas dan Martinus Rubiarso yang selalu
memberikan semangat dan dorongan kepada penulis.
9. Partner skripsiku Rosalia Suryaningtyas atas kesabaran, kerjasama, suka duka
dan bantuannya selama mengerjakan penelitian dan penyusunan skripsi ini.
10.Romo Irsan Rimawal, SJ., atas dukungan dan doa yang diberikan kepada
penulis.
11.Emmanuella Venni dan Yustina Retno Larasati yang banyak membantu dan
mendukung penulis dalam penyelesaian skripsi ini.
12.Teman-teman satu laboratorium yang sering memberi masukan kepada penulis
selama penelitian Yoestenia, Devina, Palma, dan Ita.
13.Teman-teman yang telah menghibur penulis dalam kepenatan selama
penelitian dan penyusunan skripsi Emilia Jevina, Karonia “Inem”, dan Febrian
Cahyadi.
14.Teman-teman Kos Muria: Mbak Hana, Mbak Astrid, Kak Sofi, Arvita, Kak
Frada, Jessi dll. Terimakasih telah menemani penulis begadang dalam
ix
15.Terimakasih kepada teman-teman Farmasi: Rosa, Titi, Sita, Sisca, Epong,
Apong, Nita, Widya dan teman-teman FST B. Atas kebersamaannya selama
ini.
16.Semua pihak yang tidak dapat disebutkan satu persatu yang telah membantu
penulis dalam menyelesaikan skripsi ini
Penulis menyadari bahwa penyusunan dan penyelesaian skripsi ini masih banyak
kekurangan. Oleh karena itu, penulis membutuhkan saran dan kritik yang
membangun dari berbagai pihak. Akhir kata, penulis mengharapkan semoga
skripsi ini kiranya dapat memberikan inspirasi dan manfaat dan kegunaannya bagi
pembaca dan dapat berguna bagi perkembangan ilmu pengetahuan.
Yogyakarta, 5 Agustus 2014
x DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERSETUJUAN PUBLIKASI KARYA ILMIAH ... vi
xi
E. Pengukuran Diameter Zona Hambat ... 12
F. Daun Beluntas ... 12
1. Sodium Carboxy Methyl Cellulose (CMC-Na) ... 17
K. Formulasi ... 18
1. Surfaktan (Sodium Lauryl Sulphate) ... 18
2. Humektan ... 19
a. Gliserol ... 19
xii
a. Pengumpulan bahan daun beluntas ... 30
b. Pembuatan serbuk daun beluntas ... 30
2. Pembuatan ekstrak etanol daun beluntas ... 30
a. Ekstraksi serbuk daun beluntas ... 30
b. Penetapan kadar total fenolik ... 31
3. Uji potensi antibakteri ekstrak etanol daun beluntas ... 31
a. Pembuatan stok isolat bakteri tangan ... 31
b. Pembuatan suspensi isolat bakteri uji ... 31
c. Pembuatan konsentrasi ekstrak etanol daun beluntas ... 32
d. Uji aktivitas antibakteri ekstrak etanol daun beluntas... 33
xiii
4. Pembuatan sediaan gel sabun cuci tangan antibakteri ekstrak etanol
daun beluntas ... 34
a. Modifikasi formula gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas ... 34
b. Pembuatan gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas ... 35
5. Evaluasi sediaan gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas ... 35
a. Sifat fisik ... 35
b. Stabilitas fisik ... 36
6. Uji aktivitas antibakteri sediaan gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas terhadap isolat bakteri tangan ... 37
a. Pembuatan suspensi bakteri uji ... 37
b. Uji aktivitas sediaan gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas ... 37
F. Analisis Data ... 38
BAB IV HASIL DAN PEMBAHASAN ... 39
A. Pengumpulan Bahan dan Determinasi Tanaman ... 39
B. Pembuatan Serbuk Daun Beluntas ... 40
C. Pembuatan Ekstrak Etanol Daun Beluntas ... 41
D. Uji Potensi Antibakteri Ekstrak Etanol Daun Beluntas ... 42
1. Isolasi bakteri tangan ... 42
2. Uji aktivitas antibakteri ekstrak etanol daun beluntas ... 43
E. Pembuatan Sediaan Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 50
F. Uji Sifat Fisik Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 53
1. Uji organoleptis ... 53
2. Uji pH ... 54
xiv
4. Ketahanan busa ... 57
G. Uji Stabilitas Fisik Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 59
1. Organoleptis dan pH ... 59
2. Viskositas ... 59
3. Ketahanan busa ... 61
H. Uji Aktivitas Antibakteri Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 62
BAB V KESIMPULAN DAN SARAN ... 65
A. Kesimpulan ... 65
B. Saran ... 65
DAFTAR PUSTAKA ... 67
LAMPIRAN ... 71
xv
DAFTAR TABEL
Halaman
Tabel I. Struktur Sel Bakteri ... 8
Tabel II. Formula Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak
Etanol Daun Beluntas ... 34
Tabel III. Variasi Jumlah CMC-Na pada Formula Sediaan Gel Sabun Cuci
Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 35
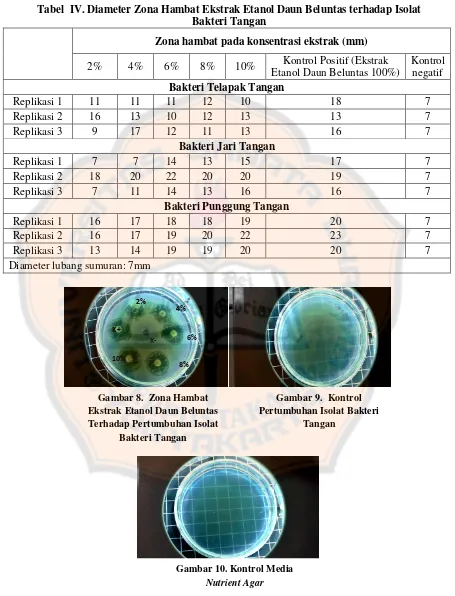
Tabel IV. Diameter Zona Hambat Ekstrak Etanol Daun Beluntas terhadap
Isolat Bakteri Tangan ... 45
Tabel V. Nilai Probabilitas uji Shapiro-Wilk Diameter Zona Hambat Ekstrak
Etanol Daun Beluntas terhadap Isolat Bakteri Tangan ... 47
Tabel VI. Hasil Uji Kruskal-Wallis Diameter Zona Hambat Ekstrak Etanol
Daun Beluntas terhadap Isolat Bakteri Tangan ... 48
Tabel VII. Hasil Uji Wilcoxon Diameter Zona Hambat Ekstrak Etanol Daun
Beluntas terhadap Isolat Bakteri Punggung Tangan ... 49
Tabel VIII. Formula Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak
Etanol Daun Beluntas ... . 52
Tabel IX. Data Uji Organoleptis Sediaan Gel Sabun Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas Selama 48 jam
Penyimpanan ... 54
Tabel X. Data Uji pH Sediaan Gel Sabun Gel Cuci Tangan Antibakteri
Ekstrak Etanol Daun Beluntas Selama 48 jam Penyimpanan ... 54
Tabel XI. Data Viskositas Sediaan Gel Sabun Gel Cuci Tangan Antibakteri
xvi
Tabel XII. Uji Shapiro-Wilk Viskositas Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas Selama 48 jam
Penyimpanan ... 55
Tabel XIII. Nilai Probabilitas Uji Post Hoc Viskositas Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas Selama 48 jam
Penyimpanan ... 56
Tabel XIV. Data Ketahanan Busa Sediaan Gel Sabun Cuci Tangan Antibakteri
Ekstrak Etanol Daun Beluntas Selama 48 jam Penyimpanan ... 57
Tabel XV. Nilai P-Value Ketahanan Busa Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas Selama 48 jam
Penyimpanan ... 58
Tabel XVI. Data Viskositas Sediaan Gel Sabun Cuci Tangan Antibakteri
Ekstrak Etanol Daun Beluntas Selama Beberapa Hari Penyimpanan ... 60
Tabel XVII. Data Uji Ketahanan Busa Sediaan Gel Sabun Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas Selama Beberapa Hari
Penyimpanan ... 61
Tabel XVIII. Diameter Zona Hambat Sediaan Sabun Gel Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas terhadap Isolat Bakteri
xvii Pertumbuhan Isolat Bakteri Tangan ... 45
Gambar 9. Kontrol Pertumbuhan Isolat Bakteri Tangan ... 45
Gambar 10. Kontrol Media Nutrient Agar ... 45
Gambar 11. Grafik Pengaruh Konsentrasi CMC-Na terhadap Viskositas Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Selama 48jam Penyimpanan ... 57
Gambar 12. Grafik Pengaruh Konsentrasi CMC-Na terhadap Ketahanan Busa Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 58
Gambar 13. Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas Selama 48 jam Penyimpanan ... 59
xviii
Gambar 15. Grafik Stabilitas Viskositas Sediaan Gel Sabun Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas Selama Beberapa Hari
Penyimpanan ... 60
Gambar 16. Grafik Stabilitas Ketahanan Busa Sediaan Gel Sabun Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas Selama Beberapa Hari
Penyimpanan ... 61
Gambar 17. Gambar Uji Ketahanan Busa ... 62
Gambar 18. Zona Hambat Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak
Etanol Daun Beluntas terhadap Isolat Bakteri Tangan, Kontrol
Pertumbuhan Isokat Bakteri Tangan, dan Kontrol Media Nutrient
xix
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat Keterangan Identifikasi Daun Beluntas ... 72
Lampiran 2. Certificate of Analysis (CoA) Ekstrak Etanol Daun Beluntas
(Pluchea indica (L.) Less) dari LPPT UGM ... 73 Lampiran 3. Langkah Kerja Ekstraksi Etanol Daun Beluntas (Pluchea indica (L.)
Less) dari LPPT UGM ... 74
Lampiran 4. Keterangan Ekstrak Etanol Daun Beluntas (Pluchea indica (L.)
Less) dari LPPT UGM ... 75
Lampiran 5. Penetapan Kadar Total Fenolik Ekstrak Etanol Daun Beluntas
(Pluchea indica (L.) Less) dari LPPT UGM ... 76 Lampiran 6. Sampel Ekstrak Etanol Daun Beluntas dan Foto Isolat Bakteri
Tangan ... 77
Lampiran 7. Foto Zona Hambat Ekstrak Etanol Daun Beluntas terhadap Isolat
Bakteri Tangan ... 78
Lampiran 8. Uji Normalitas Shapiro-Wilk Diameter Zona Hambat Ekstrak
Etanol Daun Beluntas terhadap Isolat Bakteri Tangan ... 79
Lampiran 9. Uji Kruskal-Wallis Diameter Zona Hambat Ekstrak Etanol Daun
Beluntas terhadap Isolat Bakteri Tangan ... 80
Lampiran 10. Uji Wilcoxon Diameter Zona Hambat Ekstrak Etanol Daun
Beluntas terhadap Isolat Bakteri Tangan ... 81
Lampiran 11. Perhitungan Ekstrak Daun Beluntas dan Foto Sediaan Gel Sabun
Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 84
Lampiran 12. Foto Sediaan Gel Sabun Cuci Tangan Ekstrak Etanol Daun
Beluntas Setelah 28 hari Penyimpanan ... 85
Lampiran 13. Data Uji Organoleptis dan pH Sediaan Gel Sabun Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas Selama Beberapa Hari
Penyimpanan ... 86
Lampiran 14. Data Uji Viskositas Sediaan Gel Sabun Cuci Tangan Antibakteri
xx
Lampiran 15. Hasil Uji Statistik Sifat Fisik Viskositas Sediaan Gel Sabun Cuci
Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 88
Lampiran 16. Hasil Uji Statistik Stabilitas Viskositas Sediaan Gel Sabun Cuci
Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 89
Lampiran 17. Data Uji Sifat Fisik dan Uji Statistik Ketahanan Busa Sediaan Gel
Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 92
Lampiran 18. Hasil Uji Statistik Stabilitas Ketahanan Busa Sediaan Gel Sabun
Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 95
Lampiran 19. Foto Zona Hambat Sediaan Gel Sabun Cuci Tangan Antibakteri
Ekstrak Etanol Daun Beluntas terhadap Isolat Bakteri Tangan dan
Basis Sediaan Gel Sabun Cuci Tangan ... 99
Lampiran 20. Diameter Zona Hambat Sediaan Gel Sabun Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas terhadap Isolat Bakteri
Tangan ... 100
Lampiran 21. Uji Normalitas Shapiro-Wilk Zona Hambat Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas terhadap Isolat
Bakteri Tangan ... 101
Lampiran 22. Uji Kruskal Wallis Zona Hambat Sediaan Gel Sabun Cuci Tangan
Antibakteri Ekstrak Etanol Daun Beluntas ... 104
Lampiran 23. Uji Wilcoxon Zona Hambat Sediaan Gel Sabun Cuci Tangan
Ekstrak Etanol Daun Beluntas dibandingkan dengan Basis Sediaan
Gel Sabun Cuci Tangan ... 105
Lampiran 24. Nilai Probabilitas Uji Wilcoxon: Perbandingan Antara Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas
dengan Basis Sediaan Gel Cuci Tangan ... 107
Lampiran 25. Uji Wilcoxon Zona Hambat Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas dibandingkan dengan
Kontrol Positif ... 108
Lampiran 26. Nilai probabilitas Uji Wilcoxon: Perbandingan Antara Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas
xxi INTISARI
Senyawa fenolik merupakan kandungan utama dalam ekstrak etanol daun beluntas (Pluchea Indica (L.) Less) yang memiliki potensi antibakteri. Penelitian ini dilakukan untuk mengetahui konsentrasi optimum ekstrak etanol daun beluntas yang dapat digunakan sebagai antibakteri terhadap isolat bakteri tangan dengan metode difusi dan untuk mengetahui pengaruh gelling agent terhadap sifat fisik dan stabilitas fisik yang meliputi pH, viskositas, pergeseran viskositas dan ketahanan busa.
Penelitian ini merupakan penelitian eksperimental. Hasil pengukuran diameter zona hambat dianalisis dengan mengunakan uji Kruskal-Wallis
kemudian dilanjutkan uji Wilcoxon, sementara hasil pengukuran data sifat fisik dan stabilitas fisik kemudian dianalisis menggunakan uji One Way ANOVA, untuk mengetahui signifikansi pengaruh gelling agent terhadap sifat fisik dan stabilitas fisik gel. Data yang diperoleh, dianalisis dengan menggunakan software
R 3.1.0
Hasil dari penelitian menunjukkan bahwa konsentrasi 6% ekstrak etanol daun beluntas, dapat memberikan daya hambat terhadap isolat bakteri tangan. Terdapat perbedaan viskositas yang signifikan pada penggunaan variasi jumlah
gelling agent. Namun variasi jumlah gelling agent tidak menunjukkan adanya pengaruh terhadap respon ketahanan busa dan pergeseran viskositas.
xxii ABSTRACT
Phenolic compounds are the major chemical compounds of beluntas leaves (Pluchea indica (L.) Less) ethanol extract that have potential as an antibacterial. This study aimed to determine the optimum concentration of beluntas leaves ethanol extract which can be used as antibacterial towards hand bacterial isolates with diffusion method, and to figure out the effect of gelling agent towards physical properties which consist of pH, viscosity, viscosity shift, and foam stability.
This study is an experimental study. The data of measurement result of inhibiton zones statiscally analyzed with the Kruskal-Wallis test followed the Wilcoxon test, whereas the data of measurement result of physical properties and physical stability statically analyzed with the One Way ANOVA test; to find the significance of gelling agent effect towards physical characteristics and gel physical stability. Data was analyzed by using the R 3.1.0 software.
Beluntas leaves (Pluchea indica (L.) Less) ethanol extract showed antibacterial activity towards bacterial isolate at a concentration of 6%. There was a significant viscosity difference at the usage on the amount variance of gelling agent, whereas the amount of variance of gelling agent did not show any significant differences towards foam stability response and viscosity shift.
1 BAB I
PENDAHULUAN
A. Latar Belakang
Penyakit infeksi masih merupakan jenis penyakit yang paling banyak
diderita oleh penduduk di negara berkembang, termasuk Indonesia. Salah satu
penyebab penyakit infeksi adalah bakteri. Menurut Radji (2009) bakteri
merupakan mikroorganisme yang tidak dapat dilihat dengan mata telanjang, tetapi
hanya dilihat dengan bantuan mikroskop.
Penyakit infeksi dapat dikurangi dengan kebiasaan berperilaku hidup
bersih dan sehat. Perilaku hidup bersih dan sehat merupakan semua perilaku
kesehatan yang dilakukan atas dasar kesadaran diri. Salah satu contoh sederhana
perilaku hidup bersih dan sehat adalah dengan menjaga kebersihan tubuh.
Tangan merupakan bagian tubuh yang sering digunakan untuk menyentuh
dan memegang benda, karena itu tangan disebut perantara yang paling sering
menularkan bakteri penyakit. Berdasarkan data WHO, tangan mengandung
bakteri sebanyak 39.000-460.000 CFU per sentimeter kubik, yang berpotensi
tinggi menyebabkan penyakit infeksi menular (Rochimawati, 2013).
Kebersihan tangan yang kurang, juga menyebabkan penyakit terkait
makanan seperti infeksi Salmonella dan E. coli. Beberapa dapat mengalami gejala
yang menganggu seperti mual, muntah, dan diare. Tangan yang terlihat bersih
belum tentu terbebas dari bakteri penyakit, karena itu kebersihan tangan tetap
Sabun berfungsi untuk melarutkan kotoran dan minyak ada permukaan
kulit dengan menggunakan air sehingga dapat diangkat dengan mudah dari kulit.
Sabun dapat membersihkan minyak, kotoran, dan keringat yang menempel di kulit
(Izhar, 2009).
Dewasa ini, telah banyak sabun cuci tangan yang beredar di pasaran
dengan berbagai merk dan bentuk sediaan. Kebanyakan sabun cuci tangan yang
beredar di pasaran berbahan dasar triclosan sebagai antibakteri. Triclosan
diketahui dapat menyebabkan resistensi antibiotik sehingga dapat menghambat
kerja obat-obatan yang sebelumnya memiliki potensi antibiotik. Selain itu,
penggunaan triclosan yang terlalu sering dan berlebihan dapat membunuh flora
normal kulit yang sebenarnya merupakan salah satu mikroba untuk perlindungan
kulit (Gusviputri, 2013). Dilihat dari adanya dampak negatif yang dapat
ditimbulkan oleh triclosan, maka perlu dipikirkan bahan alternatif lain yang dapat
menggantikan triclosan sebagai antibakteri. Dalam hal ini, digunakan ekstrak
etanol beluntas sebagai antibakteri untuk mengurangi pemakaian bahan sintetik
dalam formulasi sabun cuci tangan. Bahan alami juga cenderung tidak
memberikan dampak yang buruk bagi kulit dalam pemakaian jangka panjang.
Daun beluntas (Pluchea indica (L.) Less.) biasa digunakan sebagai obat
untuk menghilangkan bau badan, obat penurun panas, obat batuk dan obat
antidiare. Selain itu daun beluntas yang telah direbus sering pula digunakan untuk
mengobati penyakit kulit (Winarno dan Sundari, 1998). Setelah diteliti secara
ilmiah, daun beluntas (Pluchea indica (L.) Less.) diketahui memiliki kandungan
antimikroba terhadap Staphylococcus aureus, E. coli, Pseudomonas fluorecens
dan Salmonela thypi (Ardiansyah et al., 2003). Hasil uji total kandungan fenolik
menyatakan bahwa semakin muda daun, kadar total fenol semakin besar (Saffan
dan El-Mousallamy, 2008).
Pada penelitian ini akan dibuat sediaan sabun cuci tangan antibakteri
ekstrak etanol daun beluntas dalam bentuk gel. Gel mengandung komposisi air
dalam jumlah tinggi sehingga dapat meningkatkan disolusi obat dan juga
memudahkan migrasi obat melalui basis utamanya (Jones, 2008). Bentuk sediaan
ini tentu diharapkan dapat membuat ekstrak daun beluntas menjadi nyaman
digunakan sebagai antibakteri.
Viskositas sediaan merupakan salah satu faktor yang mempengaruhi
stabilitas sediaan gel. Viskositas merupakan ukuran kekentalan fluida yang
menyatakan besar kecilnya gesekan di dalam fluida. Viskositas di pengaruhi oleh
gelling agent. Gelling agent yang digunakan dalam penelitiaan ini adalah
CMC-Na. Dalam hal ini digunakan CMC-Na karena CMC-Na memiliki gugus natrium
yang dapat mengikat air (terhidrasi) tanpa perlu pemanasan selain itu CMC-Na
stabil pada rentang pH 5-9 sehingga dalam formulasi tidak diperlukan
penambahan agen pembasa.
Pada penelitiaan ini dilakukan formulasi sediaan sabun cuci tangan
antibakteri ekstrak etanol daun beluntas dengan menggunakan variasi jumlah
CMC-Na sebagai gelling agent. Variasi jumlah CMC-Na dilakukan untuk
mengetahui pengaruh CMC-Na sebagai gelling agent terhadap sifak fisik dan
1. Rumusan Masalah
Berdasarkan data di atas maka dapat disusun permasalahan :
a. Apakah ekstrak etanol daun beluntas memiliki aktivitas antibakteri
terhadap isolat bakteri di tangan?
b. Apakah terdapat perbedaan sifat fisik dan stabilitas fisik dalam penggunaan
variasi jumlah CMC-Na sebagai gelling agent pada sabun cuci tangan
antibakteri ekstrak etanol daun beluntas?
2. Keaslian Penelitian
Sejauh penelusuran yang dilakukan penulis, penelitian mengenai variasi jumlah
CMC-Na sebagai gelling agent pada formulasi sabun cuci tangan antibakteri
ekstrak etanol daun beluntas, belum pernah dilakukan. Beberapa penelitian
yang terkait formulasi ekstrak etanol daun beluntas yang pernah dilakukan
sebelumnya antara lain :
1. Perbedaan Sifat Fisik dan Stabilitas Fisik Deodoran Ekstrak Etanol Daun
Beluntas (Pluchea indica (L.) Less) dengan Variasi Jumlah Sorbitan
Monooleate sebagai Emulsifying agent (Hardita, 2012).
2. Perbedaan Sifat Fisik dan Stabilitas Fisik Deodoran Ekstrak Etanol Daun
Beluntas (Pluchea indica (L.) Less) dengan Variasi Jumlah Sorbitan
Monostearate sebagai Emulsifying agent (Lesmana, 2012).
3. Aktivitas Antimikroba Ekstrak Etanol Daun Beluntas (Pluchea indica L.)
dan Stabilitas Aktivitasnya pada Berbagai Konsentrasi Garam dan Tingkat
3. Manfaat Penelitian
a. Manfaat teoritis
Menambah pengetahuan mengenai formulasi sabun cuci tangan antibakteri
dari bahan alam daun beluntas (Pluchea indica (L.) Less) dengan
menggunakan CMC-Na sebagai gelling agent.
b. Manfaat praktis
Memperoleh informasi sifat fisik dan stabilitas fisik sabun cuci tangan
antibakteri ekstrak daun beluntas dengan menggunakan variasi jumlah
B. Tujuan Penelitian 1. Tujuan umum
Mengetahui perbedaan sifat fisik dan stabilitas fisik sabun cuci tangan
antibakteri ekstrak etanol daun beluntas (Pluchea indica (L.) Less) dengan
variasi jumlah CMC-Nasebagai gelling agent.
2. Tujuan khusus
a. Mengetahui aktivitas antibakteri ekstrak etanol daun beluntas terhadap isolat
bakteri di tangan.
b. Untuk mengetahui perbedaan sifat fisik dan stabilitas fisik yang signifikan
pada variasi jumlah CMC-Na dalam sabun cuci tangan antibakteri ekstrak
7 BAB II
PENELAAHAN PUSTAKA
A. Cuci Tangan
Cuci tangan merupakan salah satu cara untuk menghindari penularan
penyakit terutama penyakit yang ditularkan melalui makanan. Kebiasaan mencuci
tangan secara teratur perlu dilatih. Jika sudah terbiasa mencuci tangan sehabis
bermain atau ketika akan makan makan diharapkan kebiasaan tersebut akan
terbawa sampai tua. Mencuci tangan yang baik dilakukan pada air yang mengalir
(Djauzi, 2009).
Cuci tangan sama dengan proses membuang kotoran dan debu secara
mekanis dari kedua belah tangan dengan memakai sabun dan air, dengan tujuan
untuk mencegah kontaminasi silang (manusia ke manusia atau benda
terkontaminasi ke manusia) suatu penyakit atau perpindahan kuman. Pentingnya
membudayakan cuci tangan memakai sabun secara baik dan benar didukung oleh
data WHO yang menunjukkan, setiap tahun rata-rata 100.000 anak di Indonesia
meninggal dunia karena diare (Apryani, 2012).
B. Bakteri
Bakteri merupakan mikroba prokariotik uniseluler, berkembang biak
secara aseksual dengan pembelahan sel. Semua bakteri memiliki struktur sel yang
relatif sederhana. Berdasarkan komposisi dan struktur dinding sel, maka bakteri
dibagi ke dalam dua golongan yaitu bakteri gram positif dan bakteri gram negatif
Berdasarkan bentuk bakteri digolongkan menjadi tiga golongan utama,
yaitu bentuk coccus (bulat), bentuk basil (batang), dan bentuk spiral. Komponen
utama struktur bakteri terdiri atas makromolekul, yaitu DNA, RNA, protein,
polisakarida, dan fosfolipida. Makromolekul terdiri atas sub-unit primer, yaitu
nukleotida, asam amino dan karbohidrat. Secara keseluruhan, struktur utama
makromolekul sangat mempengaruhi sifat-sifat suatu sel dan menentukan
perbedaan fungsi sel itu dalam sistem biologi (Radji, 2009).
Tabel I. Struktur Sel Bakteri (Radji, 2009)
Makromolekul Penyusun Materi Sel Bakteri
Makromolekul Sub-unit primer Terdapat pada
Asam nukleat
Flagel, pili, dinding sel, membran sitoplasma, ribosom, sitoplasma
Polisakarida Karbohidrat Kapsul bakteri, badan inklusi, dinding sel
Fosfolipida Asam lemak Membran Sel
Bakteri dapat ditemukan sebagai flora normal dalam tubuh manusia yang
sehat. Sebagai flora normal manusia, bakteri merupakan hal yang sangat penting
dalam melindungi tubuh dari datangnya bakteri patogen. Namun pada beberapa
kasus dapat menyebabkan infeksi jika manusia tersebut mempunyai toleransi yang
rendah terhadap mikroorganisme. Contohnya E. coli paling banyak dijumpai
Penyebaran bakteri pada manusia dapat terjadi melalui kulit, hidung
atapun mulut. Kulit secara konstan berhubungan dengan bakteri dari udara atau
dari benda-benda, tetapi kebanyakan bakteri ini tidak tumbuh pada kulit karena
kulit tidak sesuai untuk pertumbuhannya. Pada umumnya bakteri pada kulit
mampu bertahan lama karena kulit mengeluarkan substansi bakterisidal (Pelczar,
2005). Bakteri dapat menimbulkan penyakit pada mahkluk hidup lain karena
memiliki kemampuan menginfeksi, mulai dari infeksi ringan sampai infeksi berat
(Radji, 2009).
Dalam penelitian berjudul “Identifikasi Mikroorganisme Pada Tangan
Tenaga Medis dan Paramedis di Unit Perinatologi Rumah Sakit Abdul Moeloek
Bandar Lampung” ditemukan berbagai macam bakteri di tangan paramedis seperti
Staphylococcus epidermidis, Staphylococcus saprophyticus, Staphylococcus
aureus, Serratia liquefacients, Pseudomonas aeruginosa, Enterobacter aerogenes,
Citrobacter freundii, dan Salmonella sp (Pratami, Apriliana, dan Rukmono,
2014).
C. Isolasi Mikroba
Isolasi merupakan suatu tindakan pengambilan mikroorganisme yang
terdapat di alam kemudian menumbuhkannya dalam suatu medium buatan
(Sutedjo, Kartasapoetra, dan Sastroatmodjo, 1996). Untuk dapat mengisolasi
mikroba dari suatu mikroba, dapat digunakan beberapa perangkat prosedur yaitu:
1. Metode taburan (pour plate)
Dalam proses ini suspensi bakteri dalam cairan dicampur dengan agar yang
cawan petri, dibiarkan mendingin supaya membeku dan diinkubasi. Bakteri akan
tumbuh dibawah atau di atas permukaan agar (Tarigan, 1988).
2. Metode sebaran (spread plate)
Dalam metode ini suspensi bakteri diencerkan dalam cairan tertentu dan
disebarkan pada media nutrient agar, kemudian sebuah batang gelas yang
dibengkokkan dapat digunakan untuk menyebarkan suspensi bakteri yang akan
diisolasi. Cara ini dilakukan beberapa kali sehingga hanya diperoleh satu jenis
mikroba (Tarigan, 1988).
3. Metode goresan (steak plate)
Apabila ingin mengisolasi suatu mikroba yang terdapat di dalam tanah
maka kita dapat membuat suspensi tanah tersebut dengan air yang steril. Lalu
ambil nutrient agar dan dituangkan ke dalam cawan petri yang steril. Setelah
dingin diinokulasi suspensi tersebut pada nutrient agar dengan menggunakan
loop dan menggoreskannya pada permukaan media yang digunakan. Inkubasi
dalam incubator dengan suhu 37oC dan setelah 3-4 hari dapat diamati
pertumbuhan bakteri tersebut (Tarigan, 1988).
D. Uji Potensi Senyawa Antibakteri
Uji potensi senyawa antibakteri bertujuan untuk mengetahui kemampuan
suatu senyawa uji dalam menghambat pertumbuhan bakteri dengan mengukur
respon pertumbuhan populasi mikroorganisme terhadap agen antibakteri (Pratiwi,
2008). Metode uji potensi suatu senyawa antibakteri dapat dilakukan dengan cara
1. Metode difusi sumuran
Metode difusi merupakan metode uji potensi antimikroba secara kualitatif
untuk menentukan aktivitas antimikroba (Boyd, 1984). Metode difusi didasarkan
pada kemampuan obat untuk berdifusi ke dalam media tempat bakteri uji
berkembang biak secara optimal (Hugo dan Russel, 1987).
2. E-test
Metode ini digunakan untuk mengestimasi KHM (Kadar Hambat
Minimum), yaitu konsentrasi minimal suatu agen antibakteri untuk dapat
menghambat pertumbuhan mikroorganisme. Metode ini menggunakan strip
plastik yang mengandung agen antibakteri dari kadar terendah hingga kadar
tertinggi dan diletakkan pada permukaan media agar yang telah diinokulasikan
dengan bakteri uji (Pratiwi, 2008).
3. Metode ditch-plate
Metode ini dilakukan dengan cara menghilangkan potongan agar dari
cawan dan mengisi lubang yang terbentuk dengan agar yang telah berisi senyawa
antibakteri. Medium dapat diatur sedemikian rupa hingga beberapa bakteri dapat
diinokulasikan secara streakplate pada agar yang telah mengandung antibakteri
tersebut. Metode ini cocok untuk pengujian senyawa terhadap sejumlah besar
bakteri (Pratiwi, 2008).
4. Metode disc diffusion
Metode ini digunakan untuk menggunakan papper disc yang berisikan
bakteri uji, kemudian area jernih yang terbentuk menunjukkan adanya hambatan
pertumbuhan bakteri (Pratiwi, 2008).
E. Pengukuran Diameter Zona Hambat
Zona hambat merupakan zona terhambatnya pertumbuhan bakteri yang
disebabkan oleh suatu senyawa antibakteri. Pengukuran diameter zona hambat
dapat diukur dengan menggunakan jangka sorong (Pelczar, 1986). Selain
menggunakan jangka sorong, dapat digunakan Sorcerer Image Analysis System
untuk mengukur zona hambat. Prinsip pengukuran zona hambat dengan
membandingkan perbedaan secara kontras antara zona jernih dan zona
pertumbuhan bakteri. Zona hambat dapat dianalisis secara tunggal atau beberapa
zona hambat dengan menggunakan program scanning measurement frames. Data
dapat dikirim langsung ke Microsoft Excel atau database Oracle untuk diolah
lebih lanjut (Reynolds, 2013).
F. Daun Beluntas (Pluchea indica (L.) Less) 1. Taksonomi tanaman
2. Nama tanaman
Nama daerah : Luntas (Jawa Tengah), Beluntas (Sunda), Baluntas
(Madura) , Lamutasa (Makasar), dan Lenabou (Timor)
Nama asing : : Marsh heabane dan Luan yi (Cina) (Hariana, 2002).
3. Deskripsi tanaman
Gambar 1. Tanaman Beluntas (Dalimartha, 1999)
Tanaman beluntas memiliki habitat perdu dengan tinggi 1-1,5 m.
Batangnya berkayu, bulat, tegak, bercabang, bila masih mudah berwarna ungu
setelah tua putih kotor. Daunnya tunggal, berbentuk bulat telur, tepi rata, ujung
runcing, pangkal tumpul, berbulu halus, panjang 3,8-6,4 cm, lebar 2-4 cm,
tulangnya menyirip, berwarna hijau. Bunganya majemuk, mahkota lepas, putik
bentuk jarum, panjang kurang lebih 6 mm, berwarna hitam kecoklatan, kepala sari
berwarna putih kekuningan. Akar beluntas merupakan akar tunggang dan
bercabang (Syamsuhidayat dan Hutapea, 1991).
Perbanyakan tumbuhan beluntas dilakukan dengan stek batang. Beluntas
dirawat dengan disiram air cukup, dijaga kelembapan tanahnya, dan dipupuk
kering pada tanah yang keras dan berbatu atau ditanam sebagai tanaman pagar.
Tumbuhan ini memerlukan cukup cahaya matahari atau sedikit naungan
(Dalimartha, 1999).
4. Kandungan kimia
Kandungan kimia yang terdapat pada daun beluntas (Pluchea indica (L.)
Less) antara lain alkaloid, flavonoid, tanin, minyak atsiri, natrium, kalium,
aluminium, kalsium, magnesium, dan fosfor. Sedangkan akarnya mengandung
flavonoid dan tanin (Dalimartha, 1999).
5. Manfaat daun beluntas
Daun beluntas berbau khas aromatis dan rasanya getir, berkhasiat untuk
meningkatkan nafsu makan (stomatik), penurun demam (antipiretik), peluruh
keringat (diaforetik), penyegar, TBC kelenjar, nyeri pada rematik dan keputihan
(Dalimartha, 1999). Penelitian lain yang telah dilakukan dan menunjukkan bahwa
daun beluntas (Pluchea indica (L.) Less) memiliki aktivitas antibakteri karena
adanya senyawa flavonoid (Purnomo, 2001). Daun beluntas yang telah direbus
juga dipercaya untuk mengobati penyakit kulit (Winarno dan Sundari, 1998).
G. Ekstraksi
Ekstraksi tanaman obat adalah pemisahan secara kimia atau fisika
suatu/sejumlah bahan padat atau bahan cair dari suatu padatan, yaitu tanaman obat
(Agoes, 2009). Pemilihan metode ekstraksi harus mempertimbangkan berbagai
keadaan, diantaranya sifat jaringan tanaman, sifat kandungan zat aktif serta
digolongkan ke dalam dua bagian besar, yaitu ekstraksi cair-cair dan ekstraksi cair
padat (Harborne, 1996).
Ekstrak adalah sediaan kering, kental, atau cair dibuat dengan menyari
simplisia nabati atau hewani menurut cairan yang cocok. Cairan penyari yang
digunakan dalam pembuatan ekstrak adalah air, eter atau campuran etanol dan air
(Departemen Kesehatan Republik Indonesia, 1995).
1. Maserasi
Maserasi merupakan proses paling tepat dimana serbuk yang sudah halus
dimungkinkan untuk direndam dalam penyari sampai meresap dan melunakkan
susunan sel, sehingga zat-zat yang mudah larut akan melarut (Ansel, 1989).
Maserasi digunakan untuk penyarian simplisia yang mengandung zat aktif yang
mudah larut dalam cairan penyari, tidak mengandung zat yang mudah
mengembang dalam cairan penyari (Departemen Kesehatan Republik Indonesia,
1986).
Proses pemilihan cairan penyari harus dipertimbangkan dan sesuai dengan
zat aktif yang berkhasiat yang artinya dapat memisahkan zat aktif tersebut dari
senyawa lainnya dalam bahan, sehingga ekstrak yang dihasilkan mengandung
sebagian besar senyawa aktif berkhasiat tersebut (Departemen Kesehatan
Republik Indonesia, 2000). Kelebihan dari metode ini adalah cara pengerjaan dan
peralatan yang digunakan relatif sederhana dan mudah. Kekurangan dari metode
ini adalah pengerjaan lama dan penyarian kurang sempurna (Departemen
H. Sabun
Mekanisme pembersihan sabun: surfaktan pada sabun akan menurunkan
tegangan antarmuka antara kotoran dan permukaan kulit. Bagian polar dari
surfaktan akan berinteraksi dengan air, sedangkan bagian non-polar akan
berinteraksi dengan kotoran yang biasanya berupa lemak. Surfaktan-surfaktan
tersebut akan menyusun diri membentuk misel dengan kotoran yang terjebak di
dalamnya. Bagian luar misel adalah gugus polar yang mudah dicuci dengan air
(Rieger, 2000).
I. Gel
Gel adalah sediaan semi solid dimana terdapat interaksi antar partikel
koloid dengan suatu pembawa berupa cairan. Berdasarkan sifat alami jaringan
struktur tiga dimensi yang terbentuk, terdapat dua macam gel, yaitu: dispersi
padatan dan polimer hidrofilik (Jones, 2008). Gel dapat digunakan secara topikal
atau dimasukkan kedalam lubang tubuh (Dirjen POM, 1995). Gel merupakan
sistem penghantaran obat yang sempurna untuk cara pemberian yang beragam dan
kompatibel dengan banyak bahan obat yang berbeda (Allen dan Loyd, 2002).
J. Gelling Agent
Pada formulasi sediaan gel terdapat gelling agent. Komposisi gelling agent
berpengaruh terhadap sifat fisik dan stabilitas fisik sediaan gel, karena gelling
agent akan membentuk sistem jaringan tiga dimensi yang menjebak medium
pendispersi. Sifat fisik yang dipengaruhi oleh gelling agent meliputi daya sebar
penghantaran zat aktif. Oleh karena itu diperlukan konsistensi formula yang
optimum (Garg, Aggrawal. Garg, dan Singla, 2002)
Menurut Pena (cit., Kurniawan, 2013), saat didispersikan dalam suatu
pelarut yang sesuai gelling agent bergabung dan saling menjerat, kemudian
membentuk struktur jarring koloid tiga dimensi. Jaring ini yang akan membatasi
aliran cairan. Struktur ini juga menahan deformasi dan bertanggung jawab
terhadap viskositas gel.
1. Sodium Carboxy Methyl Cellulose (CMC-Na)
CMC-Na merupakan polimer sintetik dengan berat molekul besar yang
terdiri atas rantai silang antara asam akrilat dengan alil sukrosa atau alil ester dari
pentaerythritol. Pemeriannya adalah tidak berwarna, asam, halus, serbuk
higroskopis dengan bau khas. CMC-Na mengandung 52-68% gugus asam
karboksilat (COOH) dalam bentuk kering. CMC-Na berada pada range
konsentrasi 3,0-6,0% yang berfungsi sebagai gelling agent (Rowe, Sheskey, dan
Quinn, 2009).
CMC-Na larut di dalam air di segala temperatur. Garam natrium yang
terbentuk dapat didispersikan di dalam air dingin dengan cepat sebelum partikel
terhidrasi dan mengembang menjadi gumpalan-gumpalan padatan membentuk
sistem gel yang lengket. Viskositas produk dapat menurun jika pH yang
dihasilkan berada pada kisaran pH di bawah 5 dan bila berada di kisaran pH di
CMC-Na sering digunakan pada formulasi sediaan oral, topikal dan
beberapa sediaan parenteral. CMC-Na juga dapat digunakan pada sediaan
kosmetik, dan produk makanan (Rowe, Sheskey, dan Quinn, 2009).
Gambar 2. Struktur CMC-Na (Sodium Carboxy Methyl Cellulose) (Rowe, Sheskey, dan Quinn 2009)
K. Formulasi 1. Surfaktan
Surfaktan adalah zat yang mempunyai gugus hidrofil dan lipofil sekaligus
dalam molekulnya. Zat ini akan berada di permukaan cairan atau antar muka dua
cairan dengan cara teradsorbsi (Moechtar, 1989). Surfaktan berdasarkan
karakteristik muatannya, dikelompokkan menjadi golongan anionik (contoh:
sodium lauryl sulphate), golongan kationik, golongan amfoterik dan golongan
nonionik (Attwood, 2008).
a. Sodium lauryl sulphate
Sinonim dodecylalcohol, hydrogen sulphate, sodium salt, dodecyl sodium
sulphate, dodecylsulphate sodium salt, lauryl sodium sulphate. Klasifikasi: alkyl
sulphate salt. Sodium lauryl sulphate dignakan sebagai detergent, penurun
tegangan permukaan, wetting agent, emulsifying, foaming agent. Untuk sediaan
topikal digunakan pada konsentrasi 0,1 – 12,7% (Michael and Ash, 2004).
Sodium lauryl sulphate memiliki panjang rantai 12 atom karbon dan
merupakan satu dari sekian banyak surfaktan yang umum digunakan. Secara
umum, alkyl sulphate merupakan pembusa yang baik, terlebih pada air sadah
(Barel, 2009).
Sodium lauryl sulphate banyak digunakan dalam kosmetik dan formulasi
sediaan topikal. Sodium lauryl sulphate stabil pada kondisi penyimpanan normal.
Namun dalam larutan di bawah kondisi ekstrim, yaitu pH 2,5 atau kurang dari itu,
dapat mengalami hidrolisis terhadap alkohol, dan natrium lauril bisulfat. Materi
bentuk serbuk harus disimpan dalam wadah tertutup baik di tempat yang sejuk
dan kering (Rowe, Sheskey, dan Quinn, 2009).
b. Humektan
Humektan juga berfungsi menjaga kandungan lembab dan stabilitas dari
sediaan kosmetik itu sendiri (Mitsui, 1997).
a. Gliserol
Gliserol merupakan cairan seperti sirup jernih dengan rasa manis. Dapat
sering digunakan sebagai stabilisator dan sebagai suatu pelarut pembantu dalam
hubungannya dengan air dan alkohol (Ansel, 1989).
Gliserol dapat bercampur dengan air dan dengan etanol, tidak larut dalam
kloroform, dalam eter, dalam minyak lemak dan dalam minyak menguap. Bobot
jenisnya tidak kurang dari 1,249 (Departemen Kesehatan Republik Indonesia,
1995). Gliserol digunakan sebagai emollient dan humektan dalam sediaan topikal
dengan rentang konsentrasi 0,2 – 65,7% (Smolinske, 1992).
Gambar 4. Struktur Gliserol (Rowe, Sheskey, dan Quinn, 2009)
b. Propilen glikol
Propilen glikol, C3H8O2, memiliki BM 76,09. Pemerian: cairan kental,
jernih, tidak berwarna, rasa khas, praktis tidak berbau, menyerap air pada udara
lembab. Kelarutan: dapat bercampur dengan air, kloroform, aseton; larut dalam
eter dan dalam beberapa minyak essensial; tidak dapat bercampur dengan minyak
lemak (Departemen Kesehatan Republik Indonesia, 1995).
Gambar 5. Struktur Propilen Glikol (Rowe, Sheskey, dan Quinn., 2009)
c. Pengawet
Pengawet merupakan bahan untuk mencegah tumbuhnya, atau bereaksi
pada produk. Pengawet harus memiliki aktivitas berspektrum luas, stabil, tidak
berbau dan berwarna, efektif dalam konsentrasi rendah dan aman (Tranggono dan
Latifah, 2007).
Kesehatan Republik Indonesia, 1995).
Dalam peraturan Kepala Badan Pengawas Obat dan Makanan (BPOM)
Republik Indonesia No: HK.00.05.42.1018 tentang Bahan Kosmetik
menyantumkan bahwa penggunaan bahan 4-hydroxybenzoic acid, its salt and
esters dengan nomor ACD 12, di jelaskan bahwa kadar maksiumum 0,4 persen
(asam) untuk ester tunggal serta 0,8 persen (asam) untuk ester campuran yang
ditambahkan ke dalam sediaan kosmetik. Di jelaskan bahwa ester adalah methyl,
ethyl, propyl, isopropyl, butyl, isobutyl, dan phenyl (Badan POM RI, 2008).
Metil paraben secara digunakan sebagai antimikroba pada kosmetik,
produk makanan, dan sediaan farmasi. Konsentrasi penggunaan metil paraben
sebagai antimikroba pada sediaan topikal adalah 0,02-0,3%. Metil paraben
bersifat nonmutagenik, nonteratogenik, dan nonkarsinogenik (Rowe, Sheskey, dan
Gambar 6. Struktur Metil Paraben (DepKes RI,1979)
d. Etanol
Etanol adalah campuran etil alkohol dan air. Etanol mengandung tidak
kurang dari 94,7% v/v atau 92,0% dan tidak lebih dari 95,2% v/v atau 92,7%
C2H6O. Pemeriannya cairan tidak berwarna, jernih, mudah menguap dan mudah
bergerak; berbau khas; rasa panas. Mudah terbakar dengan memberikan nyala biru
yang tak berasap (Departemen Kesehatan Republik Indonesia, 1979).
e. Aquadest (Air Murni)
Air murni adalah air yang dimurnikan yang diperoleh dengan destilasi,
perlakuan menggunakan penukar ion, osmosis balik, atau proses lain yang sesuai.
Dibuat dari air yang memenuhi persyaratan air minum. Tidak mengandung zat
tambahan lain. Pemerian: cairan jernih, tidak berwarna; dan tidak berbau
(Departemen Kesehatan Republik Indonesia, 1995).
L. Sifat Fisik dan Stabilitas Fisik
Sediaan uji harus dievaluasi untuk menjamin bahwa sediaan memiliki
karakteristik yang diinginkan. Karakteristik tersebut harus mencakup penampilan
sediaan, warna, keseragaman bentuk, berat jenis, pH, dan viskositas. Parameter
tersebut harus direkam untuk stabilitas pada kondisi penyimpanan dengan interval
1. Viskositas
Rheology berasal dari bahasa Yunani, “Rheo” berarti “aliran” dan “Logos” yang berarti “ilmu”. Rheology didefinisikan sebagai aliran suatu cairan. Sifat alir
berperan dalam aplikasi formulasi sediaan farmasi. Penggolongan bahan menurut
tipe aliran dan deformasinya dibagi menjadi dua yaitu, sistem Newton dan sistem
non-Newton (Martin, Swarbick, dan Cammarata, 1993). Sifat alir Newton
menunjukkan adanya hubungan linier antara gaya geser (shear stress) dengan
kecepatan geser (Lieberman, Rieger, dan Banker, 1996).
Viskositas adalah suatu pernyataan tahanan dari suatu cairan untuk
mengalir, makin tinggi viskositas maka makin besar tahanannya. Semakin tinggi
viskositas maka tahanan suatu cairan untuk dapat mengalir semakin besar pula
(Martin, Swarbick, dan Cammarata, 1993). Uji stabilitas merupakan proses
evaluasi untuk menjamin bahwa sifat-sifat utama produk tidak berubah selama
waktu yang dapat diterima oleh konsumen. Pergerseran viskositas adalah uji yang
biasa dilakukan untuk melihat stabilitas viskositas selama penyimpanan. Adanya
variasi pada ukuran atau jumlah droplet dapat dideteksi dengan pergeseran
viskositas secara nyata (Aulton dan Diana, 1991).
2. Penetapan pH
Harga pH merupakan harga yang dapat ditentukan dengan alat
potensiometrik (pH meter atau indicator pH) yang sesuai dan telah dibakukan.
Pengukuran dilakukan pada suhu ±250C, kecuali dinyatakan lain dalam
3. Ketahanan busa
Stabilitas busa merupakan kemampuan busa untuk mempertahankan
parameter utamanya dalam keadaan konstan selama waktu tertentu. Parameter
tersebut meliputi ukuran gelembung, kandungan cairan, dan total volume busa.
Foam lifetime (waktu hidup busa) merupakan ukuran paling sederhana untuk
menunjukkan stabilitas busa (Exerowa, 1998).
Beberapa faktor yang dapat mempengaruhi ketahanan busa, antara lain
adalah viskositas yang tinggi. Pada viskositas tinggi dapat memperlambat proses
drainage, sehingga busa sulit terbentuk (Myers, 2006).
M. Landasan teori
Bakteri dapat ditemukan sebagai flora normal dalam tubuh manusia yang
sehat, namun pada beberapa kasus dapat menyebabkan infeksi jika manusia
tersebut mempunyai toleransi yang rendah terhadap mikroorganisme. Bakteri
dapat ditularkan melalui tangan manusia.
Ekstrak etanol daun beluntas telah diteliti memiliki kandungan senyawa
fenolik yang terbukti memiliki aktivitas antimikroba terhadap Staphylococcus
aureus, E. coli, Pseudomonas fluorecens dan Salmonela thypi. Dalam penelitian
ini, dibuat sediaan sabun cuci tangan dengan ekstrak etanol daun beluntas.
Sediaan sabun cuci tangan dibuat dalam bentuk sediaan gel. Gel merupakan
sediaan semi solid dimana terdapat interaksi antar partikel koloid dengan suatu
pembawa berupa cairan.
Sifat fisik (viskositas, pH, organoleptis, ketahanan busa) dan stabilitas
dipengaruhi oleh jumlah gelling agent yang terdapat dalam suatu formula gel.
Penambahan gelling agent perlu diperhatikan dalam formulasi sediaan gel sabun
cuci tangan. Gelling agent yang digunakan dalam formulasi ini adalah CMC-Na.
N. Hipotesis
1. Ekstrak etanol daun beluntas (Pluchea indica (L.) Less) memiliki potensi
antibakteri terhadap isolat bakteri tangan.
2. Terdapat perbedaan sifat fisik dan stabilitas fisik pada variasi jumlah
CMC-Na sebagai gelling agent pada formulasi sediaan sabun cuci tangan ekstrak
26 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan penelitian eksperimental murni.
B. Variabel Penelitian
Variabel dalam penelitian ini yaitu:
1. Variabel bebas dalam penelitian ini adalah variasi jumlah CMC-Na dengan konsentrasi sebesar 3%, 4%, 5% , 6% dan variasi konsentrasi ekstrak etanol
daun beluntas yaitu 2%, 4%, 6%, 8% dan 10%.
2. Variabel tergantung dalam penelitian ini adalah zona hambat aktivitas antibakteri ekstrak etanol daun beluntas, sifat fisik dan stabilitas fisik sediaan
sabun cuci tangan ekstrak etanol daun beluntas yang meliputi pH, organoleptis,
viskositas, dan ketahanan busa.
3. Variabel pengacau terkendali dalam penelitian ini adalah alat percobaan, wadah penyimpanan, lama penyimpanan sabun cuci tangan, lama dan
kecepatan pencampuran.
C. Definisi Operasional
1. Sabun cuci tangan antibakteri adalah molekul surfaktan yang memiliki
kemampuan untuk membersihkan dan berfungsi menekan bertumbuhan kuman,
yang diaplikasikan pada tangan.
2. Serbuk daun beluntas (Pluchea indica (L.) Less) merupakan serbuk daun
beluntas yang diperoleh dari hasil budidaya tanaman beluntas yang ada di CV.
Merapi Farma.
3. Ekstrak etanol daun beluntas adalah ekstrak hasil maserasi simplisia daun
beluntas menggunakan pelarut etanol 70%. Penetapan kadar total fenolik
dilakukan oleh LPPT Universitas Gadjah Mada.
4. Gel merupakan sediaan semi solid dimana terdapat interaksi antar partikel
koloid
dengan suatu pembawa berupa cairan.
5. CMC-Na merupakan senyawa yang pada rentang konsentrasi 3-6% dapat
berfungsi sebagai gelling agent.
6. Isolat bakteri tangan merupakan hasil isolasi mikroba dari 3 bagian tangan
yaitu telapak tangan, jari tangan dan punggung tangan.
7. Uji potensi antibakteri merupakan uji yang dilakukan untuk mengetahui
kemampuan ekstrak etanol daun beluntas untuk menghambat pertumbuhan
bakteri.
8. Zona hambat merupakan zona jernih disekitar sumuran, yang menghambat atau
9. Sifat fisik sediaan gel dipengaruhi oleh viskositas, homogenitas, dan distribusi
ukuran partikel. Stabilitas fisik sediaan gel merupakan kemampuan gel sabun
cuci tangan ekstrak daun beluntas untuk bertahan dalam batas spesifiasi yang
diterangkan selama penyimpanan dan penggunaan.
10.Organoleptis merupakan pengamatan yang dilakukan secara visual terhadap
warna, bentuk dan bau sediaan gel sabun cuci tangan ekstrak daun beluntas
setelah penyimpanan 48 jam dan setelah penyimpanan 28 hari.
11.Viskositas adalah ketahanan alir sediaan sabun cuci tangan yang dikukur 48
jam, 7 hari, 14 hari, 21 hari, dan 28 hari.
12. Ketahanan busa adalah kemampuan sediaan untuk mempertahankan volume
busa. Pergeseran ketahanan busa diamati tiap-tiap minggu dalam jangka
waktu satu bulan. Hal ini bertujuan untuk mengetahui perubahan ketahanan
busa yang terjadi selama penyimpanan.
13.Penetapan pH merupakan uji yang dilakukan untuk mengetahui harga pH
sediaan gel sabun cuci tangan ekstrak etanol daun beluntas agar sesuai dengan
D. Bahan dan Alat Penelitian 1. Bahan penelitian
Bahan yang digunakan dalam penelitian ini adalah aquadest steril, Texapon®
(kualitas farmasetis dari PT. Brataco), gliserol (kualitas farmasetis dari PT.
Brataco), propilen glikol (kualitas farmasetis dari PT Brataco), CMC-Na
(kualitas farmasetis PT Brataco), metil paraben, etanol 70%, serbuk daun
beluntas (CV. Merapi Farma), ekstrak etanol daun beluntas (LPPT Universitas
Gadjah Mada Yogyakarta), kultur isolat bakteri tangan dari 3 probandus di
Laboratorium Mikrobiologi Universitas Sanata Dharma Yogyakarta.
2. Alat penelitian
Alat penelitian yang digunakan dalam penelitian: cawan petri, glassware,
paper disk, indikator pH, termometer, jarum ose, spreader, autoklaf (Model
KT-40), bunsen, mikropipet, timbangan analitik (Precise 2000C-2000D1),
Viscometer Rion seri VT 04 (RION-JAPAN), mixer (Philip), mikroskop, oven,
E. Tata Cara Penelitian 1.Pembuatan serbuk daun beluntas
a. Pengumpulan bahan daun beluntas
Bahan yang digunakan adalah daun beluntas yang diperoleh dari CV.
Merapi Farma yang terletak di Jl. Kaliurang Km. 21, Sleman, Yogyakarta.
Pengambilan daun beluntas dipilih berdasarkan warna daun yaitu berwarna
hijau muda serta letak daun yang diambil pucuk 1-6 daun dari atas
tanaman beluntas. Setidaknya daun berumur 50 hari. Identifikasi dilakukan
oleh CV. Merapi Farma yang menyatakan bahwa daun yang digunakan
adalah benar daun beluntas (Pluchea indica (L.) Less).
b. Pembuatan serbuk daun beluntas
Daun beluntas yang telah dipanen, dicuci dengan air mengalir, kemudian
dikeringkan dibawah sinar matahari dengan ditutupi kain hitam. Setelah
pengeringan, dilakukan penyerbukan dengan menggunakan mesin
penyerbuk dengan pengayakan berdiameter 1 mm. Penyerbukan daun
beluntas dilakukan oleh CV. Merapi Farma.
2. Pembuatan ekstrak etanol daun beluntas
a. Ekstraksi serbuk daun beluntas
Ekstraksi serbuk daun beluntas dilakukan dengan metode maserasi
menggunakan pelarut etanol 70% berdasarkan CoA (Ceritificate of
Analysis) yang dilakukan Lembaga Penelitian dan Pengujian Terpadu
b. Penetapan kadar total fenolik
Penetapan kadar total fenolik dilakukan dengan metode spektrofotometri
berdasarkan CoA (Ceritificate of Analysis) yang dilakukan Lembaga
Penelitian dan Pengujian Terpadu Universitas Gadjah Mada (LPPT
UGM).
3. Uji potensi antibakteri ekstrak etanol daun beluntas
a. Pembuatan stok isolat bakteri tangan
Isolasi bakteri dari tangan dilakukan kepada tiga probandus dari bagian
tangan yang berbeda, dengan ktiteria: Probandus telah melakukan
kegiatan dan belum cuci tangan atau belum menggunakan produk
antiseptik untuk tangan. Isolasi dilakukan dengan menempelkan bagian
tangan pada cawan petri berisi media Nutrient Agar (NA) 15 mL secara
aseptis. Tiga bagian tangan tersebut adalah bagian punggung tangan, jari
tangan, dan bagian telapak tangan. Kemudian diinkubasi terbalik selama
24 jam pada suhu 37oC. Isolat bakteri tangan dari tiga probandus yang
telah tumbuh pada media NA cawan petri diambil dengan menggunakan
ose dan ditanam di media NA miring. Kemudian diinkubasi pada suhu
37oC selama 24 jam. Hasil isolasi akan digunakan untuk uji potensi
antibakteri ekstrak etanol daun beluntas. Uji dilakukan dalam
Microbiological Safety Cabinet (MSC).
b. Pembuatan suspensi isolat bakteri uji
Tabung reaksi berisi media Nutrient Broth (NB) disiapkan sebanyak 10
diinokulasikan ke dalam media NB dengan jarum ose, dan diinkubasikan
pada suhu 37oC selama 24 jam. Setelah diinkubasi, media NB di lihat
kekeruhannya (setara dengan standar Mac Farland 1,5 x 108 CFU/mL).
Jika kekeruhannya belum setara dengan standar Mac Farland 1,5 x 108
CFU/mL ditambahkan NB steril sampai kekeruhannya setara dengan
standar Mac Farland 1,5 x 108 CFU/mL.
c. Pembuatan konsentrasi ekstrak etanol daun beluntas
1.) Konsentrasi ekstrak etanol daun beluntas 2%
Ditimbang 0,2 g ekstrak etanol daun beluntas, kemudian dilarutkan
dengan sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur
10 mL, lalu ditambahkan dengan aquadest steril sampai tanda.
2.) Konsentrasi ekstrak etanol daun beluntas 4%
Ditimbang 0,4 g ekstrak etanol daun beluntas, kemudian dilarutkan
dengan sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur
10 mL, lalu ditambahkan dengan aquadest steril sampai tanda.
3.) Konsentrasi ekstrak etanol daun beluntas 6%
Ditimbang 0,6 g ekstrak etanol daun beluntas, kemudian dilarutkan
dengan sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur
10 mL, lalu ditambahkan dengan aquadest steril sampai tanda.
4.) Konsentrasi ekstrak etanol daun beluntas 8%
Ditimbang 0,8 g ekstrak etanol daun beluntas, kemudian dilarutkan
dengan sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur
5.) Konsentrasi ekstrak etanol daun beluntas 10%
Ditimbang 1 g ekstrak etanol daun beluntas, kemudian dilarutkan dengan
sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur 10 mL,
lalu ditambahkan dengan aquadest steril sampai tanda.
6.) Konsentrasi ekstrak etanol daun beluntas 100%
Konsentrasi ekstrak etanol daun beluntas 100% digunakan sebagai
kontrol positif. Ditimbang 10 g ekstrak etanol daun beluntas, kemudian
dilarutkan dengan sedikit aquadest steril. Ekstrak dimasukkan ke dalam
labu ukur 10 mL, lalu ditambahkan dengan aquadest steril sampai tanda.
d. Uji aktivitas antibakteri ekstrak etanol daun beluntas
Potensi antibakteri ekstrak etanol daun beluntas diuji terhadap isolat
bakteri tangan dengan metode difusi sumuran. Seri konsentrasi ekstrak
etanol daun beluntas adalah 2%, 4%, 6%, 8%, dan 10% dengan
konsentrasi 100% sebagai kontrol positif. Media NA yang digunakan
dibagi menjadi 2 bagian yaitu base layer (10 mL) dan seed layer (15
mL). Bagian base layer dituang ke cawan petri steril dan dibiarkan
memadat terlebih dahulu. Untuk seed layer, diambil 1 mL dari stok
suspensi bakteri uji yang sudah disetarakan kemudian diinokulasikan ke
media NA secara pour plate. Media NA yang mengandung bakteri
dibiarkan sampai memadat. Dibuat sumuran pada petri dengan pelubang
gabus no. 4. Kemudian dengan menggunakan mikropipet, diinokulasikan
50 μL ekstrak etanol daun beluntas dengan berbagai seri konsentrasi.
e. Penentuan konsentrasi ekstrak yang akan diformulasikan ke dalam
sediaan gel sabun cuci tangan antibakteri
Diamati zona jernih pada bakteri. Konsentrasi ekstrak etanol daun
beluntas ditentukan dengan melihat aktivitas antibakteri yang paling baik
dengan mengamati zona hambat yang terbentuk dan membandingkannya
dengan kontrol negatif. Dilakukan analisis statistik untuk melihat
perbandingan diameter zona hambat antar konsentrasi secara signifikan.
4. Pembuatan sediaan gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas
a. Modifikasi formula gel sabun cuci tangan antibakteri ekstrak etanol
daun beluntas
Formula yang digunakan dalam pembuatan sediaan gel sabun cuci
tangan antibakteri
Tabel II. Formula Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak
Etanol Daun Beluntas
Bahan Jumlah (g)
Sodium Lauryl Sulphate : Texapon® 2,5
Gliserol 30
Propilen Glikol 15
Metil Paraben 0.10
CMC-Na 3-6
Ekstrak Etanol Daun Beluntas 6
Tabel III.Variasi Jumlah CMC-Na pada Formula Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas
b. Pembuatan gel sabun cuci tangan antibakteri ekstrak etanol daun
yang dibuat 48 jam setelah pembuatan sediaan gel sabun cuci tangan.
2. Viskositas
Gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas
dimasukkan ke dalam wadah dan dipasang pada viscostester VT 04.
Nilai viskositas sediaan ditunjukkan oleh jarum penunjuk saat
viscostester dinyalakan. Pengukuran dilakukan 48 jam setelah
pembuatan sediaan gel sabun cuci tangan kemudian hasilnya dicatat.
3. Ketahanan busa
busa. Pengukuran dilakukan 48 jam setelah pembuatan sediaan gel
sabun cuci tangan.
4. Pengukuran pH
Penentuan pH sediaan dilakukan dengan cara mencelupkan pH meter
ke dalam setiap sediaan sabun cuci tangan gel. Pengukuran dilakukan
48 jam setelah pembuatan sediaan gel sabun cuci tangan kemudian
hasilnya dicatat.
b. Stabilitas fisik
Stabilitas fisik dilihat dengan mengamati sifat fisik sediaan meliputi
penyimpanan, yaitu pada waktu 48 jam, 7 hari, 14 hari, 21 hari, dan 28
hari penyimpanan.
6. Uji aktivitas antibakteri sediaan gel sabun cuci tangan antibakteri terhadap isolat bakteri tangan
a. Pembuatan suspensi bakteri uji
Tabung reaksi berisi media NB disiapkan sebanyak 9 ml. Kemudian kultur
bakteri yang telah tumbuh pada media NA miring diinokulasikan ke dalam
media NB dengan jarum ose, dan diinkubasikan pada suhu 370C selama 24
jam. Setelah diinkubasi, media NB dilihat kekeruhannya (setara dengan
standar Mac Farland 1,5 x 108 CFU/mL). Jika kekeruhannya belum setara
dengan standar Mac Farland 1,5 x 108 CFU/mL ditambahkan NB steril
sampai kekeruhannya setara dengan standar Mac Farland 1,5 x 108
CFU/mL.
b. Uji aktivitas sediaan gel sabun cuci tangan antibakteri ekstrak etanol daun
beluntas
Gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas dengan
berbagai konsentrasi yang dibuat diletakkan pada masing-masing lubang
sumuran yang tersedia pada media yang sebelumnya telah diinokulasikan
bakteri uji secara pour plate. Kontrol positif yang digunakan adalah sabun
cuci tangan Lifebuoy Color Changing® dan kontrol negatif yang
digunakan adalah basis gel. Diinkubasi selama 24 jam pada suhu 37oC,
kemudian diamati hasilnya. Diameter zona hambat yang dihasilkan
sebagai dasar untuk mengamati daya antibakteri yang dibandingkan
F. Analisis Data
Data yang dihasilkan berupa data diameter zona hambat, viskositas,
ketahanan busa, pergeseran viskositas dan pergeseran ketahanan busa. Data yang
diperoleh, dianalisis dengan menggunakan software R (www.r-project.org) dari program R 3.1.0. untuk melihat signifikansi dari variasi jumlah CMC-Na sebagai
gelling agent terhadap sifat fisik dan stabilitas fisik sediaan sabun cuci tangan.
Data yang memenuhi kriteria parametrik dianalisis menggunakan One Way
ANOVA untuk mengetahui perbedaan data dilanjutkan dengan uji t-independent
untuk mengetahui signifikansi pengaruh gelling agent terhadap sifat fisik. Untuk
stabilitas fisik gel dilakukan uji t-berpasangan. Data yang memenuhi kriteria
non-parametrik dianalisis menggunakan uji Kruskal-Wallis untuk mengetahui
perbedaan data lebih dari dua kelompok, sedangkan uji Wilcoxon untuk melihat
perbedaan yang signifikan dari dua kelompok data. Pada taraf kepercayaan 95%
data berbeda signifikan jika nilai probabilitas lebih kecil dari 0,05 (p-value <