PENGARUH VARIASI JUMLAHCARBOPOL®SEBAGAIGELLING AGENTTERHADAP SIFAT FISIK DAN STABILITAS FISIK SEDIAAN
SABUN CUCI TANGAN EKSTRAK ETANOL DAUN BELUNTAS (Pluchea indica (L.) Less) DAN UJI AKTIVITAS ANTIBAKTERI
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
oleh :
Rosalia Suryaningtyas
NIM : 108114162
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH VARIASI JUMLAHCARBOPOL®SEBAGAIGELLING AGENTTERHADAP SIFAT FISIK DAN STABILITAS FISIK SEDIAAN
SABUN CUCI TANGAN EKSTRAK ETANOL DAUN BELUNTAS (Pluchea indica (L.) Less) DAN UJI AKTIVITAS ANTIBAKTERI
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
oleh :
Rosalia Suryaningtyas
NIM : 108114162
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Faith is not believing that God can, it is knowing that
God will.
I can do all things through God who
strengthens me
I dedicate my work to :
My Great God who always help me up when I feel down
My Parents Viperiyanto and Winarti, my uncle Winarto and aunt Purwiani,
vii PRAKATA
Puji dan syukur kepada Tuhan Yang Maha Esa untuk segala berkat dan
penyertaan-Nya sehingga penulis dapat menyelesaikan penelitian guna memenuhi
tugas akhir dengan judul “Pengaruh Variasi Jumlah Carbopol® sebagai Gelling Agent terhadap Sifat Fisik dan Stabilitas Fisik Sediaan Sabun Cuci Tangan Ekstrak Etanol Daun Beluntas (Pluchea indica (L.) Less) dan Uji Aktivitas
Antibakteri” dengan lancar dan tepat waktu. Tugas akhir ini disusun untuk
memenuhi salah satu syarat memperoleh gelar Sarjana Strata Satu pada Program
Studi Farmasi (S.Farm.).
Dalam menyelesaikan skripsi ini, penulis mengalami permasalahan dan
kesulitan tetapi karena bimbingan, dukungan dan motivasi dari berbagai pihak,
penulis dapat meyelesaikan tugas akhir ini dengan baik. Oleh karena itu, dengan
segala hormat, penulis ingin mengucapkan terima kasih kepada :
1. Bapak Ipang Djunarko, M.Sc., Apt selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
2. Bapak Septimawanto Dwi Prasetyo, M.Si. Apt selaku Dosen Pembimbing
atas segala dukungan, arahan dan masukan selama proses penyusunan
skripsi.
3. Bapak Prof. Dr. C. J. Soegihardjo, Apt. selaku Dosen Penguji yang telah
memberikan waktu, saran, kritik dan masukan kepada penulis.
4. Ibu Melania Perwitasari, M.Sc, Apt. selaku Dosen Penguji yang telah
viii
5. Seluruh Dosen Fakultas Farmasi Universitas Sanata Dharma yang telah
memberikan ilmunya selama penulis belajar di Program Studi Farmasi.
6. Seluruh staf laboratorium dan karyawan Fakultas Farmasi Universitas
Sanata Dharma yang telah banyak membantu dan bersedia untuk
direpotkan selama penulis mengerjakan penelitian skripsi ini.
7. Kedua orang tua penulis yang sudah memberikan kepercayaan dan
semangat dalam menyelesaikan skripsi ini. Serta adik penulis Thomas dan
Jojo yang membuat penulis selalu tersenyum dan semangat.
8. Soulmate dari awal semester sekaligus mitra kerja skripsi, Marcelina
Widani Amanda Rompas untuk setiap kebersamaan, kerja sama,
perbedaan pendapat, dan dukungan yang diberikan dari awal sampai
selesainya penyusunan laporan akhir ini.
9. H.Roy Wiranata yang selalu memberikan semangat dan masukan kepada
penulis saat mengalami kendala.
10. Astuti Malyawati, Eva Christiana, Elizabeth Sita, Sisca Kristi atas
persahabatan yang luar biasa selama masa perkuliahan.
11. Teman-teman Kost Agatha Maria Magdalena Lita, Maria Karina,
Gabriella Septiana, Trifonia Rosa dan khususnya kak Hetty Doja atas
semangat yang diberikan untuk menyelesaikan laporan akhir skripsi ini.
12. Puspita Sari, Palma, Yoestenia, Devina Permatasari atas kebersamaan dan
perjuangannya di Laboratorium Mikrobiologi Universitas Sanata Dharma.
13. Yustina Wahyu, Victoria Bintang dan Desty Natasari yang tidak pernah
ix
14. Teman-teman angkatan 2010 atas kebersamaannya yang selalu mewarnai
hari-hari penulis selama menjalani masa perkuliahan.
15. Semua pihak yang tidak dapat disebutkan satu per satu karena keterbatasan
penulis, terimakasih untuk bantuan dan semangat yang telah diberikan
kepada penulis.
Penulis menyadari bahwa dalam penyusunan laporan akhir skripsi ini
masih banyak kekurangan dan jauh dari kata sempurna. Penulis mengharapkan
kritik dan saran yang membangun dari pembaca. Penulis juga berharap laporan
akhir skripsi ini bermanfaat bagi seluruh pihak terutama dalam bidang farmasi.
Yogyakarta, 30 Mei 2014
x DAFTAR ISI
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN ... iv
HALAMAN PERSETUJUAN PUBLIKASI... v
PERNYATAAN KEASLIAN KARYA ... vi
PRAKATA... vii
DAFTAR ISI... x
DAFTAR TABEL... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
INTISARI... xvii
ABSTRACT... xviii
BAB I. PENDAHULUAN ... 1
A. Latar Belakang ... 1
1. Rumusan masalah... 4
2. Keaslian penelitian ... 4
3. Manfaat penelitian... 5
a. Manfaat teoritis ... 5
xi
B. Uji Potensi Senyawa Antibakteri... 8
1 Metode dilusi ... 8
F. Sabun Cuci Tangan ... 14
G. Gel ... 14
L. Uji Sifat Fisik Dan Stabilitas Gel... 18
1. Sifat Fisik ... 18
a. Pengamatan organoleptis ... 18
b. Viskositas ... 18
c. Ketahanan busa ... 19
xii
M. Landasan Teori... 20
N. Hipotesis... 22
BAB III. METODOLOGI PENELITIAN ... 23
A. Jenis dan Rancangan Penelitian ... 23
B. Variable Penelitian ... 23
C. Definisi Operational ... 24
D. Bahan dan Alat Penelitian... 25
1. Bahan penelitian... 25
2. Alat penelitian ... 26
E. Tata Cara Penelitian ... 26
1. Pembuatan serbuk daun beluntas ... 26
2. Pembuatan ekstrak etanol daun beluntas... 27
3. Uji potensi antibakteri ekstrak etanol daun beluntas ... 28
4. Pembuatan sediaan gel sabun cuci tangan antibakteri ... 31
5. Evaluasi sediaan gel sabun cuci tangan antibakteri ... 32
6. Uji aktivitas sediaan gel sabun cuci tangan antibakteri ekstrak etanol daun beluntas ... 33
F. Analisis Data ... 34
BAB IV. HASIL DAN PEMBAHASAN ... 35
A. Pembuatan Serbuk Daun Beluntas ... 35
1. Pengumpulan bahan daun beluntas ... 35
2. Pembuatan serbuk daun beluntas ... 36
B. Pembuatan Ekstrak Etanol Daun Beluntas... 37
1. Ekstraksi serbuk daun beluntas ... 37
2. Penetapan kadar total fenolik ... 38
C. Uji Potensi Antibakteri Ekstrak Etanol Daun Beluntas ... 38
1. Pembuatan stok isolat bakteri tangan ... 38
xiii
D. Pembuatan Sediaan Sabun Cuci Tangan
Ekstrak Etanol Daun Beluntas ... 46
E. Uji Sifat Fisik dan Uji Stabilitas Fisik Sediaan Gel Sabun Cuci Tangan Antibakteri Ekstrak Etanol Daun Beluntas ... 49
1. Uji organileptis dan pH ... 50
2. Uji viskositas... 51
3. Pergeseran viskositas ... 53
4. Ketahanan busa ... 55
F. Uji Aktivitas Antibakteri Sediaan Gel Sabun Cuci Tangan Ekstrak Etanol Daun Beluntas ... 56
BAB V. KESIMPULAN DAN SARAN... 59
A. Kesimpulan ... 59
B. Saran... 59
DAFTAR PUSTAKA ... 60
LAMPIRAN ... 65
xiv
DAFTAR TABEL
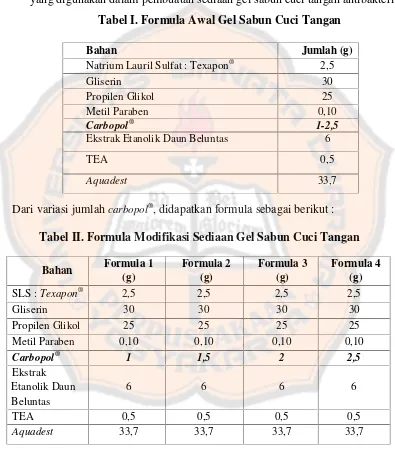
Tabel I. Formula Awal Gel Sabun Cuci Tangan ... 31
Tabel II. Formula Modifikasi Sediaan Gel Sabun Cuci Tangan... 31
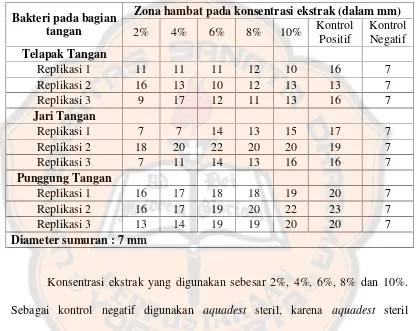
Tabel III. Diameter Zona Hambat Ekstrak Etanol Daun Beluntas
terhadap Isolat Bakteri tangan... 41
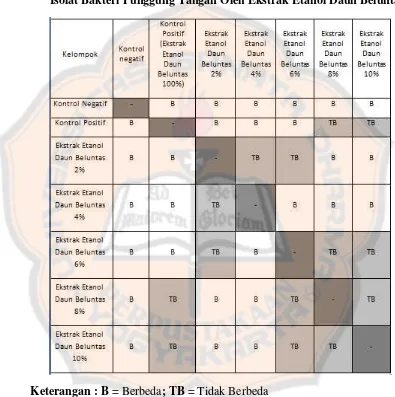
Tabel IV. Hasil UjiWilcoxonDiameter Zona Hambat Pertumbuhan Isolat Bakteri Punggung Tangan oleh Ekstrak Etanol Daun Beluntas... 44
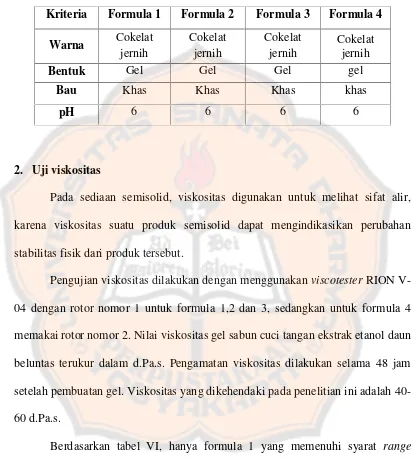
Tabel V. Data Uji Organoleptis dan pH Sediaan Sabun Cuci
Tangan Ekstrak Etanol Daun Beluntas ... 51
Tabel VI. Data Viskositas Sediaan Gel Sabun Cuci Tangan
setelah 48 Jam Pembuatan ... 52
Tabel VII. Hasil Uji Normalitas Shapiro-Wilk untuk Viskositas 48 Jam ... 52
Tabel VIII.Hasil Uji t Berpasangan Pergeseran Viskositas Sediaan
Gel Sabun Cuci Tangan ... 54
Tabel IX. Rata-rata dan SD Ketahanan Busa Setiap Minggu ... 55
Tabel X. Uji Normalitas Ketahanan Busa Gel pada 48 jam ... 56
Tabel XI. Rata-Rata Dan SD Zona Hambat Sediaan
xv
DAFTAR GAMBAR
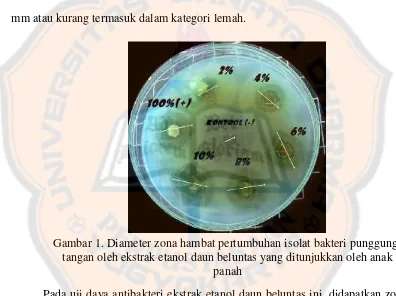
Gambar 1. Diameter Zona Hambat Pertumbuhan Isolat Bakteri
Punggung Tangan oleh Ekstrak Etanol Daun Beluntas...42
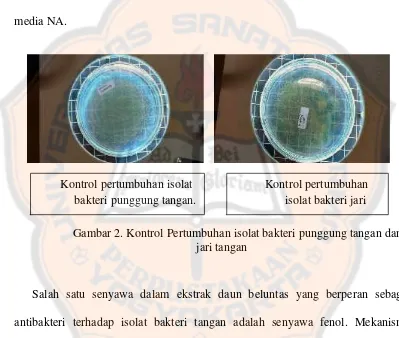
Gambar 2. Kontrol Pertumbuhan Isolat Bakteri Punggung Tangan
dan Jari Tangan ...45
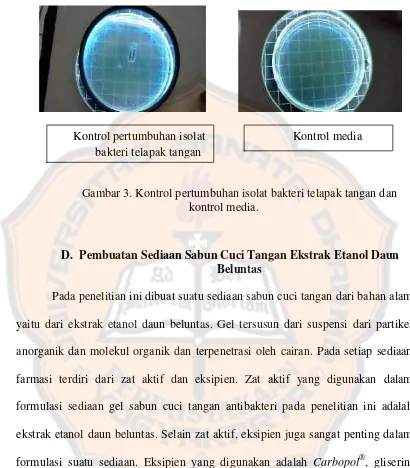
Gambar 3. Kontrol Pertumbuhan Isolat Bakteri Telapak Tangan
dan Kontrol Media ...46
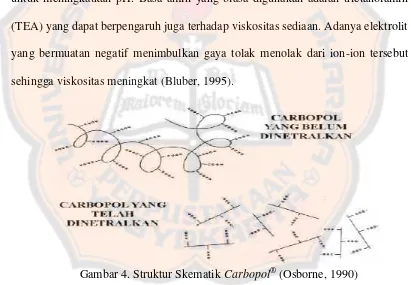
Gambar 4. Struktur SkematikCarbopol®...48 Gambar 5. Grafik PengaruhCarbopol®terhadap Viskositas Gel
Sabun Cuci Tangan setelah 48 Jam Pembuatan...53
xvi
DAFTAR LAMPIRAN
Lampiran 1. Surat Keterangan Simplisia Daun Beluntas ... 66
Lampiran 2. Surat Keterangan Permintaan Pembuatan Ekstrak Maserasi di LPPT UGM ... 67
Lampiran 3. Prosedur pembuatan ekstrak etanol daun beluntas... 68
Lampiran 4. Laporan hasil uji total fenolik ... 70
Lampiran 5. Certificate of Analysis Carbopol 940®...71
Lampiran 6. Tabel diameter zona hambat dan tabel uji Wilcoxon ...72
Lampiran 7. Hasil uji statistikKruskal Wallis...75
Lampiran 8. Hasil uji daya antibakteri ekstrak etanol daun beluntas terhadap isolat bakteri tangan... 76
Lampiran 9. Hasil pengukuran viskositas dan pergeseran viskositas sediaan gel sabun cuci tangan ekstrak etanol daun beluntas... 78
Lampiran 10. Hasil analisis statistik viskositas dan pergeseran viskositas... 79
Lampiran 11. Gambar sediaan gel sabun cuci tangan ekstrak etanol daun beluntas ... 84
Lampiran 12. Gambar dan hasil uji ketahanan busa sediaan gel sabun cuci tangan ekstrak etanol daun beluntas... 85
Lampiran 13. Hasil uji statistik ketahanan busa ... 86
Lampiran 14. Hasil uji aktivitas antibakteri sediaan gel sabun cuci tangan ekstrak etanol daun beluntas ... 89
xvii INTISARI
Penelitian mengenai pengaruh variasi jumlah carbopol® sebagai gelling agent terhadap sifat fisik dan stabilitas fisik sediaan sabun cuci tangan ekstrak etanol daun beluntas (Pluchea indica (L.) Less) dan uji aktivitas antibakteri dilakukan untuk mengetahui perbedaan sifat fisik dan stabilitas fisik pada variasi jumlah Carbopol® dalam sediaan sabun cuci tangan antibakteri ekstrak etanol daun beluntas.
Pada penelitian ini, akan ditentukan konsentrasi ekstrak etanol daun beluntas yang dapat digunakan sebagai agen antibakteri terhadap isolat bakteri pada tangan dengan menggunakan metode difusi sumuran. Pada formulasi sediaan terdapat empat formula yang menggunakan Carbopol® pada konsentrasi 1%,1,5%,2%,2,5% sebagai gelling agent. Respon yang diukur dalam penelitian ini adalah viskositas, pergeseran viskositas, dan ketahanan busa. Data yang diperoleh selanjutnya dianalisis menggunakan software R 3.1.0 dengan taraf kepercayaan 95% untuk melihat signifikasi (p<0,05) dari setiap respon.
Hasil penelitian menunjukkan bahwa ekstrak dengan konsentrasi 6% dapat memberikan daya hambat terhadap isolat bakteri tangan. Variasi konsentrasi
Carbopol® mempengaruhi kenaikan viskositas sediaan gel sabun cuci tangan ekstrak etanol daun beluntas. Sedangkan pada respon pergeseran viskositas dan ketahanan busa, variasi konsentrasi Carbopol® tidak mempengaruhi respon keduanya.
xviii ABSTRACT
Research about the effect of Variation amount of carbopol® as gelling agent toward physical properties and stability of hand soap with beluntas leaf (Pluchea indica ( L.) Less) ethanolic extract and antibacterial activity response conducted to determine the difference of physical properties and stability of the hand soap dosage form with variation amount of carbopol®as gelling agent.
In this study, will be decided the concentration of ethanolic extract of
beluntasleaf that will be used for antibacterial agent toward hand bacterial isolate with punch hole diffusion method. In formulation, will be used four formula that use carbopol® in 1%,1.5%,2%, and 2.5% concentration as gelling agent. Responses were measured in this study , such as viscosity, shifting of viscosity and foam stability. The data obtained next would be analyze using R.3.1.0 software with 95% confidence interval to see the significance (p<0,05) for each responses.
The result showed that ethanolic extract with 6% concentration could give inhibition toward hand bacterial isolate. Variation amount of carbopol® affect viscosity increases of hand soap dosage form. While in shifting viscosity and foam stability, variation amount of carbopol®didn’t affect both responses.
1
BAB I
PENDAHULUAN
A. Latar Belakang
Ada banyak bakteri penyebab penyakit yang hidup di lingkungan sekitar
kita. Untuk menghindari adanya kemungkinan terjangkit penyakit oleh karena
bakteri-bakteri tersebut, kita memproteksi diri dengan produk-produk antibakteri.
Produk antibakteripun beragam bentuknya, mulai dari sabun, hand sanitaizer,
pasta gigi dan lain-lain. Produk antibakteri ini akan mencegah adanya kontaminasi
bakteri yang dapat menyebabkan penyakit infeksi. Penyakit infeksi ini merupakan
masalah yang sering dihadapi dalam dunia kesehatan karena hampir tiap orang
pasti pernah mengalami penyakit infeksi (Darmadi, 2008).
Tangan dapat menjadi penyebab berbagai penyakit. Data Organisasi
Kesehatan Dunia (WHO) menunjukkan bahwa tangan mengandung bakteri
sebanyak 39.000-460.000 CFU per sentimeter kubik (Rochimawati, 2013). Hal ini
berpotensi tinggi dalam menyebabkan penyakit infeksi yang menular. Langkah
yang mudah dan cepat untuk mencegah penyebaran bakteri-bakteri pada tangan
adalah mencuci tanggan menggunakan sabun secara teratur.
Pemakaian zat-zat kimia tertentu sebagai agen antibakteri untuk mencegah
penularan bakteri dapat memunculkan berbagai masalah setelah puluhan tahun
pemakaian, yaitu dapat menimbulkan resistensi terhadap antimikroba (Green,
2005). Karena alasan inilah, orang-orang mulai sadar akan kelemahan dari zat-zat
mempunyai manfaat yang sama serta didukung dengan penelitian-penelitian
terdahulu yang mendukung penggunaan herbal untuk pengobatan penyakit.
Tanaman beluntas (Pluchea indica(L.) Less) sejak lama telah dikenal oleh masyarakat Indonesia sebagai tanaman pagar di halaman rumah penduduk. Secara
tradisional beluntas dapat digunakan sebagai obat untuk menghilangkan bau
badan, obat turun panas, obat batuk dan obat diare. Selain itu, beluntas juga
mempunyai aktivitas sebagai antibakteri (Purnomo, 2001). Aktivitas antibakteri
dari beluntas ini diperoleh dari beberapa kandungan kimia yang terdapat pada
daun beluntas seperti alkaloid, minyak atsiri, dan flavonoid (Hariana, 2006).
Adanya informasi secara tradisional dari masyarakat yang telah lama
menggunakan daun beluntas, mendorong para peneliti untuk mengadakan
penelitian tentang aktivitas antibakteri dari beluntas. Pada penelitian kali ini akan
dilakukan penelitian tentang aktivitas ekstrak etanol daun beluntas sebagai
komponen antibakteri terhadap isolat bakteri pada tangan.
Masyarakat lebih umum mencuci tangan dengan air saja, tetapi sebenarnya
hal ini tidak efektif untuk menjaga kesehatan. Mencuci tangan dengan sabun
terbukti lebih efektif dibandingkan mencuci tangan hanya dengan air (Awalia,
2013). Seringkali orang malas mencuci tangan dengan sabun karena
membutuhkan waktu lebih lama saat mencuci tangan, namun penggunaan sabun
menjadi efektif karena lemak dan kotoran yang menempel akan terlepas saat
Pada penelitian ini akan dibuat sabun cuci tangan (hand soap) dari ekstrak etanol daun beluntas (Pluchea indica (L.) Less) yang memiliki aktivitas antibakteri terhadap bakteri penyebab infeksi yang terdapat di tangan. Sabun cuci
tangan yang dibuat dalam penelitian ini berbentuk gel karena sediaan gel dapat
memberikan sensasi dingin ketika pemakaian sehingga dapat lebih diterima oleh
masyarakat. Diharapkan sabun cuci tangan dari ekstrak etanol beluntas ini dapat
meningkatkanacceptabilitydari konsumen bila dibandingkan dengan penggunaan ekstrak etanol beluntas secara langsung.
Gel merupakan bentuk sediaan setengah padat yang tersusun dari suspensi
partikel organik ukuran kecil atau molekul organik yang berukuran besar yang
tersusun dengan baik serta meresap dalam suatu cairan (Ansel, 2005). Salah satu
hal yang perlu diperhatikan dalam pembuatan gel sabun cuci tangan dengan
ekstrak etanol daun beluntas adalah peran dari gelling agent karena bahan inilah yang dapat mempengaruhi sifat fisik dan stabilitas dari sediaan gel. Gelling agent
dapat membentuk struktur tiga dimensi yang merupakan faktor penting dalam
sistem gel. Peningkatan jumlahGelling agentdapat memperkuat jaringan struktur gel sehingga terjadi kenaikan viskositas (Zatz dan Kushla, 1996). Gelling agent
yang digunakan pada penelitian ini adalah Carbopol®. Carbopol® merupakan salah satu jenis gelling agent yang digunakan di dalam cairan atau sediaan formulasi semisolid sebagai agent penambah kekentalan. Carbopol® merupakan senyawa tidak toksik, tidak iritan serta tidak menimbulkan hipersensitivitas pada
Variasi jumlah Carbopol® dalam formula sabun cuci tangan perlu diperhatikan karena akan berpengaruh pada parameter sediaan gel sabun cuci
tangan yaitu viskositas yang nantinya berpengaruh juga dalam nilai kemanfaatan
dan penerimaan sediaan oleh pasien. Pada penelitian ini akan dilakukan penelitian
awal mengenai pengaruh variasi jumlahCarbopol®sebagaigelling agentterhadap sifat fisik dan stabilitas fisik sabun cuci tangan ekstrak etanol daun beluntas.
1. Rumusan masalah
a. Apakah ekstrak etanol daun beluntas (Pluchea indica (L.) Less) memiliki daya antibakteri terhadap isolat bakteri pada tangan?
b. Apakah ada pengaruh dari variasi jumlah Carbopol® dalam sediaan gel sabun cuci tangan ekstrak etanol daun beluntas (Pluchea indica (L.) Less) terhadap sifat fisik dan stabilitas fisik?
2. Keaslian penelitian
Sejauh penelusuran yang dilakukan oleh penulis, penelitian mengenai
“Pengaruh Carbopol® sebagai Gelling Agent terhadap Sifat Fisik dan Stabilitas Fisik Sediaan Sabun Cuci Tangan Ekstrak Etanol Daun Beluntas
(Pluchea indica (L.) Less) dan Uji Aktivitas Antibakteri” belum pernah
dilakukan. Adapun penelitian yang pernah dilakukan sebelumnya, seperti :
b. Perbedaan Sifat Fisik dan Stabilitas Fisik Deodoran Ekstrak Etanol Daun Beluntas (Pluchea indica (L.) Less) dengan Variasi Jumlah Sorbitan MonooleatesebagaiEmulsifying Agent(Hardita, 2012).
3. Manfaat penelitian
a. Manfaat teoritis. Menambah pengetahuan tentang sediaan gel sabun cuci tangan ekstrak etanol daun beluntas (Pluchea indica (L.) Less) menggunakan variasi jumlahCarbopol®sebagaigelling Agent.
b. Manfaat Praktis. Memperoleh informasi tentang perbedaan sifat fisik dan stabilitas fisik sediaan gel sabun cuci tangan ekstrak etanol daun beluntas
(Pluchea indica (L.) Less) dengan menggunakan variasi jumlah
Carbopol®sebagaigelling agent.
B. Tujuan Penelitian
1. Tujuan umum
Mengetahui perbedaan sifat fisik dan stabilitas fisik sediaan gel sabun cuci
tangan ekstrak etanol daun beluntas (Pluchea indica(L.) Less) yang bersifat antibakteri dengan variasi jumlahCarbopol®sebagaigelling agent.
2. Tujuan khusus
a. Mengetahui adanya daya antibakteri ekstrak etanol daun beluntas
b. Mengetahui perbedaan sifat fisik dan stabilitas fisik pada variasi jumlah
7
BAB II
PENELAAHAN PUSTAKA
A. Mencuci Tangan
Berdasarkan studi Basic Human Services (BHS) di Indonesia tahun 2006, perilaku masyarakat dalam mencuci tangan adalah sebagai berikut
1) setelah buang air besar (12%),
2) setelah membersihkan tinja bayi dan balita (9%),
3) sebelum makan (14%),
4) sebelum memberi makan bayi (7%), dan
5) sebelum menyiapkan makanan (6 %)
(Depkes RI, 2008).
Bakteri banyak ditemukan disekitar manusia, contohnya pada tangan
manusia yang banyak berinteraksi dengan dunia luar. Terdapat berbagai jenis
bakteri yang ada ditangan manusia. Adapun bakteri yang umum ditemukan pada
tangan diantaranya adalah Staphylococcus aureus, Escherichia coli, Salmonella, Vibrio cholerae,danShigella(BSN Medical, 2009).
Cuci tangan pakai sabun adalah perilaku cuci tangan dengan menggunakan
sabun dan air bersih yang mengalir. Sabun adalah bahan yang digunakan untuk
mencuci dan mengemulsi, terdiri dari dua komponen utama yaitu asam lemak
dengan rantai karbon C16 dan sodium atau potassium (Qisti, 2009). Pada sabun
terdapat rantai karbon hidrofobik dan hidrofilik. Rantai karbon hidrofobik
yang sangat halus. Ketika dibilas dengan air, sabun melunturkan molekul tersebut
bersama kuman. Dengan mekanisme inilah sabun mampu memutus rantai
penyebaran kuman penyebab penyakit menular (Depkes RI, 2008).
B. Uji Potensi Senyawa Antibakteri
Penentuan aktivitas antibakteri secara dapat dikelompokkan dalam dua
metode, yaitu :
1. Metode dilusi
Metode dilusi digunakan untuk mengukur Kadar Hambat Minimum
(KHM) dan Kadar Bunuh Minimum (KBM) yaitu kadar minimal yang
diperlukan untuk menghambat pertumbuhan bakteri dan kadar minimal yang
diperlukan untuk membunuh bakteri (Agboret al., 2011).
Kemampuan antibakteri dikatakan kuat apabila memiliki nilai KHM antara
0,05-0,50 mg/mL, sedang apabila nilai KHM antara 0,6-1,5 mg/mL, dan
lemah apabila di atas 1,5 mg/mL (Diazet al, 2010).
Aktivitas antibakteri ditentukan oleh spektrum kerja, cara kerja, dan
ditentukan pula oleh konsentrasi hambat minimum (KHM). Konsentrasi
Hambat Minimum (KHM) adalah konsentrasi minimum dari suatu zat yang
mempunyai efek daya hambat pertumbuhan mikroorganisme. Penetapan KHM
dapat dilakukan dengan dua cara (Entjang, 2003), yaitu :
a. Cara cair. Pada cara ini digunakan media cair yang telah ditambahkan zat
yang dapat menghambat pertumbuhan bakteri atau jamur dengan
dalam jumlah yang sama. Respon zat uji ditandai dengan kejernihan atau
kekeruhan pada tabung setelah diinkubasi (Entjang, 2003).
b. Cara padat. Pada cara ini digunakan media padat yang telah dicampur
dengan larutan zat uji dengan berbagai konsentrasi. Dengan cara ini satu
cawan petri dapat digores lebih dari satu jenis mikroba untuk memperoleh
nilai KHM (Entjang, 2003).
2. Metode difusi
Pada cara difusi agar digunakan media agar padat danreservoiryang dapat berupa cakram kertas, silinder atau cekungan yang dibuat pada media padat.
Larutan uji akan berdifusi dari pecadang ke permukaan media agar padat yang
telah diinokulasi bakteri. Bakteri akan terhambat pertumbuhannya dengan
pengamatan berupa lingkungan atau zona di sekeliling pencadang (Entjang,
2003).
Berikut yang termasuk dalam metode difusi :
a. Metode cakram kertas (disc diffusion). Metode ini dilakukan dengan menggunakan disk yang terbuat dari kertas diresapi dengan sejumlah tertentu agen antibakteri yang telah diketahui konsentrasinya. Senyawa
antibakteri tersebut akan berdifusi ke dalam medium sekitarnya dan
membentuk gradien konsentrasi sekitar disk. Penghambatan bakteri tampak sebagai zona melingkar pada cawan agar (Agboret al., 2011). b. Metodeditch. Metode ini dilakukan dengan cara menghilangkan potongan
agar dari cawan dan mengisi lubang yang terbentuk dengan agar yang
c. Metode sumuran (punch hole diffusion). Metode ini dilakukan dengan pembuatan lubang sumuran pada cawan agar yang sebelumnya telah
diinolkulasikan bakteri uji. Masing-masing lubang diisi dengan senyawa
antibakteri yang telah diketahui konsentrasinya secara tepat (Agbor et al., 2011).
C. Beluntas 1. Deskripsi tanaman
Beluntas (Pluchea indica (L.) Less) merupakan tanaman herba famili Asteraceae yang telah dimanfaatkan sebagai pangan dan sediaan obat bahan
alam tumbuh liar di daerah kering di tanah yang keras dan berbatu atau
ditanam sebagai tanaman pagar. Memerlukan cukup cahaya matahari atau
sedikit naungan. Banyak ditemukan di daerah pantai dekat laut sampai
ketinggian 1.000 m dpl. Perdu kecil, tumbuh tegak sampai 2 m atau lebih.
Bercabang banyak, berusuk halus, berambut lembut. Daun bertangkai
pendek, letak berseling, helaian daun bulat telur sungsang. Ujung bulat
melancip, tepi bergigi, berkelenjar, panjang 2,5 sampai 9 cm. Lebar 1-5,5 cm.
dengan warna hijau terang bila diremas mengeluarkan bau harum. Bunga
majemuk dengan bentuk malai rata, keluar dari ketiak daun dan ujung
tangkai. Bunga berbentuk bonggol, bergagang ataupun duduk, berwarna putih
kekuningan sampai ungu. Buah berbentuk gasing, kecil, keras berwarna
coklat dengan sudut -sudut berwarna putih. Biji kecil, coklat keputih-putihan.
Cabang bunga sangat banyak sehingga membentuk rempuyung cukup
besar antara 2,5-12,5 cm. Bunga berbentuk bonggol, bergagang atau duduk.
Bentuknya seperti silinder sempit dengan panjang 5-6 mm. Panjang daun
pembalut sampai 4 mm. Daun pelindung bunga tersusun dari 6 -7 helai. Daun
pelindung yang terletak di dalam berbentuk sudut (lanset) dan di luar
berbentuk bulat telur. Daun pelindung berbulu lembut, berwarna ungu dan
pangkalnya ungu muda. Kepala sari menjulur dan berwarna ungu. Tangkai
putik pada bunga betina lebih panjang. Buah beluntas longkah berbentuk
seperti gasing, warnanya coklat dengan sudut-sudut putih dan lokos 10
(gundul atau licin) panjang bauh 1 mm (Sumitro, 2002).
2. Taksonomi
Menurut Purnomo (2001) tanaman beluntas dikelompokkan menjadi
seperti di bawah ini:
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Asterales
Famili : Asteraceae
Genus : Pluchea
3. Nama daerah
Sumatera: Beluntas, Jawa: Baluntas (Madura), baruntas, huntas (Jawa
Tengah), Nusatenggara: Lenaboui, Sulawesi: Lamutasa (Syamsuhidayat dan
Hutapea, 1991).
4. Kegunaan
Beluntas digunakan sebagai tanaman pagar dan pembatas di perkebunan.
Masyarakat Indonesia memanfaatkan daun beluntas untuk menghilangkan
bau badan dengan cara direndam kemudian dioleskan (Winarno dan Sundari,
1998).
Secara tradisional daunnya digunakan sebagai obat untuk menghilangkan
bau badan, obat penurun panas, obat batuk dan obat anti diare. Daun beluntas
yang telah direbus sering pula digunakan untuk mengobati penyakit kulit.
Selain itu, daun beluntas juga sering dikonsumsi sebagai lalapan (Winarno
dan Sundari, 1998).
Flavonoid daun beluntas memiliki aktifitas antibakteri terhadap
Staphylococcus sp, Propinobacterium sp, dan Corneybacterium (Purnomo, 2001). Ekstrak etanol daun beluntas telah diteliti secara ilmiah memiliki
aktivitas antimikroba terhadap Staphylococcus aureus, Pseudomonas fluorecens, Escherichia coli dan Salmonela typhii. Skrining fitokimia menunjukkan hasil ekstrak etanol mengandung flavonoid, fenol hidrokuinon,
D. Ekstrak
Ekstraksi merupakan proses pemisahan bahan dari campurannya dengan
menggunakan pelarut. Jadi, ekstrak adalah sediaan yang diperoleh dengan cara
ekstraksi tanaman obat dengan ukuran partikel tertentu dan menggunakan medium
pengekstraksi (menstruum) yang tertentu pula (Goeswin, 2009).
Ekstraksi dapat dilakukan dengan berbagai cara. Ekstrak yang diperoleh
sesudah pemisahan cairan dari residu tanaman obat dinamakan micella. Micella
ini dapat diubah menjadi bentuk obat siap pakai, seperti ekstrak cair dan tingtura
atau sebagai produk/bahan antara yang selanjutnya dapat diproses menjadi ekstrak
kering (Goeswin, 2009).
Masalah utama dalam pengembangan sediaan cair yang mengandung ekstrak
adalah masalah kelarutan. Ekstrak harus diencerkan dalam larutan atau dilarutkan
kembali jika berbentuk kering di dalam sistem pelarut. Masalah ini terjadi
beberapa waktu setelah terbentuknya endapan atau terjadi kekeruhan yang
disebabkan pelarutan yang tidak sempurna dari bahan aktif atau komponen
sekunder (Goeswin, 2009).
E. Maserasi
Proses maserasi merupakan proses yang sederhana untuk mendapatkan ekstrak
dan diuraikan dalam kebanyakan farmakope. Cara ini sesuai, baik untuk skala
kecil maupun skala industri. Proses yang paling sederhana hanyalah dengan cara
merendam simplisia di dalam pelarut. Sesudah mengatur waktu sehingga sesuai
ekstraksi dicuci dengan pelarut yang segar sampai didapat berat yang sesuai.
Prosedur ini sama dengan pembuatan tinktur atau ekstrak khusus, dan
kadang-kadang merupakan satu-satunya prosedur untuk tanaman yang mengandung zat
berlendir (muscilago) yang tinggi (Goeswin, 2009).
Peralatan untuk maserasi secara statis berukuran besar. Sistem berupa sistem
kontinyu tertutup. Simplisia akan berkontak dengan pelarut selama waktu tertentu.
Sesudah itu, ekstrak diperoleh dengan cara penyaringan atau dekantasi (Goeswin,
2009).
F. Sabun Cuci Tangan
Sabun berfungsi untuk mengemulsi kotoran–kotoran berupa minyak ataupun zat pengotor lainnya. Sabun dibuat melalui proses saponifikasi lemak
minyak dengan larutan alkali membebaskan gliserol. Lemak minyak yang
digunakan dapat berupa lemak hewani, minyak nabati, lilin, ataupun minyak ikan
laut (Jongko, 2009).
Zat pembersih berbentuk sabun ini baik yang padat maupun cair akan
membantu proses pelepasan kotoran dan kuman yang menempel di permukaan
luar kulit tangan dan kuku. Dengan mencuci tangan yang benar menggunakan
sabun maka kotoran dan kuman akan terangkat sebagian, sehingga hal ini
membantu mengurangi penularan bakteri (Depkes RI, 2008).
G. Gel
Gel merupakan sistem semipadat terdiri dari suspensi yang dibuat dari
partikel anorganik yang kecil atau molekul organik yang besar, terpenetrasi oleh
Zat-zat pembentuk gel digunakan sebagai pengikat dalam granulasi, koloid
pelindung dalam suspensi, pengental untuk sediaan oral dan sebagai basis
supositoria. Secara luas sediaan gel banyak digunakan pada produk obat-obatan,
kosmetik dan makanan juga pada beberapa proses industri. Pada kosmetik yaitu
sebagai sediaan untuk perawatan kulit, sampo, sediaan pewangi dan pasta gigi
(Herdiana, 2007).
Gel dapat diklasifikasikan menjadi hidrogel dan organogel. Hidrogel meliputi
komponen koloid yang larut air dan juga organik hidrogel seperti gum alam dan
sintetis dan juga hidrogel anorganik. Organogel meliputi hidrokarbon, lemak
hewan atau nabati, dan organogel hidrofilik (Allen, 1999).
H. Surfaktan Anionik
Surfaktan atau zat aktif permukaan adalah molekul dan ion yang diabsorbsi
pada antar muka. Molekul surfaktan ini disebut amfifatik karena memiliki bagian
polar (hidrofilik) dan non polar (hidrofobik) sehingga bersifat amfifilik. Sifat ini
menyebabkan surfaktan dapat diabsorbsi pada antar muka sehingga menurunkan
tegangan antar muka atau tegangan permukaan (Swarbrick, 2007).
Surfaktan anionik merupakan garam natrium yang akan terionisasi
menghasilkan Na+ dan ion surfaktannya bermuatan negatif. Surfaktan anionik
dapat membentuk ion negatif atau anion dalam mekanisme penurunan tegangan
I. Gelling Agent
Gelling agentmerupakan basis dari sediaan gel dan harus bersifat inert, aman dan tidak reaktif terhadap komponen lain dalam suatu formulasi gel. Gel dan
polisakarida alam mudah mengalami degradasi oleh mikroba sehingga
ditambahkan pengawet dalam formula gel untuk mencegah degradasi gel oleh
mikroba. Peningkatan konsentrasi gelling agent dapat memperkuat struktur gel sehingga viskositas meningkat (Zatz dan Kushla, 1996).
J. Carbopol®
Sinonim: Carbomer; acrylic acid polymer; polyacrylic acid; carboxyvinyl polymer; karboksipolietilen (Roweet al., 2009).
Karbomer adalah polimer sintetik dari asam akrilat yang mempunyai
ikatan silang dengan ether allyl sucrose atau sebuah allyl ethers dari
pentaerythritol. Karbomer mengandung asam karboksilat antara 56%- 68% pada keadaan kering. BM teoritis diperkirakan sekitar 7 x 105 hingga 4 x 109(Rowe et al., 2009).
Serbuk putih, sedikit berbau khas, asam, higroskopik. Larut dalam air dan
setelah netralisasi larut dalam etanol (95%) dan gliserin. Tingkat viskositas yang
lebih tinggi pada pH 6-11 dan viskositas akan menurun pada pH di bawah 3 atau
di atas 12 (Roweet al., 2009).
mengakibatkan naiknya viskositas. Carbopol® dengan kadar 1% dengan penambahan TEA akan membentuk struktur seperti sarang lebah. Jejaring struktur
sarang lebah ini lebih kuat dibandingkan struktur jejaring berserat-serat tidak
teratur. Semakin banyak Carbopol® yang digunakan maka struktur sarang lebah
ini akan membentuk “dinding” yang makin kuat pula (Kimet al.,2003).
K. Formulasi 1. Propilen glikol
Sinonim: 1,2 Dihydroxypropane; E1250; 2-hydroxypropanol; Methyl ethylene glycol; methyl glycol; propane-1,2-diol. Rumus molekul: C3H8O2
Pemerian: cairan kental, jernih, tidak berwarna, tidak berbau, rasa sedikit manis,
higroskopik. Bobot molekul: 76,09. Titik didih: 188°C. Titik leleh: 59°C (Roweet al., 2009).
Larut dalam aseton, kloroform, etanol 95%, gliserin, dan air. Larut dalam
1: 6 bagian eter. Tidak bercampur dengan minyak mineral dan minyak murni.
Tidak larut dalam beberapa minyak esensial (Roweet al., 2009).
2. Gliserin
Sinonim: croderol; E422; glycerine; glycon G-100; kemstrene; optim; pricerine; 1,2,3-propanetriol; trihydroxypropane glycerol. Rumus molekul: C3H8O3. Pemerian: cairan jernih seperti sirup; tidak berwarna, rasa manis, berbau
khas lemah (tajam atau tidak enak); higroskopik, netral terhadap lakmus.
3. Triethanolamin
Sinonim: daltogen, tealan, triethanolamin, trihydroxytriethylamine; tris (hydroxyethyl) amin. Rumus molekul: C6H15NO3. Berat molekul: 149,19. Fungsi:
bahan pembasah, bahan pengemulsi, penstabil pH, pelarut, polymer plastisizer
dan humektan. Titik didih: 335°C. Titik leleh: 20°C-21°C. Viskositas: 590 mPas
(590Cp) pada 30°C. Stabilitas: perubahan warna dapat terjadi dengan adanya
paparan cahaya dan kontak dengan logam dan ion logam. TEA 85% cenderung
terpisah pada suhu 15oC, homogenitas dapat diperbaiki dengan pemanasan dan
pencampuran sebelum digunakan (Roweet al, 2009).
L. Uji Sifat Fisik dan Stabilitas Gel 1. Sifat fisik
a. Pengamatan organoleptis. Pengamatan dilihat secara langsung bentuk,
warna, dan bau dari gel yang dibuat. Gel biasanya jernih dengan
konsistensi setengah padat (Ansel, 1989).
b. Viskositas. Viskositas adalah suatu pertahanan dari suatu cairan untuk
mengalir, semakin tinggi viskositas maka semakin besar bertahannya
(Sinko, 2006)
Viskositas suatu zat cairan murni atau larutan merupakan indeks hambatan
aliran cairan. Viskositas dapat diukur dengan mengukur laju aliran cairan,
yang melalui tabung berbentuk silinder. Cara ini merupakan salah satu
cara yang paling mudah dan dapat digunakan baik untuk cairan maupun
Makin kental suatu cairan, makin besar gaya yang dibutuhkan untuk
membuatnya mengalir pada kecepatan tertentu. Viskositas dispers koloid
dipengaruhi oleh bentuk partikel dari fase dispers dengan viskositas
rendah, sedang disperse system yang mengandung koloid-koloid linier viskositasnya lebih tinggi (Joshita, 2002).
c. Ketahanan busa. Busa merupakan suatu sistem dispersi yang terdiri atas
gelembung gas yang dibungkus oleh lapisan cairan. Karena adanya
perbedaan densitas yang signifikan antara gelembung dan medium cairan,
makasistem akan memisah menjadi dua lapisan dimana gelembung akan
naik ke atas (Tadros, 2005).
Mekanisme pembentukan busa dimulai ketika gelembung gas masuk ke
dalam larutan surfaktan. Surfaktan akan terabsorpsi pada antarmuka cairan
dan terbentuk gelembung gas yang terbungkus oleh lapisan film atau
disebut busa (Exerowa,1998).
Stabilitas busa merupakan kemampuan busa untuk mempertahankan
parameter utamanya dalam keadaan konstan selama waktu tertentu.
Parameter tersebut meliputi ukuran gelembung, kandungan cairan, dan
total volume busa. Foam lifetime (waktu hidup busa) merupakan ukuran paling sederhana untuk menunjukkan stabilitas busa (Exerowa, 1998).
Penyebab utama dari pecahnya busa adalah penipisan (thinning) lapisan film dan koalesen. Penipisan terjadi karena busa cenderung naik ke atas
namun sekaligus ditarik ke bawah karena adanya aliran cairan akibat gaya
gradient tekanan gas, dimana busa-busa kecil akan bergabung menjadi
lebih besar (koalesen) sehingga semakin mudah pecah (Tadros 2005).
d. Pengukuran pH. pH adalah skala logaritmik untuk menyatakan keasaman
atau kebasaan. pH dapat didefinisikan sebagai –log10C, dengan C adalah
konsentrasi ion hidrogen dalam mol per dm3. pH di bawah 7 menyatakan
bahwa suatu larutan bersifat asam dan pH di atas 7 menyatakan larutan
basa (Daintith, 1994).
Penentuan pH sediaan dilakukan dengan menggunakan stik pH universal
yang dicelupkan ke dalam sampel gel yang telah diencerkan. Setelah
tercelup dengan sempurna, pH universal tersebut dilihat perubahan
warnanya dan dicocokkan dengan standar pH universal. pH sediaan gel
harus sesuai dengan pH kulit yaitu 4,5–6,5 (Tranggono, 2007).
M. Landasan Teori
Banyak bakteri ditemukan di sekitar manusia. Tangan manusia merupakan
anggota tubuh yang paling sering berhubungan langsung dengan lingkungan
sehingga tangan sering menjadi penyebab penularan penyakit infeksi oleh bakteri.
Cuci tangan dengan sabun secara teratur sangat diperlukan untuk mencegah
penularan bakteri penyebab infeksi. Hal inilah yang mendorong Departemen
Kesehatan mengadakan program budaya mencuci tangan untuk masyarakat. Hal
ini juga yang melandasi peneliti untuk memformulasikan sebuah sediaan sabun
Salah satu tanaman asli Indonesia yang tersebar dengan luas di beberapa
daerah di Indonesia serta berpotensi untuk dikembangkan yaitu tanaman beluntas.
Selama ini khasiat antibakteri beluntas hanya dipercaya secara empiris untuk
mengobati infeksi yang disebabkan oleh bakteri. Daun beluntas merupakan
tanaman asli Indonesia yang memiliki berbagai kandungan metabolit sekunder
antara lain alkaloid, flavonoid, tannin, minyak atsiri, dan asam klorogenik.
Sebagian besar senyawa yang terkandung di dalam ekstrak etanol daun beluntas
merupakan senyawa fenolik (Radjani, 2013 ). Menurut peneliti sebelumnya, yaitu
Sumitro (2002) dan Hariana (2006), berkhasiatnya daun beluntas sebagai
antibakteri diperoleh dari beberapa kandungan kimia seperti alkaloid, minyak
atsiri, dan flavonoid. Hal inilah yang mendorong peneliti untuk meneliti lebih
lanjut daya antibakteri daun beluntas terutama terhadap isolat bakteri tangan.
Sabun cuci tangan yang akan dibuat berbentuk gel. Gel merupakan sediaan
semisolid terdiri dari suspensi yang dibuat dari partikel anorganik yang kecil atau
molekul organik yang besar, terpenetrasi oleh suatu cairan (Dirjen POM, 1995).
Pada formulasi sediaan gel terdapat komponen utama yaitu gelling agent yang
berperan dalam meningkatkan viskositas sediaan. Pada penelitian ini digunakan
N. Hipotesis
1. Ekstrak etanol daun beluntas (Pluchea indica (L.) Less) memiliki daya antibakteri terhadap isolat bakteri pada tangan
2. Terdapat perbedaan dari variasi jumlah Carbopol® terhadap sifat fisik dan stabilitas fisik dalam sediaan gel sabun cuci tangan ekstrak etanol daun
23
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan rancangan eksperimental murni dengan pola searah,
untuk membandingkan sifat fisik dan stabilitas fisik yang meliputi organoleptis,
viskositas, ketahanan busa, dan pH dari formula sediaan sabun cuci tangan ekstrak
etanol daun beluntas dengan variasi jumlahCarbopol®sebagaigelling agent.
B. Variabel Penelitian
Variabel dalam penelitian ini yaitu:
1. Variabel bebas adalah variasi jumlahCarbopol®dengan konsentrasi sebesar 1%, 1,5%, 2% dan 2,5% dari keseluruhan formula.
2. Variabel tergantung adalah sifat fisik dan stabilitas fisik sediaan sabun cuci tangan ekstrak etanol daun beluntas yang meliputi organoleptis, viskositas,
ketahanan busa, pergeseran viskositas dan pH.
3. Variabel pengacau terkendali adalah alat percobaan, wadah penyimpanan, lama penyimpanan sabun cuci tangan, lama dan kecepatan pencampuran.
C. Definisi Operasional
1. Sabun cuci tangan adalah campuran dari molekul surfaktan dan ekstrak etanol
daun beluntas yang memiliki kemampuan untuk membersihkan dan berfungsi
menekan bertumbuhan kuman pada tangan.
2. Serbuk daun beluntas (Pluchea indica (L.) Less) merupakan serbuk daun beluntas yang diperoleh dari hasil budidaya tanaman beluntas yang ada di CV.
MERAPI FARMA.
3. Ekstrak etanol daun beluntas adalah ekstrak hasil maserasi simplisia daun
beluntas menggunakan pelarut etanol 70%. Penetapan kadar total fenolik
dilakukan oleh Lembaga Penelitian dan Pengujian Terpadu Universitas Gajah
Mada.
4. Gel merupakan sediaan semi solid yang terdapat interaksi antar partikel koloid
dengan suatu pembawa berupa cairan.
5. Carbopol® atau Carbopol 940® merupakan senyawa yang pada rentang konsentrasi 0,5-2% dapat berfungsi sebagaigelling agent.
6. Sabun cuci tangan antibakteri merupakan sabun yang memiliki kemampuan
untuk menghambat pertumbuhan mikroba pada tangan.
7. Isolat bakteri tangan merupakan hasil isolasi mikroba dari tiga bagian tangan,
yaitu telapak tangan, jari tangan dan punggung tangan.
8. Uji potensi antibakteri merupakan uji yang dilakukan untuk mengetahui
9. Stabilitas fisik sediaan gel merupakan kemampuan gel sabun cuci tangan
ekstrak daun beluntas untuk bertahan dalam batas penyimpanan dan
penggunaan sabun selama 28 hari.
10. Organoleptis merupakan pengamatan yang dilakukan secara visual terhadap
warna, bentuk dan bau sediaan gel sabun cuci tangan ekstrak daun beluntas 48
jam setelah sediaan dibuat dan setelah penyimpana 28 hari.
11. Viskositas adalah suat pernyataan tahan dari suatu cairan untuk mengalir, yang
diukur 48 jam setelah sediaan dibuat dan setelah penyimpanan selama 28 hari.
12. Ketahanan busa adalah kemampuan busa untuk bertahan atau tidak hilang
setelah divortex dan didiamkan selama 20 menit. Hasil yang dicatat merupakan selisih dari tinggi busa pada menit ke 0 setelah divortex sampai menit ke 20 dalam satuan cm.
13. Penetapan pH merupakan uji yang dilakukan untuk mengetahui pH sediaan
gel sabun cuci tangan ekstrak etanol daun beluntas sesuai dengan pH kulit
(4,5-6,5), dilakukan 48 jam setelah sediaan dibuatdan setelah penyimpanan
selama 28 hari.
14. One way ANOVA merupakan statistika parametrik yang digunakan untuk
menguji hipotesis komparatif rata-rata sampel, bila pada setiap sampel terdiri
dari satu kategori.
D. Bahan dan Alat Penelitian 1. Bahan penelitian
Bahan yang digunakan dalam penelitian ini adalah aquadest steril, Texapon®
Brataco), propilen glikol (kualitas farmasetis dari PT Brataco), Carbopol®
(kualitas farmasetis dari PT. Medika Jaya), serbuk daun beluntas (CV.
MERAPI FARMA), ekstrak etanol daun beluntas (LPPT Universitas Gajah
Mada Yogyakarta), kultur isolat bakteri tangan dari 3 probandus di
Laboratorium Mikrobiologi Universitas Sanata Dharma Yogyakarta.
2. Alat penelitian
Alat penelitian yang digunakan dalam penelitian ini adalah alat-alat gelas, strips pH, jarum ose, spreader, autoklaf (Model KT-40), bunsen, mikropipet, timbangan analitik (Precise 2000C-2000D1), Viscometer Rion seri VT 04
(RION-JAPAN), mikroskop, oven (Memmert), dancentrifuge.
E. Tata Cara Penelitian 1. Pembuatan serbuk daun beluntas
a. Pengumpulan bahan daun beluntas. Bahan tumbuhan yang
digunakan adalah daun beluntas (Pluchea indica (L.) Less) yang merupakan hasil budidaya dari CV. Merapi Farma Herbal yang terletak di Jl. Kaliurang
Km. 21, Sleman, Daerah Istimewa Yogyakarta. Pengambilan sampel daun
beluntas dipilih berdasarkan warna daun dan pucuk daun yaitu berwarna hijau
muda tanpa bercak serta letak daun yang diambil pucuk 1-6 daun dari atas
tanaman beluntas. Bahan yang diperoleh berupa daun segar setidaknya
berumur 50 hari. Identifikasi daun beluntas dilakukan oleh CV. Merapi Farma
Herbal yang menyatakan bahwa daun yang digunakan adalah benar daun
b. Pembuatan serbuk daun beluntas. Penyerbukan sampel daun
beluntas dilakukan oleh CV. Merapi Farma Herbal. Daun beluntas yang telah
dipanen, dicuci dengan air mengalir untuk menghilangkan kotoran yang
menempel pada daun. Daun yang telah dicuci, diangin-anginkan sampai
benar-benar kering dan mudah dipatahkan. Kemudian dilakukan penyerbukan
dengan menggunakan mesin penyerbuk (grinder) dengan lubang pengayak berdiameter 1mm (setara dengan pengayak nomor 18). Serbuk yang diambil
adalah serbuk yang memiliki derajad kehalusan sebesar 18. Semakin kecil
ukuran partikel serbuk, maka luas permukaan untuk kontak dengan penyari
semakin besar.
2. Pembuatan ekstrak etanol daun beluntas
a. Ekstraksi serbuk daun beluntas. Ekstraksi serbuk daun beluntas
dilakukan dengan metode maserasi menggunakan pelarut etanol 70%
berdasarkan CoA (Ceritificate of Analysis) yang dilakukan Lembaga Penelitian dan Pengujian Terpadu Universitas Gajah Mada. Serbuk daun
beluntas ditambah etanol 70%. Diaduk selama 30 menit dan didiamkan selama
24 jam. Proses maserasi ini dilakukan sebanyak tiga kali. Kemudian filtrat
diuapkan dengan vacuum rotary evaporator dan dilanjutkan pemanasan dengan menggunakan waterbathpada suhu 70oC. Hasil ekstrak daun beluntas ditimbang dan dikemas.
b. Penetapan kadar total fenolat. Penetapan kadar total fenolik
dilakukan dengan metode spektrofotometri berdasarkan CoA yang dilakukan
3. Uji potensi antibakteri ekstrak etanol daun beluntas
a. Pembuatan stok isolat bakteri tangan. Isolasi bakteri dari tangan dilakukan kepada 3 probandus dari bagian tangan yang berbeda, yang seharian
telah melakukan kegiatan dan belum cuci tangan atau belum menggunakan
produk antiseptik untuk tangan. Isolasi dilakukan dengan menempelkan
punggung tangan pada pada cawan petri berisi media NA 15 mL secara
aseptis, menempelkan jari pada media NA 15 mL dalam cawan petri secara
aseptis dan menempelkan bagian telapak tangan pada media NA 15 mL dalam
cawan petri secara aseptis. Kemudian diinkubasi terbalik selama 24 jam pada
suhu 37oC. Isolat bakteri tangan dari 3 probandus yang telah tumbuh pada
media NA cawan petri diambil dengan menggunakan ose dan ditanam di
media NA miring. Kemudian diinkubasi pada suhu 37oC selama 24 jam. Hasil
isolasi akan digunakan untuk uji potensi antibakteri ekstrak etanol daun
beluntas.
b. Pembuatan suspensi bakteri uji. Tabung reaksi berisi media NB
disiapkan sebanyak 10mL. Kemudian kultur bakteri yang telah tumbuh pada
media NA miring diinokulasikan ke dalam media NB dengan jarum ose, dan
diinkubasikan pada suhu 37oC selama 24 jam. Setelah diinkubasi, media NB
di lihat kekeruhannya (setara dengan standarMac Farland 1,5.108 CFU/mL). Jika kekeruhannya belum setara dengan standar Mac Farland 1,5.108 CFU/mL ditambahkan NB steril sampai kekeruhannya setara dengan standar
c. Pembuatan konsentrasi ekstrak etanol daun beluntas.
1.) Konsentrasi ekstrak etanol daun beluntas 2%
Ditimbang 0,2 g ekstrak etanol daun beluntas, kemudian dilarutkan dengan
sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur 10 mL,
lalu di add dengan aquadest steril sampai tanda.
2.) Konsentrasi ekstrak etanol daun beluntas 4%
Ditimbang 0,4 g ekstrak etanol daun beluntas, kemudian dilarutkan dengan
sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur 10 mL,
lalu di add dengan aquadest steril sampai tanda.
3.) Konsentrasi ekstrak etanol daun beluntas 6%
Ditimbang 0,6 g ekstrak etanol daun beluntas, kemudian dilarutkan dengan
sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur 10 mL,
lalu di add dengan aquadest steril sampai tanda.
4.) Konsentrasi ekstrak etanol daun beluntas 8%
Ditimbang 0,8 g ekstrak etanol daun beluntas, kemudian dilarutkan dengan
sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur 10 mL,
lalu di add dengan aquadest steril sampai tanda.
5.) Konsentrasi ekstrak etanol daun beluntas 10%
Ditimbang 0,2 g ekstrak etanol daun beluntas, kemudian dilarutkan dengan
sedikit aquadest steril. Ekstrak dimasukkan ke dalam labu ukur 10 mL,
6.) Konsentrasi ekstrak etanol daun beluntas 100%.
Konsentrasi ekstrak etanol daun beluntas 100% digunakan sebagai kontrol
positif. Ditimbang 10 g ekstrak etanol daun beluntas, kemudian dilarutkan
dengan sedikitaquadeststeril. Ekstrak dimasukkan ke dalam labu ukur 10 mL, lalu diadddenganaquadeststeril sampai tanda.
d. Uji aktivitas antibakteri ekstrak etanol daun beluntas. Potensi
antibakteri ekstrak etanol daun beluntas diuji terhadap isolat bakteri tangan
dengan metode difusi sumuran. Seri konsentrasi ekstrak etanol daun beluntas
adalah 2%, 4%, 6%, 8%, dan 10% dengan konsentrasi 100% sebagai kontrol
positif. Media NA yang digunakan dibagi menjadi 2 bagian yaitu base layer
(10 mL) dan seed layer (15 mL). Bagian base layer dituang ke cawan petri steril dan dibiarkan memadat terlebih dahulu. Untuk seed layer, diambil 1 mL dari stok suspensi bakteri uji yang sudah disetarakan kemudian diinokulasikan
ke media NA secara pour plate. Media NA yang mengandung bakteri dibiarkan sampai memadat. Dibuat sumuran pada petri dengan pelubang gabus
no. 4. Kemudian dengan menggunakan mikropipet, diinokulasikan 50μ L ekstrak etanol daun beluntas dengan berbagai seri konsentrasi. Kemudian
diinkubasi selama 24 jam pada suhu kamar.
e. Penentuan konsentrasi ekstrak yang akan diformulasikan ke dalam
sediaan gel sabun cuci tangan antibakteri.Diamati zona keruh dan jernih pada
bakteri. Konsentrasi ekstrak etanol daun beluntas ditentukan dengan melihat
aktivitas antibakteri yang paling baik dengan mengamati zona hambat yang
4. Pembuatan sediaan gel sabun cuci tangan antibakteri
a. Modifikasi formula gel sabun cuci tangan antibakteri. Formula
yang digunakan dalam pembuatan sediaan gel sabun cuci tangan antibakteri:
Tabel I. Formula Awal Gel Sabun Cuci Tangan
Dari variasi jumlahcarbopol®, didapatkan formula sebagai berikut :
Tabel II. Formula Modifikasi Sediaan Gel Sabun Cuci Tangan
b. Pembuatan gel sabun cuci tangan antibakteri. Carbopol®
dikembangkan dalam aquadest 22 mL (setengah dari total aquadest pada formula) selama 24 jam. Kemudian Carbopol® yang telah dikembangkan
Bahan Jumlah (g)
Natrium Lauril Sulfat : Texapon® 2,5
Gliserin 30
Propilen Glikol 25 25 25 25
Metil Paraben 0,10 0,10 0,10 0,10
dicampur dengan gliserin, propilen glikol, metil paraben dan Texapon®
menggunakan mortir dan stamper selama 1 menit, lalu ditambahkan TEA
hingga basis netral. Ekstrak etanol daun beluntas dilarutkan dalam aquadest
sisa dalam formula kemudian ditambahkan ke campuran.Kemudian dicampur kembali sampai terbentuk masa yang homogen, lalu diamkan 5 menit hingga
membentuk masa yang kental. Pada masing-masing formula dibuat replikasi 3
kali untuk dilakukan uji sifat fisik dan stabilitas fisik.
5. Evaluasi sediaan gel sabun cuci tangan antibakteri
a. Sifat fisik
1) Pengamatan organoleptis. Pengamatan dilihat secara langsung
bentuk, warna, dan bau dari gel yang dibuat 48 jam setelah
pembuatan sediaan gel sabun cuci tangan.
2) Viskositas. Gel sabun cuci tangan antibakteri ekstrak etanol daun
beluntas dimasukkan ke dalam wadah dan dipasang pada
viscostesterVT 04. Nilai viskositas sediaan ditunjukkan oleh jarum penunjuk saat viscostester dinyalakan. Pengukuran dilakukan 48 jam setelah pembuatan sediaan gel sabun cuci tangan kemudian
hasilnya dicatat.
3) Ketahanan busa. Ditimbang gel sabun cuci tangan sebanyak 0,1
gram dan larutkan dalam 10 mL air. Kemudian masukkan ke dalam
sampai menit 20. Hitung selisih tinggi busa pada menit ke 0 dan
menit ke 20 sebagai nilai ketahanan busa. Pengukuran dilakukan
48 jam setelah pembuatan sediaan gel sabun cuci tangan.
4) Pengukuran pH. Penentuan pH sediaan dilakukan dengan cara
mencelupkan strips pH ke dalam setiap sediaan sabun cuci tangan
gel lalu mencocokan warna yang terbentuk dengan standar warna
pH. Pengukuran dilakukan 48 jam setelah pembuatan sediaan gel
sabun cuci tangan kemudian hasilnya dicatat.
b. Stabilitas fisik
Stabilitas fisik dilihat dengan mengamati sifat fisik sediaan meliputi
organoleptis, viskositas, ketahanan busa, dan pH selama masa
penyimpanan 28 hari.
6. Uji aktivitas sediaan gel sabun cuci tangan antibakteri terhadap isolat bakteri tangan
a. Pembuatan suspensi bakteri uji. Tabung reaksi berisi media NB disiapkan
sebanyak 9 mL. Kemudian kultur bakteri yang telah tumbuh pada media NA
miring diinokulasikan ke dalam media NB dengan jarum ose, dan diinkubasikan
pada suhu 370C selama 24 jam. Setelah diinkubasi, media NB di lihat
kekeruhannya (setara dengan standar Mac Farland 1,5.108 CFU/mL). Jika kekeruhannya belum setara dengan standar Mac Farland 1,5.108 CFU/mL ditambahkan NB steril sampai kekeruhannya setara dengan standar Mac Farland
b. Uji aktivitas sediaan gel sabun cuci tangan antibakteri ekstrak
etanol daun beluntas. Gel sabun cuci tangan antibakteri ekstrak etanol daun
beluntas dengan berbagai konsentrasi yang dibuat diletakkan pada masing-masing
lubang sumuran yang tersedia pada media yang sebelumnya telah diinokulasikan
bakteri uji secara pour plate. Kontrol positif yang digunakan adalah sabun cuci tangan Lifebuoy Color Changing® dan kontrol negatif yang digunakan adalah basis gel. Diinkubasi selama 24 jam pada suhu 37oC, kemudian diamati hasilnya.
Diameter zona hambat yang dihasilkan sebagai dasar untuk mengamati daya
antibakteri yang dibandingkan dengan kontrol positif dan kontrol negatif.
F. Analisis Data
Data yang dihasilkan berupa data, viskositas, ketahanan busa dan pergeseran
viskositas. Data yang diperoleh, dianalisis dengan menggunakan software R OpenOffice.org (www.molmod.org) dari program R 3.1.0. untuk melihat signifikansi dari variasi jumlah Carbopol® sebagai gelling agent terhadap sifat fisik dan stabilitas fisik sediaan sabun cuci tangan. Signifikansi dinyatakan
melalui nilai p, apabila p <0.05 menunjukkan bahwa variasi jumlah Carbopol®
berbeda signifikan terhadap sifat fisik dan stabilitas fisik sabun cuci tangan. Nilai
35
BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Serbuk Daun Beluntas 1. Pengumpulan bahan daun beluntas
Daun beluntas yang digunakan dalam penelitian ini didapatkan dari CV
Merapi Farma Herbal yang terletak di Jl. Kaliurang Km. 21, Sleman, Daerah
Istimewa Yogyakarta. Determinasi juga dilakukan oleh CV Merapi Farma Herbal
dengan mencocokan morfologi tanaman dengan kunci determinasi (Van Steenis
dan Bloembergen, 1987). Hasil determinasi tersebut menyatakan bahwa tanaman
yang digunakan adalahPluchea indica(L.) Less
Pengumpulan bahan dilakukan pada bulan Oktober 2013 dan berasal dari
satu tempat dengan tujuan untuk mendapatkan hasil yang seragam. Pengumpulan
bahan dilakukan pada sore hari untuk mendapatkan kandungan total fenolik yang
optimal. Daun beluntas yang dipilih adalah daun yang berwarna hijau muda dan
berada di pucuk, sekitar 1-6 daun dari bagian pucuk. Daun beluntas yang dipilih
juga harus bersih dan bebas dari jamur dan bercak serta dipilih daun yang segar,
setidaknya daun yang berumur 50 hari.
Dilakukan pencucian dengan air mengalir untuk menghilangkan cemaran
seperti debu, serangga, sisa-sisa tanah dan cemaran asing lainnya yang dapat
mengganggu kualitas hasil penelitian. Simplisia yang telah dicuci kemudian
dikeringkan dibawah sinar matahari selama lima hari. Pengeringan ini bertujuan
untuk mengurangi kandungan air pada daun beluntas yang dapat menyebabkan
yang dapat menyebabkan daun membusuk. Pada saat pengeringan dibawah
sinar matahari, daun ditutup dengan kain hitam yang bertujuan untuk mencegah
dekomposisi kandungan kimia dari daun dan mencegah penguapan kandungan
fenolik yang berlebihan dari daun beluntas.
Pengeringan dihentikan ketika kadar air dalam simplisia kurang dari 10%
karena reaksi enzimatik tidak akan berlangsung bila kadar air pada simplisia
kurang dari 10% (Nurfina, 1998). Hal ini dapat dilihat ketika simplisia diremas
akan mudah patah. Simplisia yang benar- benar kering maka akan tahan disimpan
dalam waktu lama dan dapat mempertahankan mutunya.
2. Pembuatan serbuk daun beluntas
Penyerbukan dilakukan oleh CV Merapi Farma Herbal. Menurut hasil
wawancara dari pihak CV Merapi Farma Herbal, penyerbukan dilakukan dengan
menggunakan mesin penyerbuk dengan lubang pengayak berdiameter 1mm.
Tujuan dari penyerbukan adalah untuk memperkecil ukuran simplisia, bila ukuran
simplisia semakin kecil maka luas permukaan semakin besar dan kemungkinan
untuk kontak dengan penyari pada saat ekstraksi juga semakin besar. Lubang
pengayak yang berdiameter 1,00 mm menunjukkan pengayak dengan nomor 18
(Dirjen POM, 1995). Derajat kehalusan serbuk dinyatakan dengan nomor
pengayak (Dirjen POM, 1995) sehingga derajat serbuk simplisia daun beluntas ini
sebesar 18 yang berarti semua simplisia dapat melewati pengayak dengan nomor
18. Selanjutnya, serbuk simplisia yang sudah terkumpul disimpan dalam wadah
B. Pembuatan Ekstrak Etanol Daun Beluntas 1. Ekstraksi serbuk daun beluntas
Ekstraksi serbuk daun beluntas dilakukan oleh LPPT UGM. Sesuai dengan
Certificate of Analysis yang diberikan oleh LPPT UGM, ekstraksi dilakukan dengan metode maserasi dengan pelarut etanol 70%. Metode maserasi dipilih
karena metode ini tidak memerlukan pemanasan yang dapat mengganggu
stabilitas ekstrak dan termasuk metode yang sederhana karena menggunakan
peralatan yang sederhana. Prinsip dari metode ekstraksi maserasi adalah
merendam serbuk simplisia dalam cairan penyari dengan bantuan penggojogan,
kemudian cairan penyari tersebut akan menembus dinding sel dan masuk ke
dalam rongga sel yang mengandung zat aktif. Zat aktif akan terlarut dan karena
adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan diluar
sel, maka larutan yang paling pekat akan terdesak keluar sampai terjadi
kesetimbangan antara larutan di luar sel dengan larutan di dalam sel (Depkes RI,
1986).
Serbuk daun beluntas yang telah ditambahkan etanol 70% didiamkan selama
24 jam, kemudian hasilnya disaring. Proses maserasi diulang sebanyak 3 kali
untuk mendapatkan hasil ekstrak etanol yang optimal. Filtrat kemudian diuapkan
dengan Vacuum Rotary Evaporator dengan suhu 70oC. Tujuan dari penguapan denganVacuum Rotary Evaporatoradalah untuk menghilangkan pelarut dari hasil penyaringan. Hasil dari proses ini adalah ekstrak kental yang kemudian akan
Pada proses maserasi ini digunakan cairan penyari etanol 70% karena senyawa
aktif yang akan diambil adalah senyawa fenolik yang bersifat polar. Senyawa
fenolik yang bersifat polar seperti flavonoid dan eugenol mengandung gugus
hidroksi yang mudah larut dalam etanol (Robinson, 1991). Selain itu, kapang dan
kuman sulit tumbuh dalam etanol dengan konsentrasi diatas 20% dan panas yang
diperlukan untuk pemekatan relatif lebih sedikit (Dirjen POM, 1995).
2. Penetapan kadar total fenolik
Penetapan kadar total fenolik secara kualitatif dan kuantitatif dilakukan oleh
LPPT UGM. Metode penetapan kadar yang digunakan adalah spektrofotometri
UV-Vis karena pada dilihat dari struktur kimianya senyawa fenol memiliki gugus
kromofor dan auksokrom. Adanya gugus kromofor dan auksokrom ini
memungkinkan senyawa fenol untuk terdeteksi bila dilakukan analisis dengan
menggunakan spektrofotometer UV-Vis. Berdasarkan laporan hasil uji yang
dikeluarkan oleh pihak LPPT UGM, diperoleh kadar total fenolik sebesar 3,26 %.
C. Uji Potensi Antibakteri Ekstrak Etanol Daun Beluntas 1. Pembuatan stok isolat bakteri tangan
Isolasi merupakan suatu cara untuk mengambil mikroorganisme yang
terdapat di alam dan menumbuhkannya dalam suatu medium buatan
(Dwidjoseputro, 1998). Bakteri tangan diisolasi dari tiga probandus dengan
bagian tangan yang berbeda, yaitu telapak tangan, jari tangan dan punggung
penyebab infeksi yang murni berasal dari tangan sehingga nantinya dapat dilihat
efektifitas sediaan terhadap isolat bakteri tangan tersebut. Tangan merupakan
bagian tubuh yang paling sering kontak dengan dunia luar sehingga sangat
memudahkan terjadinya kontak dengan mikroorganisme dan mentransfernya ke
objek lain (Pratami, 2013).
Isolasi bakteri dari tangan dilakukan kepada tiga probandus dari bagian
tangan yang berbeda, yang seharian telah melakukan kegiatan dan belum cuci
tangan atau belum menggunakan produk antiseptik untuk tangan. Bagian tangan
langsung ditempelkan ke dalam media NA (Nutrient Agar) secara aseptis agar tidak terjadi kontaminasi dan kemurnian biakan dapat dipertahankan.
Karena adanya keterbatasan waktu, peneliti tidak melakukan identifikasi
terhadap isolat bakteri tangan dari 3 probandus. Tetapi peneliti melakukan studi
literatur tentang bakteri apa saja yang sering berada di tangan. Flora normal yang
menempati kulit dibagi menjadi dua jenis yaitu flora transient (sementara) dan floraresidence(tetap). Floratransient biasanya terdapat di tangan, ujung jari dan dibawah kuku. Flora transient umumnya tidak menimbulkan penyakit, namun karena terjadinya perubahan keseimbangan menjadi dapat menimbulkan penyakit
(cit., Jawetz, 2005). Flora transient adala mikroorganisme yang diisolasi dari kulit, tetapi mikroorganisme ini tidak selalu ada di kulit. Jenis mikroorganisme ini
bisa ada di kulit karena kulit banyak terjadi kontak dengan berbagai sumber
mikroorganisme terutama tangan. Bakteri patogen yang mungkin dijumpai di
Berdasarkan penelitian yang dilakukan oleh Pratami (2013), bakteri yang
ditemukan pada tangan tenaga medis dan paramedis adalah Staphylococcus epidermidis,Staphylococcus saprophyticus,Staphylococcus aureus,Pseudomonas aeruginosa, dan Enterobacter aerogenes. Bakteri yang ada di setiap tangan masing-masing orang dapat berbeda-beda, tergantung aktivitas sehari-hari
masing-masing orang. Staphylococcus aureus merupakan flora normal pada mukosa hidung, perpindahanya ke tangan dapat terjadi karena tangan sering
kontak langsung dengan bagian mukosa hidung dan dapat menjadi awal dari
menularnya penyakit infeksi (cit., Baron, 1996). Staphylococcus aureus dalam jumlah lebih dari 106per gram dapat menyebabkan infeksi pada kulit (cit., Snyder, 2001).
2. Uji aktivitas antibakteri ekstrak etanol daun beluntas
Uji aktivitas antibakteri ekstrak etanol daun beluntas bertujuan untuk
mengetahui panjang diameter zona hambat yang terbentuk terhadap isolat bakteri
tangan. Uji aktivitas ini dilakukan dengan metode sumuran karena yang akan diuji
dalam bentuk ekstrak yang memiliki kepolaran berbeda-beda sehingga diharapkan
seluruh komponen dalam ekstrak dapat terdifusi ke dalam media.
Hasil dari uji aktivitas antibakteri adalah terbentuknya zona jernih di
sekitar lubang sumuran. Zona jernih ini menggambarkan bahwa bakteri tidak
dapat tumbuh karena adanya aktivitas penghambatan pertumbuhan bakteri dari