I Wayan Rai Widarta1), I Gusti Putu Tengah1), I Ketut Suter1), I Wayan Arnata2) 1)Staf Pengajar Jurusan Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Unud 1) Staf Pengajar Jurusan Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Unud
Email: rai_widarta@yahoo.com
Bekatul merupakan limbah penggilingan padi yang mengandung komponen bioaktif yang tinggi. Penelitian ini bertujuan mendapatkan metode ekstraksi komponen bioaktif yang tepat sehingga menghasilkan aktivitas antioksidan yang tinggi dan mendapatkan sistem pangan yang tepat untuk aplikasinya. Pada penelitian tahap I dilakukan ekstraksi komponen bioaktif pada bekatul beras merah pada konsentrasi etanol yang berbeda (48%, 60%, 78% dan 96%). Hasil terbaik pada tahap ini digunakan pada penelitian tahap II yaitu ekstraksi dengan pelarut etanol dengan dan tanpa pengasaman serta waktu maserasi yang berbeda (6, 12, 18, 24, 30 dan 36 jam). Ekstrak terpilih hasil penelitian ini, selanjutnya diuji aktivitas antioksidannya pada sistem pangan (aqoeus dan minyak). Parameter yang diamati meliputi: total fenolik, total antosianin, aktivitas antioksidan dan IC50. Data yang diperoleh dianalisis keragamannya dan dilakukan uji
perbandingan berganda Duncan. Hasil penelitian menunjukkan bahwa ekstraksi bekatul beras merah dengan pelarut etanol 96% dalam waktu ekstraksi optimum 30 jam dengan pelarut yang diasamkan menghasilkan total antosianin, total fenolik dan aktivitas antioksidan yang paling tinggi yaitu 106,90 mg/100 g bekatul, 4,30 mg/100 g bekatul, dan 88,07% dengan nilai IC50 sebesar 0,51%. Sistem pangan yang tepat digunakan untuk
aplikasi ekstrak bekatul beras merah adalah dalam sistem aqoeus.
Kata kunci : aktivitas antioksidan, bekatul beras merah, ekstraksi, sistem pangan
!" # $! % &
! '( ' ( )" )! % *
+ %
$! &
)"
-." " .' /
+
0 1
Proses penggilingan padi dengan kadar air 14% akan menghasilkan rendemen
beras 57>60%, sekam 18>20%, dan bekatul 8>10%. Bekatul merupakan limbah proses
penggilingan padi yang jarang dimanfaatkan sebagai produk makanan oleh masyarakat,
padahal potensinya sangat besar apabila dapat dimanfaatkan secara optimal. Hasil
penelitian menunjukkan bahwa bekatul mengandung komponen bioaktif yang tinggi seperti
antioksidan senyawa fenolik (Wiboonsirikul 2007). Sompong (2010) melaporkan
bahwa beras merah yang diperoleh di China, Thailand dan Sri Lanka mengandung
senyawa polifenol dan antosianin yang berbeda>beda tergantung tempat tumbuhnya yang
juga dapat berperan sebagai antioksidan yang baik. Menurut Rattanachitthawat .
(2010) pigmen merah pada beras merah dapat berperan dalam pencegahan stres oksidatif
pada tikus percobaan. Oleh karena itu, penelitian untuk mendapatkan komponen bioaktif
dan aktivitas antioksidan pada bekatul beras merah perlu dilakukan untuk pengembangan
lebih lanjut bekatul beras merah sebagai pangan fungsional.
Penelitian yang berkembang saat ini lebih banyak menggali komponen bioaktif dan
aktivitas antioksidan pada berasnya (Sompong 2010). Komposisi komponen bioaktif
pada bekatul berbeda>beda tergantung pada tempat tumbuh dan salinitas lahan pertanian
(Daiponmak 2010). Untuk mendapatkan ekstrak komponen bioaktif, ada beberapa
hal yang harus diperhatikan diantaranya metode ekstraksi, jenis/polaritas pelarut, pH,
waktu ekstraksi, dan rasio antara bahan dengan pelarut (Hismath 2011).
Menurut deMan (1997), penambahan asam sebagai pelarut tidak selalu
diperlukan. Metode ekstraksi yang digunakan untuk analisis kuantitatif harus diperiksa
secara menyeluruh pada tanaman dan jenis pigmen tertentu. Jika terdapat gugus asil pada
antosianin misalnya di dalam kubis ungu, maka penggunaan asam sebagai campuran
pelarut harus dihindarkan. Hal ini disebabkan ikatan asil ini mudah terhidrolisis. Oleh
mengandung gugus asil atau tidak maka dilakukan tahapan penelitian mengenai pengaruh
pelarut etanol yang diasamkan dan tidak diasamkan terhadap komposisi komponen
bioaktif khususnya total antosianin dan total fenolik dalam ekstrak bekatul.
Selain metode yang tepat, faktor lain yang juga penting adalah kestabilan ekstrak
yang diperoleh karena aplikasinya pada produk pangan membutuhkan stabilitas dan sifat
kelarutan yang baik. Dalam aplikasinya, aktivitas antioksidan juga dipengaruhi oleh sistem
pangan yang merupakan medium bagi antioksidan tersebut (Tensiska . 2003). Oleh
karena itu, pengujian aktivitas antioksidan dalam sistem pangan perlu dilakukan sehingga
diperoleh sistem pangan yang paling tepat untuk aplikasi ekstrak bekatul beras merah
sebagai indgridien pangan fungsional.
Bahan>bahan yang digunakan adalah bekatul (dedak halus) dari varietas beras
merah cendana dan beras putih bali yang diperoleh dari pabrik penyosohan beras di
Kecamatan Penebel, Kabupaten Tabanan, Bali. Bekatul yang telah diayak dengan ayakan
60 mesh, etanol 95%, standar asam galat, DPPH, reagen Folin>Ciocalteu, HCl, etanol pa,
sodium karbonat, aquades, buffer potasium klorida (pH 1), buffer sodium asetat (pH 4,5).
Penelitian ini dilaksanakan dalam tiga tahapan. Tahapan penelitian pertama
adalah penentuan konsentrasi etanol yang tepat sehingga dihasilkan aktivitas antioksidan
ekstrak bekatul beras merah yang tertinggi. Konsentrasi etanol yang digunakan adalah
42%, 60%, 78%, dan 96%. Parameter yang diamati adalah aktivitas antioksidan (Sompong
. 2011). Hasil terbaik dari penelitian tahap I digunakan dalam penelitian tahap II.
Penelitian tahap kedua adalah penentuan waktu ekstraksi komponen bioaktif
bekatul beras merah dengan pelarut etanol yang diasamkan dan tanpa pengasaman.
Sebanyak 20 g bekatul beras merah dilarutkan dengan pelarut etanol (untuk perlakuan
dengan pengasaman, pelarut etanol diasamkan dengan HCl 37% sampai pH 1).
Perbandingan bahan dengan pelarut adalah 1 : 6 b/v kemudian di 2 merk Eyela
dengan kertas saring whatman no 1. Filtrat yang diperoleh di pekatkan dalam rotari
evaporator vakum merk IKA pada suhu 30oC.
Penelitian tahap kedua ini menggunakan Rancangan Acak Kelompok (RAK)
faktorial. Faktor pertama adalah keasaman pelarut (A) dan yang kedua adalah waktu
maserasi (B).
Faktor pertama terdiri dari dua taraf yaitu :
A1 = Etanol tanpa pengasaman
A2 = Etanol dengan pengasaman (pH 1)
Faktor kedua terdiri dari tiga taraf yaitu :
W1 = waktu maserasi 6 jam
percobaan. Data yang diperoleh dianalisis dengan sidik ragam, dan apabila terdapat
pengaruh perlakuan terhadap parameter yang diamati, maka akan dilanjutkan dengan uji
Duncan (Steel dan Torrie 1993). Parameter yang diamati meliputi : Total fenol dianalisis
dengan metode Folin–Ciocalteau (Garcia 2007), penentuan kadar total antosianin
dengan metode 3differential (Giusti dan Wrolstad 2001), penentuan aktivitas antioksidan
dengan 2,2>diphenyl>1>picrylhydrazyl (DPPH) (Sompong . 2011), dan Pengukuran IC50
(Pourmorad 2006). Hasil terbaik penelitian tahap kedua digunakan untuk penelitian
tahap ketiga.
Penelitian tahap ketiga adalah pengujian aktivitas antioksidan ekstrak bekatul
terbaik hasil penelitian tahap kedua pada sistem pangan (sistem aqueos dan minyak).
Aktivitas antioksidan ekstrak bekatul beras merah dalam sistem aqueos (Skerget .
2005). Larutan β>karoten dibuat dengan melarutkan 2,0 mg β>karoten dalam 10 ml
Chloroform. Sebanyak 1 ml larutan tersebut dipipet ke dalam erlenmeyer. Setelah itu
ditambahkan 20 ml asam linoleat, 0,2 ml Tween 20, 2 mgl ekstrak antioksidan, dan 50 ml
air destilasi yang sudah diaerasi dengan oksigen selama 15 menit. Campuran kemudian
pada suhu 50oC. Segera emulsi ditambahkan pada masing>masing tabung dan absorbansi
pada waktu 0 menit dibaca pada panjang gelombang 470 nm yang merupakan panjang
gelombang β>karoten. Absorbansi berikutnya segera dibaca setelah sampel disimpan pada
penangas air suhu 50oC selama 120 menit. Aktivitas antioksidan sampel (s) dihitung
sebagai persen penghambatan oksidasi terhadap kontrol (k).
% aktivitas antioksidan dalam sistem =
−
−
; dimana : As
adalah absorbansi sampel pada waktu t= 0 menit dan t=120 menit, sedangkan Ak adalah
absorbansi kontrol pada waktu t=0 menit dan t=120 menit.
Aktivitas antioksidan ekstrak bekatul beras merah dalam sistem minyak (Azizkhani
dan Zandi 2010). Aktivitas antioksidan dalam sistem minyak dilakukan dengan uji
Rancimat. Sebanyak 200 ppm ekstrak dan 0,5% tween 80 ditambahkan ke dalam minyak
kedelai murni. Periode induksi sampel ditentukan dengan rancimat pada suhu 110oC.
!
Hasil penelitian pendahuluan (tahap I) menunjukkan bahwa konsentrasi etanol
terbaik yang mampu menghasilkan ekstrak bekatul beras merah dengan aktivitas
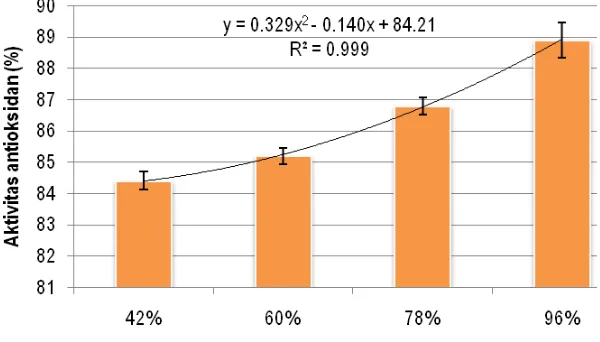
antioksidan yang tinggi adalah konsentrasi pelarut etanol 96%. Hal ini dapat dilihat pada
Gambar 1 Hubungan antara konsentrasi etanol dengan aktivitas antioksidan ekstrak bekatul beras merah
Semakin tinggi konsentrasi etanol maka semakin tinggi pula aktivitas antioksidan
ekstrak bekatul beras merah. Hal ini dapat disebabkan oleh polaritas komponen bioaktif
pada ekstrak bekatul beras merah yang memberikan aktivitas sebagai antioksidan mirip
dengan polaritas etanol 96%. Menurut Franco (2008), polaritas pelarut berpengaruh
terhadap aktivitas antioksidan dari ekstrak yang dihasilkan. Hasil penelitiannya
menunjukkan bahwa ekstrak yang diperoleh dari pelarut etanol menghasilkan aktivitas
antioksidan yang lebih tinggi dibandingkan dengan ekstrak dari pelarut air dan metanol,
dimana polaritas pelarut etanol lebih rendah dari metanol dan air.
Hasil analisis keragaman menunjukkan bahwa perlakuan waktu maserasi dan
pengasaman pelarut berpengaruh sangat nyata terhadap kadar total antosianin (P<0,01).
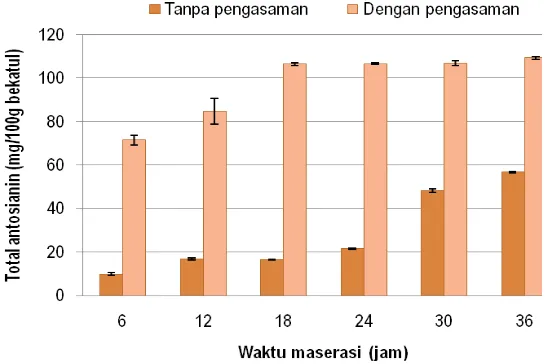
Nilai rata>rata total antosianin (mg/100g bekatul) dapat dilihat pada Gambar 2.
Gambar 2 Hubungan antara waktu maserasi dengan total antosianin ekstrak bekatul beras merah pada pelarut dengan dan tanpa pengasaman
Gambar 2 menunjukkan bahwa waktu maserasi berpengaruh nyata terhadap
kadar total antosianin ekstrak bekatul beras merah. Semakin lama waktu maserasi maka
semakin tinggi pula kadar antosianin yang dihasilkan hingga pada waktu tertentu. Begitu
pula dengan pengaruh pelarut yang diasamkan, pada waktu maserasi yang sama terlihat
dibandingkan dengan pelarut yang tidak diasamkan. Kadar total antosianin tertinggi
diperoleh dengan waktu maserasi 36 jam menggunakan pelarut yang diasamkan yaitu
sebesar 109,33 mg/100g bekatul yang tidak berbeda nyata dengan waktu maserasi 18, 24
dan 30 jam yaitu 106,41, 106,70, 106,90 mg/100g bekatul. Kadar total antosianin tertinggi
yang diperoleh pada penelitian ini tidak berbeda nyata dengan kadar total antosianin yang
diperoleh dari bekatul beras ketan hitam yang diekstraksi dengan pelarut metanol yang
diasamkan dengan 1% HCl yaitu 116,75 ± 12,84 mg/100g, sedangkan ekstraksi dengan
larutan basa menghasilkan rendemen antosianin yang lebih rendah (Hanum 2000).
Tananuwong dan Tewaruth (2010) melaporkan bahwa keasaman pelarut memberikan
hasil yang lebih besar terhadap kadar total monomer antosianin. Lebih lanjut dilaporkan
bahwa pada durasi ekstraksi yang sama, pelarut yang diasamkan menghasilkan total
monomer antosianin yang lebih besar dibandingkan pelarut yang tidak diasamkan. Hal ini
disebabkan oleh stabilitas antosianin yang lebih tinggi dalam larutan asam.
"
Hasil analisis keragaman menunjukkan bahwa perlakuan waktu maserasi dan
pengasaman pelarut berpengaruh sangat nyata terhadap kadar total fenolik (P<0,01). Nilai
rata>rata total fenolik (mg/100g bekatul) dapat dilihat pada Gambar 3.
Gambar 3 Hubungan antara waktu maserasi dengan total fenol ekstrak bekatul beras merah pada pelarut dengan dan tanpa pengasaman
Gambar 3 menunjukkan bahwa waktu maserasi berpengaruh nyata terhadap
kadar total fenolik ekstrak bekatul beras merah. Semakin lama waktu maserasi maka
Menurut Tananuwong dan Tewaruth (2010), waktu reaksi yang pendek belum
menunjukkan reaksi yang sempurna pada ekstraksi senyawa fenolik. Hal serupa juga
dilaporkan oleh Devi dan Arumughan (2007) bahwa waktu ekstraksi berpengaruh terhadap
rendemen ekstrak senyawa fitokimia termasuk senyawa fenolik. Pengaruh pelarut yang
diasamkan pada waktu maserasi yang sama terlihat bahwa pelarut yang diasamkan
menghasilkan total fenolik yang lebih tinggi dibandingkan dengan pelarut yang tidak
diasamkan. Menurut Lestario (2001) diacu dalam Dewi (2007) menyatakan
bahwa penggunaan pelarut yang diasamkan dengan HCl disarankan karena HCl dapat
mendestruksi sel tumbuhan sehingga senyawa antioksidan yang terdapat dalam sel dapat
terekstrak dengan baik. Kadar total fenolik tertinggi diperoleh dengan waktu maserasi 36
jam menggunakan pelarut yang diasamkan yaitu sebesar 4,38 mg/100g bekatul yang tidak
berbeda nyata dengan waktu maserasi 18, 24 dan 30 jam yaitu sebesar 4,20, 4,21 dan
4,30 mg/100g bekatul. Kadar total fenolik terendah diperoleh dengan waktu maserasi 6
jam dengan pelarut yang tidak diasamkan yaitu sebesar 1,62 mg/100g bekatul.
#
Hasil analisis keragaman menunjukkan bahwa perlakuan waktu maserasi dan
pengasaman pelarut berpengaruh sangat nyata terhadap aktivitas antioksidan ekstrak
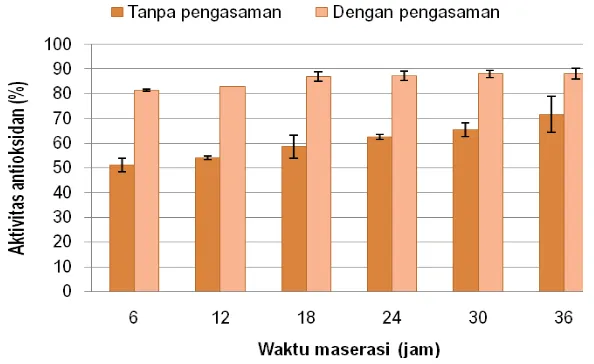
bekatul beras merah (P<0,01). Nilai rata>rata aktivitas antioksidan dapat dilihat pada
Gambar 4.
Berdasarkan Gambar 4 dapat dilihat bahwa waktu maserasi berpengaruh nyata
terhadap aktivitas antioksidan ekstrak bekatul beras merah. Semakin lama waktu maserasi
maka semakin tinggi pula aktivitas antioksidan yang dihasilkan. Begitu pula dengan
pengaruh pelarut yang diasamkan, pada waktu maserasi yang sama terlihat bahwa pelarut
yang diasamkan menghasilkan aktivitas antioksidan yang lebih tinggi dibandingkan dengan
pelarut yang tidak diasamkan. Aktivitas antioksidan tertinggi diperoleh dengan waktu
maserasi 36 jam menggunakan pelarut yang diasamkan yaitu sebesar 88,10% yang tidak
berbeda nyata dengan waktu maserasi 30 jam yaitu sebesar 88,07%. Hal ini dapat
disebabkan oleh kadar komponen bioaktif (total antosianin dan fenolik) pada ekstrak
bekatul beras merah yang dihasilkan semakin tinggi dengan semakin lamanya waktu
maserasi. Hasil analisis regresi linier antara kadar total antosianin dan total fenolik
terhadap aktivitas antioksidan ekstrak bekatul beras merah yang diekstrak dalam pelarut
asam menunjukkan koefisien determinasi yang tinggi mendekati 1 dengan persamaan
garis y=0,185x+67,64; r2=0,973 dan y=16,80x+20,99; r2=0,931.
Adanya gugus hidroksil yang terikat pada cincin aromatis pada molekul senyawa
fenolik dan antosianin memberikan kemampuan mendonorkan proton ke senyawa radikal
sehingga dapat berperan sebagai antioksidan (Franco 2008). Aktivitas antioksidan
yang diperoleh pada penelitian ini lebih tinggi dibandingkan yang diperoleh oleh
Damayanthi (2010) yaitu sebesar 83,89% dan lebih lanjut dilaporkan bahwa aktivitas
antioksidan jus tomat lebih rendah dibandingkan bekatul yaitu sebesar 60,74%.
Pourmorad (2006) melaporkan bahwa ekstrak M. yang
mengandung senyawa fenolik dan flavonoid paling tinggi menghasilkan aktivitas
antioksidan yang tertinggi. Sifat antioksidan yang tinggi disebabkan oleh gugus hidroksil
yang ada dalam struktur kimia senyawa fenolik dapat memberikan komponen yang
diperlukan sebagai penangkap senyawa radikal. Tananuwong dan Tewaruth (2010) juga
melaporkan bahwa ekstrak kasar yang diperoleh dari waktu ekstraksi yang lebih lama
cenderung memiliki aktivitas antioksidan yang lebih besar.
$%&
IC50 didefinisikan sebagai konsentrasi substrat yang menyebabkan 50%
kehilangan aktivitas DPPH yang dihitung dengan regresi linier antara persentase aktivitas
bahwa senyawa tersebut memiliki kemampuan menangkap radikal bebas yang tinggi (Riaz
2012). Berdasarkan persamaan yang diperoleh y = 8,203x + 7,629 maka dapat
ditentukan nilai IC50 ekstrak bekatul beras merah adalah 0,51%.
# ! ' ' ' ( !
Prinsip uji aktivitas antioksidan dengan metode ini adalah sejauh mana proteksi
antioksidan yang diuji terhadap oksidasi asam linoleat dan β>karoten akibat pengaruh
oksidasi air yang jenuh dengan oksigen dan pemanasan. Metode ini didasarkan pada
hilangnya warna kuning β>karoten akibat bereaksi dengan radikal yang terbentuk melalui
oksidasi asam linoleat dalam emulsi. Laju pemucatan β>karoten dapat dihambat dengan
adanya antioksidan (Almeida . 2011). Hasil pengujian aktivitas antioksidan ekstrak
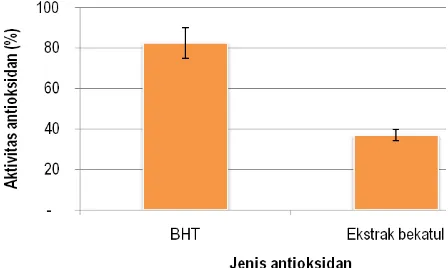
bekatul beras merah dapat dilihat pada Gambar 5.
Gambar 5 menunjukkan bahwa ekstrak bekatul beras merah memiliki aktivitas
antioksidan yang lebih rendah dalam sistem aqoeus dibandingkan dengan BHT. Hal
serupa juga dilaporkan oleh Almeida (2011) bahwa BHT memiliki aktivitas
antioksidan yang paling kuat dalam sistem β>karoten linoleat dibandingkan dengan BHA,
asam askorbat serta ekstrak tanaman 4 dan 5 .
# ! ' ' ' ' )
Aktivitas antioksidan dalam sistem minyak diuji dengan menggunakan alat
Rancimat. Medium yang digunakan adalah minyak kedelai murni. Proses oksidasi
dipercepat dengan adanya aliran udara dan panas. Aktivitas antioksidan dinyatakan
dengan waktu induksi (Tensiska 2003). Standar yang digunakan adalah tokoferol,
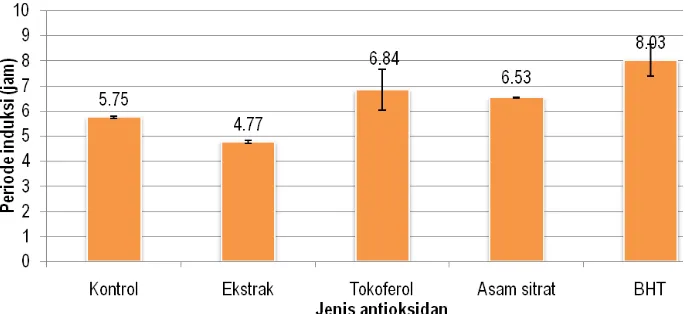
Gambar 6 Periode induksi masing>masing jenis antioksidan dan kombinasinya pada sistem minyak
Berdasarkan Gambar 6 dapat dilihat bahwa ekstrak bekatul beras merah tidak
menunjukkan aktivitas antioksidan dalam sistem minyak. Periode induksi minyak kedelai
yang ditambahkan ekstrak bekatul beras merah bahkan lebih rendah dari kontrol (tanpa
antioksidan). Antioksidan BHT menunjukkan aktivitas antioksidan yang paling tinggi
dibandingkan yang lain. Maisuthisakul (2005) juga melaporkan bahwa antioksidan
BHT lebih efektif dalam sistem minyak dibandingkan dengan ekstrak Teaw
Dyer). Gugus butil tersier BHT efektif dalam menghambat reaksi gugus >OH
aktif melalui dan selanjutnya meningkatkan stabilitas radikal antioksidan
serta memperpanjang masa aktif antioksidan.
Hasil penelitian menunjukkan bahwa ekstrak bekatul beras merah terbaik
diperoleh dengan menggunakan pelarut etanol 96% dalam kondisi asam dengan waktu
maserasi optimum 30 jam. Pada kondisi tersebut dihasilkan total antosianin, total fenolik
dan aktivitas antioksidan yang paling tinggi yaitu 106,90 mg/100g bekatul, 4,30 mg/100 g
bekatul, dan 88,07% dengan nilai IC50 sebesar 0,51%. Berdasarkan hasil pengujian
ekstrak bekatul beras merah dalam dua sistem pangan yang berbeda (aqueos dan
minyak) dapat disimpulkan bahwa ekstrak bekatul beras merah lebih tepat diaplikasikan
*
Almeida JRGDS, Oliveira MRD, Guimarães AL, Oliveira APD, Ribeiro LADA, Lúcio ASSC, Júnior LJQ. 2011. Phenolic quantification and antioxidant activity of 4
and (Annonaceae). Int J Pharma and Bio Sci 2(4): P367>P374
Azizkhani M dan Zandi P. 2010. Effects of some natural antioxidant mixtures on margarine stability. Pak J Agri Sci 47(3): 251>257
Daiponmak W, Theerakulpisut P, Thanonkao P, Vanavichit A, Prathepha P. 2010. Changes of anthocyanin cyanidin>3>glucoside content and antioxidant activity in Thai rice varieties under salinity stress. Science Asia 36: 286–291
Damayanthi E, Kustiyah L, Khalid M, Farizal H. 2010. Aktivitas antioksidan bekatul lebih tinggi daripada jus tomat dan penurunan aktivitas antioksidan serum darah setelah intervensi minuman kaya antioksidan. Jurnal Gizi dan Pangan 5(3): 205–210
deMan JM. 1997. Kimia Makanan. Penerbit ITB, Bandung
Devi RR, Arumughan C. 2006. Phytochemical characterization of defatted rice bran and optimization of a process for their extraction and enrichment. Bioresource Technol 98: 3037>3043. DOI:10.1016/j.biortech.2006.10.009
Dewi JR, Estiasih T, Murtini ES. 2007. Aktivitas antioksidan dedak sorgum lokal varietas coklat ( ) hasil ekstraksi berbagai pelarut. J Teknologi Pertanian. Vol 8 (3):184>192
Franco D, Sineiro J, Rubilar M, Sánchez M, Jerez M, Pinelo M, Costoya N, Núñez MJ. 2008. Polyphenols from plant materials: extraction and Antioxidant power. Electron J Env Agric Food Chem. 7 (8) :3210>3216
Garcia CA, Gavino G, Mosqueda MB, Hevia P, Gavino VC. 2007. Correlation of tocopherol, tokotrienol, γ>oryzanol and total polyphenol content in rice bran with different antioxidant capacity assays. J Food Chem 102 : 1228–1232. DOI:10.1016/j.foodchem.2006.07.012
Giusti MM dan Wrolstad RE. 2001. Unit F1.2: Anthocynins. Characterization and Measurement with UV>visible Spectroscopy. In “Current Protocols in Food Analytical Chemistry”. pp. 1>13. Wrolstad, R.E., ed. John Wiley and Sons. New York, USA.
Hanum T. 2000. Ekstraksi dan stabilitas zat pewarna dari katul beras ketan hitam (6 & ). Buletin Teknologi dan Industri Pangan Vol XI. No. 1, 2000
Maisuthisakul P, Pongsawatmanit R, Gordon MH. 2005. Antioxidant properties of Teaw (- Dryer) extract in soybean oil and emulsions. Kasetsart University, Thailand
Pourmorad F, Hosseinimehr SJ, Shahabimajd N. 2006. Antioxidant activity, phenol and flavonoid contents of some selected Iranian medicinal plants. Afr J Biotechnol Vol. 5 (11): 1142>1145
Rattanachitthawat S, Suwannalert P, Riengrojpitak S, Chaiyasut C, Pantuwatana S. 2010. Phenolic content and antioxidant activities in red unpolished Thai rice prevents oxidative stress in rats. J Med Plants Res 4(9): 796>801. Doi: 10.5897/JMPR10.067
Riaz T, Abbasi MA, Rehman A, Shahzadi T, Ajaib M, Khan KM. 2012. Phytochemical screening, free radical scavenging, antioxidant activity and phenolic content of
5 Jacq. J Serb Chem Soc. 77 (4):423–435. Doi:
10.2298/JSC110621183R
Skerget M, Kotnik P, Hadolin M, Hras AR, Simonic M, Knez Z. 2005. Phenols, proanthocyanidins, flavones and flavonols in some plant materials and their antioxidant activities. Food Chem 89:191–198. Doi:10.1016/j.foodchem.2004.02.025
Sompong R, Siebenhandl>Ehn S, Linsberger>Martin G, Berghofer E.2011. Physicochemical and antioxidative properties of red and black rice varieties from Thailand, China and Sri Lanka. J Food Chem 124 (2011) 132–140. Doi:10.1016/j.foodchem.2010.05.115
Tananuwong K danTewaruth W. 2010. Extraction and application of antioxidants from black glutinous rice. J Food Sci and Tech. 43 : 476–481. DOI:10.1016/j.lwt.2009.09.014
Tensiska, Wijaya CH, Andarwulan N. 2003. Aktivitas antioksidan ekstrak buah andaliman (7 DC) dalam beberapa sistem pangan dan kestabilan aktivitasnya terhadap kondisi suhu dan pH. Jurnal Teknol. dan Industri Pangan. Vol. XIV (1): 29>39