BAB 5
STOIKIOMETRI
5.1 Tata Nama Senyawa Sederhana 5.2 Hukum-hukum Dasar Kimia 5.3 Persamaan Reaksi
5.4 Hukum Gay Lussac dan Hipotesis Avogadro
5.5 Konsep Mol
Tata Nama Senyawa Anorganik
a. Senyawa Molekul (Senyawa Kovalen) Biner
Senyawa biner adalah senyawa yang hanya terdiri dari dua jenis unsur, misalnya air (H2O), amonia (NH3), dan karbon dioksida (CO2).
1. Rumus Senyawa: unsur yang terdapat lebih dahulu dalam urutan berikut ditulis di depan.
B – Si – C – Sb – As – P – N – H – S – I – Br – Cl – O – F
Contoh:
2. Nama Senyawa: nama senyawa kovalen biner adalah rangkaian nama kedua jenis unsur dengan akhiran ida pada nama unsur yang kedua.
Contoh: HCl : hidrogen klorida H2S : hidrogen sulfida
Jika pasangan unsur membentuk lebih dari sejenis senyawa, maka dibedakan dengan menyebutkan angka indeks dalam bahasa Yunani.
Contoh: CO : karbon monoksida CO2 : karbon dioksida
3. Senyawa yang sudah umum dikenal tidak perlu mengikuti aturan di atas.
Senyawa ion terdiri atas suatu kation dan suatu anion.
1. Rumus senyawa
: kation ditulis di depan.
Contoh:
Rumus kimia natrium klorida ditulis NaCl, bukan
ClNa.
2. Nama senyawa
: nama senyawa ion adalah
rangkaian nama kation (di depan), nama anionnya,
angka indeks tidak disebut.
Contoh:
CaCl2 (kalsium klorida)
Jika unsur logam mempunyai lebih dari sejenis bilangan oksidasi, senyawa-senyawanya dibedakan dengan
menuliskan bilangan oksidasinya.
Contoh:
FeCl2 : besi (II) klorida FeCl3 : besi (III) klorida
Menurut cara lama, senyawa dari unsur logam yang
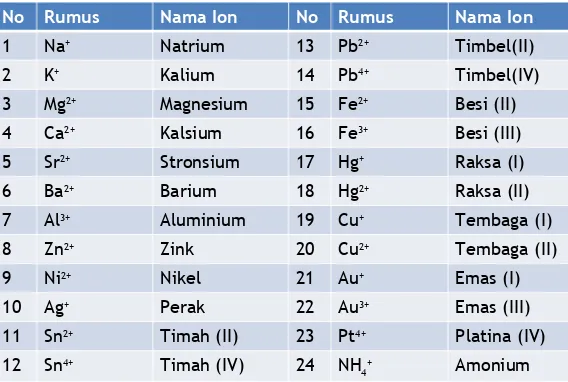
TABEL BEBERAPA JENIS KATION
No Rumus Nama Ion No Rumus Nama Ion
1 Na+ Natrium 13 Pb2+ Timbel(II)
2 K+ Kalium 14 Pb4+ Timbel(IV)
3 Mg2+ Magnesium 15 Fe2+ Besi (II)
4 Ca2+ Kalsium 16 Fe3+ Besi (III)
5 Sr2+ Stronsium 17 Hg+ Raksa (I)
6 Ba2+ Barium 18 Hg2+ Raksa (II)
7 Al3+ Aluminium 19 Cu+ Tembaga (I)
8 Zn2+ Zink 20 Cu2+ Tembaga (II)
9 Ni2+ Nikel 21 Au+ Emas (I)
10 Ag+ Perak 22 Au3+ Emas (III)
11 Sn2+ Timah (II) 23 Pt4+ Platina (IV)
12 Sn4+ Timah (IV) 24 NH
BEBERAPA JENIS ANION
No Rumus Nama Ion No Rumus Nama Ion
1 OH Hidroksida 16 SO42− Sulfat
2 O2- Oksida 17 PO
33− Fosfit
3 F− Flourida 18 PO
43− Fosfat
4 Cl− Klorida 19 AsO
33− Arsenit
5 Br− Bromida 20 AsO
43− Arsenat
6 I− Iodida 21 SbO
33− Antimonit
7 CN− Sianida 22 SbO
43− Antimonat
8 S 2− Sulfida 23 ClO− Hipoklorit
9 CO32− Karbonat 24 ClO
2− Klorit
10 SiO32− Silikat 25 ClO
3− Klorat
11 C2O42− Oksalat 26 ClO
4− Perklorat
12 CH3COO− Asetat 27 MnO
4− Permanganat
13 NO2− Nitrit 28 MnO
42− Manganat
14 NO3− Nitrat 29 CrO
42− Kromat
15 SO32− Sulfit 30 Cr
2O72− Dikromat
c. Tata Nama Asam
Tata Nama Asam dan Basa
Asam
adalah senyawa hidrogen yang di dalam air
mempunyai rasa masam.
Rumus kimia asam umumnya terdiri dari atom
hidrogen dan suatu anion yang disebut sisa
masam.
Contoh:
H3PO4 Nama asam: asam fosfat
Rumus sisa asam: PO4
d. Tata Nama Basa
Basa adalah senyawa ion dari suatu logam dengan ion hidroksida (OH).
Tata nama basa sama dengan tata nama senyawa ion.
Contoh:
NaOH : natrium hidroksida (soda kaustik)
Ca(OH)2: kalsium hidroksida (kapur sirih)
Al(OH)3: alumunium hidroksida (dlm obat maag)
Tata Nama Senyawa Organik
Senyawa organik adalah senyawa-senyawa karbon
dengan sifat-sifat tertentu.
Berikut ini adalah nama lazim dari beberapa senyawa
organik
1. CH4 : metana (gas rawa, gas alam, atau gas tambang)
2. CO(NH2)2 : urea (ureum)
3. CH3COOH : asam cuka (asam asetat)
4. C6H12O6 : glukosa (gula darah, gula anggur) 5. HCHO : formaldehida (bahan formalin)
Hukum-Hukum Dasar Kimia
Hukum Lavoiser (Hukum Kekekalan Massa)
• “Dalam sistem tertutup, massa zat
sebelumnya dan sesudah reaksi adalah sama”
Hukum Proust (Hukum Perbandingan Tetap)
• “Perbandingan massa unsur-unsur dalam
suatu senyawa adalah tertentu dan tetap”
Hukum Dalton (Hukum Kelipatan Berganda)
• “Hukum kelipatan berganda berkaitan
dengan pasangan unsur yang dapat
Persamaan Reaksi
Tanda panah menunjukkan arah reaksi.
Huruf kecil miring dalam tanda kurung menyatakan wujud
atau keadaan zat.
Huruf g berarti gas,l berarti cairan atau (liquid), s berarti padat (solid), dan aq berarti larutan dalam air (aqueous)
Bilangan yang mendahului rumus kimia zat dalam persamaan reaksi disebut koefisien reaksi.
Persamaan reaksi yang sudah diberi koefisien yang sesuai disebut persamaan setara.
Menuliskan Persamaan Reaksi
Contoh:
Alumunium bereaksi dengan larutan asam sulfat membentuk alumunium sulfat dan gas hidrogen.
Langkah 1: menuliskan persamaan kata-kata Alumunium + larutan asam sulfat larutan alumunium sulfat + gas hidrogen
Langkah 2: menuliskan persamaan rumus
Al(s) + H2SO4 (aq) Al2(SO4)3(aq) + H2(g) (belum
setara)
Langkah 3: penyetaraan
2Al(s) + 3H2SO4(aq) Al2(SO4)3(aq) + 3H2(g)
Menyetarakan Persamaan Reaksi
Contoh:
Al(s) + HCl (aq) AlCl3(g) (belum setara)
1. Tetapkan koefsien AlCl3 = 1, sedangkan zat
lainnya dengan koefsien sementara .
aAl(s) + bHCl(aq) 1AlCl3(g) + cH2(g)
2. Setarakan atom Al dan Cl
Penyetaraan atom Al: Jumlah atom Al di ruas kiri = a,
sedangkan di ruas kanan = 1, berarti a = 1.
Penyetaraan atom Cl: Jumlah atom Cl di ruas kiri = b,
sedangkan di ruas kanan = 3 berarti b = 3.
3. Setarakan H: Jumlah atom H di ruas kiri =
3, di ruas kanan = 2c, berarti 2c = 3,
atau c = 1,5
1
Al(
s
) + 3HCl(
aq
)
1
AlCl
3(
g
) +
1,5H
2(
g
)
Akhirnya, untuk membulatkan pecahan
setengah, semua koefsien dikalikan 2:
2Al(
s
) + 6HCl(
aq
)
2AlCl
3(
g
) + 3H
2(
g
)
Hukum Gay Lussac
Contoh:
Pada reaksi antara gas nitrogen dengan gas hidrogen membentuk amonia, perbandingan volumnya adalah 1 : 3 : 2.
Gay Lussac menyimpulkan penemuannya dalam suatu perbandingan volum, yaitu:
“Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan gas hasil reaksi berbanding sebagai bilangan bulat dan
Hipotesis Avogadro
Hukum Perbandingan Volum Avogadro:
Jadi, perbandingan volum gas-gas itu juga
merupakan perbandingan jumlah molekul yang terlibat dalam reaksi atau perbandingan volum gas-gas yang bereaksi sama dengan koefsien reaksinya.
“Pada suhu dan tekanan sama, semua gas bervolum sama
Contoh:
Reaksi antara gas hidrogen dengan gas klorin membentuk gas hidrogen klorida.
1H
x(
g
) + 1Cl
y(
g
) 2H
aCl
b(
g
)
Nilai paling sederhana untuk x dan y yangmembuat persamaan di atas setara adalah x = 2 dan y = 2.
Dengan x = , maka nilai a = 1. Dengan y = 2, maka nilai b = 1. Jadi, persamaan di atas menjadi:
Konsep Mol
1 mol = 6,02 x 10 (= 602 miliar triliun)
23
Bilangan 6,02 x 10 ini disebut tetapan
Avogadro dan dinyatakan dengan lambang L.
L
= 6,02 x 10
23
23
Hubungan jumlah mol (n) dengan jumlah partikel (χ)
χ = n x 6,02 x 10
Massa Molar (
m
m)
m = n x
m
m( Mr)23 Contoh:
Diketahui Ar Ca = 40 dan Mr CO2 = 44, maka - massa 1 mol Ca (= 6,02 x 10 atom Ca) = 40 gram.
- massa 1 mol CO2 (= 6,02 x 10 molekul CO2)
= 44 gram.
23
Untuk unsur yang partikelnya berupa atom: mm =
Ar gram mol
Untuk zat lainnya : mm = Mr gram mol
-1
-1
dengan m = massa n = jumlah mol
Volum Molar Gas (V
m)
V = n x V
m23 Contoh:
Diketahui Ar Ca = 40 dan Mr CO2 = 44, maka
- massa 1 mol Ca (= 6,02 x 10 atom Ca) = 40 gram.
- massa 1 mol CO2 (= 6,02 x 10 molekul CO2)
= 44 gram.
23
Pada keadaan STP : Vm = 22,4 liter mol Pada keadaan RTP : Vm = 24 liter mol
-1
-1
Keterangan: V = volum n = jumlah mol
Persamaan Gas Ideal
V = nRT
P
Persamaan gas ideal:
PV
= nRT
Keterangan: P = tekanan gas (dalam atm)
V = volum gas (dalam liter) n = jumlah mol gas
R = tetapan gas (0,082 L atm mol K )
T = suhu mutlak gas
(dalam Kelvin = 273 + suhu Celcius)
Kemolaran Larutan
M =
Keterangan: M = kemolaran
larutan
n = jumlah mol zat terlarut V = volum larutan
Satuan kemolaran adalah
mol L atau mmol mL .
-1 -1 Konsentrasi (kemolaran)larutan biasanya ditunjukkan
dengan label yang tertempel ada botol.
Menentukan Rumus Empiris
Rumus empiris atau rumus perbandingan suatu senyawa menyatakan perbandingan paling sederhana dari atom-atom unsur
penyusun senyawa.
Data yang diperlukan untuk penentuan rumus empiris adalah:
1) Jenis unsur penyusun senyawa
2) Perbandingan massa antarunsur dalam
Conto
h
-1
Suatu senyawa mengandung unsur karbon, hidrogen, dan oksigen. Dari analisis dikerahui bahwa dalam 3gram senyawa itu terdapat 1,2 gram karbon, 0,2 gram hidrogen, dan sisanya adalah oksigen.
(Ar H= 1; C = 12; dan O = 16)
Jumlah mol C = 1,2 g = 0,1 mol 12 g mol
Jumlah mol H = 0,2 g = 0,2 mol 1 g mol
Massa O = 3 – (1,2 + 0,2) gram = 1,6 gram. Jumlah mol O = 1,6 g = 0,1 mol
16 g mol
Perbandingan mol C : H : O = 0,1 : 0,2 : 0,1 = 1 : 2 : 1.
Rumus empiris senyawa tersebut adalah CH2O.
-1
Menentukan Rumus Molekul
Secara umum, jika rumus empiris senyawa adalah RE, maka rumus molekulnya dapat dinyatakan
sebagai (RE)n; harga n bergantung pada massa
molekul relatif (Mr) dari senyawa yang
bersangkutan.
Contoh:
Senyawa X mempunyai rumus empiris CH2O dan massa molekul relatif (Mr) = 60.
Diketahui rumus empiris senyawa adalah CH2O.
Misalkan rumus molekul senyawa itu (CH2O)χ.
Mr (CH2O)χ = 60 (12 + 2 + 16)χ = 60
30χ = 60
χ = 2
Jadi, rumus molekul senyawa itu adalah (CH2O)2
Kadar Unsur dalam Senyawa
χ adalah jumlah atom unsur dalam 1 molekul
senyawa = indeks dari unsur yang bersangkutan dalam rumus kimia senyawa.
Contoh:
Kadar C dan N dalam urea, CO(NH2)2? (Ar H = 1;
C = 12; dan O = 16)
Kadar unsur X = χ x Ar unsur X x 100%
Mr senyawa
Mr urea = 12 + 16 + 28 + 4 = 60
Kadar C = (1 x 12) x 100% = 20% 60
Pereaksi Pembatas
Pereaksi pembatas adalah pereaksi yang habis
lebih dahulu.
Contoh:
4Al(
s
) + 3O
2(
g
) 2Al
2O
3(
s
)
Persamaan reaksi menunjukkan bahwa
perbandingan mol alumunium dengan oksigen adalah 4 : 3.
Jika jumlah mol yang direaksikan sesuai
dengan perbandingan itu, maka kedua pereaksi itu akan habis.
Jika jumlah mol yang direaksikan tidak 4 : 3,
Pereaksi Pembatas
Pereaksi pembatas adalah pereaksi yang habis
lebih dahulu.
Contoh:
4Al(
s
) = 3O
2(
g
) 2Al
2O
3(
s
)
Persamaan reaksi menunjukkan bahwa
perbandingan mol alumunium dengan oksigen adalah 4 : 3.
Jika jumlah mol yang direaksikan sesuai
dengan perbandingan itu, maka kedua pereaksi itu akan habis.
Jika jumlah mol yang direaksikan tidak 4 : 3,
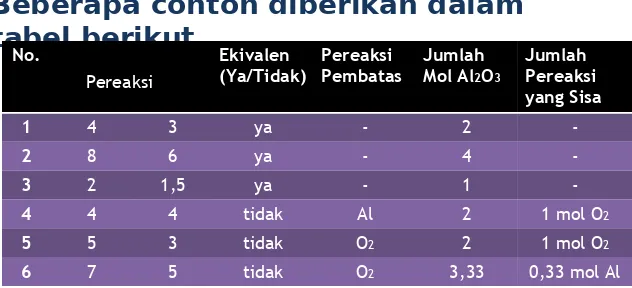
Beberapa contoh diberikan dalam
tabel berikut.
No. Jumlah Mol Ekivalen
(Ya/Tidak) Pereaksi Pembatas Jumlah Mol Al2O3
Jumlah Pereaksi yang Sisa
1 4 3 ya - 2
-2 8 6 ya - 4
-3 2 1,5 ya - 1
-4 4 4 tidak Al 2 1 mol O2
5 5 3 tidak O2 2 1 mol O2
6 7 5 tidak O2 3,33 0,33 mol Al
Menentukan Rumus Kimia Hidrat
Hidrat adalah zat padat yang mengikat beberapa molekul air sebagai bagian dari struktur kristalnya.
Contoh:
1. Terusi, CuSO4.5H2O : tembaga(II) sulfat pentahidrat
2. Gipsum, CaSO4.2H2O : kalsium sulfat dihidrat
3. Garam inggris, MgSO4.7H2O : magnesium sulfat heptahidrat
Menentukan Rumus Kimia Hidrat
Jika suatu hidrat dipanaskan, sebagian atau seluruh air kristalnya dapat lepas (menguap).