LAPORAN PRAKTIKUM KIMIA ANORGANIK I PERCOBAAN II
KALIUM NITRAT
OLEH
NAMA : AMRIN
STAMBUK : F1C1 14 059
KELOMPOK : X (SEPULUH)
ASISTEN : KARTIKA APRIYANTI
JURUSAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS HALU OLEO
I. PENDAHULUAN
A. Latar Belakang
Kalium Nitrat adalah suatu senyawa garam nitrat dari kalium dengan rumus molekul KNO3. Senyawa ini dkenal orang dengan istilah sendawan, sedangkan garam nitrat dari logam natrium dikenal sebagai sendawan chili, terutama dalam bentuk natrium nitrat. Garam natrium memiliki daya jual yang murah, oleh karena itu untuk memenuhi berbagai kebutuhan dengan nilai jual relatif lebih tinggi, garam natrium sebaiknya diubah ke bentuk garam kalium.
Penggunaan kalium nitrat dalam pasta gigi untuk gigi sensitif telah bertambah secara dramatis, walau nyatanya telah tak ditampakkan untuk membantu dengan sebenarnya hipersensitivitas gigi. Dengan melihat banyaknya manfaat yang ditimbulkan oleh senyawa Kalium Nitrat, maka berdasarkan latar belakang diatas perlu dilakukan percobaan tentang pembuatan Kalium Nitrat.
Berdasarkan uraian diatas, maka perlu dipelajari lebih lanjut cara pembuatan dari Kristal KNO3 tersebut, dimana caranya adalah dengan mengkristalisasi dan menrekristalisasi KI dengan NaNO3.
B. Rumusan Masalah
C. Tujuan
Tujuan yang mendasari terjadinya praktikum Kalium Nitrat adalah untuk memberikan gambaran tentang teknik dan proses pembuatan garam kalium nitrat dengan menggunakan bahann dasar natrium nitrat.
D. Manfaat
II. TINJAUAN PUSTAKA
Kalium adalah logam putih perak yang lunak, logam ini melebur pada 63,6oC. Ia tak berubah dalam udara kering, tetapi dengan cepat teroksidasi dalam udara lembab, menjadi tertutup dengan suatu lapisan biru. Logam itu menguraikan air dengan dahsyat, sambil melepaskan hydrogen dan terbakar dengan nyala lembayung. Garam-garam kalium mengandung kation monovalen K+. Garam-garam ini biasanya larut dan membentuk larutan yang berwarna, kecuali bila anionnya berwarna (Vogel, 1979).
Kalium adalah mineral yang memiliki manfaat bagi tubuh manusia yaitu berfungsi mengendalikan tekanan darah, terapi darah tinggi, serta membersihkan karbondioksida di dalam darah. Kekurangan kalium dapat berefek buruk dalam tubuh karena mengakibatkan hipokalemian yang menyebabkan frekuensi denyut jantung melambat. Sedangkan untuk kelebihan kalium mengakibatkan hiperkalemia yang menyebabkan aritmia jantung, konsentrasi yang lebih tinggi lagi yang dapat menimbulkan henti jantung atau fibrilasi jantung (Fitriani dkk., 2012)
masyarakat menurut keputusan Menteri Perindustrian dan Perdagangan No. 15/MPP/KEP/2/1998 (Assadad dan Bagus, 2011).
Nitrat dan nitrit merupakan salah satu zat pengawet yang digunakan dalam proses pengawetan daging untuk memperoleh warna yang baik dan mencegah pertumbuhan mikroba. Nitrit sebagai pengawet diijinkan penggunaannya, akan tetapi perlu diperhatikan penggunaannya dalam makanan agar tidak melampaui batas, sehingga tidak berdampak negatif terhadap kesehatan manusia. Konsumsi nitrit yang berlebihan dapat menimbulkan kerugian bagi pemakainya, baik yang bersifat langsung, yaitu keracunan, maupun yang bersifat tidak langsung, yaitu nitrit bersifat karsinogenik (Hayati dan Dyah, 2011)
III. METODOLOGI PRAKTIKUM A. Waktu dan tempat
Praktikum ini dilaksanakan pada hari Kamis, tanggal 22 Oktober 2015 pukul 07.30 – 10.00 WITA dan bertempat di Laboratorium Kimia Anorganik, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Halu Oleo, Kendari.
B. Alat dan Bahan 1. Alat
Alat-alat yang digunakan dalam pembuatan Kalium Nitrat terdiri dari gelas kimia 50 mL, gelas ukur 25 mL, hot plate, corong, batang pengaduk, penangas air, timbangan analitik dan pipet tetes.
2. Bahan
C. Prosedur Kerja
Prosedur kerja percobaan Kalium Nitrat adalah sebagai berikut :
Natrium Nitrat (NaNO3) Kristal Kalium Iodida (KI)
-ditimbang 8,5 gram dengan teliti
-dilarutkan dengan 25 mL air panas dalam gelas kimia 100 mL
-ditimbang 7,5 gram dengan teliti
-dilarutkan dengan 25 mL aquades dalam gelas kimia 100 mL
Larutan B
Filtrat Residu
-diuapkan hingga volume menjadi setengah -diuapkan sampai volume larutan
IV. HASIL DAN PEMBAHASAN
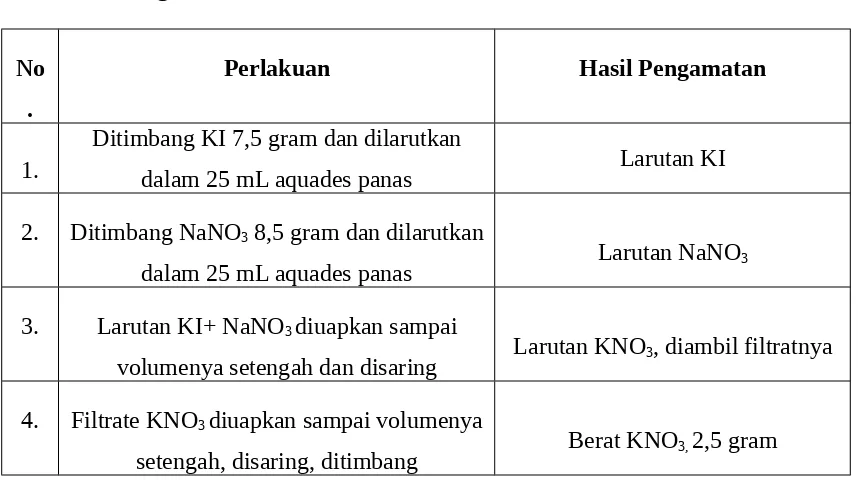
Ditimbang KI 7,5 gram dan dilarutkan
dalam 25 mL aquades panas Larutan KI 2. Ditimbang NaNO3 8,5 gram dan dilarutkan
dalam 25 mL aquades panas Larutan NaNO3 3. Larutan KI+ NaNO3 diuapkan sampai
volumenya setengah dan disaring Larutan KNO3, diambil filtratnya 4. Filtrate KNO3 diuapkan sampai volumenya
setengah, disaring, ditimbang Berat KNO3, 2,5 gram Massa kertas saring : 1,377 gram
2. Reaksi-reaksi yang Terjadi
K+(aq) + I- (aq) KI(aq) Na+(aq) + NO3-(aq) NaNO3(aq) KI(aq) + NaNO3(S) NaI(aq) + KNO3(aq)
3. Analisis Data
Menghitung % Rendamen KNO3 Dik : Berat KI = 7,5 gram
Mr KI = 167 gram/mol Berat NaNO3 = 8,5 gram Mr NaNO3 = 85 gram/mol Mr KNO3 = 101 gram/mol Berat kristal praktek = 2,5 gram Dit : % Rendamen = . . . ? Penyelesaian :
a. Mol KNO3 :
KI + NaNO3 NaI + KNO3 1 mol KI 1 mol KNO3
Mol KI = berat KI Mr KI
= 1677,5gramgram/mol
= 0,04 mol
b. Berat teoritis KNO3
Berdasarkan keterangan reaksi diatas 1 mol KI 1 mol KNO3
Sehingga berat teoritis KNO3 = Mol KNO3 × Mr KNO3 = 0,04 mol × 101 gram/mol
= 4,53 gram c. % Rendamen
% Rendamen = Berat Praktikum
Berat Teori × 100%
= 4,532,5gramgram × 100%
= 55,19 %
B. Pembahasan
Kristalisasi adalah proses pembentukan bahan padat dari pengendapan
larutan, melt (campuran lelehan), atau pengendapan langsung dari gas, namun hal ini
padat-cair, di mana terjadi perpindahan massa (mass transfer) dari suatu zat terlarut
(solute) dari cairan larutan ke fase kristal padat.
Pemisahan dengan teknik kristalisasi didasari atas pelepasan pelarut dari zat terlarutnya dalam sebuah campuran homogeen atau larutan, sehingga terbentuk kristal dari zat terlarutnya. Proses ini adalah salah satu teknik pemisahan padat-cair yang sangat penting dalam industri, karena dapat menghasilkan kemurnian produk hingga 100%.
Rekristalisasi adalah pemurnian suatu zat padat dari campuran atau pengotornya dengan cara mengkristalkan kembali zat tersebut setelah dilarutkan dalam pelarut yang cocok. Prinsip rekristalisasi adalah perbedaan kelarutan antara zat yang akan dimurnikan dengan kelarutan zat pencampur atau pencemarnya. Larutan yang terjadi dipisahkan satu sama lain, kemudian larutan zat yang diinginkan dikristalkan dengan cara menjenuhkannya.
Mula-mula molekul zat terlarut membentuk agrerat dengan molekul pelarut, lalu terjadi kisi-kisi diantara molekul zat terlarut yang terus tumbuh membentuk Kristal yang lebih besar diantara molekul pelarutnya, sambil melepaskan sejumlah energy. Kristalisasi dari zat akan menghasilkan Kristal yang identik dan teratur bentuknya sesuai dengan sifat Kristal senyawanya. Dan pembentukan Kristal ini akan mencapai optimum bila berada dalam kesetimbangan.
pada temperatur kamar, senyawa tersebut telah larut sempurna di dalam pelarut, maka tidak perlu lagi dilakukan pemanasan. Pemanasan hanya dilakukan apabila senyawa tersebut belum atau tidak larut sempurna pada keadaan suhu kamar. Salah satu faktor penentu keberhasilan proses kristalisasi dan rekristalisasi adalah pemilihan zat pelarut.
Membuat Kristal KNO3 dimulai dengan melarutkan 7,5 gram Kristal KI dan 8,5 gram kristal NaNO3 dengan masing-masing 50ml aquades panas yang telah didinginkan. Setelah larut, kedua larutan dicampur dan diaduk. Kemudian diuapkan sampai volume habis menjadi separuhnya. Setelah itu disaring dalam keadaan panas. Filtratnya diuapkan hingga menjadi separuh volumenya. Kemudian didinginkan sampai terbentuk Kristal. Tahap ini disebut tahap kristalisasi.
Kristal yang terbentuk di pisahkan dari larutannya dan kemudian dicuci dengan aquades untuk menghilangkan kandungan kloridanya. Kemudian ditimbang untuk mengetahui randemennya. Hal ini dilakukan untuk menentukan kemurnian Kristal tersebut. Tahap ini disebut tahap re-kristalisasi.
V. KESIMPULAN
DAFTAR PUSTAKA
Assadad, L., dan Bagus, S.B.U. 2011. Pemanfaatan Garam dalam Industri Pengolahan Produk Perikanan. Jurnal Squalen. Vol. 6(1).
Fitriani, N.L.C., Walanda, D.K., dan Rahman, N. 2012. Penentuan Kadar Kalium (K) dan Kalsium (Ca) dalam Labu Siam (Sechium Edule) serta Pengaruh Tempat Tumbuhnya. Jurnal Akademika Kimia. Vol. 1(4).
Nur, H.H., dan Dyah, S. 2011. Analisis Kandungan Nitrit dalam Sosis pada Distributor Sosis Di Kota Yogyakarta. Jurnal KESMAS. ISSN: 1978-0575. Underwood. 2002. Analisis Kimia Kuantitatif. Erlangga. Jakarta