PENGARUH PENAMBAHAN PEMLASTIS POLIETILEN GLIKOL 400,
DIETILEN GLIKOL, DAN DIMETIL FTALAT TERHADAP
PROSES BIODEGRADASI BIOPLASTIK POLI- -HIDROKSIALKANOAT
PADA MEDIA CAIR DENGAN UDARA TERLIMITASI
Oleh
AHMAD ARBAN KHOIRI F 34102122
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PENGARUH PENAMBAHAN PEMLASTIS POLIETILEN GLIKOL 400,
DIETILEN GLIKOL, DAN DIMETIL FTALAT TERHADAP
PROSES BIODEGRADASI BIOPLASTIK POLI- -HIDROKSIALKANOAT
PADA MEDIA CAIR DENGAN UDARA TERLIMITASI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
AHMAD ARBAN KHOIRI F 34102122
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
iii FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
PENGARUH PENAMBAHAN PEMLASTIS POLIETILEN GLIKOL 400,
DIETILEN GLIKOL, DAN DIMETIL FTALAT TERHADAP
PROSES BIODEGRADASI BIOPLASTIK POLI- -HIDROKSIALKANOAT
PADA MEDIA CAIR DENGAN UDARA TERLIMITASI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
AHMAD ARBAN KHOIRI F 34102122
Dilahirkan pada tanggal 4 April 1984, di Bogor
Tanggal Lulus: 7 Maret 2007
Bogor, Maret 2007 Menyetujui,
Dr. Ir. Krisnani Setyowati Dr. Ir. Khaswar Syamsu, M.Sc
Ahmad Arban Khoiri. F 34102122. Pengaruh Penambahan Pemlastis Polietilen Glikol 400, Dietilen Glikol, dan Dimetil Ftalat terhadap Proses Biodegradasi Bioplastik Poli- -hidroksialkanoat pada Media Cair dengan Udara Terlimitasi. Di Bawah Bimbingan Krisnani Setyowati dan Khaswar Syamsu. 2007.
RINGKASAN
Saat ini, produksi berbagai jenis polimer sintetis berbahan dasar minyak bumi di seluruh dunia telah mencapai 140 juta ton/tahun. Jumlah tersebut meningkat hingga 20 kali lipat jika dibandingkan dengan produksi polimer sintetis berbahan dasar minyak bumi pada dekade 1950. Pertumbuhan penggunaan plastik yang signifikan ini dikarenakan oleh sifat plastik yang memiliki banyak keunggulan, seperti: (1) mudah dibentuk sesuai dengan kebutuhan; (2) bobot yang lebih ringan jika dibandingkan dengan bahan-bahan lain; (3) daya tahan yang sangat baik; (4) ketahanan terhadap bahan kimia, air, dan benturan; serta (5) biaya produksi yang tidak besar. Akan tetapi, sebagian besar polimer yang diproduksi dan dikonsumsi pada akhirnya akan menjadi limbah industri di lingkungan. Hal tersebut dikarenakan mayoritas polimer sintetis yang diproduksi merupakan polimer dengan ketahanan yang baik terhadap penguraian secara biologis.
Poli- -hidroksialkanoat merupakan salah satu jenis biopolimer yang mampu terdegradasi secara biologis. Poli- -hidroksialkanoat merupakan biopolimer yang berpotensi besar menjadi alternatif pengganti polimer sintetis berbahan dasar minyak bumi. Salah satu karakteristik yang mengagumkan dari poli- -hidroksialkanoat adalah kemampuan terurainya pada kondisi lingkungan yang berbeda-beda. Bioplastik poli- -hidroksialkanoat memiliki karakter yang kurang baik, seperti rapuh dan tidak elastis. Penambahan pemlastis merupakan salah satu cara untuk memperbaiki sifat fisik dan mekanis bioplastik poli -hidroksialkanoat tersebut. Sebagai polimer yang dapat terdegradasi secara biologis, penambahan pemlastis akan mempengaruhi kemampuan bioplastik poli- -hidroksialkanoat untuk terdegradasi. Karena itu diperlukan suatu studi khusus untuk mengetahui proses biodegradasi bioplastik poli- -hidroksialkanoat serta pengaruh penambahan pemlastis terhadap proses biodegradasi bioplastik poli- -hidroksialkanoat.
Studi ini bertujuan untuk mengetahui pengaruh penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat terhadap kemampuan bioplastik poli- -hidroksialkanoat untuk terdegradasi pada media cair berupa air danau dengan penambahan inokulum pendegradasi berupa limbah cair nata de coco pada kondisi udara terlimitasi, dengan melakukan pengukuran akumulasi produksi CO2 dan laju produksi CO2 sebagai parameter biodegradasi.
Bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat, mampu terdegradasi secara biologis pada media cair dengan udara terlimitasi. Hal tersebut dibuktikan dengan diproduksinya CO2 selama proses biodegradasi.
Penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat memberikan pengaruh yang negatif bagi proses biodegradasi bioplastik. Akumulasi produksi CO2 lebih kecil dan laju produksi CO2 berlangsung lebih lambat jika dibandingkan dengan jumlah CO2 yang dihasilkan pada proses biodegradasi bioplastik tanpa pemlastis. Bioplastik poli- -hidroksialkanoat tanpa penambahan pemlastis sebagai pembanding memiliki akumulasi produksi CO2 terbesar dan laju produksi CO2 paling cepat dengan akumulasi produksi CO2
v Pada hari ke-50, bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400 merupakan bioplastik dengan penambahan pemlastis yang paling cepat terdegradasi. Hal tersebut dibuktikan dengan akumulasi produksi CO2 tertinggi dan laju produksi CO2 tercepat jika dibandingkan dengan sampel bioplastik dengan penambahan pemlastis lainnya. Bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400 memiliki akumulasi produksi CO2 sebesar 23,76 mg dan laju produksi CO2 sebesar 0,48 mg CO2/hari, diikuti oleh bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dietilen glikol dengan akumulasi produksi CO2 sebesar 18,92 mg dan laju produksi CO2 sebesar 0,38 mg CO2/hari. Bioplastik poli -hidroksialkanoat dengan penambahan pemlastis dimetil ftalat merupakan bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis yang terdegradasi paling lambat. Hal tersebut dibuktikan dengan akumulasi produksi CO2 terkecil dan laju produksi CO2 paling lambat dibandingakan semua sampel. Bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dimetil ftalat memiliki akumulasi produksi CO2 sebesar 16,72 mg, serta laju produksi CO2 sebesar 0,33 mg CO2/hari.
Pasokan udara yang terbatas berpengaruh negatif terhadap proses biodegradasi. Pasokan udara yang terbatas pada proses biodegradasi akan berakibat pada akumulasi produksi CO2 yang lebih kecil dan laju produksi CO2 yang lebih lambat jika dibandingkan dengan proses biodegradasi yang dipasok udara secara terus menerus dengan menggunakan pompa aerasi.
Ahmad Arban Khoiri. F 34102122. Influence of Polyethylene Glycol 400, Diethylene Glycol, and Dimethyl Phthalate addition to Biodegradation Process of Poly- -hydrokxyalkanoates Bioplastic in Water Media with Air Limitation. Supervised by Krisnani Setyowati and Khaswar Syamsu. 2007.
SUMMARY
Nowadays, a wide variety of petroleum-based synthetic polymers are produced worldwide to the extent of approximately 140 million tones per year. It means that we produce and use 20 times more plastic today than we did in 1950s. The considerable growth in plastic use is due to the beneficial properties of plastics. These include: (1) extreme versatility and ability to be tailored to meet very specific technical needs; (2) lighter weight than competing materials; (3) extreme durability; (4) resistance to chemicals, water, and impact; (5) good safety and hygiene properties for food packaging; and (6) relatively inexpensive to produce. However, the majority of synthetic polymers are introduced in the ecosystem as industrial waste products. This problem occurred due to the majority of synthetic polymers are extremely resistant to microbial attack.
Poly- -hydroxyalkanoates is one of various biopolymers which are able to degrade biologically. Poly- -hydroxyalkanoates are a biopolymer with a great potential to substitute the petroleum based synthetic polymers, due to its ability to degrade in various environments. But unfortunately, poly- -hydroxyalkanoates have a rigid and brittle characteristic. An addition of plasticizer is needed to improve the physical and mechanical properties of poly- -hydroxyalkanoates. As a biodegradable polymer, the addition of plasticizer will give an influence to the poly- -hydroxyalkanoates biodegradability. A study is needed to determine the biodegradation process of poly- -hydroxyalkanoates bioplastic and the influence of plasticizer addition to the biodegradation process of poly- -hydroxyalkanoates bioplastic.
The objective of this study is to determine the influence of polyethylene glycol 400, diethylene glycol, and dimethyl phthalate addition towards biodegradability of poly- -hydroxyalkanoates bioplastic in lake water media with nata de coco waste as degradation inoculums in limited air condition, by measuring the CO2 production accumulation and the production rate of CO2 as the biodegradation parameter.
The poly- -hydroxyalkanoates bioplastic plasticized with polyethylene glycol 400, diethylene glycol, and dimethyl phthalate, were able to degrade biologically in water media with air limitation. This conclusion was made based on the CO2 production during the biodegradation process was conducted.
The addition of polyethylene glycol 400, diethylene glycol, and dimethyl phthalate has a negative influence to the poly- -hydroxyalkanoates bioplastic biodegradation process. The CO2 production accumulation has a smaller value and the CO2 production rate has became slower compared to CO2 production accumulation and CO2 production rate of nonplasticized poly -hydroxyalkanoates bioplastic. The non-plasticized poly- --hydroxyalkanoates bioplastic, has the biggest value of CO2 production accumulation of 27,28 mg and the fastest CO2 production rate of 0,55 mg CO2/day.
After 50 days test, the poly- -hydroxyalkanoates bioplastic plasticized with polyethylene glycol 400 was the fastest to degrade plasticized bioplastic. The poly- -hydroxyalkanoates bioplastic plasticized with polyethylene glycol 400 has the value of CO2 production accumulation of 23,76 mg and CO2 production
vii plasticized with diethylene glycol with CO2 production accumulation of 18,92 mg and CO2 production rate of 0,38 mg CO2/day. The poly- -hydroxyalkanoates bioplastic plasticized with dimethyl phthalate was the slowest to degrade plasticized bioplastic, with CO2 production accumulation of 16,72 mg and CO2 production rate of 0,33 mg CO2/day.
The air limitation during the biodegradation process has giving a negative influence to the biodegradation process. The air limitation during the biodegradation process has causing a smaller amount of CO2 production accumulation and a slower CO2 production rate compared to biodegradation process held with continuous air supply using the aeration pump.
LEMBAR PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul : “Pengaruh Penambahan Pemlastis Polietilen Glikol 400, Dietilen Glikol, dan Dimetil Ftalat terhadap Proses Biodegradasi Bioplastik Poli- -hidroksialkanoat pada Media Cair dengan Udara Terlimitasi” adalah karya asli saya sendiri, dengan arahan dosen pembimbing akademik, kecuali yang dengan jelas ditunjukkan rujukannya.
Bogor, Maret 2007
Yang Membuat Pernyataan
Nama : Ahmad Arban Khoiri NRP : F 34102122
ix BIODATA RINGKAS
Penulis dilahirkan di Bogor pada tanggal 4 April 1984 dari pasangan H. M. Tamsur Marse dan Dida Djamilah. Penulis merupakan anak ke-2 dari dua bersaudara. Penulis memulai pendidikan dasarnya di SD Negeri Panaragan 2 Kota Bogor pada tahun 1990 dan menyelesaikannya pada tahun 1996. penulis melanjutkan pendidikannya di SLTP Negeri 4 Bogor hingga tahun 1999, yang kemudian dilanjutkan ke SMU Negeri 5 Bogor hingga selesai pada tahun 2002.
Pada tahun 2002, penulis melanjutkan pendidikan tinggi di Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB) dan menyelesaikan studinya pada tahun 2007.
Selama masa studinya di Departemen Teknologi Industri Pertanian, penulis aktif terlibat dalam berbagai kegiatan. Penulis aktif menjadi asisten Mata Kuliah Laboratorium Bioproses dan Mata Kuliah Sistem Informasi Manajemen serta menjadi pengurus Himpunan Mahasiswa Teknologi Industri (HIMALOGIN) periode 2003-2004 sebagai staf Departemen Kesekretariatan dan Sebagai Staf Departemen Sosial dan Kesejahteraan Mahasiswa, Badan Eksekutif Mahasiswa Fakultas Teknologi Pertanian periode 2004-2005.
Pada tahun 2005, penulis melakukan praktek lapang di PT. Badranaya Putra Bandung dengan topik “Mempelajari Aspek Proses Produksi dan Pengemasan Produk Sosis di PT. Badranaya Putra Bandung”. Pada tahun 2006 penulis melakukan penelitian di Laboratorium Departemen Teknologi Industri Pertanian dengan judul penelitian “Pengaruh Penambahan Pemlastis Polietilen Glikol 400, Dietilen Glikol, dan Dimetil Ftalat terhadap Proses Biodegradasi Bioplastik Poli- -hidroksialkanoat pada Media Cair dengan Udara Terlimitasi”. Penulis menyelesaikan studinya di Departemen Teknologi Industri Pertanian dan meraih gelar Sarjana Teknologi Pertanian pada bulan Maret 2007.
KATA PENGANTAR
Alhamdulillah, segala puji bagi Allah SWT, karena atas berkat kekuasaan dan rahmat-Nyalah penulis dapat menyelesaikan tugas akhir penulis yang berjudul “Pengaruh Penambahan Pemlastis Polietilen Glikol 400, Dietilen Glikol, dan Dimetil Ftalat terhadap Proses Biodegradasi Bioplastik Poli -hidroksialkanoat pada Media Cair dengan Udara Terlimitasi”.
Selama pelaksanaan penelitian hingga selesainya tugas akhir ini, penulis banyak mendapat bantuan, dorongan, dan bimbingan dari banyak pihak. Karena itu pada kesempatan ini, penulis ingin mengucapkan terima kasih kepada:
1. Dr. Ir. Krisnani Setyowati, selaku dosen pembimbing I yang selama ini telah memberikan arahan, bimbingan dan juga kesabarannya kepada penulis. 2. Dr. Ir. Khaswar Syamsu, M.Sc, selaku dosen pembimbing II atas ide-ide,
masukan, dan saran bagi penulis.
3. Prayoga Suryadarma, S.TP, MT, sebagai dosen penguji atas evaluasi dan saran yang diberikan demi perbaikan tugas akhir ini.
4. Ayah, ibu, serta seluruh keluarga penulis atas dukungan tanpa henti dan cinta tiada batas.
5. Staf pengajar Dept. Teknologi Industri Pertanian, atas semua ilmu yang diberikan selama penulis berada di Departemen Teknologi Industri Pertanian. 6. Rekan-rekan penelitian Riset Unggulan Terpadu Bioplastik 2006 atas
kerjasama, bantuan, dan ikatan persahabatan yang erat.
7. Staf laboratorium Dept. Teknologi Industri Pertanian dan Pusat Antar Universitas IPB atas bantuan dan fasilitas yang diberikan selama penulis melakukan penelitian.
8. Rekan-rekan TIN kelas 2002 (TIN ’39). Terima kasih atas jalinan yang tercipta selama ini.
9. Semua pihak yang telah membantu proses penelitian ini, yang tidak dapat penulis sebutkan satu- persatu.
Semoga karya kecil ini bisa bermanfaat dan memberikan inspirasi bagi siapapun yang membacanya.
Bogor, Maret 2007 Penulis
xi
DAFTAR ISI
LEMBAR PENGESAHAN ... iii
RINGKASAN ... iv
LEMBAR PERNYATAAN ... viii
BIODATA RINGKAS ... ix
KATA PENGANTAR ... x
DAFTAR ISI ... xi
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
I. PENDAHULUAN ... 1
A. LATAR BELAKANG ... 1
B. TUJUAN ... 4
C. RUANG LINGKUP PENELITIAN ... 4
II. TINJAUAN PUSTAKA ... 5
A. POLI- -HIDROKSIALKANOAT (PHA) ... 5
B. PEMLASTIS ... 7
C. BIODEGRADASI ... 9
D. PENGUJIAN BIODEGRADASI ... 12
III. METODE PENELITIAN ... 15
A. BAHAN DAN ALAT ... 15
B. METODE PENELITIAN ... 16
IV. HASIL DAN PEMBAHASAN ... 19
A. KARAKTERISASI MEDIA PENDEGRADASI ... 19
B. UJI BIODEGRADASI BIOPLASTIK POLI- -HIDROKSIALKA- NOAT DENGAN MENGGUNAKAN METODE RESPIROMETRI 22
V. KESIMPULAN DAN SARAN ... 33
A. KESIMPULAN ... 33
B. SARAN ... 34
DAFTAR PUSTAKA ... 35
DAFTAR TABEL
Tabel 1. Sifat fisik dan mekanis polipropilen (PP) dan poli- -hidroksi-
butirat (PHB) ... 6
Tabel 2. Mikroorganisme pendegradasi poli- -hidroksialkanoat ... 9
Tabel 3. Ringkasan beberapa metode uji biodegradasi beserta bebera- pa faktor positif dan negatif untuk setiap jenis uji ... 13
Tabel 4. Hasil kuantifikasi mikroorganisme hari ke-0 ... 19
Tabel 5. Hasil kuantifikasi mikroorganisme hari ke-50 ... 19
Tabel 6. Pengukuran suhu dan pH media pada hari ke-0 ... 21
xiii
DAFTAR GAMBAR
Gambar 1. Struktur dasar poli- -hidroksialkanoat ... 5
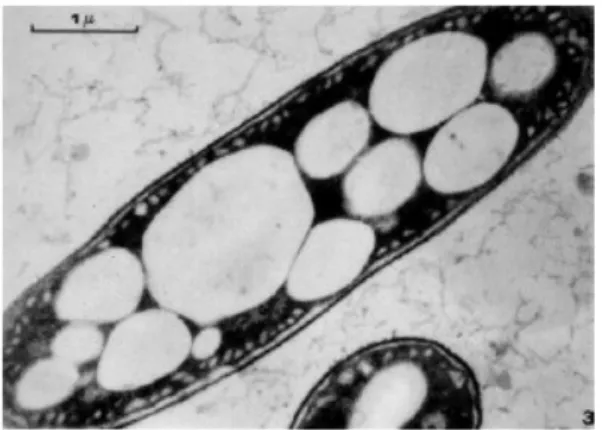
Gambar 2. Granula poli- -hidroksialkanoat di dalam sel ... 6
Gambar 3. Struktur molekul polietilen glikol ... 8
Gambar 4. Struktur molekul dietilen glikol ... 8
Gambar 5. Struktur molekul dimetil ftalat ... 8
Gambar 6. Dogma dasar biodegradasi polimer ... 10
Gambar 7. Reaksi umum pada tahapan mineralisasi ... 12
Gambar 8. Disain botol biometer ... 14
Gambar 9. Disain botol biometer modifikasi... 14
Gambar 10. Biometer ... 15
Gambar 11. Reaksi pada tahapan mineralisasi ... 23
Gambar 12. Grafik akumulasi produksi CO2 selama proses biodegradasi 23 Gambar 13. Kurva regresi produksi CO2 ... 30
DAFTAR LAMPIRAN
Lampiran 1. Diagram alir uji biodegradasi bioplastik poli- -hidroksialka-
noat ... 39 Lampiran 2. Diagram alir evaluasi kadar CO2 ... 40 Lampiran 3. Rekapitulasi pengukuran produksi CO2 blanko (tanpa bio-
plastik poli- -hidroksialkanoat) ... 41 Lampiran 4. Rekapitulasi pengukuran produksi CO2 poli- -hidroksialka-
noat tanpa penambahan pemlastis ... 42 Lampiran 5. Rekapitulasi pengukuran produksi CO2 poli- -hidroksialka-
noat dengan penambahan pemlastis polietilen glikol 400 ... 43 Lampiran 6. Rekapitulasi pengukuran produksi CO2 poli- -hidroksialka-
noat dengan penambahan pemlastis dietilen glikol ... 44 Lampiran 7. Rekapitulasi pengukuran produksi CO2 poli- -hidroksialka-
noat dengan penambahan pemlastis dimetil ftalat ... 45 Lampiran 8. Rekapitulasi gabungan pengukuran produksi CO2 ... 46 Lampiran 9. Estimasi kurva regresi produksi CO2 poli- -hidroksialka-
noat tanpa penambahan pemlastis ... 47 Lampiran 10. Estimasi kurva regresi produksi CO2 poli- -hidroksialka-
noat dengan penambahan pemlastis polietilen glikol 400 .. 48 Lampiran 11. Estimasi kurva regresi produksi CO2 poli- -hidroksialka-
noat dengan penambahan pemlastis dietilen glikol ... 49 Lampiran 12. Estimasi kurva regresi produksi CO2 poli- -hidroksialka-
noat dengan penambahan pemlastis dimetil ftalat ... 50 Lampiran 13. Data perbandingan produksi CO2 dan laju produksi CO2
pada kondisi udara terlimitasi dengan produksi CO2 dan
laju produksi CO2 kondisi aerasi ... 51 Lampiran 14. Bioplastik poli- -hidroksialkanoat dengan penambahan
pemlastis (a) polietilen glikol 400; (b) dietilen glikol; dan
I. PENDAHULUAN
A. LATAR BELAKANG
Saat ini, produksi dan konsumsi berbagai jenis polimer sintetis berbahan dasar minyak bumi di seluruh dunia telah mencapai 140 juta ton/tahun (Kim dan Rhee, 2003; Anonima, 2006). Jumlah tersebut meningkat hingga 20 kali lipat jika dibandingkan dengan produksi polimer sintetis berbahan dasar minyak bumi pada dekade 1950. Sebagian besar polimer yang diproduksi dan dikonsumsi tersebut pada akhirnya akan menjadi limbah industri di lingkungan. Hal ini dikarenakan mayoritas polimer sintetis yang diproduksi merupakan polimer yang memiliki ketahanan terhadap penguraian secara biologis. Hal tersebut disebabkan oleh bobot molekul yang sangat besar, jumlah cincin aromatik yang sangat tinggi, dan ikatan-ikatan yang kompleks. (Kim dan Rhee, 2003). Karena hal tersebut, maka akumulasi skala besar limbah plastik di lingkungan telah menimbulkan masalah polusi lingkungan yang tidak bisa disebut sebagai masalah ringan.
Solusi dari permasalahan ini dapat ditemukan pada polimer biodegradabel, suatu jenis polimer yang dapat terurai secara biologis. Diantara berbagai jenis polimer biodegradabel, terdapat polimer yang dihasilkan oleh mikroorganisme dengan substrat yang diturunkan dari sumber daya yang dapat diperbaharui, seperti pati dan lemak, dan dapat terurai secara biologis pada tanah dan air. Poli- -hidroksialkanoat merupakan salah satu polimer yang dihasilkan oleh mikroorganisme sebagai cadangan makanan akibat adanya keterbatasan nutrisi. Salah satu jenis poli -hidroksialkanoat adalah poli- -hidroksibutirat, yang termasuk ke dalam kelompok poli- -hidroksialkanoat rantai pendek (jumlah atom C berkisar antara 3 sampai 5 atom), dan memiliki sifat yang rapuh dan tidak elastis.
Untuk memperbaiki sifat dan karakter bioplastik poli -hidroksialkanoat tersebut diperlukan penambahan bahan tertentu, seperti pemlastis. Penelitian mengenai pembuatan bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis telah banyak dilakukan. Rais (2007), Delvia (2006), dan Juari (2006) telah melakukan studi tentang pengaruh penambahan pemlastis polietilen glikol 400, dietilen glikol dan dimetil ftalat terhadap sifat fisik dan mekanis bioplastik poli hidroksialkanoat (poli
-hidroksibutirat) hasil kultivasi bakteri Ralstonia eutropha dengan substrat hidrolisat pati sagu. Untuk mengetahui kemampuan terdegradasi ketiga bioplastik tersebut, maka dilakukanlah uji biodegradasi bioplastik poli -hidroksialkanoat yang dihasilkan oleh studi tersebut.
Proses degradasi bioplastik poli- -hidroksialkanoat bergantung pada aktivitas mikrobial di lingkungan dan pada permukaan polimer. Di sisi lain, kristalinitas, bobot molekul dari bahan, temperatur, hidrofilitas bahan merupakan faktor-faktor penting yang mempengaruhi pertumbuhan mikroorganisme pada permukaan polimer.
Polietilen glikol, dietilen glikol dan dimetil ftalat merupakan beberapa jenis pemlastis yang banyak digunakan pada industri plastik. Pemlastis dari kelompok etilen glikol banyak digunakan pada industri plastik terutama untuk pembuatan serat poliester dan resin, termasuk polyethylene terephtalate yang digunakan dalam produksi botol plastik untuk minuman ringan (botol PET). Dimetil ftalat sering digunakan sebagai pemlastis pada industri plastik
polyvinyl chloride (PVC).
Pemlastis dari kelompok etilen glikol telah digunakan sebagai bahan campuran pada beberapa jenis polimer biodegradabel, seperti poly(3-caprolactone) (PCL) dan poly (L-lactide) (PLA). Pemlastis dari kelompok etilen glikol memiliki sifat fisik dan mekanis yang baik, seperti kelarutan yang baik pada air dan pelarut organik, tingkat toksik yang rendah, dan sifat hidrofilik yang tinggi. Sedangkan dimetil ftalat merupakan pemlastis yang dapat larut pada pelarut organik tetapi tidak dapat larut di dalam air. Dimetil ftalat telah banyak digunakan pada industri plastik untuk menghasilkan plastik
polyvinyl chloride (PVC) dengan karakter yang lebih fleksibel dan lentur. Pada studi ini, diamati pengaruh penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat terhadap proses biodegradasi bioplastik poli- -hidroksialkanoat. Parameter yang diamati adalah akumulasi produksi CO2 dan laju produksi CO2 selama pengujian dilakukan. Gas CO2 merupakan gas yang dihasilkan pada tahapan mineralisasi pada proses biodegradasi.
Beberapa studi mengenai biodegradasi bioplastik ataupun polimer sintetis telah dilakukan. Parra et al. (2006) melakukan pengujian biodegradasi bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 300 pada konsentrasi yang berbeda-beda. Pengujian dilakukan dengan
3 menggunakan metode enzyme assay atau pengujian dengan menggunakan enzim pada media agar. Parra et al. (2006) menyatakan, konsentrasi pemlastis polietilen glikol 300 yang berbeda-beda akan memberikan kemampuan terdegradasi yang berbeda. Semakin tinggi konsentrasi polietilen glikol 300, maka bioplastik poli- -hidroksialkanoat semakin mudah dan cepat terdegradasi.
Studi biodegradasi yang dilakukan oleh Parra et al. (2006) tidak melakukan perbandingan antara berbagai macam jenis pemlastis dan perbandingan dengan bioplastik PHA tanpa penambahan pemlastis. Sehingga tidak didapatkan informasi mengenai pengaruh penambahan pemlastis yang berbeda-beda terhadap proses biodegradasi. Maka pada studi biodegradasi kali ini digunakan tiga macam pemlastis yang berbeda, sehingga bisa diketahui pemlastis mana yang memberikan sifat fisik mekanis terbaik bagi bioplastik poli- -hidroksialkanoat dan juga memberikan kemampuan terdegradasi mendekati bioplastik poli- -hidroksialkanoat tanpa pemlastis.
Selain tidak adanya data perbandingan antara berbagai macam jenis pemlastis, studi biodegradasi yang dilakukan oleh Parra et al. (2006) tidak menggunakan media yang berasal dari alam. Sehingga studi yang dilakukan oleh Parra et al. (2006) tidak dapat memberikan informasi mengenai kemampuan bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 300 untuk terdegradasi di alam. Karena itu pada studi ini digunakan media yang dapat mewakili/mendekati kondisi alam dari segi media yang digunakan.
Pada studi ini digunakan media berupa air danau dan inokulum pendegradasi berupa limbah nata de coco yang tidak diberi perlakuan sebelum proses biodegradasi dilakukan. Media berupa air danau dipilih karena diduga mengandung beberapa jenis bakteri yang dapat mendegradasi bioplastik poli- -hidroksialkanoat (Brandl et al., 1995). Sedangkan inokulum pendegradasi berupa limbah cair nata de coco merupakan limbah yang diduga mengandung bakteri penghasil biopolimer, selulosa, sehingga diduga mampu untuk mendegradasi jenis biopolimer yang lain.
B. TUJUAN
Studi ini bertujuan untuk mengetahui pengaruh penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat terhadap kemampuan bioplastik poli- -hidroksialkanoat untuk terdegradasi pada media cair berupa air danau dengan penambahan inokulum pendegradasi berupa limbah cair nata de coco pada kondisi udara terlimitasi, dengan melakukan pengukuran akumulasi produksi CO2 dan laju produksi CO2 sebagai parameter biodegradasi.
C. RUANG LINGKUP PENELITIAN
Melakukan pengujian biodegradasi terhadap bioplastik poli -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat dengan menggunakan metode respirometri untuk mengetahui jumlah CO2 hasil tahapan mineralisasi pada proses biodegradasi sebagai parameter biodegradasi. Sebagai data pelengkap penelitian utama dilakukan karakterisasi media berupa pengukuran pH media dan kuantifikasi mikroorganisme pada hari ke-0 dan hari ke-50 proses biodegradasi.
II. TINJAUAN PUSTAKA
A. POLI- -HIDROKSIALKANOAT (PHA)
Poli- -hidroksialkanoat mikrobial merupakan poliester alifatik atau kopolimer dari asam [R]- -hidroksialkanoat, yang terbentuk selama fase pertumbuhan dengan nutrisi terbatas pada berbagai jenis sumber karbon termasuk gula (Kaplan et al. dalam Ching et al., 1993). Sedangkan menurut Jendrossek dan Handrick (2002), poli- -hidroksialkanoat merupakan kumpulan simpanan karbon dan energi yang terakumulasi selama fase pertumbuhan tidak seimbang pada banyak jenis bakteri, sebagai contohnya pada keadaan dimana terjadi kelebihan karbon dan pertumbuhan terlimitasi oleh adanya nutrien lain (contohnya, nitrogen). Struktur dasar poli -hidroksialkanoat dapat dilihat pada Gambar 1.
n = 1 R = Hydrogen Poly (-3-hydroxypropionate) Methyl Poly (-3-hydroxybutyrate) Ethyl Poly (-3-hydroxyvalerate) Propyl Poly (-3-hydroxyhexanoate) Pentyl Poly (-3-hydroxyoctanoate) Nonyl Poly (-3-hydroxydecanoate) n = 2 R = Hydrogen Poly (-4-hydroxybutyrate) n = 3 R = Hydrogen Poly (-5-hydroxyvalerate)
Gambar 1. Struktur dasar poli- -hidroksialkanoat (Ojumu et al., 2004) Poli- -hidroksialkanoat disimpan di dalam sel (intraseluler) dalam bentuk granula yang terlihat sebagai globula-globula cemerlang berukuran 100-500 nm dan dapat mencapai bobot 90% dari bobot sel kering. Gambar 2 merupakan gambar granula poli- -hidroksialkanoat di dalam sel.
Poli hidroksialkanoat terbagi menjadi tiga kelas, yaitu poli -hidroksialkanoat rantai pendek (sclPHA, C3 - C5), poli- --hidroksialkanoat rantai sedang (mclPHA, C6 - C14), dan poli- -hidroksialkanoat rantai panjang (lclPHA, > C14). (Zinn et al., 2001). Salah satu jenis poli- -hidroksialkanoat yang sering ditemukan dan digunakan adalah poli- -hidroksibutirat, yang termasuk ke dalam poli- -hidroksialkanoat rantai pendek.
Gambar 2. Granula poli- -hidroksialkanoat di dalam sel (Lenz dan Marches-sault, 2005)
Atifah (2006) telah melakukan penelitian untuk memproduksi poli -hidroksialkanoat melalui kultivasi batch dan fed-batch dengan bakteri
Ralstonia eutropha. Pada penelitian tersebut digunakan sumber karbon dari hidrolisat pati sagu dengan nitrogen sebagai substrat pembatas. Atifah (2006) menyatakan bahwa kultivasi fed-batch dengan bakteri Ralstonia eutropha dan sumber karbon hidrolisat pati sagu akan menghasilkan poli- -hidroksialkanoat jenis poli- -hidroksibutirat.
Poli- -hidroksibutirat memiliki sifat fisik dan mekanis yang baik. Sifat fisik dan mekanis poli- -hidroksibutirat tersebut merupakan sifat yang dapat dibandingkan dengan polipropilen, plastik sintetis berbahan dasar minyak bumi. Sifat fisik dan mekanis polipropilen dan poli- -hidroksibutirat dapat dilihat pada Tabel 1.
Tabel 1. Sifat fisik dan mekanis polipropilen (PP) dan poli- -hidroksibutirat (PHB) (Timmins et al. dalam Ching et al., 1993).
Parameter PP PHB
Titik leleh, oC 171-186 171-182
Temperatur transisi gelas, oC -15 5-10
Kristalinitas, % 65-70 65-80
Densitas, g/cm3 0,905-0,94 1,23-1,25
Bobot molekul rata-rata, x 10-5 2.2-7.0 1-8
Modulus kelenturan, Gpa 1,7 3,5-4,0
Kuat tarik, Mpa 39 40
Perpanjangan putus, % 400 6-8
Ketahanan terhadap UV Buruk Baik
Ketahanan terhadap pelarut Baik Buruk
Permeabilitas oksigen, cm3/m2/atm/d 1700 45
7 B. PEMLASTIS
Di samping sifat-sifatnya yang dapat dibandingkan dengan polipropilen, poli- -hidroksibutirat memiliki derajat kristalinitas yang tinggi dan sifat yang kaku, sehingga membatasi aplikasinya pada berbagai bidang. (Choi dan Lee, 1999). Untuk dapat diaplikasikan secara luas, diperlukan penambahan bahan tertentu seperti pemlastis untuk memperbaiki sifat poli -hidroksibutirat tersebut.
Pemlastis adalah bahan kimia yang dapat digunakan untuk mengurangi kekakuan resin termoplastik. Prinsip kerja pemlastis adalah membentuk interaksi molekuler rantai polimer untuk meningkatkan kecepatan respon viskoelastis pada polimer. Hal tersebut akan meningkatkan mobilitas molekuler rantai polimer dan akibatnya dapat menurunkan suhu transisi kaca (Tg) (Hammer, 1978). Ikatan-ikatan yang terbentuk antara polimer dengan pemlastis diduga merupakan ikatan hidrogen (Spink dan Waychoff, 1958).
Polietilen glikol, dietilen glikol dan dimetil ftalat merupakan beberapa jenis pemlastis yang banyak digunakan pada industri plastik. Pemlastis dari kelompok etilen glikol banyak digunakan pada industri plastik terutama untuk pembuatan serat poliester dan resin, termasuk polyethylene terephtalate yang digunakan dalam produksi botol plastik untuk minuman ringan (botol PET) (Anonimb, 2006). Dimetil ftalat sering digunakan sebagai pemlastis pada industri plastik polyvinyl chloride (PVC) untuk menghasilkan plastik polyvinyl chloride yang lebih lentur dan fleksibel (Anonimc, 2006).
Polietilen glikol merupakan golongan senyawa polieter dari etilen oksida. Rumus umum polietilen glikol adalah C2nH4n+2On+1 dengan bobot molekul rata-rata sesuai dengan angka yang tertera setelahnya. Polietilen glikol 400, memiliki bobot molekul rata-rata 400 g/mol atau berkisar antara 380-420 g/mol. Menurut Parra et al. (2006), polietilen glikol memiliki sifat-sifat yang baik, termasuk kelarutan yang baik di dalam air dan pelarut organik, sifat toksik yang rendah, tidak bersifat antigen dan imunogen, serta bersifat hidrofilik atau mudah berikatan dengan air. Polietilen glikol biasa digunakan sebagai emulsifier, bahan tambahan deterjen, pemlastis, humektan, dan pelumas larut air untuk melapisi tekstil (Anonimd, 2006).
Bobot molekul polietilen glikol dapat dihitung dengan menggunakan rumus BM = 44n+18 g/mol. Dari rumus tersebut dapat diperkirakan berapa nilai n dari suatu molekul polietilen glikol. Nilai n dari polietilen glikol 400
dengan rumus tersebut dapat diketahui antara 8,23-9,14 atau n = 9. Sehingga rumus molekul polietilen glikol 400 adalah C18H38O10 dan bobot molekulnya 414 g/mol. Dengan n = 9 maka dapat dikatakan bahwa polietilen glikol 400 merupakan suatu oligomer dari etilen oksida. Struktur molekul polietilen glikol dapat dilihat pada Gambar 3.
Gambar 3. Struktur molekul polietilen glikol (Anonimd, 2006)
Dietilen glikol (HO-CH2-CH2-O-CH2-CH2-OH) merupakan senyawa yang tidak berwarna, hampir tidak berbau, higroskopis dan memiliki rasa manis yang tajam dengan titik didih 244-245 oC. Dietilen glikol dapat bercampur dengan air, alkohol, eter, aseton, etilen glikol dan tidak dapat bercampur dengan karbon tetraklorida, benzene dan toluen (Anonime, 1999). Dietilen glikol memiliki rumus molekul C4H10O3 dan bobot molekul 106,12 g/mol. Struktur molekul dietilen glikol dapat dilihat pada Gambar 4.
Gambar 4. Struktur molekul dietilen glikol (Anonimb, 2006)
Dimetil ftalat merupakan pemlastis yang bersifat dapat larut dalam alkohol, eter, dan kloroform, tetapi tidak dapat larut dalam air. Penampakan dimetil ftalat adalah tidak berwarna dan tidak berbau. Struktur kimia dimetil ftalat dapat dilihat pada Gambar 5. Dimetil ftalat memiliki rumus molekul C6H4(COOH)2 dengan bobot molekul 166,14 g/mol.
9 C. BIODEGRADASI
Biodegradasi didefinisikan sebagai suatu proses yang dilakukan oleh sebuah sistem biologis (oleh bakteri atau fungi) dimana suatu rantai polimer diputus melalui aktivitas enzimatis (Kaplan et al. dalam Ching et al., 1993). Biodegradasi juga dapat didefinisikan sebagai penyederhanaan sebagian atau penghancuran total struktur molekul suatu bahan oleh suatu reaksi fisiologis yang dikatalis oleh mikroorganisme (Madsen dalam Hurst et al., 1997).
Terdapat beberapa faktor penting yang dapat mempengaruhi biodegradasi suatu bahan. Faktor-faktor tersebut antara lain: (1) aktivitas mikrobial pada lingkungan (media) dan pada permukaan bahan/sampel (aksesibilitas pada permukaan polimer); (2) kristalinitas; (3) bobot molekul bahan/sampel; (4) temperatur media (akan berpengaruh pada pertumbuhan mikroorganisme); (5) pH; (6) komposisi monomerik; (7) titik leleh; dan (8) hidrofilitas pemlastis pada sampel (Jendrossek dan Handrick, 2002; Tokiwa dan Calabia, 2004; Parra et al., 2006).
Mikroorganisme memegang peranan penting dalam proses biodegradasi. Menurut Brandl et al. (1995), terdapat berbagai jenis mikroorganisme pada berbagai macam ekosistem yang dapat mendegradasi poli- -hidroksialkanoat, seperti ditunjukkan pada Tabel 2.
Tabel 2. Mikroorganisme pendegradasi poli- -hidroksialkanoat (Brandl et al., 1995).
Ekosistem Organisme
Tanah dan Kompos Acidovorax delafieldii; Acremonium sp; Acidovorax facilis;
Arthrobacter viscosus; Aspergilus fumigatus; Bacillus polymyxa; Cephalosporium sp; Cladosporium sp;
Cytophaga johnsonae; Eupenicillium sp; Mucor sp;
Paecilomyces marquandii; Penicillium adametzii; Penicillium chermisinum; Penicillium daleae; Penicillium funicolosum;
Penicillium ochlochloron; Penicillium resrictum; Poliporus circinatus; Pseudomonas sp; Pseudomonas lemoignei;
Pseudomonas syringae; Xanthomonas monophilia; Zooglea ramigera; Aspergillus sp; Bacillus megaterium; Penicillium simplicissimum; Streptomyces sp; Variovorax paradoxus;
Verticillium leptobactrum.
Lumpur Alcaligenes faecialis.
Sedimen estuaria Ilyobacter delafieldii.
Air danau Comamonas acidovorans; Pseudomonas cepacia;
Pseudomonas stutzeri; Pseudomonas vesicularis.
Air laut Comamonas testoteroni.
Selain mikroorganisme, sifat pemlastis memberikan pengaruh yang signifikan pada proses biodegradasi. Pemlastis hidrofilik akan meningkatkan laju biodegradasi, dan penambahan konsentrasi pemlastis hidrofilik akan meningkatkan laju degradasi enzimatis (Parra et al., 2006). Polietilen glikol 400 dan dietilen glikol merupakan pemlastis hidrofilik akibat adanya gugus hidroksil (-OH) pada molekul-molekulnya. Selain dari gugus hidroksil (-OH) kemampuan mengikat air pada polietilen glikol 400 dan dietilen glikol diduga terjadi melalui ikatan hidrogen pada gugus O yang terdapat pada molekul polietilen glikol 400 dan dietilen glikol (Israelachvili, 1997). Dimetil ftalat merupakan pemlastis yang memiliki kelarutan yang buruk pada air karena sifatnya yang non-polar. Sehingga dapat dikatakan, dimetil ftalat merupakan pemlastis yang hidrofobik (Anonimc, 2006).
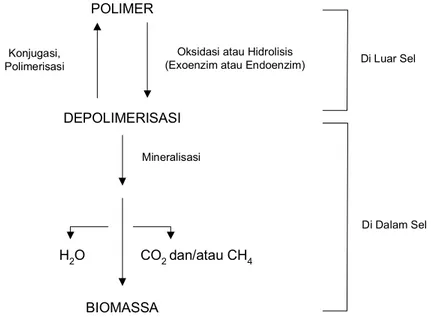
Pada proses biodegradasi biopolimer, terdapat dua tahapan kunci yang terjadi. Pertama, tahapan depolimerisasi dan kedua, tahapan mineralisasi. Gambar 6 menunjukkan dogma dasar biodegradasi sebuah polimer, dimana dua tahapan kunci terjadi pada proses tersebut.
!" !"# $ %& '
"
"
Gambar 6. Dogma dasar biodegradasi polimer (Kaplan et al. dalam Ching et al., 1993).
Proses depolimerisasi merupakan proses dimana rantai-rantai polimer diputus melalui reaksi enzimatis. Enzim ekstraseluler bertanggungjawab atas tahapan tersebut, bertindak secara endo (pemecahan secara acak unit monomer terminal pada rantai polimer utama) ataupun ekso (pemecahan
11 secara berurutan unit monomer terminal pada rantai polimer utama) (Kaplan
et al. dalam Ching et al., 1993).
Proses degradasi mikrobial poli- -hidroksialkanoat berlangsung akibat adanya erosi enzimatis pada permukaan polimer yang merubahnya menjadi monomer dan/atau oligomer yang larut air. Enzim yang berfungsi sebagai pemecah ikatan polimer poli- -hidroksialkanoat adalah PHA-depolimerase ekstraseluler.
PHA-depolimerase dikenal dengan nama PHB-depolimerase pada tata nama dan klasifikasi enzim, serta memiliki nama sistematis poly[(R)-3-hydroxybutyrate] hydrolase. Enzim tersebut memiliki nomor klasifikasi enzim EC 3.1.1.75. Pernyataan Komisi Enzim (Enzyme Comission) pada tahun 1961 di dalam Moss (2004) menyatakan, ada empat elemen dalam tata cara penamaan enzim, keempat elemen tersebut adalah tata cara penyusunan angka-angka dan maknanya dalam penamaan enzim dengan sistem EC. Keempat elemen tersebut adalah:
1. Nomor pertama menunjukkan nomor kelas dari enam kelas utama enzim, 2. Nomor kedua menunjukkan subkelas enzim tersebut,
3. Nomor ketiga menunjukkan sub-subkelas enzim tersebut,
4. Nomor keempat merupakan nomor seri dari enzim tersebut pada sub-subkelas.
Semua nama enzim dalam tata nama enzim Enzyme Comission, selalu diawali oleh EC sebelum angka-angka klasifikasinya.
Merujuk pada tata cara penamaan enzim menurut Enzyme Comission
tersebut, maka PHA-depolimerase/PHB-depolimerase berada pada kelas utama enzim hidrolase, subkelas enzim pemecah ikatan ester (esterase), sub-subkelas enzim penghidrolisis ester karboksilat (carboxylic ester hydrolases) (Anonimf, 2001).
Tahapan kedua setelah proses depolimerisasi adalah mineralisasi. Setelah monomer dan oligomer yang berukuran lebih kecil terbentuk pada tahapan depolimerisasi, monomer dan oligomer-oligomer tersebut ditransfer ke dalam sel dimana oligomer tersebut dimineralisasi. Mineralisasi merupakan proses konversi polimer menjadi biomassa, mineral dan garam-garaman, air, dan gas seperti CO2, CH4, dan N2 (Kaplan et al. dalam Ching et al., 1993). Proses mineralisasi pada kondisi aerobik melibatkan proses reaksi oksidasi dengan O2 bertindak sebagai oksidator (Fardiaz, 1992; Narayan,
2006). Reaksi yang terjadi pada tahapan mineralisasi dapat dilihat pada gambar 7:
Gambar 7. Reaksi umum pada tahapan mineralisasi (Narayan, 2006)
D. PENGUJIAN BIODEGRADASI
Ada beberapa cara sederhana menurut Albertsson dalam Hamid (2000) untuk menguji dan mengamati kemampuan suatu bahan untuk terdegradasi, diantaranya:
1. Pengamatan visual pertumbuhan miselium pada permukaan polimer. 2. Estimasi kuantitatif pertumbuhan mikroorganisme.
3. Estimasi kuantitatif pengurangan bobot polimer.
4. Pengukuran dari perubahan sifat polimer, seperti perubahan bobot molekul, perubahan gugus fungsi, kristalinitas, kuat tarik, atau kombinasi dari hal-hal tersebut.
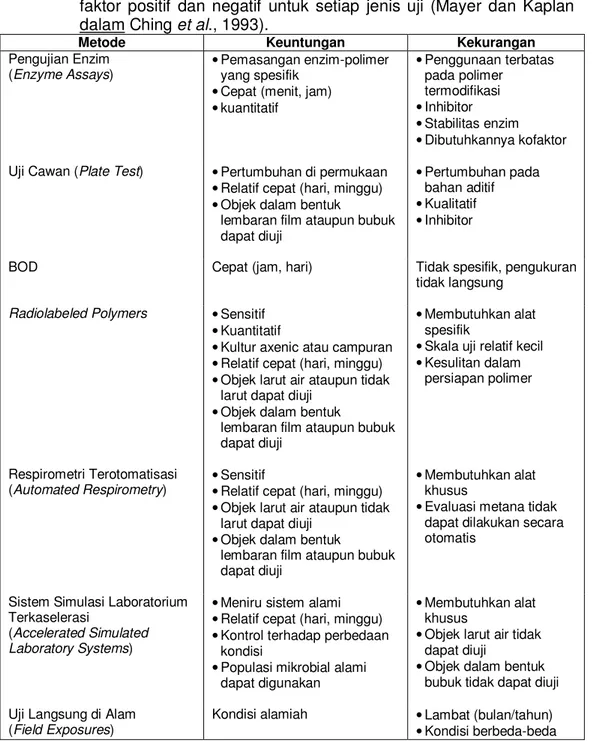
Selain cara-cara sederhana tersebut, terdapat beberapa cara dan metode yang lebih baik serta lebih kompleks untuk melakukan uji biodegradasi. Beberapa cara dan metode tersebut dijabarkan pada Tabel 3, beserta kelebihan dan kekurangannya.
Salah satu metode yang umum digunakan dalam uji biodegradasi adalah metode respirometri. Menurut Mayer dan Kaplan dalam Ching et al. (1993), metode respirometri, terutama dengan sistem yang terotomatisasi, memberikan pendekatan yang lebih praktis dan sensitif pada pengujian mineralisasi. Andrady dalam Hamid (2000), menggunakan metode respirometri untuk melakukan pengujian biodegradasi polimer. Pengujian tersebut dilakukan dengan menggunakan botol biometer (juga disebut biometer) yang berisi polimer yang diketahui massanya, media biotik (biasanya tanah yang diinokulasi dengan kultur mikroorganisme), dan larutan alkali untuk mengikat gas yang dihasilkan selama proses. Larutan alkali diganti secara periodik dan dititrasi dengan menggunakan larutan asam untuk memperkirakan jumlah CO2 yang diserap oleh larutan alkali tersebut. Perlu diperhatikan, bahwa evaluasi kadar CO2 perlu dilakukan sebelum larutan
13 alkali berubah menjadi netral. Karena itu, titrasi setiap hari diperlukan untuk mengetahui jumlah CO2 yang terserap larutan alkali.
Tabel 3. Ringkasan beberapa metode uji biodegradasi beserta beberapa faktor positif dan negatif untuk setiap jenis uji (Mayer dan Kaplan dalam Ching et al., 1993).
Metode Keuntungan Kekurangan
Pengujian Enzim
(Enzyme Assays) • Pemasangan enzim-polimer yang spesifik
• Cepat (menit, jam)
• kuantitatif • Penggunaan terbatas pada polimer termodifikasi • Inhibitor • Stabilitas enzim • Dibutuhkannya kofaktor
Uji Cawan (Plate Test) • Pertumbuhan di permukaan
• Relatif cepat (hari, minggu)
• Objek dalam bentuk
lembaran film ataupun bubuk dapat diuji
• Pertumbuhan pada
bahan aditif
• Kualitatif
• Inhibitor
BOD Cepat (jam, hari) Tidak spesifik, pengukuran
tidak langsung
Radiolabeled Polymers • Sensitif
• Kuantitatif
• Kultur axenic atau campuran
• Relatif cepat (hari, minggu)
• Objek larut air ataupun tidak
larut dapat diuji
• Objek dalam bentuk
lembaran film ataupun bubuk dapat diuji
• Membutuhkan alat
spesifik
• Skala uji relatif kecil
• Kesulitan dalam
persiapan polimer
Respirometri Terotomatisasi
(Automated Respirometry) •• Sensitif Relatif cepat (hari, minggu)
• Objek larut air ataupun tidak
larut dapat diuji
• Objek dalam bentuk
lembaran film ataupun bubuk dapat diuji
• Membutuhkan alat
khusus
• Evaluasi metana tidak
dapat dilakukan secara otomatis
Sistem Simulasi Laboratorium Terkaselerasi
(Accelerated Simulated Laboratory Systems)
• Meniru sistem alami
• Relatif cepat (hari, minggu)
• Kontrol terhadap perbedaan
kondisi
• Populasi mikrobial alami
dapat digunakan
• Membutuhkan alat
khusus
• Objek larut air tidak
dapat diuji
• Objek dalam bentuk
bubuk tidak dapat diuji Uji Langsung di Alam
(Field Exposures) Kondisi alamiah •• Lambat (bulan/tahun) Kondisi berbeda-beda
Gambar 8 merupakan botol biometer yang digunakan oleh Andrady dalam Hamid (2000) dalam melakukan pengujian biodegradasi.
( )*+ ( "
Gambar 8. Disain botol biometer (Andrady dalam Hamid, 2000). Dari Gambar 8, dilakukan modifikasi biometer sehingga dapat digunakan sesuai dengan kebutuhan dan perlakuan-perlakuan tertentu. Disain biometer tersebut dapat dilihat pada Gambar 9.
Gambar 9. Disain botol biometer modifikasi dari biometer Andrady dalam Hamid (2000).
III. METODE PENELITIAN
A. BAHAN DAN ALAT
Bahan-bahan yang digunakan dalam penelitian ini adalah bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400, bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dietilen glikol, dan bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dimetil ftalat. Sebagai pembanding, digunakan bioplastik poli -hidroksialkanoat tanpa penambahan pemlastis. Media cair yang digunakan merupakan air danau LSI – IPB dengan penambahan inokulum pendegradasi berupa limbah cair industri nata de coco. Bahan-bahan kimia yang digunakan, antara lain larutan NaOH 0,1 N, larutan HCl 0,1 N sebagai titran, indikator
phenolphtalein (PP), indikator metil jingga, dan urea serta K2HPO4 sebagai sumber nitrogen dan sumber fosfor. Bahan lain yang digunakan adalah aquadest dan nutrient agar yang digunakan pada proses kuantifikasi mikroorganisme.
Peralatan yang digunakan pada penelitian ini antara lain, biometer hasil modifikasi yang mengacu pada Andrary dalam Hamid (2000), peralatan gelas (gelas piala, erlenmeyer, pipet tetes, tabung ulir, cawan petri); peralatan ukur (pipet mohr, gelas ukur, buret, neraca, pH meter, dan colony counter). Peralatan lain yang digunakan adalah rotary shaker incubator. Biometer yang digunakan dalam penelitian ini dapat dilihat pada Gambar 10.
Proses kuantifikasi grafik dilakukan dengan menggunakan perangkat lunak SPSS 13 dan Microsoft Office Excel 2003.
B. METODE PENELITIAN
Penelitian ini dibagi menjadi dua tahap, yaitu tahap karakterisasi media dan tahap uji biodegradasi dengan menggunakan metode respirometri. a. Karakterisasi Media
Karakterisasi media pada penelitian ini dilakukan untuk mengetahui karakter media yang akan digunakan pada proses biodegradasi, dan perubahan apa yang terjadi setelah uji biodegradasi selesai dilakukan. Karakterisasi media yang dilakukan pada penelitian ini adalah kuantifikasi mikroorganisme dengan metode total plate count
(TPC) dan pengukuran pH media. Karakterisasi dilakukan pada hari ke-0 dan hari ke-50 uji biodegradasi.
i. Total Plate Count
Total Plate Count (TPC) dilakukan untuk mengetahui jumlah bakteri yang terdapat pada media biodegradasi. Sebanyak 1 mL sampel dimasukkan ke dalam cawan petri, kemudian nutrient agar dituangkan ke dalam cawan petri yang sudah berisi sampel. Proses inkubasi berlangsung selama 2 x 24 jam pada suhu 36,5 oC. Setelah proses inkubasi selesai dilakukan penghitungan jumlah koloni mikroorganisme. ii. Pengukuran pH
Sampel sebanyak 10 mL diukur dengan menggunakan pH meter, dengan terlebih dahulu dilakukan standarisasi dengan buffer pH 4,0 dan 7,0. pengukuran sampel dilakukan dengan mencelupkan elektroda pH meter ke dalam sampel dan skala dibaca setelah angka konstan. b. Uji Biodegradasi dengan Menggunakan Metode Respirometri
Pengujian biodegradasi bioplastik poli- -hidroksialkanoat dilakukan dengan menggunakan medium air danau LSI – IPB yang dicampur inokulum pendegradasi berupa limbah cair industri nata de coco
dalam biometer yang dibuat dari botol yang dimodifikasi. Ke dalam media di botol pertama, ditambahkan urea dan K2HPO4 sebagai sumber nitrogen
17 dan fosfor dengan konsentrasi 0,1% dan 0,05% dari bobot bioplastik
poli--hidroksialkanoat.
Perbandingan antara bahan aktif berupa limbah nata de coco
dengan air danau adalah 1:10 (10 mL:100 mL). Sampel bioplastik yang akan diuji masing-masing berbobot 0,1 g, diperkecil ukurannya kemudian dicampurkan secara merata ke dalam media yang sudah disiapkan. Digunakan blanko, berupa media pendegradasi tanpa bioplastik sebagai kontrol atau faktor koreksi dari media pendegradasi yang berisi sampel bioplastik poli- -hidroksialkanoat.
Selama proses degradasi berlangsung, dilakukan pembatasan udara yang masuk ke dalam botol berisi media, sehingga udara yang tersedia hanyalah yang terdapat pada ruang kosong botol di atas permukaan media. Pengamatan biodegradasi bioplastik poli -hidroksialkanoat dilakukan dengan mengukur gas CO2 yang diproduksi sebagai hasil mineralisasi polimer sebagai salah satu aktivitas mikroorganisme dalam proses biodegradasi bioplastik poli -hidroksialkanoat.
Larutan NaOH 0,1 N dengan volume 50 mL ditempatkan pada botol kedua. Selama proses biodegradasi berlangsung akan dihasilkan gas CO2 yang akan terlarut dalam NaOH. Jumlah gas CO2 yang bereaksi dapat ditentukan melalui titrasi dengan larutan asam klorida standar (HCl 0,1 N). Larutan NaOH yang telah mengandung CO2 terlarut ditetesi dengan indikator phenolphtalein (PP) dan dititrasi sampai larutan tidak berwarna. Titrasi ke dua dilanjutkan dengan menggunakan indikator metil jingga hingga larutan berwarna merah muda. Titrasi kedua berhubungan dengan jumlah CO2 yang terdapat dalam larutan NaOH.
Jumlah CO2 yang dihasilkan dalam biometer dikoreksi terhadap blanko. Larutan NaOH pada botol kedua diganti secara berkala setiap 2 hari untuk pengujian kadar CO2 dengan lama waktu pengujian dilakukan selama periode 50 hari. Dari hasil tersebut diperoleh grafik hubungan antara mineralisasi dan waktu.
Dilakukan kuantifikasi grafik untuk menjadi suatu persamaan matematik, sehingga perbandingan antara masing-masing nilai pada grafik tidak hanya dilakukan secara kualitatif namun juga secara kuantitatif. Proses pengkuantifikasian grafik dilakukan dengan cara
mencari persamaan regresi yang sesuai dengan masing-masing garis grafik produksi CO2. Persamaan regresi hanya berlaku untuk periode pengujian yang telah dilakukan, yaitu hingga hari ke-50.
Penentuan jenis regresi dilakukan dengan metode curve estimation/curve fit yang terdapat pada perangkat lunak SPSS 13 terhadap tiap-tiap jenis kurva yang mungkin dapat digunakan, seperti regresi logaritmik, power, growth, dan eksponensial, sehingga diketahui bahwa pola degradasi dari bahan yang diuji mengikuti persamaan kurva yang paling sesuai. Untuk menentukan kurva regresi mana yang paling sesuai dengan data yang disajikan, digunakan dua faktor yang dijadikan pertimbangan. Kedua faktor tersebut adalah (1) nilai R2 masing-masing kurva; (2) nilai standard error masing-masing kurva.
IV. HASIL DAN PEMBAHASAN
A. KARAKTERISASI MEDIA PENDEGRADASI
Di antara beberapa faktor yang mendukung proses biodegradasi adalah sifat fisik media pendegradasi dan kandungan mikroorganisme di dalam media pendegradasi. Karena itu perlu dilakukan karakterisasi media, yang di dalamnya meliputi kuantifikasi mikroorganisme yang terdapat pada media dan pengukuran pH serta suhu media. Hasil kuantifikasi mikroorganisme pada hari ke-0 dan hari ke-50 proses biodegradasi dapat dilihat pada pada Tabel 4 dan Tabel 5.
Tabel 4. Hasil kuantifikasi mikroorganisme hari ke-0.
Sampel Total Koloni (koloni/mL)
Media mengandung bioplastik PHA
tanpa penambahan pemlastis 51,25 x 106
Media mengandung bioplastik PHA
dengan penambahan pemlastis polietilen glikol 400 51,25 x 106 Media mengandung bioplastik PHA
dengan penambahan pemlastis dietilen glikol 51,25 x 106 Media mengandung bioplastik PHA
dengan penambahan pemlastis dimetil ftalat 51,25 x 106
Media blanko 51,25 x 106
Tabel 5. Hasil kuantifikasi mikroorganisme hari ke-50.
Sampel Total Koloni (koloni/mL)
Media mengandung bioplastik PHA
tanpa penambahan pemlastis 116,05 x 106
Media mengandung bioplastik PHA
dengan penambahan pemlastis polietilen glikol 400 55,55 x 106 Media mengandung bioplastik PHA
dengan penambahan pemlastis dietilen glikol 56,95 x 106 Media mengandung bioplastik PHA
dengan penambahan pemlastis dimetil ftalat 63,60 x 106
Perhitungan mikroorganisme pada awal pengujian biodegradasi dilakukan untuk mengetahui bahwa di dalam media terdapat sejumlah mikroorganisme yang diduga dapat mendegradasi bioplastik yang terdapat dalam media. Dalam jangka waktu 50 hari pengujian biodegradasi berlangsung, dapat dilihat pada Tabel 5, telah terjadi pertumbuhan mikroorganisme. Hal ini menandakan bahwa mikroorganisme telah menggunakan sumber nutrisi yang terdapat dalam media untuk pertumbuhannya. Sumber nutrisi yang terdapat pada media antara lain urea sebagai sumber N, K2HPO4 sebagai sumber fosfor; dan bioplastik poli -hidroksialkanoat sebagai sumber karbon. Pertumbuhan mikroorganisme ini juga membuktikan bahwa proses biodegradasi telah terjadi. Bioplastik poli -hidroksialkanoat sebagai salah satu sumber nutrisi telah didegradasi untuk kemudian dikonversi menjadi sumber nutrisi berupa karbon bebas. Pertumbuhan mikroorganisme ini juga bisa dikaitkan dengan produksi CO2. Dengan adanya pertumbuhan mikroorganisme ini, maka dapat dikatakan bahwa gas CO2 yang dihasilkan selama proses biodegradasi merupakan hasil dari metabolisme mikroorganisme.
Tabel 5 menunjukkan bahwa, pada hari ke-50 proses biodegradasi jumlah mikroorganisme terbanyak terdapat pada media blanko, diikuti dengan media mengandung bioplastik poli- -hidroksialkanoat tanpa penambahan pemlastis, media mengandung bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400, media mengandung bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dietilen glikol, dan media mengandung bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dimetil ftalat. Data ini menunjukkan ketidaksesuaian dengan data produksi CO2, khususnya pada data bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis. Bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400 memiliki akumulasi produksi CO2 tertinggi dan laju produksi CO2 tercepat, diikuti oleh bioplastik poli -hidroksialkanoat dengan penambahan pemlastis dietilen glikol, dan bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dimetil ftalat. Ketidaksesuaian ini diduga karena tidak semua mikroorganisme di dalam media mampu/merupakan mikroorganisme pendegradasi bioplastik poli -hidroksialkanoat.
21 Media yang digunakan dalam uji biodegradasi bioplastik ini adalah media air danau dengan penambahan limbah cair industri nata de coco
sebagai bahan aktif. Air danau mengandung beberapa jenis bakteri dari genus Comamonas dan Pseudomonas (famili Pseudomonadaceae) yang dapat mendegradasi secara biologis bioplastik poli- -hidroksialkanoat. Beberapa diantaranya adalah Comamonas acidovorans; Pseudomonas cepacia; Pseudomonas stutzeri; Pseudomonas vesicularis (Brandl et al., 1995). Terdapat kemungkinan bahwa masih ada jenis bakteri lain yang hidup di dalam media, tetapi bukan dari jenis yang mampu untuk mendegradasi bioplastik poli- -hidroksialkanoat.
Pada Tabel 6 dan Tabel 7 dapat dilihat bahwa pertumbuhan mikroorganisme selama proses biodegradasi berlangsung tidaklah signifikan. Pertumbuhan yang tidak signifikan ini diduga karena pembatasan udara pada media, sehingga menghambat proses metabolisme mikroorganisme. Mikroorganisme dari famili Pseudomonadaceae merupakan mikroorganisme aerobik yang membutuhkan O2 untuk metabolismenya (Fardiaz, 1992). Pembatasan faktor ini memberikan pengaruh berupa kecilnya nilai pertumbuhan mikroorganisme selama proses biodegradasi berlangsung.
Selain melakukan kuantifikasi mikroorganisme, pengujian sifat fisik dan kimia media juga dilakukan. Pengujian tersebut meliputi pengukuran suhu dan pH media. Pengukuran suhu dan pH media dilakukan pada hari ke-0 proses biodegradasi dan hari ke-5ke-0. Hasil pengukuran suhu dan pH disajikan pada Tabel 6 dan Tabel 7.
Tabel 6. Pengukuran suhu dan pH media pada hari ke-0.
Parameter Air Danau Limbah Campuran
Suhu (oC) 28 27 28
pH 6,24 3,55 3,24
Tabel 7. Pengukuran suhu dan pH media pada hari ke-50.
Sampel Suhu (oC) pH
Media mengandung bioplastik PHA
tanpa penambahan pemlastis 28 7,97
Media mengandung bioplastik PHA
dengan penambahan pemlastis polietilen glikol 400 28 7,62
Media mengandung bioplastik PHA
dengan penambahan pemlastis dietilen glikol 28 7,77
Media mengandung bioplastik PHA
dengan penambahan pemlastis dimetil ftalat 28 7,42
Pada Tabel 6 dan 7 dapat dilihat bahwa rentang suhu media berada pada kisaran 27-28 oC. Bakteri dari famili Pseudomonadaceae (termasuk di dalamnya genus Pseudomonas dan Acetobacter) memiliki kisaran suhu optimum pertumbuhan antara 20-30 oC. Suhu media pada awal dan akhir proses biodegradasi berada pada kisaran suhu yang baik bagi pertumbuhan bakteri-bakteri tersebut, sehingga memungkinkan pertumbuhan bakteri secara optimum selama proses biodegradasi berlangsung (Fardiaz, 1992),.
Selama proses biodegradasi, terjadi perubahan pH (derajat keasaman) yang cukup signifikan. Pada Tabel 6 dan 7 dapat dilihat bahwa media berubah sifat dari asam menjadi basa. Pada awal proses biodegradasi (H0), pH media (campuran antara limbah dengan air danau) berada pada pH 3,24. Sifat asam media tersebut disebabkan oleh sifat asam limbah nata de coco yang menjadi bahan aktif dalam media. Sifat asam limbah cair industri
nata de coco disebabkan oleh kandungan asam asetat dalam limbah yang dihasilkan oleh Acetobacter xylinum selama proses produksi nata de coco. Menurut Anonimg (2006), Acetobacter merupakan genus bakteri asam asetat yang terkarakterisasi oleh kemampuannya dalam mengkonversi alkohol (etanol) menjadi asam asetat secara aerobik.
Pada akhir proses biodegradasi (H50) terjadi perubahan pH menjadi di atas pH netral (basa). Diduga perubahan pH terjadi karena asam organik (asam asetat) di dalam media digunakan oleh bakteri sebagai sumber karbon untuk memproduksi PHA-depolimerase. Sintesis enzim PHA-depolimerase pada bakteri biasanya terjadi jika sumber karbon terlarut yang cocok, seperti glukosa dan asam organik, tersedia (Jendrossek dan Handrick, 2002).
Pada Tabel 7, terlihat pH akhir dari media berada pada kisaran 7,42-7,97. Hal tersebut dikarenakan enzim PHA-depolimerase bekerja pada pH optimum alkali antara 7,5-9,8, sehingga bakteri mengkondisikan lingkungannya agar sesuai dengan kondisi optimum PHA-depolimerase dalam melakukan proses biodegradasi bioplastik.
B. UJI BIODEGRADASI BIOPLASTIK POLI- -HIDROKSIALKANOAT DENGAN MENGGUNAKAN METODE RESPIROMETRI
Mineralisasi merupakan salah satu tahapan pada proses biodegradasi yang dapat dijadikan parameter biodegradasi. Penggunaan mineralisasi
23 sebagai parameter biodegradasi dilakukan dengan cara mengukur produksi gas CO2 selama proses biodegradasi berlangsung.
Tahapan mineralisasi pada proses biodegradasi melibatkan reaksi oksidasi dengan oksigen bertindak sebagai oksidator. Pada proses biodegradasi bioplastik -hidroksialkanoat, khususnya dari golongan
poli--hidroksibutirat, reaksi ini ditunjukkan pada gambar 11:
Gambar 11. Reaksi pada tahapan mineralisasi (Narayan, 2006)
Metode respirometri merupakan metode yang dapat digunakan untuk mengukur proses biodegradasi dengan melakukan pengamatan terhadap proses mineralisasi. Gambar 12 merupakan grafik akumulasi produksi CO2, hasil pengukuran produksi CO2 dengan menggunakan metode respirometri selama 50 hari pengujian.
0 5 10 15 20 25 30 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 32 34 36 38 40 42 44 46 48 50 Hari Ke-n C O 2 (m g)
Gambar 12. Grafik akumulasi produksi CO2 selama proses biodegradasi [Bioplastik
poli- -hidroksialkanoat tanpa penambahan pemlastis ( ; akumulasi produksi CO2 = 27,28 mg); Bioplastik poli- -hidroksialkanoat dengan
penambahan pemlastis polietilen glikol 400 ( ; akumulasi produksi CO2
= 23,76 mg); Bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dietilen glikol ( ; akumulasi produksi CO2 = 18,92 mg); dan
Bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dimetil ftalat ( ; akumulasi produksi CO2 = 16,72 mg)].
Pengukuran jumlah produksi CO2 dilakukan selama 50 hari dengan evaluasi dilakukan setiap 2 hari hingga hari ke-38. Evaluasi CO2 kembali dilakukan pada hari ke-50 untuk mengetahui jumlah produksi CO2 pada akhir periode biodegradasi. Pengujian per 2 hari dihentikan pada hari ke-38 karena pada hari ke-30 pengujian, produksi CO2 cenderung menurun. Jika pengujian per 2 hari tetap dilakukan, jumlah CO2 yang dihasilkan dirasa kurang signifikan sehingga pada grafik akumulasi pertambahan CO2 per titik pengujian kurang terlihat. Rekapitulasi data produksi CO2 dan akumulasi produksi CO2 selama proses biodegradasi berlangsung dapat dilihat pada Lampiran 3-8.
Dengan menggunakan metode respirometri, suatu bahan dapat dikatakan mampu terdegradasi secara biologis, jika terdapat gas CO2 mulai diproduksi oleh sistem biologis pada biometer. Gambar 12 menunjukkan grafik akumulasi produksi CO2 sebagai hasil mineralisasi proses biodegradasi bioplastik poli- -hidroksialkanoat. Merujuk pada Gambar 12, dapat disimpulkan bahwa bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat, mampu terdegradasi secara biologis. Hal tersebut dibuktikan dengan adanya gas CO2 yang diproduksi selama proses biodegradasi berlangsung.
Pada pengujian biodegradasi ini poli- -hidroksialkanoat tanpa pemlastis digunakan sebagai pembanding. Secara keseluruhan, bioplastik poli- -hidroksialkanoat tanpa penambahan pemlastis terdegradasi dengan laju produksi CO2 paling cepat dan akumulasi produksi CO2 tertinggi dibandingkan dengan poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat. Hal tersebut didukung oleh data akumulasi produksi CO2 dan data laju produksi CO2 selama 50 hari pengujian. Pada hari ke-50, jumlah total CO2 yang dihasilkan oleh proses mineralisasi poli- -hidroksialkanoat tanpa pemlastis mencapai 27,28 mg, dengan laju produksi CO2 mencapai 0,55 mg/hari. Nilai laju produksi didapat dengan menggunakan perhitungan ,y/,t = (yi - yo) / (ti - to)., dengan yi =
jumlah akumulasi produksi CO2 pada hari ke-i; yo = jumlah akumulasi produksi CO2 pada hari ke-0; ti = hari ke-i; dan to = hari ke-0.
Fakta bahwa bioplastik poli- -hidroksialkanoat tanpa penambahan pemlastis mampu terdegradasi lebih cepat dan menghasilkan CO2 lebih banyak, mendukung teori bahwa penambahan pemlastis akan mempengaruhi
25 proses biodegradasi bioplastik poli- -hidroksialkanoat, dan pada studi biodegradasi ini pengaruh tersebut berupa perlambatan proses biodegradasi. Dibandingkan dengan poli- -hidroksialkanoat dengan penambahan pemlastis, poli- -hidroksialkanoat tanpa penambahan pemlastis memiliki struktur kimia yang lebih sederhana, karena ikatan-ikatan yang terdapat pada bioplastik hanyalah ikatan antar monomer poli- -hidroksialkanoat sendiri. Sedangkan pada poli- -hidroksialkanoat dengan penambahan pemlastis terbentuk ikatan-ikatan antara molekul-molekul yang terdapat pada poli- -hidroksialkanoat dan pemlastis. Ikatan tersebut menyebabkan struktur kimia poli- -hidroksialkanoat dengan penambahan pemlastis menjadi lebih kompleks dibandingkan dengan struktur kimia poli- -hidroksialkanoat tanpa penambahan pemlastis sehingga sampel poli- -hidroksialkanoat dengan penambahan pemlastis lebih sulit terdegradasi.
Sampel yang menjadi fokus pada penelitian ini adalah sampel dengan penambahan pemlastis polietilen glikol 400, dietilen glikol, dan dimetil ftalat. Dari Gambar 12, bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400 memiliki kemampuan terdegradasi paling cepat dibandingkan bioplastik poli- -hidroksialkanoat dengan pemlastis dietilen glikol dan bioplastik poli- -hidroksialkanoat dengan penambahan dimetil ftalat. Selama 50 hari pengujian, jumlah CO2 yang dihasilkan oleh proses mineralisasi sampel bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis polietilen glikol 400, bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dietilen glikol, dan bioplastik poli- -hidroksialkanoat dengan penambahan pemlastis dimetil ftalat masing-masing adalah 23,76 mg, 18,92 mg, dan 16,72 mg, dengan laju produksi CO2 masing-masing 0,48 mg/hari, 0,38 mg/hari, dan 0,33 mg/hari. Data akumulasi produksi CO2 dapat dilihat pada Lampiran 8.
Polietilen glikol 400 dan dietilen glikol merupakan pemlastis hidrofilik. Pemlastis hidrofilik akan meningkatkan laju biodegradasi, dan penambahan konsentrasi pemlastis hidrofilik akan meningkatkan laju degradasi enzimatis. Penambahan jumlah pemlastis hidrofilik yang semakin besar akan meningkatkan jumlah gugus polar (-OH) pada sampel, dan mengakibatkan adanya interaksi antara gugus polar tersebut dengan molekul air pada proses hidrolisis, proses yang menyebabkan terjadinya biodegradasi. Akibat adanya interaksi antara gugus polar yang terdapat pada pemlastis dengan molekul air,