xvi INTISARI
Cabai rawit putih (Capsicum frutescens L.) merupakan buah yang sering
digunakan baik sebagai bahan pangan dan pengobatan. Kandungan utama dalam buah cabai rawit putih adalah kapsaisin yang memiliki gugus fenolik sehingga memiliki aktivitas antioksidan. Antioksidan dapat menangkap radikal bebas sehingga mengurangi resiko terjadinya penyakit kronis. Penelitian ini bertujuan untuk menetapkan aktivitas antioksidan yang terdapat pada ekstrak etanol buah cabai rawit putih dan menetapkan kadar kapsaisin dalam buah cabai rawit putih.
Penentuan aktivitas antioksidan dilakukan dengan metode DPPH (1,1-difenil-2-pikrilhidrazil). Prinsip metode DPPH adalah penangkapan DPPH yang merupakan radikal bebas oleh senyawa antioksidan sehingga intensitas absorbansi DPPH berkurang. Pengukuran absorbansi dilakukan dengan spektrofotometer visibel pada panjang gelombang 517,5 nm. Penetapan kadar kapsaisin menggunakan metode KLT – densitometri dengan fase diam silika gel 60 F254 dan fase gerak toluena-kloroform-aseton (45:25:30, v/v/v).
Penurunan intensitas berkorelasi dengan kadar antioksidan. Hasil penelitian menunjukkan aktivitas antioksidan ekstrak etanol cabai rawit putih yang dinyatakan sebagai IC50 sebesar (90,02±10,16) µg/mL. Hasil analisis
kuantitatif kadar kapsaisin ekstrak etanol buah cabai rawit putih sebesar (0,1099±0,0001)% (b/b) dengan catatan metode yang digunakan belum tervalidasi.
Kata kunci : Buah cabai rawit putih (Capsicum frutescens L.), kapsaisin, radikal
xvii
ABSTRACT
White chili pepper (Capsicum frutescens L.) is a fruit that often used as
food and medicine. White chili pepper contains capsaicin which has phenolic group that has antioxidant activity. Antioxidant can scavenge free radical thereby reducing the risk of chronic diseases. This experiment aimed to determine antioxidant activity and the contents of capsaicin in ethanol extract of chili pepper fruit.
The antioxidant activity was tested by DPPH (1,1-diphenyl-2-picrylhydrazyl) method. The principle of DPPH method was scavenging DPPH as free radical by antioxidant compounds which could reduce intencity of DPPH absorbance. Absorbance was measured by visible spectrophotometer in maximum wave lenght (517,5 nm). Level of capsaicin was assayed by TLC –
densitometry and used silica gel 60 F254 as stationary phase and toluene-chloroform-acetone (45:25:30, v/v/v) as mobile phase.
The intencity decrement is correlated with antioxidant concentration. The result of examination showed that antioxidant activity in ethanol extract of chili pepper fruit as IC50 is (90,02±10,16) µg/mL. Level of capcaicin in ethanol extract of white variety of chili pepper fruit is (0,1099±0,0001)% (w/w) but the TLC –
densitometry method has not been validated yet.
Keywords : White chili pepper (Capsicum frutescens L.), capsaicin, free radical,
UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOLIK BUAH CABAI RAWIT PUTIH (Capsicum frutescens L.) DENGAN METODE DPPH (1,1-difenil-2-pikrilhidrazil) DAN PENETAPAN KADAR KAPSAISIN SECARA KROMATOGRAFI LAPIS TIPIS (KLT) – DENSITOMETRI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh :
Vanny Christy Silviani NIM : 098114068
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOLIK BUAH CABAI RAWIT PUTIH (Capsicum frutescens L.) DENGAN METODE DPPH (1,1-difenil-2-pikrilhidrazil) DAN PENETAPAN KADAR KAPSAISIN SECARA KROMATOGRAFI LAPIS TIPIS (KLT) – DENSITOMETRI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh :
Vanny Christy Silviani NIM : 098114068
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
vii PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa atas rahmat, kasih, dan penyertaanNya yang selalu dilimpahkan sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi berjudul “Uji Aktivitas Antioksidan Ekstrak Etanolik Buah Cabai Rawit Putih (Capsicum Frutescens L.) Dengan Metode
DPPH (1,1-Difenil-2-Pikrilhidrazil) dan Penetapan Kadar Kapsaisin secara Kromatografi Lapis Tipis (KLT) – Densitometri”. Skripsi ini dibuat sebagai syarat memperoleh gelar Sarjana Farmasi (S.Farm).
Penulis menyadari bahwa dalam penyelesaian skripsi tidak lepas dari bantuan, dukungan, bimbingan, kritikan, dan saran dari berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih kepada :
1. Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Prof. Dr. C. J. Soegihardjo, Apt. selaku Dosen Pemimbing yang telah memberikan bimbingan, saran, kritikan, dan motivasi kepada penulis selama penelitian hingga penyelesaian skipsi.
3. Yohanes Dwiatmaka, M.Si., selaku Dosen Penguji yang memberikan arahan, kritik, dan saran untuk skripsi ini.
viii
5. Agustina Setiawati, M.Sc., Apt. selaku Dosen Pembimbing Akademik yang telah memberikan nasihat dan dukungan selama penulis menyelesaikan masa studi di Fakultas Farmasi Universitas Sanata Dharma.
6. Rini Dwiastuti, M.Sc., Apt. selaku Kepala Laboratorium Fakultas Farmasi Universitas Sanata Dharma.
7. Seluruh staff laboratorium, terutama Mas Bimo, Mas Wagiran, Pak Parlan, Mas Kayat atas segala bantuan yang diberikan selama penelitian skripsi. 8. Mama terkasih yang selalu mendukung penulis dengan doa, semangat, dan
cinta sehingga penulis dapat menyelesaikan pendidikan.
9. Yenny dan Christina, teman seperjuangan dalam penelitian skripsi. Terima kasih untuk semua dukungan, kerjasama, diskusi, persahabatan, canda, dan doa dari kalian berdua.
10.Pdt. Drs. Samuel J. Suwondo dan keluarga yang selalu memberi dukungan kepada penulis selama menempuh pendidikan.
11.Hanna Silviani yang membantu penulis dalam menyempurnakan naskah skripsi serta selalu mendukung penulis.
12.Teman-temanku tersayang, Adel, Rizza, Evy, Yani, Prita yang selalu memberikan motivasi, dukungan, kerjasama, keceriaan, dan pengalaman berharga yang tak terlupakan.
ix
14.Teman-teman FST 2009, kelas B 2009, kelompok praktikum B 2009 atas kebersamaannya yang mengisi canda dan tawa serta motivasi selama perkuliahan.
15.Semua pihak yang tidak dapat disebutkan satu per satu yang telah membantu dan mendukung dari awal penelitian hingga penyelesaian skripsi.
Penulis menyadari masih banyak kekurangan dalam penulisan skripsi ini sehingga dengan penuh kerendahan hati penulis menerima setiap kritikan dan saran yang dapat membangun sehingga dapat memperbaiki skripsi ini. Akhir kata, penulis berharap agar skripsi ini dapat bermanfaat bagi pembaca dan meningkatkan pengetahuan mengenai farmasi, terutama dalam bidang bahan alami.
Yogyakarta, 17 Januari 2013
x DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN PENULIS ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ... vi
xi
F. Ekstraksi ... 15
G. Spektrofotometri Visibel ... 17
H. Kromatografi Lapis Tipis ... 18
I. Densitometri ... 20
J. Validasi Metode Analisis ... 20
K. Landasan Teori ... 24
L. Hipotesis ... 25
BAB III METODOLOGI PENELITIAN... 26
A. Jenis dan Rancangan Penelitian ... 26
B. Variabel ... 26
1. Variabel bebas ... 26
2. Variabel tergantung ... 26
3. Variabel pengacau terkendali ... 26
4. Variabel pengacau tak terkendali ... 26
C. Definisi Operasional ... 27
3. Pembuatan ekstrak buah cabai rawit putih... 29
4. Penentuan aktivitas antioksidan dengan metode DPPH ... 29
a. Pembuatan larutan DPPH ... 29
b. Pembuatan larutan stok kapsaisin ... 29
c. Pembuatan larutan seri baku kapsaisin ... 29
d. Pembuatan larutan uji ... 30
e. Uji pendahuluan aktivitas antioksidan ... 30
f. Penentuan panjang gelombang maksimum ... 30
g. Penentuan operating time (OT) ... 30
xii
i. Validasi metode uji aktivitas antioksidan ... 31
j. Estimasi aktivitas antioksidan ... 32
5. Penentuan kadar kapsaisin ... 32
a. Pembuatan fase gerak ... 32
b. Pembuatan larutan stok kapsaisin ... 32
c. Pembuatan larutan seri baku kapsaisin ... 32
d. Pembuatan larutan uji ... 32
e. Penentuan kadar kapsaisin buah cabai rawit putih ... 33
F. Analisis Hasil ... 33
E. Hasil Optimasi Metode Uji Aktivitas Antioksidan ... 42
1. Penentuan panjang gelombang maksimum ... 42
2. Penentuan operating time (OT) ... 44
F. Hasil Validasi Metode Uji Aktivitas Antioksidan ... 46
1. Spesifisitas metode uji aktivitas antioksidan ... 47
2. Akurasi metode uji aktivitas antioksidan ... 48
3. Presisi metode uji aktivitas antioksidan ... 49
4. Linearitas metode uji aktivitas antioksidan... 50
G. Hasil Estimasi Aktivitas Antioksidan dengan Radikal DPPH ... 51
H. Hasil Penetapan Kadar Kapsaisin ... 58
I. Analisis Statistik Aktivitas Antioksidan ... 64
xiii
DAFTAR TABEL
Tabel I. Kriteria akurasi yang masih dapat diterima menurut
Harmita (2004) ... 22
Tabel II. Kriteria presisi yang masih dapat diterima menurut Harmita (2004) ... 23
Tabel III. Hasil pengukuran panjang gelombang maksimum DPPH ... 43
Tabel IV. Hasil pengukuran absorbansi seri kurva baku kapsaisin yang direaksikan dengan DPPH ... 46
Tabel V. Nilai perolehan kembali (% recovery) uji aktivitas antioksidan pada baku kapsaisin ... 48
Tabel VI. Nilai CV uji aktivitas antioksidan pada baku kapsaisin ... 49
Tabel VII. Hasil aktivitas antioksidan ekstrak etanol buah cabai rawit putih ... 54
Tabel VIII. Hasil perhitungan IC50 baku kapsaisin dan ekstrak etanol buah cabai rawit putih ... 57
Tabel IX. Tingkat kekuatan aktivitas antioksidan ... 58
Tabel X. Data nilai Rf baku kapsaisin dan sampel ... 61
xiv
DAFTAR GAMBAR
Gambar 1. Struktur senyawa kapsaisin (Henderson And Slickman,
1999) ... 10 Gambar 2. Reaksi penangkapan radikal DPPH oleh antioksidan
(Prakash, Rigelhof, Miller, 2001) ... 15 Gambar 3. Penyarian dengan alat Soxhlet (Cornell University, 2011) .... 17 Gambar 4. Morfologi berbagai spesies Capsicum (Bosland, Bailey,
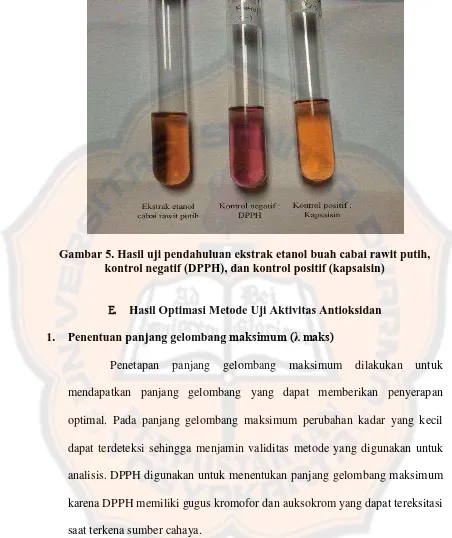
Iglesias-Olivas, 1996) ... 35 Gambar 5. Hasil uji pendahuluan ekstrak etanol buah cabai rawit
putih, kontrol negatif (DPPH), dan kontrol positif
(kapsaisin)... 42 Gambar 6. Gugus kromofor dan gugus auksokrom DPPH
(Witt, Lalk, Hager, dan Voigt, 2010) ... 43 Gambar 7. Grafik penentuan Operating Time baku kapsaisin ... 45
Gambar 8. Struktur senyawa kapsaisin ... 52 Gambar 9. Mekanisme penghambatan radikal bebas oleh senyawa
kapsaisin ... 53 Gambar 10. Kurva persamaan regresi linier aktivitas antioksidan
ekstrak etanol buah cabai rawit putih replikasi I ... 55 Gambar 11. Kurva persamaan regresi linier aktivitas antioksidan
ekstrak etanol buah cabai rawit putih replikasi II ... 55 Gambar 12. Kurva persamaan regresi linier aktivitas antioksidan
ekstrak etanol buah cabai rawit putih replikasi III ... 56 Gambar 13. Interaksi kapsaisin dengan fase diam silika gel 60 F254 ... 60 Gambar 14. Interaksi kapsaisin dengan fase gerak
xv
DAFTAR LAMPIRAN
Lampiran 1. Gambar buah cabai rawit putih dari Pasar Beringharjo,
Yogyakarta ... 71 Lampiran 2. Sertifikat analisis kapsaisin ... 72 Lampiran 3. Perhitungan rendemen ekstrak etanol buah cabai rawit
putih ... 73 Lampiran 4. Data penimbangan bahan untuk uji aktivitas antioksidan ... 74 Lampiran 5. Data perhitungan konsentrasi bahan untuk uji aktivitas
antioksidan ... 75 Lampiran 6. Scanning larutan pengoreksi untuk uji aktivitas
antioksidan ... 80 Lampiran 7. Optimasi metode uji aktivitas antioksidan ... 82 Lampiran 8. Data uji aktivitas antioksidan menggunakan radikal
DPPH ... 86 Lampiran 9. Perhitungan nilai IC50 baku kapsaisin dan ekstrak etanol
buah cabai rawit putih ... 89 Lampiran 10. Sistem KLT densitometri yang digunakan ... 91 Lampiran 11. Data perhitungan konsentrasi bahan untuk penetapan kadar
kapsaisin ... 92 Lampiran 12. Kromatogram baku kapsaisin ... 94 Lampiran 13. Data persamaan kurva baku kapsaisin ... 95 Lampiran 14. Kromatogram kapsaisin dalam ekstrak etanol buah cabai
rawit putih ... 96 Lampiran 15. Data dan perhitungan kadar kapsaisin dalam ekstrak
etanol buah cabai rawit putih ... 97 Lampiran 16. Uji statistik dengan SPSS 16.0 ... 98
xvi INTISARI
Cabai rawit putih (Capsicum frutescens L.) merupakan buah yang sering
digunakan baik sebagai bahan pangan dan pengobatan. Kandungan utama dalam buah cabai rawit putih adalah kapsaisin yang memiliki gugus fenolik sehingga memiliki aktivitas antioksidan. Antioksidan dapat menangkap radikal bebas sehingga mengurangi resiko terjadinya penyakit kronis. Penelitian ini bertujuan untuk menetapkan aktivitas antioksidan yang terdapat pada ekstrak etanol buah cabai rawit putih dan menetapkan kadar kapsaisin dalam buah cabai rawit putih.
Penentuan aktivitas antioksidan dilakukan dengan metode DPPH (1,1-difenil-2-pikrilhidrazil). Prinsip metode DPPH adalah penangkapan DPPH yang merupakan radikal bebas oleh senyawa antioksidan sehingga intensitas absorbansi DPPH berkurang. Pengukuran absorbansi dilakukan dengan spektrofotometer visibel pada panjang gelombang 517,5 nm. Penetapan kadar kapsaisin menggunakan metode KLT – densitometri dengan fase diam silika gel 60 F254 dan fase gerak toluena-kloroform-aseton (45:25:30, v/v/v).
Penurunan intensitas berkorelasi dengan kadar antioksidan. Hasil penelitian menunjukkan aktivitas antioksidan ekstrak etanol cabai rawit putih yang dinyatakan sebagai IC50 sebesar (90,02±10,16) µg/mL. Hasil analisis
kuantitatif kadar kapsaisin ekstrak etanol buah cabai rawit putih sebesar (0,1099±0,0001)% (b/b) dengan catatan metode yang digunakan belum tervalidasi.
Kata kunci : Buah cabai rawit putih (Capsicum frutescens L.), kapsaisin, radikal
xvii
ABSTRACT
White chili pepper (Capsicum frutescens L.) is a fruit that often used as
food and medicine. White chili pepper contains capsaicin which has phenolic group that has antioxidant activity. Antioxidant can scavenge free radical thereby reducing the risk of chronic diseases. This experiment aimed to determine antioxidant activity and the contents of capsaicin in ethanol extract of chili pepper fruit.
The antioxidant activity was tested by DPPH (1,1-diphenyl-2-picrylhydrazyl) method. The principle of DPPH method was scavenging DPPH as free radical by antioxidant compounds which could reduce intencity of DPPH absorbance. Absorbance was measured by visible spectrophotometer in maximum wave lenght (517,5 nm). Level of capsaicin was assayed by TLC – densitometry and used silica gel 60 F254 as stationary phase and toluene-chloroform-acetone (45:25:30, v/v/v) as mobile phase.
The intencity decrement is correlated with antioxidant concentration. The result of examination showed that antioxidant activity in ethanol extract of chili pepper fruit as IC50 is (90,02±10,16) µg/mL. Level of capcaicin in ethanol extract of white variety of chili pepper fruit is (0,1099±0,0001)% (w/w) but the TLC – densitometry method has not been validated yet.
Keywords : White chili pepper (Capsicum frutescens L.), capsaicin, free radical,
1 BAB I PENGANTAR
A. Latar Belakang
Penelitian di bidang kesehatan mengenai antioksidan semakin banyak dilakukan untuk mencegah timbulnya penyakit yang disebabkan oleh senyawa radikal bebas. Radikal bebas, seperti reactive oxygen species (ROS) bersifat
sangat reaktif dan dapat mengoksidasi substansi-substansi dalam tubuh sehingga dapat menyebabkan terjadinya berbagai penyakit seperti jantung, kanker, penuaan dini, dan penyakit degerenatif lain (Parke, 1999; Prakash, Rigelhof, dan Miller, 2001). Untuk mengatasi radikal bebas tersebut, maka diperlukan suatu senyawa antioksidan yang dapat menangkap radikal bebas sehingga menghambat terbentuknya penyakit yang merugikan.
memiliki satu elektron dan bersifat sangat reaktif untuk mengambil elektron dari senyawa lain. Reaksi radikal dapat menyebabkan terjadinya reaksi berantai (Simex, 2008). Radikal bebas dapat mengoksidasi lipid, protein, DNA, dan asam nukleat tak jenuh dalam tubuh untuk mencapai kestabilan elektron sehingga menyebabkan terjadinya penyakit degeneratif (Prakash, Rigelhof, dan Miller, 2001). Oleh karena berbahayanya radikal bebas bagi tubuh, maka perlu dilakukan penelitian mengenai senyawa antioksidan yang dapat menangkal kerja radikal bebas.
Cabai rawit (Capsicum frutescens L.) merupakan salah satu buah yang
sering digunakan masyarakat di Indonesia sebagai bahan pangan. Cabai rawit memiliki manfaat sebagai obat sariawan, tonik, stimulan kuat untuk jantung dan aliran darah, antirematik, antikoagulan, stomakik, karminatif, diaforetik, dan diuretik (Sentra Informasi Ilmu Pengetahuan dan Teknologi, 2005). Menurut Sentra Informasi Ilmu Pengetahuan dan Teknologi (2005), buah cabai rawit memiliki tiga macam varietas, yaitu cabai rawit merah (cabai kecil), cabai rawit putih (cabai domba), dan cabai rawit hijau (ceplik).
Di dalam buah cabai rawit terkandung berbagai macam senyawa seperti kapsaisin, kapsantin, karotenoid, alkaloid atsiri, resin, flavonoid, minyak atsiri, provitamin A, vitamin B1 dan vitamin C (Sentra Informasi Ilmu Pengetahuan dan Teknologi, 2005; Howard, Talcott, Brenes, dan Villalon, 2000). Salah satu kandungan tertinggi dalam buah cabai rawit adalah kapsaisin. Kapsaisin merupakan senyawa yang bertanggung jawab dalam menghasilkan rasa pedas.
Kapsaisin memiliki aktvitas dalam menghambat pertumbuhan sel kanker. Menurut Henderson dan Slickman (1999), kapsaisin memiliki aktivitas antioksidan dengan menangkap radikal bebas. Gugus fenol pada kapsaisin yang bertanggung jawab atas aktivitas antioksidan. Selain itu, bentuk isomer cis – trans kapsaisin juga memiliki peran dalam menangkap radikal bebas. Karena itu, perlu diteliti mengenai kegunaan kapsaisin sebagai antioksidan dalam buah cabai rawit putih sehingga dapat dikembangkan sebagai salah satu free radical scavenger
Ekstraksi yang digunakan pada buah cabai rawit ini menggunakan larutan etanol. Alasan pemilihan ekstraksi didasari pada sifat fisika kimia dari senyawa yang akan diuji, yaitu kapsaisin yang bersifat non polar. Dengan demikian digunakan etanol agar kapsaisin dapat terekstraksi. Pada beberapa penelitian yang telah dilakukan, ekstraksi kapsaisin terbukti paling efektif dan menghasilkan rendemen yang tinggi menggunakan penyarian dengan alat Soxhlet (Boonkird, Phisalaphong, Phisalaphong, 2008; Gonzáles and Al-Tamirano, 1973) sehingga digunakan alat Soxhlet untuk mengekstraksi buah cabai rawit putih.
Metode yang digunakan untuk uji aktivitas antioksidan buah cabai rawit putih ini adalah metode DPPH. Metode DPPH adalah metode yang mengukur kemampuan antioksidan dalam menghambat radikal bebas DPPH. Metode ini digunakan untuk pengujian senyawa antioksidan yang memiliki mekanisme dengan mendonorkan hidrogen atau mendonorkan elektron pada senyawa radikal sehingga reaksi radikal terhenti (Prakash, Rigelhof, dan Miller, 2001). Tujuan pengujian dengan metode DPPH adalah untuk mengetahui konsentrasi dari senyawa antioksidan yang ekuivalen dapat memberikan 50% efek antioksidan dan dinyatakan sebagai Inhibition Concentration 50 (IC50).
karena metode ini mudah digunakan, cepat, dan menghasilkan hasil yang reprodusibel (Dehpour, Ebrahimzadeh, Fazel, dan Mohammad, 2009).
Pada penelitian ini juga dilakukan uji kandungan kapsaisin karena kapsaisin merupakan senyawa dalam buah cabai rawit yang memiliki aktivitas antioksidan. Penentuan kadar kapsaisin dilakukan dengan metode kromatografi lapis tipis (KLT) – densitometri. Penentuan kadar kapsaisin dilakukan untuk menentukkan jumlah kapsaisin yang terdapat dalam sampel.
1. Permasalahan
a. Berapa nilai aktivitas antioksidan buah cabai rawit putih yang dinyatakan dengan IC50 menggunakan metode DPPH?
b. Berapa kadar kapsaisin buah cabai rawit putih dengan metode kromatografi lapis tipis – densitometri?
2. Keaslian penelitian
Penelitian mengenai uji aktivitas antioksidan pada cabai pernah dilakukan oleh Bachtiar (2009). Penelitian yang dilakukan adalah mengamati pengaruh suhu dan lama penyimpanan dingin terhadap kandungan vitamin C dan aktivitas antioksidan pada cabai merah (Capsicum annum L.) dengan
menggunakan metode DPPH. Howard, Talcott, Brenes, dan Villalon (2000) melakukan penelitian mengenai aktivitas antioksidan pada berbagai spesies
Amarowicz, Shahidi (2011) meneliti aktivitas antioksidan pada buah Jalapeno dan Serrano Peppers menggunakan metode DPPH.
Perbedaan penelitian ini dengan penelitian yang telah dilakukan adalah pada penelitian ini menguji aktivitas antioksidan buah cabai rawit putih (Capsicum frutescens L.) dengan menggunakan DPPH dan menetapkan
kadar kapsaisin dengan metode kromatografi lapis tipis (KLT) – densitometri. Sejauh penelusuran peneliti, penelitian ini belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian ini diharapkan dapat memberikan perkembangan ilmu pengetahuan dalam bidang farmasi mengenai aktivitas antioksidan buah cabai rawit putih pada radikal bebas DPPH yang dinyatakan sebagai IC50.
B. Tujuan 1. Tujuan umum
Menguji aktivitas antioksidan buah cabai rawit putih dengan menggunakan metode DPPH.
2. Tujuan khusus
a. Mengetahui nilai aktivitas antioksidan buah cabai rawit putih yang
dinyatakan sebagai IC50 dengan menggunakan metode DPPH.
8 BAB II
PENELAAHAN PUSTAKA
A. Cabai Rawit Putih 1. Klasifikasi tanaman
Klasifikasi tanaman cabai rawit putih dalam sistematika tumbuhan menurut Plantamor (2008) adalah sebagai berikut.
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh) Super Divisi : Spermatophyta (Tumbuhan berbiji) Divisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (Tumbuhan berkeping biji dua) Sub Kelas : Asteridae
Ordo : Solanales
Famili : Solanaceae (Suku terung-terungan)
Genus : Capsicum
Spesies : Capsicum frutescens L.
2. Morfologi tanaman
pangkal menyempit, tepi rata, pertulangan menyirip, panjang 5-9,5 cm, lebar 1,5-5,5 cm, berwarna hijau. Bunga keluar dari ketiak daun, mahkota bentuk bintang, bunga tunggal atau 2-3 bunga letaknya berdekatan, berwarna putih, putih kehijauan, kadang-kadang ungu. Buahnya berupa buah buni, tegak, kadang-kadang merunduk, berbentuk bulat telur, lurus atau bengkok, ujung meruncing, panjang 1-3 cm, lebar 2,5-12 mm, bertangkai panjang, dan rasanya pedas. Buah muda berwarna hijau tua, putih kehijauan, atau putih, buah yang masak berwarna merah terang (Sentra Informasi Ilmu Pengetahuan dan Teknologi, 2005).
3. Kandungan kimia
Buah cabai rawit putih mengandung kapsaisin, kapsantin, karotenoid, alkaloid atsiri, resin, minyak menguap, vitamin (A dan C), dan flavonoid. Kapsaisin memberikan rasa pedas pada cabai, berkhasiat untuk melancarkan aliran darah serta pemati rasa kulit. Biji mengandung alkaloid, antara lain solanina, solamidina, solamargina, solasodina, solasomina, dan steroid saponin (kapsisidin) (Sentra Informasi Ilmu Pengetahuan dan Teknologi, 2005; Howard, Talcott, Brenes, dan Villalon, 2000).
4. Kegunaan buah cabai rawit putih
karminatif, diaforetik, dan diuretik (Sentra Informasi Ilmu Pengetahuan dan Teknologi, 2005).
B. Kapsaisin
Kapsaisin adalah senyawa yang menimbukan rasa pedas. Kapsaisin (trans-8-methyl-N-vanillyl-6-nonenamide), senyawa alkaloid berbentuk kristal,
lipofilik, tidak berwarna, dan tidak berbau memiliki formula C18H27NO3. Kapsaisin memiliki kelarutan di dalam lemak, minyak, dan alkohol (Escogido, Mondragon, Tzompantzi, 2011).
Kapsaisin disintesis secara alami dari plasenta buah cabai dari kondensasi enzimatik vanililamina dan rantai asam lemak yang diperpanjang oleh enzim fatty acid synthase. Penelitian menunjukkan bahwa kapsaisinoid, khususnya kapsaisin
memiliki aktivitas biologi dan fisiologi yang bervariasi seperti antioksidan, antikarsinogenik, metabolisme energi dan pengurangan akumulasi lemak, serta antiinflamasi (Escogido, Mondragon, Tzompantzi, 2011).
Substituen pada posisi 3 dan 4 dari cincin aromatis fenolik khususnya gugus 4-OH fenolik memiliki kemampuan aktivitas agonis. Sifat donor-akseptor ikatan hidrogen pada gugus fenol merupakan kunci aktivitas agonis (Escogido, Mondragon, Tzompantzi, 2011).
Kapsaisin memiliki aktivitas antioksidan dengan menangkap radikal bebas. Gugus fenol pada kapsaisin yang bertanggung jawab atas aktivitas antioksidan dalam mendonorkan elektron kepada radikal bebas (Henderson and Slickman, 1999).
C. Radikal Bebas
Untuk hidup, kita memerlukan oksigen, namun oksigen juga merupakan sumber radikal bebas. Radikal bebas tersebut beberapa di antaranya toksik (beracun) dan sangat reaktif dapat mempercepat proses penuaan dan kematian (Kochar and Rossell, 1990).
Radikal bebas merupakan atom atau gugus atom yang memiliki satu elektron tidak berpasangan. Radikal bebas bersifat sangat reaktif dan berenergi tinggi karena adanya elektron tidak berpasangan (Fessenden dan Fessenden, 1982).
Awal terjadinya radikal bebas antara lain dari proses reduksi molekul oksigen dalam rangkaian transport dalam mitokondria atau dalam proses-proses lain yang terjadi secara acak dari berbagai proses kimiawi dalam tubuh yang melibatkan senyawa organik maupun inorganik. Radikal bebas yang berupa peroksil anion ini akan bereaksi dengan dua proton (2H+) membentuk hidrogen peroksida (H2O2) (Pratt, 1992).
terbentuk ini mempunyai masa paruh yang sangat pendek, tetapi tetap mempunyai potensi besar yang dapat merusak sel. Radikal hidroksil, yang diduga dalam kehidupan kita banyak terbentuk dianggap lebih berbahaya dibanding bentuk radikal bebas yang lain (Pratt, 1992).
D. Antioksidan
Antioksidan didefinisikan sebagai senyawa yang dapat menunda, memperlambat, dan mencegah proses oksidasi lipid. Dalam arti khusus, antioksidan adalah zat yang dapat menunda atau mencegah terjadinya reaksi antioksidasi radikal bebas dalam oksidasi lipid (Kochar and Rossell, 1990).
Antioksidan sangat beragam jenisnya. Berdasarkan sumbernya antioksidan dibagi dalam dua kelompok yaitu antioksidan sintetik (antioksidan yang diperoleh dari hasil sintetis reaksi kimia) dan antioksidan alami (antioksidan hasil ekstraksi bahan alami). Antioksidan alami di dalam makanan dapat berasal dari senyawa antioksidan yang sudah ada dari satu atau dua komponen makanan, senyawa antioksidan yang terbentuk dari reaksi-reaksi selama proses pengolahan, senyawa antioksidan yang diisolasi dari sumber alami dan ditambahkan ke makanan sebagai bahan tambahan pangan (Pratt, 1992).
Berdasarkan mekanisme kerjanya, antioksidan diklasifikasikan menjadi dua kategori, yaitu antioksidan pencegah dan antioksidan pemutus rantai. Antioksidan pencegah bekerja dengan menghambat pembentukan reactive oxygen species, seperti enzim katalase, peroksidase, superoksida dismutase, dan
radikal oksigen kemudian memutus rangkaian rantai reaksi radikal, contohnya vitamin C, vitamin E, asam urat, bilirubin, polifenol, dan sebagainya. Antioksidan pemutus rantai memiliki dua jalur reaksi. Jalur pertama merupakan jalur transfer atom hidrogen dengan mekanisme radikal oksigen menangkap hidrogen dari antioksidan sehingga terbentuk kompleks antioksidan-radikal yang bersifat stabil. Jalur kedua, antioksidan mendeaktivasi radikal bebas dengan transfer elektron tunggal. Transfer elektron tunggal sangat dipengaruhi oleh kestabilan pelarut pada muatan tertentu (Ou, Huang, Woodill, Flanagan, and Deemer, 2002).
E. Metode DPPH
Metode yang paling sering digunakan untuk menguji aktivitas antioksidan tanaman obat adalah metode uji dengan menggunakan radikal bebas DPPH (1,1-difenil-2-pikrilhidrazil). Tujuan metode ini adalah mengetahui parameter konsentrasi yang ekuivalen memberikan 50% efek aktivitas antioksidan (IC50). Hal ini dapat dicapai dengan cara menginterpretasikan data eksperimental
dari metode tersebut. DPPH merupakan radikal bebas yang dapat bereaksi dengan senyawa yang dapat mendonorkan atom hidrogen, dapat berguna untuk pengujian aktivitas antioksidan komponen tertentu dalam suatu ekstrak (Dehpour, Ebrahimzadeh, Fazel, dan Mohammad, 2009).
antioksidan dapat mengubah warna larutan DPPH dari ungu menjadi kuning. Perubahan absorbansi akibat reaksi ini telah digunakan secara luas untuk menguji kemampuan beberapa molekul sebagai penangkap radikal bebas (Dehpour, Ebrahimzadeh, Fazel, dan Mohammad, 2009).
Metode DPPH merupakan metode yang cepat, sederhana, dan tidak membutuhkan biaya tinggi dalam menentukan kemampuan antioksidan menggunakan radikal bebas 2,2-difenil-1-pikrilhidrazil (DPPH). DPPH sering digunakan untuk menguji senyawa yang berperan sebagai free radical scavengers
atau donor hidrogen dan mengevaluasi aktivitas antioksidannya, serta mengkuantifikasi jumlah kompleks radikal-antioksidan yang terbentuk. Metode DPPH dapat digunakan untuk sampel yang berupa padatan maupun cairan (Prakash, Rigelhof, Miller, 2001).
Gambar 2. Reaksi penangkapan radikal DPPH oleh antioksidan (Prakash, Rigelhof, Miller, 2001)
F. Ekstraksi
Tujuan ekstraksi adalah menyari zat pokok atau komponen kimia yang diinginkan dari bahan mentah obat menggunakan pelarut yang sesuai dengan kelarutan zat sehingga zat yang diinginkan masuk dalam cairan penyari. Bahan mentah yang berasal dari tumbuh-tumbuhan ataupun hewan tidak perlu diproses lebih lanjut kecuali dikumpulkan atau dikeringkan. Tiap-tiap bahan mentah obat disebut ekstrak, tidak mengandung hanya satu unsur saja tetapi berbagai unsur, tergantung pada obat yang digunakan dan kondisi dari ekstraksi (Fouad, 2005). Semakin banyak permukaan simplisia yang bersentuhan dengan penyari maka proses ekstraksi bertambah baik ( Harborne, 1987).
molekul bahan pelarut. Kemampuan pelarut untuk mengikat zat perancah selulose menyebabkan struktur perancah tersebut menjadi longgar, sehingga terbentuk ruang antarmiselar, yang memungkinkan pelarut mencapai ke dalam ruang dalam sel. Masuknya pelarut dalam intrasel menyebabkan protoplasma membengkak dan zat yang terkandung dalam sel akan terlarut sesuai dengan kelarutannya. Perbedaan konsentrasi larutan di dalam sel dengan cairan pengekstraksi yang baru (tidak mengandung zat aktif) akan menyebabkan terjadinya proses difusi melalui ruang antarmiselar. Zat di dalam sel akan keluar menuju pelarut hingga mencapai kesetimbangan konsentrasi (Voigt, 1994).
Gambar 3. Penyarian dengan alat Soxhlet (Cornell University, 2011) Keuntungan dari penyarian dengan alat Soxhlet adalah tidak membutuhkan pelarut dalam jumlah yang banyak dan pelarut yang masuk ke dalam bahan yang akan diekstraksi secara terus menerus diperbaharui dengan pelarut yang tidak mengandung zat aktif (Voigt, 1994).
G. Spektrofotometri Visibel
Spektrofotometri visibel merupakan teknik spektroskopik yang memakai sumber radiasi elektromagnetik sinar tampak (380-780 nm) dengan memakai instrumen spektrofotometer. Distribusi elektron didalam suatu senyawa organik secara umum yang dikenal sebagai orbital elektron pi (п), sigma (α) dan elektron tidak berpasangan (n). Apabila pada molekul dikenakan radiasi elektromagnetik maka akan terjadi ekstasi elektron ke tingkat energi yang lebih tinggi yang dikenal sebagai orbital elektro anti bonding (Mulja dan Suharman, 1995).
sekitar 200 ke 700 nm yang digunakan dalam eksperimen dan karenanya memerlukan gugus kromofor dalam molekul itu (Day dan Underwood, 1999).
Kromofor merupakan gugus tak jenuh kovalen yang dapat menyerap radiasi dalam daerah-daerah UV dan visibel, pada senyawa organik dikenal pula gugus auksokrom, yaitu gugus jenuh yang terikat pada kromofor. Terikatnya gugus auksokrom pada kromofor dapat mengubah panjang gelombang dan intensitas serapan maksimum (Sastrohamidjojo, 2001).
DPPH memberikan absorbansi maksimal di daerah visibel (cahaya tampak), sehingga untuk menganalisis penurunan absorbansi DPPH karena adanya senyawa antioksidan dapat menggunakan spektrofotometer visibel. Berkurangnya absorbansi dari reaksi DPPH dengan antioksidan menunjukkan aktivitas penangkapan radikal bebas. Semakin rendah absorbansi mengindikasikan semakin tinggi kemampuan aktivitas antioksidan (Chaisawvong and Sangsrichan, 2009).
H. Kromatografi Lapis Tipis
yang menyerap, walaupun dapat pula dipakai sebagai penyangga zat cair. Fase geraknya mengalir karena kerja kapiler (Gritter, 1991).
Fase diam pada KLT dapat berupa serbuk halus yang berfungsi sebagai permukaan penyerap (kromatografi cair-padat) atau berfungsi sebagai penyangga untuk lapisan zat cair (kromatografi cair-cair) empat penyerap (fase diam) yang paling umum dipakai adalah silika gel (asam silikat), alumina (aluminium oksida), kiselgur (tanah diatome) atau selulosa (Gritter, 1991).
Fase gerak adalah medium angkut yang terdiri atas satu atau beberapa pelarut. Fase gerak bergerak di dalam fase diam, yaitu suatu lapisan berpori karena ada gaya kapiler. Yang digunakan hanyalah pelarut tingkat mutu analitik dan bila diperlukan sistem pelarut multi komponen ini harus berupa suatu campuran sederhana yang terdiri atas maksimum tiga komponen. Angka banding campuran dinyatakan dalam bagian volume sedemikian rupa sehingga volume total 100 (Stahl, 1985).
Kromatografi lapis tipis (KLT) adalah teknik yang mudah digunakan dalam memisahkan komponen dari suatu kompleks, seperti ekstrak dari jaringan tanaman. Bila kromatografi lapis tipis dikombinasikan dengan detektor yang tepat, KLT dapat menjadi metode kuantitatif senyawa yang memiliki pemisahan yang baik (Gonzáles, Lara, Carbajal, and Flota, 2007).
teknik yang sering digunakan karena kemampuan sistem analisis yang sensitif dan peningkatan kemampuan dari KLT dalam menganalisis (Turner, Subrahmanyam, and Piletsky, 2009).
I. Densitometri
Densitometri merupakan metode analisis instrumental berdasarkan interaksi analit dengan radiasi elektromagnetik dalam bentuk bercak pada KLT. Densitometri dilakukan untuk analit dengan konsentrasi kecil yang memerlukan pemisahan terlebih dahulu dengan KLT. Evaluasi bercak KLT discanning dengan
sumber sinar dalam bentuk celah. Sinar yang dipantulkan ditangkap oleh detektor untuk diukur. Pengukuran absorbansi dapat dibuat dengan absorbansi maupun fluorosensi (Rohman, 2009).
Kebanyakan pengukuran densitometri dilakukan dengan cara absorbansi pada kisaran sinar UV (190-380 nm). Signal optik oleh adanya partikel pada lempeng menghasilkan persamaan matematis yang menyatakan hubungan antara absorbansi dengan konsentrasi analit melalui kurva kalibrasi (Rohman, 2009).
J. Validasi Metode Analisis
yang diharapkan dengan accuracy dan prescision yang memadai (Mulya dan
Suharman, 1995). Pedoman-pedoman kesahihan metode analisis didukung oleh parameter-parameter sebagai berikut.
1. Accuracy (kecermatan)
Accuracy berarti kedekatan hasil analisis yang diperoleh dengan
menggunakan metode tersebut terhadap harga yang sebenarnya. Accuracy
biasanya dinyatakan berupa persen perolehan kembali (recovery) dari
penambahan zat atau sampel yang diketahui kadarnya (Hong and Shah, 2000).
Akurasi dipengaruhi oleh sebaran galat (kesalahan) sistematik dalam seluruh tahapan analisis, sehingga untuk mengurangi kesalahan sistematik dapat dilakukan dengan menggunakan instrumen yang telah terkalibrasi, menggunakan pelarut dan pereaksi yang berkualitas untuk analisis, pengontrolan faktor-faktor yang dapat mempengaruhi hasil analisis, dan pelaksanaan penelitian sesuai prosedur yang ditetapkan (Harmita, 2004).
Tabel I. Kriteria akurasi yang masih dapat diterima menurut Harmita (2004)
Analit pada matrik sampel, dalam % Rata-rata yang diperoleh, %
100 98-102
2. Precision (ketelitian atau keseksamaan)
Precision merupakan ukuran kedekatan masing-masing hasil analisis
dari beberapa pengukuran di bawah kondisi analisis yang sama. Menurut USP 23/NF 18, presisi diartikan sebagai derajat antara hasil uji individual ketika prosedur diaplikasikan berulang kali dengan pengambilan sampel berulang kali dari sampel yang homogen (Hong and Shah, 2000).
Tabel II. Kriteria presisi yang masih dapat diterima menurut Harmita (2004) Analit pada matrik sampel, dalam % RSD yang diperoleh, %
> 1 2,5
0,1 5
0,0001 (1 ppm) 16
0,0000001 (1 ppb) 32
Untuk menentukan presisi metode analisis diperlukan penentuan berulang kali dengan prosedur yang sama. Makin kecil kadar zat yang dianalisis dan makin panjang tahapan prosedur metode analisis akan didapat harga simpangan relatif yang makin besar (Mulya dan Suharman, 1995). 3. Specificity (selektivitas)
Menurut USP 23/NF 18 (1995), Specificity adalah kemampuan
pengukuran analit secara akurat dan spesifik dengan kehadiran komponen lain dalam matriks sampel. Komponen tersebut mungkin mengandung zat aktif, ekspien, pengotor, dan produk degredasi.
Selektivitas seringkali dinyatakan sebagai derajat penyimpangan (degree of bias) metode pada sampel yang mengandung bahan tambahan,
seperti cemaran, hasil penguraian, senyawa yang memiliki kemiripan struktur, senyawa asing dibanding sampel yang tidak mengandung bahan tambahan (Harmita, 2004).
4. Sensitivity (Sensitivitas)
Sensitivity metode analisis adalah kemampuan metode analisis untuk
5. Linearity (rentang kelurusan)
Rentang kelurusan yaitu suatu rentangan kadar yang terendah sampai kadar tertinggi yang ditentukan dengan kadar dan direlasikan dengan serapan pada spektrofotometri dengan koefisien korelasi yang mendekati satu (Mulya dan Suharman, 1995).
Linearitas dinyarakan sebagai variansi di sekitar garis regresi yang dihitung dari data hasil uji analit pada berbagai konsentrasi menggunakan persamaan matematik. Persamaan matematik dalam penentuan linearitas adalah melalui persamaan garis lurus dengan metode kuadrat terkecil antara hasil uji dengan konsentrasi analit (Harmita, 2004).
K. Landasan Teori
Radikal bebas merupakan senyawa yang tidak stabil karena memiliki satu elektron yang tidak berpasangan. Radikal bersifat sangat reaktif untuk menstabilkan kekurangan elektronnya dengan menyerang elektron pada molekul di sekitarnya, namun dapat menyebabkan kerusakan sel sehingga timbul penyakit-penyakit degeneratif. Dengan demikian, diperlukan adanya senyawa yang dapat menghambat reaksi radikal bebas yang disebut sebagai antioksidan.
Metode yang digunakan untuk menguji aktivitas antioksidan adalah metode DPPH. DPPH merupakan radikal bebas yang memberikan serapan kuat pada panjang gelombang 517 nm. Senyawa antioksidan akan berpasangan dengan elektron bebas DPPH yang menyebabkan penurunan absorbansi. Dari nilai perubahan absorbansi dapat dihitung IC50yang merupakan parameter kemampuan (aktivitas) dari antioksidan tersebut yang dapat menghambat 50% senyawa radikal.
Kapsaisin yang merupakan senyawa dalam cabai rawit yang mempengaruhi aktivitas antioksidan, maka perlu ditetapkan kadar kapsaisin dalam cabai rawit putih. Kadar kapsaisin ditetapkan secara kromatografi lapis tipis – densitometri. Dari bercak yang dihasilkan, dapat ditetapkan kadarnya dengan
scanning bercak menggunakan densitometri.
L. Hipotesis
1. Ekstrak etanol buah cabai rawit putih mempunyai aktivitas antioksidan yang dapat dinyatakan sebagai IC50 menggunakan metode DPPH.
26 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian aktivitas antioksidan pada cabai rawit putih ini merupakan jenis penelitian eksperimental karena adanya perlakuan terhadap subyek uji dan menggunakan rancangan deskriptif.
B. Variabel
1. Variabel bebas pada penelitian ini adalah konsentrasi ekstrak etanol cabai rawit putih.
2. Variabel tergantung pada penelitian ini adalah aktivitas penangkapan radikal bebas DPPH (%IC) dan kadar kapsaisin dalam ekstrak etanol cabai rawit
putih.
3. Variabel pengacau terkendali pada penelitian ini adalah lokasi pengambilan sampel, umur tanaman, bobot sampel tanaman yang digunakan, dan waktu pemanenan.
C. Definisi Operasional
1. Cabai rawit putih adalah buah yang belum masak dari tanaman cabai rawit (Capsicum frutescens L.) yang didapat dari Pasar Beringharjo, Yogyakarta.
2. Ekstrak etanol buah cabai rawit putih adalah ekstrak kental yang didapat dari penyarian buah cabai rawit putih dengan alat Soxhlet menggunakan pelarut etanol.
3. Metode DPPH adalah metode pengujian aktivitas antioksidan dalam menangkap radikal bebas DPPH (1,1-difenil-2-pikrilhidrazil). Reaksi DPPH dengan senyawa antioksidan dapat menyebabkan perubahan intensitas warna sehingga absorbansi menurun.
4. Persen inhibition concentration (%IC) adalah persen yang menyatakan
kemampuan ekstrak etanol cabai rawit putih dalam menangkap radikal bebas DPPH.
5. Inhibition concentration 50 (IC50) merupakan nilai konsentrasi ekstrak etanol
cabai rawit putih yang dapat menangkap 50% radikal bebas DPPH.
D. Bahan dan Alat Penelitian 1. Bahan penelitian
Bahan yang digunakan pada penelitian ini, yaitu cabai rawit putih (Capsicum frutescens L.) yang didapat dari pasar Beringharjo, Yogyakarta,
(E.Merck), aseton (E.Merck), DPPH (Sigma-Aldrich), silica gel 60 F254 dan aluminium foil.
2. Alat penelitian
Alat-alat yang digunakan pada penelitian ini, yaitu vortex,
spektrofotometer UV-VIS (Shimadzu), blender, corong Buchner, oven,
mikropipet 10 – 1000 µL; 1 – 10 mL (Socorex), neraca analitik (Ohaus),
vacuum rotary evaporator (Junke & Kunkel), waterbath (Memmet),
densitometer (Shimadzu), tabung reaksi bertutup (Schott), dan alat-alat gelas yang lazim digunakan di laboratorium analisis (Pyrex dan Iwaki).
E. Tata Cara Penelitian 1. Determinasi buah
Determinasi buah cabai rawit putih yang digunakan berdasarkan pengamatan morfologinya dilakukan dengan membandingkan literatur dari Bosland, Bailey, Iglesias-Olivas (1996).
2. Pengumpulan bahan
3. Pembuatan ekstrak buah cabai rawit putih
Buah cabai rawit putih sebanyak 1 kg yang masih segar dibersihkan dan dicuci kemudian dibuang bagian tangkainya. Buah cabai rawit putih dikeringkan pada oven dengan suhu 500C, kemudian dihaluskan dengan
blender. Simplisia yang telah halus ditimbang sebanyak 25,0 g, dibungkus
menggunakan kertas saring. Simplisia dimasukkan dalam labu alas bulat berisi 350,0 mL etanol p.a. Soxheltasi dilakukan pada suhu 700C selama 8 jam sampai didapat hasil ekstrasi yang jernih. Filtrat hasil ekstraksi dipekatkan dengan menggunakan vacuum rotary evaporator.
4. Penentuan aktivitas antioksidan dengan metode DPPH
a. Pembuatan larutan DPPH, sebanyak 15,80 mg serbuk DPPH dilarutkan dengan 100,0 mL etanol p.a hingga diperoleh larutan DPPH dengan konsentrasi 0,4 mM. Larutan DPPH ditutup dengan aluminium foil dan
harus selalu dibuat baru.
b. Pembuatan larutan stok kapsaisin, sebanyak 2,50 mg kapsaisin dimasukkan dalam labu ukur 10 mL, kemudian dilarutkan etanol p.a hingga batas.
d. Pembuatan larutan uji, sejumlah 25,0 mg ekstrak buah cabai rawit putih ditimbang kemudian ditambahkan etanol p.a sampai 25,0 mL. Dari larutan tersebut diambil 1,0; 2,0; 3,0; 4,0 dan 5,0 mL kemudian ditambah etanol p.a sampai 10,0 mL sehingga diperoleh larutan uji dengan konsentrasi 100; 200; 300; 400 dan 500 µg/mL.
e. Uji pendahuluan aktivitas antioksidan, sebanyak 1,0 mL larutan DPPH dimasukkan ke dalam masing-masing tiga tabung reaksi. Masing-masing tabung reaksi ditambahkan 1,0 mL etanol p.a, larutan baku kapsaisin 75 µg/mL, dan larutan uji 300 µg/mL. Kemudian ditambahkan 3,0 mL etanol p.a pada masing-masing larutan. Larutan divortex selama 30 detik. Setelah 30 menit, perubahan warna yang terjadi diamati.
f. Penentuan panjang gelombang maksimum, pada 3 labu ukur 10 mL, dimasukkan masing-masing 0,50; 1,0; dan 1,50 mL larutan DPPH. Larutan ditambahkan dengan etanol p.a hingga tanda batas sehingga konsentrasi DPPH menjadi 0,020; 0,040; dan 0,080 mM. Larutan divortex selama 30 detik. Lalu dilakukan scanning panjang gelombang
serapan maksimum dengan spektrofotometer visibel pada panjang gelombang 400 – 600 nm.
g. Penentuan operating time (OT), sebanyak 1,0 mL larutan DPPH
absorbansinya dengan spektrofotometer visibel pada panjang gelombang 517 nm setiap 5 menit selama 1 jam.
h. Penentuan aktivitas antioksidan buah cabai rawit putih,
i. Pengukuran absorbansi larutan DPPH (kontrol), pada labu ukur 5 mL, dimasukkan sebanyak 1,0 mL larutan DPPH. Larutan ditambahkan dengan etanol p.a hingga tanda batas. Kemudian larutan tersebut dibaca absorbansinya pada saat OT dan panjang
gelombang maksimum. Pengerjaan dilakukan sebanyak tiga kali. Larutan ini digunakan sebagai kontrol untuk menguji larutan baku dan larutan uji.
ii. Pengukuran absorbansi larutan pembanding dan larutan uji, sebanyak 1,0 mL larutan DPPH dimasukkan ke dalam labu ukur 5 mL kemudian ditambah dengan 1,0 mL larutan pembanding dan larutan uji pada berbagai seri konsentrasi yang telah dibuat. Selanjutnya, larutan tersebut ditambah dengan etanol p.a hingga tanda batas. Larutan tersebut kemudian divortex selama 30 detik dan didiamkan selama OT. Larutan dibaca absorbansinya dengan
spektrofotometer visibel pada panjang gelombang maksimum hasil optimasi. Pengujian dilakukan dengan tiga kali replikasi.
i. Validasi metode uji aktivitas antioksidan, hasil dari prosedur 4h (i) dan (ii) divalidasi akurasi (% recovery), presisi (% CV), spesifisitas (spektra
kontrol), dan linearitas (nilai r).
Standar e iasi rata rata konsentrasi standar kapsaisin terukurS konsentrasi standar kapsaisin terukur
j. Estimasi aktivitas antioksidan, hasil dari prosedur 4h (i) dan (ii), dihitung nilai % IC dan IC50 untuk kapsaisin dan ekstrak buah cabai rawit putih.
5. Penentuan kadar kapsaisin
a. Pembuatan fase gerak, fase gerak yang digunakan pada penelitian ini dibuat dalam perbandingan, yaitu toluena - kloroform - aseton (45:25:30, v/v/v). Fase gerak dituang dalam bejana kromatografi kemudian kertas saring dimasukkan dalam bejana yang berisi fase gerak. Bejana ditutup rapat dan dibiarkan hingga seluruh kertas saring terbasahi oleh fase gerak.
b. Pembuatan larutan stok kapsaisin, baku kapsaisin ditimbang seksama 5,0 mg ditimbang seksama dan dimasukkan ke dalam labu takar 10 ml, kemudian dilarutkan dengan metanol sampai tanda batas sehingga diperoleh larutan stok kapsaisin 0,50 mg/mL.
c. Pembuatan larutan seri baku kapsaisin, larutan stok kapsaisin 0,50 mg/mL ditotolkan dengan volume 1,0; 2,0; 4,0; dan 8,0 L pada lempeng silika gel 60 F254 sehingga diperoleh seri kapsaisin dengan jumlah 0,5; 1,0; 2,0; dan 4,0 µg.
menit dan disaring dengan ayakan mesh 60. Larutan uji dibuat replikasi sebanyak tiga kali.
e. Penetuan kadar kapsaisin buah cabai rawit putih, sebanyak 10,0 L larutan uji ditotolkan pada lempeng silika gel 60 F254, kemudian dikembangkan dalam bejana kromatografi yang telah dijenuhkan dengan fase gerak toluena - kloroform - aseton (45:25:30, v/v/v). Pengembangan dilakukan setinggi 10 cm, lempeng silika kemudian dikeluarkan dan ditunggu hingga kering. Bercak diamati di bawah lampu UV 254 nm kemudian dianalisis dengan densitometer pada panjang gelombang maksimum. Bercak seri baku kapsaisin diukur AUC-nya dengan densitometri pada panjang gelombang pengamatan yang telah diperoleh. Puncak kromatogram dan nilai AUC yang muncul diamati. Dengan metode regresi linear, nilai seri kadar (µg/mL) diplotkan terhadap nilai AUC masing-masing seri larutan baku sehingga diperoleh persamaan y = bx + a dimana y merupakan nilai respon (AUC), x merupakan konsentrasi senyawa baku, a adalah intersept, dan b adalah slope. Kadar
kapsaisin dalam sampel ditentukan berdasarkan persamaan kurva baku yang paling baik.
F. Analisis Hasil
Aktivitas penangkapan radikal (%) dapat dihitung dengan menggunakan rumus :
bsorbansilarutan kontrol – bsorbansilarutan baku uji
Data aktivitas tersebut dianalisis dan dihitung nilai IC50 menggunakan
persamaan regresi linear dengan sumbu x adalah konsentrasi larutan uji maupun larutan baku kapsaisin, sedangkan sumbu y adalah % IC, Lalu dianalisis secara
statistik untuk menentukan ada atau tidak adanya perbedaan bermakna antara IC50
larutan baku kapsaisin dan larutan uji.
Uji kadar kapsaisin total dilakukan secara kromatografi lapis tipis. Nilai kadar tersebut didapatkan dari analisis data kromatogram dengan menggunakan densitometer. Analisis kualitatif dilakukan dengan membandingkan nilai Rf
sampel dengan nilai Rf baku. Analisis kuantitatif yang dilakukan berdasarkan data
35 BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Determinasi Buah
Determinasi buah cabai rawit putih merupakan tindakan awal yang dilakukan dalam suatu penelitian yang menggunakan buah sebagai bahan uji. Determinasi dilakukan untuk memastikan kebenaran identitas dari buah yang digunakan untuk penelitian dan menghindari adanya kesalahan pengambilan sampel. Jaminan kebenaran sampel sangat penting karena pada buah cabai terdiri dari berbagai macam spesies dan varietas. Masing-masing spesies buah cabai memiliki kandungan fitokimia yang berbeda. Determinasi buah dilakukan dengan membandingkan beberapa spesies dari Capsicum yang mengacu pada Bosland, Bailey, Iglesias-Olivas (1996).
Pembuktian determinasi buah dilakukan dengan membandingkan ciri-ciri dari buah dengan karakteristik spesies Capsicum pada literatur, yaitu panjang buah 2,5 – 5 cm; lebar buah 0,6 cm; bentuk buah datar (tidak bergelombang) dan tegak lurus; rasa buah sangat pedas; dan warna buah yang kuning kehijauan pucat saat belum masak. Morfologi buah cabai rawit putih yang digunakan sama dengan morfologi Tabasco (Capsicum frutescens L.) seperti yang terlihat di gambar 4..
Dari hasil determinasi tanaman, telah dibuktikan bahwa buah yang digunakan pada penelitian ini merupakan buah cabai rawit putih (Capsicum frutescens L.).
B. Hasil Pengumpulan Bahan
C. Hasil Preparasi Sampel
Buah cabai rawit putih yang telah dikumpulkan, dibersihkan, dibuang bagian tangkai, dan dicuci untuk menghilangkan pengotor-pengotor yang ada. Kemudian buah cabai rawit dikeringkan dengan pengovenan selama tiga hari pada suhu 40–600C agar menghilangkan kandungan air yang terdapat di dalam simplisia. Pengeringan simplisia dilakukan untuk mempermudah pembentukan serbuk simplisia yang kemudian diekstraksi dengan alat Soxhlet.
Simplisia yang telah dikeringkan kemudian diblender dengan tujuan memperkecil ukuran partikel sehingga meningkatkan jumlah senyawa dalam buah cabai rawit putih yang terekstraksi. Semakin kecil ukuran partikel, maka luas permukaan spesifik partikel semakin besar sehingga jumlah penyari yang kontak dengan serbuk simplisia semakin besar. Semakin banyak pelarut kontak dengan simplisia maka pelarut makin mudah menembus sel dan mudah menarik senyawa dalam sel untuk keluar sehingga jumlah senyawa yang terekstraksi makin banyak pula. Serbuk simplisia yang digunakan diayak dengan pengayak nomor 40 agar didapat serbuk dengan ukuran yang cukup halus.
Ekstraksi yang dilakukan adalah ekstraksi padat cair, yang melibatkan perpindahan senyawa dari padatan ke dalam cairan pengekstrak. Prinsip ekstraksi padat cair adalah adanya kontak antara pelarut dengan suatu padatan sehingga terjadi perpindahan massa zat aktif yang mula-mula berada dalam sel tanaman menuju pelarut dengan atau tanpa adanya faktor luar seperti aliran pelarut ataupun panas yang dapat mempercepat dan meningkatkan efektivitas ekstraksi (Rohman, 2009). Sampel yang digunakan adalah serbuk simplisia dari buah cabai rawit putih yang diekstrak menggunakan etanol.
Metode ekstraksi yang digunakan pada penelitian ini adalah penyarian dengan alat Soxhlet. Penyarian dengan alat Soxhlet merupakan metode ekstraksi dengan pelarut yang mengalir dan menggunakan panas. Penyarian dengan alat Soxhlet dipilih karena telah digunakan pada beberapa penelitian dan terbukti memberikan hasil ekstraksi kapsaisin dengan rendemen yang tinggi. Keuntungan dari penggunaan alat Soxhlet adalah pelarut yang digunakan hanya sedikit dibanding perklorasi dan pelarut selalu baru, hasil dari penguapan secara kontinyu sehingga hasil ekstraksi yang didapat lebih banyak dibanding ekstraksi menggunakan maserasi karena kemungkinan terjadinya kejenuhan pelarut pada metode maserasi.
pada suhu tersebut karena memberikan rendemen hasil ekstraksi yang tinggi (Boonkird, Phisalaphong, Phisalaphong, 2008) serta suhu 700C sudah dapat digunakan untuk menguapkan pelarut etanol tanpa merusak senyawa kapsaisin.
Ekstraksi dengan alat Soxhlet dihentikan setelah delapan jam, yaitu saat hasil penyarian pada tabung Soxhlet bening karena kapsaisin telah terekstraksi sempurna. Selama delapan jam ekstraksi, penyarian dengan Soxhlet mengalami sirkulasi pelarut sebanyak delapan kali. Hasil ekstraksi yang didapat berupa ekstrak cair berwarna hijau muda.
mendorong senyawa dalam sel untuk terekstraksi. Etanol dapat mendenaturasi enzim polifenol oksidase sehingga mencegah terjadinya browning.
Ekstrak yang didapat kemudian diuapkan pelarutnya dengan rotary vacuum evaporator pada kondisi suhu 600C. Prinsip dari rotary vacuum evaporator adalah destilasi hampa udara. Kondisi hampa udara dapat
mengakibatkan penurunan tekanan sehingga pelarut dapat teruapkan pada suhu di bawah titik didih pelarut. Penurunan titik didih dapat mencegah terjadinya kerusakan senyawa dalam pelarut akibat suhu yang terlalu tinggi. Hasil dari penguapan dengan rotary vacuum evaporator berupa ekstrak pekat etanol yang
kemudian diuapkan lagi pada waterbath sehingga didapat ekstrak kental etanol
buah cabai rawit putih. Bobot ekstrak etanol yang didapat adalah 4,0943 g sehingga rendemen yang didapat dari ekstrak etanol buah cabai rawit putih sebesar 13,65 %.
D. Hasil Uji Pendahuluan
penangkapan radikal bebas atau donor hidrogen sehingga menggambarkan kemampuan aktivitas antioksidan secara kualitatif.
Senyawa antioksidan pada ekstrak buah cabai rawit putih berperan sebagai radical scavenger. Atom hidrogen dari gugus fenol kapsaisin akan
ditangkap oleh DPPH yang bersifat radikal sehingga terbentuk kompleks DPPH-kapsaisin yang bersifat stabil (Ou, Huang, Woodill, Flanagan, and Deemer, 2002). Saat DPPH membentuk kompleks dengan antioksidan, maka terjadi perubahan warna.
Gambar 5. Hasil uji pendahuluan ekstrak etanol buah cabai rawit putih, kontrol negatif (DPPH), dan kontrol positif (kapsaisin)
E. Hasil Optimasi Metode Uji Aktivitas Antioksidan
1. Penentuan panjang gelombang maksimum (λ maks)
Gambar 6. Gugus kromofor dan gugus auksokrom DPPH (Witt, Lalk, Hager, dan Voigt, 2010)
Secara teoritis, panjang gelombang maksimum DPPH berkisar antara 515 – 520 nm (Molyneux, 2004). Pentingnya menetapkan panjang gelombang maksimum karena instrumen yang digunakan memiliki kondisi yang berbeda-beda dalam memberikan serapan. Oleh karena itu, panjang gelombang maksimum perlu diukur agar didapat absorbansi maksimum sebelum menetapkan aktivitas antioksidan. Larutan DPPH yang akan diukur panjang gelombang maksimumnya diencerkan dengan etanol sebagai kontrol sehingga dapat diketahui absorbansi maksimal tanpa adanya gangguan dari senyawa-senyawa lain. Panjang gelombang maksimum didapat dari scanning DPPH
dari 400 – 600 nm. Konsentrasi larutan DPPH yang digunakan adalah 0,020 mM; 0,040 mM; dan 0,080 mM.
Tabel III. Hasil pengukuran panjang gelombang maksimum DPPH Konsentrasi larutan
DPPH maksimum hasil scanning maksimum rata-rata
0,020 mM 517,5 nm
517,5 nm
0,040 mM 517,0 nm
Dari hasil scanning ketiga konsentrasi larutan DPPH, didapat
rata-rata panjang gelombang maksimum pada 517,5 nm. Panjang gelombang maksimum yang didapat tidak berbeda jauh dengan panjang gelombang maksimum DPPH secara teoritis, yaitu pada 517 nm (Azeez, Adeoye, Majolagbe, Lawal, Badiru, 2012). Dengan demikian, panjang gelombang yang digunakan untuk penetapan aktivitas antioksidan buah cabai rawit putih, yaitu 517,5 nm.
2. Penentuan operating time (OT)
Penentuan operating time perlu dilakukan untuk mengetahui waktu
yang optimal DPPH bereaksi dengan senyawa antioksidan. Reaksi antioksidan dengan DPPH yang optimal akan meminimalkan kesalahan yang terjadi karena reaksi kedua senyawa telah bereaksi sempurna. Saat reaksi berjalan sempurna, maka akan didapat absorbansi pengukuran yang stabil.
Operating time diperoleh dari pengukuran absorbansi DPPH yang telah
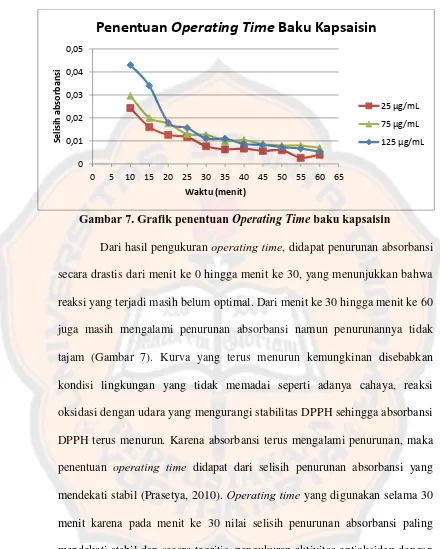
Gambar 7. Grafik penentuan Operating Time baku kapsaisin
Dari hasil pengukuran operating time, didapat penurunan absorbansi
secara drastis dari menit ke 0 hingga menit ke 30, yang menunjukkan bahwa reaksi yang terjadi masih belum optimal. Dari menit ke 30 hingga menit ke 60 juga masih mengalami penurunan absorbansi namun penurunannya tidak tajam (Gambar 7). Kurva yang terus menurun kemungkinan disebabkan kondisi lingkungan yang tidak memadai seperti adanya cahaya, reaksi oksidasi dengan udara yang mengurangi stabilitas DPPH sehingga absorbansi DPPH terus menurun. Karena absorbansi terus mengalami penurunan, maka penentuan operating time didapat dari selisih penurunan absorbansi yang
mendekati stabil (Prasetya, 2010). Operating time yang digunakan selama 30
menit karena pada menit ke 30 nilai selisih penurunan absorbansi paling mendekati stabil dan secara teoritis, pengukuran aktivitas antioksidan dengan metode DPPH digunakan operating time pada menit ke 30 (Andayani,
Penentuan Operating Time Baku Kapsaisin
25 µg/mL
75 µg/mL
F. Hasil Validasi Metode Uji Aktivitas Antioksidan
Tujuan metode validasi adalah menjamin bahwa metode yang digunakan dalam penelitian ini valid dan memenuhi persyaratan parameter yang telah ditetapkan sehingga memberikan hasil analisis sesuai dengan yang diharapkan. Dengan demikian perlu adanya suatu pedoman yang dapat menjamin kevalidan suatu metode analisis. Metode analisis yang valid dapat memberikan hasil analisis yang akurat dan memiliki ketelitian tinggi pada penelitian yang dilakukan. Validasi metode analisis tidak hanya menentukan karakteristik metode yang digunakan tetapi juga verifikasi bahwa metode yang digunakan sesuai dengan tujuan sehingga mengurangi kemungkinan terjadinya kesalahan pada sampel dengan jumlah yang sedikit.
Validasi metode yang digunakan pada penelitian ini dilakukan dengan menguji akurasi, presisi, linearitas, dan spesifisitas dari kurva standar baku kapsaisin. Validasi dilakukan sebanyak tiga kali replikasi. Untuk analisis, digunakan hasil dari validasi yang menunjukkan hasil terbaik.
Tabel IV. Hasil pengukuran absorbansi seri kurva baku kapsaisin yang direaksikan dengan DPPH
Hasil yang didapat dari seri kurva baku kapsaisin digunakan untuk pengukuran akurasi dan presisi. Persamaan regresi linier yang digunakan untuk menghitung akurasi dan presisi adalah persamaan regresi linier replikasi I karena memiliki nilai r yang paling baik dari ketiga replikasi. Nilai r yang baik adalah nilai r yang mendekati satu. Persamaan yang digunakan adalah y = -0,0143x + 0,6695 dengan nilai r 0,9999 (Tabel IV)
1. Spesifisitas metode uji aktivitas antioksidan
Spesifisitas merupakan kemampuan suatu metode untuk mengukur analit secara akurat tanpa adanya gangguan dari komponen-komponen lain seperti matriks sampel, produk hasil sintesis, eksipien, produk degradasi, dan senyawa pengotor (Gonzáles and Herrador, 2007). Spesifisitas pada penelitian ini dilakukan dengan membaca absorbansi senyawa-senyawa lain yang digunakan dalam uji aktivitas antioksidan pada panjang gelombang maksimum DPPH, yaitu 517,5 nm. Penentuan aktivitas antioksidan dilakukan dengan mengukur absorbansi DPPH, namun senyawa yang diukur tidak hanya DPPH sehingga perlu adanya pengujian spesifisitas dari metode. Adanya senyawa lain yang terbaca pada panjang gelombang yang digunakan akan mempengaruhi hasil pembacaan absorbansi sehingga memungkinkan ketidakvalidan metode.
Dari hasil scanning larutan baku kapsaisin (Lampiran 7), larutan uji
absorbansi yang terukur hanyalah absorbansi dari DPPH hasil reaksi. Berdasarkan hasil tersebut, metode uji aktivitas antioksidan memenuhi persyaratan validasi untuk spesifisitas.
2. Akurasi metode uji aktivitas antioksidan
Akurasi adalah ukuran derajat kedekatan hasil analisis dengan kadar analit secara teoritis yang dinyatakan dalam nilai persen perolehan kembali (% recovery). Hasil akurasi yang baik untuk sampel dengan konsentrasi analit
sebesar 10 ppm bila persen perolehan kembali yang didapat antara 90 – 107% (González and Herrador, 2007).
Pengukuran akurasi dilakukan pada baku kapsaisin peringkat rendah (5 µg/mL), peringkat sedang (15 µg/mL), dan peringkat tinggi (25 µg/mL) dengan replikasi sebanyak tiga kali.
Tabel V. Nilai perolehan kembali (% recovery) uji aktivitas antioksidan pada baku kapsaisin
Peringkat Kadar kapsaisin (µg/mL) % Recovery
Replikasi I Replikasi II Replikasi III
Rendah 5 99,72% 96,77% 104,96%
Sedang 15 100,65% 101,42% 106,34%
Tinggi 25 100,27% 97,61% 103,63%
yang baik sehingga pada penetapan aktivitas antioksidan ekstrak etanol buah cabai rawit putih dapat memberikan akurasi yang baik pula.
3. Presisi metode uji aktivitas antioksidan
Presisi merupakan derajat penyebaran hasil pengukuran sampel bila metode dilakukan secara berulang dan pengambilan sampel harus homogen (Harmita, 2004). Presisi dinyatakan berdasarkan nilai Coeffisient of Variant
(CV), semakin kecil nilai CV menunjukkan bahwa penyebaran hasil makin kecil yang berkorelasi dengan semakin baiknya presisi dari metode yang digunakan sehingga validitas metode memenuhi kriteria parameter yang ditentukan. Penentuan nilai presisi yang diperbolehkan bergantung pada kadar analit yang terdapat dalam matriks sampel, instrumen yang digunakan, dan tahapan prosedur penelitian yang dilakukan. Untuk sampel dengan konsentrasi ppm, batas CV yang diperbolehkan ≤ 5 (González and Herrador, 2007).
Pengukuran presisi dilakukan pada baku kapsaisin konsentrasi peringkat rendah (5 µg/mL), peringkat sedang (15 µg/mL), dan peringkat tinggi (25 µg/mL) dengan replikasi sebanyak tiga kali.
Tabel VI. Nilai CV uji aktivitas antioksidan pada baku kapsaisin Peringkat kapsaisin Kadar
tinggi dengan nilai CV berturut-turut 4,23%; 3,15%; dan 3,10%. Metode yang digunakan telah memenuhi batas presisi, yaitu kurang dari 5%, sehingga menjamin presisi yang baik pula pada uji aktivitas antioksidan ekstrak etanol buah cabai rawit putih.
4. Linearitas metode uji aktivitas antioksidan
Kurva kalibrasi pada metode ini merupakan hubungan proposional antara absorbansi analit (respon) dengan konsentrasi analit (Gonzáles and Herrador, 2007). Hasil dari kurva kalibrasi dapat diukur secara matematik sehingga menunjukkan linearitas metode. Linearitas dinyatakan dalam koefisien korelasi (r). Linearitas dikatakan semakin baik apabila koefisien korelasi dari kurva kalibrasi menunjukkan hasil semakin mendekati satu (Mulja dan Hanwar, 2003). Linearitas dilakukan dengan mengukur regresi linier dari konsentrasi baku kapsaisin dengan aktivitas antioksidan dengan tiga kali replikasi.
Dari pengukuran tiga replikasi, replikasi I menunjukkan nilai linearitas yang paling baik dengan nilai r = 0,9999, sedangkan nilai linearitas baku kapsaisin replikasi II dan III berturut-turut 0,9990 dan 0,9989. Nilai r ini memenuhi syarat linearitas yang baik, sehingga dapat disimpulkan bahwa metode ini memenuhi parameter linearitas.