Uji Kuantitatif Lipida 1 I. JUDUL : Uji Kuantitatif Lipida
II.TANGGAL PERCOBAAN : Senin, 30 Oktober 2017/Pukul 7.00 WIB
III. SELSESI PERCOBAAN : Senin, 30 Oktober 2017/Pukul 9.30 WIB
IV. TUJUAN :
Menentukan Angka Peroksida dan Asam Lemak Bebas
V. DASAR TEORI :
1. Lipida
Lipida (dari kata Yunani, Lipos, lemak) dikenal oleh masyarakat
awam sebagai minyak (organik, bukan minyak mineral atau minyak
bumi), lemak, dan lilin. Istilah "lipida" mengacu pada golongan senyawa
hidrokarbon alifatik nonpolar dan hidrofob, yang esensial dalam
menyusun struktur dan menjalankan fungsi sel hidup. Karena nonpolar,
lipida tidak larut dalam pelarut polar, seperti air atau alkohol, tetapi larut
dalam pelarut nonpolar, seperti eter atau kloroform.
Lipid didefinisikan sebagai senyawa organik yang terdapat dalam
alam sertatak larut dalm air, tetapi larut dalam pelarut organik non-polar
seperti suatuhidrokarbon atau dietil eter. Lipid berbeda dengan biomolekul lain yang ada dialam (karbohidrat, protein, dan asam
nukleat), yaitu bahwa lipid bukanlah suatu polimer. Lemak dan minyak
merupakan salah satu kelas dalam lipid. Lemak dan minyak adalah
trigliserida, atau trigliserol. Perbedaan suatu lemak dengan minyak
bersifat sebarang: pada temperature kamar lemak berbentuk padat dan
minyak bersifat cair (Fessenden, 1982).
Lipid adalah senyawa organik berminyak atau berlemak yang
tidak larut dalam air, dapat diekstrak dari sel dan jaringan oleh pelarut
nonpolar, seperti kloroform dan eter. Asam lemak adalah komponen unit
pembangun pada hamper semua lipid. Asam lemak adalah asam organic
berantai panjang yang mempunyai atom karbondari 4 sampai 24. Asam
lemak memiliki gugus karboksil tunggal dan ekor hidrokarbon nonpolar
yang panjang. Hal ini membuat kebanyakan lipid bersifat tidak larut
Uji Kuantitatif Lipida 2 Fungsi lipid :
Penyimpan energi
Transportasi metabolik sumber energi
Sumber zat untuk sintese bagi hormon, kelenjar empedu serta
menunjang proses pemberian signal signal transducing
Struktur dasar atau komponen utama membran semua jenis sel.
Pelindung organ tubuh dan Alat angkut vitamin larut lemak
Pembentukan sel dan sumber asam lemak esensial
Klasifikasi Lipid :
a. Klasifikasi menurut Lehninger
1. Lipid komplek (yang bisa mengalami saponifikasi) contoh :
trigliserida
2. Lipid sederhana (yang tidak bisa mengalami saponifikasi karena
tidak mengandung gliserol). contoh : terpen, steroid, prostaglandin dll.
b. Klasifikasi menurut Bloor
1. Lipid sederhana : ester asam lemah dengan berbagai alkohol
2. Lemak : ester asam lemak dengan gliserol lemak cair dikenal
sebagai minyak
3. Malam/wax : ester asam lemak dengan alkohol monohidrat Berat
Molekul tinggi
4. Lipid komplek : ester asam lemak yang mengandung gugus lain
disamping alkohol dan asam lemak
5. Fosfolipid : mengandung residu as fosfat. contoh : gliserofosfo
lipid, sfingosin
6. Glukolipid : mengandung karbohidrat. contoh : sfingosin
7. Lipid komplek lainnya. contoh : sulfo lipid, amino lipid,
lipoprotein
8. Derivat lipid /prekursor lipid
Bentuk ini mencakup : asam lemak, gliserol, steroid, aldehid
Uji Kuantitatif Lipida 3 Ada 2 bentuk Asam Lemak
Asam lemak, terdiri atas asam lemak jenuh dan asam lemak tak jenuh.
Asam lemak merupakan asam monokarboksilat rantai panjang. Adapun
rumus umum dari asam lemak adalah :
Rentang ukuran dari asam lemak adalah C12 sampai dengan C24. Ada dua
macam asam lemak yaitu:
1. Asam lemak jenuh (saturated fatty acid). Asam lemak ini tidak
memiliki ikatan rangkap. Asam lemak jenuh merupakan asam lemak
yang mengandung ikatan tunggal pada rantai hidrokarbonnya. Asam
lemak jenuh mempunyai rantai zig-zig yang dapat cocok satu sama lain,
sehingga gaya tarik vanderwalls tinggi, sehingga biasanya berwujud
padat. Misalnya,
Asam butirat, CH3(CH2)2CO2H
Asam palmitat, CH3(CH2)14CO2H
Asam stearat, CH3(CH2)16CO2H
Asam laurat, CH3(CH2)10CO2H
2. Asam lemak tak jenuh (unsaturated fatty acid). Asam lemak tak jenuh
merupakan asam lemak yang mengandung satu ikatan rangkap pada
rantai hidrokarbonnya .asam lemak dengan lebih dari satu ikatan dua
tidak lazim,terutama terdapat pada minyak nabati,minyak ini disebut
poliunsaturat. Trigliserida tak jenuh ganda (poliunsaturat) cenderung
berbentuk minyak sedangkan trigliserida jenuh cenderung berbentuk
lemak. Misalnya,
CH3(CH2)5CH=CH(CH2)7CO2H (asam palmitoleat)
CH3(CH2)7CH=CH(CH2)7CO2H (asam oleat)
CH3(CH2)4CH=CHCH2CH=CH(CH2)7CO2H (asam linoleat)
Pada hakekatnya, asam lemak tidak jenuh memiliki titik lebur
yang lebih rendah dibandingkan asam lemak jenuh. Contohnya, asam
Uji Kuantitatif Lipida 4
monoenoat (asam oleat) melebur pada 13 oC dan suatu bentuk dienoat
(asam linoleat) pada -5 oC.
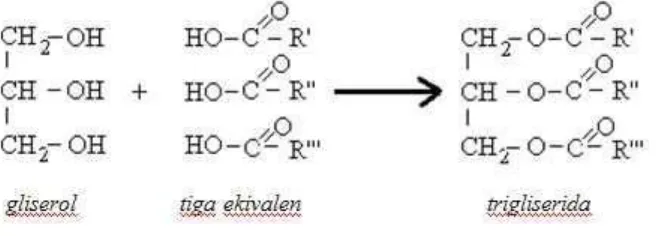
Lipida yang paling sederhana dan paling banyak mengandung
asam lemak sebagai asam lemak penyusunnya adalah trialgliserol,
juga sering disebut lemak, lemak netral, atau trigliserida. Jenis lipid
ini merupakan contoh lipid yang paling sering dijumpai baik pada
manusia, hewan, dan tumbuhan. Triasilgliserol adalah komponen utama
dari lemak penyimpan atau depot lemak pada sel tumbuhan dan
hewan, tetapi umumnya tidak dijumpai pada membran.
Triasilgliserol adalah molekul hidrofobik nonpolar, karena molekul
ini tidak mengandung muatan listrik atau gugus fungsional dengan
polaritas tinggi.
Gambar stukturasam lemak
Lipid mempunyai sifat umum sebagai berikut menurut (Poedjiadi,
2009):
a. Tidak larut dalam air
b. Larut dalam pelarut organik seperti benzena, eter, aseton, kloroform,
dan karbontetraklorida
c. Mengandung unsur-unsur karbon (C), hidrogen (H), dan oksigen
(O). Kadang-kadang juga mengandung nitrogen (N) dan fosfor (P).
d. Bila dihidrolisis akan menghasilkan asam lemak
Uji Kuantitatif Lipida 5 Berbeda dengan karbohidrat dan protein, lipid bukan suatu polimer,
tidak mempunyai satuan yang berulang. Pembagian yang didasarkan
atas hasil hidrolisisnya (Poedjiadi, 2009).
Adapun sifat-sifat fisika lipid adalah (Poedjiadi dan Supriyanti,
2009):
a. Tidak larut dalam air, tetapi larut dalam satu atau lebih dari satu
pelarut organik misalnya eter, aseton, kloroform, benzena, yang sering juga disebut “pelarut lemak”.
b. Ada hubungan dengan asam-asam lemak atau esternya.
c. Mempunyai kemungkinan digunakan oleh makhluk hidup.
Reaksi- Reaksi Lipid
1. Hidrogenasi Minyak.
Ikatan rangkap pada minyak dapat dijenuhkan dengan cara
hidrogenasi sehingga menjadi lemak padat.Untuk menunjukkan derajat
ketidakjenuhan asam (banyaknya ikatan rangkap) dinyatakan dengan
angka yod, yaitu angka yang menyatakan banyaknya gram yodium yang
dapat diadisikan pada 100 gram lemak. 2. Reaksi Penyabunan.
Reaksi antara gliserida dengan basa menghasilkan sabun dikenal
dengan reaksi penyabunan (saponifikasi). Sabun yang mengandung
logam Na (dari lemak + NaOH) disebut sabun keras (sabun cuci), sedang
yang mengandung logam K disebut sabun lunak (sabun mandi). Untuk
menyatakan banyaknya asam yang terkandung dalam lemak digunakan
reaksi penyabunan dengan KOH, yang dinyatakan dengan angka
penyabunan, yaitu angka yang menunjukkan berapa mg KOH yang
digunakan uuntuk menyabunkan 1 gram lemak.
3. Reaksi Hidrolisis.
Dengan adanya enzim lipase, lemak atau minyak dapat
Uji Kuantitatif Lipida 6 2. Angka Peroksida
Angka peroksida didefiniskan sebagai jumlah meq peroksida
dalam setiap 1000 g (1 kg) minyak atau lemak. Angka peroksida ini
menunjukan tingkat kerusakan lemak atau minyak. Angka peroksida
adalah indeks jumlah lemak atau minyak yang telah mengalami oksidasi.
Angka peroksida sangat penting untuk identifikasi tingkat oksidasi
minyak. Minyak yang mengandung asam- asam lemak tidak jenuh dapat
teroksidasi oleh oksigen yang menghasilkan suatu senyawa peroksida.
Bilangan peroksida adalah indeks jumlah lemak atau minyak yang
telah mengalami oksidasi Angka peroksida sangat penting untuk
identifikasi tingkat oksidasi minyak. Minyak yang mengandung asam-
asam lemak tidak jenuh dapat teroksidasi oleh oksigen yang
menghasilkan suatu senyawa peroksida. Cara yang sering
digunakan untuk menentukan angka peroksida adalah dengan metoda
titrasi iodometri. Penentuan besarnya angka peroksida dilakukan dengan
titrasi iodometri. Salah satu parameter penurunan mutu minyak goreng
adalah bilangan peroksida.
Peroksida dapat mempercepat proses timbulnya bau tengik dan
flavor yang tidak dikehendaki dalam bahan pangan. Jika jumlah peroksida
lebih dari 100 meq peroksida/kg minyak akan bersifat sangat beracun dan
mempunyai bau yang tidak enak. Kenaikan bilangan peroksida merupakan
indikator bahwa minyak akan berbau tengik.
Bilangan Peroksida =
Penentuan bilangan peroksida didasarkan pada pengukuran
sejumlah iod yang dibebaskan dari kalium iodide melalui reaksi oksidasi
oleh peroksida pada suhu ruang didalam medium asam asetat/ chloroform.
Proses oksida dapat berlangsung bila terjadi kontak antara sejumlah
oksigen dengan minyak dan lemak. Minyak kelapa sawit yang berkualitas
baik menurut SNI 3741: 2013 mempunyai angka peroksida tidak lebih dari
Uji Kuantitatif Lipida 7 3. Asam Lemak Bebas (FFA)
Asam lemak bebas adalah asam lemak yang berada sebagai asam
bebas tidak terikat sebagai trigliserida. Asam lemak bebas dihasilkan
oleh proses hidrolisis dan oksidasi biasanya bergabung dengan lemak
netral. Hasil reaksi hidrolisa minyak sawit adalah gliserol dan ALB.
Reaksi ini akan dipercepat dengan adanya faktor-faktor panas, air,
keasaman, dan katalis (enzim). Semakin lama reaksi ini berlangsung,
maka semakin banyak kadar ALB yang terbentuk.
Asam lemak bebas berasal dari proses hidrolisa minyak ataupun
dari kesalahan proses pengolahan. Kadar asam lemak yang tinggi berarti
kualitas minyak tersebut semakin rendah. Penentuan kadar asam lemak
bebas dalam minyak ini bertujuan untuk menentukan kualitas minyak.
Penentuan kadar asam lemak bebas ini berdasarkan pada jenis asam lemak
apa yang paling dominan dalam sampel minyak atau lemak yang
digunakan. Penentuan asam lemak dapat dipergunakan untuk mengetahui
kualitas dari minyak atau lemak, hal ini dikarenakan bilangan asam dapat
dipergunakan untuk mengukur dan mengetahui jumLah asam lemak bebas dalam suatu bahan atau sample.Semakin besar angka asam maka dapat
diartikan kandungan asam lemak bebas dalam sample semakin tinggi,
besarnya asam lemak bebas yang terkandung dalam sampel dapat
diakibatkan dari proses hidrolisis ataupun karena proses pengolahan yang
kurang baik.
Penentuan presentase asam lemak bebas (FFA) berprinsip pada
titrasi sampel yang dilarutkan dengan alkohol netral oleh NaOH untuk
menetralkan asam lemak bebas. NaOH digunakan untuk membuat asam
lemak bebas dapat larut dalam air dan terpisah dari lemaknya
(Winarno,1984). Penggunaan larutan NaOH 0,1 N pada titrasi larutan
sampel berfungsi membuat larutan terbebas dari lemak yang terkandung
dalam minyak curah yang digunakan (Aisyah,2010). Menurut spesifikasi
SNI nomor 01/3741/2002 bahwa minyak goreng yang aman dikonsumsi
memiliki persentase FFA sebesar 0,3%. Perhitungan persentase FFA dapat
Uji Kuantitatif Lipida 8
% FFA = X 100%
4. Minyak Jelantah
Minyak jelantah adalah minyak goreng yang digunakan berulang
kali untuk menggoreng, dan biasanya berwarna menjadi kehitaman.
Menggunakan minyak jelantah untuk menggoreng berbahaya bagi
kesehatan. Dalam kehidupan sehari-hari, jika kita membeli makanan atau
gorengan, bisa saja minyak yang digunakan adalah minyak jelantah.
Minyak jelantah mengandung berbagai radikal bebas, yang setiap
saat siap untuk mengoksidasi organ tubuh secara perlahan. Minyak
jelantah kaya akan asam lemak bebas. Terlalu sering mengkonsumsi
minyak jelantah dapat menyebabkan potensi kanker meningkat. Menurut
para ahli kesehatan, minyak goreng hanya boleh digunakan dua sampai
empat kali menggoreng (Winarno, 1999).
5. Minyak Kelapa Sawit
Minyak kelapa sawit dapat dihasilkan dari inti kelapa sawit yang
dinamakan minyak inti kelapa sawit (palm kernel oil) . Faktor-faktor
yang mempengaruhi kualitas minyak sawit adalah air dan kotoran, asam
lemak bebas, bilangan peroksida dan daya pemucatan. Faktor-faktor lain
adalah titik cair, kandungan gliserida padat, refining loss, plasticity dan
spreadability, sifat transparan, kandungan logam berat dan bilangan
penyabunan. Semua faktor ini perlu dianalisis untuk mengetahui mutu
Uji Kuantitatif Lipida 9
Salah satu asam lemak yang paling mudah diperoleh adalah asam
palmitat atau asam heksadekanoat. Asam palmitat adalah asam lemak
jenuh yang tersusun dari 16 atom karbon (CH3(CH2)14COOH).
Tumbuh-tumbuhan dari famili Palmaceae, seperti kelapa (Cocos nucifera) dan
kelapa sawit (Elaeis guineensis) merupakan sumber utama asam lemak ini.
6. Titrasi Iodometri
Prinsip kerja dari titrasi iodometri (redoksimetri) termasuk dalam
titrasi dengan cara tidak langsung, dalam hal ini ion iodide sebagai
pereduksi diubah menjadi iodium yang nantinya dititrasi dengan larutan
baku Na2S2O3. Cara ini digunakan untuk penentuan oksidator H2O2. Pada
oksidator ditambahkan larutan KI dan asam sehingga akan terbentuk
iodium yang akan dititrasi dengan Na2S2O3. Sebagai indikator, digunakan
larutan kanji. Indikator penambahan amilum yang dilakukan saat
mendekati titik akhir titrasi dimaksudkan agar amilum tidak membungkus
iod karena akan menyebabkan amilum sukar dititrasi untuk kembali ke
senyawa semula. Proses titrasi harus dilakukan sesegera mungkin, hal ini
disebabkan sifat I2 yang mudah menguap. Pada titik akhir titrasi iod yang
terikat juga hilang bereaksi dengan titran sehingga warna biru mendadak
hilang dan perubahannya sangat jelas. Penggunaan indikator ini untuk
memperjelas perubahan warna larutan yang terjadi pada saat titik akhir
titrasi. Sensitivitas warnanya tergantung pada pelarut yang digunakan.
Kompleks iodium-amilum memiliki kelarutan yang kecil dalam air,
Uji Kuantitatif Lipida 10 VI. ALAT DAN BAHAN
A. ALAT
1. Gelas kimia 100 mL 1 buah
2. Pipet tetes 8 buah
3. Buret 1 set
4. Erlenmeyer 3 buah
5. Gelas ukur 50 mL 1 buah
6. Gelas ukur 10 mL 2 buah
B. BAHAN
1. Minyak/lemak
2. Larutan asam asetat – kloroform (3 : 2)
3. Larutan KI jenuh
4. Na2S2O3 0,1 N
5. Larutan pati 1 %
6. Larutan NaOH 0,1 N
7. Larutan baku oksalat 0,1 N
8. Indikator PP 1 %
Uji Kuantitatif Lipida 11 VII. ALUR PERCOBAAN
1. Penentuan Angka Peroksida
a. Larutan sampel
5 gram sampel (minyak / lemak)
- Dimasukkan dalam erlenmeyer
- Ditambah 30 mL larutan asam asetat kloroform
- Digoyangkan sampai bahan larut sempurna
- Ditambahkan 0,5 mL larutan KI jenuh
- Didiamkan selama 20 menit dengan sesekali
diigoyang
- Ditambahkan 30 mL aquades
- Dititrasi dengan larutan Na2S2O3 0,1 N sampai
warna kuning hampir hilang
Volume Na2S2O3 0,1 N
- Ditambahkan 0,5 mL larutan pati 1 %
- Dititrasi kembali dengan Na2S2O3 0,1 N
sampai jernih
Volume Na2S2O3 0,1 N
- Dihitung angka peroksidanya
Uji Kuantitatif Lipida 12
b. Larutan Blanko
5 gram aquades
- Dimasukkan dalam erlenmeyer
- Ditambah 30 mL larutan asam asetat kloroform
- Digoyangkan sampai bahan larut sempurna
- Ditambahkan 0,5 mL larutan KI jenuh
- Didiamkan selama 20 menit dengan sesekali
diigoyang
- Ditambahkan 30 mL aquades
- Dititrasi dengan larutan Na2S2O3 0,1 N sampai
warna kuning hampir hilang
Volume Na2S2O3 0,1 N
- Ditambahkan 0,5 mL larutan pati 1 %
- Dititrasi kembali dengan Na2S2O3 0,1 N
sampai jernih
Volume Na2S2O3 0,1 N
- Dihitung angka peroksidanya
Uji Kuantitatif Lipida 13
2. Penentuan Asam Lemak Bebas (FFA) pada Sampel
Penentuan Asam Lemak Bebas (FFA) pada Blanko 6 gram sampel minyak
- Dimasukkan dalam erlenmeyer
- Ditambahkan 10 mL alkohol 96 %
- Ditambahkan 3 tetes indikator PP
- Dititrasi dengan larutan NaOH 0,1 N yang telah
distandarisasi sampai merah jambu dan
perubahan tidak hilang selama 30 menit
Volume NaOH
6 gram aquades
- Dimasukkan dalam erlenmeyer
- Ditambahkan 10 mL alkohol 96 %
- Ditambahkan 3 tetes indikator PP
- Dititrasi dengan larutan NaOH 0,1 N yang telah
distandarisasi sampai merah jambu dan
perubahan tidak hilang selama 30 menit
Uji Kuantitatif Lipida 14 VIII.DATA PENGAMATAN
No. perc.
Prosedur Perobaan Hasil Pengamatan Dugaan/ Reaksi
Kesimpulan
1. Penentuan Angka Peroksida ( larutan sampel) Sebelum :
Minyak Sawit :
Standart angka peroksida yang
berbahaya menurut SNI 2013 adalah
yang telah dilakukan,
diperoleh angka
peroksida dari sampel
minyak sawit sebesar
204,2618 meq/kg. Jadi
- Dimasukkan dalam erlenmeyer
- Ditambah 30 ml larutan asam asetat-kloroform
(3:2)
- Digoyangkan sampai bahan larut sempurna
- Ditambah 0,5 ml larutan KI jenuh
- Didiamkan selama 20 menit dengan sesekali
digoyang
- Ditambah 30 ml aquades
- Dititrasi dengan larutan Na2S2O3 0,1 N sampai warna kuning hampir hilang
5 gram sampel minyak/lemak
-Ditambah 0,5 ml larutan pati 1%
Uji Kuantitatif Lipida 15 Lapisan atas : kuning
kecoklatan
Lapisan bawah :
larutan kuning
Minyak sawit +
asetat-kloroform+ KI jenuh :
terbentuk 2 lapisan.
Lapisan atas : Larutan
kuning kecoklatan
Lapisan bawah :
larutan kuning.
Didiamkan 20 menit :
terbentuk 2 lapisan.
Lapisan atas : larutan
berwarna kuning
Lapisan bawah :
larutan tidak berwarna
Ditambah aquades :
Dititrasi dengan
Uji Kuantitatif Lipida 16 1. V. Na2S2O3 : 1,4 mL
2. V. Na2S2O3 : 1,6 mL
3. V. Na2S2O3 : 1,4 mL
Pengulangan 1,2, dan
3 terbentuk 2 lapisan.
Lapisan atas : larutan
berwarna kuning
kecoklatan (++)
lapisan bawah : larutan
berwarna kuning keruh
Ditambah larutan pati
1 % :
pengulangan 1,2 dan 3
: Larutan terbentuk 2
lapisan. Lapisan atas :
larutan berwarna
kuning kecoklatan (+)
lapisan atas : larutan
berwarna kuning muda
Uji Kuantitatif Lipida 17 dengan . Na2S2O3 :
1. V. Na2S2O3:10,1 mL
2. V. Na2S2O3:10,7 mL
3. V. Na2S2O3:10,6 mL
Pengulangan 1,2, dan
3 terbentuk 2 lapisan.
Lapisan atas : larutan
berwarna kuning
kecoklatan
lapisan bawah : larutan
tidak berwarna
Bilangan peroksida :
1. 195,4917 meq/kg
2. 211,7459 meq/kg
3. 205,5478 meq/kg
Rata-rata bilangan
peroksida : 204,2618
Uji Kuantitatif Lipida 18 Penentuan Bilangan Peroksida pada Blanko
- Ditambah 30 ml larutan asam asetat kloroform
- Digoyangkan sampai bahan larut sempurna
- Ditambah 0,5 ml larutan KI jenuh
- Ditambah 0,5 ml larutan pati 1%
- Dititrasi kembali dengan Na2S2O3 0,1 N
sampai jernih
Volume Na2S2O3 0,1 N
Uji Kuantitatif Lipida 19
1. Penentuan Asam Lemak Bebas pada Sampel (FFA)
tidak berwarna
Berdasarkan SNI NO 01/3741/2002
tentang standar mutu minyak goreng
kadar asam lemak yang baik kurang
dari 0,3%. Asam lemak bebas
menunjukkan hasil kerusakan
minyak.
- Ditambahkan 10 ml larutan alkohol 96%
- Ditambahkan 5-8 tetes indikator PP
- Dititrasi dengan larutan NaOH 0,1 N yang telah
distandarisasi sampai merah jambu dan
perubahan tidak hilang selama 30 detik
- Diulang 3x
Uji Kuantitatif Lipida 21 Penentuan Asam Lemak Bebas (FFA) dalam Blanko
pengulangan :
- Ditambahkan 10 ml larutan alkohol 96%
- Ditambahkan 5-8 tetes indikator PP
- Dititrasi dengan larutan NaOH 0,1 N yang telah
distandarisasi sampai merah jambu dan
perubahan tidak hilang selama 30 detik
Uji Kuantitatif Lipida 22 IX. ANALISIS DAN PEMBAHASAN
Pada percobaan ini bertujuan untuk menentukan angka peroksida dan
persen asam lemak bebas yang terkandung di dalam suatu sampel minyak kelapa
sawit (Sunco) yang telah digunakan beberapa kali. Percobaan uji kuantitatif
lipida ini, digunakan minyak “Sunco” sebagai sampel yang akan diuji oleh
praktikan. Sebelumnya minyak telah digunakan untuk menggoreng beberapa
kali.
1. Angka Peroksida
Penentuan bilangan atau angka peroksida didasarkan pada pengukuran
sejumlah iod yang dibebaskan dari kalium iodida melalui reaksi oksidasi oleh
peroksida pada suhu ruang di dalam medium asam asetat atau kloroform.
Proses oksida ini dapat berlangsung jika terjadi kontak atau sentuhan antara
sejumlah oksigen dengan minyak dan lemak. Minyak kelapa sawit yang
berkualitas baik menurut SNI 3741: 2013 mempunyai angka peroksida tidak
lebih dari 10 meq/kg.
Untuk melakukan percobaan ini hal pertama yang dilakukan yaitu
menyiapkan 3 buah erlenmeyer dan sampel minyak sawit yang telah dipakai beberapa kali atau minyak jelantah. Dalam percobaan ini sampel minyak
jelantah yang kami gunakan berwarna coklat pekat. Selanjutnya ditimbang
sebanyak ± 5 gram pada masing-masing erlenmeyer. Dimana diperoleh massa
pada erlenmeyer 1 sebesar 5,013 gram, pada erlenmeyer 2 massanya sebesar
5,006 gram, Erlenmeyer 3 massanya sebesar 5,011 gram.
Selanjutnya, pada masing-masing erlenmeyer yang telah berisi sampel
minyak, ditambahkan 30 mL larutan asam asetat-kloroform (larutan tak
berwarna) sehingga terbentuk 2 lapisan, pada lapisan atas larutan berwarna
kuning kecoklatan sedangkan lapisan bawah laruan berwarna kuning muda.
Kemudian digoyang-goyangkan hingga sampel minyak terlarut sempurna.
Sehingga terbentuk larutan berwarna kuning kecoklatan yang homogen, artinya
minyak telah larut sempurna. Fungsi penambahan larutan asam
asetat-kloroform yaitu memberikan suasana asam dan sebagai pelarut senyawa non
polar. Minyak terlarut dalam larutan tersebut karena minyak merupakan
Uji Kuantitatif Lipida 23 terdapat di alam serta tidak larut dalam air, tetapi larut dalam pelarut organik
non-polar misalnya, Kloroform (CHCl3), benzena dan hidrokarbon lainnya,
lemak dan minyak dapat larut dalam pelarut tersebut karena minyak
mempunyai polaritas yang sama dengan pelarut tersebut.
Setelah itu ditambahkan 0,5 mL larutan KI jenuh (larutan tidak
berwarna). Fungsi penambahan KI jenuh adalah untuk menentukan bilangan
peroksida, karena KI akan dioksidasi peroksida menjadi I2 oleh peroksida.
Semakin banyak iod (I2) yang dibebaskan maka semakin banyak peroksida dari
dalam minyak.
Setelah ditambahkan larutan KI jenuh, kemudian campuran didiamkan
selama 20 menit sambil sesekali digoyangkan. Sehingga terbentuk larutan
berwarna jingga. Fungsi pendiaman selama 20 menit dan sesekali digoyangkan
yaitu agar reaksi oksidasi berjalan sempurna. Dimana larutan KI jenuh akan
teroksidasi oleh peroksida dari minyak dan membebaskan iod. Terbentuknya
iod ditandai dengan perubahan warna menjadi kekuningan.
Kemudian setelah 20 menit, ke dalam masing-masing labu Erlenmeyer
ditambahkan 30 mL aquades (cairan tak berwarna) yang bersifat polar. Fungsi
penambahan aquades yaitu untuk memisahkan fasa air dan fasa organik. Dalam hal ini senyawa yang bersifat polar akan larut dalam aquades, namun
iod yang dibebaskan tidak akan larut dalam air karena iod bersifat nonpolar
dan larut dalam KI.
Setelah itu iod yang dibebaskan dititrasi dengan larutan Na2S2O3 0,1 N
(larutan tak berwarna) sampai warna kuning hampir hilang, sehingga terbentuk
2 fasa dimana bagian atas larutan menjadi larutan berwarna kuning kecoklatan
jernih ,sedangkan pada fasa bagian bawah berupa larutan berwarna kuning
minyak. Larutan Na2S2O3 merupakan agen pereduksi yang biasa digunakan
untuk mereduksi iod (I2) menjadi ion I-. Warna kuning hampir hilang karena
iod bereaksi dengan Na2S2O3 membentuk iodida. Titrasi dihentikan setelah
warna kuning hampir hilang, setelah itu ditambahkan indikator larutan pati 1%
(larutan tak berwarna) sebanyak 0,5 mL. Penambahan pati 1% berfungsi
sebagai indikator untuk mengetahui titik akhir titrasi. Pada percobaan ini
Uji Kuantitatif Lipida 24 iodin tinggal sedikit dan larutan yang dititrasi berwarna kuning. Apabila
larutan pati ditambahkan di awal titrasi, ketika masih banyak terdapat iodin
dalam larutan, maka sejumlah besar senyawa iod-kanji yang terbentik akan
bereaksi lambat dengan tiosulfat (Widodo,2010). Kemudian larutan tersebut
dititrasi kembali dengan larutan Na2S2O3 0,1 N hingga terbentuk larutan jernih.
Setelah larutan dititrasi dan terbentuk dua lapisan , lapisan atas kuning jernih
dan lapisan bawah berwarna kuning minyak. Hal ini mengindikasikan bahwa
titik akhir titrasi telah tercapai karena semua iod telah bereaksi dengan larutan
Na2S2O3 0,1 N sehingga larutan berubah menjadi jernih. Kemudian titrasi
dihentikan. Kemudian didapat volume pada pengulangan 1 hingga 3 diperoleh
secara berturut-turut yakni sebanyak 1,4 mL, 1,6 mL, 1,4 mL.
Berikut reaksi yang terjadi :
CH3COOH (aq) + CHCl3 (aq) CH3CH2CCl3 (aq) + O2 (g)
Dari hasil yang diperoleh, dapat ditentukan angka peroksida dari
sampel minyak jelantah dari sawit yaitu dengan rumus :
Bilangan peroksida =
Dalam percobaan ini didapat angka peroksida pada pengulangan 1
hingga 3 secara berturut-turut sebanyak 195,4917 meq/kg ; 211,7459 meq/kg ;
dan 205,5478 sehingga diperoleh juga rata-rata bilangan peroksida pada
sampel sebanyak 204,2618 meq/kg. Hal ini menandakan bahwa minyak
sampel yang digunakan telah melebihi ambang batas dari ketentuan atau
standart yang ditetepatkan SNI yaitu sebesar 10 meq/kg. Maka minyak ini
tidak layak digunakan karena mengandung angka peroksida yang tinggi dan
Uji Kuantitatif Lipida 25 dengan udara, adanya pemanasan, dan penambahan air. Hal tersebut
menandakan bahwa minyak telah rusak. Pada minyak yang rusak terjadi
proses oksidasi, polimerisasi dan hidrolisis. Proses tersebut menghasilkan
peroksida yang bersifat toksik dan asam lemak bebas yang sukar dicerna oleh
tubuh.
Larutan Blanko
Percobaan selanjutnya yaitu pembuatan larutan blanko. Larutan blanko
menggunakan aquades. Pertama menimbang aquades sebanyak ± 5 gram
(cairan tak berwarna) dan diperoleh massa untuk blanko sebanyak 5,014 gram.
. Kemudian ditambahkan 30 mL larutan asetat-kloroform (larutan tidak
berwarna) sambil digoyang-goyangkan membentuk larutan tak berwarna.
Kemudian ditambah dengan 0,5 mL larutan KI jenuh larutan tetap tidak
berwarna. Setelah itu, didiamkan selama 20 menit sambil sesekali
digoyangkan, campuran berupa larutan yang tidak berwarna. Selanjutnya
larutan tersebut ditambahkan dengan 30 mL aquades (cairan tidak berwarna)
dan tidak terjadi perubahan. Kemudian dititrasi dengan larutan Na2S2O3 0,1 N
larutan tidak mengalami perubahan yakni larutan tetap tidak berwarna. Lalu dibaca skala volume pada buret dipeoleh voleme sebnyak 0,8 mL. Langkah
selanjutnya pada larutan tersebut ditambah 0,5 mL larutan pati 1% (tidak
berwarna), dan tidak terjadi perubahan. Hal tersebut dikarenakan tidak
terbentuknya kompleks pati-iodin, karena dalam pembuatan larutan blanko ini,
tidak terjadi reaksi oksidasi dari I- menjadi I2. Sehingga tidak ada iod yang
dibebaskan. Setelah itu dititrasi kembali dengan larutan Na2S2O3 0,1 N hingga
terbentuk larutan jernih. Kemudian dibaca skala volume pada buret diperoleh
volume sebanyak 0,9 mL. Sehingga diperoleh volume total Na2S2O3 0,1 N
larutan menjadi jernih tidak berwarna. Sehingga diperoleh volume total
sebanyak 1,7 mL.
Berdasarkan rumus berikut :
Bilangan peroksida =
Larutan blanko digunakan sebagai faktor pengurang dalam menghitung
Uji Kuantitatif Lipida 26 larutan blanko ini hasilnya tidak lebih besar dari jumlah volume Na2S2O3 pada
sampel, karena seperti yang telah dijelaskan sebelumnya larutan blanko
merupakan faktor pengurang.
2. Persen Asam Lemak Bebas pada Sampel (%FFA)
Penentuan presentase asam lemak bebas (FFA) berprinsip pada titrasi
sampel yang dilarutkan dengan alkohol netral oleh NaOH untuk menetralkan
asam lemak bebas. NaOH digunakan untuk membuat asam lemak bebas dapat
larut dalam air dan terpisah dari lemaknya (Winarno,1984). Penggunaan
larutan NaOH 0,1 N pada titrasi larutan sampel berfungsi membuat larutan
terbebas dari lemak yang terkandung dalam minyak jelantah atau minyak
bekas yang beberapa kali digunakan (Aisyah,2010). Menurut spesifikasi SNI
nomor 01/3741/2002 bahwa minyak goreng yang aman dikonsumsi memiliki
persentase FFA kurang dari 0,3%.
Pada percobaan ini bertujuan untuk menentukan asam lemak bebas
(FFA) dari sampel yang telah diuji. Asam lemak bebas ditentukan sebagai
kandungan asam lemak yang terdapat paling banyak dalam suatu minyak tertentu. Asam lemak dalam sampel minyak kelapa sawit yang digunakan yaitu
asam palmitat dengan rumus CH3(CH2)14COOH.
Pertama, disiapkan 3 buah erlenmeyer. Kemudian ditimbang massa
sampel dalam erlenmeyer masing-masing sebanyak ± 6 gram, dimana
diperoleh berat massa sampel 1 = 6,002 gram, berat massa sampel 2 = 6,010
gram, berat massa sampel 3 = 6,003 gram minyak jelantah dari kelapa sawit.
Kemudian pada labu erlenmeyer 1,2, dan 3 masing-masing
ditambahkan 10 mL alkohol 96% (larutan tak berwarna). Fungsi penambahan
alkohol adalah untuk melarutkan lemak atau minyak dalam sampel agar
dapat bereaksi dengan basa alkali. Setelah itu ditambahkan indikator PP
sebanyak 5 tetes larutan kuning keruh. Penambahan PP berfungsi sebagai
indikator titik akhir titrasi. Indikator PP merupakan indikator bersifat asam
yang digunakan sebagai indikator untuk menentukan titik akhir titrasi ditandai
dengan terbentuknya larutan berwarna merah muda ketika bereaksi dengan
Uji Kuantitatif Lipida 27 Kemudian larutan tersebut dititrasi dengan larutan NaOH 0,1 N (larutan
tak berwarna). Sehingga terjadi perubahan warna larutan pada lapisan atas
berupa larutan berwarna merah jambu dan lapisan bawah berupa larutan
berwarna kuning. Dalam hal ini larutan NaOH bereaksi dengan asam lemak
bebas pada minyak membentuk garam, ketika semua asam lemak telah
bereaksi dengan NaOH maka kelebihan NaOH akan bereaksi dengan indikator
PP. Warna larutan bagian atas menjadi merah jambu dikarenakan PP bereaksi
dengan Na+ membentuk PP-Na yang berwarna merah jambu. Setelah terjadi
perubahan menjadi berwarna merah jambu, kemudian titrasi dihentikan dan
dibaca skala volume pada buret. Sehingga diperoleh volume NaOH 0,1 N yang
digunakan pada :
Labu Erlenmeyer 1 = 0,3 mL
Labu Erlenmeyer 2 = 0,2 mL
Labu Erlenmeyer 2 = 0,2 mL
Beriku reaksi yang terjadi :
CH3(CH2)14COOH (s) + CH3CH2OH (aq) CH3(CH2)14COOCH2 CH3 (aq) +
H2O (l)
CH3(CH2)14COO CH2 CH3 (aq) + NaOH CH3(CH2)14COONa (aq) +
CH3CH2OH (aq)
Berdasarkan data yang diperoleh maka dapat dihitung persentase asam
lemak bebas pada sampel minyak dengan rumus:
Sehingga dari hasil perhitungan diperoleh :
%FFA labu erlenmeyer 1 : 0,0863%
%FFA labu erlenmeyer 2 : 0,043 %
%FFA labu erlenmeyer 3 : 0,043 %
Rata-rata %FFA sampel : 0,057%
Berdasarkan SNI No. 01/3741/2002 tentang standar mutu minyak goreng
dan batas maksimal persentase kadar asam lemak bebas pada minyak goreng
maksimal sebesar 0,3%. Sehingga dapat diketahui bahwa dalam pengujian ini
Uji Kuantitatif Lipida 28 0,3%
Jika angka lemak bebas tinggi hal tersebut menunjukkan kualitas minyak
yang tidak baik. Asam lemak bebas menunjukkan sejumlah asam lemak bebas
yang dikandung oleh minyak yang rusak, terutama karena peristiwa oksidasi dan
hidrolisis.
Larutan Blanko
Pada percobaan selanjutnya yaitu pembuatan larutan blanko. Dalam hal
ini pembuatan larutan blanko menggunakan aquades. Hal pertama yang harus
dilakukan yakni menimbang aquades sebanyak ± 6 gram (cairan tak berwarna).
Dalam hal ini massa yang diperoleh sebesar 6,002 gram. Selanjunya dimasukkan
ke dalam labu Erlenmeyer lalu ditambahkan 10 mL alkohol 96% (larutan tak
berwarna). Fungsi penambahan alkohol adalah untuk melarutkan lemak atau
minyak dalam sampel agar dapat bereaksi dengan basa alkali. Setelah itu
ditambahkan indikator PP sebanyak 5 tetes larutan tidak berwarna. Penambahan
PP berfungsi sebagai indikator titik akhir titrasi. Indikator PP merupakan
indikator bersifat asam yang digunakan sebagai indikator untuk menentukan titik
akhir titrasi ditandai dengan terbentuknya larutan berwarna merah jambu ketika bereaksi dengan basa.selanjutnya dititrasi dengan menggunakan larutan NaOH
(larutan tidak berwarna) larutan berubah warna yang awalnya larutan tidak
berwarna lalu berubah menjadi merah jambu. Volume NaOH yang digunakan
untuk larutan berubah warna menjadi merah jambu yakni sebesar 0,1 mL. dalam
percobaan ini, pembuatan larutan blanko memiliki perlakuan yang sama seperti
pembuatan sampel hanya saja, sampel minyak dignatikan dengan aquades.
Pembuatan larutan blanko ini bertujan untuk membandingkan dengan hasil yang
diperoleh pada sampel.
X. KESIMPULAN
Dari percobaan yang telah dilakukan, dapat disimpulkan bahwa:
1. Didapatkan rata-rata bilangan peroksida sebesar 204,2618 meq/g dari
sampel minyak sawit yang praktikan gunakan sehingga ketengikan minyak
Uji Kuantitatif Lipida 29
2. Didapatkan persentase asam lemak bebas (FFA) sebesar 0,057% dari
sampel minyak yang digunakan, sehingga minyak goreng yang diuji masih
layak digunakan lagi dikarenakan belum terlalu tingginya tingkat
kerusakan lemak pada minyak curah tersebut. Yakni menurut teori sebesar
Uji Kuantitatif Lipida 30 XI. JAWABAN PERTANYAAN
1.Tuliskan semua reaksi yang menyertai uji asam lemak pada percobaan
ini.
Persen Asam Lemak Bebas (FFA)
CH3(CH2)14COOH (s) + CH3CH2OH (aq) CH3(CH2)14COOCH2 CH3(aq)
+ H2O (l)
CH3(CH2)14COOCH2CH3 (aq) + NaOH(aq) CH3(CH2)14COONa(aq) +
CH3CH2OH (aq)
2. Sebutkan yang termasuk asam lemak essensial bagi tubuh. Mengapa
asam arakidonat bukan merupakan asam lemak essensial?
Asam lemak esensial merupakan sebutan bagi asam lemak yang tidak
dapat dibuat sendiri oleh suatu spesies hewan (termasuk manusia), atau dapat
dibuat tetapi tidak mencukupi kebutuhan minimal yang diperlukan untuk
memenuhi fungsi fisiologinya. Hal ini terjadi karena spesies yang
bersangkutan tidak memiliki,atau memiliki tetapi kurang fungsional, enzim
yang bertanggung jawab dalam melakukan sintesis asam lemak tersebut. Bagi setiap spesies, asam lemak yang esensial berbeda-beda. Bagi
manusia, asam lemak esensial mencakup golongan asam lemak tak jenuh
jamak (polyunsaturated fatty acids, PUFA) tipe cis, khususnya dari kelompok
asam lemak Omega-3, seperti misalnya asam α-linolenat (ALA), Asam
eikosapentaenoat (EPA), dan asam dokosaheksaenoat (DHA), dan asam
lemak Omega-6, seperti misalnya asam linoleat. Tubuh manusia tidak
Uji Kuantitatif Lipida 31 merombak PUFA.
Asam arakidonat bukan merupakan lemak essensial karena tubuh
dapat mensintesisnya.Turunan asam lemak yang berasal dari ALE adalah
asam arakidonat dari asam linoleat dan eikosapentanoat (EPA) dan
dekosaheksanoat (DHA). Ketiga asam lemak tersebut bukan asam lemak
esensial karena tubuh dapat mensintetis. Minyak ikan laut yang hidup di
perairan dalam kaya EPA dan DHA.
3. Apa perbedaan asam lemak jenuh dan tak jenuh pada proses oksidasi ?
a. Asam lemak jenuh merupakan asam lemak dimana dua atom hidrogen
terikat pada satu atom karbon. Dikatakan jenuh karena atom karbon
telah mengikat hidrogen secara maksimal. (C-C)
b. Asam lemak tak jenuh Asam lemak jenuh merupakan asam lemak yang
memiliki ikatan rangkap. Dalam hal ini, atom karbon belum mengikat
atom hidrogen secara maksimal karena adanya ikatan rangkap. (C=C)
4. Apa perbedan antara minyak dan lemak ditinjau dari struktur
molekulnya?
Berdasarkan strukturnya, maka minyak dan lemak dapat dibedakan
sebagai berikut :
1. Minyak memiliki struktur ikatan rangkap pada rantai karbon C.
2. Sedangkan lemak tidak mempunyai ikatan rangkap pada rantai
Uji Kuantitatif Lipida 32 DAFTAR PUSTAKA
Chafid, Achmas. 2010. Modifikasi Tpung Sagu Menjadi Maltodekstrin
Menggunakan enzim α-amilase. Semarang : Jurusan Teknik Kimia FT UNDIP.
Dwidjoseputro, D., 1992, Pengantar Fisiologi Tumbuhan, Gramedia Pustaka
Utama, Jakarta
Lehninger, A.L., 1997, Dasar-dasar Biokimia Jilid 1, Erlangga, Jakarta.
Page, D, S., 1989. Prinsip-Prinsip Biokimia edisi II. Erlangga, Jakarta
Pine, S.H., Hendrickson, J.B., Cram, D.J., dan Hammond, G.S. 1988. Kimia
Organik II, Penerbit ITB, Bandung.
Poedjiadi, A. 1994, Dasar-dasar Biokimia, UI-Press, Jakarta
Poedjiadi, Anna. 2006. Dasar-Dasar Biokimia. Jakarta : UI Press
Sadikin, Mohamad. 2002. Biokimia Enzim. Jakarta : Widya Medika.
Simanjuntak, M.T. 2003. Biokimia Bandung : ITB
Soewoto, Hafiz, dkk. 2000. Biokimia Eksperimen Laboratorium.Jakarta: Widya
Uji Kuantitatif Lipida 33 LAMPIRAN PERHITUNGAN
1. Menentukan bilangan peroksida
Diketahui:
1. Bilangan peroksida pengulangan 1
Bilangan peroksida =
= 195,4917 meq/kg
2. Bilangan peroksida penguulangan 1
Bilangan peroksida =
Uji Kuantitatif Lipida 34
3. Bilangan peroksida penguulangan 1
Bilangan peroksida =
= 205,5478 meq/kg
Rata-rata bilangan peroksida =
= 204,2618 meq/kg
Jadi, bilangan peroksida sampel minyak sawit pada percobaan ini sebesar
204,2618 meq/kg.
2. Menentukan persen asam lemak bebas (%FFA)
Uji Kuantitatif Lipida 35
= 0,043%
3. %FFA =
= 0,043%
Rata-rata %FFA =
= 0,057%
Uji Kuantitatif Lipida 36 LAMPIRAN FOTO
Alat dan Bahan
Gambar Keterangan Gambar Keterangan
Alkohol 96% Larutan KI
jenuh
Indikator PP NaOH 0,1 M
Minyak sawit dengan 2
kali penggorengan
Beberapa buah
Uji Kuantitatif Lipida 37
4 buah erlenmeyer Gelas ukur
1 set statif dan klem
beserta buret Gelas kimia
1. Penentuan bilangan peroksida dan blanko
minyak sawit
ditimbang dalam neraca analitis
sebanyak 5 gram
Ditambah 30
mL larutan asam
asetat-kloroform
Ditambah 0,5 mL KI
jenuh
Ditambah 30
Uji Kuantitatif Lipida 38 Dititrasi dengan
Na2S2O3
Ditambah
larutan pati 1%
Dititrasi kembali
dengan Na2S2O3
Dihasilkan
warna 1a,1b,1c
(terbentuk 2
lapisan), dan
larutan blanko
(larutan tidak
berwarna)
2. Penentuan asam lemak bebas pada sampel dan blanko
minyak sawit
ditimbang dalam
neraca analitis
sebanyak 6 gram
Ditambahkan
10 mL alkohol