PENETAPAN KEASAMAN PADA MADU
TUGAS AKHIR
Oleh:
SONANG MIDA ROGATE 162410017
PROGRAM STUDI DIPLOMA III ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2020
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan berkat dan kasih karuania-Nya sehingga penulis dapat menyelesaikan Tugas Akhir yang berjudul “Penetapan Keasaman Pada Madu”.
Tujuan penyusunan Tugas Akhir ini sebagai salah satu persyaratan untuk menyelesaikan pendidikan Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara. Tugas Akhir ini disusun berdasarkan apa yang penulis lakukan pada Praktek Kerja Lapangan (PKL) di Balai Riset dan Standarisasi Industri Medan.
Selama penulisan Tugas Akhir ini penulis menyadari sepenuhnya bahwa tanpa bantuan dan bimbingan dari berbagai pihak, penulis tidak akan dapat menyelesaikan Tugas Akhir ini sebagaimana mestinya. Oleh karena itu, penulis megucapkan terimakasih kepada semua pihak yang telah membantu penulis dalam menyelesaikan Tugas Akhir ini, yaitu kepada :
1. Ibu Prof. Dr. Masfria, M.S., Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara.
2. Bapak Popi Patilaya, S.Si,. M.Sc. Apt., selaku Ketua Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara.
3. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Dosen Pembimbing yang telah banyak meluangkan waktu dalam memberikan nasihat dan bimbingan hingga Tugas Akhir ini selesai.
4. Bapak M. Nilzam, selaku Kepala Baristand Industri Medan, serta seluruh staf dan pegawai.
5. Teristimewa kepada orang-orang terkasih yang selalu menjadi bagian inspirasi: Ayahanda B.P. Simangunsong dan Ibunda Sonta Nainggolan yang senantiasa mendoakan, memberi semangat dan mendukung penulis dalam keadaan apapun.
6. Sahabat-sahabat seperjuangan yang selalu ada dalam suka dan duka, yaitu: Menanti Sianipar, Evi Theresia Silaban, Putri Natalia Simanjuntak, Sabrina Gracela Simamora, Desy Fransiska Sitanggang, dan Kristin Theresia Hutagalung, terima kasih buat persahabatan yang terjalin selama ini dan terima kasih buat segala bantuan semangat dan dukungan yang diberikan dalam penyelesaian Tugas Akhir ini maupun dalam kuliah selama ini.
7. Teman-teman mahasiswa D3 Analis Farmasi dan Makanan angkatan 2016 untuk kebersamaan, kerjasama dan kenangan selama 3 tahun masa perkuliahan.
Penulis menyadari bahwa penulisan Tugas Akhir ini kurang dari sempurna.
Oleh karena itu, kritik dan saran yang bersifat membangun sangat penulis harapkan demi penyempurnaan Tugas Akhir ini. Semoga Tugas Akhir ini dapat bermanfaat bagi ilmu pengetahuan dan pendidikan.
Medan, Mei 2019 Penulis
Sonang Mida Rogate
NIM 162410017
PENETAPAN KEASAMAN PADA MADU
ABSTRAK
Latar Belakang: Menurut Standar Nasional Indonesia (SNI), madu adalah cairan alami yang umumnya mempunyai rasa manis yang dihasilkan lebah madu (Apis sp.) dari sari bunga tanaman (floral nectar) atau bagian lain dari tanaman (ekstra floral). Madu yang bermutu harus memenuhi persyaratan mutu yang telah ditentukan oleh SNI, salah satunya yaitu keasaman madu.
Tujuan: Penelitian ini bertujuan untuk menentukan keasaman pada madu hutan dan madu sachet.
Metode: Bahan yang digunakan dalam penelitian ini adalah madu hutan dan madu sachet. Penetapan keasaman madu dilakukan secara Titrasi Asidi- Alkalimetri dengan menggunakan fenolftalein sebagai indikator dan larutan standar baku NaOH 0,1 N sebagai pentiter. Penelitian dilakukan di Balai Riset dan Standardisasi (Baristand) Industri Medan. Penetapan keasaman madu dilakukan dengan cara sampel yang sudah dilarutkan air dan ditambahkan indikator dititrasi dengan larutan pentiter hingga mencapai titik akhir titrasi yang ditandai dengan terjadinya perubahan warna analit kemudian dihitung nilai keasaman berdasarkan ketentuan SNI 01-3534-2013.
Hasil: Hasil penelitian penetapan keasaman pada madu menunjukkan bahwa nilai keasaman madu hutan dan madu sachet merek B sebesar 48,39 ml NaOH 0,1 N/
kg dan 38,07 ml NaOH 0,1 N/ kg, memenuhi syarat sesuai dengan SNI 01-3534- 2013 yaitu maksimal 50 ml NaOH 0,1 N/ kg, sedangkan nilai keasaman madu sachet merek A sebesar 80,89 ml NaOH 0,1 N/ kg, tidak memenuhi syarat.
Kesimpulan: Nilai keasaman madu hutan dan madu sachet merek B memenuhi persyaratan SNI 01-3534-2013, sedangkan nilai keasaman madu sachet A tidak memenuhi persyaratan SNI 01-3534-2013.
Kata kunci: madu, keasaman, metode asidi-alkalimetri.
DAFTAR ISI
HALAMAN PENGESAHAN ... ii
SURAT PERNYATAAN ORISINALITAS ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2 Tujuan ... 2
1.3 Manfaat ... 2
BAB II TINJAUAN PUSTAKA ... 3
2.1 Madu ... 3
2.1.1 Pengertian madu ... 3
2.1.2 Cara madu terbentuk ... 3
2.1.3 Komposisi madu ... 4
2.1.4 Manfaat madu ... 5
2.1.5 Persyaratan mutu madu ... 6
2.2 Keasaman Madu ... 7
2.3 Metode Penentuan Keasaman Madu Secara Titrasi Asidi-Alkalimetri ... 11
BAB III METODE PENELITIAN... 14
3.1 Tempat Penelitian ... 14
3.2 Alat ... 14
3.3 Bahan ... 14
3.4 Prosedur Kerja ... 14
3.4.1 Pembuatan larutan standar baku NaOH 0,1 N ... 14
3.4.2 Pembakuan larutan standar NaOH 0,1 N ... 14
3.4.3 Penetapan keasaman madu ... 15
BAB IV HASIL DAN PEMBAHASAN ... 16
4.1 Keasaman Pada Madu ... 16
BAB V KESIMPULAN DAN SARAN ... 19
5.1. Kesimpulan ... 19
5.2. Saran ... 19
DAFTAR PUSTAKA ... 20
LAMPIRAN ... 22
DAFTAR TABEL
Tabel
2.1. Komposisi Madu ... 5
2.2. Persyaratan Mutu Madu ... 6
2.3. Keasaman Pada Berbagai Jenis Madu ... 10
4.1. Keasaman Pada Madu ... 16
DAFTAR LAMPIRAN
Lampiran
1. Daftar Spesifikasi Sampel ... 22
2. Data Perhitungan Pembakuan Larutan Standar NaOH 0,1 N ... 23
3. Contoh Perhitungan Penetapan Keasaman Pada Madu ... 24
4. Hasil Penetapan Keasaman Pada Madu... 25
5. Gambar Hasil Titrasi ... 26
BAB I PENDAHULUAN
1.1 Latar Belakang
Madu adalah cairan alami yang umumnya mempunyai rasa manis yang dihasilkan lebah madu (Apis sp.) dari sari bunga tanaman (floral nectar) atau bagian lain dari tanaman (ekstra floral). Madu disimpan dalam sel-sel sarang.
Kemudian, madu akan mengalami ekstraksi air, pembentukan monosakarida, dan pengayaan dengan campuran aromatik. Setelah 3-7 hari, lebah menutup sel dengan malam yang akan mematangkannya menjadi madu siap panen. Madu mengandung gula fruktosa dan glukosa, air, kalori, enzim, asam amino esensial, vitamin dan mineral (SNI, 2013; Suranto, 2007).
Madu termasuk makanan yang berpotensi basa, sedangkan daging, telur, lemak dan biji-bijian bersifat asam. Keasaman yang menetralisir garam basa sangat penting untuk tubuh kita, agar keseimbangan antara keasaman dan kebasaan tetap terpelihara. Ciri-rasa (flavor) dan aroma madu sebagian disumbang oleh asam-asam yang dikandungnya. Keasaman madu ditentukan oleh disosiasi hidrogen dalam larutan air. Saat ini, banyak sekali beredar madu palsu. Secara kasat mata, madu asli dan palsu sulit dibedakan, sehingga perlu pengujian kuantitatif untuk memastikan keaslian dan mutunya, salah satunya yaitu pengujian keasaman madu (Suranto, 2007; Sihombing, 1997; Sumoprastowo dan Suprapto, 1993).
Pemerintah telah menetapkan persyaratan mutu yang telah ditentukan dalam Standar Nasional Indonesia (SNI) 01-3534-2013. Oleh karena itu, penelitian ini
bertujuan untuk melakukan penetapan keasaman pada madu untuk mengetahui kualitas produk yang dipasarkan untuk dikonsumsi oleh masyarakat.
1.2 Tujuan
Adapun tujuan dari penetapan keasaman pada madu adalah untuk mengetahui apakah keasaman pada madu sudah memenuhi persyaratan yang sudah ditetapkan dalam Standar Nasional Indonesia (SNI).
1.3 Manfaat
Manfaat yang diperoleh dari penetapan keasaman pada madu adalah agar mengetahui bahwa madu hutan dan madu sachet yang beredar dipasaran memenuhi persyaratan keasaman madu yang ditetapkan dalam Standar Nasional Indonesia (SNI) sehingga produk layak dikonsumsi oleh masyarakat.
BAB II
TINJAUAN PUSTAKA
2.1 Madu
2.1.1 Pengertian madu
Madu adalah cairan kental yang dihasilkan oleh lebah dari nektar bunga.
Madu juga merupakan suatu campuran gula yang dibuat oleh lebah dari larutan gula alami hasil dari bunga yang disebut nektar. Madu yang dihasilkan oleh lebah ditampung dengan metode pengambilan modern berupa cairan jernih dan bebas dari benda asing (Molan, 1999).
Madu murni menurut Farmakope Indonesia adalah madu yang diperoleh dari sarang lebah madu. Apis mellifera dan spesies lainnya dimurnikan dengan pemanasan sampai 70oC. Setelah dingin, kotoran yang mengapung disaring.
Selanjutnya, madu dapat ditambah dengan air secukupnya untuk pengenceran sehingga bobot madu per ml memenuhi persyaratan yang telah dibakukan (Sarwono, 2001).
2.1.2 Cara madu terbentuk
Menurut Sihombing (1997), pada umumnya, madu dihasilkan terutama dari nektar bunga dan dari manna (honeydew). Lebah madu lebih suka akan nektar yang terdiri dari campuran berbagai gula. Lebah madu akan lebih tertarik juga oleh aroma nektar. Lebah madu menghasilkan madu yang dibuat dari nektar sewaktu musim tumbuhan berbunga. Sewaktu nektar dikumpulkan oleh lebah pekerja dari bunga, bahan tersebut masih mengandung air tinggi (80%) dan juga gula (sukrosa) tinggi. Setelah lebah menguah nektar menjadi madu, kandungan air jadi rendah dan sukrosa diubah menjadi fruktosa (gula buah; levulosa) dan
glukosa (dekstrosa). Air disingkirkan melalui evaporasi. Lebah membantu evaporasi dengan menempatkan nektar setengah penuh dalam sel-sel sarang agar luas permukaan meningkat dan lebah mengipaskan udara ke nektar segar tadi.
Bunyi dengung sayap mengipas nektar dalam sarang di sore hari adalah suatu tanda terdpat nektar baik dan segar. Lebah pekerja meminum madu dan memuntahkannya kembali sambil menambah enzim yang disebut enzim intervase.
Enzim ini akan mengubha sukrosa menjadi dekstrosa dan levulusa. Madu yang telah matang mengandung renadh air (17%) dan tinggi gula buah fruktosa. Air yang rendah akan menjaga madu dari kerusakan untuk jangka waktu relatif lama.
Dekstrosa akan membuat madu berkristal membentuk madu-premanen.
Kandungan akan menentukan lama dan bentuk kristal. Kristal desktrosa dapat dilelehkan dengan memanaskan madu sehingga kembali dalam keadaan cair.
2.1.3 Komposisi madu
Dalam air batang terdapat gula-gula yang bervariasi di dalam satu hari maupun dalam satu musim. Selain karbohidrat, air batang juga mengandung senyawa-senyawa lain dalam jumlah yang sedikit, yakni senyawa nitrogen, asam organik, lemak, asam nukleat, vitamin dan mineral. Dari senyawa nitrogen yang terbanyak adalah asam-asam amino dan amida, namun pada tumbuhan tertentu terdapat juga derivat urea, seperti asam alantoat,alantoin, sitrulin, dan putresin.
Kandungan madu antara lain air, fruktosa, glukosa, sukrosa dan asam bebas.
Madu juga mengandung enzim – enzim seperti diastase, glukosa oksidase, katalase serta vitamin A, betakaroten, vitamin B kompleks lengkap, vitamin C, D, E dan K. Selain itu juga dilengkapi mineral (Molan, 1999; Sihombing, 1997).
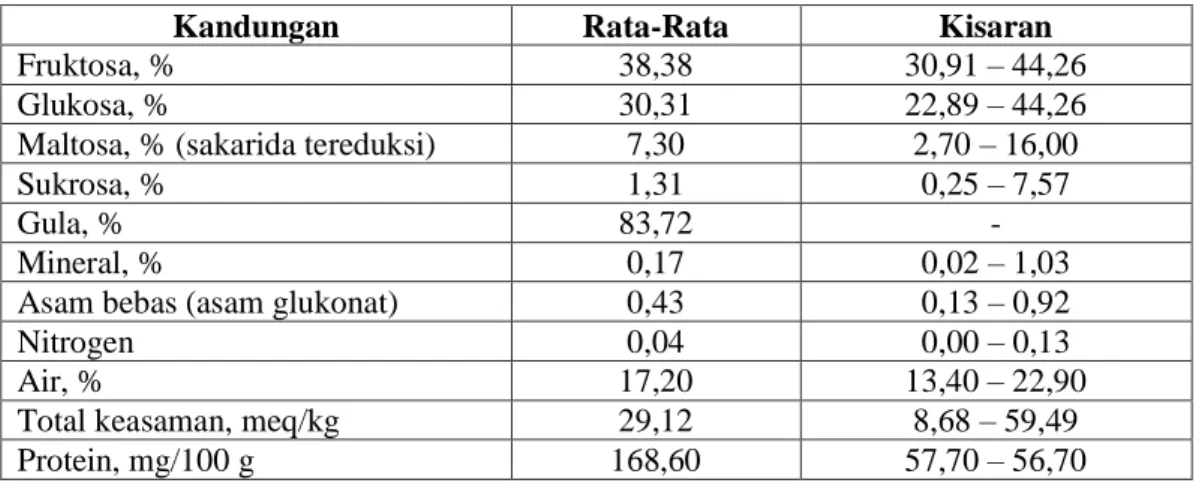
Komposisi madu dapat dilihat pada Tabel 2.1.
Tabel 2.1 Komposisi Madu
Kandungan Rata-Rata Kisaran
Fruktosa, % 38,38 30,91 – 44,26
Glukosa, % 30,31 22,89 – 44,26
Maltosa, % (sakarida tereduksi) 7,30 2,70 – 16,00
Sukrosa, % 1,31 0,25 – 7,57
Gula, % 83,72 -
Mineral, % 0,17 0,02 – 1,03
Asam bebas (asam glukonat) 0,43 0,13 – 0,92
Nitrogen 0,04 0,00 – 0,13
Air, % 17,20 13,40 – 22,90
Total keasaman, meq/kg 29,12 8,68 – 59,49
Protein, mg/100 g 168,60 57,70 – 56,70
Sumber: Suranto, 2007
2.1.4 Manfaat madu
Manfaat madu antara lain: (Molan, 1999).
a. Antimikroba mikroba. Madu memiliki aktivitas antimikroba, melawan peradangan dan infeksi. Didalam kandungan fisik dan kimiawi seperti kadar keasaman dan pengaruh osmotik berperan untuk membunuh.
b. Kemampuan penyembuh luka. Madu memiliki kemampuan untuk membersihkan luka, mengabsorbsi cairan edema di sekitar luka dan menambah nutrisi.
c. Luka bakar. Membangkitkan reaksi pencegahan untuk menyembuhkan luka bakar.
d. Antioksidan. Kandungan plasma darah semakin bertambah untuk melawan oksidasi dengan kadar yang lebih tinggi setelah minum madu. Dan terdapat juga fenolik didalam madu yang sangat efektif untuk ketahanan tubuh
Madu dipakai karena memiliki kelebihan-kelebihan yaitu: (Sarwono, 2001).
a. Madu mencegah terjadinya peragian dalam saluran pencernaan, dan kandungan gizinya cepat diserap oleh tubuh.
b. Madu bertindak sebagai sedatif sehingga dapat menyebabkan tidur nyenyak.
c. Madu memiliki efek laksatif sehingga mencegah rasa mual.
d. Di dalam tubuh, madu dimetabolisisr seperti halnya gula sehingga menyebabkan kadar snotonin (senyawa yang dapat meredakan aktivitas otak) dalam otak meninggi yang menginduksi pada relaksasi dan keinginkan untuk tidur.
Perusahaan-perusahaan kue terkadang menggunakan madu sebagai pengganti gula. Banyak obat pilek mengandung madu. Di Indonesia ada juga dikenal sate kambing madu sebagai obat, “sutema” (susu, telur, madu) sebagai minuman yang dijual di restoran ataupun warung makan (Sihombing, 1997).
2.1.5 Persyaratan mutu madu
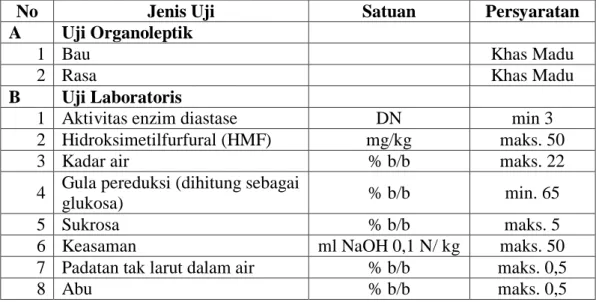
Kualitas madu merupakan pertimbangan yang sangat penting. Kualitas madu ditentukan oleh beberapa parameter diantaranya kadar air, keasaman, dan gula total yang merupakan parameter yang bertanggung jawab dalam menentukan stabilitas dan ketahanan terhadap kontaminasi mikroba selama penyimpanan (Fatma, dkk., 2017). Persyaratan mutu pada madu dapat dilihat pada Tabel 2.2.
Tabel 2.2 Persyaratan Mutu Pada Madu
No Jenis Uji Satuan Persyaratan
A Uji Organoleptik
1 Bau Khas Madu
2 Rasa Khas Madu
B Uji Laboratoris
1 Aktivitas enzim diastase DN min 3
2 Hidroksimetilfurfural (HMF) mg/kg maks. 50
3 Kadar air % b/b maks. 22
4 Gula pereduksi (dihitung sebagai
glukosa) % b/b min. 65
5 Sukrosa % b/b maks. 5
6 Keasaman ml NaOH 0,1 N/ kg maks. 50
7 Padatan tak larut dalam air % b/b maks. 0,5
8 Abu % b/b maks. 0,5
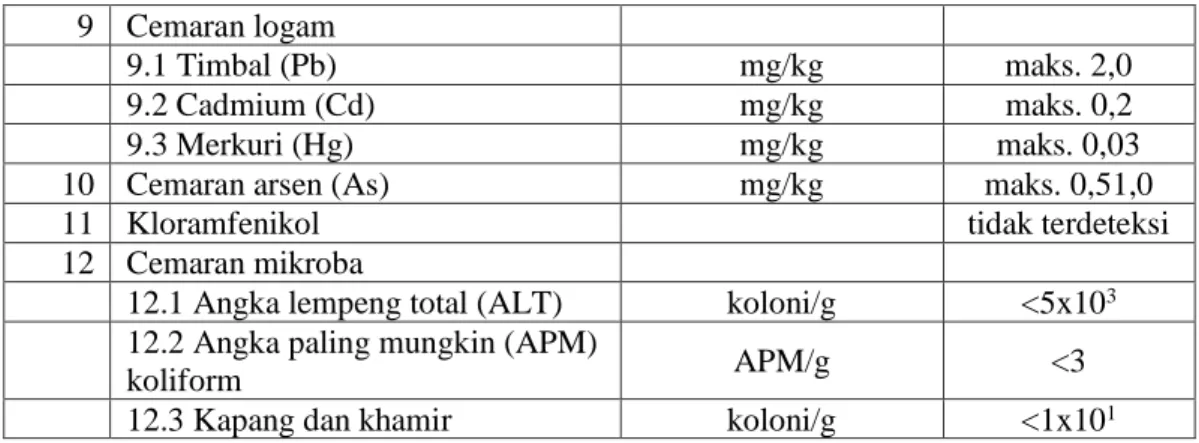
Tabel 2.2 Lanjutan 9 Cemaran logam
9.1 Timbal (Pb) mg/kg maks. 2,0
9.2 Cadmium (Cd) mg/kg maks. 0,2
9.3 Merkuri (Hg) mg/kg maks. 0,03
10 Cemaran arsen (As) mg/kg maks. 0,51,0
11 Kloramfenikol tidak terdeteksi
12 Cemaran mikroba
12.1 Angka lempeng total (ALT) koloni/g <5x103 12.2 Angka paling mungkin (APM)
koliform APM/g <3
12.3 Kapang dan khamir koloni/g <1x101
Sumber: SNI 3545:2013
2.3 Keasaman Madu
Dalam ciri-rasa (flavor) dan aroma madu sebagian disumbang oleh asam- asam yang dikandungnya sebagai perlindungan terhadap mikroorganisme.
Keasaman madu ditentukan oleh disosiasi hidrogen dalam larutan air. Keasaman madu merupakan salah satu parameter yang digunakan untuk menentukan kualitas madu. Kadar keasaman ini menunjukkan jumlah asam bebas per kg madu (Wulandari, 2017; Sihombing, 1997).
Keasaman juga mempengaruhi kualitas madu, hal ini karena di dalam madu terdapat sejumlah asam organik yang berperan dalam proses metabolisme tubuh pada lebah madu. Keasaman madu memberikan kontribusi terhadap rasa dan bertanggung jawab atas stabilitas yang sangat baik dari madu terhadap mikroorganisme. Keasaman madu yang meningkat terjadi karena adanya fermentasi. Syarat nilai keasaman pada madu berdasarkan SNI (2013) yaitu maksimal 50 ml NaOH/kg. Analisis dilakukan secara titrasi asam-basa. Menurut penelitian Khasanah, dkk. (2017), keasaman madu dari kelima wilayah di Kabupaten Wonosobo masih di dalam nilai standar batas maksimum. Hal ini mengindikasikan bahwa madu di wilayah tersebut termasuk berkualitas baik.
Madu dengan keasaman yang tinggi mengindikasikan terjadinya fermentasi gula menjadi alkohol sehingga menurunkan kualitas madu (Suhartini, dkk., 2018;
Khasanah, dkk., 2017).
Tinggi rendahnya nilai keasaman suatu madu dapat dipengaruhi oleh pengaruh penyimpanan. Menurut penelitian oleh Wulandari (2017) tentang kualitas madu berdasarkan perbedaan suhu penyimpanan, semakin meningkatnya kadar keasaman merupakan suatu indikator telah terjadinya proses fermentasi dan proses transformasi alkohol menjadi asam organik. Penyimpanan madu pada suhu dingin lebih disarankan daripada suhu ruang, karena pada suhu ruang tingkat kelembaban lebih tinggi, sehingga madu lebih mudah menyerap air.
Nilai keasaman madu sangat dipengaruhi oleh kadar air. Menurut Savitri, dkk. (2016), kadar air madu yang rendah menyebabkan mikroba pembusuk tidak dapat hidup. Rendahnya kadar air juga mempengaruhi keberadaan khamir yang menyebabkan terjadinya fermentasi. Semakin tinggi nilai ml NaOH/kg dalam madu maka tingkat keasaman semakin tinggi. Madu memiliki sifat higroskopis yang menyebabkan kadar air meningkat karena madu merupakan larutan jenuh gula dengan gugus OH- bebas.
Menurut Fatma, dkk. (2017), variasi kadar keasaman madu di antara sampel madu disebabkan oleh adanya kekhasan komposisi vegetasi tanaman berbunga sumber pakan lebah madu sehingga terdapat perbedaan preferensi sumber pakan lebah madu pada masing-masing wilayah, perbedaan komposisi tanah, serta perbedaan penanganan madu selama penyimpanan. Variasi kadar keasaman berkaitan dengan asal bunga. Selain itu, variasi keasaman madu tergantung pada asal flora, lokasi budidaya, musim panen, manajemen panen dan paska panen
lebah madu. Parameter kadar keasaman penting dalam menentukan kualitas karena berkontribusi dalam menentukan stabilitas madu selama masa penyimpanan dan menentukan tekstur dan rasa madu. Beberapa asam berasal dari nektar yang konsentrasinya tergantung asal bunga pakan lebah dan sebagian besar diproduksi oleh lebah itu sendiri dengan adanya enzim glukosa oksidase (glukosidae) yang mengatalisis oksidasi glukosa madu menghasilkan asam glukonat.
Madu olahan yang diberi sari rasa buah dapat meningkatkan nilai keasaman.
Menurut penelitian Fitri, dkk. (2017) tentang konsentrasi gula dan sari buah terhadap kualitas sirup belimbing, keasaman sirup yang dihasilkan mengalami penurunan seiring dengan meningkatnya jumlah sari buah yang ditambahkan sehingga dengan semakin tinggi jumlah sari buah yang ditambahkan maka keasaman sirup yang dihasilkan akan semakin rendah (asam). Asam-asam dari buah dapat meningkatkan tingkat keasaman.
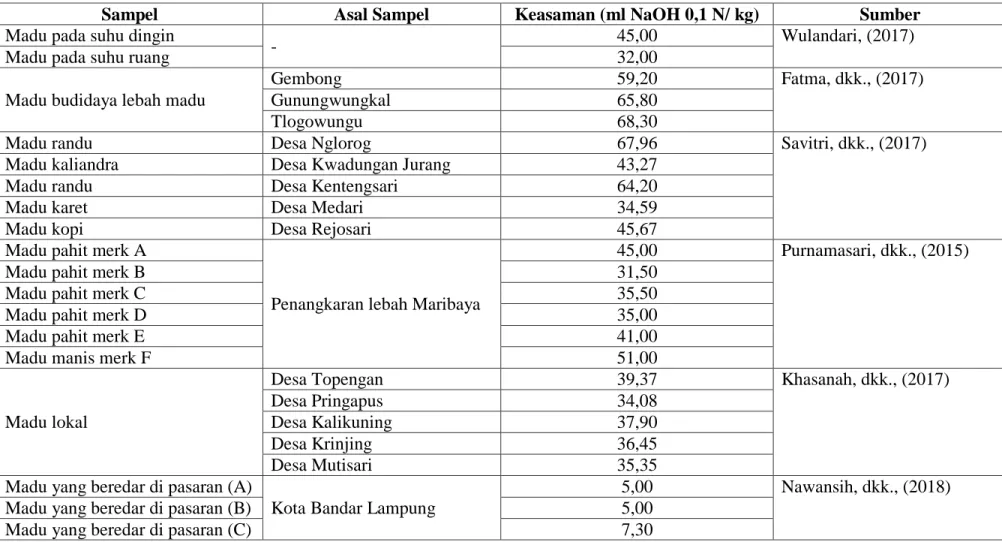
Adanya pengatur keasaman mempengaruhi keasaman madu. Fungsi pengatur pengasaman pada pangan adalah untuk membuat pangan menjadi lebih asam, lebih basa, atau menetralkan pangan. Tujuan utama penambahan asam adalah untuk memberikan rasa asam. Asam juga dapat mengintensifkan penerimaan rasa-rasa lain. Asam yang banyak digunakan pada bahan makanan adalah asam organik seperti asam asetat, asam sitrat, asam malat, asam suksinat, dan asam tartrat (Kamariah, 2006). Beberapa penelitian yang dilakukan menunjukkan tingkat keasaman pada berbagai jenis madu, diantaranya dapat dilihat pada Tabel 2.3.
Tabel 2.2 Keasaman Pada Berbagai Jenis Madu
Sampel Asal Sampel Keasaman (ml NaOH 0,1 N/ kg) Sumber
Madu pada suhu dingin
- 45,00 Wulandari, (2017)
Madu pada suhu ruang 32,00
Madu budidaya lebah madu
Gembong 59,20 Fatma, dkk., (2017)
Gunungwungkal 65,80
Tlogowungu 68,30
Madu randu Desa Nglorog 67,96 Savitri, dkk., (2017)
Madu kaliandra Desa Kwadungan Jurang 43,27
Madu randu Desa Kentengsari 64,20
Madu karet Desa Medari 34,59
Madu kopi Desa Rejosari 45,67
Madu pahit merk A
Penangkaran lebah Maribaya
45,00 Purnamasari, dkk., (2015)
Madu pahit merk B 31,50
Madu pahit merk C 35,50
Madu pahit merk D 35,00
Madu pahit merk E 41,00
Madu manis merk F 51,00
Madu lokal
Desa Topengan 39,37 Khasanah, dkk., (2017)
Desa Pringapus 34,08
Desa Kalikuning 37,90
Desa Krinjing 36,45
Desa Mutisari 35,35
Madu yang beredar di pasaran (A)
Kota Bandar Lampung
5,00 Nawansih, dkk., (2018)
Madu yang beredar di pasaran (B) 5,00
Madu yang beredar di pasaran (C) 7,30
Menurut penelitian Wulandari (2017), keasaman madu pada suhu dingin dan suhu ruang menunjukkan bahwa penyimpanan madu pada suhu dingin lebih disarankan daripada suhu ruang karena pada suhu ruang tingkat kelembaban lebih tinggi, sehingga madu lebih mudah menyerap lebih banyak air, dengan kadar air tinggi akan lebih mudah menyebabkan terjadinya fermentasi. Hal inilah yang menyebabkan kadar keasaman madu pada suhu ruang lebih tinggi daripada madu suhu dingin.
Menurut penelitian Fatma, dkk. (2017), tingginya kadar keasaman pada sampel madu dalam penelitiannya terkait dengan tingginya kadar air madu.
Fermentasi madu akan mengubah glukosa dan fruktosa menjadi karbon dioksida dan alkohol. Alkohol dengan adanya oksigen akan teroksidasi dan dikonversi menjadi asam asetat dan air yang berkontribusi meningkatkan keasaman madu.
Fermentasi ini tidak akan terjadi jika madu mengandung kadar air kurang dari 17%, karbohidrat lebih dari 83%, serta suhu penyimpanan kurang dari 11°C.
2.3 Metode Penentuan Keasaman Madu Secara Titrasi Asidi-Alkalimetri Dalam penentuan keasaman madu dapat digunakan metode Titrasi Asidi- Alkalimetri. Menurut SNI (2013), prinsip pengujian keasaman madu yaitu netralisasi asam dengan basa dimana terjadinya reaksi antara pemberi proton (asam) dengan penerima proton (basa). Asidimetri dan alkalimetri termasuk reaksi netralisasi yakni reaksi antara ion hidrogen yang berasal dari asam dengan ion hidroksida yang berasal dari basa untuk menghasilkan air yang bersifat netral.
Alkalimetri merupakan penetapan kadar senyawa-senyawa yang bersifat asam dengan menggunakan baku basa (Gandjar dan Rohman, 2007).
Titrasi asam-basa termasuk teknik analisis yang cepat dan akurat dalam
penentuan senyawa asam atau basa dalam sampel. Metode titrasi asam-basa digunakan untuk penentuan senyawa anorganik dan senyawa organik yang memiliki sifat asam atau basa. Titik akhir titrasi (titik ekivalen) pada titrasi asam basa dapat diketahui melalui perubahan warna dengan menggunakan indikator.
Keberhasilan analisis secara titrasi asam-basa tergantung pada pemilihan dan ketersediaan senyawa pentiter yang dapat bereaksi terhadap senyawa analit sehingga titik akhir titrasi dapat diperoleh dengan cepat, tepat dan akurat (Situmorang, 2012).
Dalam titrasi asam kuat dengan basa kuat, terjadi perubahan nilai pH secara tiba-tiba. Pada titik ekivalen, penambahan sedikit pentiter dapat mengubah nilai pH beberapa unit, sehingga beberapa jenis indikator yang mempunyai skala transisi pada titik ekivalen ini dapat dipergunakan seperti fenolftalein, metil merah dan indikator lain. Konsentrasi pentiter pada titrasi asam-basa umumnya dilakukan sekitar 0,1 – 0,5 M (Situmorang, 2012).
Indikator asam-basa adalah senyawa asam atau basa lemah yang berwarna dan memberikan warna yang kontras pada suasana asam atau basa larutan. Dalam titrasi asam dengan NaOH indikator lebih lemah dibanding terhadap asam dan disamping itu konsentrasi indikator di dalam larutan biasanya sangat kecil sehingga tidak banyak berpengaruh terhadap titrasi. Misalkan indikator asam berwarna dan setelah dinetralisasi dengan basa kuat indikator akan berubah yang memberikan perubahan warna dari warna semula (dalam bentuk asam), dan biasanya masih susah membedakan perubahan warna sebelumnya. Dengan melanjutkan titrasi dengan basa kuat maka warna akan berubah (suasana basa) (Situmorang, 2012).
Indikator asam-basa adalah zat yang berubah warna atau membentuk fluoresen pada suatu range pH tertentu. Indikator asam-basa terletak pada titik ekivalen dan ukuran dari pH. Zat-zat indikator dapat berubah asam atau basa dan menunjukkan perubahan warna yang kuat serta biasanya adalah zat organik.
Perubahan warna disebabkan oleh resornasi isomer elektron. Berbagai indikator mempunyai tetapan ionisasi yang berbeda dan akibatnya mereka menunjukkan warna pada range pH yang berbeda (Khopkar, 1990).
Untuk mendapatkan hasil titrasi yang akurat dengan pengamatan secara visual maka perlu dipertimbangkan jenis indikator yang dapat memberikan perubahan warna indikator pada saat tercapai titik ekivalen reaksi. Sebagai contoh, titrasi asam kuat dengan basa kuat yang sering digunakan adalah indikator fenolftalein karena pada keadaan basa akan memberikan warna merah jambu dan pada suasana asam tidak berwarna, sehingga titik akhir titrasi akan diperoleh pada saat warna larutan berubah dari tidak berwarna menjadi warna merah jambu (Situmorang, 2012).
Senyawa yang bersifat asam dititrasi dengan menggunakan larutan standar basa dengan persamaan reaksi sebagai berikut: (Situmorang, 2012).
HA (yang dititrasi) + OH-(NaOH sebagai pentiter) A- + H2O
Jika intensitas warna suatu larutan setara dengan konsentrasi senyawa berwarna maka perubahan akan menunjukkan perubahan konsentrasi senyawa tersebut. Sebaliknya, hal yang sama akan dapat terjadi bila senyawa yang berwarna adalah analit. Penambahan senyawa pentiter terhadap larutan berwarna tidak akan mengubah warna larutan sampai seluruh senyawa pentiter telah bereaksi dengan analit dan mencapai titik akhir titrasi (Situmorang, 2012).
BAB III METODE PENELITIAN
3.1 Tempat Penelitian
Pengujian keasaman pada madu dilakukan di Laboratorium Makanan Minuman dan Hasil Pertanian Balai Riset dan Standardisasi Industi Medan yang berada di Jalan Sisingamangaraja No. 24 Medan.
3.2 Alat
Alat-alat yang digunakan adalah batang pengaduk, beaker glass 500 ml (Pyrex), buret, erlenmeyer 250 (Pyerx), gelas ukur 100 ml (Pyrex), klem, neraca analitik, pipet tetes, statif.
3.3 Bahan
Bahan yang di analisis adalah madu hutan dan madu sachet merek A dan B.
Bahan-bahan kimia yang digunakan adalah air suling, indikator PP, NaOH 1 N.
Spesifikasi daftar sampel dapat dilihat pada Lampiran 1.
3.4 Prosedur Kerja
3.4.1 Pembuatan larutan standar baku NaOH 0,1 N
Sebanyak 2,1275 g dilarutkan dalam 500 ml air bebas CO2.
3.4.2 Pembakuan larutan standar NaOH 0,1 N
Sebanyak 0,05 g asam oksalat dilarutkan dalam 100 ml air. Kemudian ditambahkan 2-3 tetes indikator PP. Larutan dititar dengan larutan NaOH 0,1 N sampai titik akhir ditandai dengan perubahan warna menjadi merah jambu.
3.4.3 Penetapan keasaman madu
Penetapan keasaman madu dilakukan dengan metode titrasi asidi-alkalimetri (asam-basa) yang mengacu pada SNI (2013). Sebanyak 10 g madu ditimbang dan dimasukkan ke dalam erlenmeyer 250 ml. Kemudian dilarutkan dengan 75 ml air suling dan ditambahkan 4 - 5 tetes indikator PP. Madu dititar dengan larutan NaOH 0,1 N sampai titik akhir ditandai dengan perubahan warna menjadi merah jambu yang tetap selama 10 detik. Volume NaOH 0,1 N yang digunakan untuk titrasi dicatat dan hasil keasaman dalam madu dihitung dengan mernggunakan rumus perhitungan:
Dimana:
a = volume NaOH 0,1 N yang digunakan dalam titrasi (ml) b = normalitas NaOH 0,1 N
c = berat sampel (g)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Keasaman Pada Madu
Perubahan warna yang terjadi saat titrasi dapat dilihat pada Lampiran 5.
Contoh perhitungan keasaman pada madu dapat dilihat pada Lampiran 3. Hasil penetapan keasaman pada madu dapat dilihat pada Lampiran 4. Nilai keasaman pada madu yang diperoleh dapat dilihat pada Tabel 4.1.
Tabel 4.1 Keasaman Pada Madu
Sampel Keasaman (ml NaOH 0,1 N/ kg)
A 48,43
B 80,89
C 38,10
Keterangan: data di atas merupakan merupakan rata-rata dari dua kali pengulangan. A. Madu Hutan B. Madurasa C. Madu TJ
Berdasarkan Tabel 4.1, hasil penetapan keasaman pada madu menunjukkan bahwa nilai keasaman sampel A dan C sebesar 48,43 ml NaOH 0,1 N/ kg dan 38,10 ml NaOH 0,1 N/ kg, memenuhi syarat sesuai dengan SNI 01-3534-2013 yaitu maksimal 50 ml NaOH 0,1 N/ kg, sedangkan nilai keasaman sampel B sebesar 80,89 ml NaOH 0,1 N/ kg, tidak memenuhi syarat. Dari hasil tersebut dapat dilihat madu Madurasa memiliki nilai keasaman tertinggi, sedangkan Madu TJ memiliki nilai keasaman lebih rendah daripada madu hutan. Keasaman madu yang diperoleh menunjukkan nilai keasaman yang lebih besar daripada penelitian Savitri, dkk. (2017) yaitu 68 ml NaOH 0,1 N/ kg dan penelitian Nawansih, dkk.
(2018) yaitu 5 ml NaOH 0,1 N/ kg. Tinggi rendahnya nilai keasaman suatu madu dapat dipengaruhi oleh pengaruh penyimpanan. Menurut penelitian oleh Wulandari (2017) tentang kualitas madu berdasarkan perbedaan suhu
penyimpanan, semakin meningkatnya kadar keasaman merupakan suatu indikator telah terjadinya proses fermentasi dan proses transformasi alkohol menjadi asam organik. Penyimpanan madu pada suhu dingin lebih disarankan daripada suhu ruang, karena pada suhu ruang tingkat kelembaban lebih tinggi, sehingga madu lebih mudah menyerap air.
Menurut Fatma, dkk. (2017), variasi kadar keasaman madu di antara sampel madu disebabkan oleh adanya kekhasan komposisi vegetasi tanaman berbunga sumber pakan lebah madu sehingga terdapat perbedaan preferensi sumber pakan lebah madu pada masing-masing wilayah, perbedaan komposisi tanah, serta perbedaan penanganan madu selama penyimpanan. Variasi kadar keasaman berkaitan dengan asal bunga. Selain itu, variasi keasaman madu tergantung pada asal flora, lokasi budidaya, musim panen, manajemen panen dan paska panen lebah madu. Parameter kadar keasaman penting dalam menentukan kualitas karena berkontribusi dalam menentukan stabilitas madu selama masa penyimpanan dan menentukan tekstur dan rasa madu. Beberapa asam berasal dari nektar yang konsentrasinya tergantung asal bunga pakan lebah dan sebagian besar diproduksi oleh lebah itu sendiri dengan adanya enzim glukosa oksidase (glukosidae) yang mengatalisis oksidasi glukosa madu menghasilkan asam glukonat. Keasaman madu disebabkan oleh adanya asam organik, terutama asam glukonat, asam piruvat, asam malat dan asam sitrat.
Nilai keasaman madu sangat dipengaruhi oleh kadar air. Menurut Savitri, dkk. (2016), kadar air madu yang rendah menyebabkan mikroba pembusuk tidak dapat hidup. Rendahnya kadar air juga mempengaruhi keberadaan khamir yang menyebabkan terjadinya fermentasi. Semakin tinggi nilai ml NaOH/kg dalam
madu maka tingkat keasaman semakin tinggi. Madu memiliki sifat higroskopis yang menyebabkan kadar air meningkat karena madu merupakan larutan jenuh gula dengan gugus OH- bebas.
Madu olahan yang diberi sari rasa buah dapat meningkatkan nilai keasaman.
Menurut penelitian Fitri, dkk. (2017) tentang konsentrasi gula dan sari buah terhadap kualitas sirup belimbing, keasaman sirup yang dihasilkan mengalami penurunan seiring dengan meningkatnya jumlah sari buah yang ditambahkan sehingga dengan semakin tinggi jumlah sari buah yang ditambahkan maka keasaman sirup yang dihasilkan akan semakin rendah (asam). Asam-asam dari buah dapat meningkatkan tingkat keasaman.
Adanya pengatur keasaman mempengaruhi keasaman madu. Fungsi pengatur pengasaman pada pangan adalah untuk membuat pangan menjadi lebih asam, lebih basa, atau menetralkan pangan. Tujuan utama penambahan asam adalah untuk memberikan rasa asam. Asam juga dapat mengintensifkan penerimaan rasa-rasa lain. Asam yang banyak digunakan pada bahan makanan adalah asam organik seperti asam asetat, asam sitrat, asam malat, asam suksinat, dan asam tartrat (Kamariah, 2006).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil penetapan keasaman pada madu yang dilakukan dapat disimimpulkan bahwa sampel A dan C memenuhi syarat mutu madu sesuai dengan SNI 01-3534-2013, sedangkan sampel B tidak memenuhi syarat mutu madu. Dimana persyaratan keasaman madu yaitu maksimal 50 ml NaOH 0,1 N/
kg.
5.2 Saran
Diharapkan kepada penulis selanjutnya agar menggunakan madu dengan merek dagang yang lain dipasaran agar wawasan kita tentang produk madu dan olahannya yang baik dan memenuhi persyaratan semakin luas sehingga aman untuk dikonsumsi masyarakat.
DAFTAR PUSTAKA
Badan Standarisasi Nasional. Madu. SNI 3545:2013. Jakarta: Dewan Standardisasi Nasional.
Fatma, I.I., Haryanti, S., Suedy, S.W.A. (2017). Uji Kualitas Madu Pada Beberapa Wilayah Budidaya Lebah Madu di Kabupaten Pati. Jurnal Biologi. (6)2: 59, 62.
Fitri, E., Harun, N. dan Johan, V.S. (2017). Konsentrasi Gula dan Sari Buah Terhadap Kualitas Sirup Belimbing Wuluh (Averrhoa blimbi L.). JOM Faperta UR. (4)1: 4.
Gandjar, I.G. dan Rohman, A. (2007). Kimia Analisis Farmasi. Yogyakarta:
Penerbit Pustaka Pelajar. hlm. 375-376.
Kamariah, R. (2006). Bahan Tambahan Pangan (Food Additive). Diunduh dari:
https://www.academia.edu/6850709/BAHAN_TAMBAHAN_PANGAN_F OOF_ADDITIVE pada tanggal 26 Mei 2019. hlm. 14-15.
Khasanah, R., Parman, S. dan Suedy, S. W. A. (2017). Kualitas Madu Lokal dari Lima Wilayah di Kabupaten Wonosobo. Jurnal Biologi. 6(1): 32.
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Penerjemah: A.
Saptorahardjo. Jakarta: UI Press. hlm. 43.
Molan, P.C. (2006). Using Honey in Wound Care. International Journal of Clinical Aromatheraphy France. (3)2: 21-24.
Nawansih, O., Nurainy, F., Rangga, A. dan HTF, N. A. (2018). Pengujian Mutu Madu yang beredar di Bandar Lampung Secara Kimia dan Secara Sederhana. Seminar Nasional “Inovasi Pangan Lokal Untuk Mendukung Ketahanan Pangan” Universitas Mercu Buana Yogyakarta. 149.
Purnamasari, N., Aprilia, H. dan Sukanta. (2015). Perbandingan Parameter Fisikokimia Madu Pahit (Aktivitas Enzim Diastase, Gula Pereduksi (Glukosa), Keasaman, Cemaran Abu dan Arsen) dengan Madu Manis Murni. Prosiding Penelitian SPeSIA. 49.
Sarwono, B. (2001). Kiat Mengatasi Permasalahan Praktis Lebah Madu. Jakarta:
PT Argo Media Pustaka. hlm. 62, 68.
Savitri, N.P.T., Hastuti, E.D. dan Suedy, S.W. (2017). Kualitas Madu Lokal dari Beberapa Wilayah di Kabupaten Temanggung. Buletin Anatomi dan Fisiologi. (2)1: 64.
Sihombing, D.T.H. (1997). Ilmu Ternak Lebah Madu. Yogyakarta: Universitas Gadjah Mada Press. hlm. 31-32, 35, 100-101, 106.
Situmorang, M. (2012). Kimia Analitik Dasar. Medan: Universitas Negeri Medan.
hlm. 258-355.
Sumoprastowo, R.M. dan Suprapto, R. (1993). Beternak Lebah Madu Modern.
Jakarta: Bhratara. hlm. 46.
Suranto, A. (2007). Terapi Madu. Jakarta: Penerbit Penebar Plus. hlm. 27.
Wulandari, D.D. (2017). Kualitas Madu (Keasaman, Kadar Air, dan Kadar Gula Pereduksi) Berdasarkan Perbedaan Suhu Penyimpanan. Jurnal Kimia Riset.
(2)1: 17-18.
Lampiran 1. Daftar Spesifikasi Sampel
No Sampel Spesifikasi
1
Merek: Madu Hutan Komposisi: -
Tanggal Kadaluarsa: - Produsen: -
2
Merek: Madurasa Rasa Jeruk Nipis
Komposisi: Madu (2,271%), fruktosa, glukosa, pengatur keasaman asam sitrat, konsentrat sari buah jeruk nipis (0,076%), pengatur keasaman asam malat, antioksidan asam askorbat, pewarna Karmoisin CI 14720
Tanggal Kadaluarsa: November 2021
Produsen: PT Madurasa Unggulan Nusantara Wonogiri
3
Merek: Madu TJ Rasa Strawberry
Komposisi: Madu 285,93 mg, royal jelly 4 mg, fruktosa, glukosa, perisa strawberry, asam sitrat, pewarna Eurocert Brown HT
Tanggal Kadaluarsa: Juli 2021
Produsen: Ultrasakti Bekasi
Lampiran 2. Data Perhitungan Pembakuan Larutan Standar NaOH 0,1 N
No Berat Asam Oksalat (g) Volume NaOH (ml)
1 0,0497 8,0
2 0,0504 8,10
3 0,0510 8,15
N1 =
= 0,0986 N
N2 = = 0,0988 N
N3 = = 0,0993 N
N = = 0,0989 N
Lampiran 3. Contoh Perhitungan Penetapan Keasaman Pada Madu
Dimana:
a = volume NaOH 0,1 N yang digunakan dalam titrasi (ml) b = normalitas NaOH 0,1 N
c = bobot contoh, dalam gram.
Contoh perhitungan:
Bobot sampel = 10,0207 g V1 = 4,90 ml N1 = 0,0989 N N2 = 0,1 N
V1 x N1 = V2 x N2
4,90 x 0,0989 = V2 x 0,1
V2 = = 4,85 ml
= 48,40 ml NaOH 0,1 N/ kg
Perhitungan nilai keasaman tiap-tiap sampel untuk 2 kali pengulangan dilakukan seperti contoh di atas.
Lampiran 4. Hasil Penetapan Keasaman Pada Madu
Sampel
Berat Contoh
(g)
V1 (ml)
N1 ( N NaOH)
V2 (ml)
N2 (N NaOH)
Keasaman (ml N NaOH/
kg)
A1 10,0207 4,90 0,0989 4,85 0,1 48,40
A2 10,1106 4,95 0,0989 4,90 0,1 48,46
Rata-Rata 48,43
B1 10,0267 8,15 0,0989 8,06 0,1 80,39
B2 10,0261 8,25 0,0989 8,16 0,1 81,39
Rata-Rata 80,89
C1 10,0177 3,80 0,0989 3,76 0,1 37,53
C2 10,1147 3,95 0,0989 3,91 0,1 38,66
Rata-Rata 38,10
Lampiran 5. Gambar Hasil Titrasi
(a) (b)
(c) (d)
(e) (f)
Keterangan: (a) Madu hutan sebelum dititrasi; (b) Madu hutan setelah dititrasi; (c) Madurasa sebelum dititrasi; (d) Madurasa setelah dititrasi; (e) Madu TJ sebelum dititrasi; (f) Madu TJ setelah dititrasi.