DI PERAIRAN DANAU SIOMBAK DAN DESA JARING HALUS SUMATERA UTARA
PUPUT MELATI 150302038
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA 2019
DI PERAIRAN DANAU SIOMBAK DAN DESA JARING HALUS SUMATERA UTARA
SKRIPSI
PUPUT MELATI 150302038
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA 2019
DI PERAIRAN DANAU SIOMBAK DAN DESA JARING HALUS SUMATERA UTARA
SKRIPSI
PUPUT MELATI 150302038
Skripsi Sebagai Satu Diantara Beberapa Syarat untuk Memperoleh Gelar Sarjana
Perikanan di Program Studi Manajemen Sumberdaya Perairan Fakultas Pertanian Universitas Sumatera Utara
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA 2019
Saya yang bertanda tangan di bawah ini : Nama : Puput Melati
NIM : 150302038
Menyatakan bahwa skripsi yang berjudul “Analisis Kandungan Logam Berat Kadmium (Cd) dan Besi (Fe) pada Daging Kepiting Bakau (Scylla olivacea) di Perairan Danau Siombak dan Desa Jaring Halus Sumatera Utara” adalah benar merupakan hasil karya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka dibagian akhir skripsi ini.
Medan, September 2019
Puput Melati NIM. 150302038
PUPUT MELATI. Analisis Kandungan Logam Berat Kadmium (Cd) dan Besi (Fe) pada Daging Kepiting Bakau (Scylla olivacea) di Perairan Danau Siombak dan Desa Jaring Halus Sumatera Utara. Dibimbing oleh ERI YUSNI.
Kehadiran logam berat di lingkungan akuatik harus dipantau terus menerus keberadaannya agar tidak membahayakan makhluk hidup di dalam perairan.
Penelitian ini bertujuan untuk mengetahui kandungan logam berat kadmium (Cd) dan besi (Fe) pada air, sedimen dan kepiting bakau (Scylla olivacea) di perairan Danau Siombak dan Perairan Desa Jaring Halus dan menentukan tingkat kelayakan konsumsi pada kepiting yang terpapar logam berat sesuai dengan standart baku mutu cemaran logam berat yang diperbolehkan dalam pangan.
Pengambilan sampel air, sedimen dan kepiting dilakukan pada bulan Juni-Juli 2019. Metode menentukan kandungan Cd dan Fe menggunakan perangkat AAS (Atomic Absorption Spectrophotometer) dilakukan di Laboratorium Kesehatan Daerah Medan. Diketahui bahwa kandungan Cd pada sedimen di perairan Danau Siombak sudah melebihi nilai baku mutu dan Perairan Desa Jaring Halus pada stasiun I dan III belum melebihi baku mutu tetapi pada stasiun II sudah melebihi baku mutu USEPA 1986 yaitu ≤ 0.006 mg/kg, sedangkan pada logam Besi (Fe) pada kedua lokasi telah melampaui baku mutu quality guideline values for metals and associated levels of concern to be used in doing assessments of sediment quality (2003) yaitu ≥ 20 mg/kg. Kandungan Cd pada air di kedua lokasi telah melampaui ambang batas baku mutu Kepmen LH No 51 tahun 2004 yaitu ≥ 0.0010 mg/l sedangkan untuk logam Besi (Fe) juga telah melampaui ambang batas baku mutu USEPA (1986) yaitu ≥ 0.5 mg/l. Kandungan Cd pada kepiting masih dibawah baku mutu BPOM RI No 5 Tahun 2018 yaitu ≤ 0.1 mg/kg, sedangkan untuk logam Besi (Fe) telah melampaui baku mutu SNI 7387 Tahun 2009 yaitu ≥ 1 mg/kg. Dengan demikian perairan Danau Siombak dan Perairan Desa Jaring Halus sudah tergolong tercemar logam berat Cd dan Fe.
Kata Kunci: Logam berat, Kadmium (Cd), Besi (Fe), Kepiting Bakau (Scylla olivacea)
PUPUT MELATI. Analysis of heavy metal content Cadmium (Cd) and Iron (Fe ) on mangrove crab meat in the waters of Lake Siombak and the fine net village, north Sumatra. Supervised by ERI YUSNI
The presence of heavy metals in the aquatic environment must be monitored continuously so that they do not endanger living things in the waters.
This study aims to determine the amount of heavy metal content of Cadmium (Cd) and Iron (Fe) exposed in Water, Sediments and Mangrove Crabs (Scylla olivacea) in Lake Siombak waters and the waters of Jaring Halus Village and determine the level of eligibility for consumption of crabs exposed to heavy metals in accordance with the quality standards of heavy metals allowed in food.
Sampling of water, sediments, and mangrove crabs (Scylla olivacea) was carried out in June- July 2019. To determine the value of the content of Cadmium (Cd) and Iron (Fe) using the AAS (Atomic Absorption Spectrophotometer) device and conducted in the Medan Regional Health Laboratory. It is known that the content of Cadmium (Cd) heavy metals in sediments in Lake Siombak waters has exceeded the quality standard and The waters of Jaring Halus Village at Station I and III have not exceeded the quality standard but at Station II have exceeded the 1986 USEPA quality standard of ≤ 0.006 mg / kg, whereas in heavy metals Iron (Fe) has exceeded the quality standard quality guideline values for metals and associated levels of concern to be used in doing assessments of sediment quality (2003) that is ≥ 20 mg/kg. It is known that the content of Cadmium (Cd) in the waters of Lake Siombak and the waters of Jaring Halus Village in the water has exceeded the threshold quality standard Kepmen LH No. 51 of 2004 which is ≥ 0.0010 mg / l, whereas for ferrous metals (Fe) also exceeded the USEPA (1986) quality standard threshold of ≥ 0.5 mg / l. It is known that the content of Cadmium (Cd) in the waters of Lake Siombak and the waters of Jaring Halus Village in crabs is still below the quality standard of BPOM RI No 5 of 2018 which is ≤ 0.1 mg / kg, whereas for heavy metals iron (Fe) has exceeded the quality standard of SNI 7387 in 2009 which is ≥ 1 mg / kg. Thus the waters of Lake Siombak and Jaring Halus waters have been classified as polluted by heavy metals Cadmium (Cd) and Iron (Fe).
Keywords: Heavy Metal, Cadmium (Cd), Iron (Fe), Mangrove Crab (Scylla olivacea)
Penulis dilahirkan di Buntu Pagar, Desa Sidomulyo, Kecamatan Tinggi Raja, Kabupaten Asahan pada tanggal 24 April 1997. Anak dari pasangan Bapak Darwin dan Ibu Mardiah, yang merupakan putri kedua dari 3 bersaudara.
Penulis mengawali pendidikan formal pertama di SD Negeri 010109 Piasa Ulu pada tahun 2003-2009 Bersamaan dengan berakhirnya pendidikan dasar, penulis melanjutkan pendidikan di MTSs Amaliyah Piasa Ulu pada tahun 2009-2012. Pada tahun yang sama penulis diterima di MAN Kisaran dengan jurusan IPA pada tahun 2012-2015.
Penulis melanjutkan pendidikan di Program Studi Manajemen Sumberdaya Perairan Fakultas Pertanian, Universitas Sumatera Utara melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN) tahun 2015.
Pada tahun 2017 penulis melaksanakan Magang di PT. Anugerah Maritim Lestari Perbaungan. Pada tahun 2018 penulis melaksanakan Kuliah Kerja Nyata (KKN) di Desa Bakal Julu Kabupaten Dairi dilanjutkan pada tahun 2019 penulis melaksanakan Praktik Kerja Lapangan (PKL) di Pengawasan Sumberdaya Kelautan dan Perikanan (PSDKP) Sibolga, Sumatera Utara .
Selain mengikuti perkuliahan penulis juga menjadi asisten Laboratorium Produktivitas Primer pada tahun 2017-2018 dan asisten Laboratorium Rancangan Percobaan pada tahun 2017-2018. Pada tahun 2016 penulis menjadi salah satu wakil atlet Sumatera Utara dalam mengikuti kejuaraan Pekan Olahragan Nasional
aktif dalam kegiatan Sumut Mengajar Batch IV dan sebagai anggota Ikatan Mahasiswa Manajemen Sumberdaya Perairan (IMASPERA) di Program Studi Manajemen Sumberdaya Perairan, Fakultas Pertanian, Universitas Sumatera Utara.
Syukur Alhamdulillah penulis panjatkan kehadirat Allah SWT yang telah memberikan kesehatan, sehingga penulis dapat menyelesaikan penelitian dengan judul “Analisis Kandungan Logam Berat Kadmium (Cd) dan Besi (Fe) pada Daging Kepiting Bakau (Scylla olivacea) di Perairan Danau Siombak dan Desa Jaring Halus Sumatera Utara” yang merupakan salah satu syarat untuk memperoleh gelar Sarjana Perikanan di Program Studi Manajemen Sumberdaya Perairan, Fakultas Pertanian Universitas Sumatera Utara.
Ungkapan terima kasih yang tak ternilai penulis ucapkan kepada ayahanda dan ibunda tercinta Bapak Darwin dan Ibu Mardiah atas kasih sayang, dukungan doa, materi dan semangatnya sehingga ananda dapat menyelesaikan studi ini.
Kepada kaka saya Nurhidayah dan adik saya Muhammad Fhikry Ali Wardana, terima kasih atas doa dan dukungan semangat yang diberikan, serta kepada seluruh keluarga.
Penulis juga menyadari bahwa penulisan skripsi ini tidak mungkin selesai tanpa bantuan dari berbagai pihak. Pada kesempatan ini penulis menyampaikan ucapan terima kasih kepada :
1. Ibu Dr. Eri Yusni, M.Sc selaku Ketua Program Studi Manajemen Sumberdaya Perairan dan Dosen pembimbing yang telah memberikan banyak sekali ilmu, masukan, arahan dan bimbingan kepada penulis.
2. Bapak Rizky Febriansyah Siregar, S.Pi, M.Si selaku sekretaris Program Studi dan Dosen Penguji yang telah memberikan banyak sekali ilmu, masukan, arahan dan bimbingan kepada penulis.
penulis.
4. Bapak Ahmad Muhtadi Rangkuti, S.Pi, M.Si yang telah membantu penulis dalam pelaksanaan penelitian ini.
5. Seluruh Dosen Program Studi Manajemen Sumberdaya Perairan Fakultas Pertanian Sumatera Utara, dan staf tata usaha Bapak Ashari Wardana.
6. Bapak Umar dan keluarga, serta Bapak dan keluarga yang telah membantu penulis dalam pelaksanan penelitian di lapangan.
7. Tim penelitian Danau Siombak yang telah membantu penulis di lapangan maupun pengerjaan skripsi ini.
8. Sahabat tersayang: Yuli Sarah, Intan Permata Sari, Tri Pardiana Setiani, Layla Syahara, Sri Watina, Khairunnisa, Dina Juniyanti, Raihan Uliya, Dayun Ifanda, Nur Rohim, Maiyah, Azizah, Henny Kharina, Dina Alfiyani, Puji, Nadia, Lia, Memel, Anggi, Kinan, Nada, Asih, Yulia, yang selalu menemani dan memberikan semangat kepada penulis selama penelitian hingga selesainya skripsi ini.
9. Seluruh teman-teman MSP Angkatan 2015 yang telah bersama selama 4 tahun, terima kasih atas semua bantuan dan dukungannya.
Terima kasih juga disampaikan kepada semua pihak yang telah memberikan dukungan dalam menyelesaikan skripsi ini. Semoga skripsi ini bermanfaat bagi pengembangan ilmu pengetahuan, khususnya bidang Manajemen Sumberdaya Perairan
Medan, September 2019
Puput Melati
ABSTRAK ... i
ABSTRACT... ii
RIWAYAT HIDUP ... iii
KATA PENGANTAR ... v
DAFTAR ISI ... vii
DAFTAR GAMBAR ... x
DAFTAR TABEL ... xi
DAFTAR LAMPIRAN ... xiii
PENDAHULUAN Latar Belakang ... 1
Perumusan Masalah ... 3
Kerangka Pemikiran ... 4
Tujuan Penelitian ... 5
Manfaat Penelitian... 5
TINJAUAN PUSTAKA Klasifikasi dan Morfologi Kepiting Bakau (Scylla olivacea) ... 6
Habitat Kepiting Bakau (Scylla olivacea) ... 7
Parameter Lingkungan Suhu ... 8
pH ... 9
Kecerahan ... 10
Oksigen Terlarut (DO) ... 11
Salinitas ... 12
Sedimen ... 13
Pencemaran Logam Berat ... 14
Logam Berat Kadmium (Cd) ... 15
Besi (Fe) ... 16
Logam Berat di Air ... 18
Logam Berat di Sedimen ... 19
Toksisitas Logam Berat ... 21
METODE PENELITIAN Waktu dan Lokasi Penelitian ... 23
Alat dan Bahan Penelitian ... 25
Prosedur Penelitian Pengukuran Parameter Fisika Kimia Air ... 26
Pengambilan Sampel Sedimen ... 26
Analisis Sampel Sedimen ... 27
Pengambilan Sampel Air ... 28
Analisis Sampel Air ... 28
Pengambilan Sampel Kepiting Bakau (Scylla olivacea) ... 29
Analisis Kepiting Bakau (Scylla olivacea) ... 29
Analisis Data Konsentrasi Logam Berat ... 33
Biokonsentrasi Faktor (BCF) ... 34
Analisa Komponen Utama ... 34
Analisi Deskriptif ... 35
HASIL DAN PEMBAHASAN Hasil Parameter Fisika dan Kimia Air ... 36
Kandungan Logam Berat di Perairan Danau Siombak ... 37
Kandungan Logam Berat di Perairan Desa Jaring Halus ... 39
Nilai Biokonsentrasi Faktor (BCF) ... 41
Analisis Korelasi Komponen Utama ... 43
Pembahasan Kualitas Air Suhu ... 45
Salinitas ... 47
Derajat Keasaman (pH) ... 48
Oksigen Terlarut (DO) ... 50
Logam Berat di Air Kadmium (Cd) ... 52
Besi (Fe) ... 54
Logam Berat di Sedimen Kadmium (Cd) ... 55
Besi (Fe) ... 57
Logam Berat di Kepiting Bakau (Scylla olivacea) Kadmium (Cd) ... 58
Besi (Fe) ... 60
Biokonsentrasi Faktor (BCF) BCF Cd dan Fe pada Kepiting dengan Air... 62
Analisis Korelasi Komponen Utama ... 63
Rekomendasi Pengelolaan ... 68
KESIMPULAN DAN SARAN Kesimpulan ... 70
Saran ... 71
No. Teks Halaman
1. Kerangka Penelitian ... 4
2. Kepiting Bakau (Scylla olivacea) ... 6
3. Lokasi Penelitian ... 23
4. Perairan Danau Siombak ... 24
5. Perairan Desa Jaring Halus ... 25
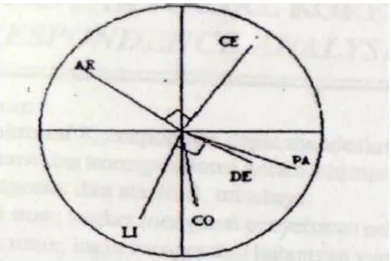
6. Simulasi Hasil Analisis PCA dalam Bentuk Lingkaran Korelasi ... 35
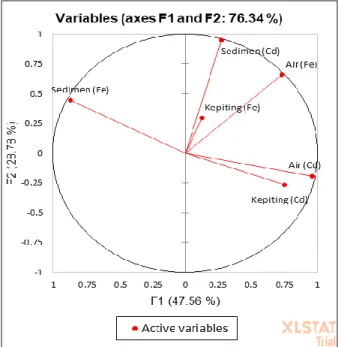
7. Analisis Korelasi Komponen Utama Cd dan Fe di Perairan Danau Siombak ... 44
8. Analisis Korelasi Komponen Utama Cd dan Fe di Perairan Desa Jaring Halus ... 44
No. Teks Halaman
1. Komposisi Karkas Kepiting Bakau ... 7
2. Standart Baku Mutu Cemaran Logam Berat dalam Pangan ... 17
3. Standart Baku Mutu Air Terhadap Logam Berat... 19
4. Standart Baku Mutu Logam Berat Cd dan Fe dalam Sedimen ... 20
5. Standart Baku Mutu Logam Berat Cd dalam Sedimen ... 21
6. Parameter yang Diukur ... 26
7. Nilai Rata- rata Parameter Fisika dan Kimia Air di Perairan Danau Siombak ... 36
8. Nilai Rata- rata Parameter Fisika dan Kimia Air di Perairan Desa Jaring Halus ... 37
9. Hasil Analisis Rata- rata Logam Berat Cd pada Air, Sedimen dan Kepiting di Perairan Danau Siombak ... 38
10. Hasil Analisis Rata- rata Logam Berat Fe pada Air, Sedimen dan Kepiting di Perairan Danau Siombak ... 39
11. Hasil Analisis Rata- rata Logam Berat Cd pada Air, Sedimen dan Kepiting di Perairan Desa Jaring Halus ... 40
12. Hasil Analisis Rata- rata Logam Berat Fe pada Air, Sedimen dan Kepiting di Perairan Desa Jaring Halus ... 41
13. Nilai BCF Cd pada Kepiting dengan Air di Perairan Danau Siombak . 42
14. Nilai BCF Cd pada Kepiting dengan Air di Perairan Desa Jaring Halus ... 42
Halus ... 43
No. Teks Halaman
1. Alat dan Bahan yang Digunakan ... 79
2. Pengambilan Sampel ... 85
3. Proses Destruksi ... 86
4. Perhitungan Konsentrasi Logam Berat ... 89
5. Baku Mutu Air Laut Untuk Biota Laut ... 90
6. Data Panjang dan Berat Kepiting ... 92
7. Data Dasar Konsentrasi Logam Berat ... 93
8. Hasil Analisis di Laboratorium Kesehatan Daerah Medan ... 95
9. Nilai Koefisien Determinasi (R2) dan Koefisien Korelasi (r) pada Air, Sedimen dan Kepiting ... 107
PENDAHULUAN
Latar Belakang
Danau Siombak adalah danau yang terbentuk karena adanya pengerukan tanah yang dilakukan untuk pembangunan jalan tol Belmera (Belawan Medan Tanjung Morawa). Tanah dikeruk dan terisi oleh air hujan dan air sungai sehingga terbentuklah Danau Siombak (Sandy et al., 2017). Danau Siombak dialiri oleh tiga sungai yaitu Sungai Badera, Sungai Terjun dan Sungai Paluh Besar, yang mana di sepanjang ketiga sungai tersebut banyak ditemukan aktivitas kehidupan manusia yang menghasilkan berbagai jenis limbah cair dari kegiatan domestik, industri pabrik, pertanian dan pertambakan yang mencemari lingkungan perairannya.
Desa Jaring Halus merupakan daerah pesisir yang terletak di kecamatan Secanggang, Kabupaten Langkat Sumatera Utara. Desa ini berbatasan langsung dengan Suaka Margasatwa Langkat Timur Laut yang didominasi oleh tumbuhan mangrove dan beberapa biota (Nasution, 2017). Banyaknya aktivitas kapal yang hilir mudik untuk mengangkat bahan- bahan pokok seperti sandang, pangan dan papan tanpa henti juga dapat mempengaruhi kondisi perairan Desa Jaring Halus akibat buangan minyak dan lain sebagainya dan banyak aktivitas kehidupan manusia yang limbah cairnya dialirkan langsung ke badan perairan yang dapat mempengaruhi penurunan kualitas perairan.
Adanya limbah dari kegiatan manusia akan mencemari perairan, baik limbah organik maupun anorganik. Pencemaran air oleh komponen anorganik, diantaranya adalah berbagai macam pencemaran logam berat yang berbahaya
bagi sistem perairan, termasuk biota-biota yang terdapat di dalamnya (Connell dan Miller, 1995).
Logam berat merupakan jenis limbah yang potensial merusak lingkungan hidup karena mengandung Bahan Beracun Berbahaya (B3). Logam berat seperti kadmium (Cd), merkuri (Hg) dan timbal (Pb) merupakan jenis logam non esensial. Pada tingkatam konsentrasi tertentu logam ini menjadi logam yang beracun bagi makhluk hidup. Merkuri (Hg) bersama logam- logam lainnya seperti besi (Fe), arsen (As), kadmium (Cd), timbal (Pb), nikel (Ni), krom (Cr), seng (Zn), dan tembaga (Cu) merupakan unsur-unsur logam berat yang potensial menimbulkan pencemaran pada lingkungan (Juhriah dan Alam, 2016).
Kepiting merupakan salah satu jenis biota perairan yang mempunyai ketahanan hidup yang baik pada habitatnya. Selama ini keberadaan kepiting sering dijadikan sebagai bioindikator perairan karena kemampuannya dalam mengakumulasi logam berat yang cukup tinggi dibandingkan dengan biota lainnya (Fitriani, 2017).
Berdasarkan informasi yang diperoleh diketahui bahwasanya populasi kepiting bakau (Scylla olivacea) di perairan Danau Siombak dan Perairan Desa Jaring Halus telah mengalami pengurangan karena adanya pencemaran perairan yang disebabkan limbah pabrik maupun limbah domestik yang masuk ke badan perairan salah satunya adalah logam berat. Untuk membuktikan hal tersebut maka perlu dilakukan penelitian dengan cara menganalisis kandungan logam berat yang terdapat pada daging kepiting, air dan sedimen di dalam perairan tersebut untuk kemudian dibandingkan dengan ketetapan Batas Maksimum Cemaran Logam Berat Dalam Pangan. Maka dari itu perlu dilakukan penelitian tentang analisis
logam berat pada daging kepiting, air dan sedimen di dalam suatu perairan tersebut.
Perumusan Masalah
Kepiting bakau (Scylla olivacea) merupakan jenis kepiting yang bernilai ekonomis penting yang dapat dijumpai dengan mudah di beberapa pasar tradisional kota Medan. Selama ini keberadaan kepiting bakau (Scylla olivacea) yang diperjual belikan tersebut sering kali diperoleh dari perairan yang diduga tercemar logam berat seperti perairan Danau Siombak dan perairan Desa Jaring Halus. Hal ini tentunya sangat berbahaya bagi masyarakat yang mengkonsumsi kepiting bakau (Scylla olivacea) tersebut, mengingat fungsi ekologisnya sebagai biota yang mempunyai kemampuan dalam menyerap logam berat seperti kadmium (Cd) dan besi (Fe). Oleh karena itu analaisis kandungan logam berat kadmium (Cd) dan besi (Fe) pada kepiting bakau (Scylla olivacea) yang berasal dari perairan Danau Siombak dan perairan Desa Jaring Halus diharapkan dapat memberikan informasi bagi instansi terkait dan masyarakat pada umumnya agar dapat lebih bijaksana dalam memilih bahan pangan yang aman untuk dikonsumsi.
1. Seberapa besarkah kandungan logam berat kadmium (Cd) dan besi (Fe) pada air, sedimen dan daging kepiting bakau (Scylla olivacea) di perairan Danau Siombak dan perairan Desa Jaring Halus?
2. Apakah air, sedimen dan kepiting bakau (Scylla olivacea) yang diperoleh dari perairan Danau Siombak dan perairan Desa Jaring Halus telah melampaui baku mutu?
Kerangka Penelitian
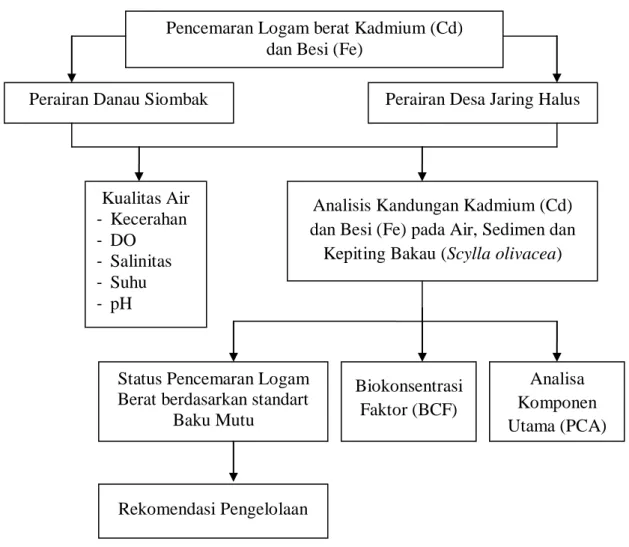
Kepiting bakau (Scylla olivacea) merupakan bahan pangan yang disukai masyarakat karena memiliki nilai gizi yang baik dan cita rasa yang lezat. kepiting bakau (Scylla olivacea) dapat mengakumulasi logam berat seperti kadmium (Cd) dan besi (Fe). Untuk memperoleh informasi kandungan logam berat yang ada pada kepiting bakau (Scylla olivacea) air dan sedimen di perairan Danau Siombak dan perairan Desa Jaring Halus maka diperlukan analisis kandungan logam berat kadmium (Cd) dan besi (Fe) yang terkandung pada daging kepiting bakau (Scylla olivacea) air dan sedimen yang ada diperairan tersebut. Berikut adalah kerangka pemikiran penulis dapat dilihat pada Gambar 1.
Gambar 1. Kerangka Penelitian
Analisa Komponen Utama (PCA)
Rekomendasi Pengelolaan
Biokonsentrasi Faktor (BCF) Kualitas Air
- Kecerahan - DO
- Salinitas - Suhu - pH
Pencemaran Logam berat Kadmium (Cd) dan Besi (Fe)
Perairan Danau Siombak Perairan Desa Jaring Halus
Analisis Kandungan Kadmium (Cd) dan Besi (Fe) pada Air, Sedimen dan
Kepiting Bakau (Scylla olivacea)
Status Pencemaran Logam Berat berdasarkan standart
Baku Mutu
Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengetahui kandungan logam berat kadmium (Cd) dan besi (Fe) pada air, sedimen dan daging kepiting bakau (Scylla olivacea)di perairan Danau Siombak dan Perairan Desa Jaring Halus
2. Mengetahui tingkat status pencemaran kandungan logam berat kadmium (Cd) dan Besi (Fe) pada air, sedimen dan kepiting bakau (Scylla olivacea) yang diperoleh dari perairan Danau Siombak dan perairan Desa Jaring Halus dengan standart baku mutu yang sudah ditentukan
Manfaat Penelitian
Adanya informasi mengenai kandungan logam berat kadmium (Cd) dan besi (Fe) pada daging kepiting bakau (Scylla olivacea) yang terdapat di perairan Danau Siombak dan perairan Desa Jaring Halus dan dapat bermanfaat bagi masyarakat dalam memilih dan mengolah makanan menjadi makanan yang layak konsumsi (aman dan sehat). Selain itu, penelitian ini juga bermanfaat sebagai bahan perbandingan untuk penelitian selanjutnya yang memiliki relevansi dengan penelitian ini.
TINJAUAN PUSTAKA
Klasifikasi dan Morfologi Kepiting Bakau (Scylla olivacea)
Gambar 2. Kepiting Bakau (Scylla olivacea)
Kepiting bakau merupakan jenis kepiting yang termasuk ke dalam kelompok famili Portunidae yang berbentuk pipi dan melebar serta memiliki lima pasang kaki. Secara taksonomi klasifikasi kepiting bakau adalah sebagai berikut:
Filum : Arthropoda Kelas : Crustacea Subkelas : Malacostraca Ordo : Decapoda Famili : Portunidae Genus : Scylla
Spesies : Scylla olivacea (Motoh, 1977)
Kepiting bakau (Scylla olivacea) memiliki ukuran lebar kerapas lebih besar dari ukuran panjang tubuhnya. Dengan permukaan kerapas agak licin. Pada
dahi antara sepasang matanya terdapat enam buah duri dan disamping kanan dan kiri masing- masing terdapat Sembilan duri (Chairunnisa, 2004).
Kepiting bakau memiliki bentuk morfologi, yakni pada bentuk duri yang terdapat di antara dua tangkai mata serta bentuk dan jumlah duri pada bagian sisi luar karapasnya. Scylla tranquebarica memiliki bentuk duri diantara mata yang agak rendah, bulat, namun lebih tinggi dari duri Scylla olivacea. Bagian tubuh kepiting juga dilengkapi bulu dan rambut sebagai indera penerima, bulu tersebut terdapat hampir di seluruh tubuh yang sebagian besar bergerombol pada kaki jalan. Scylla tranquebarica memiliki warna hijau zaitun atau hijau ungu (Trivedi dan Vachhrajani, 2013).
Menurut Syafiq (2015) kepiting dikenal sebagai salah satu makanan dari laut (seafood) yang digemari oleh masyarakat kita. Kepiting adalah sumber protein yang baik (mengandung sekitar 18-19.5 gram protein per 100 gram).
Komposisi zat gizi dari kepiting dibandingkan ikan/seafood lainnya, yang dapat dilihat pada Tabel 1.
Tabel 1. Komposisi karkas Kepiting Bakau (Scylla olivacea)/100 gr Spesies Energi
(keal)
Air (g)
Protein (g)
Lemak (g)
Kolestrol (mg)
Kalsium (mg)
Besi (mg)
Niacin (mg)
Kepiting 87 79.02 18.06 1.08 78 89 0.74 -
Lobster 90 76.76 18.80 0.90 95 - - 1.455
Kerang 81 82.06 9.45 2.30 - 8 5.11 2.010
Tiram 88 78.57 16.78 0.76 33 24 0.29 1.150
Udang 106 75.86 20.31 1.73 152 52 2.41 2.552 Sumber : Syafiq (2015)
Habitat Kepiting Bakau (Scylla olivacea)
Kepiting bakau termasuk hewan nokturnal, keluar dari persembunyiannya beberapa saat setelah matahari terbenam dari bergerak sepanjang malam terutama
untuk mencari makan, kemudian akan membenamkan dirinya kembali pada saat matahari akan terbit. Beberapa jenis satwa yang hidup di sekitar perakaran mangrove, baik di substrat yang keras maupun lunak (lumpur) antara lain adalah jenis kepiting bakau, kerang dan golongan invertebrata lainnya. Kepiting bakau (Scylla spp.) merupakan hewan yang berasosiasi kuat dengan hutan mangrove dan memiliki daerah penyebaran yang luas. Hal ini disebabkan karena kepiting bakau memiliki toleransi terhadap faktor abiotik terutama pada suhu dan salinitas (Gita et al., 2015).
Parameter Lingkungan Suhu
Suhu di perairan dipengaruhi oleh musim, lintang, ketinggian dari permukaan laut, waktu dalam hari, sirkulasi udara, penutupan awan, aliran serta kedalaman badan air. Perubahan suhu air berpengaruh terhadap sifat fisik, kimia, dan biologi perairan. Peningkatan suhu akan meningkatkan viskositas, reaksi kimia, evaporasi dan volatilisasi. Sebagian besar proses fisik, biologi dan karakter kimia pada air permukaan dipengaruhi oleh temperatur. Peningkatan suhu berkorelasi positif dengan proses kimia yang terjadi pada air. Peningkatan suhu juga dapat membahayakan biota air. Peningkatan suhu menyebabkan penurunan kelarutan gas dalam air, seperti gas O2, CO2, N2 dan CH4 (Effendi, 2003).
Berdasarkan daur hidupnya kepiting bakau dalam menjalani hidupnya diperkirakan melewati berbagai kondisi perairan. Pada saat pertama kali kepiting ditetaskan, suhu air laut umumnya berkisar 25-270C. Secara gadual suhu air kearah pantai akan semakin rendah. Kepiting muda yang baru berganti kulit dari
megalopa yang memasuki muara sungai dapat mentoleransi suhu di atas 180C (Nasution, 2017).
Pola temperatur atau oksigen di perairan danau terutama dipengaruhi oleh intensitas cahaya matahari sehingga umumnya pada lapisan permukaan perairan akan mempunyai temperatur yang lebih tinggi dibandingkan pada lapisan air yang lebih dalam. Apabila temperatur meningkat maka kelarutan oksigen akan menurun dan sebaliknya. Dengan demikian maka khususnya untuk ekosistem perairan di daerah tropis yang umumnya mempunyai temperatur yang relatif tinggi akan mempunyai keterbatasan dalam menyerap oksigen. Kisaran nilai kelarutan oksigen ini menunjukkan kualitas perairan yang masih baik. Salah satu faktor yang sangat mempengaruhi kelarutan oksigen dalam air adalah temperatur air (Barus, 2004).
Pengaruh suhu secara langsung menentukan kehadiran spesies akuatik, mempengaruhi pemijahan, penetasan, aktivitas dan pertumbuhan organisme.
Sedangkan secara tidak langsung dapat menyebabkan perubahan kesetimbangan kimia. Suhu sangat mempengaruhi kehidupan biota di dalam suatu perairan (Odum, 1996). Suhu merupakan salah satu parameter untuk mempelajari transfortasi dan penyebaran polutan yang masuk ke lingkungan laut. Sebagai contoh, suhu air di permukaan laut mempengaruhi sifat tumpahan minyak dan juga pengendaliannya (Mukhtasor, 2007) .
pH (Derajat Keasaman)
Derajat keasaman (pH) merupakan fungsi dari kandungan CO2 yang terlarut dalam air. Kadar CO2 akan berkurang oleh kegiatan fotosintesis dan akan bertambah karena respirasi. Derajat keasaman (pH) merupakan tingkat keasaman
dari suatu perairan. Nilai pH ideal untuk perairan adalah 6,5-8,5. Organisme perairan mempunyai kemampuan yang berbeda dalam bertoleransi pH perairan.
Kematian lebih sering diakibatkan karena pH yang rendah daripada pH yang tinggi. Batas toleransi organisme perairan terhadap pH bervariasi dan dipengaruhi banyak faktor antara lain suhu, oksigen terlarut, alkalinitas, adanya berbagai anion dan kation, jenis dan stadia organisme (Pescod, 1973).
Barus (2001) menyatakan bahwa nilai pH ideal untuk organisme di perairan adalah antara 7 - 8,5 dan pada kondisi yang berlebihan yaitu sangat basa dan sangat asam dapat berbahaya untuk kelangsungan hidup organisme karena menyebabkan terjadinya gangguan metabolisme dan respirasi. Menurut Barus (2004) pH yang sangat rendah akan menyebabkan mobilitas berbagai senyawa logam berat terutama ion aluminium yang bersifat toksik akan semakin tinggi yang akan mengancam kelangsungan hidup organisme air sedangkan pH yang tinggi akan menyebakan kadar ammonium dan amoniak akan meningkat.
Derajat keasaman (pH) juga berpengaruh terhadap toksisitas suatu senyawa kimia. Sebagian besar biota akuatik sensitif terhadap perubahan pH serta menyukai pH berkisar 7-8,5. Nilai pH sangat berpengaruh terhadap proses biokimia perairan, misalnya proses nitrifikasi akan berakhir jika pH rendah (Effendi, 2003).
Kecerahan
Kecerahan air merupakan ukuran kejernihan suatu perairan berdasarkan kemampuan penetrasi cahaya pada air. Semakin tinggi suatu kecerahan perairan semakin dalam cahaya menembus ke dalam air. Kecerahan air menggambarkan sifat optik air yang ditentukan berdasarkan banyaknya cahaya yang diserap dan
dipancarkan oleh partikel-partikel padat tersuspensi yang terdapat di dalam air.
Berkurangnya kecerahan pada suatu perairan dapat mengurangi kemampuan fotosintesis tumbuhan air dan kegiatan fisiologi biota air atau dengan kata lain partikel-partikel padat di dalam suatu perairan terutama yang berupa suspensi dapat mempengaruhi aktivitas kehidupan berbagai biota perairan, salah satunya adalah kepiting bakau (Adha, 2015).
Kekeruhan/kecerahan air dapat disebabkan oleh adanya bahan-bahan organik dan ananorganik yang tersuspensi dalam kolam air maupun yang terlarut, sedangkan kecerahan adalah kemampuan cahaya matahari menembuh kolam air.
Dengan demikian semakin keruh air, akan semakin rendah kecerahan airnya.
Secara langsung kecerahan/kekeruhan air ini tidak besar pengaruhnya terhadap pertumbuhan ikan yang dibudidayakan, namun air kolam yang keruh akan menghalangi masuknya cahaya matahari ke dalam air sehingga proses fotosintesis akan terhambat (Parlaungan, 1996).
Oksigen Terlarut (Dissolved oxygen/ DO)
Disolved Oxygen (DO) merupakan banyaknya oksigen terlarut dalam suatu perairan. Oksigen terlarut ini merupakan suatu faktor yang sangat penting di dalam ekosistem perairan, terutama dibutuhkan untuk respirasi bagi sebagian besar organisme air. Oleh sebab itu kelarutan oksigen dalam air sangat dipengaruhi suhu. Kepiting dapat hidup pada perairan yang memiliki kandungan oksigen terlarut lebih dari 4 mg/liter (Daulay, 2013).
Kadar oksigen terlarut yang tinggi tidak menimbulkan pengaruh fisiologi bagi manusia. kepiting dan organisme akuatik lain membutuhkan oksigen dengan jumlah cukup. Kebutuhan oksigen sangat dipengaruhi oleh suhu, dan bervariasi
antarorganisme. Keberadaan logam berat yang berlebihan di perairan mempengaruhi sistem respirasi organisme akuatik sehinga pada saat kadar oksigen terlarut rendah dan terdapat logam berat dengan konsentrasi tinggi, organisme akuatik lebih menderita (Effendi, 2003).
Semakin tinggi temperatur dan salinitas perairan maka tingkat kelarutan O2 dalam air semakin rendah. Lapisan atas permukaan laut dalam keadaan normal mengandung O2 terlarut sebesar 4,5 – 9,0 mg/l. Untuk kehidupan biota laut secara layak kelarutan O2 harus lebih besar daripada 5,0 mg/l (Kep.51/MENKLH/2004). Selain temperatur dan salilnitas, kelarutan O2 juga dipengaruhi oleh tekanan hidrostatik. Semakin dalam laut maka kelarutan O2 semakin kecil. Pada kedalaman laut 1.000 m (tekanan hidrostatik 100 atm), maka tekanan parsial O2 meningkat sebesar ± 13% dan kelarutannya menurun sebesar ± 0,1% (Sanusi, 2006).
Dekomposisi bahan organik dan oksidasi bahan organik dapat mengurangi kadar oksigen di perairan hingga mencapai nol (anaerob). Kebutuhan oksigen sangat dipengaruhi oleh suhu dan bervariasi tiap jenis. Keberadaan limbah yang masuk ke suatu perairan akan menurunkam kadar oksigen di perairan. Hal tersebut terkait dengan pemanfaatan yang berlebih terhadap oksigen terutama pada proses penguraian bahan organik oleh bakteri pengurai (Effendi, 2003).
Salinitas
Air laut merupakan larutan (solution) kompleks yang mengandung berbagai senyawa atau elemen-elemen kimia baik organik maupun anorganik.
Kandungan elemen-elemen kimia terlarut dalam air laut dinyatakan sebagai salinitas atau klorinitas (Sanusi, 2006). Sebaran salinitas di air laut dipengaruhi
oleh berbagai faktor seperti pola sirkulasi air, penguapan, curah hujan dan aliran sungai (Nontji, 2007). Nybakken (1992), mengemukakan bahwa perbedaan salinitas terjadi karena perbedaan dalam penguapan dan presipitasi (hujan).
Salinitas merupakan salah satu faktor bagi organisme akuatik yang dapat memodifikasi perubah fisika dan kimia air menjadi satu kesatuan pengaruh yang berdampak terhadap organisme. Hal ini sangat berpengaruh terhadap proses metabolisme kepiting yang dapat berpengaruh pada tingkat pembelanjaan energi.
Oleh sebab itu, pertumbuhan kepiting yang maksimum hanya dapat dihasilkan apabila penggunaan energi untuk metabolisme (Sagala et al., 2013).
Salinitas merupakan faktor lingkungan yang sangat penting pada keberadaan mangrove dan kepiting bakau. Kepiting bakau hidup dengan baik pada kisaran salinitas 10–35‰. Kepiting bakau pada salinitas terendah 8,9‰. Pengaruh salinitas secara tidak langsung mengakibatkan perubahan komposisi dalam suatu ekosistem (Romimohtarto, 2009).
Sedimen
Karakteristik sedimen diketahui juga menentukan kehidupan komunitas mangrove, substrat sedimen didaerah hutan mangrove mempunyai ciri-ciri selalu basah, mengandung garam, memiliki oksigen yang sedikit, berbutir-butir dan kaya akan bahan organik. Perbedaan tingkat kerapatan vegetasi mangrove serta jenis mangrove yang ditemukan juga berpengaruh terhadap kandungan bahan organik pada substrat dimana sesuai dengan besarnya nilai tingkat kerapatan suatu mangrove akan mempengaruhi proses penguraian dari bahan organik tersebut (Darmadi et al, 2012).
Substrat merupakan faktor pembatas utama terhadap pertumbuhan dan distribusi mangrove. Substrat dasar merupakan salah satu faktor ekologi utama yang mempengaruhi sruktur komunitas makrobentos sehingga sebagai penggali pemakan deposit jumlahnya sangat banyak pada sedimen lunak dan berlumpur karena daerah tersebut kaya akan bahan organik. Substrat di sekitar hutan mangrove sangat mendukung kehidupan kepiting bakau, terutama untuk melangsungkan perkawinannya dan melakukan pergantian kulit dalam kaitannya dengan kehidupan dan sebaran kepiting, maka substrat tanah dasar perairan hutan mangrove merupakan faktor yang sangat penting (Prianto, 2007).
Pencemaran Logam Berat
Peningkatan jumlah industri akan selalu diikuti oleh pertambahan jumlah limbah, baik berupa limbah padat, cair dan gas. Limbah industri terutama yang bersumber dari pabrik elektronik, plastik, kertas dan sebagainya dapat membahayakan lingkungan sebab salah satu diantara limbah tersebut diperkirakan mengandung logam berat antara lain adalah Pb (timbal) dan logam berat lainnya (Hasan et al., 2017).
Bahan pencemar dari limbah industri dapat mencemarkan perairan dan berdampak negatif yaitu terjadinya perubahan ekosistem muara berupa perubahan temperatur, pH, BOD dan COD serta kandungan logam berat yang sangat mempengaruhi kehidupan flora dan fauna perairan. Limbah ini biasanya berasal dari industri maupun rumah tangga yang melibatkan unsur-unsur logam seperti Timbal (Pb), Arsen (As), Kadmium (Cd), Merkuri (Hg), Krom (Cr), Nikel (Ni), Kalsium (Ca), Magnesium (Mg), dan Cuprum (Cu). Limbah tersebut umumnya
merupakan limbah yang tidak dapat atau sulit didegradasi oleh mikroorganisme (Heriyanto, 2011).
Logam berat
Toksisitas logam berat dapat dibagi ke dalam 3 kelompok, yaitu bersifat toksik tinggi yang terdiri dari atas unsur-unsur Hg, Cd, Pb, Cu, dan Zn, bersifat toksik sedang terdiri dari unsur-unsur Cr, Ni, dan Co, dan bersifat toksik rendah terdiri atas unsur Mn dan Fe. Taraf toksisitas logam berat sangat beragam bagi berbagai organisme, tergantung dari berbagai aspek yang antara lain spesies, cara toksikan memasuki tubuh, frekuensi dan lamanya paparan, konsentrasi toksikan, bentuk dan sifat fisika/kimia toksikan serta kerentanan berbagai spesies terhadap toksikan. Taraf toksisitas logam berat terhadap hewan air mulai dari yang paling tinggi adalah Hg, Cd, Zn, Pb, Cr, Ni dan Co. Sementara itu, tingkat toksisitas terhadap manusia dari yang paling toksik adalah Hg, Cd, Ag, Ni, Pb, As, Cr, Sn dan Zn (Fitriani, 2017).
a.) Kadmium (Cd)
Kadmium bersumber dari aktivitas alamiah dan antropogenik. Secara alamiah Cd didapat dari letusan gunung berapi, jatuhan atmosferik, pelapukan bebatuan, dan jasad organik yang membusuk. Logam Cd juga didapat dari kegiatan manusia, yaitu industri kimia, pabrik tekstil, pabrik semen, tumpahan minyak, pertambangan, pengolahan logam, pembakaran bahan bakar, dan pembuatan serta penggunaan pupuk fosfat. Dalam kehidupan sehari-hari, mainan anak-anak, fotografi, tas dari vinil, dan mantel merupakan sumber Cd (Darmono, 1995).
Kadar Cd di perairan alami berkisar antara 0,29 – 0,55 ppb dengan rata- rata 0,42 ppb. Kadmium tergolong logam berat dan memiliki afinitas yang tinggi terhadap grup sulfhidrid daripada enzim dan meningkat kelarutannya dalam lemak. Di perairan tawar kemampuan pembentukan kompleks Cd oleh asam humus sekitar 2,7% daripada total Cd terlarut, sementara di perairan estuari lebih rendah dari 1% daripada total Cd terlarut. Jadi, selain ditentukan oleh kadar asam humus dan Cd terlarut, parameter pH dan salinitas berperan dalam membentuk ikatan kompleks logam berat-asam humus. Logam berat Cd terlarut dalam air akan mengalami proses adsorpsi oleh partikel tersuspensi dan mengendap di sedimen. Proses adsorpsi akan diikuti oleh proses desorpsi yang mengembalikan Cd dalam bentuk terlarut dalam badan air (Sanusi, 2006). Menurut Rangkuti (2009) Kadmium dalam air laut berbentuk senyawa klorida (CdCl2), sedangkan pada perairan tawar kadmium berbentuk karbonat (CdCO3). Pada perairan payau kedua senyawa tersebut berimbang.
b.) Besi (Fe)
Logam besi (Fe) sebenarnya adalah mineral yang dibutuhkan tubuh untuk pembentukan hemoglobin, terdapat pada buah, sayuran, serta suplemen makanan.
Fe dapat berasal dari buangan limbah pabrik ataupun limbah rumah tangga hingga mencemari lingkungan sungai, dalam jumlah yang berlebihan pada tubuh manusia Fe akan bersifat racun, cepat terserap dalam saluran pencernaan, dan sifat korosif pada besi akan lebih meningkatkan penyerapan racun (Pratama et al., 2012).
Buangan industri yang mengandung persenyawaan logam berat Fe bukan hanya bersifat toksik terhadap tumbuhan tetapi juga terhadap hewan dan manusia.
Hal ini berkaitan dengan sifat-sifat logam berat yang sulit didegradasi, sehingga
mudah terakumulasi dalam lingkungan perairan dan keberadaannya secara alami sulit dihilangkan, dapat terakumulasi dalam biota perairan termasuk kepiting, kerang, ikan dan sedimen, memiliki waktu paruh yang tinggi dalam tubuh biota laut serta memiliki nilai faktor konsentrasi yang besar dalam tubuh organisme (Supriyantini dan Endrawati, 2015).
Sekalipun besi (Fe) diperlukan oleh tubuh manusia, tetapi dalam dosis besar dapat merusak dinding usus, kematian sering kali disebabkan oleh rusaknya dinding usus ini, debu besi juga dapat terakumulasi di dalam alveoli dan dapat menyebabkan berkurangnya fungsi paru-paru (Soemirat, 2004). Berdasarkan standart baku mutu cemaran logam berat yang diperbolehkan dalam pangan yaitu menurut Badan Pengawas Obat dan Makanan No 5 Tahun 2018 dan SNI 7387 Tahun 2009 disajikan pada Tabel 2. dibawah ini :
Tabel 2. Standar baku mutu cemaran logam berat dalam pangan
Logam Simbol Standart Baku (mg/l)
BPOM RI1 SNI2
Kadmium Cd 0.1 -
Besi Fe - 1
Sumber : SNI 7387:2009. Batas Maksimum Cemaran Logam Berat dalam Pangan. Panitia Teknis 67-02 Bahan Tambahan Pangan dan Kontaminan. Badan Standarnisasi Nasional, Jakarta1. BPOM No 5. 2018. Batas Maksimum Cemaran Logam Berat dalam Pangan Olahan. Badan Pengawas Obat dan Makanan. Jakarta2.
Keberadaan besi diperairan dapat berasal dari buangan logam besi yang mengalami korosif dan pelarutan di air, serta buangan limbah domestik dan industri yang mengandung kadar besi. Di perairan kadar besi (Fe2+) yang tinggi berkorelasi dengan kadar bahan organik yang tinggi, atau kadar besi yang tinggi terdapat pada air yang berasal dari air tanah dalam yang bersuasana anaerob atau dari lapisan dasar perairan yang sudah tidak mengandung oksigen. Keberadaan besi juga dapat memberikan penampakan keruh dan berwarna pada air, serta
meninggalkan noda pada pakaian yang dicuci oleh air yang mengandung besi (Amansyah dan Syarif, 2014).
Logam Berat di Air
Logam berat yang terlarut dalam badan perairan pada konsentrasi tertentu akan berubah fungsi menjadi sumber racun bagi bagi sistem kehidupan di perairan. Walaupun daya racun yang ditimbulkan oleh satu logam berat terhadap biota perairan tidak sama, namun kehancuran suatu kelompok dapat menjadikan terputusnya satu rantai makanan. Pada tingkatan selanjutnya dapat menghancurkan tatanan suatau ekosistem perairan (Palar, 1994).
Konsentrasi bahan pencemar yang masuk ke perairan bisa mempengaruhi kehidupan organisme di perairan. Sebagaimana diketahui unsur logam berat yang masuk ke perairan berasal dari berbagai kegiatan industri selain bersumber dari alam itu sendiri (alamiah). Logam berat yang dilimpahkan ke perairan, baik di sungai ataupun laut akan dipindahkan dari badan airnya melalui beberapa proses yaitu : pengendapan, adsorbsi dan absorbsi oleh organisme perairan. Logam berat mempunyai sifat yang mudah mengikat bahan organik dan mengendap di dasar perairan dan bersatu dengan sedimen sehingga kadar logam berat dalam sedimen lebih tinggi dibandingkan dalam air (Harahap, 1991).
Berdasarkan peraturan pemerintah kandungan logam berat yang boleh masuk ke perairan laut mempunyai batasan tertentu. Baku mutu air laut untuk biota laut berdasarkan Keputusan Menteri Lingkungan Hidup No.51 Tahun 2004 dan baku mutu berdasarkan Environmental Protection Agency (EPA) 1986 dapat di lihat pada Tabel 3.
Tabel 3. Standar baku mutu air laut untuk biota laut terhadap logam berat
Logam Simbol Standart Baku (mg/l)
Kep Men LH1 EPA2
Kadmium Cd 0.0010 0.0093
Besi Fe - 0.5
Sumber : KepMen LH No 51 Tahun 20041. USEPA.(1986). Quality Criteria for Water. EPA- 440/5-86-001, Office of Water Regulation Standards, Washington DC, USA2
Logam Berat di Sedimen
Menurut Sanusi (2006) tekstur atau ukuran partikel sedimen terbentuk terutama disebabkan oleh adanya kekuatan arus. Dengan kata lain, faktor arus (hidrodinamika) merupakan energi sortasi sedimen. Perairan yang memiliki kondisi arus yang dinamis (high energy environment – dynamic waters), memiliki tekstur sedimen yang kasar (kerikil, pasir). Sementara perairan dimana kondisi arusnya tenang atau tidak dinamis (low energy environment – sluggish waters) memiliki tekstur sedimen yang lebih halus (lumpur, liat). Perairan yang sering terjadi deposisi material tersuspensi (organik dan anorganik) umumnya memiliki tekstur sedimen yang halus.
Zat-zat yang masuk ke laut akan berakhir menjadi sedimen. Dalam prosesnya semua zat yang ada terlibat proses biologi dan kimia yang terjadi sepanjang ke dalaman laut. Sebelum mencapai dasar laut dan menjadi sedimen, zat tersebut melayang-layang di kolom perairan. Setelah mencapai dasar laut pun, sedimen tidak diam tetapi sedimen akan terganggu ketika hewan laut-dalam mencari makan. Sebagian sedimen mengalami erosi dan tersuspensi kembali oleh arus bawah sebelum kemudian jatuh kembali dan tertimbun. Terjadi reaksi kimia antara butir-butir mineral dan air laut sepanjang perjalanannya kedasar laut dan reaksi tetap berlangsung setelah penimbunan, yaitu ketika air laut terperangkap di antara butiran mineral (Supangat dan Muawanah).
Sifat fisik kimia material padatan tersuspensi yang memiliki kemampuan mengadsorpsi logam berat terlarut dalam kolom air, maka deposisi padatan tersuspensi dalam suatu perairan akan menyebabkan akumulasi logam berat tersebut selain material organik dalam sedimen. Makin tinggi kandungan polutan organik dan anorganik dalam kolom air, makin tinggi pula akumulasi polutan tersebut dalam sedimen. Oleh karena itu kualitas fisik kimia sedimen suatu perairan dapat dijadikan indikator baik buruknya kualitas suatu perairan. Dilihat dari aspek kimia, akumulasi bahan organik dalam substrat halus akan menentukan status reduksi-oksidasi, bergantung ketersediaan O2 terlarut dalam air jebakan dan pH sedimen (Sanusi, 2006).
Baku mutu logam berat di dalam lumpur atau sedimen di Indonesia belum ditetapkan, sehingga sebagai acuan dapat digunakan baku mutu yang dikeluarkan oleh IADC/CEDA (1997) dan USEPA (1986) mengenai kandungan logam yang dapat ditoleransi keberadaannya dalam sedimen berdasarkan standar kualitas Belanda. Seperti dapat dilihat pada tabel 4 dan 5 dibawah ini adalah sebagai berikut :
Tabel 4. Baku mutu logam berat Kadmium (Cd) dan Besi (Fe) dalam sedimen
Logam Simbol Standart Baku Mutu
(mg/kg)
Kadmium Cd 0.006*
Besi Fe 20**
Sumber: Baku mutu sedimen dengan standar sediment quality guideline values for metals and associated levels of concern to be used in doing assesments of sediment quality (2003)*. USEPA.(1986) dalam Widiyanto 2005**.
Tabel 5. Baku mutu logam berat Kadmium (Cd) dalam sedimen Logam
Berat
Simbol Level Target
Level Limit
Level Test
Level Intervensi
Level Bahaya
Kadmium Cd 0.8 2 7.5 12 30
Merkuri Timbal
Hg Pb
0.3 85
0.5 530
1.6 530
10 530
15 1000
Sumber: IADC/CEDA (1997) Keterangan :
a. Level target. Jika konsentrasi kontaminan yang ada pada sedimen memiliki nilai yang lebih kecil dari nilai level target, maka substansi yang ada pada sedimen tidak terlalu berbahaya bagi lingkungan.
b. Level limit. Jika konsentrasi kontaminan yang ada di sedimen memiliki nilai maksimum yang dapat ditolerir bagi kesehatan manusia maupun ekosistem.
c. Level tes. Jika konsentrasi kontaminan yang ada di sedimen berada pada kisaran nilai antara level limit dan level tes, maka dikategorikan sebagai tercemar ringan.
d. Level intervensi. Jika konsentrasi kontaminan yang ada di sedimen berada pada kisaran nilai antara level tes dan level intervensi, maka dikategorikan sebagai tercemar sedang.
e. Level bahaya. Jika konsentrasi kontaminan berada pada nilai yang lebih besar dari baku mutu level bahaya maka harus dengan segera dilakukan pembersihan sedimen.
Toksisitas Logam Berat
Kadmium (Cd) merupakan salah satu jenis logam berat yang berbahaya karena elemen ini beresiko tinggi terhadap pembuluh darah. Apabila kadmium masuk ke dalam tubuh maka sebagian besar akan terkumpul di dalam ginjal, hati dan sebagian yang dikeluarkan lewat saluran pencernaan. Kadmium dapat mempengaruhi otot polos pembuluh darah secara langsung maupun tidak langsung lewat ginjal, sebagai akibatnya terjadi kenaikan tekanan darah. Senyawa ini bisa mengakibatkan penyakit liver dan gangguan ginjal serta tulang. Senyawa yang mengandung kadmium juga mengakibatkan kanker (Saragih, 2018).
Kadmium dalam tubuh terakumulasi dalam hati dan ginjal terutama terikat sebagai metalotienin. Kadmium lebih beracun bila terhisap melalui saluran pernapasan daripada melalui saluran pencernaan. Dalam beberapa jam korban akan mengeluh gangguan pernapasan, nausea, muntah, kepala pusing dan sakit
pinggang. Selain itu menyerang sistem saraf pusat sehingga menyebabkan gangguan saraf sensoris, gangguan saraf motorik (Darmono, 2001).
Salah satu efek utama yang ditimbulkan dari keracunan kadmium adalah lemah dan rapuh tulang. Umumnya tulang belakang dan kaki sakit, dan gaya berjalan pincang karena cacat tulang yang disebabkan oleh Kadmium. Rasa sakit kemudian melemahkan, dengan patah tulang yang lebih umum dibandingkan tulang yang melemah. Komplikasi lain yang tejadi adalah batuk, kanker, anemia, dan gagal ginjal, yang kemudian menyebabkan kematian. Penderita penyakit ini banyak terjadi pada wanita pasca menopause (Surbakti, 2011).
Logam Fe merupakan logam essensial yang keberadaannya dalam jumlah tertentu sangat dibutuhkan oleh organisme hidup, namun dalam jumlah berlebih dapat menimbulkan efek racun. Tingginya kandungan logam Fe akan berdampak terhadap kesehatan manusia diantaranya bisa menyebabkan keracunan (muntah), kerusakan usus, penuaan dini hingga kematian mendadak, radang sendi, cacat lahir, gusi berdarah, kanker, sirosis ginjal, sembelit, diabetes, diare, pusing, mudah lelah, hepatitis, hipertensi, insomnia (Parulian, 2009).
METODE PENELITIAN
Waktu dan Lokasi Penelitian
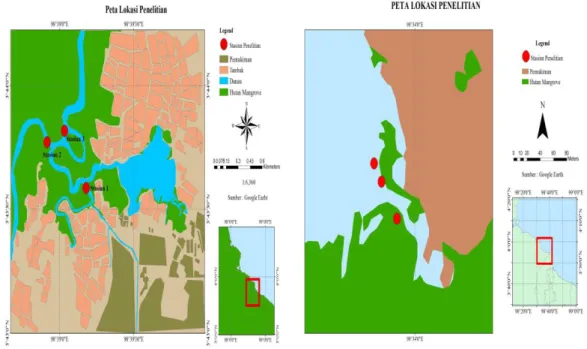
Penelitian ini dilakukan pada bulan Juni - Juli 2019 yang meliputi pengambilan sampel air, sedimen dan kepiting bakau (Scylla olivacea) di perairan Danau Siombak Kota Medan dan Perairan Desa Jaring Halus Kecamatan Secanggang. Pengambilan sampel faktor fisika dan kimia air akan dilakukan secara langsung dilapangan (in situ). Untuk analisis logam berat sampel air, substrat dan kepiting bakau (Scylla olivacea) dianalisis di Laboratorium Kesehatan Daerah Medan dengan metode Atomic Absorption Spectrophotometer (AAS). Peta lokasi penelitian dapat dilihat pada Gambar 3.
(a) (b)
Gambar 3. Lokasi Penelitian (a) Danau Siombak (b) Desa Jaring Halus
Deskripsi Area
a.) Perairan Danau Siombak
Perairan ini berada di bagian Sungai Bedera (3°43'35.13" LU dan 98°39'10.71" BT), Sungai Terjun (3°43'46.22" LU dan 98°38'54.92" BT) dan Sungai Paluh Besar (3°43'51.59" LU dan 98°39'2.06" BT) ; dikelilingi oleh tambak dan mangrove (Gambar 4).
Gambar 4. Perairan Danau Siombak b.) Perairan Desa Jaring Halus
Perairan ini berada tidak jauh dari sekitaran penduduk Desa Jaring Halus yang wilayahnya dikelilingi oleh hutan mangrove. Secara geografis terletak pada koordinat (Stasiun I) 3o73'483.4" LU dan 98o33'.98.5" BT, (Stasiun II) (Stasiun III) (Gambar 5).
Gambar 5. Perairan Desa Jaring Halus