Laporan Praktikum Hari/tanggal : Rabu / 22 April 2016
Teknologi Pati, Gula Gol : P3
dan Sukrokimia Dosen : Dr. Indah Yuliasih, M.Si
Asisten : 1. Fiona Arintika (F34120090) 2. Amanda Dwi G (F34120110)
PRODUKSI DAN KARAKTERISASI PRODUK BERBASIS
GULA
Disusun oleh: Januardi (F34130083) Nisrina Rofifah (F34130072) Andri Imam M (F34130089) Rizkya Hatami (F34130086)DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PENDAHULUAN Latar belakang
Pati dan gula merupakan sumber karbohidrat yang berfungsi sebagai sumber energi bagi tubuh. Pati dapat diperoleh dari biji-bijian, umbi-umbian, sayuran, maupun buah-buahan. Sumber alami pati antaralain adalah jagung, labu, kentang,ubi jalar, pisang, barley, gandul, beras,sagu, ubi kayu, ganyong, dan sorgum. Pati merupakan karbohidrat polimer glukosa yang t terdiri atas amilosa dan amilopektin tersimpan di dalam biji, umbi, akar dan bagian dalam dari batang tanaman yang berfungsi sebagai cadangan makanan Gula adalah suatu karbohidrat sederhana karena yang dapat larut dalam air dan langsung diserap tubuh untuk diubah menjadi energi. Sumber gula banyak berasal dari tebu, bit, aren, dan kelapa.
Pemanfaatan pati sejauh ini masih belum optimal secara ekonomis karena sifat fisik dan kimianya belum sesuai. Oleh karena itu diperlukan berbagai perlakuan untuk memodifikasi pati agar dapat digunakan secara luas baik secara fisik kimia, ataupun keduanya. Selain dilakukan modifikasi perlu diketahui sifat dan karakteristik dari pati serta standar kualitas yang baik agar dapat dihasilkan produk modifikasi yang sesuai.
Seperti halnya pati, pemanfaatan gula juga belum ekonomis. Hal ini terkait dengan proses dan teknologi yang digunakan untuk membuat gula pada saat sekarang. Oleh karena itu untuk memperbaiki proses tersebut perlu juga diketahui proses pembuatan berbagai jenis gula, baik itu gula pasir, gula aren, gula kelapa, gula invert dan jenis-jenis gula lainnya.
Berdasarkan hal tersebut maka penting untuk mengetahui karakteristik komoditas pati dan gula, maka dilakukan praktikum mengenai proses pembuatan berbagai jenis gula, seperti gula merah, gula semut, dan gula invert. Kemudian dilakukan analisa mutu produk gula yang dihasilkan sehingga dapat diketahui faktor-faktor apa saja yang menyebabkan menurun atau meningkatnya mutu gula.
Tujuan
Praktikum ini bertujuan untuk mempelajari proses pembuatan gula merak cetak dari nira tebu, mempelajari proses pembuatan gula semut dari gula kelapa dan gula aren, mempelajari proses pembuatan gula invert dengan metode asam tartarat dan metode HCl, mempelajari proses pembuatan produk hidrolisat pati, dan menganalisis sifat fisik dan kimia produk gula merah, gula semut, gula invert, dan produk hidrolisat pati.
METODOLOGI Alat dan Bahan
Alat dan bahan yang digunakan dalam praktikum ini antara lain serealia, umbi-umbian, kacang-kacangan, buah, micrometer, timbangan, gelas ukur, panci, kukusan, pisau, tebu, kapur (CaO), minyak nabati, wajan, saringan, kompor, pengaduk kayu, penggiling tebu, cetakan dari bambu, nira aren, gula aren, gula palem, gula pasir, gula kelapa, asam tartarat, HCl, Sodium bikarbonat, air, gelas piala, termometer, sendok, pemanas, pati, CaCO3, termamil 60 L, amiloglukosidase, iod, arang aktif, kertas saring, kertas pH, erlenmeyer, hot stirrer, autoclave, pipet tetes, inkubator goyang, corong bunchner, penyaring vakum, labu penyaring vakum, larutan Luff, KI 20%, H2SO4 24%, Na2S2O5 0,1 N, indikator kanji 0,5%, DNS, NaOH, potasium sodium tartarat, phenol, sodium metabisulfit, glukosa, tabung reaksi, spectrofotometer, kuvet, colorimeter, buret, refraktometer, dan pendingin balik.
Metode Karakterisasi sifat fisik serealia
1. Jumlah biji per kg 3.Dimensi biji
2. Chalkiness 4. Presentase beras kepala
Biji jagung atau beras Biji-bijian
Dihitung jumlah butirnya dalam 1 kg.
Jumlah biji
Diukur dimensinya dengan micrometer
Dimensi panjang, lebar, dan tebal.
Bulir beras Bulir beras
Dihitung presentase bobot pecah dan beras kepala Ditentukan ada atau tidaknya bintik
putih. Diitung presentasenya
Presentase beras kepala Persen chalkiness
5. Densitas kamba
Karakteristik umbi-umbian dan buah
1. Densitas kamba 2. Reaksi enzimatis
3. Pengaruh pemasakan Sampel
Gelas ukur ditimbang, sampel dimasukan sampai tera, lalu ditimbang kembali. Dihitung
selisih beratnya Densitas kamba
Buah dan umbi Satu umbi utuh
Diiris lalu dibiarkan dalam udara terbuka 15-30 menit Bobot umbi ditimbang. Wadah
ditimbang, diisi air hingga penuh dan ditimbang.
Perubahan warna Buah dimasukan dalam wadah,
ditambahkan air hingga penuh.
Densitas kamba
Umbi dan buah
Dikukus selama 15 menit. Amati perubahannya.
Pembuatan gula merah cetak Pembuatan gula semut
Pembuatan gula invert
1. metode asam tartarat 2. Metode HCl
Nira tebu Nira tebu Penyaringan Penyaringan Pemasakan nira Kristalisasi Pengayakan Pemasakan nira Pencetakan Pengeringan Gula semut
Gula merah cetak Pengemasan
Gula Gula
100 gr gula ditambah larutan HCl 42 ml
Gula, air, dan asam tartarat dicampur dan dipanaskan
hingga mendidih
Dipanaskan pada suhu 70 derajat selama 1,5 jam Suhu dipertahankan pada 100
derajat, diaduk terus selama 30 menit
Dinginkan dan diberikan 0.111 sodium bikarbinat dengan
kecepatan konstan Tambahkan 0.113 g sodium
tartarat
Gula invert Gula invert
Pembuatan hidrolisat pati
1. Maltodekstrin dengan katalis asam 3. Maltodekstrin dengan katalis enzim
2. Sirup glukosa dengan katalis asam 4. Sirup glukosa dengan katalis enzim Pati, CaCl2, HCl, larutan enzim Pati, HCl, NaOH
250 ml pati diatur keasamannya dengan HCl 1 N hingga pH 2.
Dipanaskan dan diaduk
Larutan pati ditambah CaCl2, keasaman diatur hingga 5,2 dengan HCl, ditambah enzim,
dipanaskan dan diaduk Dinetralkan dengan NaOH
hingga pH 4,2 . dituangkan pada loyang, dikeringkan dalam oven sampai kering
Dituangkan dalam loyang lalu didinginkan. Dibekukan selama 11 jam, keringkan di oven sampai
kering. Digiling dan ayak. Maltodekstrin
Maltodekstrin
Pati, HCl, larutan enzim Pati, HCl, NaOH, iod
Larutan pati diatur keasaman dengan HCl hingga 2. Dipanaskan, diuji dengan iod
Larutan pati diatur keasamannya dengan HCl hingga 6. Ditambahkan larutan enzim. Dipanaskan dan diaduk. Dinetralkan dengan NaOH.
Dituangkan dalam loyang dikeringkan dalam oven suhu
50 hingga kering.
Didinginkan pada suhu 60 derajat. Diatur pH hingga 5. Ditambahkan
enzim amiloglukosidase. Diinkubasi suhu 60 selama 48 jam. Sirup glukosa
Analisa produk gula
1. Uji warna 3. Uji kekerasan
2. Bagian yang tidak larut air 4. Gula pereduksi
Sampel Sampel
Diukur kadar kekerasannya dengan penetrometer. Diukur kadar warnanya dengan
colorimeter.
Nilai L, a, dan b Nilai kekerasan
Sampel Sampel
Sampel dilarutkan dalam air dan dimasukan dalam labu ukur Sampel dilarutkan dalam air
panas. Langsung disaring, dikeringkan.
Labu ukur dikocok dan ditera. Dikocok 12 kali. Larutan disaring. Kertas saring ditimbang,
dikeringkan pada oven. Didinginkan lalu ditimbang.
10 ml hasil saringan dimasukan erlenmeyer ditambah akuades
dan larutan luff. Gula invert
Pendingin balik dipasang. Dilakukan pemanasan selama 10 menit.
Ditambahkan KI dan H2SO4. Titrasi dengan larutan tio indikator kanji
5. Gula pereduksi 6. Kadar sukrosa
7. Kandungan total gula
Sampel Sampel
50 ml sampel dimasukan dalam labu ukur. Ditambahkan HCl, dihidrolisis 10 menit
Persen sukrosa
Ditambahkan KI dan H2SO4. Titrasi dengan larutan tio indikator kanji Didinginkan dan dinetralkan dengan
NaOH. Ditera, kocok 12 kali. 2 ml sampel dipipet, dimasukan ke
tabung reaksi. Ditambahkan 6 ml DNS
Diletakan dalam air mendidih 5 menit. Dibaca di spektrofotometer.
10 ml dimasukan ke erlenmeyer, ditambah akuades dan larutan
luff. Dipanaskan 10 menit Diukur dan dicatat nilai
absorbansinya. Blanko dibuat juga
Dibuat kurva standar. Dengan 100 ppm, 150, 200, dan 250 ppm.
Persen gula pereduksi
Sampel
2 ml sampel ditambah fenol dan dikocok.
Ditambahkan asam sulfat. Dibiarkan hingga dingin.
Diukur absorbansinya. Dan dibuat kurva standarnya.
HASIL DAN PEMBAHASAN Hasil
[Terlampir]
Pembahasan
Pati adalah karbohidrat yang merupakan polimer glukosa, dan terdiri atas amilosa dan amilopektin (Jacobs dan Delcour 1998). Pati berbentuk granul yang terdapat dalam organ tanaman. Granul tersebut dapat tersimpan di dalam biji, umbi, akar dan bagian dalam dari batang tanaman yang berfungsi sebagai cadangan makana. Pati memiliki cicri ciri berwarna putih dan memiliki ukuran 2-100 mikrometer. Pati dapat diperoleh dari biji-bijian, umbi-umbian, sayuran, maupun buah-buahan. Sumber alami pati antara lain adalah jagung, labu, kentang,ubi jalar, pisang, barley, gandul, beras, sagu, amaranth, ubi kayu, ganyong, dan sorgum (Herawati 2011).
Karakteristik pati berdasarkan sumbernya memiliki perbedaan antara satu dengan yang lanya Leach (1965) menyatkan bahwa pati serealia dan biji-bijian mempunyai sifat pengembangan granula dan pelarutan pati yang terbatas disebabkan hubungan antarmolekul yang kuat. Contohnya pati jagung tidak mengalami gelatinisasi yang sempurna ketika pemanasan seperti pada kentang dan ubi kayu, sehingga lebih ssulit untuk dicerna.Sedangkan pati dari akar atau batang mempunyai suhu gelatinisasi lebih rendah daripada patiserealia dan biji-bijian, selain itu granula patinya mengalami pengembangan serta tingkat pelarutan pati yang lebih besar.Hal ini menunjukkan pati dari akar atau batang mempunyai derajat ikatan antar molekul pati yang lebih rendah daripada pati serealia, sedangkan pati dari umbi-umbian memiliki tingkat pengembangan granula dan pelarutan yang tinggi yang menunjukkan lemahnya ikatan antar molekul pati.
Pada umbi-umbian yang dibiarkan setelah dipotong terjadi reaksi enzimatis. Reaksi enzimatis melibatkan enzim polifenol oksidase yang menyebabkan oksidasi yang membentuk melanin yang menyebabkan warna umbi menjadi coklat. Reaksi ini dapat terjadi secara enzimatik atau non enzimatik. Reaksi yang menyebabkan warna cokelat ini merupakan suatu reaksi kimia yang dikenal sebagai oksidatif enzimatik dengan oksigen sebagai katalisator dalam reaksi tersebut. Sedangkan Browning non enzimatik terjadi karena komponen karbohidrat pada umbi ini akan bertemu dengan asam amino (Dwidjoseputro 1994). Percobaaan lain yang dilakukan saat praktikum adalah merebus umbi lalu diamati perbedaanya. Umbi yang telah direbus akan memiliki rasa yang lebih manis dibandingkan umbi saat mentah. Hal ini arena umbi h memiliki rantai karbohidrat yang panjang ketika masih mentah. Ketika umbi dimasak rantai karbohidrat tersebut akan terputus oleh perlakuan panas sehingga rantainya menjadi pendek yang lebih sederhana dan rasanya menjadi manis (Husnah 2010).
Berdasarkan hasil praktikum, praktikan diminta untuk menghitung beberapa karakteristik pada komoditas serealia dan biji bijian yang mengandung karbhidrat. Pertama pada beras merah didapat hasil data bahwa panjangnya 6.03 mm, lebar 1.08 mm, bobot per 1000 biji ialah 20 gram, dan densitasnya 0.78 g/cm3. Sedang menurut Badan Standardisasi Nasional (1999) densitas dari beras merah berkisar antara 0.545 sampai 0.554 g/ cm3, bobot per 1000 biji ialah 26.02-28.2 gram, panjangnya 6.54-6.97 mm, dan memiliki lebar 2.2-2.29
mm.dari hasil data, secara uji MAPE maka antara standar mutu dengan hasil percobaan didapat eror sebesar 30.66 %. Hal ini terjadi karena bentuk beras yang bervariasi sehinga sulit untuk menyamakannya.
Selanjutnya jagung memiliki panjang 9.07 mm, lebar 6.79 mm, bobor per 1000 biji ialah 140.31, tebalnya 4.64 mm dan densitasnya 0.9162 g/cm3. Richana dkk (2012) berpendapat bahwa bobot jagung per 1000 biji ialah 19.8 - 33.74 gram, kalau panjang 7.98 – 10.15 mm, lebar 2.83 – 8.43 mm, tebal 4.36 – 10.51 mm, dan densitasnya berkisar 0.659 – 0.83. Perbedaan hanya terkadi di bobot per 1000 biji yang paling signifikan, sisanya sesuai dengan literatur. Sedang pada densitasny perbedaannya memiliki nilai MAPE 10.39 %.
Kemudian ada kacang hijau dengan data bobotnya 0.00606 gram atau 6.06 mg, kemudian bobot per seribu bijinya adalah 60.6 gram, dan warnanya hijau. Menurut Islamia(2012), Kacang hijau bobot tiap butirnya 0.5 – 0.8 mg, bobot per seribunya 36-78 gram, dan warnanya hijau atau hijau mengkilat. Dari sini uji untuk kacang hijau sudah sesuai literatur yang ada.
Kacang merah memiliki jumlah biji per kg 247 biji, panjang 15.152 mm, lebar 7.474 mm, tebal 5.848 mm, bobot per 1000 biji 570 gram , bobotnya 0.57 gram. Untuk millet memiliki panjang 0.3188 mm, tebal 0.2373 mm, bobot per 1000 biji 7.36 gram. Sedangkan ketan hitam memiliki panjang 6.2595 mm, lebar 2.505 mm, bobot per 1000 biji 2.72 gram, dan densitas kamba 0.7165 gram/cm3. Untuk perbandingan literatur, dalam hal ini penulis tidak menemukannya.
Menurut Susilawati dkk (2008), densitas dari singkong adalah 1.15 g/ml. Dari hasil praktikum singkong memliki densitas kamba 11.1166 g/cm3 dan tidak ada reaksi enzimatis yang berperan. Hal ini tidak sesuai dengan literatur terkait dengan densitas singkong. Hal ini terjadi mungkin komoditas yang diujikan antara praktikan dengan literatur bervariasi.
Kentang dari hasil praktikum memiliki data bobot sebesar 21.5 gram, volumenya 8.35 ml sehingga berdensitas 2.58 g /ml, dan bewarna kuning kecoklatan. Dari data Darazat(2011), didapat bahwa densitas kentang ialah 0.65 – 1.5 g /ml. Dari sini secara MAPE didapat faktor eror sebesar 72 %. Ketidak sesuaian dengan literatr diakibatkan karena varias dari komoditas kentang yang beragam.
Komoditas labu memiliki bobot 18.56 gram, volume 9.5 ml, densitas 1.94 g/ml, dan reaksi enzimatis berubah menjadi warna kuning tua. Kalau Ubi merah memiliki massa 146.74 gram, volume 13.2 ml, berdensitas 1.35 g/ml, dan reaksi enzimatisnya tidak ada.untuk ubi putih memiliki bobot 19.5 kg, volume 22 ml, berdensitas 0.886 g/ml, dan tidak ada reaksi enzimatis. Kalau ubi putih massanya 21.5 kg, volume 8.35 ml, densitas 2.58 g/ml, dan bereaksi enzimatis menjadi warna kunging kecoklatan. Terakhir pisang yang bobotnya 18.28 gram dengan volume 13.37 ml, berdensitas 1.37 g/ml, dan reaksi enzimatisnya sama dengan ubi putih, yaitu kuning kecoklatan. Untuk literatur perbandingan data komoditas labu, bui merah, ubi putih, dan pisang tidak ditemui oleh praktikan.
Gula adalah suatu karbohidrat sederhana karena yang dapat larut dalam air dan langsung diserap tubuh untuk diubah menjadi energi. Secara umum, gula dibedakan menjadi dua, yaitu monosakarida dan disakarida. Monosakarida adalah gula yang terbentuk dari satu molekul gula. Contoh monosakarida adalah glukosa, fruktosa, galaktosa. Sedangkan disakarida adalah gula yang terbentuk dari dua molekul gula. Contoh disakarida adalah sukrosa yaitu gabungan glukosa dan fruktosa, laktosa yaitu abungan dari glukosa dan galaktosa dan maltosa yaitu gabungan dari dua glukosa (Darwin 2013). Gula yang banyak digunakan di masyarakat adalah gula dalam bentuk sukrosa. Sukrosa dapat diperoleh dari
nira tebu, bit, atau aren. Selain itu terdapat juga sumber-sumber gula lainnya, seperti kelapa. Sumber-sumber pemanis lain, seperti umbi dahlia, anggur, madu atau jagung juga menghasilkan gula atau pemanis, namun bukan tersusun dari sukrosa.
Salah satu produk gula yaitu gula merah cetak. Gula merah adalah gula yang berwarna kekuningan atau kecoklatan. Gula ini terbuat dari cairan nira yang dikumpulkan dari pohon kelapa, aren, tebu dan lontar. Nira merupakan cairan manis yang terdapat di dalam bunga tanaman aren, kelapa, tebu danlontar yang pucuknya belum membuka dan diperoleh dengan cara penyadapan. Cairan nira yang dikumpulkan kemudian direbus secara perlahan sehingga mengental laludicetak dan didinginkan. Setelah dingin maka gula merah siap dikonsumsi atau dijual. Cairan gula ini memiliki banyak sekali varian bergantung pada jenis bahan dasar yangdigunakan. Meskipun sama – sama nira, namun bisa berasal dari pohon yang berbeda beda. Kualitas gula yang dihasilkan serta rasanya berbeda antara satu pohon dengan pohon lainnya.
Gula merah memiliki standar mutu untuk menjaga kualitas dari produksi gula merah itu sendiri. Salah satu standar mutu yang digunakan adalah SNI 01-3743-1995.
Tabel 1 SNI 01-3743-1995 Standar Mutu Gula Kelapa
Terdapat perbedaan pada kandungan kadar sukrosa bagian tebu atas dan bagian tebu bawah. Kadar sukrosa pada batang bagian atas tebu lebih sedikit daripada batang bagian bawah tebu. Hal ini berhubungan dengan proses pembentukan gula yang terjadi pada tanaman tebu. Suhu sangat berpengaruh terhadap pembentukan sukrosa. Suhu ideal bagi tanaman tebu berkisar antara 24-34 C dengan perbedaan antara siang dan malam tidak lebih dari 10 C. Pembentukan sukrosa optimal terjadi pada suhu 30 C. Sukrosa yang terbentuk ditimbun pada batang, dimulai dari bawah pada malam hari. Sedangkan Proses penyimpanan sukrosa paling efektif pada suhu 15 C. Tanaman tebu membutuhkan penyinaran penuh selama 12-14 jam, agar proses asimilasi berlangsung secara optimal (Litbang Pertanian 2013) Pada siang hari pembentukan gula lebih banyak daripada proses penyimpanan sehingga gula diubah menjadi tepung dan disimpan di dalam daun. Pada malam hari tepung tersebut diubah menjadi sukrosa dan kemudian diangkut ke batang (Indeswari 1986).
Dari hasil praktikum, pada pengolahan tebu dibedakan menurut lokasi tebu yang diolah. Ada yang bagian atas tebu yaitu kelompok 1 dan kelompok 4. Sedangkan untuk bagian bawah ada pada kelompok 3 dan kelompok 6. Kelompok 2 dan kelompok 5 pada pengolahannya bercampur bagian atas dan bawah. Dari hasil penggilingan kelompok yang mendapat tebu bawah mendapat 14 dan 13 brix. Sedangkan tebu campur mendapat 13 dan 12 brix. Berbeda halnya dengan kelombo yang memakai tebu atas mendapat nilai 12 dan 11. Jika dilihat dengan seksama, maka akan ada perubahan nilai yang cukup signifikan pada tebu bawah, atas, dan campur. Jadi kalau menurut Indrawanto dkk (2010), semakin atas bagian tebu, maka kandungan gulanya akan semakin sedikit. Kandungan gulanya terkumpul pada bagian bawah batang tebu.
Akan tetapi jika tebu semakin tua, maka seluruh baian tebu akan rata untuk rasa manisnya. Pembuatan gula merah dibedakan pada penggunaan kapur dan tidak. Bobot yang diperoleh beda beda, pad ayang tidak memakai kapur hanya 54.98 g, 88.57 g, dan 93.56 g. Beda halnya dengan yang diberi kapur yaitu 52.45 g dan 99.32 g. Warna yang didapat sama, yaitu coklat. Rendemen dari praktikum didapat berkisar 2.01 % sampai 3.75%. Perlu diperhatikan disini pada pemberian kapurnya. Menurut Haloho dan Susanto (2015), maksud pemberian kapur ini untuk menetralkan pH dari kandungan niranya. Hal ini dilakukan karena setelah panen, maka kulaitas gula pada tebu terus menurun akbat kontaknya dengan lingkungan yang mengakibatkan pHnya semakin turun. Nira disitu terfermentasi oleh mikroba di lingkngan sehingga membuat gula semakin asam. Pemberian kapur dapat menghentkan laju ini dengan kembali menetralkan pH dari nira.
Gula semut adalah gula merah yang berbentuk serbuk atau tepung yang dikenal dengan nama palm sugar. Bahan dasar untuk membuat gula semut adalah nira dari pohon kelapa, aren atau enau, nipah, lontar maupun tebu. Gula semut memiliki beberapa kelebihan dari gula merah yang terlebih dahulu dikenal masyarakat, diantaranya gula dapat disimpan dalam waktu kurang lebih dua tahun tanpa mengalami perubahan setelah dikeringkan dan dibungkus rapat, mudah larut dan bentuknya menarik, nilai ekonomi lebih tinggi, beraroma khas, dan bentuknya kering dan tidak lembek (Anonim 1998).
Bahan baku dalam pembuatan gula semut ini yaitu nira yang berasal dari tanaman kelapa, aren, nipah ataupun lontar. Menurut Muchtadi dan Sugiyono (1992), nira merupakan cairan bening dari bunga kelapa yang pucuknya belum membuka atau pohon penghasil nira lain, seperti aren, siwalan, dan lontar yang disadap. Dalam keadaan segar nira mempunyai rasa manis, berbau harum dan tidak berwarna. Air dalam nira merupakan bagian yang terbesar yaitu antara 75 – 90 %. Sukrosa merupakan bagian zat padat terbesar berkisar 12,30 – 17,40 %. Gula reduksi antara 0,50 – 1,00 % dan sisanya merupakan senyawa organik dan anorganik. Gula reduksi dapat terdiri dari heksosa, glukosa, fruktosa, dan mannose dalam jumlah yang rendah sekali. Bahan organik terdiri dari karbohidrat, protein, asam organik, asam amino, zat warna, dan lemak. Bahan anorganik terdiri dari garam mineral (Gautara dan Soesarsono W, 1981).
Prinsip pembuatan gula semut menurut Muchtadi dan Sugiyono (1992), pada dasarnya sama seperti pembuatan gula merah cetak namun pada pembuatan gula semut prinsip utama berada pada dua tahapan penting dalam proses pembuatannya yaitu pengkristalan dan pengayakan. Nira yang telah masak didinginkan dalam wajan sambil diaduk perlahan-lahan hingga terbentuk butiran-butiran kristal, saat itu pengadukan
dipercepat menggunakan pengaduk kayu. Pengayakan dilakukan saat kristal gula semut telah terbentuk dari pemasakan nira. Pengayakan dilakukan untuk memperoleh keseragaman ukuran butiran kristal gula. Pembuatan gula semut ini membutuhkan bibit kristal saat pemasakan nira sehingga terbentuk gula semut.
Pembuatan gula semut pada praktikum ini berbahan dasar gula cetak komersil. Gula cetak tersebut yaitu gula kelapa dan gula aren cetak. Gula tersebut dilarutkan di dalam air dan dimasak di wajan dengan api sedang. Pengadukan dilakukan selama pemasakan agar gula tercampur dan panas merata. Pengadukan dilakukan hingga larutan mengental. Untuk menghindari busa ketika mendidih, ditambahkan minyak nabati sebanyak satu sendok makan. Minyak ini ditambahkan untuk menurunkan tegangan permukaan antara buih dan cairan nira (Palungkun 1993). Setelah mengental, gula diuji dengan meneteskan ke dalam air untuk memastikan gula sudah dapat diangkat dari tungku api atau kompor. Setelah dirasa sudah membentuk benang saat dimasukkan ke air, gula diangkat dari api dan terus diaduk menggunakan pengaduk kayu hingga membentuk butiran-butiran kristal. Sedangkan untuk gula yang menggumpal perlu dilakukan penggerusan untuk menegecilkan ukurannya. Adapun untuk mendapat gula semut yang seragam perlu dilakukan pengayakan.
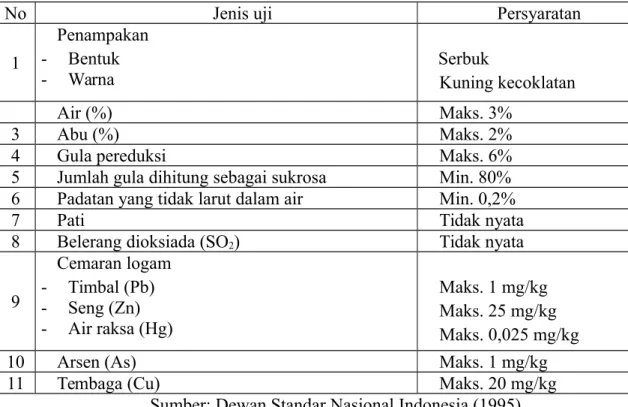
Tabel 1. Persyaratan mutu gula semut sesuai dengan SNI (SII 2043-78)
No Jenis uji Persyaratan
1 Penampakan - Bentuk - Warna Serbuk Kuning kecoklatan Air (%) Maks. 3% 3 Abu (%) Maks. 2%
4 Gula pereduksi Maks. 6%
5 Jumlah gula dihitung sebagai sukrosa Min. 80% 6 Padatan yang tidak larut dalam air Min. 0,2%
7 Pati Tidak nyata
8 Belerang dioksiada (SO2) Tidak nyata
9 Cemaran logam - Timbal (Pb) - Seng (Zn) - Air raksa (Hg) Maks. 1 mg/kg Maks. 25 mg/kg Maks. 0,025 mg/kg
10 Arsen (As) Maks. 1 mg/kg
11 Tembaga (Cu) Maks. 20 mg/kg
Sumber: Dewan Standar Nasional Indonesia (1995)
Penyebab kegagalan dalam membuat gula semut dapat disebabkan oleh beberapa faktor antara lain bahan baku yang kualitasnya buruk, proses atau kondisi proses yang tidak sesuai, dan kesalahan yang dilakukan pembuat gula semut. Bahan baku gula kelapa cetak pada umumnya menghasilkan gula semut yang tidak sesuai dengan harapan atau dengan kata lain gagal. Hal ini mungkin terjadi karena pH nira atau keasaman bahan meningkat sebelum diolah. Menurut Dinas Koperasi Perindustrian dan Perdagangan dan Dinas Pertanian Tasikmalaya (2010), nira yang baik untuk dijadikan bahan baku gula semut yaitu nira dengan pH di sekitar 7, masih segar, warna bening, dan harum. Nira yang sudah mengalami peragian
dan sudah menjadi cuka aren tidak akan bisa menjadi gula semut. Baik nira aren maupun kelapa, jika telah mengalami peningkatan asam akan sulit untuk membentuk gula semut.
Selain itu perlakuan atau kondisi proses juga menjadi faktor yang menyebabkan kegagalan. Panas yang terlalu tinggi saat pemasakan menyebabkan rasa pahit, keharuman menghilang dan berbau asap. Selain itu, lama pemasakan dan pengadukan juga berpengaruh terhadap hasil. Pengadukan yang kurang stabil saat pemasakan menyebabkan lama terbentuknya tekstur kental gula. Sedangkan waktu yang tidak tepat dalam membentuk kristal setelah gula menjadi kental dapat membuat gula semut yang diinginkan terbentuk pasta selain karena kualitas nira atau bahan yang buruk.
Pada praktikum pembuatan gula semut, kelompok 1 dan 2 mengolah gula kelapa, sedang kelompok 3, 4, dan 6 mengolah gula aren. Pada kelompok 3 dilakukan penambahan gula 100 gram sebagai feed, sama halnya dengan kelompok 6 yang menambahkan 50 gram gulu. Hasilnya adalah yang menglah gula kelapa pada pengujian warna masih terang, ditandai dengan tanda + ada satu, sedangkan pada kelompok 4 dan 6 tanda +nya ada tiga yang berarti warnanya gelap. Hal ini sesuai dengan data Pato dan Fitriani (2009) dimana gula aren biasanya warnanya jauh lebih gelap dibanding gula kelapa. Sedang pada hasil penambahan feed kelompok 2 memiliki bagian yang tidak larut air sebanyak 0.05 gram. Kelompok 6 memiliki 0.08 gram. Kelompok yang tidak diberi gula feed bagiannya larut dalam air semua. Pemberian gula ini dimaksudkan agar dapat memicu terjadinya kristalisasi yang lebih banyak sehingga didapat gula kristal yang berlebih (Razak dkk 2012). Hal ini berkaita dengan sifat ejenuhan suatu larutan yang dapat memicu proses kristalisasi dengan penambahan feed yang sama.
Gula invert merupakan produk campuran dari α-D-glukosa dan β-D-fruktosa yang diperoleh dari proses hidrolisis asam atau enzimatik dari sukrosa. Enzim yang mengkatalisis hidrolisis sukrosa disebut invertase, yaitu enzim yang memiliki efisiensi tinggi yang spesifik dalam mengubah sukrosa menjadi glukosa dan fruktosa. Adanya fruktosa bebas menyebabkan gula inversi lebih manis daripada sukrosa (Awwalurrizki dan Putra 2009). Gula invert mengandung glukosa dan fruktosa dengan jumlah sama (equimolar) yang banyak digunakan dalam industri pangan dan farmasi. Pada industri pangan gula invert digunakan sebagai pemanis, pemberi aroma dan pengawet olahan pangan, sedangkan dalam industri farmasi, gula invert digunakan sebagai pemanis pada obat bentuk sirup (Razak, Sumarni, dan Rahmat 2012). Gula invert juga digunakan untuk memperlambat kristalisasi gula pada konsentrasi larutan yang tinggi. Biasanya digunakan dalam krim non kristal, selai, madu buatan dan industri permen serta industri yang hanya memproduksi larutan gula (Safarik,
Sabatkova dan Safarikova 2009).
Terdapat tiga cara untuk membuat gula invert, yaitu menggunakan enzim invertase, hidrolisis asam kuat atau asam lemah, dan menggunakan resin penukar ion. Hidrolisis sukrosa secara enzimatik menghasilkan gula invert yang jernih dan bermutu tinggi, tetapi proses produksinya memerlukan biaya yang tinggi karena harga enzim mahal. Pada hidrolisis asam lemah bahan yang digunakan yaitu asam tartarat, sedangkan pada hidrolisis asam kuat bahan yang digunakan yaitu asam klorida (HCl). Asam klorida banyak digunakan dalam pembuatan gula invert karena memiliki daya inversi yang tinggi. Masing-masing asam memiliki kekuatan inversi yang berbeda tergantung dari kekuatan ionisasinya. Kondisi asam ini menyebabkan putusnya ikatan glikosidik yang terjadi antara glukosa dan fruktosa sehingga
dengan adanya bantuan air sukrosa terurai menjadi glukosa dan fruktosa. (Razak, Sumarni, dan Rahmat 2012). Kadar sukrosa yang terkandung dalam gula invert dengan HCl harus lebih rendah dibandingkan dengan menggunakan asam tartarat, karena asam kuat menghidrolisis sukrosa lebih cepat daripada asam lemah. Hal ini dikarenakan sifat asam yang kuat akan jauh lebih cepat memecah ikatan yang ada pada sukrosa (Hall 1973). Adanya penambahan sodium bikarbonat dalam suasana asam ini, berfungsi untuk menetralkan asam sehingga gula invert yang dihasilkan dapat dikonsumsi serta tidak bahaya dalam tubuh.
Bahan yang digunakan dalam pembuatan gula invert dengan menggunakan asam tartarat diantaranya adalah gula seperti gula pasir, asam tartarat, air, dan sodium bikarbonat. Banyaknya bahan yang digunakan tergantung volume gula invert yang diinginkan. Pertama, gula, asam tartarat, dan air dicampur sampai merata dan dipanaskan hingga mendidih. Larutan dipertahankan hingga suhu 1000 C dan diaduk selama 30 menit. Setelah itu, ditambahkan sodium bikarbonat untuk menetralkan asam dan diaduk cepat. Pembuatan gula invert dengan asam klorida hampir sama dengan pembuatan gula invert dengan asam tartarat. Perbedaannya terletak pada asam dan suhu yang digunakan. Pada pembuatan gula invert dengan asam klorida, suhu yang digunakaan adalah 700 C dan asam yang digunakan adalah asam klorida. Pada pembuatan gula invert dengan resin penukar ion bahan yang digunakan adalah zat atau bahan kimia yang memiliki daya aktif untuk mengadakan penukaran ion, salah satunya adalah arang aktif (Awwalurrizki dan Putra 2009).
Gula pasir memiliki tingkat inversi yang paling tinggi karena gula pasir merupakan gula sukrosa murni yang diperoleh dari nira tebu. Dengan banyaknya jumlah sukrosa maka akan menunjukkan tingkat inversi yang lebih tinggi. Untuk gula kelapa dan gula aren yang memiliki tingkat inversi rendah kemungkinan diakibatkan kandungan sukrosa yang tidak murni karena pada biasanya pembuatan gula kelapa dan gula aren dilakukan secara tradisional yang menyebabkan banyak zat pengotor yang ikut didalamnya. Dilihat dari tingkat inversinya gula aren memiliki tingkat inversi lebih tinggi dibandingkan dengan gula kelapa. Ini menunjukkan kadar sukrosa gula aren lebih tinggi dibandingkan dengan gula kelapa (Herman dan Yunus 1984).
Praktikum ini mengolah gula kelapa dengan gula aren memakai asam klorida atau HCL sebagai asam kuat dan asam tartrat sebagai asam lemah. Dari hasil praktikum, terdapat perubahan brix akibat pemisahan sukrosa menjadi glukosa dan fruktosa. Gula kelapa yang diberi HCL kemanisannya naik 3 brix. Gula aren dengan HCL kemanisannya bertambah 3 brix. Sedangkan gula aren yang ditambah asam tartrat bertambah 3 brix juga. Hal ini tidak sesuai dengan data Suwarno dkk (2015) dimana penggunaan asam kuat dapat menginversi gula kompleks menjadi gula sederhana dengan daya inversi yang sangat tinggi. Beda halnya emmakai asam lemah seperti asam tartrat yang daya inversinya rendah. Tetapi bukan hanya pH yang dapat mempengaruhi gula invert, tetapi suhu dan waktu pemanasan juga mempengaruhinya. Pada proses invert dengan HCL dilakukan dengan suhu 70-85 Celcius, berbeda dengan halnya asam artrat dengan suhu yang lebih tinggi berkisar 85-90 celcius. Hal ini dapat mengubah efisiensi pada bagian inversasi gula.
Pati merupakan polisakarida yang terkandung dalam tanaman dalam bentuk granula. Granula dalam tanaman banyak tersimpan di bagian akar, umbi, batang, biji, atau buah. Pati mengandung dua komponen utama, yaitu amilosa dan amilopektin dalam kadar yang berbeda. Amilosa adalah polimer rantai lurus dari glukosa dengan ikatan α-1,4 glikosidik.
Bila amilosa ditambahkan dengan sejumlah iodine, amilosa akan membentuk kompleks amilosa-iodine. Larutan amilosa memiliki viskositas yang tinggi dan relatif tidak stabil dibandingkan amilopektin (Manners, 1979). Oleh karena itu dalam pengujian sirup glukosa, ditambahkan iod agar terlihat pati sudah terhidrolisis atau belum. Jika pati sudah belum terhidrolisis, penambahan iod akan menyebabkan warna larutan berwarna biru karena iod terperangkap dalam helix pati sedangkan jika pati sudah terhidrolisis warna larutan tidak berubah.
Pati tapioka merupakan granula berwarna putih yang ukuran diameternya bervariasi antara 5 sampai 35 mikron dengan rata-rata 17 mikron. Granula inisering berbentuk mangkuk dan sangat kompak tetapi selama pengolahan, granulatersebut akan pecah menjadi komponen-komponen yang tidak teratur bentuknya(Brautlecht, 1953). Pati tapioka mengandung amilosa 17 % dan dalam pemanasantapioka akan memiliki gel yang lunak (Whistler dan Smart, 1953). Granula pati tapioca sudah terpecah sempurna di bawah suhu 80°C.
Pati sagu memiliki karakteristik yang berbeda dengan jenis pati-pati yang lain. Beberapa karakteristik penting dari pati sagu antara lain :
Karakter Bentuk atau satuan
Bentuk granula Elips
Ukuran granula 20-60 μ
Kandungan amilosa/amilopektin
27/73 % Range suhu gelatinasi 60-72 ºC Enthalpy gelatinasi 15-17 J/g
Prinsip dari pembuatan maltodekstrin dan sirup glukosa adalah pengaturan tingkat keasaman, pemanasan untuk hidrolisis dan mereduksi gula, pengadukan, dan pengeringan khusus untuk pembuatan maltodekstrin. Maltodekstrin adalah bahan yang sering digunakan dalam pembuatan makanan yang dikeringkan karena sealin bahan pengisi, maltodekstrin memiliki beberapa kelebihan antara lain tidak manis dan mudah larut dalam air. Selain itu maltodekstrin juga dapat meningkatkan vikositas, menghambat kristalisasi dan baik untuk kesehatan karena rendah kalori.
Sirup glukosa adalah suatu larutan yang diperoleh dari pati melalui hidrolisa tidak sempurna, kemudian dilakukan netralisasi dan pemekatan sampai pada tingkat tertentu. Sirup glukosa bukanlah produk yang murni tetapi merupakan campuran dari glukosa, maltosa dan dekstrin. Pada saat proses pembuatan sirup glukosa, pemilihan sumber pati harus mempertimbangkan kandungan amilosa dan amilopektinnya. Sumber pati yang mempunyai amilopektin tinggi lebih baik karena memiliki pati ISP (Insoluble Starch Particles) yang dapat dihidrolisis secara asam maupun enzimatik (Nuri 2012).
Proses pembuatan hidrolisat pati secara enzimatis dapat menghasilkan rendemen dan mutu yang lebih tinggi dibandingkan dengan hidrolisis secara asam. Pada hidrolisis secara enzimatis ikatan pati dipotong sesuai dengan jenis enzim yang digunakan, sedangkan apabila menggunakan asam pemotongan dilakukan secara acak. Pada proses pembuatan hidrolisat
pati terdapat tiga tahapan dalam mengkoversi pati yaitu tahap gelatinisasi, likuifikasi dan sakarifikasi. Tahap gelatinisasi merupakan pembentukan suspensi kental dari granula pati, tahap likuifikasi yaitu proses hidrolisis pati parsial yang ditandai dengan menurunnya viskositas dan sakarifikasi yaitu proses lebih lanjut dari hidrolisis untuk menghasilkan glukosa (Chaplin dan Buckle, 1990)
Pada tahap likuifikasi terjadi pemecahan ikatan α-1,4 glikosidik oleh enzim α-amilase pada bagian dalam rantai polisakarida secara acak sehingga dihasilkan glukosa, maltosa, maltodekstrin dan α-limit dekstrin. Enzim α-amilase merupakan enzim yang menghidrolisis secara khas melalui bagian dalam dengan memproduksi oligosakarida dari konfigurasi alfa yang memutuskan ikatan α-(1,4) glikosidik pada amilosa, amilopektin, dan glikogen. Ikatan α-(1,6) glikosidik tidak dapat diputus oleh α-amilase, tetapi dapat dibuat menjadi cabang-cabang yang lebih pendek. Setelah terjadi likuifikasi, selanjutnya bahan akan mengalami proses sakarafikasi oleh enzim amiloglukosidase. Amiloglukosidase meruapakn eksoenzim yang terutama memecah ikatan α-(1,4) dengan melepaskan unit-unit glukosa dari ujung non reduksi molekul amilosa dan amilopektin untuk memproduksi β-D-Glukosa.
Menurut Tjokroadikoesoemo (1986), hidrolisis asam sepenuhnya terjadi secara acak dan sebagian gula yang dihasilkannya berupa gula pereduksi, sehingga pengukuran gula pereduksi tersebut dapat dijadikan alat pengontrol kualitas hasil. Pada hidrolisis sempurna, dimana pati seluruhnya dikonversi menjadi dekstrosa, derajat konversi tersebut dinyatakan dengan Dextrose Equivalent (DE), dari larutan tersebut diberi indeks 100. Asam-asam mineral kuat seperti asam sulfat dan asam klorida biasa digunakan dalam proses hidrolisis pati. Sirup glukosa mempunyai nilai DE berkisar antara 30 hingga 55 (Birch dan Parker, 1979). Hidrolisis asam tidak dapat mempengaruhi distribusi gula dalam sirup glukosa. Selain itu, hidrolisis asam menghasilkan sirup dapat teretrogradasi dibawah DE 30 dan sirup yang berwarna keruh diatas DE 55.
Analisa untuk melihat mutu gula, meliputi analisa sifat fisik dan kimia. Analisa sifat fisik meliputi uji kekerasan dan warna. Sedangkan analisa sifat kimia meliputi bagian yang tak larut dalam air, kadar gula pereduksi, kadar sukrosa, dan kandungan total gula. Warna meruapakan sifat produk pangan yang dapat dipandang sebagai sifat fisik (objektif) dan sifat organoleptik (subjektif). Sabagai sifat objektif, warna merupakan manifestasi dari sifat sebagai fenomena fisik, yaitu sinar atau radiasi gelombang elektromagnetik. Parameter warna terdiri dar panjang gelombang dan intensitas cahaya. Panjang gelombang menunjukan kekuatan warna. Sedangkan intensitas cahaya menunjukkan tingkat besaran eneegi gelombang elektromagnetik yang dipancarkan. Sinar dengan intensitas tinggi akan menghasilkan cahaya yang terang, sebaliknya sinar yang intensitasnya rendah akan menghasilkan cahaya yang redup. Menurut Supardi (1993), faktor kekerasan pada gula merah diperngaruhi oleh kadar air produk, perlakuan selama penyimpanan, penambahan minyak nabati, penundaan pengolahan nira, dan penambahan pati. Semakin tinggi kadar air, maka tingkat kekerasan semakin rendah, artinya gula semakin lunak. Keadaan seperti ini mempengaruhi masa simpan gula merah menjadi tidak tahan lama dan mudah untuk ditumbuhi mikroba. Penurunan mutu selama penyimpanan disebabkan oleh pengemasan yang kurang baik sehingga masuk uap air dari lingkungan. Gula merah bersifat mudah menarik air (higrokopis) karena mengandung gula reduksi yang tinggi (± 10%) sehingga menyebabkan gula merah relatif tidak dapat bertahan lama. Kerusakan pada gula merah dapat terjadi karena
menyerap uap air dari lingkungan. Peningkatan kadar air selama penyimpanan menyebabkan gula menjadi berair dalam waktu 2-4 minggu, hal ini menurunkan mutu dan penerimaan konsumen (Sudiyanti 2004).
Bagian gula yang tidak larut dalam air menjadi salah satu faktor mutu gula, karena pada dasarnya gula murni memiliki sifat yang larut dalam air. Besarnya tingkat persentasi bagian gula yang tidak larut dalam air menunjukkan tingkat kemurnian gula. Semakin tinggi tingkat kemurnian gula maka bagian gula tidak larut dalam air kecil. Berdasarkan SNI 01-3743-1995, bagian gula yang tidak larut dalam air pada gula palma berbentuk gula cetak maksimum sebesar 2% dan berbentuk gula semut sebesar 0,2%. Menurut Faesal (1986) padatan tak larut dalam air pada gula merah terdiri dari protein, karbohidrat berpolimer tinggi dan lilin. Kandungan padatan yang tak larut pada gula merah yang melebihi standar tersebut kemungkinan disebabkan oleh kandungan protein, karbohidrat polimer tinggi, dan lilin yang berasal dari nira. Pengujian gula pereduksi menggunakan dua metode yaitu metode luff schoorl dan metode DNS. Pada metode luff schoorl, kandungan gula pereduksi diperoleh dengan menentukan jumlah kuprooksida dalam larutan sebelum direaksikan dengan gula pereduksi dan sesudah direaksikan dengan sampel gula pereduksi. Selisih keduanya sama dengan jumlah kuprooksida yang terbentuk, yang menunjukkan kandungan jumlah gula pereduksi pada sampel. DNS merupakan larutan yang menganding 3,5-dinitrosalicilic acid, potassium sodium tartarat, dan NaOH. Pengukuran DNS menggunakan spektrofotometer. Prinsip kerja spektrofotometer adalah dengan menggunakan gelombang dnegan panjang tertentu yang diatur agar menembus larutan. Semakin kecil kerapatan larutan, maka semakin mudah gelombang tersebut menembusnya, yang ditunjukkan dengan nilai absorban yang semakin kecil pula (Rohman 2007). Pengujian kadar sukrosa menggunakan metode luff schoorl diawali dengan penambahan HCl. Hal ini dimaksudkan untuk menghidrolisis kandungan sukrosa agar berubah menjadi monosakarida, yaitu glukosa dan fruktosa. Banyaknya larutan Na2S2O5 yang digunakan untuk titrasi menunjukkan besarnya kandungan glukosa dan fruktosa dalam larutan atau besarnya sukrosa yang terkonversi secara sempurna. Pengukuran kandungan total gula menggunakan metode fenol didasarkan pada prinsip abhwa gula sederhana, oligosakarida, polisakarida, dan turunannya dapat bereaksi dengan fenol dalam asam sulfat pekat menghasilkan warna oranye yang stabil (Apriyantoro dkk 1989).
PENUTUP
SimpulanKarbohidrat adalah zat gizi yang berasal dari komoditas pertanian. Zat ini dapat berguna sebagai pangan, pakan, energi, sandang, dan papan. Sumber bahan ini banyak dari biji bijin atau serealia, buah buahan, dan lainnya. Untuk standar mutu komoditas berkarbohidrat berupa serealia dan biji bijian, mememiliki jumlah biji, dimensi, warna ,chalkiness,pesentase beras kepala dan densitas kamba yang berbeda. Sedang yang umbi-umbian dan buah buahan mememiliki densitas kamba, reaksi enzimatis dan pengaruh pemasakan yang berbeda pula sesuai dengan karakteristik dan bahan yang terkandungan dalam bahan tersebut meskipun satu komoditas.
Pembuatan gula merah cetak diawali dengan proses ekstraksi gula, penyaringan, pemasakan nira sampai kental, percetakan, dan pengeringan. Mutu gula merah ditentukan oleh penampilannya, yaitu bentuk, warna dan kekerasan. Di proses pembuatannya, sumber gula yang menghasilkan gula semut yang baik dari gula aren dengan pemberian gula pasir sebagai pemicu untuk terjadinya pengkristalan.
Di proses pembuatan gula invert, paling bagus gula yang berasal dari gula pasir. Gula pasir memiliki tingkat inversi yang paling tinggi karena gula pasir merupakan gula sukrosa murni yang diperoleh dari nira tebu. Juga dapat diketahui bahwa dengan memakai asam HCL dapat memperepat proses invert.
Produk-produk gula dapat dianalisis mutunya berdasarkan paramater-paramater mutunya agar dapat mengetahui standar mutu dari produk. Uji yang dikerjakan pada analisis ini yaitu uji warna, uji kekerasan, bagian yang tidak larut dalam air, uji gula pereduksi metode Luff Schoorl, uji gula perdeuksi metode DNS, uji kadar sukrosa metode Luff Schoorl, dan uji kandungan total gula metode fenol-asam sulfat.
Saran
Dalam pelaksanaan praktikum sebaiknya praktikan lebih memperhatikan penerapan metode yang lebih sesuai dengan metode standar yang ada. Selain itu ketelitian dalam pengukuran atau pembacaan data pada suatu alat ukur akan menentukan keakuratan hasil akhir yang diperoleh pada praktikum.
Pemanfaatan komoditas gula dan pati sangat potensial dikembangkan di Indonesia. Teknologi pengolahan yang diterapkan untuk kedua sumber komoditas ini harus terus dikembangkan, baik oleh akademisi maupun pemerintah. Hal ini akan mampu meningkatkan nilai ekonomis sehingga akan berdampak pada meningkatnya devisa.
DAFTAR PUSTAKA
Anonim. 1998. Proyek Sistem Informasi Iptek Nasional Guna Menunjang Pembangunan: Gula Semut. Jakarta: Pusat Dokumentasi dan Informasi Ilmiah Lembaga Ilmu Pengetahuan Indonesia.
Anonim. 2010. Pelatihan Membuat Gula Semut dari Nira Aren di Kabupaten Tasikmalaya. Tasikmalaya (ID): Dinas Koperasi Perindustrian dan Perdagangan dan Dinas Pertanian Kabupaten Tasikmalaya.
Apriyantono A., D. Fardiaz, Ni Luh Puspitasari, Soedarnawati, Budiyanto. 1989. Analisis Pangan: Petunjuk Laboratorium. Bogor: IPB Press.
Awwalurrizki N, Putra S. 2009. Hidrolisis Sukrosa dengan Enzim Invertase untuk Produksi Etanol Menggunakan Zymonas mobilis [Skripsi]. Surabaya (ID) : Institut Teknologi Sepuluh November. Badan Standardisasi Nasional. 1995. Standar Nasional Indonesia: Gula Palma. Jakarta.
Birch GG dan KJ Parker. 1979. Sugar: Science and Technology. London: Apllied Science Publisher.
Brautlecht, C. A. 1953. Starch, Its sources Production and Uses. New York (US) : Book Division Reinhold Publishing Corporation.
Chaplin dan Buckle. 1990. Enzyme Technology. New York (US) : Cambridge University Press
Dewan Standarisasi Nasional. 1995. SNI: Gula Palma Kristal SII 2043-78. Dewan Standariasi Nasional: Jakarta.
Darwin. 2013. Menikmati Gula Tanpa Rasa Takut. Jakarta (ID): Perpustakaan Nasional Sinar Ilmu.
Dwidjoseputro D. 1994. Dasar-Dasar Mikrobiologi. Jakarta (ID): Djambatan.
Gautara dan Soesarsono Wijardi. 1981. Dasar Pengolahan Gula I. Bogor (ID): Jurusan Teknologi Industri FATETA IPB.
Hall MNA. 1973. The Small Scale Manufacture of High and Low Boiled Sweet and Toffes. London (US): Tropical Product Institute.
Herawati. 2011. Potensi Pengembangan Produk Pati Tahan Cerna Sebagai Pangan Fungsional. Jurnal Litbang Pertanian. Vol 30(1). Hal: 31-39.
Herman, A. S. Dan M. Yunus. 1984. Diversifikasi Produk Gula Merah. Bogor (ID). Balai Besar Penelitian dan Pengembangan Industri Hasil Pertanian Bogor
Huda, Thorikul. 2009. Hubungan Antara Total Suspended Solid dengan Turbidity dan Dissolved Oxygen. [http:// thorik.staff.uii.ac.id// ]. (16 April 2016).
Husnah S. 2010. Pembuatan Tepung Ubi Jalar Ungu dan Aplikasinya dalam Pembuatan Roti Tawar[Skripsi]. Bogor (ID): Fakultas Teknologi Pertanian Institut Pertanian Bogor. Indeswari NS. 1986. Penentuan Dosis Kapur dan Belerang pada Proses Pemurnian Nira
Tebu di Pabrik Gula Mini Lawang [Skripsi]. Padang(ID): Universitas Andalas.
Jacobs, H. and J.A. Delcour. 1998. Hydrothermal modifications of granular starch with retention of the granular structure. Review Agriculture Food Chemistry. 46(8): 2895−2905.
Junk, W.R. dan H.M. Pancoast. 1980. Handbook of Sugars. Avi Publishing Company. Inc. Westport, Connecticut.
Leach. 1965. Gelatinization of Starch . New York (US): Academic Press.
Litbang Pertanian. 2013. Bahan Bakar Nabati. Jakarta(ID): Departemen Pertanian SNI 01-3743-1995. Standar Mutu Gula Kelapa.
Manners, D. J. 1979. The Enzymic Degradation of Starch. London (US): Butterworths Co. Muchtadi, T.R dan Sugiyono. 1992. Ilmu Pengetahuan Bahan Pangan. Bogor (ID): PAU IPB. Nuri. 2012.Pembuatan Sirup Glukosa. [terhubung berkala]. http://pustakanuri.com/ 2012/10/kenalan-yuuukkk-sama-sirup-glukosa.html#!/2012/10/kenalan-yuuukkk-sama-sirup-glukosa.html [21 April 2016].
Palungkun, R. 1993. Aneka Produk Olahan Kelapa. Jakarta (ID): Swadaya.
Razak A, Sumarni N, Rahmat B. 2012. Optimalisasi hidrolisis sukrosa menggunakanresin penukar tipe sulfonat. Jurnal Natural Science. Vol. 1 (1) : 119-131.
Rohman. 2007. Konsep Dasar Kimia Analitik. Jakarta (ID) : UI Press
Safarik, Sabatkova Z. and Safarikova M. 2009. Invert Sugar Formation with Saccharomyces cerevisiae Cells Encapsulated in Magnetically Responsive Alginate Micro Particles.
Journal of Magnetism and Magnetic Materials. 321 : 1478–1481.
Sudiyanti, N. M., 2004. Pengaruh Jenis Konsentrasi Lemak Sebagai Bahan Edible Coating terhadap Sifat Fisik, Kimia, MikroBiologi dan Organoleptik Gula Merah Kelapa (Cocosnucifera L). Skripsi. Universitas Lampung.
Supardi D. 1993. Mempelajari Faktor- Faktor yang Mempengaruhi Kelunakan Gula Merah Kelapa Kasus di Daerah Cianjur. Bogor (ID): Fakultas Teknologi Pertanian IPB. Tjokroadikoesoemo, S. 1986. HFS dan Industri Ubi Kayu Lainnya. Jakarta (ID): PT.
Gramedia.
Whistler, R. L. dan Smart, C. L. 1953. Polysaccaride Chemistry. New York (US) : Academic Press.