INTISARI
Rosella merupakan tanaman yang banyak mengandung antosianin yang bermanfaat sebagai antioksidan. Ekstrak metanol kelopak bunga rosella dapat masuk ke dalam kulit namun kemampuan penetrasinya bervariasi, sehingga diperlukan vesikel berupa multiemulsi A/M/A dan suspensi liposom guna menjaga kemampuan penetrasi ekstrak metanol kelopak bunga rosella ke dalam kulit. Penelitian ini bertujuan untuk mengetahui sifat fisis dan stabilitas fisis sediaan multiemulsi A/M/A ekstrak metanol kelopak bunga rosella hasil optimasi formula dan mengetahui apakah sediaan multiemulsi A/M/A mampu memberikan kemampuan penetrasi ekstrak metanol kelopak bunga rosella ke dalam kulit yang lebih baik dibandingkan sediaan suspensi liposom
Penelitian ini menggunakan rancangan eksperimental murni yang bersifat eksploratif yaitu mencari formula multiemulsi A/M/A yang optimal yang ditunjukkan dengan sifat fisis dan stabilitas fisis. Kemampuan penetrasi ekstrak metanol kelopak bunga rosella dianalisis dengan melakukan uji penetrasi in vitro menggunakan metode sel difusi Franz. Jumlah ekstrak metanol kelopak bunga rosella yang terpenetrasi ke dalam kulit diukur dengan menggunakan metode spektrofotometri UV-VIS derivatif.
Hasil penelitian menunjukkan formula multiemulsi A/M/A yang optimal dan analisis statistik menunjukkan bahwa ekstrak metanol kelopak bunga rosella dalam multiemulsi A/M/A dan suspensi liposom memberikan kemampuan penetrasi yang berbeda signifikan.
ABSTRACT
Roselle (Hibiscus sabdariffa L.) is a plant that contains anthocyanins that are useful as an antioxidant. Methanol extract of roselle flower petals can penetrate into the skin but the penetration rate is not constant, so it necessary to form in multi-emulsion W/O/W dan the suspension of liposomes in order to keep penetration rate of methanol extract of roselle flower petals into the skin. The aim of this study were to get the optimal formula of multi-emulsion dan compare the penetration capability of the methanol extract of roselle flower petals multi-emulsion W/O/W dan the suspension of liposomes into the skin.
This study is an experimental design that is purely explorative study to get an optimum formula of multi-emulsion W/O/W indicated with optimal physical properties dan stability. Penetration capability of methanol extract of roselle flower petals was analyzed by conducting in vitro penetration test using Franz diffusion cell method. The amount of roselle extract which was penetrated into the skin was measured using UV-VIS spectrophotometry derivatives.
PERBANDINGAN KEMAMPUAN PENETRASI MULTIEMULSI A/M/A DAN SUSPENSI LIPOSOM YANG MENGANDUNG EKSTRAK METANOL KELOPAK BUNGA ROSELLA (Hibiscus sabdariffa L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Yolana Kwartono NIM : 118114170
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PERBANDINGAN KEMAMPUAN PENETRASI MULTIEMULSI A/M/A DAN SUSPENSI LIPOSOM YANG MENGANDUNG EKSTRAK METANOL KELOPAK BUNGA ROSELLA (Hibiscus sabdariffa L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Yolana Kwartono NIM : 118114170
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Genius is 1% talent dan 99% percent hard work
Albert Einstein
Kupersembahkan skripsi ini untuk...
Tuhan yang selalu memberkati dan memberiku kekuatan serta kesehatan,
Papa Mama dan keluargaku tercinta atas doa, dukungan, dan kasih sayang,
Teman-teman dan sahabatku terkasih,
vi
vii PRAKATA
Puji Syukur kepada Tuhan Yesus Kristus dan Bunda Maria berkat kasih karunia-Nya sehingga penulis dapat menyelesaikan penelitian serta penyusunan skripsi yang berjudul ―Perbandingan Kemampuan Penetrasi Multiemulsi A/M/A
dan Suspensi Liposom yang mengandung Ekstrak Metanol Kelopak Bunga Rosella (Hibiscus Sabdariffa L.)‖ yang disusun untuk memenuhi persyaratan memperoleh gelar Sarjana Strata Satu Program Studi Farmasi (S.Farm) dapat dikerjakan dengan baik dan lancar.
Proses pelaksanaan skripsi ini tidak akan berhasil tanpa adanya bantuan dan dukungan dari berbagai pihak, sehingga pada kesempatan ini penulis mengucapkan terima kasih kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma yang telah mengijinkan penulis menjalankan pembelajaran selama masa studi.
2. Prof. Dr. Sri Noegrohati, Apt. selaku Dosen Pembimbing Skripsi yang telah memberikan pengarahan, bantuan, tuntutan, kritik dan saran sejak awal penelitian hingga akhir penyusunan skripsi ini.
3. Dr. Erna Tri Wulandari, Apt. dan Beti Pudyastuti, M.Sc., Apt. selaku dosen penguji atas segala masukan dan bimbingannya.
4. Agustina Setiawati, M.Sc., Apt. selaku Kepala Penanggungjawab Laboratorium Fakultas Farmasi yang telah memberikan ijin dalam penggunaan fasilitas laboratorium untuk kepentingan penelitian ini.
viii
6. Pak Mus, Pak Kayat, Pak Heru, Pak Wagiran, Pak Parlan, Pak Kunto, Pak Bima, dan Pak Bimo selaku laboran Laboratorium Fakultas Farmasi yang telah membantu penulis dalam proses pelaksanaan penelitian di laboratorium. 7. Keluargaku tercinta terutama Papa dan Mama yang selalu memberi motivasi,
perhatian, dukungan dan doa demi kelancaran studi dan penyusunan naskah skripsi.
8. Partner terkasih Ko Jimmy Pieter Chua atas doa, motivasi, dukungan, nasihat, yang diberikan selama penulis menjalani studi
9. Teman seperjuangan skripsi dan sahabat : Eva Mayangsari, Me Li untuk kesabaran, kebersamaan, dan suka dukanya
10.Teman sepermainan Dara Prabandari, Monita Natalia Siregar atas keceriaan, kebersamaan, suka duka, semangat, motivasi, doa, dukungan, dan nasihat yang diberikan selama peneliti menjalani studi
11.Seluruh dosen dan teman-teman FST-B 2011, serta seluruh angkatan 2011 Fakultas Farmasi Universitas Sanata Dharma.
12.Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis dapat menyelesaikan tugas akhir ini dengan baik.
Penulis menyadari bahwa semakin banyak kekurangan dalam penelitian dan penyusunan skripsi ini mengingat keterbatasan dan kemampuan penulis, sehingga sangat diharapkan adanya masukan dan saran yang membangun untuk penulis. Semoga skripsi ini dapat bermanfaat bagi pembaca dan berguna bagi dunia ilmu pengetahuan
ix DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN SKRIPSI BERJUDUL ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PENYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... vi
PRAKATA ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xv
INTISARI ... xvi
ABSTRACT ... xvii
BAB I PENDAHULUAN ... 1
PENDAHULUAN ... 1
A. Latar Belakang ... 1
1. Perumusan masalah ... 4
2. Keaslian penelitian ... 4
3. Manfaat ... 5
B. Tujuan Penelitian ... 5
x
A. Rosella ... 7
B. Antosianin ... 9
C. Multiemulsi ... 13
D. Monografi Bahan Tambahan ... 17
E. Suspensi Liposom ... 23
F. Kulit ... 27
G. Sinar Matahari ... 30
H. Enhancer ... 32
I. Uji Penetrasi In Vitro ... 34
J. Spektrofotometri Derivatif ... 36
K. Landasan Teori ... 38
L. Hipotesis ... 40
BAB III METODOLOGI PENELITIAN ... 41
A. Jenis Penelitian ... 41
B. Variabel Penelitian ... 41
C. Definisi Operasional ... 42
D. Bahan Penelitian ... 43
E. Alat Penelitian ... 44
F. Tata Cara Penelitian ... 44
xi
BAB 4 HASIL DAN PEMBAHASAN ... 58
A. Penetapan Bobot Tetap Ekstrak Metanol Kelopak Bunga Rosella ... 59
B. Uji Penetrasi Ekstrak Metanol Kelopak Bunga Rosella ... 59
C. Optimasi Formula Multiemulsi A/M/A ... 61
D. Pembuatan Multiemulsi A/M/A ... 67
E. Evaluasi Multiemulsi A/M/A ... 69
F. Evaluasi Sediaan Suspensi Liposom ... 74
G. Kurva Baku Ekstrak Metanol Kelopak Bunga Rosella ... 76
H. Uji penetrasi ekstrak metanol kelopak bunga rosella dalam sediaan multiemulsi dan suspensi liposom ... 80
I. Statistik Uji T penetrasi ekstrak metanol kelopak bunga rosella dalam multiemulsi A/M/A dan suspensi liposom ... 91
BAB V KESIMPULAN DAN SARAN ... 93
A. Kesimpulan ... 93
B. Saran ... 93
LAMPIRAN ... 99
xii
DAFTAR TABEL
Tabel 1. Klasifikasi emulgator ... 17
Tabel 2. Variabel untuk tiap uji ... 47
Tabel 3. Formula optimum emulsi primer A/M ... 66
Tabel 4. Formula optimum multiemulsi A/M/A ... 67
Tabel 5. Perbandingan koefisien permeabilitas beberapa spesies terhadap air ... 81
Tabel 6. Uji F standar deviasi suspensi liposom dan multiemulsi A/M/A ... 92
xiii
DAFTAR GAMBAR
Gambar 1. Kelopak bunga rosella ... 8
Gambar 2. Struktur utama antosianin ... 10
Gambar 3. Perubahan struktur kimia antosianin terhadap pH ... 11
Gambar 4. Gambaran skema dan mikroskop multiemulsi A/M/A ... 13
Gambar 5. Struktur Tween 80 ... 18
Gambar 6. Struktur Span 80 ... 19
Gambar 7. Struktur setil alkohol... 20
Gambar 8. Struktur dimethicone ... 21
Gambar 9. Struktur xanthan gum ... 22
Gambar 10. Ilustrasi pembentukan liposom ... 24
Gambar 11. Klasifikasi liposom berdasarkan ukuran dan jumlah bilayer ... 25
Gambar 12. Mekanisme pelepasan obat dari liposom ... 26
Gambar 13. Struktur dan fungsi kulit ... 27
Gambar 14. Jalur umum zat aktif dalam menembus kulit ... 29
Gambar 15. Sel difusi Franz ... 34
Gambar 16. Penentuan gradien dari spektrum orde 0 ... 37
Gambar 17. Spektrogram derivatif orde 0 hingga 5 ... 38
Gambar 18. Rangkaian alat sel difusi Franz ... 47
Gambar 19. Kurva uji penetrasi ekstrak rosella ... 60
xiv
Gambar 21. Pengamatan uji kelarutan ... 71
Gambar 22. Foto partikel emulsi primer A/M dan multiemulsi A/M/A ... 72
Gambar 23. Hasil uji mekanik (sentrifugasi) ... 73
Gambar 24. Hasil uji volume creaming 28 hari setelah pembuatan ... 74
Gambar 25. Organoleptis suspensi liposom ... 75
Gambar 26. Foto partikel suspensi liposom (perbesaran 40x) ... 76
Gambar 27. Kurva baku ekstrak metanol kelopak bunga rosella dalam metanol ... 77
Gambar 28. Kurva baku ekstrak metanol kelopak bunga rosella dalam aquadest ... 79
Gambar 29. Hubungan dermal absorption orto-fenilfenol dengan waktu pada beberapa jenis kulit ... 82
Gambar 30. Kurva multiemulsi A/M/A dan suspensi liposom pada kompartemen donor ... 84
Gambar 31. Kurva sediaan multiemulsi A/M/A dan suspensi liposom pada kompartemen akseptor ... 86
xv
DAFTAR LAMPIRAN
Lampiran 1. Spektrum antosianin pada ekstrak metanol kelopak bunga
rosella (Hibiscus sabdariffa L.) ... 100
Lampiran 2. Penetapan bobot tetap ekstrak metanol kelopak bunga rosella (Hibiscus sabdariffa L.) ... 101
Lampiran 3. Data hasil optimasi emulsi primer A/M ... 102
Lampiran 4. Data hasil optimasi multiemulsi ... 103
Lampiran 5. Perhitungan mikromeritik ... 104
Lampiran 6. Data Derivated Kurva Baku Ekstrak metanol kelopak bunga rosella dalam metanol ... 106
Lampiran 7. Data Derivated Kurva Baku Ekstrak metanol kelopak bunga rosella dalam aquadest ... 107
Lampiran 8. Jumlah larutan ekstrak metanol kelopak bunga rosella Yang Terpenetrasi Ke dalam Kulit ... 108
Lampiran 9. Jumlah ekstrak metanol kelopak bunga rosella dalam multiemulsi A/M/A yang terpenetrasi ke dalam kulit ... 109
Lampiran 10. Jumlah ekstrak metanol kelopak bunga rosella dalam suspensi liposom yang terpenetrasi ke dalam kulit ... 109
Lampiran 11. Uji T untuk jumlah ekstrak metanol kelopak bunga rosella yang tertahan dalam kulit ... 110
xvi INTISARI
Rosella merupakan tanaman yang banyak mengandung antosianin yang bermanfaat sebagai antioksidan. Ekstrak metanol kelopak bunga rosella dapat masuk ke dalam kulit namun kemampuan penetrasinya bervariasi, sehingga diperlukan vesikel berupa multiemulsi A/M/A dan suspensi liposom guna menjaga kemampuan penetrasi ekstrak metanol kelopak bunga rosella ke dalam kulit. Penelitian ini bertujuan untuk mengetahui sifat fisis dan stabilitas fisis sediaan multiemulsi A/M/A ekstrak metanol kelopak bunga rosella hasil optimasi formula dan mengetahui apakah sediaan multiemulsi A/M/A mampu memberikan kemampuan penetrasi ekstrak metanol kelopak bunga rosella ke dalam kulit yang lebih baik dibandingkan sediaan suspensi liposom
Penelitian ini menggunakan rancangan eksperimental murni yang bersifat eksploratif yaitu mencari formula multiemulsi A/M/A yang optimal yang ditunjukkan dengan sifat fisis dan stabilitas fisis. Kemampuan penetrasi ekstrak metanol kelopak bunga rosella dianalisis dengan melakukan uji penetrasi in vitro menggunakan metode sel difusi Franz. Jumlah ekstrak metanol kelopak bunga rosella yang terpenetrasi ke dalam kulit diukur dengan menggunakan metode spektrofotometri UV-VIS derivatif.
Hasil penelitian menunjukkan formula multiemulsi A/M/A yang optimal dan analisis statistik menunjukkan bahwa ekstrak metanol kelopak bunga rosella dalam multiemulsi A/M/A dan suspensi liposom memberikan kemampuan penetrasi yang berbeda signifikan.
xvii ABSTRACT
Roselle (Hibiscus sabdariffa L.) is a plant that contains anthocyanins that are useful as an antioxidant. Methanol extract of roselle flower petals can penetrate into the skin but the penetration rate is not constant, so it necessary to form in multi-emulsion W/O/W dan the suspension of liposomes in order to keep penetration rate of methanol extract of roselle flower petals into the skin. The aim of this study were to get the optimal formula of multi-emulsion dan compare the penetration capability of the methanol extract of roselle flower petals multi-emulsion W/O/W dan the suspension of liposomes into the skin.
This study is an experimental design that is purely explorative study to get an optimum formula of multi-emulsion W/O/W indicated with optimal physical properties dan stability. Penetration capability of methanol extract of roselle flower petals was analyzed by conducting in vitro penetration test using Franz diffusion cell method. The amount of roselle extract which was penetrated into the skin was measured using UV-VIS spectrophotometry derivatives.
The results were obtained an optimal multi-emulsion formula W/O/W optimal dan statistical analysis showed that the penetration capability of roselle extract in multiemulsi W/O/W and the suspension of liposomes differ significantly.
1 BAB I
PENDAHULUAN
A. Latar Belakang
Indonesia merupakan negara beriklim tropis yang terletak di sepanjang garis ekuator. Sebagai negara tropis, Indonesia mendapatkan intensitas sinar matahari yang lebih besar. Penyinaran sinar matahari secara terus menerus dapat berdampak buruk bagi kulit. Sinar matahari yang masuk ke bumi dan mendapat perhatian khusus yaitu sinar ultraviolet (UV). Sinar UV yang masuk ke bumi dibagi menjadi dua yaitu sinar UV-A merupakan penyebab radiasi paling tinggi dan dapat menembus kulit sampai bagian dermis sehingga dapat merusak sel yang berada di dalamnya dan sinar UV B juga berpotensi merusak kulit namun hanya sampai lapisan luar kulit (epidermis). Adanya radiasi sinar UV ini maka akan memicu terbentuknya radikal bebas dalam tubuh terutama kulit sehingga dapat berdampak buruk bagi kulit yaitu pigmentasi kulit, kerutan (penuaan dini), kerusakan kulit, serta kanker kulit. Adanya kosmetik yang bersifat antioksidan diharapkan mampu mencegah terbentuknya Reactive Oxygen Species (ROS) di dalam kulit terutama pada lapisan epidermis dan dermis.
memiliki efek antioksidan. Senyawa fenolik yang berperan penting dalam kelopak bunga rosella yaitu antosianin yang memberikan pigmen warna merah pada kelopak bunga rosella (Rocha, Bonnlaender, Sievers, Pischel, Heinrich, 2014).
Antosianin merupakan senyawa turunan kation flavilium di mana terdapat kekurangan elektron pada inti struktur sehingga sangat reaktif dan menyebabkan antosianin mudah terdegradasi. Oksigen, cahaya, dan suhu diketahui dapat menyebabkan rusaknya antosianin serta perubahan warna pada antosinin sangat berpengaruh pada berbagai faktor seperti pH, suhu, kopigmentasi, asam askorbat, dan enzim (Hui dan Sherkat, 2005). Senyawa fenolik inilah yang berkontribusi dalam memberikan sifat antioksidan. Menurut penelitian yang dilakukan oleh Pinsuwan, Amnuaikit, Ungphaiboon, dan Itharat (2010), kelopak bunga rosella memiliki aktivitas antioksidan dengan nilai IC50
sebesar 8,45 ± 0,35 mg/ml.
dapat berpenetrasi ke dalam lapisan kulit target (epidermis dan dermis) dalam keadaan terlindungi dari pengaruh yang dapat menurunkan bioaktivitas antosianin yaitu dengan teknologi enkapsulasi.
Mengingat kepolaran ekstrak metanol kelopak bunga rosella, maka pembawa enkapsulasi yang dipilih dalam penelitian ini yaitu multiemulsi dan suspensi liposom. Multiemulsi merupakan sistem kompleks yang biasa dikenal dengan emulsi dalam emulsi, memiliki struktur yang fleksibel, mampu menjerap dan melindungi zat aktif yang bersifat hidrofilik dalam water inner phase, aplikasi dalam industri kosmetik multiemulsi mampu memberikan sensasi nyaman dengan pelepasan zat aktif yang lebih lambat. Selain itu juga akan memberikan sifat mudah tercuci dengan air
Liposom merupakan suatu vesikel berbentuk bulat dan kecil yang di dalamnya terdapat cairan yang dibungkus dengan satu atau lebih membran lipid bilayer yang umumnya terbuat dari fosfolipid alam dan kolesterol di mana mampu mengenkapsulasi dan efektif untuk penghantaran senyawa aktif baik yang bersifat hidrofilik maupun hidrofobik dan dapat digunakan sebagai vesikel non toksik untuk senyawa aktif yang larut, ukuran partikel pada liposom umumnya kecil.
daripada sediaan suspensi liposom sehingga dapat mengenkapsulasi ekstrak metanol kelopak bunga rosella dalam jumlah banyak dan memberikan kemampuan penetrasi serta tertahan dalam organ target ekstrak metanol kelopak bunga rosella di dalam kulit yang lebih baik daripada suspensi liposom.
Studi yang dilakukan pada penelitian ini meliputi penetapan bobot tetap ekstrak metanol kelopak bunga rosella, optimasi formula multiemulsi A/M/A, pembuatan multiemulsi A/M/A, serta uji perbandingan kemampuan penetrasi ekstrak metanol kelopak bunga rosella dalam sediaan multiemulsi A/M/A dan sediaan suspensi liposom.
1. Perumusan masalah
a. Bagaimana sifat dan stabilitas fisis sediaan multiemulsi A/M/A ekstrak metanol kelopak bunga rosella hasil optimasi formula?
b. Apakah sediaan multiemulsi A/M/A yang telah optimum mempunyai kemampuan sebagai pembawa ekstrak metanol kelopak bunga rosella yang lebih baik dari pada suspensi liposom dalam berpenetrasi ke dalam lapisan epidermis dan dermis?
2. Keaslian penelitian
Penelitian yang terkait dengan penelitian ini sejauh penelusuran penulis yaitu: ―Liposome-Containing Hibiscus sabdariffa Calyx Extract Formulations with Increased Antioxidant Activity, Improved Dermal Penetration dan Reduced Dermal Toxicity oleh Pinsuwan, dkk (2010). Penelitian yang akan dilakukan terdapat perbedaan yaitu pada liposom yang
dan dibandingkan dengan ekstrak metanol kelopak bunga rosella dalam
sediaan multiemulsi A/M/A.
Sejauh penelusuran pustaka oleh peneliti, penelitian mengenai perbandingan kemampuan penetrasi multiemulsi A/M/A dan suspensi liposom yang mengandung ekstrak metanol kelopak bunga belum pernah dilakukan. 3. Manfaat
a. Manfaat teoritis
Penelitian ini menambah informasi bagi dunia ilmu pengetahuan, khususnya dalam ilmu kefarmasian mengenai formulasi sediaan multiemulsi A/M/A ekstrak metanol kelopak bunga rosella dan kemampuan multiemulsi A/M/A sebagai pembawa ekstrak metanol kelopak bunga rosella yang lebih baik dari pada suspensi liposom dalam berpenetrasi ke dalam lapisan epidermis dan dermis.
b. Manfaat praktis
Penelitian ini akan menghasilkan sediaan multiemulsi A/M/A ekstrak metanol kelopak bunga rosella dan menambah variasi sediaan kosmetik antioksidan yang mengandung ekstrak metanol kelopak bunga rosella.
B. Tujuan Penelitian
1. Mengetahui sifat fisis dan stabilitas fisis sediaan multiemulsi A/M/A ekstrak metanol kelopak bunga rosella hasil optimasi formula
7
BAB II
PENELAAHAN PUSTAKA
A. Rosella 1. Klasifikasi Umum
Kerajaan : Plantae
Divisi : Magnoliophyta Kelas : Magnoliopsida Bangsa : Malvales Suku : Malvaceae Marga : Hibiscus
Jenis : Hibiscus sabdariffa L.
(Maryani dan Kristiana, 2005) 2. Morfologi
terbagi menjadi 5 ruang, dan berwarna merah. Bentuk biji menyerupai ginjal, berbulu dengan panjang 5 mm dan lebar 4 mm (Maryani dan Kristiana, 2005).
Gambar 1. Kelopak bunga rosella (Maryani dan Kristiana, 2005)
3. Kandungan kimia
4. Kegunaan
Bunga rosella dapat bermanfaat sebagai antibakteri, antifungi, antipiretik, hepatoprotektif, antikanker dan antioksidan. Beberapa penelitian baik secara in vitro maupun in vivo menemukan bahwa ekstrak metanol kelopak bunga rosella memiliki efek antioksidan yang poten (Rocha dkk., 2014). Aktivitas antioksidan yang ditimbulkan ekstrak metanol kelopak bunga rosella disebabkan oleh efek scavenging yang kuat terhadap oksigen reaktif dan radikal bebas, menghambat aktivitas xanthine oksidase, melindungi sel dari kerusakan yang disebabkan oleh lipid peroksidasi, menghambat Cu2+ dalam mediasi oksidasi LDL, dan membentuk Thiobarbituric acid reactive substances (TBARs) (Rocha dkk., 2014).
B. Antosianin
Antosianin merupakan metabolit sekunder dari keluarga flavonoid, dalam jumlah besar dapat ditemukan dalam buah-buahan dan sayur-sayuran, tidak berbahaya, dan mudah larut dalam air. Pigmen ini memiliki aneka ragam warna seperti jingga, merah muda, merah, ungu, dan biru (Pazmino, Giusti, Wrolstad, dan Gloria, 2001). Flavonoid memiliki aktivitas antioksidan dan berperan penting dalam mencegah penyakit kanker, diabetes, serta penyakit lainnya (Konczak dan Zhang, 2004).
turunan suatu struktur aromatik tunggal, yaitu sianidin, dan semuanya terbentuk dari pigmen sianidin dengan penambahan atau pengurangan gugus hidroksil, metilasi dan glikosilasi (Harbone, 1996).
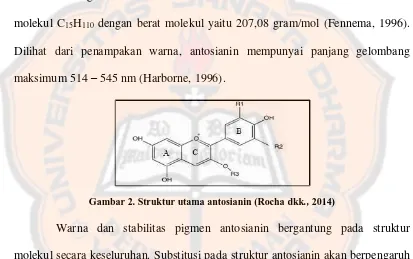
Sifat fisika dan kimia dari antosianin dilihat dari kelarutannya, antosianin larut dalam pelarut polar seperti metanol, aseton, kloroform atau dengan air yang diasamkan dengan asam klorida atau asam format. Antosianin memiliki rumus molekul C15H110 dengan berat molekul yaitu 207,08 gram/mol (Fennema, 1996). Dilihat dari penampakan warna, antosianin mempunyai panjang gelombang maksimum 514 – 545 nm (Harborne, 1996).
Gambar 2. Struktur utama antosianin (Rocha dkk., 2014)
Warna dan stabilitas pigmen antosianin bergantung pada struktur molekul secara keseluruhan. Substitusi pada struktur antosianin akan berpengaruh pada warna antosianin di mana pada kondisi asam, struktur antosianin ditentukan oleh banyaknya substitusi pada cincin B. Semakin banyak substitusi OH akan menyebabkan warna semakin biru (pelargonidin sianidin delphinidin), sedangkan metoksilasi menyebabkan warna menjadi semakin merah (sianidin peonidin pelargonidin pelargonidin – 3- glukosida) (Hui dan Sherkat, 2005).
Kestabilan antosianin dipengaruhi oleh beberapa faktor yaitu:
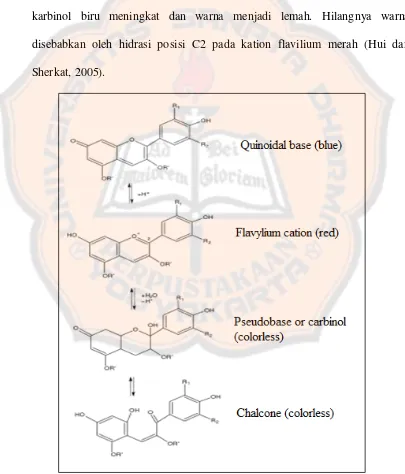
quinonoidal warna biru, kation flavilium merah(R+), basa karbinol tak berwarna, dan kalkon tak berwarna seperti ditunjukkan pada gambar 3. Kation flavilium merah, dan basa karbinol tak berwarna merupakan 2 senyawa yang sangat penting ketika terjadi perubahan pH dari pH 1-6. pH 4-6, kation flavilium merah akan mendominasi, sedangkan pada pH yang tinggi basa karbinol biru meningkat dan warna menjadi lemah. Hilangnya warna disebabkan oleh hidrasi posisi C2 pada kation flavilium merah (Hui dan Sherkat, 2005).
2. Pengaruh suhu. Degradasi pigmen antosianin dipengaruhi oleh suhu, di mana suhu dapat mengubah kesetimbangan 4 tipe antosianin menjadi kalkon tak berwarna. Perubahan yang terjadi ini bersifat irreversible. Antosianin terhidroksilasi kurang stabil pada keadaan panas daripada antosianin termetilasi terglikosilasi atau termetilasi (Hui dan Sherkat, 2005).
Quinonoid Flavilium Basa karbinol Kalkon
3. Pengaruh enzim. Adanya enzim glikosidase dan enzim polifenoloxidase dapat menyebabkan hilangnya warna dari pigmen antosianin. Enzim glikosidase akan menghidrolisis ikatan glikosida dan memproduksi gula serta aglikonnya sehingga antosianidin menjadi kurang larut air dan produksi warna menjadi berkurang. Enzim polifenoloksidase akan mengoksidasi antosianin yang mengandung oksigen dan o-difenol. Enzim polifenoloksidase akan mengoksidase o-difenol menjadi o-benzoquinon yang akan bereaksi dengan antosianin untuk membentuk antosianin teroksidasi dan produk degradasi (Hui dan Sherkat, 2005).
4. Pengaruh kopigmenasi. Kopigmen merupakan penggabungan antosianin dengan antosianin atau komponen organik lainnya di mana dapat meningkatkan stabilitas dan intensitas warna antosianin sehingga sehingga penyerapan warna pada panjang gelombang maksimum meningkat (Shi, J., Mazza, G., dan Maquer, M.L., 2002).
lebih stabil daripada antosianin yang terpapar dengan oksigen. Hal ini mengimplementasikan bahwa kemasan produk yang mengandung antosianin harus memiliki penghalang oksigen yang tinggi atau headspace kemasan diminimalisir untuk mencegah terjadinya degradasi antosianin selama penyimpanan dan pemasaran (Shi, dkk., 2002).
6. Pengaruh cahaya. Secara umum, cahaya dapat mempercepat dekomposisi pigmen antosianin. Adanya cahaya membuat antosianin tereksitasi melewati transfer elektron yang dapat mempengaruhi pigmen terdekomposisi fotokimia (Shi, dkk., 2002).
C. Multiemulsi
Multiemulsi merupakan suatu sistem dispersi cairan kompleks yang dikenal dengan istilah ‗emulsi dalam emulsi‘, di mana droplet suatu dispersi
cairan (air dalam minyak atau minyak dalam air) didispersikan ke cairan lainnya (air atau minyak) untuk menghasilkan multiemulsi A/M/A atau M/A/M (Lutz dan Aserin, 2008).
Gambar 4. Gambaran skema dan mikroskop multiemulsi A/M/A (Lutz dan Aserin, 2008)
15 – 50 µm dengan terdiri dari 50 – 100 droplet air pada setiap globul minyak dalam emulsi, sedangkan yang lainnya dapat lebih kecil berkisar antara 2 – 5 µm yang akan terdiri dari satu atau beberapa droplet air untuk setiap globul minyak dalam emulsi (Garti dan Bisperink, 1998).
Pembuatan multiemulsi dapat dilakukan secara konvensional dengan beberapa metode yaitu sonikasi, agitasi dan inversi fase (Meyers, 2006). Metode pembuatan emulsi ganda yang paling umum yaitu metode inversi fase menggunakan proses emulsifikasi 2 tahap dengan dua jenis emulgator. Emulgator hidrofobik didesain untuk menstabilkan emulsi air dalam minyak sedangkan emulgator hidrofilik untuk menstabilkan emulsi minyak dalam air (Garti dan Bisperink, 1998). Pembuatan emulsi air dalam minyak menggunakan kondisi kecepatan pengadukan yang tinggi (ultrasonifikasi dan homogenisasi) agar memperoleh droplet yang kecil, sedangkan tahap emulsifikasi kedua dibuat tanpa pengadukan yang berlebihan karena dapat merusak droplet emulsi primer (Garti, 1997).
Kegunaan utama sistem multiemulsi adalah membatasi dan melindungi sistem untuk pelepasan terkendali dari zat aktif. Namun, emulsi ganda dapat dimanfaatkan dalam berbagai bidang, diantaranya:
dan mampu menjerap reservoir untuk melindungi rasa dan aroma yang diinginkan (Lutz dan Aserin, 2008).
2. Aplikasi dalam industri kosmetik, multiemulsi A/M/A akan memberikan sensasi nyaman dengan pelepasan zat aktif yang lebih lambat. Selain itu juga akan memberikan sifat mudah tercuci dengan air (Lutz dan Aserin, 2008). 3. Sebagian besar aplikasi berhubungan dengan industri farmasetika, sediaan
multiemulsi akan memberikan keuntungan dalam meningkatkan efek kemoterapi dari obat antikanker, imobilisasi obat, pengobatan overdosis obat, dan melindungi insulin dari degradasi enzimatik (Lutz dan Aserin, 2008). 4. Aplikasi dalam industri agrikultur, emulsi ganda dapat berperan sebagai
sistem lepas lambat untuk penyubur dan pestisida (Lutz dan Aserin, 2008). 5. Aplikasi dalam kesehatan, zat aktif yang bersifat hidrofilik dapat dilarutkan
pada fase air internal dari globul emulsi, yang menunjukkan pelepasan obat diperpanjang, dan dapat mengurangi efek toksik (Kumar, Kumar, dan Mahadevan, 2012).
Kelebihan sistem multiemulsi yaitu biokompatibel, biodegradasi, dan memiliki struktur yang fleksibel, mampu menjerap dan melindungi zat aktif yang bersifat hidrofilik dan lipofilik, serta untuk pelepasan obat lepas lambat atau terkontrol. Selain kelebihan tersebut, terdapat beberapa kelemahan seperti sulit untuk diformulasikan, ukuran partikel besar dan rentan dari degradasi fisika dan kimia (Kumar, dkk., 2012).
yang tidak sama antara fase cair dalam dan luar. Tekanan osmotik pada fase air luar lebih tinggi daripada fase air dalam sehingga akan menyebabkan penyusutan cairan droplet dalam atau pecahnya lapisan minyak. Sodium klorida atau elektrolit lainnya ditambahkan pada fase air dalam maupun fase air luar pada multiemulsi tipe A/M/A yang dapat bermigrasi melewati lapisan minyak dan sampai pada fase cair lainnya melalui perpindahan melalui miselar terbalik, difusi melewati lamella emulgator tipis yang bergantung pada fluktuasi ketebalan minyak, dan perpindahan melalui emulgator terhidrasi (Benichou, Aserin dan Garti, 2004 ; Jiao dan Burgess, 2008).
Tekanan Laplace muncul disebabkan karena tegangan permukaan campuran dua cairan pada lengkungan antarmuka ketika cairan satu terdispersi sebagai droplet ke cairan lainnya. Tekanan Laplace pada proses emulsifikasi menyebabkan suatu emulsi menjadi tidak efisien secara termodinamika. Untuk membentuk droplet yang kecil, sangat melengkung, dibutuhkan energi yang lebih besar. Penambahan konsentrasi garam yang mendekati optimal pada fase dalam berada antara tekanan Laplace dan tekanan osmotik pada droplet cairan dalam sehingga mencapai stabilitas maksimum (Jiao dan Burgess, 2008).
emulgator lipofilik; dan 2) difusi sederhana karena adanya perbedaan osmotik pada kedua fase air (Kumar, dkk., 2012).
D. Monografi Bahan Tambahan 1. Emulgator
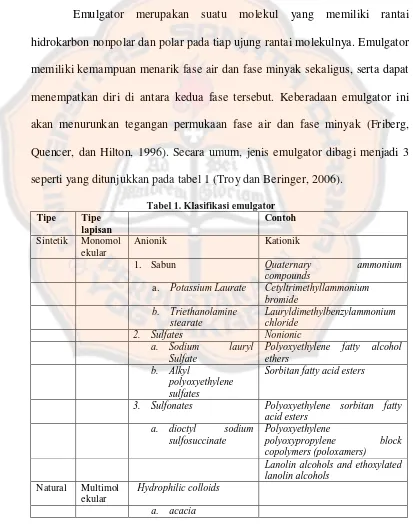
Emulgator merupakan suatu molekul yang memiliki rantai hidrokarbon nonpolar dan polar pada tiap ujung rantai molekulnya. Emulgator memiliki kemampuan menarik fase air dan fase minyak sekaligus, serta dapat menempatkan diri di antara kedua fase tersebut. Keberadaan emulgator ini akan menurunkan tegangan permukaan fase air dan fase minyak (Friberg, Quencer, dan Hilton, 1996). Secara umum, jenis emulgator dibagi menjadi 3 seperti yang ditunjukkan pada tabel 1 (Troy dan Beringer, 2006).
Tabel 1. Klasifikasi emulgator
1. Sabun Quaternary ammonium
compounds
3. Sulfonates Polyoxyethylene sorbitan fatty
acid esters
Lanolin alcohols and ethoxylated lanolin alcohols
Natural Multimol ekular
Hydrophilic colloids
b. gelatin
Surfaktan merupakan senyawa yang mampu menurunkan tegangan permukaan. Senyawa ini memiliki struktur rantai panjang serta memiliki gugus lipofil maupun hidrofil dalam molekulnya. Emulgator dalam fase air akan berorientasi sehingga bagian hidrofiliknya akan masuk ke cairan. Adsorpsi molekul emulgator pada permukan cairan menyebabkan terjadinya penurunan tegangan permukaan. Pada penambahan emulgator, tegangan permukaan mula – mula akan turun sangat cepat mencapai harga tertentu yang selanjutnya tidak akan berkurang meskipun dilakukan penambahan emulgator. Harga tertentu ini dikenal dengan CMC (critical micelle concentration) (Voight, 1995).
a. Polioksietilen sorbitan monooleat (Tween 80)
Tween 80 (gambar 5) berbentuk cairan kental berwarna kuning terang sampai kuning sawo. Tween 80 bersifat non toksik. Tween 80 mudah larut dalam air, etanol, minyak tumbuhan, etil asetat, metanol, tetapi tidak larut dalam minyak mineral. Tween 80 memiliki nilai HLB 15. Konsentrasi yang digunakan yaitu 1% - 15% apabila digunakan sebagai emulgator tunggal. Apabila dikombinasikan dengan surfaktan lipofilik, konsentrasi yang diperbolehkan yaitu 1% - 10% (Rowe, Sheskey, dan Quinn, 2009). Penggunaan Tween 80 dalam farmasi yakni sebagai emulsifying agent, wetting agent, penetrating agent, dan diffusian (Som, Bhatia, dan Yasir, 2012).
b. Sorbitan monooleat (Span 80)
Gambar 6. Struktur Span 80
jumlah yang sesuai untuk menghasilkan emulsi air dalam minyak atau minyak dalam air atau krim. Konsentrasi yang digunakan yaitu 1% - 15% apabila digunakan sebagai emulgator tunggal. Apabila dikombinasikan dengan surfaktan hidrofilik, konsentrasi yang diperbolehkan yaitu 1% - 10% (Rowe dkk., 2009).
2. Parafin cair
Parafin dalam sediaan topikal digunakan untuk meningkatkan titik leleh atau meningkatkan pengerasan (bahan pengeras). Parafin tidak menyebabkan toksik ataupun iritasi. Parafin cair berbentuk cairan kental dan tidak berwarna. Konsentrasi yang digunakan dalam sediaan topikal yaitu 1,0% – 32,0% (Rowe dkk., 2009). Parafin cair dapat berfungsi sebagai emolien
untuk mencegah dehidrasi pada saat sediaan diaplikasikan ke kulit (Tranggono, 2007).
3. Setil alkohol
Gambar 7. Struktur setil alkohol
sebagai emolien karena dapat mengabsorbsi air yang ada pada lingkungan sehingga kulit akan terjaga kelembabannya. Setil alkohol sebagai stiffening agent karena dapat menambah viskositas dan konsistensi sediaan emulsi. Setil alkohol digunakan sebagai pembantu emulgator tipe A/M karena dapat mengikat fase air dan minyak dalam sistem emulsi sehingga dapat mengurangi jumlah penambahan emulgator lain dalam sediaan. Setil alkohol dapat digunakan sebagai stiffening agent dengan konsentrasi 2% - 10% (Rowe dkk., 2009).
4. Dimethicone
Gambar 8. Struktur dimethicone
5. Xanthan gum
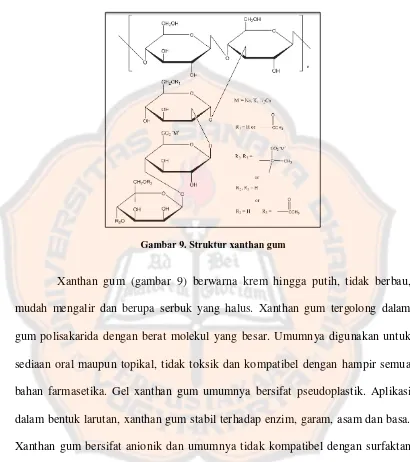
Gambar 9. Struktur xanthan gum
Xanthan gum (gambar 9) berwarna krem hingga putih, tidak berbau, mudah mengalir dan berupa serbuk yang halus. Xanthan gum tergolong dalam gum polisakarida dengan berat molekul yang besar. Umumnya digunakan untuk sediaan oral maupun topikal, tidak toksik dan kompatibel dengan hampir semua bahan farmasetika. Gel xanthan gum umumnya bersifat pseudoplastik. Aplikasi dalam bentuk larutan, xanthan gum stabil terhadap enzim, garam, asam dan basa. Xanthan gum bersifat anionik dan umumnya tidak kompatibel dengan surfaktan kationik, polimer atau pengawet karena memungkinkan terjadi pengendapan. Konsentrasi surfaktan anionik dan amfoterik diatas 15% b/v dapat menyebabkan pengendapan pula pada larutan xanthan gum (Rowe dkk., 2009).
pelepasan tidak terkendali dari bahan yang terjerap. Stabilisasi emulsi ganda ini dapat dicapai karena adanya stabilisasi deplesi. Stabilisasi deplesi diperoleh dari partikel koloidal yang diberikan oleh makromelekul yang terbebas di larutan (Lutz dan Aserin, 2008).
E. Suspensi Liposom
Liposom merupakan suatu vesikel berbentuk bulat dan kecil yang di dalamnya terdapat cairan yang dibungkus dengan satu atau lebih membran lipid bilayer yang umumnya terbuat dari fosfolipid alam dan kolesterol (Jesorka dan Orwar, 2008). Liposom mampu mengenkapsulasi dan efektif untuk penghantaran senyawa aktif baik yang bersifat hidrofilik maupun hidrofobik dan dapat digunakan sebagai vesikel non toksik untuk senyawa aktif yang larut. Liposom dapat membawa obat dalam satu atau tiga kompartemen yaitu: 1) senyawa aktif yang larut air berada pada central aqueous core; 2) senyawa aktif larut minyak berada pada lapisan membran; 3) peptida dan protein berukuran kecil berada pada permukaan air lemak (Bhai, Yadav, Mamatha, dan Prasanth, 2012).
permeabilitas molekul yang larut air untuk melewati membran (Laouini, Maalej, Blouza, Sfar, Charcosset, dan Fessi, 2012).
Pemilihan komponen bilayer dilihat dari rigiditas atau fluiditas dan charge bilayer. Fosfatidilkolin unsaturated yang berasal dari telur atau fosfatidilkolin kedelai memberikan bilayer yang lebih permeable dan elastis sehingga dapat berperan sebagai penetration enhancer, dan memfasilitasi penetrasi molekul obat melalui stratum korneum sedangkan fosfolipid saturated dengan rantai asil yang panjang seperti dipalmiitoylphos phatidylcholine membentuk struktur bilayer yang rigid namun impermeable (Akbarzadeh, Sadabady, Davaran, Joo, Zarghami, Hanifehpour, dkk., 2013).
Liposom terbentuk ketika lipid yang terdiri dari kelompok kepala hidrofilik dan ekor hidrofobik di dispersikan ke dalam air, membentuk lapisan tipis lipid bimolekular. Selama agitasi, lapisan lipid bimolekular tipis terhidrasi ini akan terpisah dan masing-masing akan bergabung membentuk vesikel yang mencegah interaksi antara hidrokarbon lapisan lipid dengan air sekitarnya, ditunjukkan pada gambar 10 (Jesorka dan Orwar, 2008).
Ukuran vesikel merupakan parameter terpenting dalam mendeterminasi liposom serta ukuran dan jumlah bilayer mempengaruhi jumlah obat yang terenkapsulasi dalam liposom. Berdasarkan ukuran dan jumlah bilayer, liposom dapat diklasifikasikan menjadi lima yaitu:
1. Small Unilamellar Vesicles (SUV). Liposom berukuran 20 – 100 nm dan terdiri dari 1 lapis bilayer
2. Large Unilamellar Vesicles (LUV). Liposom berukuran >100 nm dan terdiri dari 1 lapis bilayer
3. Giant Unilamellar Vesicles (GUV). Liposom berukuran >1000 nm dan terdiri dari 1 lapis bilayer
4. Oligolamellar Vesicles (OLV). Liposom berukuran 100 – 500 nm dan terdiri dari >1 lapis bilayer
5. Multilamellar Vesicles (MLV). Liposom berukuran >500 nm dan terdiri dari >1 lapis bilayer
(Laouini, dkk., 2012).
Gambar 11. Klasifikasi liposom berdasarkan ukuran dan jumlah bilayer (Laouini,
Liposom dimanfaatkan sebagai pembawa obat dengan alasan vesikel ini dapat memberikan keuntungan seperti: liposom dapat mengarahkan obat pada target tertentu misalnya pada long circulating liposomes yang bekerja pada target selektif area patologis tertentu; liposom dapat berfungsi sebagai reservoir obat yang melepaskan obat secara perlahan sehingga akan meningkatkan efektivitas obat dan memperpanjang masa edar obat di dalam darah; liposom dapat melindungi obat yang tidak stabil (antimikrobia, antioksidan, dan senyawa bioaktif); liposom dapat melindungi obat dari degradasi sebelum mencapai target dan melindungi pasien dari efek samping yang berbahaya (Akbarzadeh, dkk., 2013).
Mekanisme pelepasan obat melalui liposom dengan cara pertama melakukan fusi dengan membran sel plasma dengan menyisipkan lipid bilayer liposom ke membran plasma, kedua menstimulasi pelepasan obat yang terkdanung dalam liposom ke ruang interstisial untuk selanjutnya substansi secara aktif diambil oleh sel melalui transport paraseluler ditunjukkan pada gambar 12 (Akbarzadeh, dkk., 2013).
F. Kulit
Kulit merupakan organ tubuh paling besar yang melapisi seluruh tubuh. Luas kulit pada manusia rata – rata sekitar 2 m2 dengan berat 10 kg jika ditimbang dengan lemaknya atau 4 kg jika tanpa lemak, atau beratnya 16% dari berat badan seseorang (Kusantati, Prihatin, dan Wiana, 2008). Struktur dan fungsi dari kulit manusia terdiri dari empat bagian utama yaitu stratum korneum, viable epidermis, dermis, dan jaringan subkutan yang ditunjukkan pada gambar 13.
Gambar 13. Struktur dan fungsi kulit (Walters, 2002)
Struktur kulit meliputi bagian – bagian di bawah ini:
– rata ketebalan stratum korneum yaitu 10 – 20 µm dengan struktur terdiri dari
brick dan mortar yang merupakan barrier pengontrol kecepatan dalam absorbsi transdermal (Walters, 2002).
2. Epidermis merupakan bagian dari kulit yang berlapis-lapis dengan ketebalan 0,06 mm pada kelopak mata dan 0,08 mm pada telapak tangan dan telapak kaki. Epidermis tidak terdapat pembuluh darah (Benson, 2012).
3. Dermis mempunyai ketebalan yang bervariasi tergantung lokasi kulit. Dermis memiliki dua lapisan yaitu papillary layer yang berisi susunan tipis daris erat kolagen dan reticular layer yang tersusun dari seraat kolagen tebal dan tersusun sejajar dengan permukaan kulit (Brannon, 2007). Dermis mengandung banyak pembuluh darah yang memiliki peran penting dalam pengaturan suhu tubuh dan tekanan darah. Jaringan kapiler yang luas dalam stratum papiler berfungsi untuk mengatur suhu tubuh dan memberi makan epidermis di atasnya yang tidak memiliki pembuluh darah sendiri (Junquera dan Kelley, 1997).
4. Jaringan subkutan merupakan lapisan lemak dan jaringan ikat yang di dalamnya terdapat pembuluh darah dan syaraf. Lapisan ini berperan untuk pengaturan suhu kulit maupun suhu tubuh (Brannon, 2007).
Gambar 14. Jalur umum zat aktif dalam menembus kulit (Lane, 2013)
1. Jalur transepidermal. Jalur ini merupakan jalur difusi melalui stratum korneum yang terjadi melalui 2 jalur yaitu jalur transselular yang berarti jalur melalui protein di dalam sel dan melewati daerah yang kaya akan lipid, dan jalur interseluler yang berarti jalur melalui ruang antar sel. Penetrasi pada jalur transepidermal berlangsung melalui dua tahap yakni pertama, pelepasan obat dari pembawa ke stratum korneum tergantung koefisien partisi obat dalam pembawa dan stratum korneum. Kedua, difusi melalui epidermis dan dermis dibantu oleh aliran pembuluh darah dalam lapisan dermis (Benson, 2012). 2. Jalur transappendageal. Jalur ini merupakan jalur masuknya obat melalui
folikel rambut dan kelenjar keringat yang disebabkan karena adanya pori-pori di antaranya, sehingga memungkinkan obat berpenetrasi. Penetrasi obat melalui jalur transepidermal lebih baik daripada jalur transappendageal, karena luas permukaan pada jalur transappendageal lebih kecil (Benson, 2012).
Faktor – faktor yang mempengaruhi absorbsi perkutan yaitu:
2. Luas permukaan tempat absorbsi. Apabila luas permukaan tempat absorbsi semakin besar, maka jumlah obat yang diabsorbsi per unit luas permukaan akan semakin besar.
3. Karakteristik pembawa. Pembawa yang mudah menyebar pada permukaan kulit akan meningkatkan absorbsi. Pembawa yang dapat meningkatkan kelembaban kulit akan meningkatkan absorbsi.
4. Hidrasi kulit. Hidrasi stratum korneum akan meningkatkan penetrasi obat ke dalam kulit.
5. Afinitas obat terhadap kulit obat harus mempunyai afinitas terhadap kulit yang lebih besar daripada terhadap pembawa
6. Koefisien partisi obat. Koefisien partisi obat mempengaruhi kelarutan obat dalam minyak dan air.
7. Cara aplikasi obat pada kulit. Pengolesan dan penggosokkan obat pada kulit akan meningkatkan penetrasi obat ke dalam kulit.
8. Tempat aplikasi obat. Tempat aplikasi obat berpengaruh terhadap kemampuan penetrasi obat. Aplikasi pada bagian kulit yang telah tipis akan meningkatkan penetrasi obat daripada aplikasi pada bagian kulit yang lebih tebal.
9. Waktu kontak obat dengan kulit. Semakin lama waktu kontak obat dengan kulit maka akan meningkatkan penetrasi obat ke dalam kulit.
(Ansel, 2005)
G. Sinar Matahari
atmosfer hingga kemudian sampai ke permukaan bumi. Jumlah dari total radiasi matahari yang sampai ke bumi disebut insolasi (Kiil dan Houmoller, 2013). Spektrum elektromagnetik yang dipancarkan oleh matahari terdiri dari sinar tampak dan radiasi sinat tampak dekat seperti sinar X, ultraviolet, inframerah dan gelombang radio (Solarradiation, 2013). Sinar matahari ketika sampai di atmosfer akan dipantulkan oleh lapisan ozon, sedangkan sisanya diserap dan diubah menjadi panas (Kiil dan Houmoller, 2013).
Radiasi sinar ultraviolet merupakan penyebab berbagai kerusakan kulit, termasuk kanker. Radiasi yang dipancarkan sinar matahari terdiri dari beberapa jenis. Salah satunya yaitu sinar ultraviolet (UV) yang terdiri dari beberapa jenis dengan panjang gelombang yang berbeda (Anna, 2015). Sinar ultraviolet (UV) merupakan bagian dari spektrum elektromagnetik yang mempunyai panjang gelombang antara 40 sampai 400 nm. Spektrum UV dibagi menjadi UV vakum (40-190 mn), UV jauh (190-220 nm), UV C (220-290 nm), UV B (290-320 nm), dan UV A (329-400 nm) (National Aeronautics dan Space Administration, 2007).
menyebabkan kerusakan fotokimia pada DNA sel sehingga memicu timbulnya kanker kulit (Mutia, 2015).
H. Enhancer
Enhancer kimia merupakan senyawa yang dapat meningkatkan penetrasi perkutan obat dengan berpartisi pada stratum korneum dan mengubah susunan lipid-protein yang ada di kulit. Perubahan ini menyebabkan perubahan sifat dan penurunan pertahanan pada stratum korneum. Enhancer kimia dapat meningkatkan permeabilitas stratum korneum melalui beberapa mekanisme yaitu : (1) meningkatkan fluiditas lipid di kulit; (2) melalui hidrasi jalur polar; (3) melalui aksi keratolitik; (4) meningkatkan kelarutan obat; dan (5) meningkatkan partisi stratum korneum (Kumar dan Philip, 2007).
memperlambat penetrasi. Asam lemak yang banyak digunakan sebagai senyawa peningkat penetrasi yaitu asam oleat (Pathan dan Setty, 2009).
2. Minyak esensial dan terpen. Senyawa ini bekerja dengan memodifikasi sifat alami pelarut stratum korneum serta senyawa ini dapat menurunkan waku lag penetrasi (Pathan dan Setty, 2009).
3. Urea. Urea bekerja dengan menghidrasi stratum korneum dan dengan membentuk kanal difusi hidrofilik. Urea siklik memiliki gugus polar dan non polar sehingga mekanisme peningkat penetrasi disebabkan oleh aktivitas hidrofilik dan oragnisasi lipid di stratum korneum(Pathan dan Setty, 2009). 4. Azon. Azon merupakan enhancer kimia pertama yang didesain sebagai
senyawa peningkat penetrasi. Azon bekerja dengan cara mempengaruhi lipid sfingosin dan seramida yang secara alami ditemukan dilapisan kulit bagian atas (Pathan dan Setty, 2007).
I. Uji Penetrasi In Vitro
Uji penetrasi in vitro dilakukan guna mengukur kecepatan dan jumlah senyawa yang melewati kulit, yang mana hal tersebut tergantung pada obat, bentuk sediaan, eksipien, bahan peningkat penetrasi dan variabel formulasi lainnya. (Witt dan Bucks, 2003). Kelebihan utama uji penetrasi in vitro yaitu kondisi penelitian yang dilakukan dapat dikontrol secara presisi seperti variabel kulit dan material yang digunakan. Namun hal ini dapat menimbulkan kerugian seperti informasi terkait metabolism, distribusi, dan efek aliran darah terhadap permeasi tidak dapat diketahui (Walters, 2002).
Salah satu metode in vitro untuk mengukur jumlah obat yang terpenetrasi ke kulit yaitu dengan menggunakan sel difusi Franz. Sel difusi Franz merupakan sel difusi tipe vertikal untuk mengetahui penetrasi suatu senyawa ke dalam kulit secara in vitro. Sel difusi Franz terdiri dari dua kompartemen yaitu kompartemen donor dan kompartemen akseptor yang dipisahkan oleh membran seperti ditunjukkan pada gambar 15 (Walters, 2002).
Membran yang dapat digunakan uji penetrasi in vitro yaitu kulit tikus, babi, marmot, kelinci, ular, manusia, atau membran kulit sintetik. Kulit manusia merupakan pilihan utama untuk uji penetrasi in vitro namun sulit untuk didapatkan sehingga banyak digunakan kulit tikus sebagai penggantinya (Nair dan Panchagula, 2004). Bagian kulit manusia yang sering digunakan yaitu kulit abdominal atau breast sedangkan kulit hewan yang biasanya digunakan yaitu bagian flank dan back (rat) dan flank dan ear (babi) (Bartosova dan Bajgar, 2012). Uji penetrasi in vitro menggunakan kulit tikus dapat memberikan informasi yang berguna untuk memanipulasi desain pemberian obat secara transdermal, sehingga dapat dicapai permeasi obat yang menembus kulit (Al-saidan, Krishnaih, Chdanrasekhar, Lalla, Rama, Jayaram, dkk., 2004).
Cara melakukan uji penetrasi dengan sel difusi Franz yaitu sejumlah tertentu zat diaplikasikan pada membran dan dibiarkan berpenetrasi secara difusi pasif melalui membran. Mengetahui jumlah zat yang terpenetrasi maka dilakukan sampling pada cairan kompartemen akseptor selama waktu tertentu hingga mencapai kondisi tunak. Cairan dari kompartemen akseptor yang diambil harus digantikan dengan cairan awal sejumlah volume yang di ambil. Hal ini bertujuan untuk menjaga volume dalam cairan akseptor tetap konstan dan untuk menjaga supaya cairan di kompartemen akseptor tetap dalam keadaan tunak (Witt dan Bucks, 2003).
Faktor yang perlu diperhatikan dalam uji penetrasi secara in vitro yaitu: 1. Pemilihan membran. Penggunaan kulit manusia sebagai membran uji
kesulitan mengontrol jenis kelamin, ras, umur, dan kondisi kulit, sehingga untuk uji penetrasi secara in vitro bisa digunakan kulit hewan sebagai penggantinya seperti kulit tikus, babi, marmot, kelini, dan ular (Wiechers, 1989).
2. Larutan donor. Senyawa yang dilarutkan atau yang terkdanung dalam pembawa akan berdifusi dari pembawa menuju ke permukaan kulit sebelum obat diabsorpsi. Pembawa dapat mempengaruhi pelepasan senyawa dan berinteraksi dengan stratum korneum. Faktor yang mempengaruhi pelepasan obat yaitu sifat fisikokimia zat aktif dan pembawa seperti kelarutan, ukuran molekul, viskositas dan polaritas (Wiechers, 1989).
3. Larutan akseptor. Larutan yang digunakan sebaiknya tidak hanya berperan sebagai penerima obat yang mengalami penetrasi di dalamnya tetapi juga yang menyediakan air, bahan-bahan biokimia dan ion-ion yang diperlukan membran kulit dalam mempertahankan fungsinya (Skelly, 1987). Larutan yang dapat digunakan sebagai larutan akseptor seperti larutan fisiologis salin, larutan ringer, atau larutan fisiologis lainnya yang relevan. Faktor lain yang perlu diperhatikan yaitu suhu, kelarutan senyawa dalam medium dan pengadukan (Friend, 1992).
J. Spektrofotometri Derivatif
teknik analisis yang menggunakan sistem turunan orde 1 hingga 5 dari spektrum spektrofotometri UV-VIS. Kurva spektrum derivatif menggambarkan nilai turunan absorbansi suatu senyawa terhadap panjang gelombang seperti yang ditunjukkan pada persamaan berikut:
n
Dx,λ = f………(1)
Nilai n menunjukkan orde derivatif dan nDx,λ merupakan nilai derivatif pada orde ke-n dari suatu spektrum absorbansi substansi X terhadap panjang gelombang (Marczenko dan Balcerzak, 2000).
Proses yang terjadi dalam derivatisasi data spektra adalah pendiferensialan kurva secara matematis yang tak lain adalah menentukan kemiringan/gradien serapan antara panjang gelombang tertentu secara menyeluruh seperti tampak dalam gambar 16.
Gambar 16. Penentuan gradien dari spektrum orde 0(Nurhidayati, 2007)
Penentuan besar gradien secara individual adalah plot dA/dλ terhadap λ
bila diplotkan terhadap panjang gelombang menghasilkan plot derivatif kedua. Pengulangan proses ini menghasilkan orde yang lebih tinggi, plot derivatif ke-n, atau dnA/ dnλterhadap λ. Sebagai ilustrasi proses pengulangan, dari derivat kenol sampai dengan kelima ditunjukkan pada gambar 17 (Nurhidayati, 2007).
Gambar 17. Spektrogram derivatif orde 0 hingga 5 (Kus, Marczenko dan Obarski, 1996)
Metode spektrofotometri derivatif memberikan sensitivitas dan selektivitas yang tinggi dibdaningkan metode spektrofotometri normal (orde 0). Hasil selektivitas yang lebih tinggi didapatkan dengan mengurangi atau mengeleminasi noise tanpa mengurangi sinyal penting, serta mengurangi kesalahan yang disebabkan oleh spektrum senyawa lain dalam sampel yang tumbang tindih (Marczenko dan Balcerzak, 2000).
K. Landasan Teori
sinar UV A merupakan penyebab radiasi paling tinggi dan dapat menembus kulit hingga bagian dermis sedangkan radiasi UV B juga berpotensi merusak kulit namun hanya sampai lapisan luar (epidermis). Efek dari radiasi sinar UV A dan UV B ini dapat menyebabkan pigmentasi kulit, kerusakan kulit, penuaan dini, serta memicu timbulnya kanker kulit. Adanya kosmetik yang bersifat antioksidan diharapkan dapat mencegah timbulnya ROS di dalam kulit terutama pada lapisan epidermis dan dermis (Mutia, 2015).
Hibiscus sabdariffa L. atau yang biasa dikenal dengan rosella telah diketahui memiliki aktivitas antioksidan karena adanya kandungan fenolik di dalam bunga rosella. Salah satu kandungan fenolik yang ada di rosella yaitu antosianin. Antosianin merupakan metabolit sekunder dari famili flavonoid (Konczak dan Zhang, 2004).
Berdasarkan struktur serta sifatnya, stabilitas antosianin sangat dipengaruhi oleh lingkungan seperti cahaya, suhu, dan oksigen. Studi kondisi penyimpanan multiemulsi yang dilakukan oleh Li (2015) menunjukkan kondisi optimum penyimpanan multiemulsi yaitu pada suhu -4 , tertutup rapat, terlindung dari cahaya dan adanya pemberian gas nitrogen. Penggunan ekstrak metanol kelopak bunga rosella secara topikal dapat menyebabkan iritasi pada kulit (Pinsuwan dkk, 2010). Selain itu hasil penelitian pendahuluan yang dilakukan peneliti menunjukkan kemampuan penetrasi yang dihasilkan bervariasi.
kemampuan penetrasi ekstrak metanol kelopak bunga rosella supaya dapat tertahan di lapisan epidermis dan dermis sehingga tidak masuk ke sistemik. Vesikel yang digunakan yaitu multiemulsi dan suspensi liposom. Multiemulsi memiliki kemampuan penetrasi ekstrak metanol kelopak bunga rosella ke dalam kulit yang lebih baik daripada suspensi liposom dikarenakan ukuran partikel pada multiemulsi lebih besar daripada suspensi liposom menyebabkan multiemulsi lebih tertahan di dalam kulit (lapisan epidermis dan dermis). Ukuran partikel suspensi liposom yang lebih kecil memungkinkan suspensi liposom lebih mudah untuk menembus lapisan-lapisan pada kulit sehingga dapat masuk ke sistemik.
Jumlah ekstrak metanol kelopak bunga rosella yang terpenetrasi ke dalam kulit dapat diketahui dengan melakukan uji penetrasi secara in vitro menggunakan sel difusi Franz. Selanjutnya ekstrak metanol kelopak bunga rosella yang terpenetrasi ke dalam kulit dan yang tersisa dalam kulit di ukur dengan menggunakan spektrofotometri derivatif.
L. Hipotesis
1. Formula optimum multiemulsi yang terbentuk bertipe A/M/A, homogen, memiliki pH sesuai dengan pH kulit, dan stabil selama 28 hari, pada suhu penyimpanan -4 , dan pemberian gas nitrogen ditandai dengan tidak adanya pemisahan fase.
41
BAB III
METODOLOGI PENELITIAN A. Jenis Penelitian
Penelitian ini merupakan rancangan eksperimental murni yaitu untuk mengetahui sifat dan stabilitas fisis sediaan multiemulsi A/M/A ekstrak metanol kelopak bunga rosella dan mengetahui apakah sediaan multiemulsi A/M/A yang telah optimum mempunyai kemampuan sebagai pembawa ekstrak metanol kelopak bunga rosella yang lebih baik dari pada suspensi liposom dalam berpenetrasi ke dalam lapisan epidermis dan dermis.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas dalam penelitian ini dibagi menjadi dua, yaitu:
a. Variabel bebas dalam formulasi yaitu konsentrasi eksipien dan HLB multiemulsi A/M/A.
b. Variabel bebas dalam uji penetrasi dengan sel difusi Franz yaitu waktu pengambilan sampel penetrasi ekstrak metanol kelopak bunga rosella, ekstrak metanol kelopak bunga rosella dalam sediaan multiemulsi A/M/A dan suspensi liposom.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini dibagi menjadi dua, yaitu:
b. Variabel tergantung dalam uji penetrasi dengan sel difusi Franz yaitu kemampuan penetrasi ekstrak metanol kelopak bunga rosella ke dalam kulit.
3. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini dibagi menjadi dua, yaitu: a. Variabel pengacau terkendali dalam formulasi yaitu cahaya dan udara
selama pembuatan multiemulsi A/M/A.
b. Variabel pengacau terkendali dalam uji penetrasi dengan sel difusi Franz yaitu kondisi hewan uji, homogenitas sediaan, suhu, dan kecepatan pengadukan.
4. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini dibagi menjadi dua, yaitu:
a. Variabel pengacau tak terkendali dalam formula optimum yaitu kelembaban ruangan tempat pembuatan.
b. Variabel pengacau tak terkendali dalam uji penetrasi dengan sel difusi Franz yaitu ketebalan kulit, waktu penyimpanan kulit, dan berat sediaan yang diaplikasikan.
C. Definisi Operasional
2. Liposom ekstrak metanol kelopak bunga rosella adalah suatu vesikel yang terdiri dari satu lapis fosfolipid bilayer yang di dalamnya mengandung ekstrak metanol kelopak bunga rosella
3. Suspensi liposom adalah sediaan cair yang mengandung liposom ekstrak metanol kelopak bunga rosella yang didispersikan ke dalam air
4. Multiemulsi A/M/A ekstrak metanol kelopak bunga rosella adalah sistem multiemulsi A/M yang mengandung ekstrak metanol kelopak bunga rosella yang didispersikan dalam fase air dengan bantuan emulgator.
5. Emulgator adalah suatu senyawa yang berfungsi untuk menggabungkan fase minyak dengan fase air.
6. Multiemulsi A/M/A atau suspensi liposom dalam sampel larutan buffer fosfat pH 4 yang dianalisis merupakan sediaan semisolid atau sediaan cair yang terpenetrasi ke dalam kompartemen akseptor yang berisi larutan PBS pH 4. 7. Sel difusi Franz adalah serangkaian alat sel difusi Franz dengan ukuran
water jacket 9 mm, lipatan dasar datar (ground o-ring), dan volume kompartemen akseptor 3 mL.
8. Waktu pengambilan sampel adalah waktu yang diperlukan untuk mengambil sampel pada kompartemen donor dan kompartemen akseptor pada sel difusi Franz .
D. Bahan Penelitian
analysis, Merck), KCl (pro analysis, Merck), Na2HPO4 (pro analysis, Merck), KH2PO4 (pro analysis, Merck), HCl approx. 37% (pro analysis, Merck), setil alkohol (pharmaceutical grade), MgSO4 (pharmaceutical grade), dimethicone (pharmaceutical grade) diperoleh dari PT. Bratachem, Span 80 (pharmaceutical grade), xanthan gum (pharmaceutical grade), parafin (pharmaceutical grade) diperoleh dari PT. Bratachem, kulit tikus betina galur wistar, larutan ringer laktat yang diproduksi oleh PT. Widatra Bhakti, dan nitrogen teknis diperoleh dari CV. Perkasa.
E. Alat Penelitian
Hotplate Scilogex MS-H-S, waterbath Elbanton, mixer merk Miyako, alat-alat gelas, sel difusi Franz, termometer, seperangkat alat spektrofotometer UV-Vis Shimadzu UV-1800, seperangkat alat mikroskop, timbangan analitik/digital scale (Mettler Toledo), flakon, aluminium foil, sonikator (Retsch), table top sentrifuse model PLC-03, mikro pipet (Socorex), spuit injeksi 1ml, dan penggaris segitiga (zigel).
F. Tata Cara Penelitian 1. Ekstraksi kelopak bunga rosella
menggunakan corong buchner dengan kertas saring whatman no 1. Filtrat yang diperoleh selanjutnya di pekatkan dengan rotary evaporator pada suhu 40 sehingga menghasilkan ekstrak metanol kelopak bunga rosella. Ekstrak metanol kelopak bunga rosella yang dihasilkan di simpan pada botol fase gerak yang telah dilapisi dengan aluminium foil, dijenuhkan dengan N2 dan disimpan pada suhu -4 hingga analisis berikutnya. Proses ekstraksi ini dilakukan oleh Sanjayadi.
2. Penetapan bobot tetap ekstrak metanol kelopak bunga rosella
Cawan porselen yang hendak digunakan dikeringkan terlebih dahulu selama 30 menit. Kemudian cawan porselen yang telah dikeringkan ditara. 500 µL ekstrak metanol kelopak bunga rosella dimasukkan ke dalam cawan porselen dan ditimbang seksama cawan porselen beserta isinya. Kemudian dikeringkan dengan waterbath pada suhu 40 – 50 selama 1 jam. Kemudian ditimbang lagi hingga 2 kali penimbangan berturut-turut berbeda tidak lebih dari 0,5 mg tiap gram sisa yang ditimbang (Direktorat Jenderal Pengawasan Obat dan Makanan, 1979).
3.
Uji penetrasi ekstrak metanol kelopak bunga rosellapenetapan jumlah ekstrak metanol kelopak bunga rosella pada kompartemen akseptor atau donor.
a. Pembuatan 10 mM Phospate Buffer Saline (PBS) pH 4. Sebanyak 800 mL Aquabidest dimasukkan dalam gelas beker 1 L, kemudian ditambahkan 8 g NaCl, 0,2 g KCl, 1,44 g Na2HPO4, dan 0,24 g KH2PO4 diaduk dengan pengaduk magnetik hingga larut sempurna. Derajat keasaman larutan diukur dengan pH meter, dan pH larutan dibuat 4 dengan penambahan HCl. Larutan dipindahkan dalam labu takar 1 L, kemudian ditambahkan aquabidest sampai tanda. Larutan ini akan digunakan medium pada kompartmen akseptor.
Gambar 18. Rangkaian alat sel difusi Franz
c. Pemasangan alat sel difusi Franz (FDC). Sebelum digunakan kulit tikus dihidrasi terlebih dahulu dengan larutan ringer laktat selama 30 menit. Berdasarkan gambar 18, maka kulit dipasang pada FDC dengan bagian stratum korneum menghadap ke bagian kompartemen donor, lalu kompartemen akseptor diisi dengan PBS sebanyak 2,7 mL dan dimasukkan magnetic stirrer. Sebanyak 100 µl ekstrak metanol kelopak bunga rosella diaplikasikan pada kompartemen donor. Selama FDC beroperasi, suhu dijaga pada 31 – 33 , pada kompartemen akseptor tidak diperbolehkan adanya gelembung selama proses berlangsung, dan diaduk dengan magnetic stirrer dengan kecepatan 300 rpm.
d. Penetapan jumlah ekstrak metanol kelopak bunga rosella pada kompartemen akseptor. Pengambilan sampel pada uji penetrasi dengan menggunakan FDC dilakukan sebanyak 6 kali dengan kulit tikus yang berbeda yang dapat dilihat pada tabel 2.
Tabel 2. Variabel untuk tiap uji
Percobaan ke- I II III IV V VI
Waktu pengambilan
Sebanyak 100 µL ekstrak metanol kelopak bunga rosella diambil lalu diaplikasikan pada stratum korneum. Selanjutnya cairan PBS dalam kompartemen akseptor diambil pada jam yang tercantum pada tabel 2. Selanjutnya cairan PBS langsung di ukur dengan menggunakan spektrofotometri UV-VIS. Langkah ini diulangi sebanyak tiga kali sehingga terdapat tiga variasi jumlah ekstrak metanol kelopak bunga rosella pada kompartemen akseptor yang diaplikasikan.
e. Penetapan jumlah ekstrak metanol kelopak bunga rosella pada kompartemen donor. Setiap pengambilan cairan PBS pada kompartemen akseptor yang ditunjukkan dalam tabel 2, maka ekstrak metanol kelopak bunga rosella pada kompartemen donor dibilas dengan aquadest. Ekstrak metanol kelopak bunga rosella dibilas dengan 1,5 mL aquadest, lalu dimasukkan ke labu takar 5 mL dan ditambahkan dengan aquadest hingga batas selanjutnya diukur dengan spektrofotometer UV – Vis.
4. Optimasi formula multiemulsi A/M/A
- 6%); dan optimasi lama pencampuran multiemulsi (10 menit – 20 menit). Hasil optimasi dipilih yang menghasilkan % pemisahanan fase yang paling sedikit pada setiap perlakuan.
5. Pembuatan multiemulsi A/M/A
Proses pembuatan multiemulsi pada penelitian ini disiapkan dalam dua tahap yaitu pembuatan emulsi primer A/M dan pembuatan multiemulsi A/M/A
a. Pembuatan emulsi primer tipe A/M). Tween 80 dan ekstrak metanol kelopak bunga rosella dilarutkan dalam fase air internal. Span 80, dimethicone, setil alkohol, ditambahkan ke dalam parafin cair dan diaduk hingga homogen. Masing-masing fase dipanaskan pada suhu 50 ± 3 . Fase air ditambahkan sedikit demi sedikit ke dalam fase minyak, diaduk dengan mixer selama 10 menit hingga homogen. Keseluruhan proses pencampuran disertai dengan penjenuhan nitrogen, lampu ruangan dimatikan, serta wadah ditutup dengan menggunakan aluminium foil. b. Pembuatan multiemulsi tipe A/M/A. Fase air yang digunakan dalam fase
dan xanthan gum dan sambil diaduk menggunakan mixer selama 10 menit hingga homogen. Keseluruhan proses pencampuran disertai dengan penjenuhan nitrogen, lampu ruangan dimatikan, serta wadah ditutup dengan menggunakan aluminium foil. Multiemulsi A/M/A yang telah jadi dimasukkan ke dalam flakon yang telah dibungkus dengan aluminium foil dan dijenuhkan dengan nitrogen sebelum ditutup rapat dengan parafilm. 6. Evaluasi sediaan multiemulsi
Evaluasi sediaan multiemulsi dilakukan pada 1 hari setelah pembuatan multiemulsi. Evaluasi yang dilakukan meliputi sifat fisik sediaan dan stabilitas sediaan. sifat fisik sediaan yang dilakukan yaitu pengujian organoleptis, pengukuran pH, penentuan tipe emulsi, dan pengukuran mikromeritik. Stabilitas sediaan yang dilakukan yaitu uji mekanik dan uji volume creaming.
a. Pengujian organoleptis. Uji organoleptis dilakukan dengan mengamati bau, warna, dan homogenitas sediaan multiemulsi pada 1 hari setelah pembuatan
b. Penetapan pH. Sejumlah multiemulsi dioleskan pada kertas indikator dan kemudian ditentukan pH dari sediaan tersebut (Direktrorat Jenderal Pengawasan Obat dan Makanan, 1979).