PENGARUH PENINGKATAN KONSENTRASI SORBITOL DALAM SEDIAAN PASTA GIGI HPMC YANG MENGANDUNG MINYAK KAYU
MANIS (Cinnamomum burmanniiBl.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Widya Agriani Sidabutar NIM : 108114187
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH PENINGKATAN KONSENTRASI SORBITOL DALAM SEDIAAN PASTA GIGI HPMC YANG MENGANDUNG MINYAK KAYU
MANIS (Cinnamomum burmanniiBl.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Widya Agriani Sidabutar NIM : 108114187
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Halaman Persembahan
Allah turut bekerja dalam segala sesuatu untuk mendatangkan kebaikan
bagi yang mengasihi Dia.
Roma 8 : 28
Dalam segala kelemahankulah kuasa Tuhan menjadi sempurna.
2 Korintus 12 : 9
Kupersembahkan Karya Ini untuk:
Tuhan Yesus, Ayahku H. Sidabutar, Ibuku D. Ambarita, Abangku John Saputra Sidabutar, Kakakku Nirwana Sulatri Damanik, Adikku Srebrenita Desi Deria Sidabutar, Bapak Tuaku M. Sofyan Saragih, Oppungku Victor Sidabutar,
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yesus Kristus atas berkat dan kasih-Nya sehingga penulis dapat menyelesaikan penelitian skripsi yang berjudul “Pengaruh Peningkatan Konsentrasi Sorbitol dalam Sediaan Pasta Gigi HPMC yang Mengandung Minyak Kayu Manis (Cinnamomum burmannii Bl.)”. Skripsi ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm.) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Sepanjang proses perkuliahan, penelitian hingga penyusunan skripsi, penulis telah menerima banyak bantuan, dukungan, saran, kritik dan bimbingan dari berbagai pihak. Oleh karena itu, penulis ingin mengucapkan terima kasih kepada:
1. Tuhan Yesus Kristus, sebagai Tuhan sangat luar biasa dalam hidup penulis.
2. Bapak, Ibu, Abang, Kakak, Adik, Oppung dan Bapa Tua yang selalu berdoa, memberikan perhatian serta dukungan motivasi kepada penulis. 3. Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
4. Dr. T. N. Saifullah S., M.Si., Apt. selaku dosen pembimbing atas bantuan, bimbingan, pengarahan, kesabaran dan semangat selama penyusunan skripsi hingga selesainya skripsi ini.
viii
6. Dr. Sri Hartati Yuliani, M.Si., Apt. selaku dosen penguji yang memberikan masukan, saran serta kritik yang membangun kepada penulis.
7. Melania Perwitasari M.Sc., Apt. selaku dosen penguji yang memberikan masukan, saran serta kritik yang membangun kepada penulis.
8. Maria Dwi Budi Jumpowati, S.Si. sebagai dosen yang memberikan masukan, kritik dan saran dalam bidang Mikrobiologi kepada penulis. 9. Segenap Dosen Fakultas Farmasi Univerisitas Sanata Dharma yang telah
mengajar dan membimbing penulis selama perkuliahan.
10. Pak Musrifin, Pak Mukmin, Pak Parlan, Pak Iswandi, Pak Heru, Pak Agung, Pak Ottok, Pak Wagiran, Pak Sigit serta laboran-laboran yang lain yang telah membantu penulis selama penelitian.
11. Teman satu tim skripsi Hans, Eliza, Yani, Nita dan Tora.
12. Ricardo Kenny C., Lukas Surya, Leo Baktiman Ande, Yeni Natalia S., Gilda Todingbua, Stien Dwiny, Yoestenia, Vera Silaban, Maria Theresia Ghea, Agrifina Akardias atas motivasi dan dukungan kepada penulis. 13. Teman-teman FSM C, FSM D, FST A, FST B, FKK A dan FKK B 2010. 14. Semua pihak yang tidak dapat disebutkan satu per satu yang telah
membantu penulis dalam menyelesaikan skripsi ini.
Penulis menyadari bahwa naskah skripsi ini masih belum sempurna mengingat keterbatasan pengetahuan dan kemampuan penulis. Oleh karena itu, penulis mengharapkan saran dan kritik yang membangun dari seluruh pihak untuk ilmu pengetahuan.
ix DAFTAR ISI
Halaman HALAMAN JUDUL………..
HALAMAN PERSETUJUAN PEMBIMBING………. HALAMAN PENGESAHAN………
i ii iii
HALAMAN PERSEMBAHAN………. iv
PERNYATAAN KEASLIAN KARYA………. v
PERNYATAAN PERSETUJUAN PUBLIKASI………... vi
PRAKATA……….……. vii
DAFTAR ISI……….……….. ix
DAFTAR TABEL……….………….. xiv
DAFTAR GAMBAR……….…………. xv
DAFTAR LAMPIRAN……….…..………… DAFTAR PERSAMAAN………... DAFTAR SINGKATAN……… xvi xvii xviii INTISARI………... xix
ABSTRACT………..………… xx
BAB I. PENGANTAR………..……….. 1
A. Latar Belakang……….…………... 1
1. Perumusan Masalah………...………... 3
2. Keaslian Penelitian……….………...………… 3
3. Manfaat Penelitian..………..………… 4
x
BAB II. PENELAAHAN PUSTAKA………...………. 6
A. Gigi………... 6
1. Fungsi dan struktur gigi …...………... 6
2. Karies gigi dan penyakit periodontal……….……….. 6
B. BakteriS. mutans………... C. Tanaman Kayu Manis………... 1. Deskripsi………... 2. Kandungan minyak kayu manis……… 7 8 8 9 D. Pengujian Mutu Minyak Kayu Manis………. 1. Organoleptis……….... 2. Bobot jenis dan indeks bias………... E. Pengujian Potensi Antibiotik……….………. 9 9 10 10 1. Metode turbidimetri……….. 10 2. Metode difusi agar………
3. Metode cakram kertas………...
11 11 F. Levigating Agent………..………...
G. Pasta Gigi………..………...
12 12 1. Definisi………..………
2. Komponen penyusun pasta gigi………
12 13 H. Tinjauan Tentang Monografi Bahan-Bahan………...
xi 10. Minyak kayu manis……….
16 I. Pengujian Sediaan Pasta Gigi……….
1. Organoleptis………..
J. Landasan Teori……… 21
K. Hipotesis………. 22
BAB III. METODE PENELITIAN……..……….. 23
A. Jenis dan Rancangan Penelitian……….…………. 23
B. Variabel Penelitian dan Definisi Operasional………. 23
1. Variabel penelitian……… 23
2. Definisi operasional……….. 23
C. Bahan Penelitian………. 25
D. Alat Penelitian………. 25
E. Tata Cara Penelitian……… 26
xii
2. Sterilisasi peralatan dan media………...….. 3. Penyiapan stok bakteri uji……….
27 27 4. Pembuatan suspensi bakteri………..
5. Uji aktivitas antibakteri minyak kayu manis………
27 28
6. Penentuan KHM dan KBM……….……….. 28
7. Formula pasta gigi………... 29
8. Uji sifat fisik dan stabilitas pasta gigi………... 30
9. Uji aktivitas antibakteri pasta gigi minyak kayu manis terhadap S.mutansdengan difusi sumuran………... 31
10. Uji iritasi pasta gigi minyak kayu manis……….. 32
F. Analisis Hasil……….. 33
BAB IV. HASIL DAN PEMBAHASAN………..………. 34
A. Pengujian Mutu Minyak Kayu Manis………. B. Uji Daya Antibakteri Minyak Kayu Manis... C. Penentuan KHM dan KBM Minyak Kayu Manis……… 34 34 36 D. Pengujian Sifat Fisik dan Stabilitas Sediaan Pasta Gigi …………. 1. Uji organoleptis……… 2. Uji pH………...……… 3. Uji viskositas………..……….. 4. Uji daya lekat………...………... 38 38 39 40 42 E. UJi Aktivitas Antibakteri Pasta Gigi Minyak Kayu Manis……….. 44
F. Uji Iritasi ………...………... 46
xiii
A. Kesimpulan………... 48
B. Saran………. 48
DAFTAR PUSTAKA………. 49
LAMPIRAN……… 54
xiv
DAFTAR TABEL
Halaman Tabel I. Formula pasta gigi ………...……... 30 Tabel II. Penggolongan tingkat iritasi……….....…..………... 33 Tabel III. Hasil pengujian mutu minyak kayu manis.………... 34 Tabel IV. Hasil uji organoleptis pasta gigi…………...
xv
DAFTAR GAMBAR
Halaman Gambar 1. Struktur sinamaldehida……….
Gambar 2. Struktur sorbitol……...…………...…...…………... 9 16
Gambar 3. Struktur gliserin……...…………...…...…………... 16
Gambar 4. Struktur HPMC………...….………... 17
Gambar 5. Struktur silitol………..………...…….. 17
Gambar 6. Struktur metil paraben………...…………..……... 18
Gambar 7. Struktur SLS………...………... Gambar 8. Zona hambat minyak kayu manis………... 18 34 Gambar 9. Grafik Aktivitas antibakteri minyak kayu manis….…………. 34
Gambar 10. Hasil uji penentuan KHM dan KBM secara dilui padat…….. 37
xvi
DAFTAR LAMPIRAN
Halaman Lampiran 1. Sertifikat analisis minyak kayu manis……… 54 Lampiran 2. Sertifikat hasil ujiS. mutans...…..……….. 55 Lampiran 3. Sertifikat analisis HPMC……….
Lampiran 4. Uji mutu minyak kayu manis.………..………
56 57 Lampiran 5. Hasil uji aktivitas antibakteri dan penentuan KHM dan KBM
minyak kayu manis………... Lampiran 6. Hasil uji organoleptis …………..………... Lampiran 7. Hasil uji pH …………..………. Lampiran 8. Sifat fisik pasta gigi………..………. Lampiran 9. Stabilitas fisik pasta gigi…………..………... Lampiran 10. Pengukuran diameter zona antibakteri sediaan minyak kayu
manis terhadapS. mutans……….………... Lampiran 11. Uji iritasi……….……… Lampiran 12. Foto pasta gigi …………..……….. Lampiran 13. Alat-alat………...
59 61 62 63 66
xvii
DAFTAR PERSAMAAN
xviii
DAFTAR SINGKATAN CoA = Certificate of Analysis
HPMC = Hydroxypropyl Methylcellulose KBM = Kadar Bunuh Minimal
KHM = Kadar Hambat Minimal SLS = Sodium Lauryl Sulfate S. mutans =
SNI =
Streptococcus mutans
Standarisasi Nasional Indonesia TSA = Trypton Soya Agar
xix INTISARI
Bakteri S. mutans merupakan bakteri penyebab karies gigi. Sinamaldehida merupakan kandungan utama dalam minyak kayu manis yang memiliki aktivitas antibakteri. Minyak kayu manis dapat diformulasikan menjadi pasta gigi untuk meningkatkan penerimaan pengguna. Sorbitol digunakan sebagai levigating agent yang berfungsi untuk melembabkan dan melapisi partikel-partikel sediaan pasta gigi sehingga menghasilkan sediaan yang halus. Tujuan penelitian ini adalah untuk mengetahui pengaruh peningkatan konsentrasi sorbitol dalam pasta gigi minyak kayu manis terhadap sifat dan stabilitas sediaan, uji aktivitas antibakteri serta uji iritasi sediaan.
Penelitian ini merupakan eksperimental murni. Pasta gigi minyak kayu manis dibuat dengan variasi konsentrasi sorbitol 9%; 9,5%; 10%; 10,5%; 11% dan 11,5%. Sifat fisik dan stabilitas pasta gigi diuji dengan melihat organoleptis, pH, viskositas dan daya lekat. Data viskositas, daya lekat dan aktivitas antibakteri diuji statistik menggunakan perangkat R-3.0.2 untuk mengetahui signifikansi ( p-value< 0,05) dari peningkatan konsentrasi sorbitol.
Hasil penelitian menunjukkan bahwa sorbitol memberikan pengaruh terhadap viskositas dan daya lekat tetapi tidak mempengaruhi pH dan aktivitas antibakteri. Semakin tinggi konsentrasi sorbitol menyebabkan penurunan viskositas dan daya lekat. Pasta gigi minyak kayu manis dapat menghambat pertumbuhanS. mutansdan mengiritasi membran mukosa.
xx ABSTRACT
Bacteria S. mutans is the bacteria that causes dental caries. Cinnamaldehyde is the major chemical compound of cinnamon oil that has potential as an antibacterial. Cinnamon oil can be formulated into toothpaste to increase acceptance of users. Sorbitol is used as a levigating agent to moisten and coat the particles of toothpaste thus producing dosage form smooth. The purpose of this study was to determine the effect of increased concentrations of sorbitol in toothpaste cinnamon oil on the physical properties stability, antibacterial activity test and irritation test.
This research was a pure experimental explorative. Cinnamon oil toothpaste made with sorbitol concentration variation 9%; 9.5%; 10%; 10.5%; 11% and 11.5%. The physical properties and stability of toothpaste was tested by observed the organoleptic, pH, viscosity and adhesion. Data viscosity, adhesion and inhibition of bacteria were tested statistically using the R-3.0.2 to determine the significance (p-value <0.05) than the increased concentration of sorbitol.
The result of this study showed that sorbitol influence on viscosity and adhesion but did not affect the pH and antibacterial activity. Increasing concentration of sorbitol caused lower in viscosity and adhesion. Toothpaste cinnamon oil could inhibit the growth of S. mutans and irritate the mucous membranes.
1 BAB I PENGANTAR A. Latar Belakang
Gigi berfungsi untuk memotong dan menghancurkan makanan agar mudah ditelan dan dicerna (Walker, 2003). Gigi yang sehat merupakan impian setiap manusia karena selain untuk memotong makanan gigi juga berperan dalam mendukung penampilan menjadi agar terlihat lebih menarik. Gigi yang dirawat dengan cara yang tidak tepat dapat menimbulkan kerusakan pada gigi. Kerusakan gigi disebabkan oleh bakteri S. mutans karena dapat menciptakan suasana asam yang berlangsung lama pada mulut sebagai hasil dari proses fermentasi karbohidrat dan menyebabkan demineralisasi email (Renschler, 2006).
minyak kayu manis memiliki KHM sebesar 5% dan KBM sebesar 20% terhadap S.mutans.
Penggunaan minyak kayu manis secara langsung dapat menimbulkan rasa yang tidak nyaman saat penggunaan. Minyak kayu manis diformulasikan ke dalam pasta gigi untuk untuk meningkatkan kenyamanan saat penggunaan. Sediaan pasta gigi terdiri dari beberapa macam bahan penyusun antara lain bahan pengikat danlevigating agent.
Bahan pengikat berfungsi untuk mencegah terjadinya pemisahan komponen padat dengan komponen cair (Poucher, 2000). Bahan pengikat yang digunakan dalam penelitian ini adalah HPMC. HPMC bersifat hidrofil, stabil pada pH 3 – 11 (Rogers, 2009). HPMC dapat mencegah pembentukan aglomerasi dari partikel sehingga menghambat pembetukan sedimen (Marinho dan Soares, 2013).
Berdasarkan uraian di atas maka penulis tertarik untuk melakukan penelitian tentang pengaruh peningkatan konsentrasi sorbitol dalam sediaan pasta gigi minyak kayu manis. Pada sediaan pasta gigi perlu dilakukan uji sifat fisik dan stabilitas, uji daya antibakteri serta iritasi sediaan pasta gigi. Pentingnya pengujian tersebut untuk mengetahui kualitas dari sediaan pasta gigi.
1. Perumusan masalah
a. Bagaimana pengaruh peningkatan konsentrasi sorbitol terhadap sifat fisik dan stabilitas sediaan pasta gigi minyak kayu manis?
b. Apakah sediaan pasta gigi minyak kayu manis memiliki aktivitas antibakteri terhadap pertumbuhanS. mutans?
c. Apakah sediaan pasta gigi minyak kayu manis memiliki potensi mengiritasi membran mukosa?
2. Keaslian penelitian
Sejauh penelusuran pustaka yang telah dilakukan penulis, penelitian tentang pengaruh peningkatan konsentrasi sorbitol dalam sediaan pasta gigi HPMC yang mengandung minyak kayu manis dan pengujian terhadap S. mutans serta pengujian iritasi sediaan pasta gigi belum pernah dilakukan. Penelitian terkait yang pernah dilakukan adalah:
b. Pengaruh Konsentrasi Sorbitol sebagai Humektan dalam Pasta Gigi Minyak Atsiri Kayu Manis terhadap Karakteristik Fisik dan Stabilitas Sediaan (Fitria, 2013). Pada penelitian ini yang menjadi pembeda adalah bahan pengikat yang digunakan HPMC, pemanis yang digunakan silitol, pengujian aktivitas antibakteri pasta gigi terhadapS. mutansdan pengujian iritasi. c. Formulasi pasta gigi minyak cengkeh (Syzygium aromaticum(L.) Merr. dan
Perry (Masruhin, 2012). Pada penelitian ini yang menjadi pembeda adalah bahan pengikat yang digunakan HPMC, zat aktif yang digunakan minyak kayu manis dan pengujian iritasi.
3. Manfaat penelitian
a. Manfaat teoritis. Manfaat teoritis dari penelitian ini adalah memberi informasi ilmu pengetahuan tentang pengaruh peningkatan konsentrasi sorbitol dalam sediaan pasta gigi minyak kayu manis.
b. Manfaat praktis. Manfaat praktis dari penelitian ini adalah mengetahui tentang pengaruh peningkatan konsentrasi sorbitol dalam sediaan pasta gigi minyak kayu manis terhadap sifat fisik dan stabilitas sediaan pasta gigi, pengujian aktivitas antibakteri terhadap pertumbuhan S. mutans dan pengujian iritasi sediaan pasta gigi.
B. Tujuan Penelitian 1. Tujuan umum
2. Tujuan khusus
a. Untuk mengetahui pengaruh peningkatan konsentrasi sorbitol terhadap sifat fisik dan stabilitas pasta gigi minyak kayu manis.
b. Untuk mengetahui aktivitas antibakteri pasta gigi minyak kayu manis terhadap pertumbuhanS. mutans.
6 BAB II
PENELAAHAN PUSTAKA A. Gigi
1. Fungsi dan struktur gigi
Fungsi gigi secara spesifik terlepas dari organ lain di mulut yaitu untuk memotong, merobek dan menghaluskan makanan. Fungsi gigi secara umum terkait kerja sama dengan organ lain di sekitarnya seperti bibir dan lidah yaitu untuk pengunyahan makanan, berbicara dan mendukung penampilan dibandingkan dengan gigi berlubang yang terlihat kurang menarik (Erwana, 2013; Walker, 2003). Struktur gigi terdiri dari mahkota (Corona dentis), bagian leher (Cervix dentis), dan akar gigi (Radix dentis). Mahkota gigi adalah bagian gigi yang terlihat, muncul di atas Gingiva dan dilapisi oleh email (Enamelum). Bagian leher adalah tempat mahkota dan semen (sementum) yang menutupi permukaan akar. Akar gigi adalah bagian yang melekat dalam tulang (Brooker, 2005; Paulsen dan Waschke, 2011).
2. Karies gigi dan penyakit periodontal
gigi (Renschler, 2006). Penyakit periodontal ditandai dengan gingivitis (gingiva merah dan bengkak), perdarahan gusi, pembentukan rongga antara gigi dan gusi. Penyakit periodontal adalah kondisi peradangan dan degeneratif yang mengenai gusi dan jaringan penyokong gigi seringkali dimulai pada masa kanak-kanak dan menyebabkan lepasnya gigi yang signifikan pada masa dewasa. Gingivitis merupakan masalah periodontal yang paling umum terjadi yaitu penyakit peradangan reversible yang dimulai pada sebagian besar anak-anak diusia dini dan paling sering berkaitan dengan pembentukan plak gigi (Wong dkk., 2001). Plak gigi adalah lapisan yang sangat tipis berupa mukus dan dipenuhi oleh bakteri-bakteri yang ada di rongga mulut. Mukus adalah kumpulan dari mucin yang merupakan zat yang tekandung pada air liur (saliva). Mukus berfungsi sebagai sarana bakteri menempel di gigi (Erwana, 2013).
B. BakteriS. mutans
Bakteri S mutans pertama kali diisolasi dari lesi karies manusia pada tahun 1924 oleh Clarke. Pada media sukrosa yang mengandung agar menunjukan koloni putih (kadang-kadang kuning) dan menumpuk pada permukaan agar. SelS. mutans memiliki diameter 0,5-1,5µm, berbentuk bulat, oval atau memanjang. Streptococci adalah bakteri gram positif yang termasuk famili Streptococcaceae. Streptokokus adalah bakteri anaerob fakultatif (dapat hidup dalam kondisi ada atau tidak ada oksigen) (Renschler, 2006).
polisakarida ekstra sel yang sangat lengket dari karbohidrat. Polisakarida ini terdiri dari polimer glukosa yang menyebabkan matriks plak gigi mempunyai konsistensi seperti gelatin sehingga mempermudah bakteri untuk melekat pada gigi dan terbentuk plak yang semakin tebal (Kidd dan Bechal, 1992).
Bakteri S. mutans merupakan bakteri yang bersifat kariogenik karena menghasilkan asam dari hasil proses fermentasi karbohidrat. Bakteri S. mutans memiliki jalur glikolisis dan memproduksi laktat, format, etanol sebagai produk fermentasi karbohidrat. Proses fermentasi menyebabkan lingkungan menjadi asam, demineralisasi email yang menurunkan pH pada mulut yang berlangsung dalam waktu yang lama. Lingkungan asam ini merusak gigi yang menyebabkan gigi berlubang jika dibiarkan terus lubang gigi akan semakin dalam sehingga merusak pembuluh darah dan saraf dapat menjadi patogen yang menyebabkan infeksi oral seperti infeksi endokarditis (Renschler, 2006).
C. Tanaman Kayu Manis 1. Deskripsi
(kayu manis Cina). Cinnamomum burmannii Bl adalah jenis tanaman kayu manis yang banyak dikembangkan di Indonesia (Kardinan, 2005).
2. Kandungan minyak kayu manis
Komposisi kimia minyak kayu manis secara umum terdiri dari sinamaldehida, sinamilasetat, salisaldehida, asam sinamat, asam salisilat, asam benzoat, eugenol dan metilsalisaldehida. Sinamaldehida merupakan komponen utama minyak kayu manis (Puspaningtyas dan Utami, 2013). Menurut penelitian Atmania, Inna dan Prismasari (2010) serta Dwijayanti (2011) kandungan minyak kayu manis yang berperan dalam menghambat bakteri S. mutansadalah sinamaldehida. Sinamaldehida berinteraksi dengan membran sel bakteri dan menyebabkan kebocoran sel yang menyebabkan keluarnya ion-ion penting yang diperlukan untuk sintesis dinding sel bakteri sehingga bakteri mati (Gill dan Holley, 2004).
Gambar 1. Struktur sinamaldehida (Nainggolan, 2008)
D. Pengujian Mutu Minyak Kayu Manis 1. Organoleptis
Menurut SNI (2006) minyak kayu manis berwarna kuning muda sampai coklat muda dan berbau khas kayu manis.
2. Bobot jenis dan indeks bias
Bobot jenis adalah rasio bobot suatu zat terhadap bobot zat baku yang volumenya sama pada suhu yang sama dan dinyatakan dalam desimal. Kerapatan (density) adalah massa per satuan volume (bobot zat per satuan volume). Bobot jenis menggambarkan hubungan antara bobot suatu zat terhadap bobot suatu zat baku misalnya air yang merupakan zat baku untuk sebagian besar perhitungan dalam farmasi. Bobot jenis suatu zat dapat dihitung dengan mengetahui bobot zat (g) dibagi dengan bobot sejumlah volume air yang setara (g). Bobot jenis adalah faktor yang memungkinkan pengubahan jumlah zat dalam formula farmasetik dari bobot menjadi volume dan sebaliknya (Ansel dan Prince, 2004). Indeks bias adalah kemampuan suatu medium dalam membiaskan cahaya yang melewatinya (Umar, 2008). Menurut SNI (2006) bobot jenis dan indeks bias (nD20) minyak kayu manis adalah 1,008-1,030 dan 1,559-1,595.
E. Pengujian Potensi Antibiotik 1. Metode turbidimetri
ditunjukkan dengan kekeruhan media pada tabung uji. Kekeruhan dalam tabung uji dengan kekeruhan media dalam tabung antibiotik baku pembanding merupakan rasio potensi antibiotik (Harmita dan Radji, 2008).
2. Metode difusi agar ( lempeng silinder)
Prinsip metode difusi agar adalah membandingkan zona hambat pertumbuhan mikroorganisme uji oleh dosis senyawa antibiotik yang diuji terhadap zona hambat oleh dosis antibiotik baku pembanding pada media lempeng agar. Metode ini dilakukan dengan menginokulasikan mikroorganisme uji yang sesuai dan peka ke dalam media lempeng agar pada cawan petri. Silinder dipasang tegak lurus pada lapisan agar padat dalam cawan petri kemudian larutan antibiotik dimasukkan dan diinkunbasi. Mikroorganisme yang diinokulasikan dihambat pertumbuhannya pada daerah berupa lingkaran atau “zona” disekeliling silinder yang berisi larutan antibiotik. Rasio potensi antibiotik merupakan perbandingan ukuran garis tengah zona hambat yang disebabkan larutan antibiotik dan larutan antibiotik baku pembanding (Harmita dan Radji, 2008).
3. Metode difusi cakram
F. Levigating Agent
Levigating agent adalah cairan yang berfungsi untuk mengurangi ukuran partikel saat proses pencampuran dan pengadukan sehingga membentuk dispersi yang halus (Karimi, 2014). Levigating agent mengurangi ukuran partikel dengan cara menggantikan udara pada permukaan zat padat-udara dengan cairan sehingga ikatan antar partikel menjadi longgar. Contoh levigating agent yaitu gliserin, propilen glikol, sorbitol (Joseph dkk., 2013). Levigating agent mempunyai tegangan permukaan yang rendah dan agak viskos untuk meningkatkan pembasahan zat padat (Thompson dkk., 2009).
G. Pasta Gigi 1. Definisi
Pasta gigi adalah sediaan semi aqueous yang digunakan bersamaan dengan sikat gigi untuk membersihkan gigi (Buch, 2010). Pasta gigi membantu menghilangkan sisa makanan, mengkilapkan permukaan gigi dan menyegarkan bau nafas (Garlen, 1996). Menurut SNI (1995) syarat sediaan pasta gigi adalah sukrosa atau karbohidrat yang dapat terfermentasi negatif, pH 4,5-10,5, formaldehida maksimum sebagai formadehida bebas 0,1%, fluor bebas 800-1500 ppm, zat warna dan zat pengawet sesuai yang diijinkan oleh departemen kesehatan.
dari tube serta dapat mempertahankan bentuknya saat pengaplikasian pada sikat gigi. Viskositas dan daya lekat mempengaruhi konsistensi pasta. Abrasivitas adalah kemampuan dari pasta untuk membersihkan permukaan gigi. Penampilan pasta harus halus, seragam, mengkilap, bebas dari jebakan udara dan memiliki warna yang menarik. Kemampuan membentuk busa membantu menghilang sisa makanan melalui proses penyikatan. Rasa dari pasta dapat mempengaruhi konsumen untuk menggunakan produk kembali. Formulasi pasta gigi harus stabil selama penyimpanan, tidak terjadi pemisahan, mampu mempertahankan viskositas, pH dan agen terapetik aktif (Garlen, 1996).
2. Komponen penyusun pasta gigi
a. Abrasif. Abrasif merupakan komponen penting dari pasta gigi karena abrasif berfungsi untuk menghilangkan noda pelikel pada gigi (Schmalz dan Bindslev, 2009). Contoh abrasif yaitu kalsium karbonat, kalsium fosfat, silika, sodium bikarbonat. Konsentrasi abrasif yang digunakan umumnya adalah 20% - 50% dalam total formulasi (Garlen, 1996).
b. Bahan pengikat. Bahan pengikat berfungsi mencegah pemisahan antara komponen air dan minyak serta membuat formulasi menjadi kental (Harman, 2001). Contoh bahan pengikat adalah karagenan, gum selulosa dan xanthan gum. Konsentrasi binder yang digunakan umumnya adalah 0,9% - 2% dalam formulasi (Garlen, 1996).
Bindslev, 2009). Konsentrasi detergen digunakan antara 2% atau kurang agar tidak menimbulkan iritasi (Garlen, 1996).
d. Humektan. Humektan berfungsi untuk mencegah hilangnya air dan mempertahankan kelembaban pada sediaan pasta gigi sehingga pasta gigi tidak mengeras (Buch, 2010). Contoh humektan adalah sorbitol, propilen glikol atau gliserin (Jungermann dan Sonntag, 1991). Konsentrasi humektan yang digunakan dalam pasta gigi adalah 10% - 30% (Poucher, 2000).
e. Bahan pemanis. Bahan pemanis berfungsi untuk meningkatkan rasa dari pasta gigi dengan memberikan rasa yang lembut dan manis. konsentrasi pemanis yang digunakan adalah 0,05% - 0,25% (Garlen, 1996). Contoh bahan pemanis adalah sakarin, sorbitol, gliserin, silitol. Silitol merupakan bahan pemanis yang di klaim memiliki aktivitas anti karies (Buch, 2010). f. Bahan perasa. Bahan perasa berfungsi untuk memberi rasa segar pada
rongga mulut. Bahan perasa yang popular yaitu peppermint, spearmint, cinnamon. Konsentrasi bahan perasa dalam pasta gigi yang ditambahkan memberikan rasa tertentu yang spesifik dan membuat rasa yang unik sehingga hal ini perlu diperhatikan. Bahan perasa yang ditambahkan tidak boleh berlebihan serta tidak memberi kesan seperti rasa terbakar (Othmer, 2013). Konsentrasi bahan perasa dalam pasta gigi adalah 0,2% - 2% (Garlen, 2009).
dimurnikan dengan cara destilasi, perlakuan menggunakan penukar ion, osmosis balik, atau proses yang sesuai (Dirjen POM, 1995).
h. Bahan pengawet. Bahan pengawet berfungsi untuk mencegah pertumbuhan mikroorganisme pada pasta gigi. Contoh bahan pengawet yang sering digunakan yaiutu sodium benzoat, metil paraben dan etil paraben (Buch, 2010). Konsentrasi bahan pengawet yang digunakan yaitu 0,05% - 0,2% (Garlen, 1996).
H. Tinjauan Tentang Monografi Bahan-Bahan 1. Kalsium karbonat
Kalsium karbonat (CaCO3, BM 100,9) berbentuk serbuk atau kristal
putih, tidak berbau dan tidak berasa. Kalsium karbonat hampir tidak larut dalam etanol 95% dan air. Kelarutan kalsium karbonat di dalam air akan meningkat dengan adanya garam ammonium atau karbon dioksida dan kelarutan akan berkurang dengan adanya alkali hidroksida (Armstrong, 2009). Kalsium karbonat larut dalam asam asetat 1 N, dalam asam klorida 3 N dan dalam asam nitrat 2 N dengan membentuk gelembung gas (Dirjen POM, 1995). 2. Sorbitol
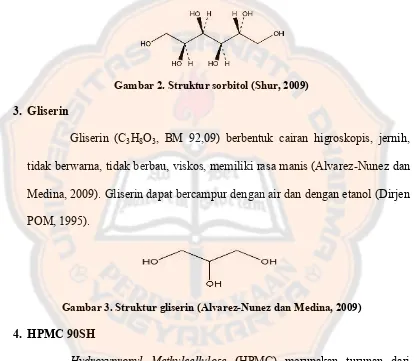
Sorbitol (C6H14O6, BM 182,17) berbentuk kristalin, serbuk
Keuntungan sorbitol yaitu tidak menurunkan pH mulut jadi tidak mendorong pertumbuhan bakteri yang dapat menyebabkan kerusakan gigi, memiliki tingkat rasa manis seperti sukrosa sekitar 60%. Larutan sorbitol menjadikan produk menjadi halus tanpa viskositas yang kental (Nabors, 2012).
Gambar 2. Struktur sorbitol (Shur, 2009)
3. Gliserin
Gliserin (C3H8O3, BM 92,09) berbentuk cairan higroskopis, jernih,
tidak berwarna, tidak berbau, viskos, memiliki rasa manis (Alvarez-Nunez dan Medina, 2009). Gliserin dapat bercampur dengan air dan dengan etanol (Dirjen POM, 1995).
Gambar 3. Struktur gliserin (Alvarez-Nunez dan Medina, 2009)
4. HPMC 90SH
penguapan air, relatif enzim-resisten dan memberikan stabilitas viskos yang baik selama penyimpanan dalam jangka waktu yang lama (Rogers, 2009).
Gambar 4. Struktur HPMC (Harwood, 2005)
5. Silitol
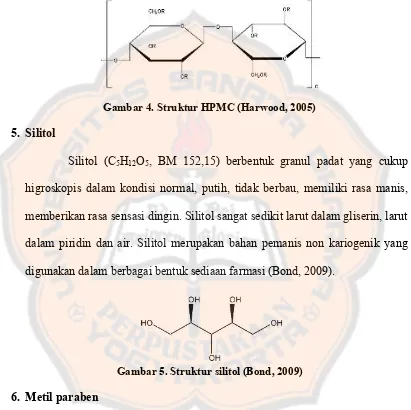
Silitol (C5H12O5, BM 152,15) berbentuk granul padat yang cukup
higroskopis dalam kondisi normal, putih, tidak berbau, memiliki rasa manis, memberikan rasa sensasi dingin. Silitol sangat sedikit larut dalam gliserin, larut dalam piridin dan air. Silitol merupakan bahan pemanis non kariogenik yang digunakan dalam berbagai bentuk sediaan farmasi (Bond, 2009).
Gambar 5. Struktur silitol (Bond, 2009)
6. Metil paraben
Metil paraben (C8H8O3, BM 152,15) berbentuk kristal tidak berwarna
sedangkan untuk penggunaan campuran dengan paraben lainnya adalah 0,8% (Annex VI, 2008).
Gambar 6. Struktur metil paraben (Haley, 2009)
7. SLS
SLS digunakan sebagai deterjen dengan membentuk busa. Penggunaan SLS menyebabkan iritasi sehingga jumlahnya harus dibatasi yaitu kurang dari 2% (Garlen, 1996). SLS berbentuk kristal berwarna putih atau kuning muda, mudah larut dalam air, praktis tidak larut dalam kloroform dan eter (Plumb, 2009).
Gambar 7. Struktur SLS (Plumb, 2009)
8. Minyak permen
lipid. Mentol menyebabkan sensasi dingin ketika diaplikasikan ke kulit (Langdon dan Mullarney, 2009).
9. Air
Air (H2O, BM 18,02) berfungsi sebagai pelarut (Dubash dan Shah,
2009). Air berbentuk cairan jernih, tidak berwarna dan tidak berbau. Air memiliki pH 5 – 7 (Dirjen POM, 1995).
10. Minyak kayu manis
I. Pengujian Sediaan Pasta Gigi 1. Organoleptis
Uji organoleptis meliputi bentuk, warna, rasa, bau. Pasta gigi harus memiliki penampilan halus, homogen dan mengkilap serta harus memiliki tampilan warna yang menarik, tidak ada udara yang terperangkap di dalamnya. Pasta gigi juga harus memiliki spesifik rasa dan aroma merupakan aspek yang dapat mempengaruhi konsumen untuk menggunakan produk tersebut (Garlen, 1996).
2. Viskositas
Viskositas adalah ukuran resistensi cairan untuk mengalir, umumnya satuan viskositas adalah poise (P) tetapi satuan centipoise (cp) lebih lazim digunakan dimana 1 poise = 100 centipoise. Viskositas dipengaruhi oleh suhu, jika suhu tinggi maka viskositas rendah. Untuk mendapatkan hasil viskositas yang akurat dengan viskometer maka suhu harus dikontrol dengan hati-hati (Kenkel, 2003). Viskositas pasta gigi umumnya memiliki range 150000 dan 300000 centipoise (Garlen, 1996).
3. pH
4. Daya lekat
Daya lekat mempengaruhi konsistensi pasta gigi. Daya lekat berkaitan dengan kemampuan melekat pada sikat gigi saat hendak diaplikasikan (Garlen, 1996). Pengujian daya lekat dilakukan dengan menimbang sebanyak 0,25 g sediaan di atas gelas objek, diberi beban sebesar 1 kg selama 1 menit kemudian dipasang pada alat uji. Alat uji yang digunakan diberi beban sebesar 80 g. Daya lekat merupakan waktu yang digunakan sediaan untuk terlepas dari gelas objek (Voigh, 1995).
J. Landasan Teori
K. Hipotesis
1. Peningkatan konsentrasi sorbitol dapat menurunkan viskositas dan daya lekat tetapi tidak mempengaruhi pH pasta gigi serta mempengaruhi stabilitas fisik viskositas dan daya lekat tetapi tidak mempengaruhi pH pasta gigi.
2. Pasta gigi minyak kayu manis dapat menghambat pertumbuhanS. mutans. 3. Pasta gigi minyak kayu manis tidak memiliki potensi mengiritasi membran
23 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian Penelitian ini merupakan rancangan eksperimental murni.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas. Variabel bebas dalam penelitian ini adalah konsentrasi sorbitol yaitu 9%; 9,5%; 10%; 10,5%; 11% dan 11,5%.
b. Variabel tergantung. Variabel tergantung dalam penelitian ini adalah sifat fisik dan stabilitas fisik sediaan (organoleptis, pH, viskositas dan daya lekat), uji aktivitas antibakteri dan uji iritasi sediaan pasta gigi.
c. Variabel pengacau terkendali. Variabel pengacau terkendali dalam penelitian ini adalah lama penyimpanan dan sifat dari wadah penyimpanan. d. Variabel pengacau tak terkendali. Variabel pengacau tak terkendali dalam
penelitian ini adalah suhu, kelembaban ruangan dan umur siput. 2. Definisi operasional
a. Pasta gigi. Pasta gigi merupakan suatu sediaan semi solid liquid yang digunakan untuk membersihkan gigi.
b. Levigating agent. Levigating agent berfungsi untuk menghasilkan sediaan yang halus dengan cara mengurangi ukuran partikel.Levigating agent yang digunakan adalah sorbitol.
d. Stabilitas pasta. Stabilitas pasta ditentukan dari besarnya nilai pergesaran viskositas 48 jam sesudah proses pembuatan pasta gigi dan sesudah penyimpanan pasta gigi selama 1 bulan.
e. Faktor. Faktor adalah variabel yang diteliti di dalam penelitian (sorbitol). f. Respon. Respon adalah besaran yang diamati perubahan efeknya dan
besarnya dapat dikuantitatifkan. Respon dalam penelitian ini adalah sifat fisik, stabilitas, uji aktivitas antibakteri dan uji iritasi pasta gigi.
g. S. mutans. S. mutans merupakan biakan murni yang diperoleh dari Laboratorium Balai Kesehatan Yogyakarta.
h. Aktivitas antibakteri. Aktivitas antibakteri adalah kemampuan minyak kayu manis dan pasta gigi minyak kayu manis dalam menghambat dan membunuh S. mutans yang memiliki perbedaan bermakna secara statistik apabila dibandingkan dengan kontrol negatif .
i. Kontrol positif. Kontrol positif dalam penelitian ini adalah pasta gigi merek “X” yang sudah beredar di pasaran yang digunakan sebagai pembanding. j. Kontrol negatif. Kontrol negatif dalam penelitian ini adalah parafin cair dan
basis pasta gigi.
k. Zona hambat. Zona hambat adalah zona jernih yang tidak menunjukan adanya pertumbuhan koloniS. mutans.
m. Metode dilusi padat. Metode dilusi padat adalah metode pengukuran aktivitas antibakteri dengan cara mengencerkan minyak kayu manis sampai beberapa konsentrasi kemudian dicampur pada media agar padat untuk melihat daya hambat minyak kayu manis serta menentukan nilai KHM dan KBM.
n. KHM. KHM adalah konsentrasi minimum minyak kayu manis yang menghambat pertumbuhanS. mutans.
o. KBM. KBM adalah konsentrasi minimum minyak kayu manis yang dapat membunuhS. mutans.
p. Mukus. Mukus adalah lendir yang dihasilkan oleh slug (siput tanpa cangkang).
C. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah minyak kayu manis yang diperoleh dari Eteris Nusantara Padang, HPMC 90SH, sorbitol, gliserin, silitol, metil paraben, minyak permen, SLS, kalsium karbonat. Seluruh bahan yang telah disebutkan di atas memiliki kualitas farmasetis. Distilled water yang digunakan adalah aquadest dari Laboratorium Kimia Organik Universitas Sanata Dharma Yogyakarta, kultur bakteri S. mutans diperoleh dari Balai Laboratorium Kesehatan Yogyakarta, trypton soya agar (OXOID), trypton soya broth(OXOID), etanol absolut 96 %,slug, larutan standar Mc Farland 0,5.
D. Alat Penelitian
Tokyo, Japan), microbiological safety cabinet, inkubator (Heraeus), pH indikator universal (Merck), sentrifuge (Heraeus), piknometer (Pyrex, Iwaki Glass), hand refractometer (Atago), oven, jarum ose, mikropipet, spuit injeksi, pelubang sumuran,object glass,jangka sorong dan alat-alat gelas.
E. Tata Cara Penelitian 1. Identifikasi dan verifikasi minyak kayu manis
a. Pengamatan organoleptis. Pengamatan organoleptis dilakukan secara visual meliputi tekstur, warna, bau dan homogenitas.
b. Verifikasi indeks bias. Indeks bias minyak kayu manis diukur menggunakan hand refractometerdengan cara penutup prisma dibuka, minyak kayu manis diteteskan 1 sampai 2 tetes pada prisma utama kemudian penutup prisma ditutup perlahan sampai menyentuh prisma utama. Ujung refraktor diarahkan ke arah cahaya yang terang, diputar-putar dan dilihat melalui lensa sampai skala terlihat jelas yaitu tampak garis batas yang memisahkan sisi yang terang dan gelap pada bagian atas dan bawah. Apabila garis batas berwarna atau tidak jelas maka ring diputar untuk menghilangakan warna hingga batas terlihat dengan jelas. Nilai indeks bias minyak kayu manis ditunjukkan oleh garis batas yang memisahkan sisi gelap dan sisi terang. c. Verifikasi bobot jenis minyak kayu manis. Bobot jenis minyak kayu manis
air yang menempel pada dinding piknometer di bagian luar dibersihkan lalu piknometer ditimbang untuk menetapkan bobot piknometer kosong dan bobot air pada suhu 25oC. Perlakuan yang sama dilakukan terhadap minyak kayu manis dengan menggunakan piknometer yang sudah dikalibrasi. Bobot jenis minyak kayu manis merupakan perbandingan antara kerapatan minyak kayu manis (g/mL) dengan kerapatan (g/mL) pada suhu 25oC.
2. Sterilisasi peralatan dan media
Peralatan dalam penelitian yang berhubungan dengan bakteri uji seperti tabung reaksi dan cawan petri sebelum digunakan disterilisasi dahulu menggunakan autoklaf pada suhu 121oC selama 20 menit dengan tekanan 1 atm sedangkan untuk media TSA dan TSB disterilisasi selama 15 menit.
3. Penyiapan stok bakteri uji
Stok bakteri uji dibuat dengan cara media TSA yang sudah disterilisasi dibiarkan memadat dalam kondisi miring kemudian biakan murni S. mutans diambil 1 – 3 ose lalu diinokulasikan dan diinkubasi selama 24 jam pada suhu 37oC.
4. Pembuatan suspensi bakteri
5. Uji aktivitas antibakteri minyak kayu manis dengan metode sumuran Pengujian aktivitas antibakteri minyak kayu manis terhadap bakteri S. mutansdilakukan dengan metode sumuran. Media TSA yang digunakan dibagi menjadi 2 bagian yaitulayerbawah danlayeratas.Layerbawah dibuat dengan cara media TSA steril sebanyak 10 mL dituang ke dalam cawan petri dan dibiarkan memadat. Layer atas dibuat dengan cara media TSA steril sebanyak 30 mL, diinokulasikan bakteri uji 0,2 mL yang sudah disetarakan dengan larutan standar Mc Farland 0,5 divortex lalu dituang ke dalam cawan petri yang berisi layer bawah yang sudah memadat dan dibiarkan memadat. Pada media yang sudah memadat secara aseptis dibuat lubang sampai batas antara layer bawah dan layeratas.
Pada media dibuat 6 lubang pada tiap petri dengan menggunakan pelubang sumuran dengan diameter 7 mm secara aseptis. Pada setiap lubang sumuran masingmasing diisi dengan minyak kayu manis konsentrasi 1% -10% dan kontrol negatif (parafin cair) masing-masing sebanyak 0,02 mL kemudian diinkubasi selama 24 jam dengan suhu 37oC.
Pengamatan diameter zona jernih dilakukan setelah inkubasi selama 24 jam. Pengukuran zona jernih menggunakan jangka sorong digital. Daya antibakteri diamati berdasarkan diameter zona jernih yang terbentuk dibandingkan dengan kontrol negatif.
6. Penentuan konsentrasi hambat minimal dan konsentrasi bunuh minimal dengan metode dilusi padat
0,5 divortex dan dituang ke dalam cawan petri. Minyak kayu manis konsentrasi 4% - 10% sebanyak 0,2 mL ditambahkan ke dalam cawan petri tersebut lalu diinkubasi selama 24 jam pada suhu 37oC.
KHM dan KBM diketahui dengan cara membandingkan tingkat kekeruhan antara media yang diinokulasikan minyak kayu manis, kontrol negatif dan kontrol pertumbuhan bakteri uji. Kekeruhan pada media berarti ada pertumbuhan bakteri. Pada media pertumbuhan yang jernih dilakukan pengujian penegasan dengan menginokulasikan bakteri dari setiap media yang jernih ke media steril yang baru secara streak plate. KHM adalah konsentrasi terkecil dari minyak kayu manis yang dapat menghambat bakteri uji ditandai dengan masih terdapat pertumbuhan bakteri pada hasil streak. KBM adalah konsentrasi terkecil yang membunuh bakteri uji ditandai dengan tidak ada pertumbuhan bakteri pada hasilstreak.
7. Formulasi pasta gigi
ditambahkan fase C. Sisa CaCO3 di masukkan ke dalam campuran dan
diaduk hingga homogen.
b. Formula variasi konsentrasi sorbitol adalah sebagai berikut: Tabel I. Formula pasta gigi dengan variasi konsentrasi sorbitol
Bahan
Total 100 100,5 101 101,5 102 102,5
8. Uji sifat fisik dan stabilitas pasta gigi
a. Uji organoleptis. Uji organoleptis yang dilakukan meliputi bau, warna, homogenitas dan tekstur pasta gigi. Uji ini dilakukan setelah 2 hari pembuatan pasta gigi sedangkan untuk mengetahui perubahan organoleptis dilakukan uji pada 7 hari, 14 hari, 21 hari dan 28 hari penyimpanan.
b. Uji pH. Uji pH dilakukan dengan menggunakan kertas pH. Uji ini dilakukan setelah 2 hari pembuatan pasta gigi sedangkan untuk mengetahui perubahan pH dilakukan uji pada 7 hari, 14 hari, 21 hari dan 28 hari penyimpanan. c. Uji daya lekat. Uji daya lekat dilakukan dengan cara 0,25 gram pasta gigi
pelepasan pasta dari gelas objek (Voigh, 1995). Uji daya lekat dilakukan setelah 2 hari pembuatan pasta gigi sedangkan untuk mengetahui ada perubahan daya lekat dilakukan uji pada 7 hari, 14 hari, 21 hari dan 28 hari penyimpanan.
d. Uji viskositas. Pengukuran viskositas menggunakan alat Viscotester Rion seri VT 04 dengan cara pasta gigi dimasukan ke dalam wadah kemudian dipasang pada portable viscotester. Viskositas pasta gigi diketahui dengan mengamati gerakan jarum penunjuk viskositas. Uji ini dilakukan setelah 2 hari pembuatan pasta gigi sedangkan untuk mengetahui pergeseran viskositas dilakukan uji pada 7 hari, 14 hari, 21 hari dan 28 hari penyimpanan.
9. Uji aktivitas antibakteri pasta gigi dengan metode difusi sumuran
a. Pembuatan suspensi bakteri. Diambil 1 - 3 ose isolat murni bakteri S. mutans yang sudah dibiakkan, diinokulasikan ke dalam TSB yang sudah disterilkan dan diinkubasi pada suhu 37oC selama 24 jam. Kekeruhan suspensi bakteri uji disetarakan dengan larutan standar Mc Farland 0,5 apabila kekeruhan melebihi larutan standar Mc Farland 0,5 maka dilakukan penambahan media TSB steril untuk memperoleh tingkat kekeruhan yang sama.
diinokulasikan bakteri uji yang sudah disetarakan dengan larutan Mc Farland sebanyak 0,2 mL lalu di vortex kemudian dituang ke dalam layer bawah yang sudah memadat.
c. Uji daya antibakteri pasta gigi dengan metode sumuran. Pada media TSA yang sudah memadat dibuat lubang secara aseptis menggunakan pelubang sumuran dengan diameter 7 mm. Pada tiap petri dibuat 4 lubang. Pada setiap lubang sumuran diinokulasikan sediaan pasta gigi F I - F VI, kontrol negatif (basis pasta gigi), kontrol positif (pasta gigi merek “X”) dan minyak kayu manis 7% menggunakan spuit injeksi 1 mL dengan volume masing-masing 0,02 mL lalu diinkubasi selama 24 jam pada suhu 37oC, kemudian diamati diameter zona jernih yang dihasilkan. Diameter zona jernih yang dihasilkan diukur menggunakan jangka sorong digital. Daya antibakteri diamati berdasarkan diameter zona jernih yang terbentuk dibandingkan dengan kontrol negatif dan positif.
10. Uji iritasi
Slug dipilih dengan berat antara 3 - 4 gram. Sediaan pasta gigi ditimbang sebanyak 500 mg pada cawan petri kemudian slug diletakkan pada sediaan tersebut selama 30 menit. Mukus yang ada pada cawan petri ditimbang. Mukus yang diproduksi (MP) dihitung dengan rumus I yaitu :
MP = ( )
( ) × 100% (I)
Tabel II. Penggolongan iritasi
Mukus Kelas Iritasi
< 15% Tidak mengiritasi 15-20% Mengiritasi ringan 20-25% Mengiritasi sedang > 25% Mengiritasi berat
F. Analisis Hasil
34 BAB IV
HASIL DAN PEMBAHASAN A. Pengujian Mutu Minyak Kayu Manis
Pengujian mutu minyak kayu manis berfungsi untuk memastikan apakah minyak kayu manis yang diperoleh dari CV Eteris Nusantara sesuai dengan CoA dan memenuhi persyaratan SNI. Pengujian mutu yang dilakukan meliputi organoleptis (bau dan warna), bobot jenis dan indeks bias. Berdasarkan hasil pengujian mutu (Tabel III) dapat disimpulkan bahwa minyak kayu manis yang diperoleh dari CV Eteris Nusantara telah sesuai dengan CoA dan memenuhi persyaratan SNI (2006).
Tabel III. Hasil pengujian mutu minyak kayu manis
Pengujian mutu Hasil CoA SNI (2006)
Bau Khas minyak kayu
manis
Manis, pedas dan hangat
Khas kayu manis
Warna Kuning Kuning Kuning muda
-kuning coklat Bobot jenis 1,0161 ± 0,0005 1,013 1,008 - 1,030
Indeks bias 1,5758 ± 0,020 1,580 1,559 - 1,595
B. Uji Daya Antibakteri Minyak Kayu Manis terhadapStreptococcus mutansdengan Difusi Sumuran
penelitian adalah parafin cair. Variasi konsentrasi minyak kayu manis yang di uji adalah 1% - 10%.
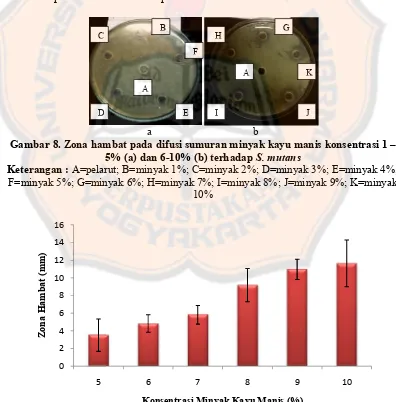
Hasil pengamatan menunjukkan kontrol negatif dan minyak kayu manis konsentrasi 1% - 4% tidak memberikan zona hambat sedangkan minyak kayu manis konsentrasi 5% - 10% memberikan zona hambat (Gambar 8a dan b). Hal ini berarti zona hambat yang terbentuk pada bakteri S. mutans berasal dari minyak kayu manis dan tidak dipengaruhi oleh pelarut. Pelarut yang menghasilkan zona hambat dapat membiaskan hasil penelitian.
a b
Gambar 8. Zona hambat pada difusi sumuran minyak kayu manis konsentrasi 1 – 5% (a) dan 6-10% (b) terhadapS. mutans
Keterangan :A=pelarut; B=minyak 1%; C=minyak 2%; D=minyak 3%; E=minyak 4%; F=minyak 5%; G=minyak 6%; H=minyak 7%; I=minyak 8%; J=minyak 9%; K=minyak
10%
Gambar 9. Grafik uji daya antibakteri minyak kayu manis
0
penelitian adalah parafin cair. Variasi konsentrasi minyak kayu manis yang di uji adalah 1% - 10%.
Hasil pengamatan menunjukkan kontrol negatif dan minyak kayu manis konsentrasi 1% - 4% tidak memberikan zona hambat sedangkan minyak kayu manis konsentrasi 5% - 10% memberikan zona hambat (Gambar 8a dan b). Hal ini berarti zona hambat yang terbentuk pada bakteri S. mutans berasal dari minyak kayu manis dan tidak dipengaruhi oleh pelarut. Pelarut yang menghasilkan zona hambat dapat membiaskan hasil penelitian.
a b
Gambar 8. Zona hambat pada difusi sumuran minyak kayu manis konsentrasi 1 – 5% (a) dan 6-10% (b) terhadapS. mutans
Keterangan :A=pelarut; B=minyak 1%; C=minyak 2%; D=minyak 3%; E=minyak 4%; F=minyak 5%; G=minyak 6%; H=minyak 7%; I=minyak 8%; J=minyak 9%; K=minyak
10%
Gambar 9. Grafik uji daya antibakteri minyak kayu manis
5 6 7 8 9
Konsentrasi Minyak Kayu Manis (%)
G
penelitian adalah parafin cair. Variasi konsentrasi minyak kayu manis yang di uji adalah 1% - 10%.
Hasil pengamatan menunjukkan kontrol negatif dan minyak kayu manis konsentrasi 1% - 4% tidak memberikan zona hambat sedangkan minyak kayu manis konsentrasi 5% - 10% memberikan zona hambat (Gambar 8a dan b). Hal ini berarti zona hambat yang terbentuk pada bakteri S. mutans berasal dari minyak kayu manis dan tidak dipengaruhi oleh pelarut. Pelarut yang menghasilkan zona hambat dapat membiaskan hasil penelitian.
a b
Gambar 8. Zona hambat pada difusi sumuran minyak kayu manis konsentrasi 1 – 5% (a) dan 6-10% (b) terhadapS. mutans
Keterangan :A=pelarut; B=minyak 1%; C=minyak 2%; D=minyak 3%; E=minyak 4%; F=minyak 5%; G=minyak 6%; H=minyak 7%; I=minyak 8%; J=minyak 9%; K=minyak
10%
Gambar 9. Grafik uji daya antibakteri minyak kayu manis
Semakin tinggi konsentrasi minyak kayu manis maka zona hambat yang dihasilkan semakin besar (Gambar 9). Menurut Bell dkk., (2009) suatu bahan dikatakan memiliki aktivitas antimikroba bila menghasilkan diameter zona hambat lebih besar dari 6 mm. Minyak kayu manis konsentrasi 5% - 10% digunakan dalam penentuan konsentrasi hambat minimal (KHM) dan konsentrasi bunuh minimal (KBM).
C. Penentuan KHM dan KBM Minyak Kayu Manis terhadap Streptococcus mutansdengan Metode Dilusi Padat
Penentuan KHM dan KBM menggunakan konsentrasi minyak kayu manis 5% - 10% dengan metode dilusi padat. Pengujian ini bertujuan untuk menentukan konsentrasi bunuh minimal minyak kayu manis terhadap S. mutans yang digunakan sebagai konsentrasi zat aktif dalam formulasi pasta gigi. Senyawa uji dikatakan memiliki aktivitas antibakteri jika memiliki tingkat kekeruhan yang lebih kecil dari kontrol pertumbuhan bakteri uji dan tingkat kejernihan yang sama dengan kontrol pelarut. Keruh berarti pada media masih terdapat pertumbuhan bakteri sedangkan jernih berarti pada media tidak terdapat pertumbuhan bakteri.
(Gambar 10). Berdasarkan hasil uji dapat disimpulkan bahwa minyak kayu manis konsentrasi 0,06% dinyatakan sebagai nilai KHM dan konsentrasi 0,08% dinyatakan sebagai nilai KBM.
Gambar 10. Perbandingan kerjernihan minyak kayu manis dengan kontrol pelarut, kontrol sterilitas media dan kontrol pertumbuhan bakteri.Keterangan: a = kontrol
pelarut; b = kontrol pertumbuhan; 5 - 10% = minyak kayu manis.
a b Gambar 11. Uji penegasan I (a) dan II (b)
Uji penegasan dilakukan untuk memastikan kebenaran nilai KHM dan KBM tersebut. Pada hasil uji penegasan pertama dan penegasan kedua menunjukkan minyak kayu manis 0,08% masih terdapat pertumbuhan bakteri sedangkan minyak kayu manis konsentrasi 0,09% tidak terdapat pertumbuhan bakteri (Gambar 11a dan b). Berdasarkan hasil uji penegasan pertama dan kedua dapat disimpulkan bahwa minyak kayu manis konsentrasi 0,08% dinyatakan
a b 5% 6%
7% 8% 9% 10%
(Gambar 10). Berdasarkan hasil uji dapat disimpulkan bahwa minyak kayu manis konsentrasi 0,06% dinyatakan sebagai nilai KHM dan konsentrasi 0,08% dinyatakan sebagai nilai KBM.
Gambar 10. Perbandingan kerjernihan minyak kayu manis dengan kontrol pelarut, kontrol sterilitas media dan kontrol pertumbuhan bakteri.Keterangan: a = kontrol
pelarut; b = kontrol pertumbuhan; 5 - 10% = minyak kayu manis.
a b Gambar 11. Uji penegasan I (a) dan II (b)
Uji penegasan dilakukan untuk memastikan kebenaran nilai KHM dan KBM tersebut. Pada hasil uji penegasan pertama dan penegasan kedua menunjukkan minyak kayu manis 0,08% masih terdapat pertumbuhan bakteri sedangkan minyak kayu manis konsentrasi 0,09% tidak terdapat pertumbuhan bakteri (Gambar 11a dan b). Berdasarkan hasil uji penegasan pertama dan kedua dapat disimpulkan bahwa minyak kayu manis konsentrasi 0,08% dinyatakan
a b 5% 6%
7% 8% 9% 10%
(Gambar 10). Berdasarkan hasil uji dapat disimpulkan bahwa minyak kayu manis konsentrasi 0,06% dinyatakan sebagai nilai KHM dan konsentrasi 0,08% dinyatakan sebagai nilai KBM.
Gambar 10. Perbandingan kerjernihan minyak kayu manis dengan kontrol pelarut, kontrol sterilitas media dan kontrol pertumbuhan bakteri.Keterangan: a = kontrol
pelarut; b = kontrol pertumbuhan; 5 - 10% = minyak kayu manis.
a b Gambar 11. Uji penegasan I (a) dan II (b)
Uji penegasan dilakukan untuk memastikan kebenaran nilai KHM dan KBM tersebut. Pada hasil uji penegasan pertama dan penegasan kedua menunjukkan minyak kayu manis 0,08% masih terdapat pertumbuhan bakteri sedangkan minyak kayu manis konsentrasi 0,09% tidak terdapat pertumbuhan bakteri (Gambar 11a dan b). Berdasarkan hasil uji penegasan pertama dan kedua dapat disimpulkan bahwa minyak kayu manis konsentrasi 0,08% dinyatakan
a b 5% 6%
sebagai nilai KHM dan minyak kayu manis konsentrasi 0,09% dinyatakan sebagai nilai KBM.
D. Pengujian Sifat Fisik dan Stabilitas Pasta Gigi
Pengujian sifat fisik dan stabilitas pasta gigi meliputi organoleptis, pH, viskositas dan daya lekat. Pengujian pada waktu 48 jam berfungsi untuk melihat profil sifat fisik pasta gigi. Pengukuran dilakukan 48 jam sesudah proses pembuatan karena pasta gigi masih dipengaruhi oleh gaya mekanik dari pengadukan saat proses pembuatan pasta gigi. Menurut Garg dkk., (2002) pengukuran pada waktu 48 jam sesudah proses pembuatan memberikan hasil pengukuran yang memiliki keterulangan dan reprodusibilitas yang baik. Pengukuran secara periodik selama 4 minggu berfungsi untuk melihat kestabilan fisik pasta gigi. Pengujian sifat dan kestabilan fisik pasta gigi yang dilakukan meliputi organoleptis, pH, viskositas dan daya lekat.
1. Pengujian organoleptis
sediaan pasta gigi. Berdasarkan hasil uji sifat fisik organoleptis dapat disimpulkan variasi konsentrasi sorbitol mempengaruhi tekstur pasta gigi.
Tabel IV. Hasil uji organoleptis pasta gigi minyak kayu manis
Formula Warna Bau Homogenitas Tekstur
I Putih kekuningan Kayu manis Homogen Sangat kental
II Putih kekuningan Kayu manis Homogen Kental
III Putih kekuningan Kayu manis Homogen Agak kental
IV Putih kekuningan Kayu manis Homogen Agak encer
V Putih kekuningan Kayu manis Homogen Encer
VI Putih kekuningan Kayu manis Homogen Encer
Keterangan :
F I : Konsentrasi sorbitol 9% F II : Konsentrasi sorbitol 9,5% F III : Konsentrasi sorbitol 10% F IV : Konsentrasi sorbitol 10,5% F V : Konsentrasi sorbitol 11% F VI : Konsentrasi sorbitol 11,5%
Pada hasil uji kestabilan fisik organoleptis pasta gigi F I – F VI tidak terjadi perubahan organoleptis. Pasta gigi memiliki warna putih kekuningan, bau khas minyak kayu manis, homogen dan tekstur yang tidak berbeda dengan 48 jam sesudah proses pembuatan pasta gigi. Hal ini berarti sorbitol mampu menjaga kelembaban pada sediaan sehingga tidak terjadi perubahan organoleptis selama penyimpanan.
2. Pengujian pH
SNI (1995) yaitu pasta gigi memiliki pH 4,5 - 10,5. Berdasarkan hasil pengujian pH dapat disimpulkan bahwa peningkatan konsentrasi sorbitol tidak mempengaruhi pH pasta gigi.
Pada hasil uji kestabilan fisik pH pasta gigi, F I – F VI tidak mengalami perubahan pH. Hal ini berarti sorbitol tidak mempengaruhi pH sediaan pasta gigi selama penyimpanan.
3. Pengujian viskositas
Tujuan pengujian viskositas untuk mengetahui kekentalan pasta gigi minyak kayu manis dengan perbedaan konsentrasi sorbitol. Viskositas yang semakin tinggi menggambarkan sediaan yang semakin kental dan sebaliknya. Sediaan yang kental menyebabkan proses penggosokan pada gigi menjadi sulit. Hasil uji sifat fisik viskositas sediaan pasta gigi (Gambar 12) menunjukkan peningkatan konsentrasi sorbitol menyebabkan penurunan viskositas sediaan pasta gigi. Hal ini karena sorbitol berfungsi sebagai levigating agentketika ada pengadukan sistem tidak dapat mengembang karena sorbitol mampu mengisi ruang kosong antar partikel sehingga partikel-partikel tersebut dibasahi/dilumasi oleh sorbitol dan menyebabkan penurunan hambatan alir (Martin dkk., 1983; Kulshreshtha dkk., 2010).
kemampuan sorbitol sudah maksimal untuk mengikat komponen bahan dalam sediaan pasta gigi sehingga penurunan viskositas tidak signifikan.
Gambar 12. Grafik uji viskositas pasta gigi minyak kayu manis
Gambar 13. Grafik uji stabilitas viskositas
Pada hasil uji kestabilan fisik viskositas pasta gigi (Gambar 13) menunjukkan viskositas pada semua formula selama penyimpanan meningkat. Hal ini karena pengukuran secara berulang-ulang selama 4 minggu pada sampel yang sama (dikeluarkan dan dimasukan dalam wadah) menyebabkan
0
kemampuan sorbitol sudah maksimal untuk mengikat komponen bahan dalam sediaan pasta gigi sehingga penurunan viskositas tidak signifikan.
Gambar 12. Grafik uji viskositas pasta gigi minyak kayu manis
Gambar 13. Grafik uji stabilitas viskositas
Pada hasil uji kestabilan fisik viskositas pasta gigi (Gambar 13) menunjukkan viskositas pada semua formula selama penyimpanan meningkat. Hal ini karena pengukuran secara berulang-ulang selama 4 minggu pada sampel yang sama (dikeluarkan dan dimasukan dalam wadah) menyebabkan
9 9,5 10 10,5 11
kemampuan sorbitol sudah maksimal untuk mengikat komponen bahan dalam sediaan pasta gigi sehingga penurunan viskositas tidak signifikan.
Gambar 12. Grafik uji viskositas pasta gigi minyak kayu manis
Gambar 13. Grafik uji stabilitas viskositas
Pada hasil uji kestabilan fisik viskositas pasta gigi (Gambar 13) menunjukkan viskositas pada semua formula selama penyimpanan meningkat. Hal ini karena pengukuran secara berulang-ulang selama 4 minggu pada sampel yang sama (dikeluarkan dan dimasukan dalam wadah) menyebabkan
cairan pada sediaan menguap dan sediaan menjadi mengeras sehingga viskositas meningkat.
Pada hasil uji t berpasangan kestabilan fisik viskositas F I dan F II menunjukan perubahan viskositas berbeda signifikan p-value < 0,05 pada waktu minggu ke 2. F III menunjukan perubahan viskositas berbeda signifikan p-value< 0,05 pada waktu minggu ke 4 . F IV - F VI memiliki viskositas yang stabil. Hal ini berarti semakin tinggi konsentrasi sorbitol maka proses penguapan dari dalam sediaan semakin lambat sehingga stabilitas viskositas sediaan terjaga selama penyimpanan.
4. Pengujian Daya lekat
Daya lekat memiliki peranan yang penting yaitu pada saat pengaplikasian terkait kemampuan melekat pada sikat gigi dan kemampuan penyebaran pada mulut. Hasil uji sifat fisik daya lekat (Gambar 14) menunjukkan peningkatan konsentrasi sorbitol menyebabkan penurunan daya lekat. Hal ini karena sorbitol berfungsi sebagai levigating agent ketika ada pengadukan sistem tidak dapat mengembang karena sorbitol mampu mengisi ruang kosong antar partikel sehingga partikel-partikel tersebut dibasahi/dilumasi oleh sorbitol. Adanya sorbitol yang melumasi partikel-partikel tersebut menyebabkan ikatan antara molekul pasta gigi dengan gelas objek semakin kecil sehingga daya lekat menurun (Martin dkk., 1983; Kulshreshtha dkk., 2010).
-10% memberikan pengaruh yang signifikan terhadap penurunan daya lekat pasta gigi sedangkan pada penambahan berikutnya 10,5 - 11,5% tidak memberikan pengaruh yang signifikan terhadap penurunan daya lekat. Hal ini karena kemampuan sorbitol sudah maksimal untuk mengikat komponen bahan pasta gigi sehingga penurunan daya lekat tidak signifikan.
Gambar 14. Grafik uji daya lekat pasta gigi minyak kayu manis
Pada hasil pengujian kestabilan sifat fisik daya lekat (Gambar 14) menunjukkan terjadi peningkatan daya lekat pada semua formula pasta gigi selama penyimpanan. Hal ini karena pengukuran secara berulang-ulang selama 4 minggu pada sampel yang sama (dikeluarkan dan dimasukkan ke dalam wadah) menyebabkan cairan di dalam sediaan menguap dan sediaan menjadi mengeras. Pada sediaan yang mengeras memiliki ikatan antara molekul pasta gigi dengan molekul kaca gelas objek yang kuat dan menyebabkan daya lekat meningkat. Pada F II minggu ke 2 menuju minggu ke 3 terjadi penurunan daya lekat namun secara statistik penurunan tersebut tidak berbeda bermakna sehingga hal ini dianggap sebagai variasi data.
0
10% memberikan pengaruh yang signifikan terhadap penurunan daya lekat pasta gigi sedangkan pada penambahan berikutnya 10,5 - 11,5% tidak memberikan pengaruh yang signifikan terhadap penurunan daya lekat. Hal ini karena kemampuan sorbitol sudah maksimal untuk mengikat komponen bahan pasta gigi sehingga penurunan daya lekat tidak signifikan.
Gambar 14. Grafik uji daya lekat pasta gigi minyak kayu manis
Pada hasil pengujian kestabilan sifat fisik daya lekat (Gambar 14) menunjukkan terjadi peningkatan daya lekat pada semua formula pasta gigi selama penyimpanan. Hal ini karena pengukuran secara berulang-ulang selama 4 minggu pada sampel yang sama (dikeluarkan dan dimasukkan ke dalam wadah) menyebabkan cairan di dalam sediaan menguap dan sediaan menjadi mengeras. Pada sediaan yang mengeras memiliki ikatan antara molekul pasta gigi dengan molekul kaca gelas objek yang kuat dan menyebabkan daya lekat meningkat. Pada F II minggu ke 2 menuju minggu ke 3 terjadi penurunan daya lekat namun secara statistik penurunan tersebut tidak berbeda bermakna sehingga hal ini dianggap sebagai variasi data.
9,5 10 10,5 11
Konsentrasi Sorbitol (%)
10% memberikan pengaruh yang signifikan terhadap penurunan daya lekat pasta gigi sedangkan pada penambahan berikutnya 10,5 - 11,5% tidak memberikan pengaruh yang signifikan terhadap penurunan daya lekat. Hal ini karena kemampuan sorbitol sudah maksimal untuk mengikat komponen bahan pasta gigi sehingga penurunan daya lekat tidak signifikan.
Gambar 14. Grafik uji daya lekat pasta gigi minyak kayu manis
Pada hasil pengujian kestabilan sifat fisik daya lekat (Gambar 14) menunjukkan terjadi peningkatan daya lekat pada semua formula pasta gigi selama penyimpanan. Hal ini karena pengukuran secara berulang-ulang selama 4 minggu pada sampel yang sama (dikeluarkan dan dimasukkan ke dalam wadah) menyebabkan cairan di dalam sediaan menguap dan sediaan menjadi mengeras. Pada sediaan yang mengeras memiliki ikatan antara molekul pasta gigi dengan molekul kaca gelas objek yang kuat dan menyebabkan daya lekat meningkat. Pada F II minggu ke 2 menuju minggu ke 3 terjadi penurunan daya lekat namun secara statistik penurunan tersebut tidak berbeda bermakna sehingga hal ini dianggap sebagai variasi data.
Gambar 15. Grafik uji stabilitas daya lekat
Pada hasil uji t berpasangan kestabilan fisik daya lekat F I menunjukan perubahan daya lekat yang berbeda signifikanp-value< 0,05 pada minggu ke 1. F II dan F III menunjukan perubahan daya lekat yang berbeda yang signifikanp-value< 0,05 pada minggu ke 3. F IV menunjukan perubahan daya lekat yang berbeda signifikan p-value < 0,05 pada minggu ke 4. F V – F VI memiliki daya lekat yang stabil. Hal ini berarti, semakin tinggi konsentrasi sorbitol maka proses penguapan dari dalam sediaan semakin lambat sehingga stabilitas daya lekat sediaan terjaga selama penyimpanan.
E. Uji Aktivitas Antibakteri Pasta Gigi terhadap BakteriS. mutans dengan Metode Difusi Sumuran
manis 7%. Kontrol positif dan negatif berfungsi untuk mengetahui perbedaan daya antibakteri antara pasta gigi minyak kayu manis dengan basis dan pasta gigi merek “X” yang beredar di pasaran. Minyak kayu manis 7% berfungsi sebagai pembanding aktivitas antibakteri minyak kayu manis sebelum dan sesudah diformulasikan dalam pasta gigi.
Gambar 16. Zona hambat difusi sumuran sampel pasta gigi
Keterangan: A = minyak 7%; B = pasta gigi; C = basis pasta gigi; D = kontrol positif
Pasta gigi minyak kayu manis menghasilkan zona hambat terhadap bakteri S. mutans (Gambar 15). Berdasarkan uji ANAVA menunjukkan peningkatan konsentrasi sorbitol tidak berbeda bermakna secara statistik terhadap peningkatan zona hambat. Hal ini berarti variasi konsentrasi sorbitol tidak berpengaruh terhadap pembentukan zona hambat. Pembentukan zona hambat dipengaruhi oleh zat aktif yang ditambahkan. Pada F I – F VI memiliki konsentrasi zat aktif yang sama.
Tabel V. Pengujian zona hambat pasta gigi
Formula Rata-rata diameter zona hambat (mm) ± SD
Basis Minyak 7% Kontrol positif Pasta Gigi I 1,03 ± 0,02
9,42 ± 0,63 8,55 ± 0,69
7,33 ± 0,20
II 1,01 ± 0,01 7,42 ± 0,21
III 1,01 ± 0,03 8,52 ±1,33
IV 1,02 ± 0,09 8,59 ±0,68
V 1,10 ± 0,03 8,67 ±0,57
VI 1,07 ± 0,07 8,28 ±0,14
D
C B
Pengujian dilanjutkan dengan uji Tukey HSD pada taraf kepercayaan 95% untuk mengetahui perbedaan aktivitas antibakteri. Hasilnya basis pasta gigi memiliki diameter zona hambat yang berbeda bermakna secara statistik dengan pasta gigi minyak kayu manis. Hal ini berarti pasta gigi minyak kayu manis memiliki aktivitas antibakteri yang lebih besar terhadap S. mutans dibandingkan dengan basis pasta gigi. Adanya zona hambat dari basis karena dalam komponen penyusun sediaan yang ditambahkan memiliki aktivitas antibakteri seperti silitol dan metil paraben. Pada F I – F II berbeda bermakna secara statistik dengan kontrol minyak 7% sedangkan F III – F VI berbeda tidak bermakna secara statistik dengan kontrol minyak 7%. Hal ini berarti F III – F VI memiliki aktivitas antibakteri yang sama dengan minyak 7% dalam menghambat pertumbuhan S. mutans. Pasta gigi F II – F VI dapat menggantikan pasta gigi merek “X” yang beredar di pasaran untuk menghambat pertumbuhan S. mutans karena secara statistik tidak berbeda bermakna dengan pasta gigi merek “X”.
F. Uji Iritasi
Siput mengeluarkan mukus sebagai bentuk pertahanan diri terhadap bahan yang bersifat iritan.
Berdasarkan hasil uji (Tabel VI) dapat disimpulkan bahwa pasta F VI mengiritasi berat karena siput mati pada waktu hari pengujian ke dua walaupun menurut Andriens (2006) klasifikasi tingkat iritasi (Tabel II) pada pustaka,range mukus yang dihasilkan tergolong mengiritasi sedang. Siput mati karena konsentrasi minyak kayu manis yang digunakan cukup besar yaitu 7% sedangkan pada hasil pengujian dilusi padat nilai KBM minyak kayu manis adalah sebesar 0,09%. Minyak kayu manis memiliki efek panas sehingga pada waktu pengaplikasian yang lama sehingga dapat mengiritasi membran mukosa (Naha, 2014; Laekeman, 2011). Berdasarkan hasil uji iritasi menggunakan siput tanpa cangkang dapat disimpulkan bahwa pasta gigi yang dihasilkan belum aman untuk digunakan karena mengiritasi berat membran mukosa.
Tabel VI. Hasil uji iritasi
Sampel Mukus (%)
Pasta gigi 23,26 ± 2,92
48 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Peningkatan konsentrasi sorbitol menyebabkan penurunan viskositas dan daya lekat tetapi tidak mempengaruhi pH pasta gigi serta mempengaruhi stabilitas viskositas dan daya lekat namun tidak mempengaruhi stabilitas pH pasta gigi.
2. Pasta gigi minyak kayu manis dapat menghambat bakteriS. mutans. 3. Pasta gigi minyak kayu manis mengiritasi berat membran mukosa.
B. Saran
1. Perlu dilakukan pengujian sifak fisik pasta gigi seperti cohesiveness, extrudability dan sag sehingga dapat dihasilkan pasta gigi yang memenuhi parameter dan karakteristik sifat fisik pasta gigi yang baik.
2. Perlu dilakukan modifikasi konsentrasi minyak kayu manis dalam sediaan pasta gigi agar tidak mengiritasi membran mukosa.
3. Perlu dilakukan uji iritasi lanjutan menggunakan spektrofotometer sehingga dapat diketahui bagian yang mengalami iritasi.