BAB II
TINJAUAN PUSTAKA II.1 EPILEPSI
II.1.1 Definisi
Definisi konseptual : (Kusumastuti dan Basuki, 2014)
Epilepsi adalah kelainan otak yang ditandai dengan kecendrungan untuk menimbulkan bangkitan epileptik yang terus menerus, dengan konsekuensi neurobiologis, kognitif, psikologis, dan sosial. Definisi ini mensyaratkan terjadinya minimal 1 kali bangkitan epileptik.
Bangkitan epileptik adalah terjadinya tanda/gejala yang bersifat sesaat akibat aktifitas neuronal yang abnormal dan berlebihan di otak.
Definisi operasional / definisi praktis dari epilepsi adalah suatu penyakit otak yang ditandai dengan kondisi/gejala berikut :
1. Minimal terdapat 2 bangkitan tanpa provokasi atau 2 bangkitan refleks dengan jarak waktu antara bangkitan pertama dan kedua lebih dari 24 jam 2. Satu bangkitan tanpa provokasi atau 1 bangkitan refleks dengan
kemungkinan terjadinya bangkitan berulang dalam 10 tahun kedepan sama dengan (minimal 60%) bila terdapat 2 bangkitan tanpa provokasi/bangkitan refleks
II.1.2 Epidemiologi
Epilepsi merupakan salah satu penyakit neurologi yang dapat dijumpai pada semua umur dan dapat menyebabkan hendaya serta mortalitas. Insidens epilepsi di negara berkembang sekitar 50 per 100.000 orang per tahun (24-70 per 100.0000 orang per tahun), dan prevalensi yaitu sekitar 4 dan 10 per 100.000 orang (Sander, 2004).
Insiden median epilepsi di dunia 50,4 per 100.000/tahun (33,6-75,6). pada negara dengan pendapatan per kapita yang tinggi, insiden median 45,0 (30,3-66,7) dan pada negara dengan pendapatan per kapita menengah dan rendah adalah 81,7 (28,0-239,5) (Octaviana dan Khosana, 2014).
Prevalensi epilepsi di negara sedang berkembang ditemukan lebih tinggi daripada negara maju. Dilaporkan prevalensi di negara maju berkisar antara 4-7 per 1000 orang dan 5-74 per 1000 orang di negara sedang berkembang. Daerah pedalaman memiliki angka prevalensi lebih tinggi dibandingkan dengan daerah perkotaan yaitu 15,4 per 1000 (4,8-49,6) di pedalaman dan 10,3 (2,8-37,7) di perkotaan. Pada negara maju, prevalensi median epilepsi yang aktif adalah 4,9 per 1000 (2,3-10,3), sedangkan pada negara berkembang di pedalaman 12,7 per 1000 (3,5-45,5) dan diperkotaan 5,9 (3,4-10,2) (Ngugi dkk 2010).
di negara Cina (Shanghai) pada usia 10-30 tahun dan > 60 tahun, sedangkan di India puncaknya pada usia 10-19 tahun (Octaviana dan Khosana, 2014).
Kelompok Studi Epilepsi Perhimpunan Dokter Spesialis Saraf Indonesia (Pokdi Epilepsi PERDOSSI) mengadakan penelitian pada 18 rumah sakit di 15 kota pada tahun 2013 selama 6 bulan. Didapatkan 2288 pasien terdiri dari 487 kasus baru dan 1801 kasus lama. Rerata usia kasus baru adalah 25,1+16,9 tahun, sedangkan rerata usia pada kasus lama adalah 29,2+16,5 tahun. Sebanyak 77,9% pasien berobat pertama kali ke dokter spesialis saraf, 6,8% berobat ke dokter umum, sedangkan sisanya berobat ke dukun dan tidak berobat (Octaviana dan Khosana, 2014).
II.1.3 Klasifikasi
Klasifikasi yang ditetapkan oleh International League Against Epilepsy
(ILAE) terdiri atas dua jenis klasifikasi, yaitu klasifikasi untuk jenis bangkitan epilepsi dan klasifikasi untuk sindrom epilepsi (Kusumastuti dan Basuki, 2014).
Klasifikasi ILAE 1981 untuk tipe bangkitan epilepsi : 1. Bangkitan parsial/fokal
1.1 Bangkitan parsial sederhana 1.1.1 Dengan gejala motorik
1.1.4 Dengan gejala psikis 1.2 Bangkitan parsial kompleks
1.2.1 Bangkitan parsial sederhana yang diikuti dengan gangguan kesadaran
1.2.2 Bangkitan parsial yang disertai gangguan kesadaran sejak awal bangkitan
1.3 Bangkitan parsial yang menjadi umum sekunder 1.3.1 Parsial sederhana yang menjadi umum 1.3.2 Parsial kompleks yang menjadi umum
1.3.3 Parsial sederhana menjadi parsial kompleks, lalu menjadi umum
2. Bangkitan umum 2.1 Lena (absence)
2.1.1 Tipikal Lena 2.1.2 Atipikal Lena 2.2 Mioklonik
2.3 Klonik 2.4 Tonik
2.5 Tonik-klonik 2.6 Atonik/astatik
Klasifikasi ILAE 1989 untuk epilepsi dan sindrom epilepsi : 1. Fokal/partial (localized related)
1.1 Idiopatik (berhubungan dengan usia awitan)
1.1.1 Epilepsi benigna dengan gelombang paku di daerah sentrotemporal (childhood epilepsy with centrotemporal spikes)
1.1.2 Epilepsi benigna dengan gelombang paroksismal pada daerah oksipital
1.1.3 Epilepsi primer saat membaca (primary reading epilepsy) 1.2 Simtomatis
1.2.1 Epilepsi parsial kontinua yang kronik progresif pada anak-anak (Kojenikow’s Syndrome)
1.2.2 Sindrom dengan bangkitan yang di presipitasi oleh suatu rangsangan
2. Epilepsi umum 2.1 Idiopatik
2.1.1 Kejang neonatus familial benigna 2.1.2 Kejang neonatus benigna
2.1.3 Kejang epilepsi mioklonik pada bayi 2.1.4 Epilepsi lena pada anak
2.1.5 Epilepsi lena pada remaja 2.1.6 Epilepsi mioklonik pada remaja
2.1.7 Epilepsi dengan bangkitan umum tonik-klonik pada saat terjaga
2.1.8 Epilepsi umum idiopatik lain yang tidak termasuk salah satu diatas
2.1.9 Epilepsi tonik-klonik yang dipresipitasi dengan aktivasi yang spesifik
2.2 Kriptogenik atau simtomatis 2.2.1 Sindrom West
2.3 Simtomatis
2.3.1 Etiologi nonspesifik
• Ensefalopati mioklonik dini
• Ensefalopati pada infantil dini dengan burst supression
• Epilepsi simtomatis umum lainnya yang tidak termasuk di
atas
2.3.2 Sindrom spesifik
2.3.3 Bangkitan epilepsi sebagai komplikasi penyakit lain 3. Epilepsi dan sindrom yang tak dapat ditentukan fokal atau umum
3.1 Bangkitan umum dan fokal 3.1.1 Bangkitan neonatal
3.1.2 Epilepsi mioklonik berat pada bayi
3.1.3 Epilepsi dengan gelombang paku kontinu selama tidur dalam
3.1.4 Epilepsi afasia yang didapat (Sindrom Landau Kleffner) 3.1.5 Epilepsi yang tidak termasuk dalam klasifikasi di atas 3.2 Tanpa gambaran tegas fokal atau umum
4. Sindrom khusus
4.1 Bangkitan yang berkaitan dengan situasi tertentu 4.1.1 Kejang demam
4.1.3 Bangkitan yang hanya terjadi bila terdapat kejadian metabolik akut, atau toksis, alkohol, obat-obatan, eklamsia, hiperglikemi nonketotik
4.1.4 Bangkitan berkaitan dengan pencetus spesifik (epilepsi reflektorik)
Etiologi epilepsi dapat dibagi ke dalam tiga kategori, sebagai berikut : 1. Idiopatik : Tidak terdapat lesi struktural di otak atau defisit neurologis.
Diperkirakan mempunyai predisposisi genetik dan umumnya berhubungan dengan usia.
2. Kriptogenik : dianggap simtomatis tetapi penyebabnya belum diketahui. Termasuk disini adalah Sindrom West, Sindrom Lennox-Gastaut dan epilepsi mioklonik. Gambaran klinik sesuai dengan ensefalopati difus.
II.2 OBAT ANTI EPILEPSI
Sejak tahun 1912 beberapa OAE telah di kenalkan namun hanya beberapa yang sering digunakan. Sebagian besar pasien epilepsi di terapi dengan 4 macam OAE, yaitu : fenobarbital, fenitoin, karbamazepin, dan asam valproat(Ambrosio dkk, 2002).
Sampai dengan tahun 1993, OAE utama yaitu fenobarbital, fenitoin, karbamazepin, dan asam valproat. Kemudian terdapat beberapa OAE lainnya, dengan prinsip farmakoterapi yang lebih baik. Obat Anti Epilepsi generasi terbaru disebut juga dengan OAE generasi kedua dan ketiga (Conway, 2012).
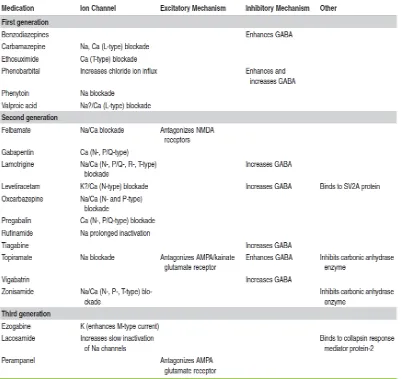
Sebagian besar mekanisme kerja OAE sebagai antikonvulsan tidak dapat dimengerti sepenuhnya. Mekanisme utama OAE yaitu menurunkan eksitasi dari neuron dengan cara memblok saluran sodium dan saluran kalsium atau reseptor glutamat antagonis. Beberapa jenis OAE dapat meningkatkan gamma amino butyric acid (GABA). Mekanisme kerja dari beberapa OAE dapat dilihat pada tabel 1 (Conway, 2012).
Tabel 1. Mekanisme Kerja Obat Anti Epilepsi
Dikutip dari : Conway, J.M. 2012. Antiepilepsy Drugs : Mechanisms of Action and Pharmacokinetics. Epilepsy.1(5): 1-11
jenis lainnya. Namun apabila OAE pertama memberikan efikasi dan toleransi yang minimal, maka dikombinasikan dengan OAE lainnya (Sander, 2004).
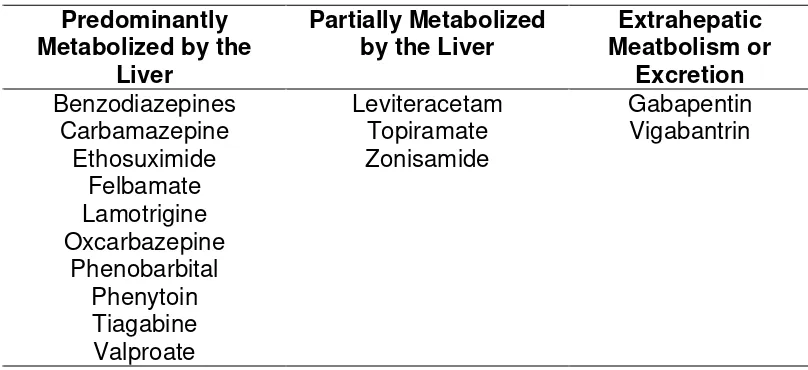
Sebagian besar OAE mengalami biotransformasi hepatik, kecuali Gabapentin dan Vigabantrin (Tabel 2). Obat-obat anti epilepsi lipofilik mengalami konversi menjadi hidrofilik untuk ekskresi ginjal. Proses-proses tersebut terdiri dari reaksi fase I dan fase II. Reaksi fase I terdiri dari oksidasi, reduksi dan hidroksilasi, sementara pada fase II yaitu konjugasi (Ahmed dan Siddiqi, 2006).
Tabel 2. Metabolisme Obat Anti Epilepsi Predominantly
Dikutip dari : Ahmed, S.N., Siddiqi, Z.A. 2006. Antiepileptic Drugs and Liver Disease.15: 156-164
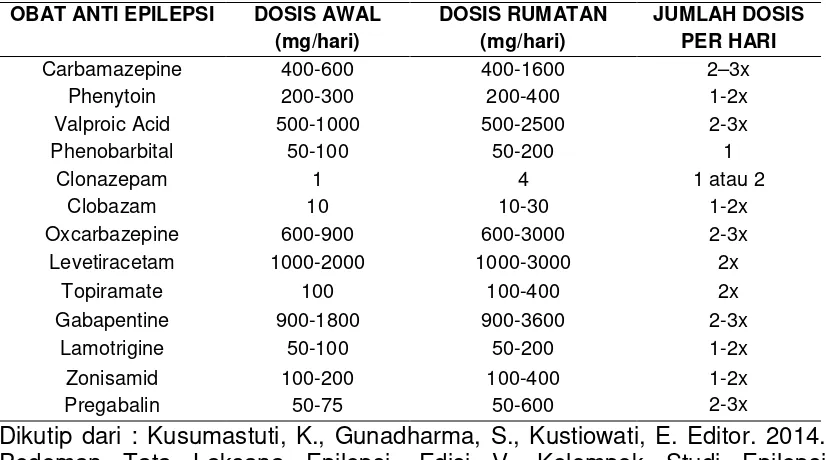
efek samping (Tabel 3). Bila dengan penggunaan OAE pertama dosis maksimum tidak dapat mengontrol bangkitan, maka diganti dengan OAE kedua. Caranya bila OAE kedua telah mencapai kadar terapi, maka OAE pertama, diturunkan bertahap (tappering off). Bila terjadi bangkitan saat penurunan OAE pertama, maka kedua OAE tetap diberikan. Bila respons yang didapat buruk, kedua OAE harus diganti dengan OAE yang lain. Penambahan OAE ketiga baru dilakukan bila terdapat respons dengan OAE kedua, tetapi respons tetap sub optimal walaupun penggunaan kedua OAE pertama sudah maksimal. Obat Anti Epilepsi kedua harus memiliki mekanisme kerja yang berbeda dengan OAE pertama (Gunadharma dkk, 2014).
Tabel 3. Dosis Obat Anti Epilepsi untuk Orang Dewasa OBAT ANTI EPILEPSI DOSIS AWAL
(mg/hari)
DOSIS RUMATAN (mg/hari)
JUMLAH DOSIS PER HARI
Carbamazepine 400-600 400-1600 2–3x
Phenytoin 200-300 200-400 1-2x
Valproic Acid 500-1000 500-2500 2-3x
Phenobarbital 50-100 50-200 1
Clonazepam 1 4 1 atau 2
Clobazam 10 10-30 1-2x
Oxcarbazepine 600-900 600-3000 2-3x
Levetiracetam 1000-2000 1000-3000 2x
Topiramate 100 100-400 2x
Gabapentine 900-1800 900-3600 2-3x
Lamotrigine 50-100 50-200 1-2x
Zonisamid 100-200 100-400 1-2x
2-3x
Pregabalin 50-75 50-600
Dikutip dari : Kusumastuti, K., Gunadharma, S., Kustiowati, E. Editor. 2014. Pedoman Tata Laksana Epilepsi. Edisi V. Kelompok Studi Epilepsi PERDOSSI. Airlangga University Press. Surabaya.
Tabel 4. Obat-obatan yang Dapat Meningkatkan Konsentrasi Serum OAE
II.3 KARBAMAZEPIN
Karbamazepin (C15H12N2O) merupakan senyawa trisiklik yang cukup efektif dalam mengobati kejang parsial. Obat ini pertama kali diperkenalkan oleh Walter Schindler di Switzerland pada tahun 1953. Karbamazepin pertama kali digunakan untuk mengobati trigeminal pada tahun 1962 dan kemudian digunakan secara luas untuk mengobati epilepsi di Inggris pada tahun 1965, lalu pada tahun 1974 diakui pemakaiannya di Amerika Serikat (Ghamari dkk, 2013).
Karbamazepin (5H-dibenzapine-5-carboxamide) merupakan OAE yang sering digunakan untuk mengobati epilepsi. Karbamazepin merupakan derivat iminodibenzyl, yang secara struktural mirip dengan antidepresan trisiklik. Obat ini dimetabolisasi di hepar, dan hanya sekitar 1% dari dosis yang diberikan yang di ekskresikan dalam bentuk yang asli (Gambar 1) (Ambrosio dkk, 2002).
Gambar 1. Struktur formula dari Karbamazepin
Secara umum, karbamazepin dapat menurunkan eksitabilitas neuron atau meningkatkan inhibisi dengan mengganggu konduktansi sodium, potasium atau kalsium atau mempengaruhi GABA, glutamat atau neurotransmiter lainnya yang berperan dalam mencetuskan kejang (Ghamari dkk, 2013).
Ikatan protein plasma karbamazepin mencapai 70-80% dan eliminasi tergantung sepenuhnya pada biotransformasi hepatik melalui proses eksposidasi dan hidroksilasi. Eliminasi karbamazepin terutama oleh sistem sitokrom P-450 dan menghasilkan metabolit aktif, kemudian karbamazepin mengalami autoinduksi. Clearance karbamazepin terjadi pada 30 hari setelah terapi dan meningkat hingga 300%. Waktu paruh karbamazepin sekitar 10 sampai dengan 20 jam, namun dikurangi dengan autoinduksi 4-12 jam (Ghamari dkk, 2013).
Efek samping karbamazepin yaitu dizziness, ataksia, diplopia, mual, kelelahan, agranulositosis, lekopeni, trombositopenia, hiponatremia, ruam, gangguan perilaku, tiks, peningkatan berat badan, disfungsi seksual, neuropati perifer (Gunadarma dkk, 2014).
Karbamazepin dapat berinteraksi dengan OAE lainnya seperti asam valproat, fenobarbital, fenitoin. Obat-obatan lain yang dapat berinteraksi dengan karbamazepin, seperti antibiotik yaitu eritromisin, cimetidine, propoxyphene, pil hormon kontrasepsi dan calcium channel blockers
II.4 ASAM VALPROAT
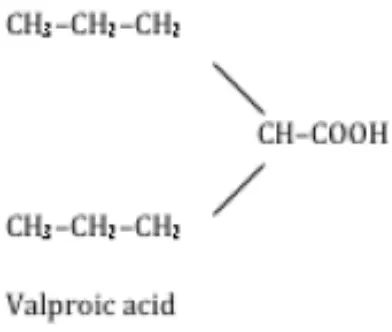
Asam valproat diperkenalkan oleh Carraz (1964) sebagai antiepilepsi dan digunakan secara luas di Amerika Serikat sejak tahun 1978. Asam valproat merupakan OAE spektrum luas yang efektif untuk berbagai tipe kejang dan sebagai pilihan pertama untuk epilepsi simtomatik dan epilepsi umum idiopatik (Gambar 2) (Fagundes,2008).
Asam valproat memiliki efek farmakologik dengan meningkatkan transmisi GABAergik, mengurangi pelepasan dan efek asam amino eksitatori, memblokade sodium chanel dan memodulasi transmisi dopaminergik dan serotonergik (Fagundes,2008).
Asam valproat tersedia dalam bentuk parenteral dan oral. Sekitar 90% asam valproat berikatan dengan protein plasma. Asam valproat dimetabolisasi secara luas oleh konjugasi mikrosom glukoronidasi, beta-oksidasi mitokondria dan sitokrom P450-dependent omega, oksidasi (omega-1) dan (omega-2) (Fagundes,2008).
Efek samping utama yaitu mual, muntah, abdominal cramps serta diare. Efek samping lainnya yaitu hepatotoksisitas dan pankreatitis (Fagundes,2008).
Gambar 2. Struktur formula dari Asam Valproat
Dikutip dari : Fagundes, S.B.R. 2008. Valproic Acid : Review. Rev Neuroscience. 16(2): 130-136
II.5 FUNGSI TIROID
Biosintesis hormon tiroid dimulai dengan pengambilan unsur yodium dari plasma dan berakhir dengan sekresinya ke dalam darah, dengan menempuh beberapa langkah yaitu : trapping, oksidasi dan yodinasi,
coupling, penyimpanan, deyodinasi, proteolisis dan sekresi hormon (Kshanti, 2008).
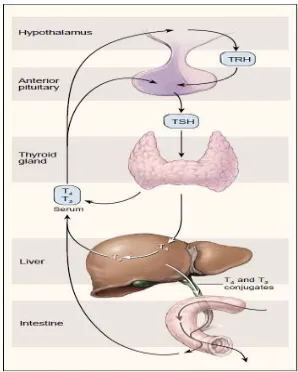
Sekresi kelenjar tiroid yang normal tergantung pada TSH. Sekresi TSH lalu di inhibisi oleh hormon tiroid dan di stimulasi oleh Thyrotropin Releasing
Hormone (TRH). Iodida dalam serum terjebak didalam sel tiroid, setelah
mengalami okidasi dan bereaksi dengan beberapa residu tyrosine dari tiroglobulin, kemudian membentuk T4 danT3 (Gambar 3) (Wood, 1995).
Gambar 3. Hypothalamic-Pituitary-Thyroid Axis dan Jalur Ekstratiroid dari metabolisme hormon tiroid
Dikutip dari : Wood, A.J.J. 1995. Drug Therapy. The New England Journal of Medicine. 333(25): 1688-1693
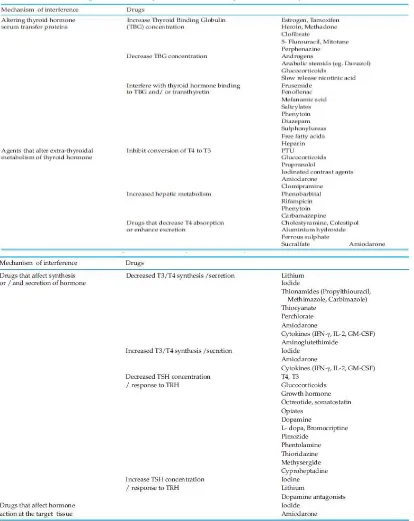
mulai dari sintesis, sekresi, transportasi atau pada organ target sehingga menyebabkan hipotiroidsm atau hipertiroidsm. Obat-obatan dapat juga mengubah konsentrasi serum hormon tiroid dengan cara mempengaruhi jumlah ikatan protein atau jumlah yang berikatan dengan hormon, sehingga dapat memodifikasi uptake selluler dan metabolisme hormon tiroid serta mengganggu kerja hormon pada jaringan. Beberapa obat yang dapat mempengaruhi fungsi tiroid dapat dilihat pada tabel 5 (George dan Joshi, 2007).
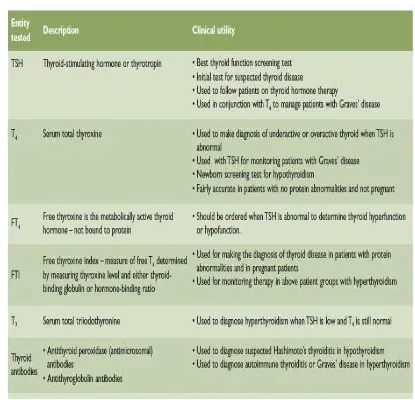
II.5.1 Tes Fungsi Tiroid
Tes fungsi tiroid adalah pemeriksaan penunjang pada kelainan tiroid yang dikelompokkan menjadi pemeriksaan untuk melihat status hormon tiroid, respons tiroid, etiologi kelainan tiroid, dan pemeriksaan khusus. Pemeriksaan untuk melihat status hormon tiroid dan respons tiroid meliputi T3, T4, free thyroxine (FT4), free triiodothyronine (FT3), dan TSH (Saksono, 2008).
Tabel 5. Obat-obatan yang dapat mempengaruhi Fungsi Tiroid
Tabel 6. Pemeriksaan Darah untuk menilai Fungsi Tiroid
Dikutip dari : Gunder, L.M., Haddow, S. 2009. Laboratoty Evaluation of
Thyroid Function. Diunduh dari :
II.5.2 Triiodothyronine (T3)
Triiodothyronine serum dapat digunakan sebagai komponen untuk
penapisan kelainan tiroid. Secara klinik, konsentrasi T3 memiliki nilai diagnosis untuk kelainan hipertiroid dan pemantauan perbaikan kondisi tiroid. Pada kelainan T3-Tirotoksikosis, dimana kadar T3 meningkat, tetapi T4 dan FT4 normal, kadar T3 menjadi faktor dominan untuk menilai status tiroid. Tetapi pada defisiensi iodium, seringkali ditemukan sedikit peningkatan T3, menunjukkan bahwa pasien tersebut dalam status eutiroid (Saksono, 2008).
Kadar T3 dipengaruhi oleh kondisi yang berhubungan dengan konsentrasi Thyroid Binding Globulin (TBG). Triiodothyronine sedikit meningkat pada kehamilan dan pasien dengan terapi estrogen.
Triiodothyronine dapat menurun pada keadaan sakit berat, malnutrisi, gagal ginjal (Saksono, 2008).
Serum total T3 normal pada dewasa sekitar 80-190 ng/dL.
Triiodothyronine menggambarkan fungsional dari jaringan perifer
dibandingkan dengan keadaan sekretori kelenjar tiroid. Sebagai tambahan, T3 juga dapat digunakan pada kasus tiroid adenoma (Shivaraj dkk, 2009).
II.5.3 Free Triidothyronine (FT3)
Free Triiodothyronine kurang lebih 0,2-0,4% dari total T3,
menggambarkan hormon tiroid yang aktif secara fisiologi. Pada umumnya FT3 meningkat lebih banyak dibandingkan FT4 pada penyakit Graves dan adenoma toksik. Serum FT3 sangat penting untuk membedakan kelainan-kelainan tersebut (Saksono, 2008).
Nilai normal FT3 yaitu 2,3-5,0 pg/mL (35-77 pmol/L) (Carvalho dkk, 2013).
II.5.4 Thyroxine (T4)
Secara umum, serum T4 menggambarkan 90% sirkulasi hormon tiroid.
Thyroxine dalam darah terdapat dalam dua bentuk : T4 berikatan dengan
protein dan FT4 (tidak berikatan dengan protein). Fraksi FT4 hanya 5% dari total T4, namun FT4 merupakan bentuk metabolit aktif dari hormon (Gunder dan Haddow, 2009).
Peningkatan T4 didapatkan pada pasien hipertiroid, dan menurun pada pasien hipotiroid. Kadar T4 berkaitan secara patologi dan fisiologi dengan kadar kapasitas TBG. Beberapa obat berkompetisi ikatan dengan TBG, sehingga kadar T4 menjadi rendah. kadar T4 pada neonatus lebih tinggi dari orang dewasa (Saksono, 2008).
II.5.5 Free Thyroxine (FT4)
Free Thyroxine adalah fraksi T4 yang tidak terikat pada TBG.
Konsentrasi FT4 ini dapat diukur secara langsung dan tidak langsung sebagai Free Thyroxine Index (FTI). Pengukuran langsung FT4 lebih lazim digunakan untuk melihat kadar FT4. Pengukuran FT4 terbaik adalah dengan menggunakan metode equilibrium dialisis. Hanya FT4 yang tidak terikat pada TBG yang akan melewati membran. Jumlah FT4 yang melewati membran akan diukur konsentrasinya sebagai FT4. Secara keseluruhan jumlah FT4 didalam sirkulasi hanya 0,02 bagian dari keseluruhan T4 (Saksono, 2008).
II.5.6 Thyroid Stimulating Hormone (TSH)
Secara fisiologis, TSH yang dihasilkan kelenjar hipofisis akan meningkat atau menurun untuk mempertahankan kadar hormon tiroid (Saksono, 2008).
Thyroid Stimulating Hormone memiliki nilai normal sekitar 0,5-4,5 mU/L. The American Association of Clinical Endocrinologists (AACE) pada tahun 2003 menetapkan nilai TSH 0,3-3,0 mU/L (Shivaraj dkk, 2009).
Endokrinologis memakai pemeriksaan TSH sebagai pemeriksaan primer untuk diagnosa dan manajemen penyakit tiroid. Dalam menilai fungsi tiroid, pemeriksaan TSH atau T4 sebagai pemeriksaan dasar yang cukup adekuat dalam menetapkan status hormon tiroid pada pasien (Shivaraj dkk, 2009).
Pada hipotiroid primer, T3 dan T4 rendah sedangkan TSH meningkat secara bermakna. Sedangkan pada hipertiroid primer, kadar hormon-hormon tiroid meningkat, sedangkan TSH seringkali tidak terdeteksi (Saksono, 2008).
II.6 FUNGSI HATI
berlebihan dan kadang pada rentang dosis terapetik juga dapat merusak organ. Lebih dari 900 obat-obatan diimplikasikan dapat merusak hepar. Beberapa obat-obatan dapat menyebabkan kerusakan subklinik yang bermanifestasi pada abnormal tes enzim hepar (Pandit, 2012).
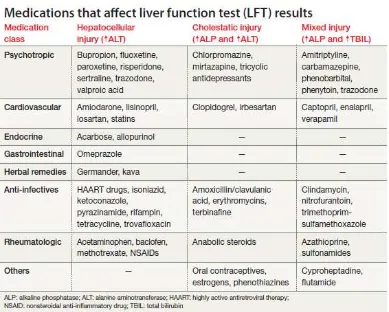
Medikasi merupakan penyebab peningkatan enzim hepar yang sering dijumpai, salah satunya yaitu antikonvulsan yang dapat menyebabkan peningkatan bilirubin, ALP, ALT (Tabel 7) (Fancher dkk, 2007).
Tabel 7. Medikasi yang dapat mempengaruhi Tes Fungsi Hati
II.6.1 Tes Fungsi Hati
Pemeriksaaan kimia darah digunakan untuk mendeteksi kelainan hati, menentukan diagnosis, mengetahui berat ringannya penyakit, mengikuti perjalanan penyakit dan penilaian hasil pengobatan. Pengukuran kadar bilirubin serum, AST, ALT, ALP, GGT, dan albumin sering disebut sebagai tes fungsi hati atau Liver Function Test. Pada banyak kasus, tes-tes ini dapat mendeteksi penyakit hati dan empedu asimtomatik sebelum munculnya manifestasi klinik. Tes-tes ini dapat dikelompokkan dalam 3 kategori utama, antara lain : (Amirudin, 2007)
1. Peningkatan aminotransferase, ALT, dan AST biasanya mengarah pada perlukaan hepatoselular atau inflamasi
2. Keadaan patologis yang mempengaruhi sistem empedu intra dan ekstrahepatik dapat menyebabkan peningkatan ALP dan GGT
3. Kelompok ketiga merupakan kelompok yang mewakili fungsi sintesis hati, seperti produksi albumin, urea dan faktor pembekuan.
dari hepar dan tulang. Bila kadar ALP meningkat secara menetap mengindikasikan kolestasis kronik atau penyakit hati infiltratif (Fancher dkk, 2007).
Nilai normal tes fungsi hati untuk bilirubin 5-18 μmol/L, ALP 30-130 IU/L, AST 5-40 IU/L, ALT 5-35 IU/L, GGT 5-50 IU/l (Amirudin, 2007).
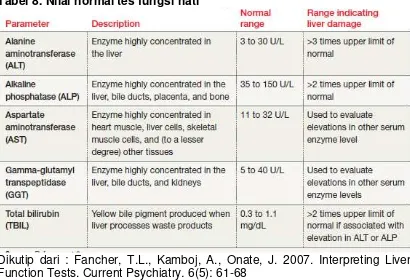
Pemeriksaan standard untuk tes fungsi hati meliputi ALT, AST, ALP, total bilirubin, albumin, dan total protein. Selain itu juga dinilai GGT dan PT. Nilai normal dan interpretasi dari tes fungsi hati dapat dilihat pada tabel 7 (Fancher dkk, 2007).
Tabel 8. Nilai normal tes fungsi hati
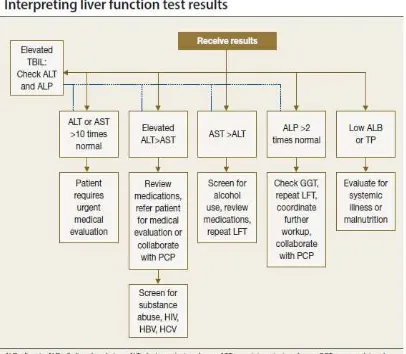
Untuk menilai hasil dari fungsi hati harus berdasarkan gejala pasien, pemeriksaan fisik, riwayat medik, riwayat penyakit dahulu dan riwayat pemakaian obat. Interpretasi dari hasil tes fungsi hati dapat dilihat pada gambar 4 (Fancher dkk, 2007).
Injury pada hepar didefinisikan apabila : (Fancher dkk, 2007) a. Kadar ALT meningkat >3 kali dari batas atas nilai normal b. Kadar ALP meningkat >2 kali dari batas atas nilai normal
c. Kadar bilirubin meningkat >2 kali dari batas atas nilai normal, bila berhubungan dengan peningkatan kadar ALT atau ALP
Bila peningkatan kadar ALT predominan, dianggap sebagai suatu
injury hepatoseluler. Bila peningkatan kadar ALP predominan, maka
Gambar 4 . Interpretasi Hasil Tes Fungsi Hati
Dikutip dari : Fancher, T.L., Kamboj, A., Onate, J. 2007. Interpreting Liver Function Tests. Current Psychiatry. 6(5): 61-68
II.6.2 Bilirubin
UDP-glucoronyltransferase. Serum bilirubin total yang normal bervariasi dari 2 sampai 21 μmol/L. Bilirubin tidak langsung (tak terkonjugasi) kurang dari 12
μmol/L dan bilirubin langsung (terkonjugasi) kurang dari 8 μmol/L (Gowda
dkk, 2009).
Kadar serum bilirubin lebih dari 17 μmol/L menunjukkan penyakit hati
dan kadar serum bilirubin lebih dari 24 μmol/L mengindikasikan tes laboratorium hati abnormal. Jaundice terjadi bila konsentrasi bilirubin sekitar
40 μmol/L, dan dapat dilihat pada sklera, kulit, dan membran mukosa.
Hiperbilirubinemia tak terkonjugasi dapat terjadi oleh karena produksi bilirubin secara berlebihan, penurunan pengambilan hati atau konjugasi atau keduanya. Pada hepatitis viral, kerusakan hepatoseluler, kerusakan hati iskemik atau oleh karena toksin dapat dijumpai kadar serum bilirubn terkonjugasi yang lebih tinggi (Gowda dkk, 2009).
II.6.3 Alkaline Phosphatase (ALP)
Alkaline Phosphatase dapat dijumpai pada mukosa epitel dari usus
kadar ALP. Penyakit lain seperti penyakit infiltratif hati, abses, penyakit hati granulomatosus dan amyloidosis dapat menyebabkan penigkatan kadar ALP (Gowda dkk, 2009).
II.6.4 Aspartate Amino Transferase (AST)
Aspartate Amino Transferase mengkatalis reaksi transaminasi.
Aspartate Amino Transferase terdapat dalam 2 bentuk isoenzim yang
berbeda secara genetik, yaitu bentuk mitokondria dan sitoplasmik. Aspartate Amino Transferase ditemukan dalam konsentrasi tertinggi yaitu di jantung, dibandingkan dengan jaringan lain dalam tubuh seperti hati, otot rangka dan ginjal. Peningkatan kadar AST mitokondria terlihat pada jaringan nekrosis yang luas selama infark miokard dan juga penyakit hati kronik. Sekitar 80% dari aktivitas AST hati merupakan kontribusi dari isoenzim mitokondria, sedangkan sebagian besar aktivitas sirkulasi AST pada orang normal berasal dari isoenzim sitosolik. Perubahan kadar AST biasanya dijumpai pada pasien sirosis hati dan juga penyakit hati lainnya dengan kadar ALT yang juga meningkat (Gowda dkk, 2009).
II.6.5 Alanine Amino Transferase (ALT)
dari reaksi transaminasi. Pada setiap cedera sel hati dapat meningkatkan kadar ALT. Peningkatan kadar ALT lebih dari 300 U/L dianggap tidak spesifik. Peningkatan kadar ALT lebih dari 500 U/L sering dijumpai pada penyakit yang mengenai hepatosit secara primer seperti hepatitis viral, kerusakan hati iskemik, dan kerusakan hati yang disebabkan oleh toksin. Meskipun terdapat hubungan antara peningkatan kadar ALT yang sangat tinggi dan spesifitas untuk penyakit hepatoseluler, puncak absolut dari peningkatan ALT tidak berhubungan dengan luasnya kerusakan sel hati. Virus hepatitis seperti A,B,C,D, dan E dapat menyebabkan peningkatan kadar ALT. Bila peningkatan kadar ALT menetap hingga lebih dari 6 bulan setelah hepatitis akut maka didiagnosa sebagai hepatitis kronik (Gowda dkk, 2009).
II.6.6 Gamma Glutamyl Transferase (GGT)
Gamma Glutamyl Transferase merupakan enzim mikrosomal yang
hepatitis C kronik. Peningkatan kadar serum GGT hingga lebih dari 10 kali dapat dijumpai pada alkoholisme. Serum GGT juga dapat sebagai marker awal dari stres oksidatif (Gowda dkk, 2009).
II.7 RISIKO KARBAMAZEPIN TERHADAP FUNGSI TIROID
Karbamazepin mempunyai efek terhadap fungsi tiroid, yaitu penurunan konsentrasi hormon tiroid. Hal ini disebabkan oleh karbamazepin sebagai OAE generasi lama mengandung zat yang dapat merangsang enzim yang dapat meningkatkan metabolisme glukoronide dari hormon tiroid (Anderson, 2004).
dari konsentrasi serum hormon tiroid selama terapi karbamazepin masih belum diketahui pasti (Verotti dkk, 2009).
Cytochrome P450 complex (CYP3A) mengandung enzim-enzim yang
berperan pada oksidatif dan mengurangi reaksi. Dimana beberapa dari enzim-enzim tersebut dapat di induksi oleh karbamazepin. Kemudian menghasilkan produk khusus yang dapat mereduksi kadar hormon tiroid (George dan Joshi, 2007).
Karbamazepin dapat mempercepat metabolisme dari hormon tiroid dengan cara menginduksi sistem enzim hepatik P450 yang kemudian menyebabkan peningkatan metabolisme hormon-hormon tiroid dan mengganggu hormon tiroid berikatan dengan tiroid-globulin (Yilmaz dkk, 2014).
Kadar hormon tiroid (T4 dan T3) menurun pada 14 hari setelah mendapat terapi karbamazepin (400mg/hari) pada subjek yang sehat. Hal ini sesuai dengan rentang waktu dari kerja enzim yang terkandung dalam karbamazepin (Anderson, 2004).
II.8 RISIKO KARBAMAZEPIN TERHADAP FUNGSI HATI
Karbamazepin dapat menginduksi enzim sehingga meningkatkan GGT dan mempengaruhi ALP. Karbamazepin dapat menyebabkan kolestatik dan
injury hepatoseluler, serta pembentukan granuloma di hepar. Metabolit
dan hepatotoksik karbamazepin. Pada studi metabolisme invitro
menggunakan inhibitor enzim dan enzim murni mengindikasikan adanya pembentukan epoksid stabil dan metabolit reaktif, yang tergantung pada CYP 3A4. Secara invivo, karbamazepin sendiri dapat menginduksi metabolitnya melalui CYP 3A4 serta pembentukan metabolit 2 dan 3 cincin hidroksil, yang kemudian berubah menjadi oksida arene sementara yang tidak stabil, dimana bentuk ini dapat menyebabkan pembentukan hapten (Pandit dkk, 2012).
Biotransformasi hepatik merupakan jalur eliminasi utama dari karbamazepin. Epoksidasi dan hidroksilasi merupakan jalur metabolik dan reaksi konjugasi yang berperan. Hasil metabolik utama yaitu 10,11-CBZ epoksida merupakan bentuk aktif secara farmakologik. Karbamazepin dapat menginduksi metabolismenya sendiri (autoinduction) yang dimulai dalam 24 jam pertama setelah terapi awal dan selesai dalam > 3-5 minggu dari terapi. Reaksi hepatotoksik biasanya dijumpai dalam 3-4 minggu setelah dimulai terapi dan tidak tergantung pada kadar serum karbamazepin. Gejala hepatotoksik biasanya membaik setelah obat dihentikan (Ahmed dan Siddiqi, 2006).
tersebut menyebabkan toksisitas hematologik dan hepatotoksisitas (Sabariah dkk, 2014).
II.9 RISIKO ASAM VALPROATTERHADAP FUNGSI TIROID
Pada penelitian terakhir dilaporkan bahwa asam valproat dapat mempengaruhi fungsi tiroid pada pemakaian lebih dari 6 bulan. Diduga asam valproat dapat menginhibisi somatostatin, yang merupakan inhibitor utama dari sekresi TSH melalui GABA (Turan dkk, 2013).
Diduga asam valproat dapat mempengaruhi fungsi tiroid dengan cara menginduksi sistem enzim mikrosom. Asam valproat mengalami metabolisasi di hepar melalui konjugasi glukoronide dan oksidasi, yang kemudian mempengaruhi kadar hormon tiroid dengan jalan menganggu jalur metabolik hepatik (Teleanu dkk, 2013).
Salah satu hipotesis menyebutkan bahwa pada pasien-pasien yang menggunakan asam valproat mengalami inhibisi somatostatin, yang merupakan inhibitor penting dalam sekresi TSH melalui stimulasi GABA. Selain itu, asam valproat juga menyebabkan defisiensi selenium dan zinc, yang berhubungan dengan kejadian hipotiroidsm subklinik (Turan dkk, 2014).
Asam valproat dapat mempengaruhi TSH, diduga oleh karena asam valproat menyebabkan peningkatan GABA, yang berpengaruh pada kelenjar pituitari dalam menghambat sekresi TSH (Gracious dkk, 2004).
II.10 RISIKO ASAM VALPROATTERHADAP FUNGSI HATI
Asam valproat sudah sejak lama diketahui dapat menyebabkan hepatotoksisitas akut. Terdapat 2 tipe asam valproat dalam menyebabkan hepatotoksisitas. Tipe pertama yaitu perubahan kadar serum enzim hati dan rendahnya kadar plasma fibrinogen yang tergantung pada dosis dari asam valproat, dimana kondisi ini kembali normal setelah asam valproat dihentikan. Tipe kedua yaitu reaksi idiosinkratik reversible, namun jarang ditemukan (Koenig dkk,2006).
yang diinduksi oleh asam valproat, defisiensi carnitine, gangguan metabolisme dan stres oksidatif sebagai akibat aktifitas radikal bebas (Silva dkk, 2008).
Beberapa mekanisme asam valproat dalam menyebabkan hepatopati
yaitu inhibisi dari oksidasi β dan posforilasi oksidatif, inhibisi glukoneogenesis
dan sintesis urea, efek steatogenik dan penurunan carnitine intraselluler. Reduksi CoA interselluler merupakan jalur sentral utama dari asam valproat dalam menyebabkan hepatotoksisitas (Koenig dkk,2006).
Asam valproat merupakan OAE yang telah dipakai secara luas. Asam valproat biasanya dapat ditoleransi dengan baik, namun perubahan pada fungsi hati dijumpai dapat dijumpai pada 20% pasien. Hipotesis tentang mekanisme toksisitas asam valproat yaitu keterlibatan asam valproat dengan
oksidasi β dari lipid endogen. Asam valproat membentuk konjugasi ester
dengan carnitine yang pada akhirnya menyebabkan defisiensi carnitine
sekunder. Pada beberapa studi invitro mengindikasikan bahwa derivat tioester dari asam valproat dan koenzim A dapat dijumpai dalam bentuk metabolik sementara pada jaringan hepar. Deplesi dari koenzim A atau asam valproat CoA ester sendiri dapat bertanggungjawab pada inhibisi dari metabolisme mitokondria, pengurangan ATP dan akhirnya menyebabkan kematian sel (Pandit dkk, 2012).
Mekanisme hiperammonemia tersebut dapat merupakan suatu keadaan kerusakan hepatik akut, namun dapat juga dijumpai pada terapi asam valproat akut. Idiosinkratik toksisitas hepatik terhadap asam valproat biasanya terjadi dalam 2-3 bulan pertama terapi (Ahmed dan Siddiqi, 2006).
Reaksi perubahan dari β-oksidasi ke bentuk ω-oksidasi merupakan
II.11 KERANGKA TEORI
metabolik hepatik kadar hormon tiroid (Teleanu dkk, (VA ↑ GABA menginhibiisi somatostatine inhibisi sekresi TSH Turan dkk, 2013) CBZ induksi CYP3A ggn
transport aktif transmembran T4
kadar T4 ↓(Verotti dkk, 2009)
CBZ induksi CYP3A metaboilisme hormon tiroid ↑ ggn hormon tiorid berkatan dgn tiroid globulin (Yilmaz dkk, 2014)
CBZ induksi CYP3A produk khusus reduksi hormon tiroid (Geeorge dkk, 2007)
CBZ
autoinduction reaksi hepatotoksik (Ahmed VI, XII (Yilmaz dkk, 2014)
CBZ T4 ↓, T3 dan TSH normal ((Isojarvi dkk, 2001 &Veroti dkk, 2009)
VA T4 ↓, T3 ↓, TSH ↑ (Punal dkk, 1999)
II.12 KERANGKA KONSEP
EPILEPSI
KARBAMAZEPIN
FUNGSI HATI FUNGSI TIROID