Laporan Mikrobiologi : Identifikasi Bakteri dengan Pewarnaan Gram
BAB I
PENDAHULUAN
1.1 Latar BelakangBakteri memiliki beberapa macam bentuk yaitu basil (tongkat), coccus, dan spirilum. Bakteri yang berbentuk tongkat maupun kokus dibagi menjadi beberapa macam. Pada bentuk basil pembagiannya yaitu basil tunggal, diplobasil, dan tripobasil.Sedangkan pada coccus dibagi menjadi monococcus, diplococcus, sampai stophylococcus. Khusus pada spirilum hanya dibagi dua yaitu setengah melengkung dan melengkung.
Melihat dan mengamati bakteri dalam kedaan hidup sangat sulit, karena selain bakteri itu tidak berwarna juga transparan dan sangat kecil. Mikroorganisme yang ada di alam ini mempunyai morfologi, struktur dan sifat-sifat yang khas, begitu pula dengan bakteri. Bakteri yang hidup hampir tidak berwarna dan kontras dengan air, dimana sel-sel bakteri tersebut disuspensikan. Salah satu cara untuk mengamati bentuk sel bakteri sehingga mudah untuk diidentifikasi ialah dengan metode pengecatan atau pewarnaan. Hal tersebut juga berfungsi untuk mengetahui sifat fisiologisnya yaitu mengetahui reaksi dinding sel bakteri melalui serangkaian pengecatan.
Prinsip dasar dari pewarnaan ini adalah adanya ikatan ion antara komponen seluler dari bakteri dengan senyawa aktif dari pewarnaan yang disebut kromogen. Terjadi ikatan ion karena adanya muatan listrik baik pada komponen seluler maupun pada pewarnaan. Berdasarkan adanya muatan ini maka dapat dibedakan pewarna asam dan pewarna basa. Teknik Pewarnaan bukan pekerjaan yang sulit tapi perlu ketelitian dan kecermatan bekerja
serta mengikuti aturan dasar yang berlaku.
Setiap sel terdiri dari berbagai bahan kimia. Setiap sel akan menunjukkan susunan kimiawi yang spesifik. Sebagai contoh, bakteri Gram negatif memiliki lipopolisakarida dalam dinding selnya, Sedangkan bakteri Gram positif tidak. Sebaliknya pada banyak bakteri Gram positif terdapat asam teikoat. Bahan kimia ini tidak ditemukan pada gram negatif. Karakteristik utamanya adalah tebalnya lapisan peptidoglikan pada dinding sel. Akibatnya, pada saat prosedur pewarnaan Gram, meninggalkan warna biru. Dinding sel Gram positif
biasa ditemukan pada Actinobacteria dan Firmicutes. Tidak seperti dinding sel Gram positif,
dinding sel Gram negatif memiliki lapisan peptidoglikan yang tipis. Hal ini menyebabkan
lunturnya warna biru/merah muda saat disiram etanol.
Uji biokimiawi bakteri adalah salah satu uji yang dilakukan untuk mengidentifikasi jenis bakteri. Hal ini karena setiap jenis bakteri memiliki sifat biokimia yang berbeda. Secara morfologis, biakan maupun sel bakteri yang berbeda dapat tampak serupa. Karena itu ciri fisiologis atau biokimiawi merupakan kriteria yang amat penting di dalam identifikasi spesimen yang tidak dikenal. Tanpa hasil pengamatan fisiologis yang memadai mengenai
organisme yang diperiksa maka penentuan spesiesnya tidaklah mungkin dilakukan. Manusia tidak dapat melihat dan mengidentifikasi bakteri tanpa diadakan percobaan.
Sifat metabolisme bakteri dalam uji biokimia biasanya dilihat dari interaksi metabolit-metabolit yang dihasilkan dengan reagen-reagen kimia. Kemampuan bakteri menggunakan senyawa tertentu sebagai sumber karbon dan sumber energiyang dapat digunakan untuk identifikasi.Identifikasi Bakteri dapat dilakukan dengan beberapa uji antara lain uji dalam melakukan fermentasi, uji oksidase, produksi katalase, uji motilase dan uji oksidase.
Bakteri di alam memiliki karakteristik sifat yang berbeda-beda. Bakteri ada yang bersifat motil, bereaksi dengan enzim katalase, bersifat oksidatif maupun fermentatif dan lain sebagainya. Tiap bakteri juga memiliki sifat kimiawi berbeda. Berdasar dari hal tersebut diatas, maka diadakanlah praktikum “Uji Biokimiawi Bakteri” ini guna memberikan pemahaman kepada kita tentang hal-hal yang berkaitan dengan sifat-sifat biokimiawi bakteri serta menambah pengetahuan dan keterampilan kita dalam mengenal karakter berbagai jenis bakteri.
1.2 Rumusan Masalah.
1.2.1 Identifikasi Bakteri dengan Pewarnaan.
1. Apa saja jenis-jenis pewarnaan pada kuman ?
2. Bagaimana langkah-langkah pembuatan preparat oles dan teknik pewarnaan pada kuman ?
3. Apa perbedaan dari bakteri gram negatif dengan bakteri gram positif ?
1.2.2 Morfologi Koloni dan Uji Biokimia
1. Apa sifat morfologi yang ditunjukkan koloni kuman ?
1.3 Tujuan Praktikum
1.3.1 Identifikasi Bakteri dengan Pewarnaan.
1. Mahasiswa mengenal macam-macam pewarnaan pada kuman
2. Mahasiswa dapat melakukan langkah-langkah pembuatan preparat oles dan teknik
pewarnaan pada kuman.
3. Mahasiswa dapat mengetahui perbedaan bakteri gram negatif dan bakteri gram positif.
1.3.2 Morfologi Koloni dan Uji Biokimia.
BAB II
TINJAUAN PUSTAKA
Pengenalan bentuk mikroba (morfologi), kecuali mikroalgae harus dilakukan pewarnaan terlebih dahulu agar dapat diamati dengan jelas. Pada umumnya bakteri bersifat tembus cahaya, hal ini disebabkan karena banyak bakteri yang tidak mempunyai zat warna. Tujuan dari pewarnaan adalah untuk mempermudah pengamatan bentuk sel bakteri, memperluas ukuran jazad, mengamati struktur dalam dan luar sel bakteri, dan melihat reaksi jazad terhadap pewarna yang diberikan sehingga sifat fisik atau kimia jazad dapat diketahui (Hadiutomo. 1990).
Metode pengecatan pertama kali ditemukan oleh Christian Gram pada tahun 1884. Dengan metode ini. Bakteri dapat dikelompokkan menjadi dua yatu, bakteri gram positif dan bakteri gram negative. Yang didasarkan dari reaksi atau sifat bakteri terhadap cat tersebut. Reaksi atau sifat bakteri tersebut ditentukan oleh komposisi dinding selnya sehingga pengecatan gram tidak bisa dilakukan pada mikroorganisme yang tidak mempunyai dinding sel seperti Mycoplasma sp (Waluyo, 2004).
Berhasil tidaknya suatu pewarnaan sangat ditentukan oleh waktu pemberian warna dan umur biakan yang diwarnai (umur biakan yang baik adalah 24 jam : Biakan muda). Bila digunakan biakan tua, terdapat kemungkinan penyimpanan hasil pewarnaan gram. Pada biakan tua, banyak sel mengalami kerusakan pada dinding-dinding selnya. Kerusakan pada dinding sel ini menyebabkan zat warna dapat keluar sewaktu dicuci dengan larutan pemucat. Ini berarti bahwa bakteri gram positif dengan dinding sel yang rusak tidak lagi dapat mempertahankan crystal violet sehingga terlihat sebagai bakteri gram negatif. Umumnya zat warna yang digunakan adalah garam-garam yang dibangun oleh ion-ion yang bermuatan positif dan negatif dimana salah satu ion tersebut berwarna. Zat warna dikelompokkan menjadi dua, yaitu zat pewarna yang bersifat asam dan basa. Jika ion yang mengandung warna adalah ion positif maka zat warna tersebut disebut pewarna basa. Dan bila ion yang mengandung warna adalah ion negatif maka zat warna tersebut disebut pewarna negatif (Hadiutomo. 1990).
Zat warna yang digunakan dalam pewarnaan bersifat basa dan asam. Pada zat warna basa bagian yang berperan dalam memberikan warna disebut disebut kromofor dan memiliki muatan positif. Sebaliknya, pada zat warna asam bagian yang berperan memberikan zat warna mempunyai muatan negatif zat warna basa lebih banyak digunakan karena muatan negatif banyak ditemukan di dinding sel, membran sel dan sitoplasma, sewaktu proses pewarnaan muatan positif pada zat warna basa akan berkaitan dengan muatan negatif dalam sel, sehingga mikroorganisme lebih jelas terlihat (Dwidjoseputro.1998).
Zat warna asam yang bermuatan negatif lazimnya tidak digunakan untuk mewarnai mikroorganisme, namun biasanya dimanfaatkan untuk mewarnai latar belakang sediaan pewarnaan. Zat warna asam yang bermuatan negatif ini tidak dapat berkaitan dengan muatan negatif yang terdapat pada struktur sel. Kadangkala zat warna negatif digunakan untuk mewarnai bagian sel yang bermuatan positif, perlu diperhatikan bahwa muatan dan daya ikat zat warna terhadap struktur sel dapat berubah bergantung pada pH sekitarnya sewaktu proses pewarnaan (Dwidjoseputro.1998).
Prosedur pewarnaan yang menghasilkan pewarnaan mikroorganisme disebut pewarnaan positif dalam prosedur pewarnaan ini dapat digunakan zat warna basa yang yang bermuatan positif maupun zat warna asam yang bermuatan negatif. Sebaliknya pada pewarnaan negatif latar belakang disekeliling mikroorganisme diwarnai untuk meningkatkan kontras dengan mikroorganisme yang tak berwarna. Pewarnaan mencakup penyiapan mikroorganisme dengan melakukan preparat ulas (Dwidjoseputro.1998)
Sebelum dilakukan pewarnaan dibuat ulasan bakteri di atas kaca objek. Ulasan ini kemudian difiksasi. Jumlah bakteri yang terdapat pada ulasan haruslah cukup banyak sehingga dapat terlihat bentuk dan penataanya sewaktu diamati. Kesalahan yang sering kali dibuat adalah menggunakan suspensi bakteri yang terlalu padat terutama bila suspensi tersebut berasal dari bukan media padat. Sebaliknya pada suatu suspensi bakteri bila terlalu encer, maka akan diperoleh kesulitan sewaktu mencari bakteri pada preparatnya (Sutedjo.1991).
Untuk pewarnaan yang mengamati morfologi sel mikroorganisme maka seringkali setelah pembuatan preparat ulas dilakukan fiksasi diikuti oleh pewarnaan. Fiksasi dapat dilakukan dengan cara melewatkan preparat diatas api atau merendamnya dengan metanol. Fiksasi digunakan untuk :
1. Mengamati bakteri oleh karena sel bakteri lebih jelas terlihat setelah diwarnai 2. Melekatkan bakteri pada glass objek
3. Mematikan bakteri
Pada pewarnaan sederhana hanya digunakan satu macam zat warna untuk meningkatkan kontras antara mikroorganisme dan sekelilingnya. Lazim, prosedur pewarnaan ini menggunakan zat warna basa seperti crystal violet, biru metilen, karbol fuchsin basa, safranin atau hijau malakit. Kadang kala digunakan zat warna negatif untuk pewarnaan sederhana : zat warna asam yang sering digunakan adalah nigrosin dan merah kongo. Prosedur Pewarnaan sederhana mudah dan cepat, sehingga pewarnaan ini sering digunakan untuk melihat bentuk ukuran dan penataan pada mikoorganisme bakteri pada bakteri dikenal bentu yang bulat (coccus), batang (basil), dan spiral. Dengan pewarnaan sederhana dapat juga terlihat penataan bakteri. Pada coccus dapat terlihat pewarnaan seperti rantai (stertococcus), buah anggur ( staphylococcus), pasangan (diplococcus), bentuk kubus yang terdiri dari 4 atau 8 (saranae) (Lay.1994).
Beberapa mikroba sulit diwarnai dengan zat warna yang bersifat basa, tetapi mudah dilihat dengan pewarnaan negatif, pada metode ini mikroba dicampur dengan tinta cina atau nigrosin, kemudian digesekkan diatas kaca objek.Zat warna tidak akan mewarnai bakteri, akan tetapi mewarnai lingkungan sekitar bakteri. Dengan mikroskop mikroba akan terlihat tidak berwarna dengan latar belakang hitam (Lay.1994).
Sel terdiri dari berbagai bahan kimia. Bila sel mikroba diberi perlakuan kimiawi, maka sel ini memperlihatkan susunan kimiawi yang spesifik. Sifat kimiawi pada susunan sel bakteri, mencakup kepada :
1. Membran Sel Prokariotik
Pada beberapa bakteri, membran mengelilingi sitoplasma tanpa menunjukkan adanya lipatan. Membran pada bakteri lain mengalami pelipatan ke dalam yang disebut mesosom. Pada bakteri fotosintetik, klorofil tidak terdapat dalam suatu kloroplas, melainkan terdapat dalam membran yang sangat berlipat-lipat di dalam sel, yang disebut membran tilakoid. Sistem
fotosintetik pada bakteri disamping menggunakan klorofil, juga karotenoid. Keduanya mengandung sistem transport elektron yangmenghasilkan ATP pada proses fotosintesis. 2. Dinding Sel
Dinding sel bakteri bersifat agak elastis dan tidak bersifat permeable terhadap garam dan senyawa tertentu dengan berat molekul rendah. Secara normal konsentrasi garam dan gula yang menentukan tekanan osmotik di dalam sel lebih tinggi daripada di luar sel. Apabila tekanan osmose di luar sel naik, air sel akan mengalir keluar, protoplasma mengalami pengkerutan, dan membran akan terlepas dari dinding sel. Proses ini disebut dengan
plasmolisis. Dinding sel bakteri gram positif: Dinding sel bakteri gram positif terdiri 40 lapis
rangka dasar murein, meliputi 30-70 % berat kering dinding sel bakteri. Senyawa lain penyusun dinding sel gram positif adalah polisakarida yang terikat secara kovalen, dan asam teikoat yang sangat spesifik. Dinding sel bakteri gram negatif: Dinding sel bakteri gram negatif hanya terdiri atas satu lapis rangka dasar murein, dan hanya meliputi + 10% dari berat kering dinding sel. Murein hanya mengandung diaminopemelat, dan tidak mengandung lisin. Di luar rangka murein tersebut terdapat sejumlah besar lipoprotein, lipopolisakarida, dan lipida jenis lain. Senyawa-senyawa ini merupakan 80 % penyusun dinding sel. Asam teikoat tidak terdapat dalam dinding sel ini.
3. Flagel dan Pili
Flagel merupakan salah satu alat gerak bakteri. Letak flagel dapat polar, bipolar, peritrik, maupun politrik. Flagel mengakibatkan bakteri dapat bergerak berputar. Penyusun flagel adalah sub unit protein yang disebut flagelin, yang mempunyai berat molekul rendah. Ukuran flagel berdiameter 12-18 nm dan panjangnya lebih dari 20 nm. Pada beberapa bakteri, permukaan selnya dikelilingi oleh puluhan sampai ratusan pili, dengan panjang 12 nm. Pili disebut juga sebagai fimbrae. Sex-pili berperan pada konjugasi sel. Pada bakteri Escherichia coli strain K-12 hanya dijumpai 2 buah pili.
5. Kapsul dan Lendir
Beberapa bakteri mengakumulasi senyawa-senyawa yang kaya akan air, sehingga membentuk suatu lapisan di permukaan luar selnya yang disebut sebagai kapsul atau selubung berlendir. Fungsinya untuk kehidupan bakteri tidak begitu esensial, namun menyebabkan timbulnya sifat virulen terhadap inangnya. Keberadaan kapsul mudah diketahui dengan metode pengecatan negatif menggunakan tinta cina atau nigrosin. Kapsul akan tampak transparan diantara latar belakang yang gelap. Pada umumnya penyusun utama kapsul adalah polisakarida yang terdiri atas glukosa, gula amino, rhamnosa, serta asam organik seperti asam piruvat dan asam asetat. Ada pula yang mengandung peptida, seperti kapsul pada bakteri Bacillus sp. Lendir merupakan kapsul yang lebih encer. Adakalanya kapsul bakteri dapat dipisahkan dengan metode penggojokan kemudian diekstrak untuk menghasilkan lendir.
Selain melalui struktur sel, kita juga dapat mengidentifikasi bakteri berdasarkan sifat kimiawi melalui proses pewarnaan. Zat warna adalah senyawa kimia berupa garam-garam yang salah satu ionnya berwarna. Garam terdiri dari ion bermuatan positif dan ion bermuatan negatif. Senyawa-senyawa kimia ini berguna untuk membedakan bakteri-bakteri karena reaksinya dengan sel bakeri akan memberikan warna berbeda. Perbedaan inilah yang digunakan sebagai dasar pewarnaan bakteri. Sel-sel warna dapat dibagi menjadi dua golongan yaitu asam dan basa. Jika warna terletak pada muatan positif dari zat warna, maka disebut zat warna basa. Jika warna terdapat pada ion negatif, maka disebut zat warna asam. Contoh zat warna basa adalah methylen blue, safranin, netral red, dan lain-lain. Sedangkan anionnya pada umumnya adalah Cl-, SO4 -, CH3COO-, COOHCOO. Zat warna asam umumnya mempunyai sifat dapat bersenyawa lebih cepat dengan bagian sitoplasma sel sedangkan zat
warna basa mudah bereaksi dengan bagian-bagian inti sel. Pewarnaan bakteri dipengaruhi oleh faktor-faktor seperti : fiksasi, peluntur warna, substrat, intensifikasi pewarnaan dan penggunaan zat warna penutup. Pada bakteri gram positif menunjukkan warna biru ungu dan bakteri gram negatif berwarna merah.
Sekali sitoplasma terwarnai, maka sel-sel organisme seperti mikobakteri menahan zat warna tersebut dengan erat, artinya tidak terpucatkan sekalipun oleh zat yang bersifat keras seperti asam alkohol (yaitu 3% HCL dalam etanol 95%). Alkohol asam ini merupakan pemucat yang sangat intensif dan jangan dikelirukan dengan alkohol-aseton yang banyak digunakan dalam prosedur pewarnaan Gram. Kondisi pewarnaan ini, organisme yang dapat menahan zat warna itu dikatakan tahan asam dan tampak merah. Bakteri biasa yang dindingnya tidak bersifat terlampau lipoidal, pewarna karbol fuksin yang mewarnai sel dapat dengan mudah dipucatkan oleh alkohol-asam dan karenanya dikatakan tak tahan asam. Tercucinya karbol fuksin dapat diperagakan oleh terserapnya pewarna tandingan biru metilen oleh sel, sehingga bakteri tersebut tampak biru (Hadioetomo, 1993).
Berikut adalah pengujian yang dapat dilakukan kepada bakteri :
1. Uji Biokimia
a. Uji oksidasi fermentasi
Uji oksidatif- fermantatif digunakan untuk menguji metabolisme bakterioksidatif atau fermentatif. Proses oksidasi terjadi didalam tabung oleh organismeaerob dan proses fermentasi oleh organisme anaerob. Proses fermentasi glukosa akan diubah menjadi glukosa G-Phospat yang kemudian dirombak menjadi asam piruvat dan oksidase akan merubah glukosa menjadi asam piruvat
b. Uji motilitas
Motilitas bakteri adalah suatu gerakan bakteri yang disebabkan adanya gerak aktif dan pasif. Gerak aktif adalah gerakan bakteri yang disebabkan karena bakteri memiliki flagel. Gerak pasif disebabkan karena faktor dari luar (gerak brown). Gerak brown adalah suatu gerakan yang dapat menggetarkan partikel-partikel secara acak atau terarah karena terus-menerus terkena pukulan molekul-molekul kecil yang tak terlihat yang terdapat dalam cairan.Motilitas dapat diamati dengan baik pada biakan yang masih baru. Pada biakan yang sudah lama,bakteri sudah mati, sehingga sangat sukar untuk mendapatkan sel yang motil, selain itu produksi asam dan produk yang bersifat racun dapat menyebabkan hilangnya motalitas sel bakteri pada biakan (Volk, 1988).
Menurut Taringan (1988) beberapa bakteri dapat melakukan gerakan meluncur yang sangat mulus yang hanya terjadi kalau persentuhan dengan benda padat. Kebanyakan bakteri yang motil dapat mendekati atau menjauhi berbagai senyawa kimia yang disebut kemotaksis.
c. Uji katalase
Uji katalase digunakan untuk mengetahui aktivitas katalase pada bakteri yang diuji.
Kebanyakan bakteri memproduksi enzim katalase yang dapat memecah H2O2 menjadi H2O
dan O2. Enzim katalase diduga penting untuk pertumbuhan aerobik karena H2O2 yang
dibentuk dengan pertolongan berbagai enzim pernafasan bersifat racun terhadap sel mikroba.
Hidrogen peroksida dengan rumus kimia H2O2 ditemukan oleh Louis Jacques Thenard
di tahun 1818. Senyawa ini merupakan bahan kimia anorganik yang memiliki sifat oksidator
kuat. Bahan baku pembuatan hidrogen peroksida adalah gas hidrogen (H2) dan gas oksigen
(O2). Teknologi yang banyak digunakan di dalam industri hidrogen peroksida adalah auto
oksidasi Anthraquinone. H2O2 tidak berwarna, berbau khas agak keasaman, dan larut dengan
baik dalam air. Dalam kondisi normal (kondisi ambient), hidrogen peroksida sangat stabil dengan laju dekomposisi kira-kira kurang dari 1% per tahun.
Mayoritas pengunaan hidrogen peroksida adalah dengan memanfaatkan dan merekayasa reaksi dekomposisinya, yang intinya menghasilkan oksigen. Pada tahap produksi hidrogen peroksida, bahan stabilizer kimia biasanya ditambahkan dengan maksud untuk menghambat laju dekomposisinya. Termasuk dekomposisi yang terjadi selama produk hidrogen peroksida dalam penyimpanan. Selain menghasilkan oksigen, reaksi dekomposisi
hidrogen peroksida juga menghasilkan air (H2O) dan panas. Reaksi dekomposisi eksotermis
yang terjadi adalah sebagai berikut:
H2O2 ----> H2O + 1/2O2 + 23.45 kcal/mol
Faktor-faktor yang mempengaruhi reaksi dekomposisi hidrogen peroksida adalah: o Bahan organik tertentu, seperti alkohol dan bensin
o Katalis, seperti Pd, Fe, Cu, Ni, Cr, Pb, Mn
o Temperatur, laju reaksi dekomposisi hidrogen peroksida naik sebesar 2.2 x setiap kenaikan
10oC (dalam range temperatur 20-100oC)
o Permukaan container yang tidak rata (active surface)
o Padatan yang tersuspensi, seperti partikel debu atau pengotor lainnya o Makin tinggi pH (makin basa) laju dekomposisi semakin tinggi
o Radiasi, terutama radiasi dari sinar dengan panjang gelombang yang pendek
Hidrogen peroksida bisa digunakan sebagai zat pengelantang atau bleaching agent pada industri pulp, kertas, dan tekstil. Senyawa ini juga biasa dipakai pada proses pengolahan limbah cair, industri kimia, pembuatan deterjen, makanan dan minuman, medis, serta industri elektronika (pembuatan PCB).
Parafin, merupakan hidrokarbon jenuh dengan rantai terbuka dan merupakan senyawa alkana. Parafin adalah campuran senyawa hidrokarbon alkana yang mengandung 21-50 atom karbon. Ketika pemisahan residu minyak bumi, jumlah atom karbon pada lilin parafin berkisar 40-50 atom. Komposisi dari setiap anggota senyawa alkana tersebut menyesuaikan
dengan rumus CnH2n+2, yang mana n adalah jumlah atom karbon dalam molekul. Di antara
anggota dari senyawa yaitu metana (CH4); etana (C2H6); propana, (C3H8); dan butana,
(C4H10).
Seluruh anggota senyawa alkana adalah anreaktif; yaitu, mereka tidak bereaksi siap pada temperatur biasa dengan seberapa bahan reaksi seperti asam, alkali, atau pembuat proses oksidasi. Pertama, empat anggota senyawa memasang gas pada temperatur dan tekanan biasa; anggota intermediate (setara) adalah mencairkan; dan anggota lebih berat adalah semipadat atau padat. Petroleum mengandung sekumpulan variasi hidrokarbon dan beberapa produk petroleum seperti bensin, minyak tanah, minyak bakar berat, minyak pelumas, vaselin, dan parafin berisi terutama dari campuran hidrokarbon parafin, yang terbentang dari anggota cair yang lebih ringan ke anggota yang padat. Parafin adalah suatu campuran dari hidrokarbon yang dipenuhi massa molekular yang tinggi, diproduksi selama penyulingan dari minyak/petroleum.
Bakteri memiliki sifat-sifat yang berbeda satu sama lain, berikut ini akan dijelaskan sifat-sifat dari bakteri :
1. Bakteri Fototrofik
Bakteri ini dicirikan memiliki Bacterioklorofil, sehingga dapat melakukan fotosintesis. Bentuk : bulat, batang, vibrio atau spiral. Gram negative. Reproduksinya dg pembelahan biner. Bergerak dengan flagella atau non motil. Habitat lingkungan aquatic.
2. Bakteri Luncur
Kelompok ini diwakili oleh beberapa tipe yang tidak umum. Myxobacteriales (miksobacter) menghasilkan apa yang disebut tubuh buah terdiri dari lendir dan sel. Sel individu dapat meluncur pada permukaan padat tetapi tidak punya flagella. Contoh lain Cytophagales, memperlihatkan gerakan meluncur.Bentuk: batang, bola atau filament. Gram negative. Sel-sel dapat terbenam dalam lendir. Habitat: tanah, sisa bahan tumbuhan membusuk, lingkungan aquatic.
3. Bakteri Berselongsong
Sel terbungkus dalam selongsong yang terbuat dari deposit senyawa, senyawa besi dan mangan yang tak larut. Bentuk: batang atau seperti filament. Gram negative. Bergerak dengan flagella atau non motil.Beberapa membentuk pelekap /dasar penghisap untuk menempelkan diri pada permukaan. Habitat lingkungan aquatic dan lumpur.
4. Bakteri Kuncup dan atau Berapendiks
Sel dengan prosteka atau pelekap. Reproduksi dengan berkuncup atau membelah. Bentuk sel: bola, oval, batang dengan ujung meruncing, beberapa menunjukkan pertumbuhan sepertii hifa. Motil karena flagella kutub atau non motil. Habitat: tanah dan lingkungan aquatic.
5. Spiroket
Sel langsing lentur berpilin (dinding tak kaku). Banyak spesies gram negative. Perbanyakan dengan Pembelahan melintang. Motil karena rotasi cepat sepanjang sumbu panjang spiralnya ataupun karena lenturan sel-selnya, gerak obeng. Habitat: Saprofit: tanah, lingk. Aquatic sedang yang parasit hidup di jaringan atau organ vascular pada tubuh termasuk daerah genital dan system saraf pusat pada manusia dan hewan. Contoh: Treponema pallidum penyebab penyakit sifilis.
6. Bakteri Spiral dan Lengkung
Bentuk batang berpilin( coma) beberapa dengan satu atau lebih putaran lengkap (dinding sel kaku). Gram negative. Motil karena ada flagella. Habitat: saprofit di lingkungan aquatic, dan yang parasit hidup di organ reproduktif, saluran pencernaan dan mulut hewan termasuk manusia. Contoh: Campylobacter fetus
7. Bakteri Batang dan Kokus Aerobik Gram Negatif
Sel bentuk batang, lonjong, bola, dimensi khas untuk bakteri yaitu 0,5-1,0 µm. Motil karena berflagela, atau nonmotil. Gram negative. Aerobic. Ciri-ciri metabolic khusus pada berbagai spesies; beberapa dapat menambat nitrogen dari udara; beberapa dapat mengoksidasi senyawa-senyawa berkarbon satu, misalnya metan atau methanol; beberapa dapat menghancurkan berbagai macam senyawa. Habitat: Saprofit di tanah dan lingkungan aquatic, air asin, sedangkan yang parasit bersifat pathogen pada hewan dan manusia, contoh:
Francisella tularensis penyebab penyakit tularemia (demam kelinci) dapat menular ke
manusia melalui luka iris atau tergores.
8. Bakteri Batang anaerobik fakultatif gram negatif
Sel batang pendek ( 0,5-1,0 x 1,0-3,0 µm). Motil: selnya peritrikus (E. coli) dan nonmotil. Anaerobic fakultatif. Gram negative. Habitat: Saprofit di lingkungan aquatic, tanah, makanan, parasit bersifat pathogen terutama di saluran pencernaan makanan dan terbawa keluar melalui faeses dan atau urine. Contoh: Escherichia coli, shigella spp.,
Salmonella spp., Yersinia pestis, Vibrio cholera 9. Bakteri gram negatif anaerobik
Sel bentuk batang lurus atau lengkung, kadang memperlihatkan sifat pleomorfik ( adanya berbagai bentuk dalam spsies yang sama). Motil selnya peritriks atau monotrik, dan beberapa spesies nonmotil. Ciri biokimiawi banyak sekali produk yang dihasilkan dari fermentasi glukosa. Anaerob obligat. Habitat: rongga alamiah pada manusia dan hewan, dan saluran pencernaan serangga. Contoh: Bacteriodes, Fusobacterium
10. Bakteri Kokus dan Kokobasillus gram negatif
Sel kokus berpasangan (diplokokus) dan dalam massa, beberapa kokobasil (batang pendek) terdapat tunggal atau berpasangan. Nonmotil, Gram negative. Aerobic.
Ciri biokimiawi berkemampuan terbatas untuk merombak berbagai senyawa (kh, protein dll). Habitat di selaput lendir manusia dan hewan, kadang bersifat pathogen. Contoh: Neisseria
gonorhoeae, N. meningitidis, Moraxella . 11. Bakteri Kokus anaerobik gram negatif
Penetapan kelompok ini berdasarkan ciri-ciri biokimiawi biakan. Sel ada yang sangat kecil (0,3-0,5µm) sampai sel bulat yang besar (2,5µm) berpasangan (dlm massa) atau rantai. Nonmotil. Anaerobic. Ciri biokimiawi merombak kh dan as. Lemak. Habitat dianggap parasit di saluran pernafasan dan pencernaan manusia dan hewan, tapi tidak pathogen. Contoh:
Veillonella, Megasphaera.
12. Bakteri gram negatif kemolitotrofik
Kelompok ini berkemampuan untuk menghasilkan energy dari oksidasi zat-zat kimia anorganik (kemolitotrofik). Morfologi sel beragam: bulat, batang, spiral, membrane berlapis banyak pada beberapa spesies, bakteri pengoksidasi belerang dapat menyimpan butir-butir belerang. Motil karena berflagela atau nonmotil. Gram negative, habitat: tanah, limbah , lingkungan aquatic, lingkungan alamiah yang banyak mengandung belerang, besi atau mangan, misalnya air tambang asam dan sumber air panas belerang. Contoh: Nitrobacter,
Nitrococcus, Nitrosobolus dan Thiospira. 13. Bakteri penghasil metan
Ciri kelompok ini kemampuannya menghasilkan metan, yaitu gas yang dibentuk dalam keadaan anaerobic. Morfologi sel: bola, batang dan spiral. Motil karena flagella kutub atau nonmotil. Gram negative atau gram positif. Anaerobic. Beberapa spesies termofilik. Habitat: saluran gastrointestinal pada binatang, endapan pada lingkungan aquatic dan limbah. Contoh:
Methanobacterium thermoauto-trophicus, M. ruminantium, Methanospirillum, Methanosacina barkeri.
Kelompok ini banyak spesies patogenik penting bagi manusia dan hewan. Sel bentuk kokus tunggal, berpasangan dalam rantai, paket atau gerombol. Nonmotil. Gram positif. Anaerobic fakultatif atau mikroaerofilik. Heterotrofik dengan persyaratan nutrient luas. Habitat: tanah, air tawar, kulit dan selaput lender pada binatang berdarahpanas termasuk manusia. Contoh: Sarcina, Streptococcus, Leuconostoc, Staphylococcus.
15. Bakteri Batang dan Kokus pembentuk endospora
Ciri pembeda kelompok ini adalah kemampuannya membentuk endospora. Kebanyakan spesies berbentuk batang, ada yang bulat dalam bentuk paket. Beberapa bersifat aerobic (genus Bacillus) dan yang lain anaerobic (genus Clostridium). Motil krn flagel atau nonmotil. Aerobik, anaerobic fakultatif, anaerobic atau mikroaerofilik. Habitat: tanah, air, lingkungan aquatic, saluran pencernaan (termasuk manusia. Contoh: Clostridium, Bacillus, Sporosarcina.
16. Bakteri gram negatif berbentuk batang tak membentuk endospora
Kelompok ini hampir semua adalah Lactobacillus. Bentuk sel batang tunggal atau rantai. Nonmotil. Gram positif. Anaerobic atau anaerobic fakultatif. Ciri metabolic: asam laktat merupakan produk akhir fermentasi. Habitat: produk persusuan, daging dan butiran (Grain), air, limbah, serta produk fermentasi, rongga mulut, vagina, serta saluran pencernaan makanan hewan (termasuk manusia).
17. Aktinomisetes & organisme sekerabat
Ciri pemersatu ialah pleomorfisme sel-selnya dan kecenderungan membentuk filament bercabang. Bentuk batang tak beraturan , filament. Nonmotil. Gram positif. Aerobic, anaerobic fakultatif atau anaerobic. Habitat: tanah, lingkungan aquatic, air, dan hewan (termasuk manusia). Contoh: Corynebacterium diphtheria, Mycobacterium tubercolosis,
Actinomyces israelli (penyebab peny. Aktinomikosis dsb Peny. Lumpy jaw/kaki gajah) 18. Riketsia
Morfologi sel: batang pendek, atau lonjong, kadang pleomorfik, ukuran lebar 0,3-0,7 µm; panjang 1,0-2,0 µm, beberapa membentuk tubuh kokoid yang berkembang menjadi tubuh buah. Gram negative. Nonmotil. Parasit obligat intraseluser pada arthopoda penghisap darah spt: caplak, kutu dan tungau. Habitat: serangga pembawa, burung, dan mammalia termasuk manusia. Contoh: Chlamydia penyebab penyakit trakoma, limfogranuloma venereum, uretritis, psitakosis, ornitosis. Riketsia penyebab demam tipus, demam bercak, Rocky mountain, tifus “scrub” dan demam Q.
19. Mikoplasma
Ciri khususnya adalah tidak adanya dinding sel sejati, terdapat membrane sel berlapis tiga tidak mengandung satuan structural asam muramat dan asam diaminopimelat yang memberikan kekakuan pada dinding sel. Sehingga sangat pleomorfik. Biasanya nonmotil. Gram negative. Anaerobic fakultatif. Habitat: selaput lendir saluran pernafasan dan saluran alat kelamin bawah. Contoh Mycoplasma pneumonia.
BAB III
3.1 Alat-Alat Laboratorium
1. Alat-alat gelas atau kaca a. Tabung reaksi b. Erlenmeyer c. Gelas ukur d. Pipet e. Cawan petri f. Kaca Objek
2. Alat-alat berbahan porselen 3. Alat-alat berbahan silika 4. Alat-alat dari logam
5. Alat-alat dari plastik atau karet 6. Alat-alat instrumen a. Neraca analitik b. pH meter c. Mikroskop d. Alat-alat sterilisasi • Autoclave • Oven
f. Automatic Colony Counter
g. Inkubator
h. Laminar Air Flow Cabinet
7. Bahan-bahan :
a. Isopropil alkohol 95 %
b. Inokulum bakteri
c. Zat warna biru metilen
d. Zat warna karbol fuksin
e. Kristal ungu
f. Larutan iodium gram
g. Etanol 95 %
h. Pewarna safranin
i. Medium nutrien cair
j. Larutan H2O2
.
3.2 Metode kerja
3.2.1 Indentifikasi Bakteri dengan Pewarnaan
1. Pembuatan Preparat Oles
Bersihkan kaca objek sehingga bebas dari lemak dan kotoran
Teteskan beberapa tetes isopropil alkohol 95 % pada kedua permukaan kaca objek dan keringkan dengan lap kertas.
Buatlah lingkaran ditengah-tengah permukaan bawah kaca objek. Hal ini untuk membantu meletakkan olesan mikroba dengan tepat.
Ambil inokulum bakteri dan sebarkan olesan tersebut hingga merata. Biarkan olesan tersebut kering udara hingga betul-betul kering.
Lakukan fiksasi panas dengan melayangkan kaca objek di atas panas api.
2. Pewarnaan Sederhana
Siapkan preparat olesan bakteri B. subtilis dan E. coli yang telah difiksasi panas dimanadibuat 2 preparat untuk tiap bakteri.
Letakkan kaca objek di atas bak pewarnaan dan genangi olesan tersebut dengan zat warnabiru metilen untuk preparat pertama dan zat warna karbol fuksin untuk preparat kedua.
Biarkan terwarnai biru metilen selama 1-2 menit atau selama 15-30 detik untuk pewarnaandengan karbol fuksin.
Peganglah kaca objek dengan penjepit dan miringkan kemudian bilas dengan air hinggazat warna hilang atau sedikit sekali.
Keringkan air pada permukaan preparat dengan kertas serap.
Amati morfologi spesien pada masing-masing preparat di bawah mikroskop. 3. Pewarnaan Gram
Buat preparat oles dari bakteri E. coli dan S. aureus. Beri kristal ungu selama 1 menit.
Buang kelebihan kristal ungu dengan memiringkan kaca objek di atas bak pewarna Bilas dengan air menggunakan botol pijit.
Tiriskan kaca objek dan kembalikan ke atas rak pada bak pewarna.
Cuci dengan etanol 95% setetes demi setetes selama 30 detik atau sampai zat ungu kristal tidak tampak lagi mengalir dari kaca objek.
Beri larutan iodium gram selama 2 menit.
Buang kelebihan iodium dengan memiringkan kaca objek. Bilas dengan air memakai botol pijit.
Beri safranin selama 30 detik.
Buang kelebihan safranin lalu bilas dengan air.
Tiriskan kaca objek dan serap kelebihan air dengan menekankan kertas serap diatasnya. Amati di bawah mikroskop.
Cuci dengan sir lalu tiriskan.
Beri safranin selama 30 detik.
Buang kelebihan safranin lalu bilas dengan air.
Tiriskan kaca objek dan serap kelebihan air dengan menekankan kertas serap diatasnya. Amati di bawah mikroskop.
3.2.2 Morfologi Koloni dan Uji Biokimia 1. Sifat Morfologi Bakteri.
Gunakan preparat hasil pewarnaan gram untuk bakteri E. coli dan S. aureus.
Perhatikan gambaran mikroskopik morfologi kedua bakteri meliputi bentuk, ukuran, tekstur, dan warna koloni.
2. Sifat Biokimia Bakteri
Menggunakan medium nutrien cair dalam tabung smith
Inokulasikan B. subtilis dan E. coli dalam tabung smith masing-masing sebanyak 2 tabung dan 1 tabung kontrol.
Inkubasikan pada suhu 37. selama 48 jam.
Pada tiap tabung tambahkan 1 ml H2O2 30% menggunakan pipet. Biarkan lartan H2O2 mengalir sendiri dan biarkan selama 1 jam Amati gas yang terdapat pada tabung yang tertutup.
Menggunakan medium nutrien agar miring
Inokulasikan B. subtilis dan E. coli dalam tabung smith masing-masing sebanyak 2 tabung dan 1 tabung kontrol.
Inkubasikan pada suhu 37. selama 48 jam.
Biarkan larutan H2O2 mengalir sendiri dan biarkan selama 1 jam. Amati gas yang terdapat pada tabung yang tertutup.
BAB IV
HASIL PENGAMATAN
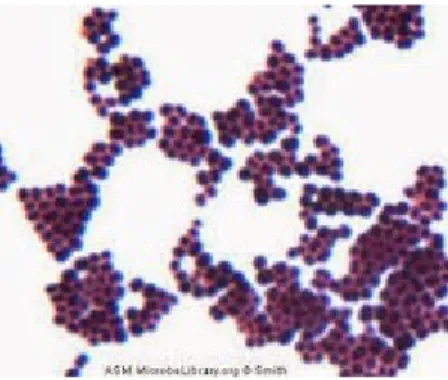
a. Pewarnaan GramBakteri St. aureus
Gambar diatas menunjukan gambar hasil pewarnaan gram bakteri St. aureus dibawah perbesaran mikroskop. Terlihat dari gambar warna keunguan yang menandakan bahwa bakteri St. aureus termasuk ke dalam golongan bakteri gram positif, dengan morfologi
bentuk coccus (bundar).
Gambar diatas menunjukan gambar hasil pewarnaan gram bakteri B. subtilus dibawah perbesaran mikroskop. Terlihat dari gambar warna keunguan yang menandakan bahwa bakteri B. subtilus termasuk ke dalam golongan bakteri gram positif, dengan morfologi
bentuk basil yang memanjang dan besar.
c. Pewarnaan Gram Bakteri E. coli
Gambar diatas menunjukan gambar hasil pewarnaan gram bakteri E.coli dibawah perbesaran mikroskop. Terlihat dari gambar warna merah yang menandakan bahwa bakteri E.coli termasuk ke dalam golongan bakteri gram negatif, dengan morfologi bentuk basil yang
memanjang kurus dan kecil-kecil.
d. Pewarnaan Sederhana Bakteri St. aureus
Gambar diatas menunjukan gambar hasil pewarnaan sederhana bakteri St. aureus dibawah perbesaran mikroskop. Terlihat dari gambar, warna ungu yang ditunjukkan untuk membantu melihat morfologi koloni maupun morfologi tunggal dari bakteri St. aureusberbentuk coccus.
BAB V
PEMBAHASAN
5.1 Identifikasi Bakteri dengan Pewarnaan.5.1.1 Jenis-jenis pewarnaan pada kuman.
Pewarnaan yang dilakukan pada kuman banyak ragam dan jenisnya. Selama ini dikenal lima macam proses pewarnaan, yaitu sebagai berikut :
1. Pewarnaan negative
- Bakteri tidak diwarnai, tapi mewarnai latar belakang.
- Ditujukan untuk bakteri yang sulit diwarnai, seperti spirochaeta. Cara pewarnaan negatif :
Sediaan hapus → teteskan emersi → lihat dimikroskop
Metode ini bukan untuk mewarnai bakteri tetapi mewarnai latar belakangnya menjadi hitam gelap. Pada pewarnaan ini mikroorganisme kelihatan transparan (tembus pandang). Teknik ini berguna untuk menentukan morfologi dan ukuran sel. Pada pewarnaan ini olesan tidak mengalami pemanasan atau perlakuan yang keras dengan bahan-bahan kimia, maka terjadinya penyusutan dan salah satu bentuk agar kurang sehingga penentuan sel dapat diperoleh dengan lebih tepat. Metode ini menggunakan cat nigrosin atau tinta cina.
2. Pewarnaan sederhana
- Menggunakan satu macam zat warna (biru metilen/air fukhsin) - Tujuan hanya untuk melihat bentuk sel
Pewarnaan sederhana, merupakan pewarna yang paling umum digunakan. Berbagai macam tipe morfologi bakteri (kokus, basil, spirilum, dan sebagainya) dapat dibedakan dengan menggunakan pewarna sederhana, yaitu mewarnai sel-sel bakteri hanya digunakan satu macam zat warna saja. Kebanyakan bakteri mudah bereaksi dengan pewarna-pewarna sederhana karena sitoplasmanya bersifat basofilik (suka akan basa) sedangkan zat-zat warna yang digunakan untuk pewarnaan sederhana umumnya bersifat alkalin (komponen kromoforiknya bermuatan positif).
3. Pewarnaan Tahan Asam
Pewarnaan ini dilakukan pada bakteri tahan asam dalam proses warna akibat Alkohol-asam, dan penggunaan pembalik warna pada tahap akhir dari proses sehingga menghasilkan warna merah.
4. Pewarnaan structural / khusus
- Untuk mewarnai struktur khusus/tertentu dari bakteri→ kapsul, spora, flagel dll a. Pewarnaan kapsul
Pewarnaan ini menggunakan larutan Kristal violet panas, lalu larutan tembaga sulfat sebagai pembilasan menghasilkan warna biru pucat pada kapsul, karena jika pembilasan dengan air dapat melarutkan kapsul. Garam tembaga juga memberi warna pada latar belakang. Yang berwana biru gelap.
b. Pewarnaan spora
Dinding spora relative tidak permeable, namun zat warna bias menembusnya dengan cara memanaskan preparat.
c. Pewarnaan flagel
Pewarnaan flagel dengan memberi suspense koloid garam asam tanat yang tidak stabil, sehingga terbentuk presipitat tebal pada dinding sel dan flagel.
d. Pewarnaan nucleoid
Pewarnaan nucleoid menggunakan pewarna fuelgen yang khusus untuk DNA.
5. Pewarnaan diferensial
- Menggunakan lebih dari satu macam zat warna - Tujuan untuk membedakan antar bakteri
- Contoh: Pewarnaan Gram, Pewarnaan Bakteri Tahan Asam
Tujuan dari pewarnaan adalah untuk memudahkan melihat bakteri dengan mikroskop, memperjelas ukuran dan bentuk bakteri, untuk melihat struktur luar dan struktur dalam bakteri seperti dinding sel dan vakuola, menghasilkan sifat-sifat fisik dan kimia yang khas daripada bakteri dengan zat warna, serta meningkatkan kontras mikroorganisme dengan sekitarnya.
5.1.2 Langkah-langkah Pembuatan Preparat Oles dan Teknik Pewarnaan Pada Kuman.
Teknik pewarnaan kuman yang kami lakukan pada praktikum ini adalah teknik pewarnaan sederhana dan teknik pewarnaan gram. Untuk teknik pewarnaan sederhana bertujuan untuk melihat morfologi dari bakteri, baik itu bentuk koloninya maupun bentuk individunya. Langkah pertama yang harus dilakukan adalah menyiapkan preparat olesan dari bakteri. Preparat yang akan diolesi bakteri ini di fiksasi dulu sebanyak 3 kali dengan api untuk menghilangkan kuman dan lemak di preparat baru kemudian di lap dengan tissue. Bakteri yang digunakan adalah bakteri B. subtilis, E. coli, dan St. Aureus. Bakteri-bakteri ini dioleskan pada bagian oval preparat, yang sebelumnya sudah ditandai dengan sepidol, penandaan bagian oval ini untuk membantu meletakkan olesan mikroba dengan tepat. Sebelum preparat dioleskan bakteri, preparat diolesi terlebih dahulu dengan NaCl steril, tujuannya karena NaCl steril merupakan garam fisiologi dari bakteri.
Langkah selanjutnya adalah menggenangi olesan bakteri pada preparat tersebut dengan zat warnakristal violet atau biru metilenselama 1-2 menit. Kemudian preparat dimiringkan dan dibilas dengan air hinggazat warna hilang atau sedikit sekali. Selanjutnya adalah keringkan air pada permukaan preparat dengan kertas serap lalu amati morfologi bakteri pada masing-masing preparat di bawah mikroskop.
Selain teknik pewarnaan sederhana, kami juga melakukan teknik pewarnaan gram, teknik ini bertujuan untuk mengidentifikasi suatu bakteri apakah dia termasuk ke dalam bakteri gram negatif atau bakteri gram positif. Langkah-langkah dalam pewarnaan ini hampir sama dengan langkah pada pewarnaan sederhana yakni membuat preparat oles dari ketiga bakteri diatas. Bedanya adalah pada beberapa reagen yang ditambahkan. Pertama, bakteri pada preparat ditetesi kristal violet selama 1 menit. Lalu kelebihan kristal violetdibuang dengan memiringkan kaca objek dan bilas dengan air mengalir secara perlahan. Preparat ditiriskan, lalu diberi larutan iodium gram selama 2 menit, kelebihan iodium dibuang dengan memiringkan kaca objek lalu dibilas dengan air seperti kristal violet. Langkah selanjutnya adalah preparat dicuci dengan etanol 95% setetes demi setetes selama 30 detik atau sampai zat ungu kristal tidak tampak lagi mengalir dari preparat, setelah dirasa warna menghilang cuci perlahan lalu tiriskan. Terakhir adalah dengan menambahkan pewarna safranin selama 30 detik pada preparat, kemudian kelebihan safranin dibuang dan dibilas dengan air. Preparat yang masih basah ditiriskan dan diserap dengan menekankan kertas serap disekitarnya.Amati preparat olesan bakteri yang sudah diwarnai tersebut di bawah mikroskop.
Jadi, dapat disimpulkan bahwa bahan-bahan pereaksi yang digunakan dalam pewarnaan gram adalah :
Zat warna utama (violet kristal)
Mordan (larutan Iodin) yaitu senyawa yang digunakan untuk mengintensifkan warna
utama.
Pencuci / peluntur zat warna (alcohol / aseton) yaitu solven organic yang digunakan
untuk melunturkan zat warna utama.
Zat warna kedua / cat penutup (safranin) digunakan untuk mewarnai kembali sel-sel
yang telah kehilangan cat utama setelah perlakuan denga alcohol. 5.1.3 Perbedaan dari bakteri gram negatif dengan bakteri gram positif.
Seperti yang kita ketahui bakteri dibagi menjadi bakteri gram negatif dan bakteri gram positif, pembagian atas keduanya didasarkan pada beberapa perbedaan, berikut perbedaan bakteri gram negatif dan bakteri gram positif :
Ciri-ciri bakteri gram negative :
- Struktur dinding selnya tipis, sekitar 10-45mm, berlapis tiga atau multi layer
- Dinding selnya mengandung lemak lebih banyak (11-22%), peptidoglikan terdapat dalam lapisan kaku, sebelah dalam dengan jumlah sedikit dan tidak mengandung asam laktat.
- Kurang rentan terhadap senyawa penisilin. - Tidak resisten terhadap gangguan fisik
Ciri-ciri bakteri gram positif :
- Struktur dindingnya tebal
- Dinding selnya mengandung lipid yang lebih normal - Bersifat lebih rentan terhadap senyawa penisilin - Komposisi yang dibutuhkan lebih rumit
- Lebih resisten terhadap gangguan fisik.
Perbedaan relatif sifat bakteri gram positif dan gram negatif.
Sifat Bakteri gram
positif (+)
Bakteri gram negatif(-) Komposisi dinding sel Kandungan lipid rendah
(1-4%) Kandungan lipid tinggi
Ketahanan terhadap penisilin
Lebih sensitif Lebih tahan
Penghambatan oleh pewarna basa (VK)
Lebih dihambat Kurang dihambat
Kebutuhan nutrisi Kebanyakan spesies
relatif kompleks Relatif sederhana
perlakuan fisik
Berdasarkan hasil pengamatan dibawah mikroskop, untuk bakteri yang termasuk gram positif akan terlihat berwarna ungu, dimana warna ungu ini sendiri merupaka warna dari kristal violet yang sebelumnya diteteskan, warna ini melekat dengan kuat karena peptidoglikan dari bakteri gram positif tebal. Sedangkan untuk bakteri gram negatif akan terlihat warna merah, dimana warna merah ini merupakan warna dari pewarna safranin yang diteteskan terakhir kali, warna ini melekat dan warna ungu sama sekali tidak terlihat karena peptidoglikan dari bakteri gram negatif relatif tipis sehingga ia tidak mampu mempertahankan warna ungu layaknya bakteri gram positif.
5.2 Morfologi Koloni dan Uji Biokimia.
5.2.1 Mahasiswa memahami sifat morfologi yang ditunjukkan koloni kuman.
Ada empat cara yang dilakukan untuk mengetahui hasil dari identifikasi morfologi koloni bakteri yaitu sebagai berikut:
1) Metode piringan goresan dan metode piringan tuangan
Untuk memelihara bakteri dalam lempengan (di dalam petridis) sampel bakteri diambil dengan ujung kawat yang bengkok. Ujung yang bengkok ini kemudiaan digesekkan dengan gerakan ke kanan dan ke kiri sampai meliputi seluruh permukaan agar-agar. Dengan demikian akan diperoleh koloni-koloni yang mengggerombol dan koloni-koloni yang memencil. Yang terakhir inilah yang menunjukkan sifat-sifat yang harus diperhatikan. Sifat-sifat koloni pada agar-agar lempengan mengenai bentuk, permukaan, dan tepi. Bentuk koloni dilukiskan sebagai titik,-titik, bulat, berbenang, tak teratur, serupa akar, serupa kumparan. Permukaan koloni dapat datar, timbul mendatar, timbul melengkung, timbul mencembung, timbul membukit, timbul berkawah. Tepi koloni ada yang utuh, ada yang berombak, ada yang berbelah-belah, ada yang bergerigI, ada yang berbenang-benang, ada yang keriting.
2) Metode tusukan agar tegak
Metode ini dapat diperoleh dengan menusukkan ujung kawat yang membawakan bakteri, lurus ke dalam medium melalui tengah-tangah medium. Bakteri yang aerob akan tampak tumbuh dekat permukaan medium. Sifat-sifat koloni tusukan dalam gelatin. Ada bakteri yang dapat mengencerkan gelatin, ada juga bakteri yang tidak mampu mengencerkan gelatin. Bentuk koloni serupa pedang, tasbih, bertonjol-tonjol, berjonjot, serupa batang, serupa kawah, mangkuk, corong, pundit-pundi (Jutono, 1980). Koloni juga dibedakan berdasarkan moril tidaknya. Bakteri dikatakan motil apabila bakteri menyebar ke sekitar tusukan, sedangkan bakteri dikatakan nonmotil bila pertumbuhannya hanya pada bekas tusukan.
3) Metode agar miring goresan
Untuk membuat piaraan disitu maka ujung kawat yang berisi bakteri digesekkan satu kali dari ujung bawah ke ujung atas sehingga garis itu merupakan diameter memanjang dari permukaan medium. Sifat khusus pada agar miring berkisar pada bentuk dan tepi koloni, dan
sifat-sifat itu dinyatakan dengan kata-kata seperti : berupa pedang, serupa duri, serupa tasbih, titik-titik, batang, dan akar.
4) Metode medium cair
Inolukasi juga dapat dilakukan degan metode adukan. Bakteri yang digunakan untuk membuaat piaaraaan adukan dapat diperoleh dari piaraan dalam medium cair, atau dari suatu koloni pada medium padat. Biakan diambil dengan kawat ose kemudian diadukkan dalam medium cair tersebut. Sifat koloni yang kelihatan akan berbeda-beda. Permukaan medium ini dapat memprlihatkan adanya serabut, cincin, langit-langit, atau selaput.
Menurut Pradhika (2008), koloni bakteri memiliki ciri-ciri yang berbeda, tergantung jenisnya dan mediumnya. Ciri-ciri tersebut adalah :
a. Pertumbuhan pada petridis.
Ukuran; pinpoint/punctiform (titik) - Small (kecil)
- Moderate (sedang)
- Large (besar)
Pigmentasi : mikroorganisme kromogenik sering memproduksi pigmen intraseluler, beberapa
jenis lain memproduksi pigmen ekstraseluler yang dapat terlarut dalam media.
Karakteristik optik : diamati berdasarkan jumlah cahaya yang melewati koloni.
- Opaque (tidak dapat ditembus cahaya)
- Translucent (dapat ditembus cahaya sebagian) - Transparant (bening) Bentuk : - Circular - Irregular - Spindle - Filamentous - Rhizoid Elevasi : - Flat - Raised - Convex - Umbonate Permukaan : - Halus mengkilap - Kasar - Berkerut
- Kering seperti bubuk
Margins :
- Entire - Lobate
- Undulate - Serrate - Felamentous - Curled
b. Pertumbuhan pada Agar Miring
Ciri-ciri koloni diperoleh dengan menggoreskan jarum inokulum tegak dan lurus pada medium.
c. Pertumbuhan pada Agar Tegak
Cara penanaman adalah dengan menusukkan jarum inokulum needle ke dalam media agar tegak.
d. Pertumbuhan pada Media Cair
BAB VI
PENUTUP
6.1 Kesimpulan1. Jenis-jenis pewarnaan pada kuman ada banyak macamnya, diantaranya pewarnaan negatif,
pewarnaan sederhana, pewarnaan tahan asam, pewarnaan structural / khusus, dan pewarnaan diferensial.
2. Sebelum melakukan pewarnaan bakteri, kita harus membuat preparat oles bakteri. sebelum
preparat diolesi bakteri harus dilakukan fiksasi dulu.
3. Teknik pewarnaan sederhana adalah teknik pewarnaan yang bertujuan untuk melihat bentuk
tunggal dan berkoloni dari suatu bakteri, sedangkan teknik pewarnaan gram bertujuan untuk mengidentifikasi bakteri termasuk dalam gram positif atau negatif.
4. Bahan pereaksi yang digunakan dalam pewarnaan gram adalah pewarna violet kristal, lalu
iodium/lugol, kemudian alkohol dan yang terakhir adalah pewarna safranin
5. Perbedaan antara bakteri gram positif dengan gram negatif setelah dilakukan pewarnaan gram
adalah: bakteri gram positif memberikan warna ungu, sedangkan gram negatif memberikan warna merah dibawah mikroskop.
6. Morfologi yang ditunjukkan koloni kuman dapat diidentifikasi dengan metode piringan
goresan, metode piringan tuangan, metode tusukan agar tegak, metode agar miring goresan, metode medium cair
6.2 Saran
Berhatil-hatilah bekerja dengan mikroorganisme sseperti bakteri karena bisa saja bakteri tersebut bersifat patogen. Gunakan selalu sarung tangan dan masker untuk menghindari kontak kulit langsung dengan bakteri. Kemudian setelah pekerjaan selesai jangan lupa untuk mencuci tangan dengan sabun lalu dengan antiseptik untu meminimalisir jumlah kuman yang menempel di tangan kita.