FORMULASI SEDIAAN KRIM EKSTRAK ETANOLIK RIMPANG
AKTIVITASNYA SEBAGAI ANTIINFLAMASI
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memenuhi Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh :
Samuel Meinardus Dwi Prasetyo
NIM : 108114084
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2014
i
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memenuhi Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh :
Samuel Meinardus Dwi Prasetyo
NIM : 108114084
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2014
FORMULASI SEDIAAN KRIM EKSTRAK ETANOLIK RIMPANG TEMU PUTIH (Curcuma zedoariaBerg. Roscoe) DENGAN PENGUJIAN
iii
vi
PRAKATA
Puji Syukur dan terima kasih penulis panjatkan kepada Tuhan Yang
Maha Esa atas berkat dan penyertaan-Nya yang selalu membimbing penulis
sehingga dapat menyelesaikan skripsi yang berjudul “Formulasi Sediaan Krim
Ekstrak Etanolik Rimpang Temu Putih (Curcuma zedoaria Berg. Roscoe)Dengan
Pengujian Aktivitasnya Sebagai Antiinflamasi” sebagai salah satu syarat
memperoleh gelar Sarjana Farmasi (S. Farm) di Fakultas Farmasi, Universitas
Sanata Dharma, Yogyakarta.
Pada kesempatan ini, penulis hendak menyampaikan ungkapan
terimakasih kepada :
1. Bapak, ibu dan kakak penulisatas doa dan kasih sayangnya kepada penulis
yang senantiasa menyertai penulis selama menyusun skripsi.
2. Dekan Fakultas Farmasi Universitas Sanata Dharma yang telah memberikan
bimbingan dan pengajaran kepada penulis .
3. Ibu Christofori Maria Ratna Rini Nastiti, M. Pharm., Apt. selaku Kaprodi
Fakultas Farmasi Universitas Sanata Dharma, sekaligus dosen pembimbing
yang selalu memberikan arahan, bimbingan, masukan, semangat serta
motivasi semenjak pembuatan proposal hingga selesainya penelitian skripsi
ini.
4. Bapak Ipang Djunarko M.Sc., Apt. sebagai dosen penguji yang telah berkenan
memberikan saran dan masukan demi kebaikan skripsi ini.
5. Bapak Yohanes Dwiatmaka M.Si. sebagai dosen penguji yang telah berkenan
vii
6. Segenap dosen Fakultas Farmasi Universitas Sanata Dharma yang telah
mengajar dan membimbing penulis selama perkuliahan.
7. Segenap laboran dan karyawan, Bapak Musrifin, Bapak Heru, Bapak
Wagiran, Bapak Parjiman, dan Mas Darto yang telah membantu selama
penelitian berlangsung.
8. Teman-teman skripsi senasib sepenanggungan Tomas, Lulu, Odilia, Wulan,
Angga, Anis dan Dian.
9. Teman-teman angkatan 2010 Fakultas Farmasi Universitas Sanata Dharma
yang juga memberikan banyak pengalaman selama masa perkuliahan penulis.
10.Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah
memberikan doa, bantuan, dan dukungan selama penelitian skripsi.
Penulis menyadari bahwa penyusunan skripsi ini masih banyak
kekurangan mengingat keterbatasan kemampuan, pengetahuan serta pengalaman
yang dimiliki.Oleh sebab itu, kritik dan saran yang membangun sangat diperlukan
oleh penulis untuk menyempurnakan skripsi ini.Semoga skripsi ini dapat
bermanfaat bagi perkembangan ilmu pengetahuan.
Yogyakarta, 23 Juli 2014
viii
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN KEASLIAN KARYA ... iv
PERNYATAAN PERSETUJUAN PUBLIKASI ... v
PRAKATA ... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
INTISARI ... xiv
ix
A. Jenis dan Rancangan Penelitian ... 20
B. Variabel Penelitian ... 20
C. Definisi Operasional ... 21
D. Bahan ... 22
A. Hasil Uji Standarisasi Ekstrak Temu Putih ... 30
B. Hasil Uji Organoleptis ... 31
C. Hasil Uji pH ... 33
x
E. Hasil Uji Stabilitas Krim Temu Putih ... 34
F. Uji Aktivitas Antiinflamasi Krim Temu Putih ... 35
BAB V. KESIMPULAN DAN SARAN ... 40
A. Kesimpulan ... 40
B. Saran ... 40
DAFTAR PUSTAKA ... 41
LAMPIRAN ... 44
xi
DAFTAR TABEL
Halaman
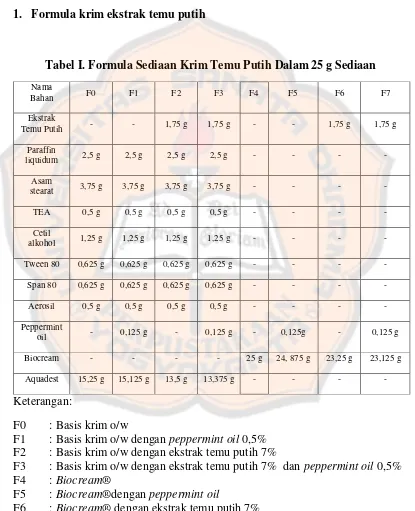
Tabel I. FormulaSediaan Krim Temu Putih Dalam 25 g Sediaan ... 23
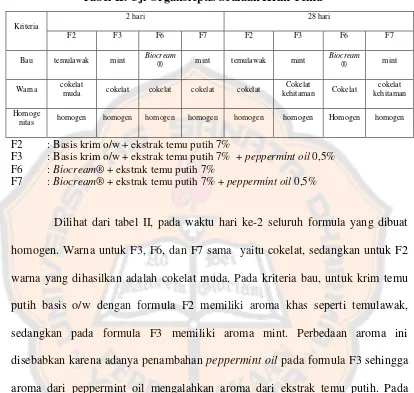
Tabel II. Uji Organoleptis Sediaan Krim Temu Putih ... 32
Tabel III. Uji pH Sediaan KrimTemu Putih ... 33
Tabel IV. Uji Viskositas Sediaan Krim Temu Putih ... 34
Tabel V. Pergeseran Viskositas Sediaan Krim Temu Putih ... 34
xii
DAFTAR GAMBAR
Halaman
Gambar 1. Rimpang Temu Putih (Curcumazedoaria) ... 11
Gambar 2. Struktur Kurkumin, Demetoksikurkumin, Bisdemetoksikurkumin 13
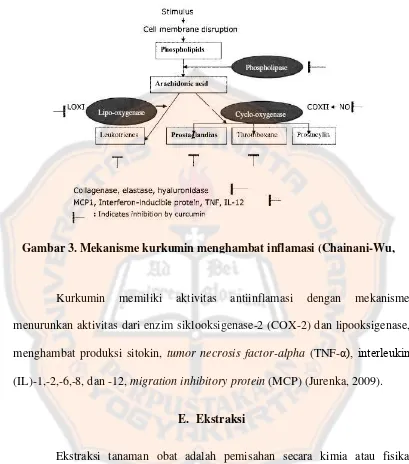
Gambar 3. Mekanisme Kurkumin Menghambat Inflamasi ... 14
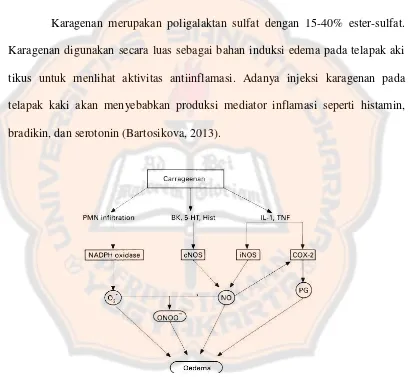
Gambar 4. Mekanisme Karagenan Menyebabkan Edema ... 17
Gambar 5. Grafik % Inhibition Sediaan Krim Temu Putih Basis o/w ... 38
Gambar 6. Grafik % Inhibition Sediaan Krim Temu Putih Basis Biocream® 38
xiii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Penetapan Kadar Air Menggunakan Metode Gravimetri... 44
Lampiran 2. Penetapan Kada Kurkumin Dengan Metode KLT Densitometri 46 Lampiran 3. Uji Statistik Jam ke-1 ... 48
Lampiran 4. Uji Statistik Jam ke-2 ... 51
Lampiran 5 Uji Statistik Jam ke-3 ... 54
Lampiran 6 Uji Statistik Jam ke-4 ... 57
Lampiran 7 Sediaan Krim Temu Putih Pada Hari ke-2 ... 60
Lampiran 8 Sediaan Krim Temu Putih Pada Hari ke-28 ... 61
Lampiran 9 Uji sifat fisis ... 65
xiv
INTISARI
Penggunaan obat antiinflamasi dari bahan alam sedang dikembangkan untuk mencegah efek samping pada saluran gastrointestinal. Penelitian ini bertujuan untuk memformulasi ekstrak kental temu putih ke dalam sediaan krim dengan basis o/w dan basis biocream, serta mengamati pengaruhpenetration
enhancerberupa peppermint oil 0,5% terhadap peningkatan aktivitas
antiinflamasi.
Penelitian ini termasuk dalam penelitian eksperimental murni dengan metodeinduksi karagenan sebagai agen inflamasi pada telapak kaki tikus betina galur Wistar secara subplantar. Edema diukur dengan alat pengukur berupa jangka sorong. Konsentrasi ekstrak yang digunakan dalam formulasi sediaan krim adalah 7% dengan kontrol negatif menggunakan basis krim dan kontrol positif menggunakan Voltaren® emulgel. Pemberian krim dilakukan 1 jam sebelum injeksi karagenan secara topikal.Analisis data menggunakan ANOVA dengan taraf kepercayaan 95% pada program R dengan versi 3.0.1.
Hasil penelitian menunjukkan bahwa sediaan krim temu putih (Curcuma zedoaria (Berg.) Roscoe) memiliki stabilitas yang baik selama penyimpanan 28 hari untuk formula F3, F6, dan F7. Seluruh sediaan krim temu putih menunjukkan aktivitas inflamasi selama 4 jam setelah injeksi karagenan 1%, tetapi tidak sekuat Voltaren® emulgel.
xv
ABSTRACT
The use of natural antiinflammatory drugs had been developed recently to anticipate adverse effects on the gastrointestinal tract. This study aim to formulate a extract of zedoary into cream preparation with o/w base and biocream base, and to investigatethe effect of penetration enhancers i.e 0.5%peppermintoil to increase antiinflammatory activity
This study was experimental, observing the antiinflamatory effect of the ethanolic extract of zedoary creams, by using carrageenan induced hind paw edema method. The paw edema was induced the subplantar injection and edema thickness measured with a vernier caliper. The concentration of the extract used in the preparation of the cream formulation was 7 % with a negative control using a cream base and a positive control using Voltaren ® emulgel. Analysis of data using ANOVA with confident level 95% in R 3.0.1 program.
The results showed that the ethanolic extract of zedoary creams has good stability during storage of 28 days for F3, F6 and F7. All of creamsshowed anti- inflammatory activity but not stronger than Voltaren® emulgel while4 hour after injection of carrageenan 1% .
1
BAB I
PENGANTAR
A. Latar Belakang
Kulit merupakan bagian terluar dari tubuh yang berhubungan langsung
dengan lingkungan, hal ini membuat kulit mudah terkena zat-zat asing yang
berbahaya seperti zat kimia, zat mikrobiologik, radiasi panas dan elektromagnetik
serta trauma fisik. Inflamasi merupakan respon biologis perlindungan diri
organisme untuk menghilangkan rangsangan penyebab luka yang dapat
disebabkan oleh faktor-faktor tersebut. Inflamasi terjadi karena adanya pelepasan
mediator kimiawi dari jaringan yang mengalami kerusakan (Mycek, 2001).
Jaringan yang mengalami kerusakan akan melepaskan inflammatory mediators
seperti bradikinin, histamin, prostaglandin, dan sitokin. Prostaglandin merupakan
mediator penting dalam proses inflamasi dan terjadiya rasa nyeri. Prostaglandin
disintesis dengan adanya enzim siklooksigenase (Kidd, 2001).
Telah banyak obat-obat antiinflamasi yang beredar. Kebanyakan obat
antiinflamasi yg beredar merupakan golongan nonsteroid (AINS). Obat AINS
memiliki mekanisme antiinflamasi dengan cara menghambat enzim
siklooksigenase untuk mencegah tersintesisinya prostaglandin (Gunawan, 2005).
Diklofenak merupakan salah satu obat antiinflamasi golongn nonsteroid yang
dilofenak dan obat AINS lainnya secara oral memiliki efek samping yang serius
pada saluran gastrointestinal (Moody,2010).
Pengobatan inflamasi secara topikal saat lebih dipilih karena pengobatan
secara topikal dapat menghindari terjadinya efek samping seperti halnya yang
terjadi pada penggunaan obat inflamasi secara oral (Schuelert, Russell, dan
McDougall, 2011). Selain itu keuntungan dari penggunaan obat inflamasi secara
topikal dibandingkan dengan oral, yaitu tidak melewati hepatic first pass
metabolism, mudah penggunaannya, mengurangi terjadinya fluktuasi level obat
dalam tubuh, dapat mencapai efikasi dengan penggunaan dosis kecil, mudah
untuk penghentian pengobatan jika dikehendaki, lebih site-spesific, meningkatkan
kepatuhan penggunaan (Moody,2010).
Pengobatan dengan menggunakan obat tradisional pada saat ini
merupakan pilihan alternatif bagi masyarakat karena khasiat dari obat tradisional
tidak kalah baiknya dengan obat-obatan sintetik. Banyak tanaman herbal yang
secara empiris berpotensi sebagai obat herbal antiinflamasi, salah satunya adalah
temu putih (Curcuma zedoaria). Berbagai manfaat dapat ditemukan dari seluruh
bagian tanaman temu putih terutama bagian rimpangnya. Temu putih memiliki
kandungan minyak atsiri berupa zingiberen, 1,8 sineol, D-kampora, D-kampen,
Dborneol, α pinen, kurkumol, zederon, kurkumeneol, kurkulon, furanodienon,
isofuranodienon. Kandungan kurkuminoid yang terdapat di temu putih berupa
kurkumin, dismetoksikurkumin, bisdesmetoksikurkumin (Badan Pengawas Obat
karena kurkumin aktif dalam menghambat peradangan (Kaushik dan
Jalalpure, 2011).
Tumor necrosis factor alpha (TNFα), interleukin-1 (IL-1), IL-6 dan IL-8
merupakan pro-inflammatory cytokines yang memiliki peran penting dalam proses
terjadinya inflamasi (Kidd, 2001). TNFα dan interleukin-1 (IL-1) banyak terdapat
di dalam jaringan epidermis. Pada saat jaringan kulit mengalami luka, TNFα dan
interleukin-1 (IL-1) dilepaskan dari jaringan epidermis dan memacu aktivasi
NF-kB. Aktivasi NF-kB menyebabkan terjadinya proses transkripsi gen
mediator-mediator inflamasi (Robert and Kupper, 1999). Salah satu mekanisme aktivitas
antiinflamasi kurkumin yaitu dengan cara menghambat kerja TNFα dan
interleukin-1 (IL-1). Penghambatan kerja TNFα dan interleukin-1 (IL-1)
menyebabkan proses transkripsi gen mediator-mediator inflamasi tidak terjadi
sehingga proses inflamasi terhambat (Chainani-Wu, 2003). Menurut Jurenka
(2009), menyatakan bahwa kurkumin dapat juga menghambat proses inflamasi
dengan cara menghambat metabolisme asam arakidonat melalui jalur
siklooksigenae dan jalur lipooksigenase.
Pemilihan formulasi untuk sediaan topikal perlu diperhatikan karena
memperantarai zat aktif masuk ke dalam jaringan kulit. Menurut Sandhu et.al
(2012),interaksi zat aktif, sistem pembawa dan karakteristik kulit mempengaruhi
permeasi dan bioavaibilitas suatu obat. Sediaan krim adalah sediaan semisolid
dengan sistem emulsi yang diaplikasikan pada kulit. Pelepasan zat aktif pada krim
dengan basis o/w lebih mudah dibandingkan dengan basis w/o (Sandhu et al,
krimo/w lebih mudah menyebar rata dan mudah dibersihkan. Biocream®®
merupakan sistem emulsi yang stabil dengan distribusi minyak dan air yang
merata (ambifilik) yang membuat Biocream®® memiliki sifat emulsi minyak
dalam air dan emulsi air dalam minyak. Biocream®® dapat dicampur dengan air,
zat-zat yang larut dalam air, minyak maupun zat-zat yang larut dalam minyak
tanpa mengganggu stabilitasnya.
Kulit memiliki barrier yang disebut stratum corneum yang dapat
menghambat permeasi dari zat aktif. Barrier ini sangat selektif terhadap molekul
yang akan masuk ke dalam jaringan kulit. Hanya molekul yang memiliki sifat
fisika-kimia yang spesifik dan sesuai dengan stratum corneum yang dapat
melewati barrier ini. Hal ini membuat penetration enhancer di dalam formulasi
sediaan topikal diperlukanuntuk membantu zat aktif masuk ke dalam jaringan
kulit (Fox, Gerber, Plessis, dan Hamman, 2011). Menurut Fox dkk. (2011),
peppermint oil merupakan salah satu jenis essential oil yang dapat digunakan
sebagai penetration enhancer karena peppermint oil dapat mengubah integritas
1. Perumusan masalah
a. Apakah ekstrak temu putih dapat dibuat sediaan topikal dan memenuhi
kriteria sebagai sediaan krim dengan basis o/w dan Biocream®?
b. Apakah ekstrak temu putih dapat memberikan aktivitas antiinflamasi dalam
penggunaannya secara topikal dengan bentuk sediaan krim dengan basis o/w
dan Biocream®?
c. Bagaimana pengaruh peppermint oil sebagai penetration enhancer terhadap
peningkatan aktivitas antiinflamasi pada sediaan krim temu putih.
2. Keaslian penelitian
Sejauh pengetahuan peneliti, penelitian mengenai formulasi sediaan krim
ekstrak etanolik rimpang temu putih dengan pengujian aktivitasnya sebagai
antiinflamasi belum pernah dilakukan. Adapun penelitian yang terkait tentang
penelitian ini yaitu:
a. Anti-inflammatory Efficacy Of Curcuma Zedoaria Rosc Root Extracts.
Penelitian dilakukan oleh Kaushik dan Jalalpure (2011). Pada penelitian ini
dilakukan uji aktivitas antiinflamasi ekstrak temu putih menggunakan 3
pelarut yaitu petroleum eter, kloroform, dan etanol yang diberikan secara oral
pada dosis 200 mg/kg dan 400 mg/kg. Metode yang digunakan adalah
carrageenan and histamine induced metode. Pengukuran volume edema
menggunakan petroleum eter dan kloroform semuanya memiliki aktivitas
antiinflamasi dibandingkan dengan kontrol obat standar (Indometasin 10
mg/kg i.p dan Rumalaya forte 200 mg/kg).
b. Efek ekstrak etanol rimpang temu putih (Curcuma zedoaria Rosc.) terhadap
pertumbuhan tumor paru fase post inisiasi pada mencit betina diinduksi
Benzo[a]piren.
Penelitian yang dilakukan oleh Murwanti, Meiyanto, Nurrochmad, dan
Kristina (2004). Penelitian ini meneliti kemampuan ekstrak etanol rimpang
temu putih untuk menghambat pertumbuhan tumor paru pada mencit betina.
Hasilnya ekstrak etanol rimpang temu putih mampu menghambat
pertumbuhan tumor paru pada mencit betina yang diinduksi oleh
benzo[a]piren pada dosis 250 mg/kgBB (49,63%), dosis 500 mg/kgBB
(73,33%), dan dosis 750 mg/kgBB (77,78%).
c. Formulation and Evaluation of Curcuminoid Based Herbal Cream.
Penelitian dilakukan oleh Sahu, Jha, dan Dubey (2011). Penelitian ini
melakukan formulasi kosmetik herbal berupa sediaan krim dengan zat aktif
serbuk rimpang kunyit. Kurkumin yang terkandung yaitu sebanyak 3,79 g per
100 g serbuk rimpang kunyit. Bahan yang digunakan dalam formulasi yaitu:
asam stearat, isopropil alkohol, TEA, almond oil, light liquid paraffin oil,
moisturizer conditioner, dan cetyl alcohol. Evaluasi yang dilakukan yaitu tipe
d. Analgesic and Antimicrobial Activities of Curcuma zedoaria.
Penelitian ini dilakukan oleh Das dan Rahman (2012). Penelitian ini
melakukan uji aktivitas dari daun, batang dan rimpang Curcuma zedoaria.
Ketiga bagian simplisia diekstraksi menggunakan metanol dan eter dengan
metode maserasi. Metode uji analgesik yang dilakukan menggunakan acetic
acid induced writhing effect method. Ekstrak metanol dan eter menunjukkan
efek analgesik. Untuk uji antimikroba dilakukan pada bakteri gram positif dan
gram negatif dan fungi menggunakan metode dilusi. Pada hasil pengujian
didapatkan ekstrak metanol dan eter daun Curcuma zedoiaria memberikan
zona hambat sebesar 10-12 mm pada bakteri gram postif dan negatif dan pada
fungi. Ekstrak eter dan metanol rhizoma, memberikan zona hambat sebesar
11-14 mm pada bakteri gram postif dan negatif dan pada fungi.Untuk ekstrak
batang baik ekstrak metanol dan eter memberikan zona hambat sebesar 7 mm
pada bakteri gram postif dan negatif dan pada fungi.
3. Manfaat penelitian
a. Manfaat teoretis : penelitian ini dapat memberikan informasi kepada
masyarakat luas dan para farmasis bahwa tanaman temu putih memiliki
khasiat yang dapat digunakan sebagai obat herbal dengan kegunaannya
sebagai antiinflamasi.
b. Manfaat praktis : penelitian ini dapat menghasilkan produk lain sediaan
B. Tujuan Penelitian 1. Tujuan umum
Untuk memperoleh formulasi sediaan topikal krim ekstrak temu putih sebagai
obat herbal antiinflamasi.
2. Tujuan khusus
a. Untuk mengetahui apakah ekstrak temu putih dapat dibentuk sediaan krim
dan memenuhi kriteria sebagai suatu sediaan krim dengan basis o/w dan
Biocream®.
b. Untuk mengetahui aktivitas antiinflamasi ekstrak temu putih dalam
penggunaannya secara topikal dengan bentuk sediaan krim dengan basis
o/w dan Biocream®.
c. Untuk mengetahui apakah peppermint oil dapat digunakan sebagai
penetration enhancer yang dapat membantu meningkatkan aktivitas
9
BAB II
PENELAAHAN PUSTAKA
A. Inflamasi
Inflamasi adalah reaksi biologis karena adanya gangguan pada jaringan
tubuh. Gangguan ini dapat terjadi karena adanya infeksi dari patogen, luka,
terpapar kontaminan, dan kerusakan sel (Medzihitov, 2008). Dengan adanya
gangguan pada jaringan, maka terjadi pelepasan mediator kimiawi dari jaringan
yang rusak (Mycek, 2001).
Inflamasi dibedakan menjadi 2 yaitu inflamasi akut dan inflamasi kronis
(Gard, 2001). Gejala inflamasi yang biasa terjadi adalah rubor, kalor, dolor,
tumor, dan functio laesa (Muschler, 1991). Gejala-gejala ini merupakan akibat
adanya pelepasan mediator-mediator inflamasi seperti histamin, serotonin,
prostaglandin dan kinin. Adanya kerusakan sel, asam arakhidonat dibebaskan
melalui aktivasi fosfolipase A2 dan akan diubah menjadi senyawa mediator
melalui 2 jalur utama yaitu jalur siklooksigenase dan jalur lipooksigenase.
Pada jalur lipooksigenase akan dihasilkan leukotrien yang merupakan
suatu mediator inflamasi, sedangkan pada jalur siklooksigenase, akan dihasilkan
senyawa eukasanoid seperti prostaglandin, prostasiklin, dan tromboksan.
Prostaglandin dibentuk melalui jalur siklooksigenase-2, sedangkan prostasiklin
dan tromboksan dibentuk melalui jalur siklooksigenase-1. Prostaglandin
prostasiklin dan tromboksan memiliki fungsi untuk melakukan perlindungan pada
lambung dan koagulasi darah (Kawai, 1998).
B. Obat Anti Inflamasi Non Steroid
Obat antiinflamasi non steroid bekerja dengan cara menghambat kerja
enzim siklooksigenase dan mengurangi produksi prostaglandin. Prostaglandin
merupakan derivat dari asam arkidonat yang dihasillkan oleh fosfolipid pada
membran sel. Enzim siklooksigenase memiliki 2 isoform yaitu 1 dan
COX-2. COX-2 merupakan enzim yang diinduksi oleh adanya inflamasi. COX-2
memiliki peran utama dalam pemecahan asam arakidonat menjadi prostaglandin
H2 (PGH2). Prostaglandin dilepaskan pada saat kondisi jaringan rusak dan adanya
inflamasi yang menyebabkan terjadinya rasa sakit (Schuelert dkk., 2011).
Diklofenak merupakan obat antiinflamasi non steroid yang bekerja
dengan menghambat enzim siklooksigenase. Diklofenak tidak selektif dalam
menghambat enzim siklooksigenase, diklofenak dapat menghambat COX-1 dan
COX-2. Padahal yang berperan dalam efek penghilang rasa sakit adalah COX-2.
Adanya penghambatan pada COX-1 memberikan efek samping pada
gastrointestinal (Schuelert dkk., 2011).
Pengembangan obat antiinflamasi non steroid topikal merupakan cara
untuk mencegah adanya efek samping pada gastrointestinal. Obat antiinflamasi
non steroid yang digunakan secara topikal memiliki mekanisme yang sama seperti
penggunaan oral yaitu menghambat sintesis prostaglandin, tetapi untuk obat
antiinflamasi non steroid topikal hanya memberikan efek lokal. Untuk konsentrasi
sistemik, jumlahnya 17 kali lebih rendah dibandingkan dengan penggunaan oral
(Schueler dkk., 2011).
C. Temu Putih (Curcuma Zedoaria Berg. Roscoe)
1. Nama daerah
Kunir putih (Jawa), temu putih (Jakarta), koneng tega (Sunda).
2. Deskripsi tanaman
Klasifikasi tanaman temu putih adalah sebagai berikut: (Windono, 2002)
Division : Spermathopyta
Subdivisio : Angiospermae
Kelas : Monocotyledonae
Bangsa : Zingiberales
Suku : Zingiberaceae
Marga : Curcuma
Jenis : Curcuma zedoaria (Berg) Roscoe
Tumbuhan berhabitus terna setahun, tinggi dapat mencapai 2 meter,
batang semu berwarna hijau atau cokelat tua, batang sejati berupa rimpang
berkembang sempurna di dalam tanah, beruas-ruas, bercabang-cabang kuat,
berwarna cokelat muda sampai cokelat gelap, bagian dalam berwarna kuning,
jingga dan ada sedikit warna biru kehijauan, berbau aromatik begitu pula pada
umbinya. Setiap batang semu tersusun atas 2-9 helai daun yang berbentuk lonjong
sampai lanset, berwarna hijau atau coklat keunguan terang sampai gelap, panjang
31-84 cm, lebar 10-18 cm, panjang tangkai daun (termasuk helaian) 43-80 cm.
Buah berambut, panjang 2 cm (BPOM, 2010).
3. Kandungan
Tanaman temu putih memiliki kandungan minyak atsiri berupa
zingiberen, 1,8 sineol, D-kampora, D-kampen, Dborneol, α pinen, kurkumol,
zederon, kurkumeneol, kurkulon, furanodienon, isofuranodienon dan kandungan
kurkuminoid yang terdapat di temu putih berupa kurkumin, dismetoksikurkumin,
bisdesmetoksikurkumin (BPOM, 2010).
4. Efek farmakologi
Menurut Murwanti, Meiyanto, Nurrochmad, dan Kristina (2004), ekstrak
etanol rimpang temu putih mampu menghambat pertumbuhan tumor paru pada
mencit betina yang diinduksi oleh benzo[a]piren pada dosis 250 mg/kgBB
(49,63%), dosis 500 mg/kgBB (73,33%), dan dosis 750 mg/kgBB (77,78%).
Pada penelitian Kaushik dan Jalalpure (2011), menunjukkan bahwa pada
aktivitas antiinflamasi dengan pemberian secara oral pada dosis 200 mg/kg dan
400 mg/kg
D. Kurkumin
Kurkuminoid merupakan senyawa fenolik yang berasal dari akar
Curcuma spp. (Zingiberaceae). Kurkuminoid ada 3 jenis yaitu kurkumin,
demetoksikurkumin, dan bisdemetoksikurkumin. Kurkumin merupakan senyawa
lipofilik polifenol yang tidak larut air, tetapi larit di dalam aseton,
dimetilsulfoksida, dan etanol. Kurkumin tidak stabil pada pH basa yang
menyebabkan kurkumin dapat terdegradasi, tetapi pada pH asam, degradasi
kurkumin lebih lama. Kurkumin tidak stabil terhadap cahaya sehingga dalam
penyimpanannya harus dilindungi dari cahaya. Kurkumin memiliki bobot molekul
368,37 dan melting point pada suhu 1830C (Sharma, Gescher, dan Steward, 2005).
Kurkumin memiliki aktivitas antiinflamasi dengan mekanisme
menurunkan aktivitas dari enzim siklooksigenase-2 (COX-2) dan lipooksigenase,
menghambat produksi sitokin, tumor necrosis factor-alpha (TNF-α), interleukin
(IL)-1,-2,-6,-8, dan -12, migration inhibitory protein (MCP) (Jurenka, 2009).
E. Ekstraksi
Ekstraksi tanaman obat adalah pemisahan secara kimia atau fisika
sejumlah bahan padata atau bahan cair dari tanaman obat menggunakan pelarut
yang sesuai. Sediaan yang diperoleh dengan cara ekstraksi tanaman obat disebut
ekstrak. Ekstrak kental adalah ekstrak yang didapatkan dari ekstrak cair yang
duapkan larutan penyarinya secara hati-hati. Ekstrak kental mengandung
bermacam-macam konsentrasi sisa kelembaban (Agoes, 2009).
Dalam pembuatan ekstrak untuk keperluan farmasis, perlu diperhatikan
beberapa hal yang penting yaitu : 1) jumlah simplisia yang akan diekstraksi; 2)
derajat kehalusan simplisia; 3) jenis pelarut; 4) suhu; 5) lama waktu penyarian;
dan 6) metode dan proses ekstraksi (Agoes, 2009).
F. Maserasi
Maserasi merupakan cara ekstraksi yang sederhana. Maserasi dilakukan
dengan cara merendam simplisia dalam pelarut dengan beberapa kali pengocokan
atau pengadukan pada temperatur ruangan. Cairan penyari akan menembus
dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif, zat aktif
akan larut, dan karena adanya perbedaan konsentrasi antara larutan zat aktif di
dalam sel dengan yang di luar sel, maka larutan yang terpekat didesak keluar.
(Depkes RI, 1986).
Secara teknologi termasuk ekstraksi dengan prinsip metode pencapaian
konsentrasi pada kesetimbangan. Maserasi kinetik berarti dilakukan pengadukan
yang kontinyu (terus-menerus). Remaserasi berarti dilakuakn pengulangan
penambahan pelarut setelah dilakukan penyaringan maserat pertama dan
seterusnya. Keuntungan penyarian dengan cara maserasi adalah cara pengerjaan
dan peralatan yang digunakan sederhana dan mudah diusahakan. (Depkes RI,
G. Krim
Krim adalah bentuk sediaan setengah padat mengandung satu atau lebih
bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai. Istilah ini
secara tradisional telah digunakan untuk sediaan setengah padat yang mempunyai
konsistensi relatif cair diformulasi sebagai emulsi air dalam minyak atau minyak
dalam air (Depkes RI, 1995). Emulsi merupakan sediaan yang mengandung dua
zat yang tidak tercampur, biasanya air dan minyak yang nantinya akan terdispersi
menjadi butiran-butiran kecil dalam cairan lain. Emulgator merupakan komponen
yang penting agar memperoleh emulsi yang stabil. Emulgator bekerja dengan
membentuk lapisan di sekeliling butiran-butiran tetesan yang terdispersi dan
lapisan in berfungsi untuk mencegah terjadinyas koalesen dan terpisahnya dua
komponen tersebut (Anief, 2000).
Krim terdiri dari obat terlarut tersuspensi dalam basis krim air larut atau
hilang dan dapat berupa :
a. Air dalam minyak (w/o)
b. Minyak dalam air (o/w) (Allen, 2002).
H. Peppermint Oil
Peppermint oil diperoleh dari daun Mentha piperita L. dan M. Arvensis
var. piperascens dengan metode destilasi. Senyawa yang terkandung di dalam
peppermint oil yaitu limonene, cineole, menthone, methofuran, isomenthone,
Menurut Fox dkk. (2011) peppermint oil dapat digunakan untuk
mengurangi rasa sakit, mengontrol nafsu makan, menstimulasi fungsi sistem
pencernaan, antiinflamasi, antitumor, antivirus, antibakteri, dan antiparasit.
I. Karagenan
Karagenan merupakan poligalaktan sulfat dengan 15-40% ester-sulfat.
Karagenan digunakan secara luas sebagai bahan induksi edema pada telapak aki
tikus untuk menlihat aktivitas antiinflamasi. Adanya injeksi karagenan pada
telapak kaki akan menyebabkan produksi mediator inflamasi seperti histamin,
bradikin, dan serotonin (Bartosikova, 2013).
J. Landasan Teori
Inflamasi adalah reaksi biologis karena adanya gangguan pada jaringan
tubuh. Gangguan ini dapat terjadi karena adanya infeksi dari patogen, luka,
terpapar kontaminan, dan kerusakan sel (Medzihitov, 2008). Salah satu
mekanisme karagenan yang dapat menyebabkan terjadinya edema pada kulit
yaitu dengan emmacu pelepasan interleukin dan TNF α. Jaringan epidermis kulit
merupakan sumber penyimpanan TNFα dan interleukin-1 (IL-1), sehingga saat
kulit diinduksi dengan karagenan, maka TNFα dan interleukin-1 (IL-1) akan
dilepaskan dari jaringan epidermis. TNFα dan interleukin-1 (IL-1) memacu
aktivasi NF-kB. Aktivasi NF-kB menyebabkan terjadinya proses transkripsi gen
mediator-mediator inflamasi yang berkaitan erat dengan kerja dari
siklooksigenase-2 dan iNOS yang menyebabkan terjadinya edema (Robert and
Kupper, 1999)
Temu putih mengandung minyak atsiri berupa zingiberen, 1,8 sineol,
D-kampora, D-kampen, Dborneol, α pinen, kurkumol, zederon, kurkumeneol,
kurkulon, furanodienon, isofuranodienon dan kandungan kurkuminoid yang
terdapat di temu putih berupa kurkumin, dismetoksikurkumin,
bisdesmetoksikurkumin. Kurkumin memiliki aktivitas antiinflamasi dengan
mekanisme menurunkan aktivitas dari enzim siklooksigenase-2 (COX-2) dan
lipooksigenase, menghambat produksi sitokin, tumor necrosis factor-alpha
(TNF-α), interleukin (IL)-1,-2,-6,-8, dan -12, migration inhibitory protein (MCP)
Krim adalah bentuk sediaan setengah padat mengandung satu atau lebih
bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai. Istilah ini
secara tradisional telah digunakan untuk sediaan setengah padat yang mempunyai
konsistensi relatif cair diformulasi sebagai emulsi air dalam minyak atau minyak
dalam air (Depkes RI, 1995). Dalam formulasi sediaan topikal perlu diperhatikan
kemampuan penetrasi zat aktif untuk masuk ke dalam jaringan kulit karena kulit
memiliki barrier yang kompleks. Untuk membantu penetrasi zat aktif masuk ke
dalam jaringan kulit diperlukan adanya penambahan penetration enhancer.
Peppermint oil merupakan salah satu essential oil yang dapat digunakan sebagai
penetration enhancer. Peppermint oil dapat memberikan efek pada integritas
kulit sehingga membantu zat aktif masuk ke dalam jaringa kulit. Peppermint oil
dapat digunakan sebagai penetration enhancer dalam konsentrasi minimal sebesar
0,1% (Fox dkk., 2011).
K. Hipotesis
1. Ekstrak temu putih dapat dibuat dalam bentuk sediaan krim dengan basis o/w
dan Biocream® yang berkualitas
2. Sediaan krim temu putih dapat memberikan aktivitas antiinflamasi
3. Peppermint oil dapat digunakan sebagai penetration enhancer yang mampu
20
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Uji aktivitas dan formulasi sediaan krim ekstrak temu putih sebagai
antiinlfamasi ini merupakan penelitian eksperimental murni dengan rancangan
acak pola searah.
B. Variabel Penelitian
Dalam penelitian yang berjudul “Formulasi Sediaan Krim Ekstrak
Etanolik Rimpang Temu Putih (Curcuma zedoaria Berg. Roscoe) Dengan
Pengujian Aktivitasnya Sebagai Antiinflamasi” terdapat dua variabel, yaitu:
1. Variabel utama
Variabel utama dalam penelitian ini meliputi:
a. Variabel bebas : basis krim (basis o/w dan basis Biocream®) dan
konsentrasi peppermint oil.
b. Variabel tergantung : tebal edema kaki pada tikus (mm) dan sifat fisik
2. Variabel pengacau
a. Variabel pengacau terkendali
1) Subjek uji : tikus betina galur Wistar
2) Umur subjek uji : 2 bulan
3) Berat badan subjek uji : 120-180 gram
4) Keadaan subjek uji : sehat
5) Proses pembuatan sediaan krim : suhu pemanasan
b. Variabel pengacau tak terkendali : suhu ruangan dan kelembaban
udara.
C. Definisi Operasional
1. Krim temu putih adalah sediaan krim yang mengandung ekstrak temu putih
sebagai zat aktif yang diindikasikan untuk antiinflamasi dengan formulasi
yang tercantum dalam penelitian ini.
2. Ekstrak temu putih adalah ekstrak kental rimpang temu putih yang diekstraksi
menggunakan penyari etanol 70% dengan prosedur ekstraksi yang sesuai
dalam penelitian ini.
3. Kontrol positif adalah pembanding yang digunakan dalam uji aktivitas
4. % inhibition adalah nilai presentase kemampuan menghambat pembengkakan
edema pada telapak kaki tikus.
5. Aktivitas antiinflamasi adalah kemampuan suatu senyawa untuk menghambat
pembengkakan pada kaki tikus yang ditunjukkan dengan nilai % inhibition.
D. Bahan
Bahan yang digunakan dalam penelitian ini adalah temu putih (BPTO),
etanol 70% (Bratachem), karagenan (Merck), paraffin liquidum (Bratachem),
asam stearat (Bratachem), NaCl, TEA, aquadest, aerosil, peppermint oil
(Laboratorium FTS-Solid Fakultas Farmasi Universitas Sanata Dharma), tween 80
(Bratachem), span 80 (Bratachem), aerosil, Biocream® (Merck) dan hewan uji
tikus galur Wistar (Laboratorium Imono Fakultas Farmasi Universitas Sanata
Dharma), Voltaren® emulgel (NOVARTIS).
E. Alat
Alat yang digunakan dalam penelitian ini adalah alat-alat gelas (Beaker
glass, pengaduk, Erlenmeyer, gelas ukur dan labu ukur merk Pyrek), rotary
evaporator (Buchi Labortechnik AG CH-9230), jangka sorong Digital Caliper
Wipro, mixer, spuit, waterbath(Memmert), termometer, indikator pH universal,
neraca analitik (Mettler Toledo GB 3002), viscotester VT-04 (Rion™ Japan), alat
uji daya sebar (modifikasi USD), mortir, stamper, cawan porselen dan perangkat
F. Formula
1. Formula krim ekstrak temu putih
Nama F2 : Basis krim o/w dengan ekstrak temu putih 7%
F3 : Basis krim o/w dengan ekstrak temu putih 7% dan peppermint oil 0,5%
F4 : Biocream®
F5 : Biocream®dengan peppermint oil
F6 : Biocream® dengan ekstrak temu putih 7%
F7 : Biocream® dengan ekstrak temu putih 7% dan peppermint oil 0,5%
G. Tata Cara Penenlitian
1. Pembuatan serbuk temu putih
Dimasukkan sejumlah simplisia rimpang temu putih ke dalam alat
penyerbukan. Setelah selesai, hasil penyerbukan diayak dengan pengayak
nomor 20. Hasil pengayakan dimasukkan ke dalam wadah tertutup dan
disimpan di tempat yang kering dan dihindarkan dari sinar matahari.
2. Pembuatan ekstrak temu putih
Ditimbang serbuk simplisia temu putih sebanyak 20 gram, lalu dimasukkan ke
dalam maserator. Sebanyak 200 ml etanol 70% ditambahkan sebagai penyari.
Maserasi dilakukan dengan menggunakan alat orbital shaker selama 1x24 jam.
Setelah 24 jam, dilakukan penyaringan dengan menggunakan alat corong
Buchner dan pompa vacuum serta kertas saring untuk memisahkan ekstrak cair
dengan ampas serbuk simplisianya. Ekstrak cair yang sudah diambil kemudian
dimasukkan ke rotary evaporator untuk dilakukan proses penguapan penyari
pada suhu 600C. Hasil dari rotary evaporator kembali diuapkan menggunakan
waterbath pada suhu 70oC. Selanjutnya dilakukan penyimpanan di dalam oven
pada suhu 40o C tiap 24 jam, hingga didapatkan bobot tetap.
3. Standarisasi ekstrak temu putih
a. Penetapan kadar kurkumin dengan metode KLT-densitometri
Ekstrak temu putih ditimbang dengan seksama dan dilarutkan
takar. Evaporasikan, dan add hingga 500 µl. Spoting sampel sebanyak 10
µl pada plate silika gel 60 F254 dengan microsyringe, sertakan regresi
standar kurkumin sintesa. Masukkan plate ke dalam chamber yang telah
berisi jenuh fase gerak kloroform-metanol (98-2). Elusikan hingga batas,
diangkat dan dianginkan. Densito spot kurkumin pada panjang gelombang
425 nm dan hitung kadar kurkumin.
b. Penetapan kadar air dengan metode gravimetri
Timbang krus kosong (A) dan timbang sampel homogen, masukkan di
dalam krus porselen (B). Panaskan di dalam oven pada suhu 1050C selama
3 jam hingga berat konstan. Eksikator dimasukkan dan ditimbang (C).
Kadar air dihitung dengan rumus :
4. Formulasi krim
a. Basis krim o/w
Pembuatan basis krim untuk formula F0 dan F1 dengan cara fase minyak
(paraffin liquidum, asam stearat, cetil alkohol, tween 80 dan span 80) dan
fase air (aerosil, TEA, dan aquadest) masing-masing dipanaskan diatas
waterbath pada suhu 60o-70o C sampai melebur. Fase air dan fase minyak
dicampur bersamaan menggunakan mikser selama 5 menit. Untuk F1,
peppermint oil dicampurkan setelah sediaan dingin dan dicampur
b. Krim ekstrak temu putih
1) Basis krim o/w: Pembuatan krim untuk formula F2 dan F3 dengan
cara fase minyak (paraffin liquidum, asam stearat, cetil alkohol,
tween 80 dan span 80) dan fase air (ekstrak temu putih, aerosil,
TEA, dan aquadest) masing-masing dipanaskan diatas waterbath
pada suhu 60o - 70o C sampai melebur. Fase air dan fase minyak
dicampurkan bersamaan menggunakan mikser selama 5 menit.
Untuk formula F3, penambahan peppermint oil dilakukan di akhir
setelah suhu pencampuran dingin. Pencampuran menggunakan
mikser selama 2 menit.
2) Basis Biocream®: Pembuatan krim untuk formula F6 dan F7
dilakukan dengan mencampurkan Biocream® dengan ekstrak temu
putih dan dilakukan pencampuran menggunakan bantuan alat mikser
selama 5 menit. Untuk F7 ditambahkan peppermint oil, dimikser
selama 5 menit.
5. Uji sifat fisis krim dan stabilitas krim
a. Uji orgnoleptis. Dilihat warna dan bau dari krim yang terbentuk. Uji
homogenitas dilakukan dengan cara menimbang 1 g sediaan krim pada
gelas objek dan ditutup dengan gelas objek lainnya. Kemudian diletakkan
sediaan. Pengujian dilakukan pada hari ke-2 dan ke-28 setelah pembuatan
sediaan krim.
b. Uji pH. Pengecekan pH krim menggunakan indikator pH universal.
Pengujian dilakukan pada hari ke-2 dan ke-28 setelah pembuatan sediaan
krim.
c. Uji daya sebar. Ditimbang 1 g krim dan diletakkan ditengah kaca bundar,
kemudian timbang kaca penutup dan diletakkan di atas massa krim.
Dibiarkan selama 1 menit kemudian diukur diameter krim yang menyebar
dengan mengambil panjang diameter rata-rata dari 4 sisi. Ditambahkan 50
g beban tambahan dan didiamkan selama 1 menit kemudian diukur
diameter reratanya. Dilanjutkan sebanyak 3 kali dengan menambah beban
tambahan 50 g kemudian dihitung luas lingkaran yang didapatkan.
Pengujian dilakukan pada hari ke-2 dan ke-28 setelah pembuatan sediaan
krim.
d. Uji viskositas. Sebanyak 20 gram krim dimasukkan perlahan-lahan ke
dalam wadah dan dipasang pada viscotester. Dilihat nilai viskositas yang
ada pada alat setelah jarum penunjuk stabil. Pengujian dilakukan pada hari
ke-2 dan ke-28 setelah pembuatan sediaan krim. Dari data uji viskositas
pada hari ke-2 dan ke-28 dihitung % pergeseran viskositas dengan
menggunakan rumus:
%
6. Uji aktivitas antiinflamasi sediaan krim temu putih
a. Penyiapan hewan uji
Hewan uji yang digunakan dalam penelitian ini adalah Tikus betina, galur
Swiss, usia 2-3 bulan, dengan berat badan 120-180 gram. Tikus
dipuasakan 1 hari sebelum penggunaaannya. Disiapkan 6 tikus untuk tiap
kontrol (F0 dan F4) dan perlakuan (F1, F2, F3, F5, F6, F7, dan Voltaren®
emulgel).
b. Pembuatan larutan NaCl 0,9%
Ditimbang 0,225 g NaCl, larutkan dengan aquadest di dalam labu takar 25
ml.
c. Pembuatan suspensi karagenan 1%
Ditimbang 0,1 g karagenan, larutkan dengan larutan NaCl 0,9% di dalam
labu takar 10 ml.
d. Uji Aktivitas antiinflamasi dengan metode carrageenan-induced rat paw
edema (Kharat et.al (2010)).
Masing-masing kaki tikus dioleskan dengan formula yang sesuai dengan
kelompoknya sebanyak 0,25 g dengan cara dioleskan sebanyak 20 kali.
Setelah 1 jam pemberian formula, 0,1 ml suspensi karagenan 1% diberikan
secara subplantar di masing-masing telapak kaki tikus. Volume
setelah pemberian suspensi karagenan 1%. % inhibition dihitung dengan
menggunakan rumus:
% inhibition =
H. Analisis Hasil
Data penelitian yang berupa % inhibition dari tiap formula diuji
normalitasnya menggunakan metode Shapiro.test. Jika didapatkan semua data
terdistribusi normal, maka dilanjutkan pada uji Levene.test untuk melihat
homogenitas. Selanjutnya data % inhibition dari tiap formula dibandingkan
menggunakan metode ANOVA yang dilanjutkan dengan uji TukeeyHSD dan uji
one tail independent T.test untuk melihat perbedaan dari tiap-tiap formula. Jika
data tidak terdistribusi normal pada uji Shapiro.test, maka uji selanjutnya adalah
membandingkan data antar formula dengan uji Wilcoxon.test. Semua uji analisis
di atas dilakukan dengan menggunakan bantuan program statistik R dengan taraf
30
BAB IV
HASIL DAN PEMBAHASAN
Penelitian ini bertujuan untuk memperoleh formulasi sediaan topikal
krim temu putih sebagai obat antiinflamasi. Simplisia rimpang temu putih yang
digunakan dalam penelitian ini telah dilakukan determinasi oleh Balai Besar
Penelitian Dan Pengembangan Tanaman Obat Dan Obat Tradisional
Tawangmangu dengan hasil yang menunjukkan bahwa simplisia yang digunakan
benar merupakan simplisia rimpang temu putih dengan kadar air 9 % (Lampiran
10). Ekstrak temu putih yang digunakan sebagai zat aktif dibuat dalam bentuk
sediaan krim. Penggunaan sediaan krim memberikan keuntungan karena memiliki
2 fase yaitu fase minyak dan fase air, sehingga ekstrak temu putih dapat
diformulasikan dan dijaga kompatibilitas dan stabilitasnya di dalam sediaan krim.
A. Hasil Uji Standarisasi Ekstrak Temu Putih
Pada penelitian ini dilakukan 2 uji standarisasi ekstrak temu putih, yaitu
penetapan kadar kurkumin dan penetapan kadar air. Tujuan dilakukan penetapan
kadar kurkumin yaitu untuk mengetahui jumlah kadar kurkumin yang terdapat di
dalam ekstrak temu putih. Kurkumin diduga merupakan salah satu senyawa yang
memberikan aktivitas antiinflamasi di dalam ekstrak temu putih karena kurkumin
telah tebukti memiliki aktivitas antiinflamasi. Dari hasil penetapan kadar
kurkumin dengan menggunakan metode KLT-densitometri didapatkan kadar
Tujuan penetapan kadar air adalah untuk mengetahui jumlah kandungan
air di dalam ekstrak temu putih. Penetapan kadar air menggunakan metode
gravimetri. Jumlah kandungan air di dalam ekstrak sangat penting diketahui
karena jika kadar air terlalu tinggi, maka akan sangat berpengaruh terhadap
stabilitas ekstrak. Kadar air yang tinggi akan memacu pertumbuhan mikroba dan
mengaktifkan kerja enzim-enzim dari mikroba tersebut. Kadar air yang
didapatkan pada penelitian ini sebesar 24,25% (Lampiran 1). Jumlah tersebut
melebihi batas standar yang ditetapkan menurut BPOM (2004) yang menyebutkan
kadar air untuk ekstrak etanol rimpang temu putih tidak lebih dari 13,5%, tetapi
dalam penelitian ini kadar air sebesar 24,25% belum bisa dipastikan bahwa
seluruhnya merupakan air karena metode yang digunakan adalah gravimetri yang
tidak selektif terhadap air. Ketidakselektifan ini disebabkan karena metode
gravimetri menggunakan pemanasan yang tinggi pada suhu 1050 C, sehingga
semua zat cair yang menguap pada suhu tersebut terhitung sebagai kadar air.
B. Hasil Uji Organoleptis
Formulasi sediaan krim temu putih dibuat dengan menggunakan dua jenis
basis yaitu basis krim o/w dan basis Biocream®. Penggunaan dua basis ini
bertujuan untuk melihat pengaruh basis terhadap pelepasan zat aktif dari ekstrak
temu putih yang dilihat dari aktivitas antiinflamasi.
Sediaan krim yang telah dibuat kemudian dilakukan uji organoleptis yang
meliputi warna, bau dan homogenitas. Uji organoleptis berfungsi sebagai
Kriteria
2 hari 28 hari
F2 F3 F6 F7 F2 F3 F6 F7
Bau temulawak mint Biocream
® mint temulawak mint
nitas homogen homogen homogen homogen homogen homogen Homogen homogen
F2 : Basis krim o/w + ekstrak temu putih 7%
F3 : Basis krim o/w + ekstrak temu putih 7% + peppermint oil 0,5%
F6 : Biocream® + ekstrak temu putih 7%
F7 : Biocream® + ekstrak temu putih 7% + peppermint oil 0,5%
Dilihat dari tabel II, pada waktu hari ke-2 seluruh formula yang dibuat
homogen. Warna untuk F3, F6, dan F7 sama yaitu cokelat, sedangkan untuk F2
warna yang dihasilkan adalah cokelat muda. Pada kriteria bau, untuk krim temu
putih basis o/w dengan formula F2 memiliki aroma khas seperti temulawak,
sedangkan pada formula F3 memiliki aroma mint. Perbedaan aroma ini
disebabkan karena adanya penambahan peppermint oil pada formula F3 sehingga
aroma dari peppermint oil mengalahkan aroma dari ekstrak temu putih. Pada
sediaan krim temu putih dengan basis Biocream® dengan formula F6 memiliki
aroma khas dari Biocream®, sedangkan pada formula F7 memiliki aroma mint.
Biocream®yang digunakan sebagai basis krim memiliki aroma yang khas
sehingga aroma dari ekstrak temu putih tidak terasa pada formula F6, sedangkan
pada formula F7 adanya penambahan peppermint oil membuat aroma mint lebih
tercium dibandingkan dengan aroma dari Biocream®. Dari hasil keseluruhan uji
organoleptis, diharapkan krim temu putih yang dibuat dapat memenuhi aspek
acceptability.
C. Hasil Uji pH Krim Temu Putih
Pada pengujian pH sediaan krim temu putih digunakan indikator
universal. Hasil pengujian dapat dilihat pada tabel III.
Formula 2 hari (pH) 28 hari (pH)
sehingga sediaan krim temu putih yang dihasilkan masuk dalam rentang pH kulit.
Hal ini diharapkan agar sediaan krim temu putih yang dibuat tidak mengiritasi
kulit, karena pH sediaan dapat berpotensi menyebabkan iritasi pada kulit.
D. Hasil Uji Viskositas dan Daya Sebar
Pengujian viskositas dan daya sebar dilakukan setelah 48 jam pembuatan
krim. Hal ini bertujuan agar sediaan krim yang dibuat telah berada dalam kondisi
yang stabil karena pengaruh dari proses pembuatan seperti suhu dan pengadukan
telah hilang. Hasil pengujian viskositas dan daya sebar dapat dilihat pada tabel IV.
Dari hasil pada tabel IV dapat dilihat bahwa viskositas setelah 2 hari
penyimpanan, dari seluruh sediaan krim temu putih masuk dalam range viskositas
yang diharapkan yaitu 150-250 d.Pa.s. Pada renge tersebut diharapkan sifat alir
dan daya sebar dari sediaan krim temu putih dapat mempermudah dalam
pemakaiannya. Hasil daya sebar pada F6 dan F7 memiliki luas daya sebar yang
lebih besar dibandingkan F2 dan F3. Hal tersebut dikarenakan viskositas pada F6
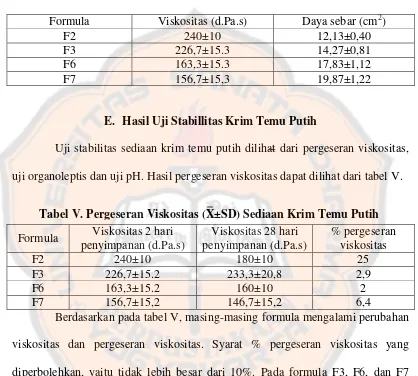
Tabel V. Pergeseran Viskositas (X±SD) Sediaan Krim Temu Putih
dan F7 lebih kecil dibanding F2 dan F3. Semakin kecil viskositas sediaan maka
sediaan yang dihasilkan semakin encer.
Formula Viskositas (d.Pa.s) Daya sebar (cm2) F2 240±10 12,13±0,40 F3 226,7±15.3 14,27±0,81 F6 163,3±15.3 17,83±1,12 F7 156,7±15,3 19,87±1,22
E. Hasil Uji Stabillitas Krim Temu Putih
Uji stabilitas sediaan krim temu putih dilihat dari pergeseran viskositas,
uji organoleptis dan uji pH. Hasil pergeseran viskositas dapat dilihat dari tabel V.
Formula Viskositas 2 hari penyimpanan (d.Pa.s)
Berdasarkan pada tabel V, masing-masing formula mengalami perubahan
viskositas dan pergeseran viskositas. Syarat % pergeseran viskositas yang
diperbolehkan, yaitu tidak lebih besar dari 10%. Pada formula F3, F6, dan F7
memiliki pergeseran viskositas yang memenuhi syarat % pergeseran viskositas
yang diperbolehkan, sehingga dapat dikatakan bahwa untuk ketiga formula
tersebut stabil dalam penyimpanan selama 28 hari. Untuk pergeseran viskositas
pada formula F2 melebihi syarat % pergeseran viskositas yang diperbolehkan,
sehingga dapat dikatakan bahwa formula F2 tidak stabil. Ketidakstabilan ini
dikarenakan F2 memiliki % pergeseran viskositas yang besar, hal tersebut
menunjukkan adanya perubahan viskositas setelah penyimpanan 28 hari.
Berdasarkan pada tabel II, menunjukkan bahwa untuk uji organoleptis
sediaan krim temu putih tidak mengalami perubahan aroma dan homogenitas,
tetapi untuk warna mengalami perubahan menjadi lebih kehitaman, tetapi masih
bisa diterima acceptabilitasnya. Untuk uji pH, dapat dilihat pada tabel.
Berdasarkan tabel dapat dilihat bahwa pH sediaan krim temu putih tidak
mengalami perubahan, yaitu berada pada pH 6 yang masuk di dalam range aman
untuk penggunaan sediaan topikal pada kulit.
F. Uji Aktivitas Antiinflamasi Krim Temu Putih
Pengujian aktivitas antiinflamasi sediaan krim temu putih bertujuan
untuk melihat pelepasan zat aktif ekstrak temu putih dari sediaan krim baik
dengan adanya perbedaan jenis basis yang digunakan maupun dengan ada
tidaknya penetration enhancer. Kemampuan aktivitas antiinflamasi dilihat dari
besarnya % inhibition. Semakin besar % inhibition maka semakin kuat potensi
aktivitas antiinflamasi yang dihasilkan. Pada pengujian ini menggunakan metode
karagenan sebagai penginduksi edema pada telapak kaki tikus. Metode penelitian
ini mengadopsi Kharat et.al.,(2010) yang menggunakan karagenan 1% sebagai
penginduksi edema. Pengukuran ketebalan telapak kaki pada penelitian ini
dilakukan menggunakan jangka sorong. Keuntungan menggunakan metode jangka
sorong adalah pemakaiannya yang sederhana dan perlakuan terhadap hewan uji
lebih dapat diterima dibanding dengan metode potong kaki.
Karagenan dipilih sebagai agen penginduksi edema dikarenakan
sel, sehingga sel yang cedera melepaskan mediator-mediator yang menyebabkan
inflamasi (Bartosikova, 2013).
Pada penelitian ini disiapkan 6 tikus untuk masing-masing kontrol dan
perlakuan. Kontrol negatif yang digunakan dalam penelitian ini ada dua, yaitu
basis krim o/w dan basis Biocream®®. Hal ini dilakukan untuk melihat apakah
basis yang digunakan dalam pembuatan sediaan krim temu putih memiliki
aktivitas antiinflamasi atau tidak dan juga digunakan sebagai pembanding
aktivitas antiinflamasi. Untuk kontrol positif digunakan Voltaren® emulgel yang
mengandung dietilamin diklofenak. Voltaren® emulgel dipilih karena telah
terbukti secara klinis sebagai obat antiinflamasi dengan zat aktif berupa dietilamin
diklofenak yang merupakan obat antiinflamasi golongan non steroid (OAINS)
yang menghambat proses sintesis prostaglandin. Pada formula F1, F3, F5, dan F7
ditambahkan peppermint oil yang diharapakan sebagai penetration enhancer yang
dapat mempercepat masuknya senyawa aktif ke dalam jaringan. Menurut Fox
dkk.(2011) peppermint oil dapat digunakan sebagai penetration enhancer pada
konsentrasi terendah 0,1%.
Pada penelitian ini edema pada telapak kaki tikus diukur pada jam ke- 1,
2, 3, dan 4 setelah diinduksi karagenan 1%. Dari hasil penelitian didapatkan
Formula % inhibition Voltaren® 18,46±0,67 13,58±0,96 11,24±0,92 10,92±0,70
F0 : Basis krim o/w
F1 : Basis krim o/w + peppermint oil 0,5% F2 : Basis krim o/w + ekstrak temu putih 7%
F3 : Basis krim o/w + ekstrak temu putih 7% + peppermint oil 0,5%
F4 : Biocream®
F5 : Biocream®+ peppermint oil
F6 : Biocream® + ekstrak temu putih 7%
F7 : Biocream® + ekstrak temu putih 7% + peppermint oil 0,5% X : Rata-rata % inhibition
SD : Standar deviasi
Dari hasil gambar 5 didapatkan bahwa dari jam ke-1 hingga ke jam ke-4
F2 dan F3 berbeda signifikan terhadap F0, sedangkan dari hasil pada gambar 6
didapatkan untuk F6 dan F7 berbeda signifikan dengan F4 pada jam ke-1 hingga
jam ke-4. Hal ini menunjukkan bahwa F2, F3, F6 dan F7 memiliki aktivitas
antiinflamasi pada jam ke-1 hingga ke-2 dibandingkan dengan masing-masing
kontrol negatif.
Untuk F1 dari berdasarkan gambar 5 , berbeda signifikan dibanding F0
pada jam ke-1 hingga jam ke-3. Hal ini menunjukkan peppermint oil yang
digunakan memberikan aktivitas antiinflamasi tapi tidak sebesar dan tidak
memiliki durasi yang lama seperti F2 dan F3. Sedangkan untuk F5 berdasarkan
Grafik
% inhibition sediaan
krim temu
putih basis
Biocream®
F4
F5
F6
F7
Gambar 5.Grafik % inhibition sediaankrim temu putih basis o/w
-5
gambar 6 berbeda signifikan dengan F4, pada jam ke-1 hingga ke-2. Hal ini
menunjukkan bahwa durasi aktivitas antiinflamasi peppermint oil di dalam basis
krim o/w lebih lama dibandingkan pada basis Biocream®.
Berdasarkan pada gambar 7, didapatkan bahwa pada jam ke-1 untuk F2,
F3, F6 dan F7 berbeda tidak signifikan dibanding Voltaren® emulgel, tetapi pada
jam ke-2 hingga ke-4, F2, F3, F6 dan F7 berbeda signifikan dibanding Voltaren®
emulgel. Hal ini menunjukkan bahwa aktivitas antiinflamasi untuk F2, F3, F6 dan
F7 memiliki aktivitas yang sama besarnya dengan Voltaren® emulgel pada jam
ke-1. Untuk pengaruh basis terhadap pelepasan zat aktif tidak berpengaruh pada
penelitian ini. Hal ini ditunjukkan dengan F2 berbeda tidak signifikan dengan F6,
sedangkan F3 berbeda tidak signifikan dengan F7. Dari hasil tersebut dapat
dikatakan juga bahwa peppermint oil yang digunakan sebagai penetration
enhancer tidak mempengaruhi aktivitas antiinflamasi pada sediaan krim temu
putih baik dengan basisi krim o/w ataupun basis Biocream®.
Gambar 7. Grafik % inhibition sediaan krim temu putih
40
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Ekstrak temu putih dapat dibuat dalam bentuk sediaan topikal berupa krim
yang memiliki kualitas yang baik dan stabil dengan formula F3, F6, dan F7.
2. Krim temu putih dalam basis o/w dan Biocream®® memiliki aktivitas
antiinflamasi selama 4 jam setelah induksi karagenan 1% namun tidak sekuat
dengan kontrol positif.
3. Peppermint oil yang digunakan sebagai penetration enhancer tidak memberi
pengaruh terhadap peningkatan aktivitas antiinflamasi pada sediaan krim temu
putih.
1. Perlu dilakukan penetapan kadar air ekstrak temu putih menggunakan metode
yang lebih selektif untuk kadar air seperti metode destilasi toluen.
2. Perlu adanya penambahan eksipien dalam formula krim temu putih berupa
colouring agent untuk membuat tampilan sediaan krim temu putih lebih dapat
diterima.
3. Perlu dilakukan uji aktivitas antiinflamasi menggunakan metode yang lebih
objektif seperti dengan menggunakan alat plethysmometer.
4. Perlu dilakukannya studi stabilitas fisik untuk optimasi sediaan formulasi yang
lebih mendalam.
DAFTAR PUSTAKA
Agoes, G., 2009, Teknologi Bahan Alam, 31-35, Penerbit ITB, Bandung.
Alankar, S., 2009, A Review on Peppermint Oil, Asian Journal of Pharmaceutical and Clinical Research, 2 (2), pp. 27-30.
Allen, V.L., 2002, The Art Science and Technology of Pharmaceutical Compounding, 2nd Edition, American Pharmaceutical Press Association, USA.
Anief, Moh., 2000, Ilmu Meracik Obat, 52-79, UGM Press, Yogyakarta.
Badan Pengawas Obat dan Makanan RI, 2004, Monografi Ekstrak Tumbuhan Obat Indonesia, Volume pertama, Badan Pengawas Obat dan Makanan RI, Jakarta.
Badan Pengawas Obat dan Makanan RI, 2010, Acuan Sediaan Herbal, Volume kelima, Edisi pertama, Badan Pengawas Obat dan Makanan RI, Jakarta.
Bartosikova, J.N.L., 2013, Carrageenan: A Review, Veterinarni Medicina, 58 (4), pp. 188, 190.
Chainani-Wu, N., 2003, Safety and Anti-Inflammatory Activity of Curcumin: A Component of Turmeric (Curcuma longa), The Journal of Alternative and Complementary Medicine, 9 (1), pp. 164.
Das, K., and Rahman, M.A., 2012, Analgesic and Antimicrobial Activities of
Curcuma zedoaria, International Journal of Pharmacy and
Pharmaceutical Sciences, 4 (5), pp. 322.
Departemen Kesehatan Republik Indonesia, 1986, Sediaan Galenik, Departemen Kesehatan Republik Indonesia, Jakarta, pp. 5-15.
Departemen Kesehatan Republik Indonesia, 1995, Farmakope Indonesia,Edisi IV, Direktorat Jendral Pengawasan Obat dan Makanan, Jakarta, pp 7.
Fox, L.T., Gerber, M., Du Plessis, J., and Hamman, J.H., 2011, Transdermal Drug Delivery Enhancement by Compounds of Natural Origin, Molecules,16, pp. 10508, 10515-10516.
Gunawan, 2005, Farmakologi dan Terapi, Edisi 5, 230 – 272, Departemen Farmakologi dan Terapetik, FKUI, Jakarta.
Kaushik, M.L., Jalalpure, S.S., 2011, Anti_Inflammatory Efficacy of Curcuma zedoaria Rosc Root Extracts, Asian Journal of Pharmaceutical and Clinical Research, 4 (3), pp. 90-92.
Kawai, S., 1998, Cyclooxygenase Selectivity and The Risk of Gastro-Intestinal Complications of Various Non-Steroidal Anti-Inflammatory Drugs: A Clinical Consideration, Inflammation Research, 47 (2), pp. 1025.
Kharat, N., Shylaja, H., Viswanatha, G.L., and Lakshman, K., 2010, Anti-Inflammatory and Analgesic Activity of Topical Preparation of Root Extracts of Ichnocarpus Frutescens (L.) R.BR, International Journal of Applied Biology and Pharmaceutical Technology, 1 (3), pp. 1102-1104. Kidd, B., 2001, Mechanisms of Inflammatory Pain, British Journal of
Anaesthesia, 87 (1), pp. 6.
Medzhitov, R., 2008, Origin and Physiological Roles of Inflammation, Nature,
454, pp. 429.
Moody, M.L., 2010, Topical Medications in the Trearment of Pain, Pain Medicine News, pp. 16.
Murwanti, R., Meiyanto, E., Nurrochmad, A., dan Kristina, S.A., 2004, Efek Ekstrak Etanol Rimpang Temu Putih (Curcuma zedoaria Rosc.) Terhadap Pertumbuhan Tumor Paru Fase Post Inisiasi Pada Mencit Betina Diinduksi Benzo[a]piren, Majalah Farmasi Indonesia, 15 (1), pp. 7.
Mustchler, E. 1991, Dinamika obat: Buku ajar Farmakologi dan toksikologi, edisi kelima, Diterjemahkan oleh Widianto, M. dan A.S Ranti, Penerbit ITB, Bandung.
Mycek, M. J, Harvey, R. A., Champe, P. C., 2001, Farmakologi Ulasan Bergambar, diterjemahkan oleh Agoes, A., Edisi 2, Widya Medika, Jakarta.
Paramapojn, S., and Gritsanapan, W., 2009, Free Radical Scavenging Activity Determination and Quantitative Analysis of Curcuminoids in Curcuma zedoaria Rhizome Extracts by HPLC Method, Current Science, 97 (7), pp. 1069.
Robert, C., and Kupper, T.S., 1999, Mechanisms of Disease, The New England Journal of Medicine, 341 (24), pp. 1817-1819.
Sahu, A.N., Jha, S., and Dubey, S.D., 2011, Formulation and Evaluation of Curcuminoid Based Herbal Face Cream, Indo-Global Journal of Pharmaceutical Sciences, 1 (1), pp. 77-79.
Sandhu et al., 2012, Additives in Topical Dosage Forms, International Journal of Pharmaceutical, Chemical and Biological Sciences, 2 (1), 79-83.
Schuelert, N., Russell, F.A., McDougall, J.J., 2011, Topical Diclofenac in The Treatment of Osteoarthritis of The Knee, Orthopedic Research and Reviews, 3, pp. 2-4.
Sharma, R.A., Gescher, A.J., And Steward, W.P., 2005, Curcumin : The Story so Far, Eropean Journal of Cancer, 41, pp. 1955-1957.
Voigt, R., 1995, Buku Pelajaran Teknologi Farmasi, Hal 790-811, UGM Press, Yogyakarta.
LAMPIRAN
Lampiran 7. Sediaan Krim Temu Putih Pada Hari ke-2
Basis Krim o/w Basis Krim o/w + Peppermint Oil
Krim o/w Temu Putih + Peppermint Oil
Krim o/w Temu Putih
Basis Biocream Basis Biocream + Peppermint Oil
Lampiran 8. Sediaan Krim Temu Putih Pada Hari ke-28
Lampi
Basis Biocream Basis Biocream + Peppermint Oil
Biocream Temu Putih Biocream Temu Putih + Peppermint Oil
Krim o/w Temu Putih Krim o/w Temu Putih + Peppermint Oil
a. Formula Biocream Ekstrak
b. Formula Biocream Ekstrak Peppermint
Replikasi 48 jam
d. Formula Krim Ekstrak Peppermint
Replikasi 48 jam
/DPSLran 9. Uji sifat fisik
2. Viskositas
b. Formula Biocream Ekstrak Peppermint
Replikasi 48 jam
d. Formula Krim Ekstrak Peppermint
3. Daya Sebar
Beban yang digunakan sebesar 100 g
Luas Daya sebar (cm2) = 2
b. Formula Biocream Ekstrak Peppermint
Replikasi 48 jam
d. Formula Krim Ekstrak Peppermint