I PENDAHULUAN
Bab ini akan menguraikan mengenai : (1) Latar Belakang Percobaan, (2) Tujuan Percobaan, (3) Prinsip Percobaan, dan (4) Reaksi Percobaan.
1.1 Latar Belakang Percobaan
Karbohidrat adalah polihidroksi aldehid atau polihidroksi keton dan meliputi kondensat polimer-polimernya yang terbentuk. Nama karbohidrat dipergunakan dalam senyawa-senyawa tersebut, mengingat rumus empirisnya yang berupa CnH2nOn atau mendekati Cn(H2O)n yaitu karbon yang mengalami hidratasi.
Terdapat beberapa uji untuk mengenali dan mengetahui adanya karbohidrat pada makanan (sampel) seperti uji molish, uji barfoed, uji benedict, dan uji selliwanof.
Uji Benedict adalah uji untuk membuktikan adanya gula pereduksi. Gula pereduksi adalah gula yang mengalami reaksi hidrolisis dan bisa diurai menjadi sedikitnya dua buah monosakarida. Karateristiknya tidak bisa larut atau bereaksi secara langsung dengan Benedict, contohnya semua golongan monosakarida, sedangkan gula non pereduksi struktur gulanya berbentuk siklik yang berarti bahwa hemiasetal dan hemiketalnya tidak berada dalam kesetimbangannya, contohnya fruktosa dan sukrosa (Razuna. 2010).
1.2 Tujuan Percobaan
Tujuan dari percobaan uji benedict adalah untuk menguji ada atau tidaknya gula pereduksi dalam suatu bahan pangan yang dianalisa.
▸ Baca selengkapnya: benedict mengandung zat
(2)1.3 Prinsip Percobaan
Prinsip dari percobaan uji benedict adalah berdasarkan pada reaksi gula pereduksi yang akan mereduksi Cu2+ jika dalam kondisi basa yang membentuk Cu2O yang menghasilkan endapan warna merah bata.
1.4 Reaksi Percobaan
Gambar 1. Reaksi Percobaan Uji Benedict
Cu
Cu
2O H
O H
C
O
C
O
2++
+
II METODE PERCOBAAN
Bab ini akan menguraikan mengenai : (1) Bahan yang Digunakan, (2) Pereaksi yang Digunakan, (3) Alat yang Digunakan, dan (4) Metode Percobaan.
2.1. Bahan yang Digunakan
Bahan yang digunakan dalam Uji Benedict adalah sampel dan pereaksi benedict.
2.2. Pereaksi yang Digunakan
Pereaksi yang digunakan dalam Uji Benedict adalah larutan benedict yang terdiri dari 173 g Na-Citrat + 100 g Na2CO3 dalam 800 ml air yang sudah dimasak, diaduk dan ditambahkan 17,3 g CuSO4 dalam 100 ml air.
2.3. Alat yang Digunakan
Alat yang digunakan dalam Uji Benedict adalah pipet tetes, tabung reaksi, rak tabung reaksi, gelas kimia, kompor (water bath), penangas air.
2.4. Metode Percobaan
Gambar 2. Metode Percobaan Uji Benedict
1m l larutan karbohidrat + 3m l larutan benedict
panaskan selam a 5 m enit
am ati terbentuknya endapan m erah bata atau biru kehijuaan
III HASIL PENGAMATAN
Bab ini akan menguraikan mengenai : (1) Hasil Pengamatan dan, (2) Pembahasan.
3.1. Hasil Pengamatan
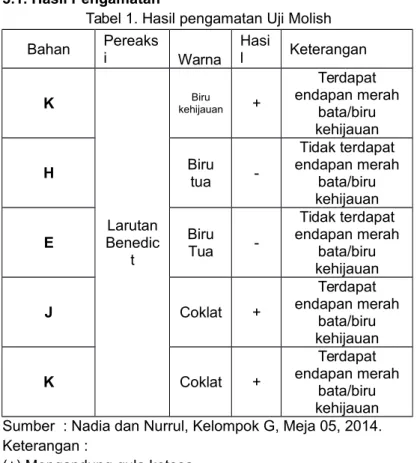
Tabel 1. Hasil pengamatan Uji Molish Bahan Pereaksi Warna Hasi l Keterangan K Larutan Benedic t Biru kehijauan + Terdapat endapan merah bata/biru kehijauan H Birutua -Tidak terdapat endapan merah bata/biru kehijauan E BiruTua -Tidak terdapat endapan merah bata/biru kehijauan J Coklat + Terdapat endapan merah bata/biru kehijauan K Coklat + Terdapat endapan merah bata/biru kehijauan Sumber : Nadia dan Nurrul, Kelompok G, Meja 05, 2014. Keterangan :
(+) Mengandung gula ketosa (-) Tidak Mengandung gula ketosa
Gambar 3. Hasil Pengamatan Uji Benedict 3.2. Pembahasan
Uji Benedict adalah uji untuk membuktikan adanya gula pereduksi. Gula pereduksi adalah gula yang mengalami reaksi hidrolisis dan bisa diurai menjadi sedikitnya dua buah monosakarida. Karateristiknya tidak bisa larut atau bereaksi secara langsung dengan Benedict, contohnya semua golongan monosakarida, sedangkan gula non pereduksi struktur gulanya berbentuk siklik yang berarti bahwa hemiasetal dan hemiketalnya tidak berada dalam kesetimbangannya, contohnya fruktosa dan sukrosa. Dengan prinsip berdasarkan reduksi Cu2+ menjadi Cu+ yang mengendap sebagai Cu2O berwarna merah bata. Untuk menghindari pengendapan CuCO3 pada larutan natrium karbonat (reagen Benedict), maka ditambahkan asam sitrat. Larutan tembaga alkalis dapat direduksi oleh karbohidrat yang mempunyai gugus aldehid atau monoketon bebas, sehingga sukrosa yang tidak mengandung aldehid atau keton bebas tidak dapat mereduksi larutan (Razuna, 2010).
Pada uji Benedict larutan tembaga alkalis akan direduksi oleh gula yang mempunyai gugus aldehid atau keton bebas dengan membentuk kuproksida yang berwarna. Gula pereduksi beraksi dengan pereaksi menghasilkan endapan merah bata (Cu2O). Pada gula pereduksi terdapat gugus aldehid dan OH laktol. OH laktol adalah OH yang terikat pada atom C pertama yang menentukan karbohidrat sebagai gula pereduksi atau bukan. Sekalipun aldosa atau ketosa berada dalam bentuk sikliknya, namun bentuk ini berada dalam kesetimbangannya dengan sejumlah kecil aldehida atau keton rantai terbuka, sehingga gugus aldehida atau keton ini dapat mereduksi berbagai macam reduktor (Razuna, 2010).
Gula pereduksi dengan larutan Benedict akan terjadi reaksi reduksi oksidasi dan dihasilkan endapan berwarna merah bata dari kupro oksida.
Berdasarkan percobaan dengan menggunakan Uji Benedict, hasil pengamatan menunjukkan bahwa sampel K, J dan A positif mengandung gula pereduksi. Hal itu dibuktikan dengan terbentuknya endapan berwarna merah bata atau biru kehijauan setelah sampel ditambahkan larutan benedict dan dipanaskan dalam penangas air.
Percobaan Uji Benedict ini menggunakan larutan benedict sebagai pereaksi yaitu larutan yang dibuat dari 173 gram Na-sitrat ditambah 100 gram Na2CO3 dalam 800 ml air yang sudah dimasak, diaduk, dan ditambahkan 17,3 gram CuSO4 dalam 100 ml air. Glukosa dapat mereduksi ion Cu2+ dari dari CuSO4 menjadi ion Cu+ yang kemudian mengendap sebagai Cu2. Adanya Na2CO3 dan Na-sitrat membuat pereaksi benedict bersifat basa lemah. Endapan yang terbentuk dapat berwarna hijau, kuning, atau merah bata. Warna endapan ini tergantung kepada konsentrasi karbohidrat yang diperiksa.
Pereaksi benedict lebih banyak digunakan untuk pemeriksaan glukosa dalam urine (Poedjiadi, 1994).
Dalam proses pengujian sampel dipanaskan dengan tujuan mempercepat terjadinya hidrolisis pada maltosa maupun laktosa, sedangkan natrium sulfat dan natrium karbonat yang terdapat pada reagen benedict akan membuat larutan sampel menjadi bersifat basa lemah yang kemudian akan direduksi. Pada dasarnya reagen Benedict hanya merupakan modifikasi dari reagen Fehling terlihat dari reaksinya yang hampir sama pada proses reduksi dan oksidasi. Pada uji ini terjadi reduksi Cu2+ menjadi Cu+, proses reduksi dilakukan oleh karbohidrat yang mempunyai gugus aldehidaatau keton bebas kepada larutan-larutan tembaga yang berkeadaan alkalis. Reduksi ini menghasilkan suatu endapan kupro oksida (Cu2O) yang memiliki warna merah bata sehingga dapat dengan mudah di identifikasi. Pengamatan yang dilakukan dalam uji benedict ini dapat dilakukan dengan mengamati perubahan warna dan terjadinya endapan. Warna larutan dapat terlihat bermacam-macam tergantung dari konsentrasi karbohidrat yang dipakai, larutan dapat merah bata dan hijau kebiruan. Pada uji Benedict terhadap glukosa dan fruktosa larutan berwarna hijau kebiruan dan terdapat endapan merah bata didalamnya yang menandakan pengujian positif, sedangkan pada maltosa danlaktosa larutan memiliki warna hijau kebiruan tanpa endapan merah bata hal ini menunjukan bahwa pengujian positif terdapat gula di dalamnya, tetapi pada pengujian terhadap sukrosa dan pati warna yang terlihat adalah biru menandakan bahwa hasil uji negatif mengindikasikan bahwa sukrosa dan pati tidak memiliki gula pereduksi yang dapat mereduksi reagen benedict (Yuli, 2012).
Perbedaan uji benedict dengan uji barfoed adalah pada suasananya, pada uji benedict terjadi reaksi pada suasana basa karena mengandung natriun karbobat, sedangkan pada uji barfoed terjadi pada suasana asam.Pada uji benedict dilakukan pemanasan lebih cepat karena waktu 5 menit merupakan suhu optimal, jika pemansan dilakukan kuarang dari 5 menit maka larutan akan berwarna kuning.
Gula pereduksi merupakan golongan gula (karbohidrat) yang dapat mereduksi senyawa-senyawa penerima elektron. Contohnya adalag glukosa dan fruktosa. Ujung dari satu gula pereduksi adalah ujung yang mengandung gugus aldehida atau keton bebas. Semua monosakarida (glukosa, fruktosa, galaktosa) dan disakarida ( (laktosa, maltosa) kecuali sukrosa dan pati ( polisakarida), termasuk sebagai gula pereduksi. Umumnya gula pereduksi yang dihasilkan berhubungan erat dengan aktivitas enzim, yaitu semakin tinggi aktivitas enzim maka semakin tinggi pula gula pereduksi yang dihasilkan (Lehninger, hal 320, 1982).
IV KESIMPULAN DAN SARAN
Bab ini akan menguraikan mengenai : (1) Kesimpulan dan (2) Saran.
4.1. Kesimpulan
Berdasarkan percobaan yang telah dilakukan, untuk mengatahui kadar karbohidrat dalam bahan pangan melalui uji Benedict, dapat disimpulkan bahwa sampel K, J dan A positif mengandung monosakarida. Dapat terlihat dari indikator positif yang terbentuk (endapan berwarna merah bata/biru kehijauan).
4.2. Saran
Dalam melakukan percobaan, diharapkan praktikan dapat menjaga kebersihan, mengerjakan tepat waktu, teliti.
DAFTAR PUSTAKA
Lehninger. (1982). Dasar-Dasar Biokimia Jilid I. Erlangga, Jakarta.
Poedjiadi, Anna. 2005. Dasar-Dasar Biokimia. Jakarta: Penerbit Universitas Indonesia.
Razuna, (2010). Karbohidrat. www.blogspot.com. Akses 19 maret 2014.
Sudarmadji, Slamet. Dkk. (2003). Analisa Bahan Makanan dan Pertanian. Penerbit Liberty, Yogyakarta.
Yuni, T. (2012). Karbohidrat.
http//http://id.scribd.com/doc/39533102/karbohidrat.