i
VALIDASI METODE KROMATOGRAFI LAPIS TIPIS (KLT)-DENSITOMETRI PADA PENETAPAN KADAR NIKOTIN DALAM
EKSTRAK ETANOLIK DAUN TEMBAKAU ( L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh : Citra Dewi Ariani NIM : 088114115
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
Persetujuan Pembimbing
VALIDASI METODE KROMATOGRAFI LAPIS TIPIS (KLT)-DENSITOMETRI PADA PENETAPAN KADAR NIKOTIN DALAM
EKSTRAK ETANOLIK DAUN TEMBAKAU ( L.)
Skripsi yang diajukan oleh :
Citra Dewi Ariani
NIM : 088114115
telah disetujui oleh
Pembimbing
iv
Halaman Persembahan
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya dari orang lain, kecuali yang telah
disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila dikemudian hari ditemukan indikasi plagiarisme dalam naskah
ini, maka saya bersedia menanggung segala sanksi sesuai peraturan
perundang-undangan yang berlaku.
Yogyakarta, 19 Desember 2011
Penulis,
vi
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma : Nama : Citra Dewi Ariani
Nomor mahasiswa : 088114115
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
VALIDASI METODE KROMATOGRAFI LAPIS TIPIS (KLT)-DENSITOMETRI PADA PENETAPAN KADAR NIKOTIN DALAM
EKSTRAK ETANOLIK DAUN TEMBAKAU ( L.)
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 19 Desember 2011 Yang Menyatakan
vii PRAKATA
Puji syukur penulis panjatkan ke hadirat Tuhan atas berkat, penyertaan,
lindungan, dan perkenananNya sehingga proses penulisan skripsi ini dapat
berjalan dengan lancar dari awal hingga akhir dan pada akhirnya penulis dapat
menyelesaikan skripsi yang berjudul Validasi Metode Kromatografi Lapis Tipis
(KLT)-Densitometri pada Penetapan Kadar Nikotin dalam Ekstrak Etanolik Daun
Tembakau ( L.). Skripsi ini disusun sebagai salah satu syarat
untuk memperoleh gelar Sarjana Farmasi (S.Farm.).
Dalam kegiatan perkuliahan, penelitian, serta proses penyusunan skripsi
ini, penulis telah mendapatkan banyak bantuan berupa bimbingan, perhatian,
semangat, dan juga kritik maupun saran yang membangun dari berbagai pihak,
sehingga skripsi ini dapat terselesaikan dengan baik. Oleh karena itu, penulis
mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Ipang Djunarko, M.Si, Apt. selaku Dekan Fakultas Farmasi Sanata Dharma.
2. Jeffry Julianus, M.Si., selaku dosen pembimbing skripsi sekaligus dosen
pembimbing akademik, atas bimbingan, masukan, perhatian, dan semangat
yang diberikan baik selama perkuliahan maupun penyusunan skripsi ini.
3. Yohanes Dwiatmaka,M.Si. selaku dosen penguji sekaligus dosen pembimbing
akademik atas segala arahan, perhatian, masukan, kritik maupun saran yang
telah diberikan kepada penulis.
4. Prof. Dr. Sudibyo Martono, M.S., Apt. selaku dosen penguji sekaligus dosen
pembimbing akademik atas segala arahan, perhatian, masukan, kritik maupun
viii
5. Christine Patramurti, M.Si., Apt. selaku dosen pembimbing akademik, atas
segala arahan, perhatian, kritik dan saran yang diberikan selama perkuliahan
dan selama penelitian skripsi ini berlangsung.
6. Mas Bimo, Pak Parlan, Mas Otok, Mas Kunto, dan Pak Timbul atas bantuan
yang telah diberikan selama penulis bekerja di laboratorium.
7. Segenap dosen dan karyawan atas segala ilmu dan pengalaman yang telah
diberikan sehingga sangat membantu dalam penyusunan skripsi ini.
8. Novi dan Cure, sebagai rekan kerja penulis atas segala bantuan, semangat,
kebersamaan, selama melakukan penelitian maupun selama perkuliahan.
9. Ayesa, Amel, Dina, sebagai teman satu tim penelitian nikotin atas semangat,
bantuan, dukungan, dan kebersamaan selama melakukan penelitian maupun
selama perkuliahan.
10. Felis, Sasa, Lele, Susi, Susan, Nona, Sari, Tere, dan Wiwi sebagai teman
seperjuangan di Laboratorium Kimia Analisis Instrumental atas semangat,
keceriaan dan kebersamaannya.
11. Ko Tony, atas dukungan, perhatian, saran, dan semangat yang telah
diberikan selama penyusunan skripsi ini.
12. Cik Yunita, Ko Beny, Mbak Tiwi, atas ilmu, pengalaman, dan semangat
yang telah diberikan sehingga sangat membantu penulis dalam penyusunan
skripsi ini.
13. Teman-teman kelompok praktikum B, atas keceriaan, pengalaman, dan
ix
14. Teman-teman FST B 2008 atas kebersamaan, pengalaman, suka duka, dan
kekompakan yang akan penulis kenang selalu.
15. Teman-teman Kos Amakusa atas kebersamaan, keceriaan, semangat dan
pengalaman yang telah dibagikan kepada penulis.
16. Semua pihak yang tidak dapat disebutkan satu per satu oleh penulis, atas
segala bantuan yang diberikan sehingga penulis dapat menyelesaikan skripsi
ini.
Penulis menyadari bahwa skripsi ini masih memiliki banyak kekurangan.
Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun dari
semua pihak. Akhir kata, semoga skripsi ini dapat berguna bagi perkembangan
ilmu pengetahuan selanjutnya.
Penulis
x DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
xi
B. Tembakau ... 6
C. Ekstrak Tembakau ... 7
D. Kromatografi Lapis Tipis ...
1. Tinjauan umum ...
BAB III METODE PENELITIAN ...
A. Jenis dan Rancangan Penelitian ...
B. Variabel Penelitian ...
C. Definisi Operasional ...
D. Bahan Penelitian ...
E. Alat Penelitian ...
F. Tata Cara Penelitian ...
1. Pembuatan fase gerak ...
2. Pembuatan larutan baku ...
3. Penetapan panjang gelombang pengamatan ...
4. Pembuatan kurva baku nikotin dan pengamatan nilai Rf ...
xii
5. Akurasi pengukuran baku dalam matriks sampel ...
BAB IV HASIL DAN PEMBAHASAN ...
A. Pembuatan Fase Gerak ...
B. Preparasi Sampel ...
C. Pembuatan Larutan Baku ...
D. Penetapan Panjang Gelombang Pengamatan Nikotin ...
E. Pengamatan Nilai (Rf) dan Pembuatan Baku
Nikotin ...
F. Validasi Metode Analisis ...
1. Selektivitas ...
2. Linearitas ...
3. Akurasi ...
4. Presisi ...
G. Penentuan Akurasi dan Presisi Baku Nikotin dalam Sampel ...
BAB V KESIMPULAN DAN SARAN ...
xiii
B. Saran ...
DAFTAR PUSTAKA ...
LAMPIRAN ...
BIOGRAFI PENULIS ...
44
45
48
xiv
Parameter analisis validasi metode ...
Kriteria rentang yang dapat diterima ...
Kriteria CV yang dapat diterima ...
Data replikasi kurva baku nikotin...
Perbandingan nilai Rf baku dan sampel, serta nilai resolusi ....
xv
Alkaloid utama dalam tembakau ...
Tanaman tembakau ...
Ilustrasi model refleksi dan transmisi ...
CAMAG’s 3 densitometer ...
Reaksi penggaraman nikotin dengan larutan HCl ...
Reaksi pembentukan molekul nikotin basa ...
Kromofor pada nikotin ...
Densitogram baku nikotin dengan konsentrasi 3 ppm dalam
pelarut etanol ...
Kromatogram baku nikotin konsentrasi 3 ppm (Rf = 0,52) ...
Interaksi hidrogen nikotin dengan fase diam silika gel 60 F254
Interaksi nikotin dengan fase gerak (n-heksan : toluen :
dietilamin) ...
Hubungan antara konsentrasi nikotin dengan AUC ...
Kromatogram baku nikotin konsentrasi 5 ppm (Rf = 0,53) ...
Kromatogram sampel replikasi I (Rf = 0,55) ...
Kromatogram sampel tanpa penambahan baku nikotin ...
Kromatogram sampel dengan penambahan baku nikotin ...
xvi
Surat keterangan keaslian baku nikotin ( ) ...
Sistem KLT-densitometri yang digunakan ...
Surat determinasi tembakau jenis dan
! ...
Data pengamatan tembakau VBN dan NO ...
Densitogram baku nikotin dengan konsentrasi 3 ppm
dalam pelarut etanol ...
Tabel data densitogram pada panjang gelombang
pengamatan nikotin (λmaks = 261 nm)...
Kromatogram seri baku nikotin replikasi III ...
Kromatogram validasi metode ...
Data penimbangan sampel dan perhitungan kadar nikotin..
Persamaan kurva baku dan gambar kurva baku nikotin ...
Nilai AUC dan contoh perhitungan nikotin ...
Contoh perhitungan CV nikotin ...
Kromatogram pemisahan sampel dan perhitungan resolusi
Kromatogram sampel tanpa penambahan baku ...
Kromatogram sampel dengan penambahan baku ...
Nilai AUC sampel dan sampel yang diadisi baku nikotin...
Contoh perhitungan baku nikotin dalam sampel..
xvii INTISARI
Nikotin merupakan senyawa alkaloid yang banyak terdapat dalam tanaman tembakau ( L.). Dewasa ini nikotin berpotensi sebagai agen terapetik. Oleh karena itu, diperlukan analisis kuantitatif melalui penetapan kadar nikotin dalam ekstrak etanolik daun tembakau dengan metode KLT - densitometri. Sebelum dilakukan penetapan kadar perlu dilakukan validasi metode untuk mengetahui apakah metode yang digunakan memberikan hasil yang dapat dipercaya.
Penelitian ini merupakan penelitian non eksperimental deskriptif. Dalam penelitian ini, sistem yang digunakan yaitu fase diam silika gel 60 F254 dan fase
gerak n-heksan : toluen : dietilamin (15,25 : 5,75 :4). Setelah pemisahan dengan KLT kemudian dilakukan analisis kuantitatif menggunakan densitometer. Parameter validasi yang diteliti adalah selektivitas, linearitas, akurasi, dan presisi.
Hasil penelitian menunjukkan bahwa metode ini memiliki selektivitas yang baik dengan resolusi pada 3 kali replikasi sampel berturut-turut adalah 1,58; 1,89; dan 1,88; linearitas yang baik pada konsentrasi 1-5 ppm dengan r = 0,999, nilai dan CV berturut-turut untuk konsentrasi nikotin 1 ppm, 3 ppm, dan 5 ppm yaitu 98,72-102,46% dan 1,50%; 99,90-101,80% dan 0,78%; 98,23-100,55% dan 0,96%. Berdasarkan hasil tersebut, maka metode KLT-densitometri ini memiliki validitas yang baik untuk menetapkan kadar nikotin dalam ekstrak etanolik daun tembakau.
xviii ABSTRACT
Nicotine is an alkaloid compound that is widely available in tobacco plants ( L.). Nowadays, nicotine potentialy become a therapeutic agent. Therefore, quantitative analysis is required through the determination of nicotine levels in the ethanolic extract tobacco’s leaves by the method of TLC - densitometry. Prior to the assay method validation needs to be done to determine whether the methods used to give reliable results.
This study is a non-experimental descriptive studies. In this study, the system used the stationary phase silica gel 60 F254 and the mobile phase n-hexane
: toluene : diethylamine (15,25:5,75:4). After separation by TLC then performed quantitative analysis using a densitometer. Validation parameters studied were selectivity, linearity, accuracy, and precision.
The results showed that this method has good selectivity with resolution of three sample replications consecutively are 1,58; 1,89, and 1,88; good linearity at concentrations of 1-5 ppm with r = 0,999; the value of and CV for the nicotine concentrations of 1 ppm, 3 ppm and 5 ppm consecutively are 98,72 – 102,46% and 1,50%; 99,90 – 101,80% and 0,78%; 98,23 – 100,55% and 0,96%. Based on these results, the TLC-densitometry method has good validity to establish the levels of nicotine in the ethanolic extract tobacco’s leaves.
1 BAB I PENGANTAR
A. Latar Belakang
Indonesia merupakan negara yang kaya akan biodiversitasnya. Obat
berbasis tumbuhan telah melekat di dalam kehidupan masyarakat sejak dahulu
kala sehingga peran tanaman berkhasiat obat sangat besar bagi kesehatan
masyarakat. Berbagai tanaman obat dan ribuan tanaman berpotensi obat di
Indonesia mengandung beraneka ragam jenis senyawa kimia alami. Salah satunya
yaitu tanaman tembakau ( L.). Tembakau biasa digunakan
sebagai bahan baku dalam pembuatan rokok, pestisida, selain itu juga berpotensi
sebagai obat. Kandungan kimia yang paling besar dalam tembakau yaitu nikotin.
Nikotin adalah senyawa organik kelompok alkaloid yang dihasilkan secara alami
pada berbagai macam tumbuhan, terutama suku terung-terungan ( )
seperti tembakau dan tomat.
Nikotin tidak hanya memberikan dampak negatif bagi kesehatan karena
keberadaannya dalam rokok, namun nikotin dapat memberikan dampak positif
karena nikotin memiliki potensi sebagai agen terapetik, yaitu sebagai obat
parkinson, obat alzheimer, serta obat (Domino, 1999). Simplisia
daun tembakau dengan kandungan nikotinnya dapat lebih bermanfaat dengan
dikembangkannya menjadi obat herbal dalam bentuk sediaan farmasetis. Obat
herbal memiliki peran penting dalam bidang kesehatan bahkan bisa menjadi
Pada tahap pengembangan simplisia menjadi obat herbal perlu diketahui
dosis yang efektif untuk pengobatan, sehingga perlu dilakukan analisis kuantitatif
berupa penetapan kadar terlebih dahulu. Penetapan kadar nikotin dalam ekstrak
etanolik daun tembakau perlu dilakukan untuk mengetahui jumlah zat aktif yang
nantinya akan berpengaruh terhadap khasiat obat herbal tersebut. Metode yang
dipilih untuk penetapan kadar nikotin dalam ekstrak etanolik daun tembakau yaitu
metode kromatografi lapis tipis (KLT)-densitometri. KLT cocok untuk analisis
obat di laboratorium farmasi karena metodenya sederhana, cepat dalam
pemisahan, sensitif, dan memerlukan jumlah cuplikan yang sangat sedikit
(Khopkar, 1990). Nikotin dapat ditetapkan kadarnya dengan metode
KLT-densitometri karena terdapat perbedaan interaksi antara nikotin dan
senyawa-senyawa lain dalam ekstrak dengan fase diam dan fase gerak yang digunakan.
Untuk dapat menetapkan kadar nikotin dalam ekstrak etanolik daun
tembakau diperlukan serangkaian penelitian terdahulu yaitu optimasi dan validasi
metode. Dalam hal ini, peneliti mengambil bagian pada tahap validasi metode
KLT-densitometri pada penetapan kadar nikotin dalam ekstrak etanolik daun
tembakau. Tahapan validasi metode ini menggunakan sistem yang telah
dioptimasi pada penelitian sebelumnya yaitu menggunakan fase diam silika gel 60
F254 dan fase gerak n-heksan: toluen: dietilamin (15,25:5,75:4). Optimasi metode
penting dilakukan sebelum melakukan validasi metode karena akan memberikan
jaminan kepada proses validasi yaitu pemisahan yang optimal dengan nilai
resolusi 3 kali replikasi sampel berturut-turut adalah 1,58; 1,89; dan 1,88;
dengan bentuk " kromatogram yang runcing dan simetris yang dilihat dari
nilai " dari 3 kali replikasi pada konsentrasi rendah, sedang,
dan tinggi adalah 1, serta reprodusibilitas nilai Rf dan dengan CV
berturut-turut adalah 1,79% dan 0%. Suatu metode analisis harus divalidasi ketika suatu
metode menggunakan sistem baru yang belum divalidasi sebelumnya. Tujuan dari
validasi yaitu untuk memberikan jaminan bahwa metode analisis yang digunakan
memenuhi parameter-parameter validasi yang meliputi selektivitas, linearitas,
akurasi, dan presisi. Oleh karena itu, tahapan validasi metode merupakan tahapan
yang penting untuk dilakukan dalam suatu penetapan kadar senyawa untuk dapat
memberikan hasil yang dapat dipercaya.
1. Permasalahan
Apakah metode KLT-densitometri pada penetapan kadar nikotin dalam
ekstrak etanolik daun tembakau memenuhi parameter-parameter validasi yaitu
selektivitas, linearitas, akurasi, dan presisi?
2. Keaslian Penelitian
Penelitian mengenai penetapan kadar nikotin dengan metode
KLT-densitometri yang pernah dilakukan yaitu penentuan kadar nikotin dalam asap
rokok (Susanna, Hartono, dan Fauzan, 2003), #
$ % & ' ( (Tyrpien, Dobosz,
Chrosciewicz, ,Ciolecka, Wielkoszyński, dan Janoszka, 2003), analisis nikotin
dalam asap dan filter rokok (Fidrianny, Supradja, dan Soemardji, 2004).
Berdasarkan penelitian di atas, penelitian validasi metode penetapan
KLT-densitometri fase diam silika gel 60 F254 dan fase gerak n-heksan: toluen:
dietilamin (15,25:5,75:4) ini belum pernah dilakukan sebelumnya.
3. Manfaat Penelitian
a. Manfaat metodologis. Penelitian ini diharapkan dapat memberikan
sumbangan ilmiah tentang penggunaan metode KLT-densitometri fase diam silika
gel 60 F254 dan fase gerak n-heksan: toluen: dietilamin (15,25:5,75:4) pada
penetapan kadar nikotin dalam ekstrak etanolik daun tembakau.
b. Manfaat praktis. Hasil penelitian diharapkan dapat memberikan
informasi mengenai selektivitas, linearitas, akurasi, dan presisi metode penetapan
kadar nikotin dalam ekstrak etanolik daun tembakau secara KLT-densitometri
yang dapat digunakan untuk penetapan kadar nikotin sebagai langkah awal untuk
penetapan dosis terapetik.
B. Tujuan
Penelitian ini bertujuan untuk mengetahui validitas metode penetapan
kadar nikotin secara KLT-densitometri dengan fase diam silika gel 60 F254 dan
fase gerak n-heksan: toluen: dietilamin (15,25:5,75:4) apakah memenuhi
parameter-parameter validasi yaitu selektivitas, linearitas, akurasi, dan presisi
sehingga dapat digunakan untuk penetapan kadar nikotin dalam ekstrak etanolik
daun tembakau.
5
BAB II
PENELAAHAN PUSTAKA
A. Nikotin
Nikotin merupakan suatu alkaloid dari daun tanaman tembakau,
L. Berwarna kekuningan, bersifat volatil, sangat higroskopis,
dapat berubah warna menjadi cokelat apabila terpapar cahaya atau udara. Titik
didih 247°C, dengan dekomposisi. Indeks refraktif 1,5280. Nikotin larut dalam
air, etanol, eter, dan kloroform. Nikotin dapat diekstraksi dengan pelarut organik
dari larutan yang bersifat alkalis (Clarke, 1969).
Gambar 1. Struktur nikotin
Jumlah nikotin sekitar 2-8% dari berat kering daun tembakau, sedangkan
alkaloid lainnya seperti anabasin, anatabin, dan nornikotin jumlahnya lebih rendah
dibandingkan nikotin. Namun, jumlah masing-masing jenis alkaloid relatif
berbeda dari semua alkaloid pada berbagai spesies (Domino, 1999).
Nikotin mengandung dua jenis gugus amin tersier yang bersifat basa
dengan pKa cincin piridin adalah 3,04 sedangkan pKa pada cincin pirolidin
adalah 7,84. Nilai pKa pada cincin aromatik piridin lebih rendah dikarenakan efek
hibridisasi sp2 yang menyebabkan orbital s bertambah sehingga elektron-elektron
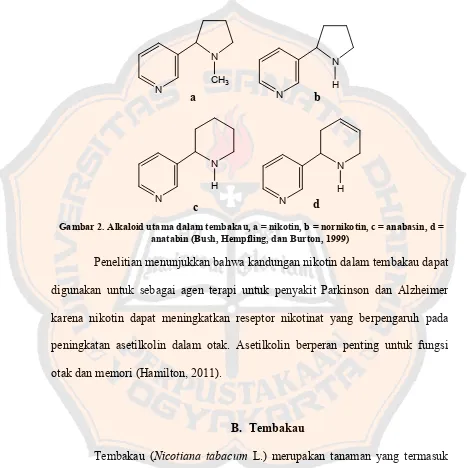
Alkaloid utama dalam tanaman tembakau meliputi nikotin, nornikotin,
anabasin dan anatabin. Struktur dari masing-masing senyawa dapat dilihat pada
gambar di bawah ini.
a b
c d
Gambar 2. Alkaloid utama dalam tembakau, a = nikotin, b = nornikotin, c = anabasin, d = anatabin (Bush, Hempfling, dan Burton, 1999)
Penelitian menunjukkan bahwa kandungan nikotin dalam tembakau dapat
digunakan untuk sebagai agen terapi untuk penyakit Parkinson dan Alzheimer
karena nikotin dapat meningkatkan reseptor nikotinat yang berpengaruh pada
peningkatan asetilkolin dalam otak. Asetilkolin berperan penting untuk fungsi
otak dan memori (Hamilton, 2011).
B. Tembakau
Tembakau ( L.) merupakan tanaman yang termasuk
dalam famili . Tanaman ini dapat tumbuh sampai dengan 3 m. Daun
tanaman tembakau berbentuk bulat lonjong (oval) atau bulat, tergantung pada
varietasnya. Daun yang berbentuk bulat lonjong ujungnya meruncing, sedangkan
bagian tepi daun agak
tanaman sekitar 28 - 32 helai (Anonim, 2011).
Gambar 3. Tanaman tembakau
au Vorstenlanden adalah produk dari daun tembak
Vorstenlanden yang ditanam di Surakarta dan Yo
saat musim penghujan, dikeringkan di los pe
disortasi (Standar Nasional Indonesia, 1995).
bakau dibagi dua berdasarkan waktu tanam dan m
musim kemarau dan tembakau musim penghuj
dalah tembakau yang ditanam pada akhir mus
usim kemarau, sedangkan tembakau ! ad
ada musim kemarau dan dipanen pada awal mus
C. Ekstrak Tembakau
tembakau adalah sediaan pekat yang dipe
aun kering yang diperoleh dari tanaman
zat aktif dari tanaman tembakau ini menggunaka
sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau
serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah
ditetapkan (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995).
Ekstraksi atau penyarian merupakan pemindahan massa zat aktif yang
semula berada dalam sel, ditarik oleh cairan penyari tertentu sehingga terjadi
pelarutan zat aktif dalam cairan penyari. Metode penyarian dipilih berdasarkan
zat aktif yang terkandung dalam simplisia dan stabilitas zat aktif tersebut dalam
cairan penyari (Anonim, 1986).
Terutama pada ekstraksi cair-cair, sedapat mungkin terdapat perbedaan
kerapatan yang besar antara pelarut dan bahan ekstraksi. Hal ini dimaksudkan
agar kedua fase dapat dengan mudah dipisahkan kembali setelah pencampuran
(pemisahan dengan gaya berat). Bila beda kerapatannya kecil, seringkali
pemisahan harus dilakukan dengan menggunakan gaya sentrifugal (misalnya
dalam ekstraktor sentrifugal).
Ekstrak dan pelarut biasanya dipisahkan dengan cara penguapan maupun
destilasi, maka titik didih kedua bahan itu tidak boleh terlalu dekat, dan keduanya
tidak membentuk aseotrop. Ditinjau dari segi ekonomi, akan menguntungkan jika
pada proses ekstraksi titik didih pelarut tidak terlalu tinggi atau dengan panas
D. Kromatografi Lapis Tipis 1. Tinjauan Umum
Kromatografi lapis tipis (KLT) merupakan bentuk kromatografi planar,
selain kromatografi kertas dan elektroforesis. Pada kromatografi lapis tipis, fase
diamnya berupa lapisan yang seragam ( ) pada permukaan bidang datar
yang didukung oleh lempeng kaca, pelat aluminium, atau pelat plastik (Gandjar
dan Rohman, 2007).
Kromatografi lapis tipis merupakan metode pemisahan
komponen-komponen atas dasar perbedaan adsorpsi atau partisi oleh fase diam di bawah
gerakan pelarut pengembang atau pelarut pengembang campur (Mulja dan
Suharman, 1995).
Kromatogram pada KLT merupakan noda-noda yang terpisah setelah
visualisasi dengan cara fisika atau kimia. Visualisasi secara fisika yaitu dengan
melihat noda kromatogram yang mengabsorpsi radiasi ultraviolet atau
berfluoresensi dengan radiasi ultraviolet. Visualisasi dengan cara kimia adalah
dengan mereaksikan kromatogram dengan pereaksi warna lewat pemberian uap
zat kimia atau pencelupan ke dalam pereaksi penampak warna yang memberikan
warna atau fluoresensi yang spesifik (Mulja dan Suharman, 1995).
Parameter karakteristik pada KLT yaitu harga Rf ( )
yang didefinisikan sebagai perbandingan antara jarak senyawa dari titik awal dan
jarak tepi muka pelarut dari titik awal (Roth, 1994). Angka Rf berjangka antara
Rf =
(Dean, 1995)
Pemisahan pada kromatografi lapis tipis yang optimal akan diperoleh
hanya jika menotolkan sampel dengan ukuran bercak sekecil dan sesempit
mungkin, jika terlalu banyak maka akan menurunkan resolusi. Penotolan sampel
yang tidak tepat akan menyebabkan bercak yang menyebar dan puncak ganda
(Gandjar dan Rohman, 2007).
Kromatografi lapis tipis (KLT) bersama-sama dengan kromatografi
kertas dengan berbagai macam variasinya dirujuk sebagai kromatografi planar.
Dibandingkan dengan kromatografi cair kinerja tinggi (KCKT) dan kromatografi
gas (KG), KLT mempunyai beberapa keuntungan yaitu :
a. Kromatografi lapis tipis memberikan fleksibilitas yang lebih besar, dalam hal
memilih fase gerak.
b. Berbagai macam teknik untuk optimasi pemisahan seperti pengembangan 2
dimensi, pengembangan bertingkat, dan pembaceman penjerap dapat dilakukan
pada KLT.
c. Proses kromatografi sederhana dan dapat dihentikan kapan saja.
d. Semua komponen dalam sampel dapat dideteksi (Rohman, 2009).
2. Sistem KLT
a. Fase diam. Penjerap yang paling sering digunakan pada KLT adalah
silika dan serbuk selulosa, sementara mekanisme sorpsi-desorpsi (suatu
mekanisme perpindahan solut dari fase diam ke fase gerak atau sebaliknya) yang
sebagai penjerap juga dapat dibuat dari silika yang telah dimodifikasi, resin
penukar ion, gel eksklusi, dan siklodekstrin yang digunakan sebagai pemisahan
kiral (Rohman, 2009).
Silika gel memiliki permukaan yang terdiri atas gugus Si-O-Si dan gugus
silanol (Si-OH). Gugus silanol bersifat sedikit asam dan polar karenanya gugus ini
mampu membentuk ikatan hidrogen dengan solut-solut yang agak polar sampai
sangat polar. Adanya air dari atmosfer yang diserap oleh permukaan silika gel
sedikit afinitas terhadap adsorben polar, sementara solut-solut yang terpolarisasi
memiliki afinitas yang kecil terhadap adsorben polar disebabkan adanya interaksi
dipol atau interaksi-interaksi yang diinduksi oleh dipol (Gandjar dan Rohman,
2007).
b. Fase gerak. Pemilihan pelarut yang digunakan untuk senyawa yang
akan dianalisis dengan metode KLT harus dapat melarutkan analit dengan
sempurna, mudah menguap, serta dapat membasahi lapisan penyerap (Sherma dan
Fried, 1996).
Fase gerak adalah medium angkut yang terdiri atas satu atau beberapa
pelarut. Fase gerak bergerak di dalam fase diam yaitu lapisan berpori karena
gerak dan bila diperlukan sistem pelarut multikomponen, maka harus berupa suatu
campuran sederhana mungkin terdiri atas maksimum tiga komponen (Stahl,
1985).
Pemilihan sistem pelarut untuk mencapai sistem pemisahan yang
diperlukan mungkin melibatkan beberapa percobaan, tetapi pilihan pelarut cukup
terbatas dengan pertimbangan interferensi respon detektor atau kerusakan yang
mungkin terjadi dari fase diam (Dean, 1995).
Berikut adalah beberapa petunjuk dalam memilih dan mengoptimasi fase
gerak:
1) fase gerak harus mempunyai kemurnian yang sangat tinggi karena KLT
merupakan teknik yang sensitif
2) daya elusi fase gerak harus diatur sedemikian rupa sehingga harga Rf solut
terletak antara 0,2-0,8 untuk memaksimalkan pemisahan (Rohman, 2009).
E. Densitometri
Densitometri merupakan metode analisis instrumental yang mendasarkan
pada interaksi radiasi elektromagnetik dengan analit yang merupakan bercak pada
KLT. Densitometri lebih dititikberatkan untuk analisis kuantitatif analit-analit
dengan kadar kecil, yang mana diperlukan pemisahan terlebih dahulu dengan
KLT (Rohman, 2009).
Untuk evaluasi bercak hasil KLT secara densitometri, bercak di
dengan sumber sinar dalam bentuk celah ( ) yang dapat dipilih baik panjangnya
maupun lebarnya. Sinar yang dipantulkan diukur dengan sensor cahaya
dengan daerah yang mengandung bercak dihubungkan dengan banyaknya analit
yang ada melalui kurva kalibrasi yang telah disiapkan dalam lempeng yang sama.
Pengukuran densitometri dapat dibuat dengan absorbansi atau dengan fluoresensi
(Rohman, 2009).
Kromatografi lapis tipis densitometri merupakan salah satu dari metode
analisa kuantitatif. Penetapan kadar suatu senyawa dengan metode ini dilakukan
dengan mengukur kerapatan bercak senyawa yang dipisahkan dengan cara KLT.
Pada umumnya pengukuran kerapatan bercak tersebut dibandingkan dengan
kerapatan bercak senyawa standar yang dielusi bersama-sama (Hardjono, 1983).
Densitometer dapat bekerja secara serapan atau fluoresensi. Kebanyakan
densitometer mempunyai sumber cahaya, monokromator untuk memilih panjang
gelombang yang cocok, sistem untuk memfokuskan sinar pada lempeng,
pengganda foton, dan rekorder (Gandjar dan Rohman, 2007).
Noda yang kecil dan intensif akan menghasilkan suatu puncak yang
sempit dan tajam, sebaliknya noda yang lebar dan kurang intensif akan
menghasilkan puncak yang lebar maupun tumpul. Penelusuran bercak dapat
dilakukan secara horizontal maupun vertikal (Mintarsih, 1990).
Terdapat dua model pembacaan pada densitometri yaitu model
pemantulan ( ) dan transmitan. Model refleksi mengukur jumlah cahaya
yang dipantulkan dari permukaan dengan menggunakan lampu yang berbeda
sebagai lampu UV/VIS. Lampu halogen dan tungsten cocok digunakan untuk
sinar tampak, sedangkan lampu xenon dan deuterium digunakan pada sinar UV.
yang dihamburkan diukur dengan ") " , ") , dan ") .
Hasil dari detektor dikonversikan ke dalam sinyal tertentu. Kekurangan model ini
adalah pengaruh posisi bercak terhadap sinyal yang dihasilkan. Kesalahan yang
signifikan disebabkan karena perbedaan konsentrasi profil sampel dengan baku.
(Sherma dan Fried,1996).
Gambar 4. Ilustrasi model (a) refleksi (b) transmisi. L= , D= ,
F= ( ), P= plate, MF= , MC= (Sherma dan Fried,1996)
Pengukuran dengan model transmitan adalah mengukur absorbansi
substansi dalam rentang cahaya tampak. Detektor fotometrik mengukur intensitas
cahaya yang ditransmisikan pada sisi plat yang tidak berfluoresensi. Sinyal yang
dihasilkan merupakan fungsi dari jumlah molekul yang mengabsorbsi cahaya dari
lampu. Kelebihan model ini adalah fluktuasi transmisi akibat perbedaan posisi
bercak maupun gradien konsentrasi yang diabaikan. Model ini lebih sensitif
dibandingkan model refleksi karena semua molekul dalam bercak mempengaruhi
sinyal, tidak hanya molekul yang berada pada permukaan dalam model refleksi.
Kekurangan model ini adalah adanya interferensi latar yang dominan (Sherma dan
Fried,1996).
Pada umumnya sumber radiasi pada densitometer memberikan rentang
gelombang penentuan 200-630 nm. Lampu D2 (Deuterium) dipakai untuk
pengukuran pada daerah ultraviolet dan lampu tungstein untuk pengukuran pada
daerah sinar tampak. Untuk penentuan pendar fluor dan pemadaman pendar fluor
dipakai lampu busur Hg bertekanan tinggi. Sama seperti pada spektrofotometri,
pada densitometri juga dilakukan penentuan transmisi atau absorpsi dan refleksi
pada panjang gelombang maksimal (Mulja dan Suharman, 1995).
Gambar 5. CAMAG's TLC 3 densitometer (Camag, 2005)
Ada dua cara penetapan dengan alat densitometer. Pertama, setiap kali
penetapan ditotolkan sediaan baku dari senyawa yang bersangkutan dan dielusi
bersama dalam satu lempeng, kemudian Area Under Curve (AUC) sampel
dibandingkan dengan AUC zat baku. Yang kedua, dengan membuat kurva
hubungan antara jumlah zat baku dengan AUC. Kurva baku diperoleh dengan
membuat totolan zat baku pada pelat KLT dengan bermacam-macam konsentrasi
(minimal tiga macam konsentrasi). Bercak yang diperoleh dicari AUC dengan
densitometer. Berdasarkan kurva baku diperoleh persamaan: y = bx + a, di mana x
adalah banyaknya zat yang ditotolkan dan y adalah AUC (Supardjan, 1987).
Alat densitometri mempunyai sumber sinar yang bergerak di atas bercak
Lempeng digerakkan menyusuri berkas sinar yang berasal dari sumber sinar
tersebut. Bercak yang kecil dan intensif akan menghasilkan suatu puncak kurva
absorbsi yang sempit dan tajam, sebaliknya bercak yang lebar akan menghasilkan
puncak kurva absorbsi yang melebar dan tumpul (Sudjadi, 1988).
Metode densitometri mempunyai cara kerja yang sederhana dan cepat.
Pada metode densitometri diperlukan adsorben dan fase gerak yang murni. Untuk
memperoleh hasil yang baik umumnya digunakan adsorben siap pakai yang telah
mengalami pra pencucian (Gritter, 1991).
F. Validasi Metode 1. Tinjauan Umum
Validasi metode menurut * $) " (* $) dilakukan
untuk menjamin bahwa metode analisis bersifat akurat, spesifik, reprodusibel, dan
tahan pada kisaran analit yang akan dianalisis. Secara singkat, validasi merupakan
aksi konfirmasi bahwa metode analisis yang akan digunakan sesuai dengan tujuan
yang diinginkan (Rohman, 2009).
Tujuan utama validasi metode adalah untuk menghasilkan hasil analisis
yang paling baik. Untuk memperoleh hasil tersebut, semua variabel yang terkait
dengan metode analisis harus dipertimbangkan seperti prosedur pengambilan
sampel, tahap penyiapan sampel, jenis penyerap yang digunakan pada
kromatografi, fase gerak, dan sistem deteksinya. Banyaknya parameter yang harus
Metode analisis menurut ) * $) " +,) tahun
2007 dibedakan menjadi 4 kategori, yaitu :
a. Kategori I, mencakup prosedur analisis kuantitatif, untuk menetapkan kadar
komponen utama bahan obat atau zat aktif dalam sediaan farmasi.
b. Kategori II, mencakup prosedur analisis kualitatif dan kuantitatif yang
digunakan untuk menganalisis " dalam ruahan obat ( ) atau produk
degradasi dalam produk obat akhir.
c. Kategori III, mencakup prosedur analisis yang digunakan untuk menentukan
karakteristik penampilan suatu sediaan farmasi, misalnya disolusi dan
pelepasan obat.
d. Kategori IV, mencakup uji identifikasi.
Setiap kategori metode analisis memiliki persyaratan validasi yang berbeda-beda
seperti yang tercantum pada tabel di bawah ini.
Tabel I. Parameter analisis validasi metode (United States Pharmacopeial Convention, 2007) Parameter
kinerja analisis
Kategori I Kategori II Kategori III Kategori IV
Kuantitatif Batas Tes
* = Mungkin diperlukan (tergantung sifat spesifik tes)
2. Parameter Validasi
a. Selektivitas. Selektivitas suatu metode analisis untuk mengukur analit
yang dituju secara tepat dan spesifik dengan adanya komponen-komponen lain
analit yang dituju dengan pengganggu lainnya harus > 1,5 (Swartz dan Krull,
1997).
b. Linearitas. Linearitas merupakan kemampuan suatu metode (pada
rentang tertentu) untuk mendapatkan hasil uji yang secara langsung proporsional
dengan konsentrasi (jumlah) analit di dalam sampel. Persyaratan data linearitas
yang bisa diterima jika memenuhi nilai koefisien korelasi (r) ≥ 0,999 (Ermer dan
Miller, 2005).
c. Akurasi. Akurasi atau kecermatan metode analisis adalah kedekatan
hasil analisis yang diperoleh dengan menggunakan metode tersebut dengan nilai
yang sebenarnya. Penentuan kecermatan metode analisis biasanya dinyatakan
dengan persen perolehan kembali terhadap sampel yang kadarnya telah diketahui
dengan pasti (Mulja dan Suharman, 1995).
Tabel II. Kriteria rentang yang dapat diterima (Garfield, ., Harmita, 2004) Analit pada matriks sampel
(%)
d. Presisi. Presisi suatu metode analisis merupakan sejumlah pencaran
hasil yang diperoleh dari analisis berulang kali pada suatu sampel homogen.
dapat dinyatakan memiliki presisi yang baik apabila memiliki nilai CV ≤ 2%
(Harmita, 2004).
Tabel III. Kriteria CV yang dapat diterima (Garfield, ., Harmita, 2004) Kadar analit (%) CV (%)
dedefinisikan sebagai konsentrasi analit terendah dalam sampel yang masih dapat
dideteksi, meskipun tidak selalu dapat dikuantifikasi. LOD merupakan batas uji
yang secara spesifik menyatakan apakah analit di atas atau di bawah nilai tertentu.
Sebagai contoh, batas deteksi merupakan banyaknya sampel yang menunjukkan
respon (S) 3 kali terhadap derau (N) atau LOD = 3 S/N (Swartz dan Krull, 1997).
f. Batas Kuantifikasi (& - atau LOQ). Batas
kuantifikasi didefinisikan sebagai konsentrasi analit terendah dalam sampel yang
dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi
operasional metode yang digunakan. Rasio 10 : 1 digunakan untuk
menentukan LOQ (Rohman, 2009).
g. Kisaran. Menurut definisi ICH, kisaran suatu prosedur analisis adalah
interval antara konsentrasi (jumlah) analit pada level atas dan pada level bawah
dalam suatu sampel, yang mana dapat ditunjukkan bahwa prosedur analisis
mempunyai level akurasi, presisi dan linearitas yang sesuai (Rohman, 2009).
h. Kekasaran ( ). Kekasaran ( ) merupakan tingkat
yang diekspresikan sebagai persen standar deviasi relatif (% RSD).
Kondisi-kondisi ini meliputi laboratorium, analis, alat, reagen, dan waktu percobaan yang
berbeda (Rohman, 2009).
i. Ketahanan ( ). Ketahanan merupakan kapasitas metode untuk
tetap tidak terpengaruh oleh adanya variasi parameter metode yang kecil.
Ketahanan dievaluasi dengan melakukan variasi parameter-parameter metode
seperti presentase pelarut organik, pH, kekuatan ionik, dan suhu (Gandjar dan
Rohman, 2007).
G. Landasan Teori
Nikotin banyak terdapat dalam tanaman tembakau. Di dalam suatu
ekstrak etanolik daun tembakau banyak terdapat senyawa lain selain nikotin,
seperti nornikotin, anabasin, dan anatabin. Nikotin dan senyawa lain dalam
ekstrak etanolik daun tembakau dapat dipisahkan dengan metode KLT karena
adanya perbedaan interaksi antara nikotin dengan senyawa-senyawa lain dalam
ekstrak dengan fase diam dan fase gerak yang digunakan. Setelah pemisahan
dengan KLT, bercak analit dapat dianalisis kuantitatif dengan metode
densitometri. Penetapan kadar dilakukan dengan mengukur kerapatan bercak
senyawa.
Suatu metode baru yang dikembangkan harus melalui tahapan validasi
metode untuk memberikan jaminan bahwa metode analisis yang digunakan
bersifat akurat, spesifik, reprodusibel, dan tahan pada kisaran analit yang akan
dipercaya. Sebelum melakukan validasi metode dilakukan optimasi metode
terlebih dahulu untuk mengoptimalkan kondisi awal analisis berupa resolusi,
bentuk " , faktor asimetri, dan reprodusibilitas nilai Rf dan . Parameter
kondisi optimum metode telah terpenuhi dengan menggunakan fase diam silika
gel 60 F254 dan fase gerak n-heksan: toluen: dietilamin (15,25:5,75:4) sehingga
diperoleh hasil bentuk " kromatogram yang simetris dan runcing yang dilihat
dari nilai " dari 3 kali replikasi pada konsentrasi rendah,
sedang, dan tinggi adalah 1, nilai resolusi 3 kali replikasi sampel berturut-turut
adalah 1,58; 1,89; dan 1,88; serta reprodusibilitas nilai R dan dengan CV
berturut-turut adalah 1,79% dan 0%.
Melalui adanya proses optimasi metode analisis, maka akan memberikan
jaminan kondisi yang optimum terhadap sistem yang digunakan dalam melakukan
proses validasi metode. Parameter validasi yang diteliti meliputi selektivitas,
linearitas, akurasi, dan presisi. Suatu metode dinyatakan valid apabila memenuhi
persyaratan parameter validasi yang ditetapkan.
H. Hipotesis
Metode KLT-densitometri pada penetapan kadar nikotin dalam ekstrak
etanolik daun tembakau memenuhi parameter-parameter validasi, yaitu
22
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan bersifat non eksperimental deskriptif karena
tidak terdapat manipulasi dan perlakuan terhadap subjek uji.
B. Variabel Penelitian
1. Variabel bebas adalah sistem KLT yang telah dioptimasi, yaitu fase diam silika
gel 60 F254 dan fase gerak n-heksan: toluen: dietilamin (15,25 : 5,75 : 4).
2. Variabel tergantung adalah parameter validasi yaitu selektivitas, linearitas,
akurasi, dan presisi.
3. Variabel pengacau terkendali adalah :
a. Pelarut, untuk mengatasinya digunakan pelarut " analisis yang memiliki
kemurnian tinggi.
b. Larutan baku nikotin yang bersifat mudah teroksidasi oleh udara atau
cahaya, untuk mengatasinya digunakan untuk menutupi
alat-alat gelas.
c. Paparan cahaya dan udara terkait dengan sifat nikotin yang fotosensitif dan
mudah teroksidasi, untuk mengatasinya pada saat preparasi semua peralatan
gelas yang akan digunakan dilapisi dengan serta dalam
pengerjaannya dilakukan dalam ruangan dengan intensitas cahaya yang
C. Definisi Operasional
1. Nikotin merupakan suatu alkaloid dari ekstrak tanaman tembakau.
2. Ekstrak tembakau yang digunakan merupakan sediaan pekat yang diperoleh
dengan mengekstraksi daun kering yang berasal dari tanaman tembakau
dengan pelarut etanol menggunakan metode ekstraksi soxhletasi.
3. Sistem KLT yang digunakan dalam penelitian adalah fase diam silika gel 60
F254 dan fase gerak n-heksan : toluen : dietilamin (15,25 : 5,75 : 4).
4. Densitometri merupakan salah satu dari metode analisa dengan mengukur
kerapatan bercak senyawa yang dipisahkan secara KLT.
5. Kadar nikotin dinyatakan dalam " " (ppm).
6. Parameter validasi yang digunakan adalah selektivitas, linearitas, akurasi, dan
presisi.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini merupakan bahan
berkualitas " analisis (" ) kecuali dinyatakan lain, yaitu baku nikotin (
), ekstrak etanolik daun tembakau, etanol, n-heksan, toluen, dietilamin,
NaOH 4M, HCl encer (22,6%), aquadest, kloroform, metanol, amonia, etanol
E. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat alat
densitometer . ' & + CAT. No. 027.6485 SER. No.160602/,
autosampler ( ' & 0 CAT. No. 027.7808. SER. No. 170610),
indikator pH, mikropipet 1 ACURA 825 (100-1000 µL), neraca analitik
( SBC 22 max 60/210 g; min 0,001 g; d=0,01/0,1mg; e=1mg),
ultrasonikator ( )tipe T460 no V935922013 Ey), stirer (2 ") MR 2002),
dan alat-alat gelas yang umum digunakan dalam analisis ($ 1).
F. Tata Cara Penelitian 1. Pembuatan fase gerak
Fase gerak yang digunakan dalam penelitian menggunakan campuran
heksan : toluen : dietilamin (15,25:5,75:4). Komponen fase gerak terdiri atas
n-heksan sebanyak 15,25 mL, toluen sebanyak 5,75 mL, dan dietilamin sebanyak 4
mL. Masing-masing komponen fase gerak dimasukkan ke dalam labu takar 25 mL
kemudian digojog sehingga campuran homogen.
2. Pembuatan larutan baku
a. Pembuatan larutan stok nikotin 50 ppm. Larutan induk (baku) nikotin
sebanyak 248 µL dipipet kemudian dimasukkan ke dalam labu takar 5 mL dan
dilarutkan dalam etanol hingga tanda.
b. Pembuatan seri larutan baku nikotin. Larutan stok nikotin sebanyak
mL kemudian diencerkan dengan etanol hingga tanda, sehingga diperoleh
konsentrasi 1, 2, 3, 4, dan 5 ppm.
3. Penetapan panjang gelombang pengamatan
Seri larutan baku konsentrasi 1 ppm, 3 ppm, dan 5 ppm masing-masing
ditotolkan dengan volume penotolan 1 µL pada plat KLT dengan fase diam silika
gel 60 F254 dan setelah kering dikembangkan dalam bejana kromatografi yang
telah dijenuhi dengan fase gerak dengan jarak pengembangan 10 cm. Setelah
mencapai jarak rambat 10 cm, plat dikeluarkan dari bejana dan dikeringkan. Plat
hasil pengembangan kemudian secepatnya di pada panjang gelombang
pengamatan (200-300 nm) menggunakan & pada densitometer.
4. Pembuatan kurva baku nikotin dan pengamatan nilai (Rf) nikotin
Seri larutan baku konsentrasi 1, 2, 3, 4, dan 5 ppm masing-masing
ditotolkan dengan volume penotolan 1 µL pada plat KLT dengan fase diam silika
gel 60 F254 dan setelah kering dikembangkan dalam bejana kromatografi yang
telah dijenuhi dengan fase gerak. Setelah mencapai jarak rambat 10 cm, plat
dikeluarkan dari bejana dan dikeringkan. Plat hasil pengembangan kemudian
secepatnya diukur AUC dan tinggi " nya dengan densitometer pada λ
pengamatan 261 nm. Replikasi dilakukan sebanyak 3 kali dan pilih persamaan
kurva baku yang paling baik. Selain itu dilihat pula nilai Rf dari masing-masing
5. Penentuan dan (CV) baku
Seri larutan baku konsentrasi 1 ppm, 3 ppm, dan 5 ppm diberi perlakuan
seperti pada poin F.4. Replikasi dilakukan sebanyak 5 kali. Selanjutnya dihitung
kadar terukur dengan menggunakan persamaan kurva baku yang telah dibuat pada
poin F.4. Berdasarkan data ini dapat ditentukan dan CVnya.
6. Penentuan dan (CV) baku dalam
matriks sampel
a. Preparasi larutan sampel (LS). Ekstrak kental daun tembakau sejumlah
1 g ditimbang seksama kemudian ditambahkan 10 mL HCl encer (22,6%) dan
diultrasonifikasi selama 30 menit. Setelah itu kloroform 10 mL ditambahkan dan
dimasukkan ke dalam corong pisah dan dilakukan penggojogan selama 5 menit
hingga terbentuk dua lapisan, kemudian diambil fase polar di bagian atas. Pada
fase tersebut NaOH 4M sebanyak 8 mL ditambahkan sambil diaduk dengan stirer
hingga larutan bersifat basa, dan dicek pH-nya dengan menggunakan pH
indikator. Setelah pH basa (pH ± 12) kemudian kloroform 10 mL ditambahkan
dan kembali digojog selama 5 menit dan didiamkan hingga terbentuk dua lapisan,
kemudian diambil fase non polar pada bagian bawah. Kloroform diuapkan di
dalam lemari asam dan setelah seluruh kloroform menguap kemudian
ditambahkan sedikit etanol dan larutan tersebut dimasukkan ke dalam labu takar 5
mL dan diencerkan dengan etanol hingga tanda.
b. Pembuatan larutan sampel dengan adisi (LSN). Larutan sampel nikotin
sebanyak 1,125 mL diambil dan dimasukkan ke dalam labu takar 5 mL. Larutan
dengan konsentrasi 50 ppm dan diencerkan dengan etanol hingga tanda, sehingga
diperoleh kadar kurang lebih 4 ppm. Replikasi dilakukan sebanyak lima kali.
c. Pengembangan dan pengukuran. LS dan LSN diberi perlakuan seperti
pada poin F.4. Setelah itu dihitung kadar baku nikotin dalam sampel
menggunakan persamaan kurva baku yang telah dibuat pada poin F.4. Kadar baku
nikotin dalam sampel adalah selisih kadar LSN dengan kadar LS. Selanjutnya
dihitung dan CVnya.
G. Analisis Hasil 1. Selektivitas
Selektivitas ditentukan dengan membandingkan nilai Rf baku dan Rf
sampel. Selain itu, selektivitas juga ditunjukkan dengan nilai resolusi > 1,5.
Resolusi (Rs) =
2. Linearitas
Linearitas dilihat dari nilai r (koefisien korelasi) hasil pengukuran seri
baku nikotin. Suatu metode memiliki linearitas yang baik jika r ≥ 0,999.
3.Akurasi
Akurasi metode analisis dinyatakan dengan yang dapat dihitung
dengan cara berikut:
4.Presisi
Presisi metode analisis dinyatakan dengan
(CV), yang dapat dihitung dengan cara berikut:
CV = " !
5. Akurasi pengukuran baku dalam matriks sampel
= "
29 BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Fase Gerak
Fase gerak yang digunakan dalam penelitian ini diperoleh dari hasil
optimasi yang dilakukan pada rangkaian penelitian ini, yaitu n-heksan : toluen :
dietilamin (15,25:5,75:4) (Chairio, 2011). Tujuan pembuatan fase gerak dengan
jenis dan komposisi tersebut adalah untuk menghasilkan polaritas fase gerak yang
sesuai sehingga dapat memisahkan nikotin secara optimal. Oleh karena itu,
dibutuhkan fase gerak yang mampu berinteraksi dengan nikotin sehingga mampu
mengelusi nikotin dari fase diam silika gel 60 F254. Sistem kromatografi pada
penelitian ini merupakan kromatografi fase normal, karena fase gerak pada
penelitian ini bersifat lebih non polar daripada fase diamnya.
B. Preparasi Sampel
Sampel yang digunakan yaitu larutan ekstrak etanolik daun tembakau.
Daun tembakau dikeringkan, diserbuk dan dilakukan ekstraksi dengan metode
soxhletasi menggunakan pelarut etanol 96%, karena nikotin larut dalam etanol.
Prinsip ekstraksi adalah pemisahan senyawa dari campuran senyawa dengan
pelarut yang sesuai. Metode soxhletasi ini menggunakan pemanasan yang
dilakukan terus-menerus, nikotin termasuk senyawa yang stabil terhadap
pemanasan, titik didih nikotin cukup tinggi yaitu 247°C, sehingga metode
metode soxhletasi karena pada soxhletasi proses penyarian simplisia berlangsung
secara berkesinambungan dan pelarut selalu baru sehingga lebih efektif dalam
penyarian nikotin, serta jumlah pelarut yang dibutuhkan lebih sedikit. Ekstrak
kental hasil soxhletasi kemudian dipreparasi dengan menambahkan HCl encer
(22,6% v/v) dan dilakukan ultrasonifikasi untuk membantu pelarutan.
+ HCl
Cl
nikotin hidroklorida nikotin
Gambar 6. Reaksi penggaraman nikotin dengan larutan HCl
Berdasarkan gambar 6, dengan adanya penambahan HCl maka nikotin
akan terprotonasi menjadi nikotin hidroklorida. Langkah selanjutnya yaitu
penambahan kloroform di dalam corong pisah dan digojog selama 5 menit
sehingga akan terjadi pemisahan. Pemisahan ini bertujuan untuk memisahkan
nikotin dari senyawa-senyawa non polar yang mungkin terikut seperti senyawa
hidrokarbon, minyak, zat lilin, dan steroid pada daun tembakau.
Senyawa-senyawa non polar tersebut dapat mengganggu proses elusi nikotin ketika
ditotolkan karena bobot molekul yang besar. Nikotin yang terprotonasi akan
berada dalam fase polar atau pada bagian atas, sedangkan senyawa-senyawa non
polar akan berada di bagian bawah. Fase polar diambil dan ditambah dengan
NaOH sehingga nikotin kembali ke bentuk molekul basanya, kemudian ditambah
+ NaOH
nikotin
+ NaCl
nikotin hidroklorida
Cl
Gambar 7. Reaksi pembentukan molekul nikotin basa
Berdasarkan gambar 7, nikotin hidroklorida bereaksi dengan NaOH
membentuk nikotin basa, maka nikotin akan berada di fase non polar (bagian
bawah) karena telah berada dalam bentuk molekulnya dan nikotin larut dalam
kloroform. Fraksi kloroform diuapkan sehingga hanya tersisa nikotin dan alkaloid
lain yang memiliki kemiripan sifat dengan nikotin, yaitu nornikotin, anabasin, dan
anatabin. Nikotin memiliki titik didih yang tinggi sehingga tidak ikut menguap
bersama kloroform. Setelah kloroform diuapkan kemudian nikotin dilarutkan
dalam etanol
Selama proses preparasi sampel, semua peralatan gelas yang digunakan
dilapisi dengan dikarenakan sifat dari nikotin yang tidak stabil
terhadap paparan cahaya dan udara. Apabila larutan nikotin dibiarkan dalam
keadaan terpapar dengan udara, maka nikotin akan teroksidasi dan berubah
menjadi warna coklat. , ) , dan nikotin N-1 oksida adalah
produk degradasi yang terbentuk akibat proses oksidasi pada nikotin.
C. Pembuatan Larutan Baku
Larutan baku nikotin dibuat dengan melarutkan baku nikotin dengan
3, 4, dan 5 ppm. Pemilihan seri konsentrasi ini disesuaikan dengan respon
detektor terhadap sinyal (" ) yang dihasilkan, sehingga tidak terganggu oleh
yang dihasilkan alat. Selain itu pemilihan seri konsentrasi ini juga bertujuan
agar respon analit dalam sampel dapat masuk dalam respon seri larutan baku yang
dibuat, sehingga persamaan kurva baku yang diperoleh dapat digunakan untuk
penetapan kadar analit dalam sampel.
D. Penetapan Panjang Gelombang Pengamatan Nikotin
Tujuan dari penetapan panjang gelombang pengamatan yaitu untuk
mendapatkan panjang gelombang analisis yang dapat memberikan serapan
nikotin. Pada penelitian ini hanya nikotin yang dianalisis, sehingga panjang
gelombang pengamatan yang digunakan adalah panjang gelombang dimana
nikotin memberikan serapan maksimum. Alasan penggunaan panjang gelombang
maksimum adalah pada panjang gelombang maksimum analit memberikan respon
yang maksimum, perubahan respon untuk setiap konsentrasi zat adalah yang
paling besar, sehingga kepekaan analisis maksimal dan dapat meminimalkan
kesalahan sewaktu pengukuran.
Gambar 8. Kromofor pada nikotin
Berdasarkan gambar 8, nikotin memiliki kromofor yang pendek pada
cincin piridinnya. Ikatan terkonjugasi yang pendek menyebabkan panjang
gelombang maksimalnya kecil, sehingga nikotin menyerap radiasi pada daerah
ultraviolet. Oleh karena itu, panjang gelombang maksimum nikotin
dilakukan pada 200-300 nm menggunakan alat densitometer.
Gambar 9. Densitogram baku nikotin dengan konsentrasi 3 ppm dalam pelarut etanol
Panjang gelombang teoritis nikotin yaitu 262 nm (Popl, Fanhrich, dan
Tatar, 1990). Berdasarkan gambar 9, hasil percobaan menunjukkan panjang
gelombang maksimum nikotin pada λ 261 nm. Jika dibandingkan dengan panjang
gelombang nikotin teoritis maka terjadi pergeseran sebesar 1 nm. Pergeseran ini
masih memenuhi ketentuan yang ditetapkan dalam Farmakope Indonesia edisi IV
(1995) karena dimaknai memenuhi syarat jika tepat atau dalam batas 2 nm dari
maksimum nikotin sesuai dengan panjang gelombang teoritis, sehingga dapat
dipastikan senyawa tersebut adalah nikotin. Menurut Moffat, Osselton, dan
Widdop (2011), pada pelarut asam dan panjang gelombang 259 nm, nikotin
memiliki # !$ sebesar 338a , maka nilai absorptivitas molarnya (ε) adalah
5482,36 M-1cm-1. Berdasarkan nilai absorptivitas molarnya, nikotin cukup sensitif
diukur dengan detektor UV pada alat densitometer.
E. Pengamatan Nilai (Rf) dan Pembuatan Baku Nikotin
Nilai Rf merupakan parameter analisis kualitatif yang nantinya digunakan
untuk mengetahui ada tidaknya analit dalam sampel. Pengamatan nilai Rf
menggunakan konsentrasi tengah seri baku nikotin, yaitu 3 ppm. Berdasarkan
pengamatan, nilai Rf baku nikotin yaitu 0,52.
Gambar 10. Kromatogram baku nikotin konsentrasi 3 ppm (Rf = 0,52)
Nilai Rf nikotin dipengaruhi oleh interaksi nikotin dengan fase diam dan
fase gerak. Interaksi nikotin dengan fase diam dan fase gerak dapat dilihat pada
H
Gambar 11. Interaksi hidrogen nikotin dengan fase diam silika gel 60 F254
Interaksi Van der Waals
Transfer muatan
Interaksi hidrogen
Gambar 12. Interaksi nikotin dengan fase gerak ( n-heksan : toluen : dietilamin)
Berdasarkan gambar 11 dan 12, nampak bahwa interaksi nikotin dengan
fase gerak lebih dominan dibandingkan dengan fase diamnya. Adanya interaksi
hidrogen antara nikotin dan fase diam menyebabkan nikotin tertambat pada fase
diam namun hanya pada permukaannya (adsorpsi), sedangkan dengan fase gerak
terjadi interaksi hidrogen, transfer muatan, dan interaksi Van der Waals. Interaksi
yang sesuai antara nikotin dengan fase diam dan fase gerak akan menghasilkan
pemisahan yang maksimal.
Fase gerak yang digunakan yaitu n-heksan : toluen : dietilamin (15,25 :
5,75 : 4). Indeks polaritas campuran dari fase gerak tersebut yaitu 1,248.
Penggunaan fase gerak tersebut menghasilkan nilai R nikotin diantara 0,2-0,8
Interaksi hidrogen
yaitu 0,52 yang menunjukkan terjadinya interaksi kesetimbangan dinamis antara
analit dengan fase diam dan fase gerak. Fase diam yang digunakan yaitu silika gel
60 F254 yaitu fase diam silika yang mengandung indikator fosforesensi sehingga
bercak nikotin akan lebih mudah terlihat dan terdeteksi di bawah sinar UV. Gugus
kromofor nikotin akan menyerap cahaya dari sinar UV sehingga sinar UV tidak
dapat mencapai indikator fosforesensi dan tidak ada cahaya yang dipancarkan
pada bercak tersebut. Oleh karena itu, terjadi peredaman bercak atau - )
dengan latar belakang fosforesensi dengan warna hijau.
Pembuatan kurva baku nikotin dilakukan 3 kali replikasi untuk
mendapatkan koefisien korelasi yang paling baik, yaitu nilainya ≥ 0,999; karena
menunjukkan adanya korelasi yang linier antara konsentrasi dan respon
pengukuran yang dihasilkan, yaitu berupa * (AUC). Respon
yang menunjukkan nilai koefisien korelasi paling baik yang digunakan dalam
pembuatan kurva baku.
Tabel IV. Data replikasi kurva baku nikotin
Baku Nikotin
Replikasi I Replikasi II Replikasi III Seri baku
Kurva baku yang digunakan adalah kurva baku yang memiliki linearitas
proporsional terhadap konsentrasi (jumlah) analit. Berdasarkan tabel IV, koefisien
korelasi paling baik ditunjukan pada replikasi III dengan r = 0,999; sehingga
persamaan kurva baku inilah yang digunakan dalam penetapan kadar. Persamaan
kurva bakunya yaitu y = 2778,69x + 2911,17.
Gambar 13. Hubungan antara konsentrasi nikotin dengan AUC (replikasi III)
F. Validasi Metode Analisis
Validasi metode analisis bertujuan untuk membuktikan bahwa metode
analisis yang digunakan telah memenuhi persyaratan validitas sehingga dapat
memberikan hasil analisis yang dapat dipercaya. Parameter validasi pada
penelitian ini meliputi selektivitas, linearitas, akurasi, dan presisi. Validasi
dilakukan dengan 3 seri konsentrasi sebanyak 5 replikasi. Konsentrasi yang
digunakan merupakan konsentrasi rendah, sedang, dan tinggi dari konsentrasi seri
baku, yaitu 1, 3, dan 5 ppm. Tiga konsentrasi tersebut yang digunakan karena
telah mewakili konsentrasi seri baku lainnya.
1. Selektivitas
Penentuan selektivitas dari metode KLT-densitometri ini dapat dilihat
dengan membandingkan nilai Rf baku dan nilai Rf analit dalam sampel. Namun,
nilai Rf merupakan parameter kualitatif, parameter kuantitatif dapat dilihat dari
nilai resolusi (Rs). Syarat selektivitas yang baik apabila memiliki nilai Rs > 1,5
(Swartz dan Krull, 1997).
Tabel V. Perbandingan nilai Rf baku dan sampel, serta nilai resolusi
Konsentrasi seri
dalam sampel menunjukkan nilai yang identik, sehingga " analit dalam sampel
tersebut merupakan " nikotin, namun harus lebih dipastikan dengan
penambahan baku nikotin dalam matriks sampel pada prosedur kerja selanjutnya.
Berdasarkan data resolusi yang diperoleh pada tabel, dapat diketahui bahwa
resolusi antara " analit dan " terdekat telah memenuhi persyaratan resolusi
Gambar 14. Kromatogram baku nikotin konsentrasi 5 ppm (Rf = 0,53)
Gambar 15. Kromatogram sampel replikasi I (Rf = 0,55)
Berdasarkan gambar 15, dapat dilihat bahwa nilai resolusi antara "
analit (peak nomor 3) dengan " terdekat (peak nomor 2) adalah 1,58. Hal ini
menunjukkan bahwa metode KLT-Densitometri ini memenuhi parameter
selektivitas dalam menetapkan kadar nikotin.
2. Linearitas
Linearitas suatu metode menunjukkan proporsionalitas nilai kadar
terhadap respon (absorbansi, luas area, tinggi puncak). Linearitas ditunjukkan oleh
nilai koefisien korelasi (r). Suatu metode dikatakan memenuhi parameter
Berdasarkan data yang diperoleh dari hasil pembuatan kurva baku pada
tabel IV, didapat nilai r untuk replikasi I = 0,998, replikasi II = 0,998, dan
replikasi III = 0,999. Nilai r yang memenuhi syarat linearitas yang baik yaitu pada
replikasi III, dengan nilai r = 0,999. Oleh karena itu, metode KLT-densitometri ini
telah memenuhi syarat linearitas yang baik dalam menetapkan kadar nikotin.
3. Akurasi
Akurasi suatu metode analisis dinyatakan dengan nilai . Suatu
metode dikatakan memiliki akurasi yang baik apabila memiliki nilai %
antara 98-102% (Garfield, ., Harmita, 2004).
Tabel VI. Data % Kadar
nikotin (ppm)
(%)
Replikasi I Replikasi II Replikasi III Replikasi IV Replikasi V
1 99,78 101,84 98,72 100,69 102,46
3 101,80 99,90 101,09 100,99 100,06
5 98,23 100,44 100,55 100,23 99,64
Berdasarkan hasil yang diperoleh pada tabel VI, nilai yang
masuk pada rentang akurasi yang baik yaitu 98-102% adalah konsentrasi level
sedang hingga tinggi. Pada level konsentrasi rendah (1 ppm), metode ini memiliki
nilai antara 98,72 - 102,46%, nilai yang diperoleh tidak
memenuhi persyaratan akurasi yang baik. Oleh karena itu, metode ini memiliki
akurasi yang baik pada kadar 3 ppm hingga 5 ppm, sehingga dapat digunakan
4. Presisi
Presisi merupakan parameter dalam mengukur suatu metode dalam
mendapatkan hasil yang reprodusibel. Presisi dinyatakan dengan nilai
(CV). Syarat presisi yang baik yaitu nilai CV≤ 2% (Harmita, 2004).
Tabel VII. Data (CV)
Berdasarkan data pada tabel VII, dapat dilihat bahwa pada konsentrasi 1
ppm, 3 ppm, dan 5 ppm telah memenuhi syarat presisi yang baik, karena nilai CV
kurang dari 2%. Oleh karena itu, metode ini memiliki presisi yang baik dalam
menetapkan kadar nikotin pada level konsentrasi tersebut.
G. Penentuan Akurasi dan Presisi Baku Nikotin dalam Sampel
Tujuan dari penentuan akurasi dan presisi baku nikotin dalam sampel
yaitu untuk memastikan bahwa " dengan nilai Rf yang identik terhadap baku
nikotin memang merupakan " senyawa nikotin. Cara mengetahuinya adalah
dengan menambahkan baku nikotin ke dalam matriks sampel. Apabila luas area
pada " tersebut bertambah ketika baku nikotin ditambahkan, maka dapat
dipastikan bahwa " tersebut merupakan " nikotin. Tujuan lain yaitu untuk
melihat apakah metode ini apabila diaplikasikan pada matriks sampel memberikan
hasil yang memenuhi akurasi dan presisi yang baik atau tidak. Metode ini
dilakukan apabila tidak memungkinkan membuat sampel plasebo karena pada
senyawa endogen (metabolit sekunder) sehingga dipakai metode adisi ini untuk
menyesuaikan matriks baku dengan matriks sampel.
Gambar 16. Kromatogram sampel tanpa penambahan baku nikotin
Gambar 17. Kromatogram sampel dengan penambahan baku nikotin
Berdasarkan gambar 16 dan 17, terjadi penambahan luas area pada "
yang memiliki Rf identik dengan baku nikotin. Maka dapat disimpulkan bahwa
" tersebut merupakan nikotin.
Setelah dapat dipastikan bahwa " dengan nilai Rf yang identik
tersebut merupakan " dari nikotin, maka selanjutnya dilakukan penentuan
ditambahkan pada matriks sampel adalah 3,1 ppm, maka nilai yang
dapat diterima yaitu 80-110% dan nilai CV ≤ 16% (Garfield, ., Harmita, 2004).
Tabel VIII. dan CV baku nikotin dalam matriks sampel Replikasi (%) CV (%)
I 90,65
3,32
II 88,71
III 86,77
IV 88,39
V 82,90
Berdasarkan tabel VIII, dapat disimpulkan bahwa metode
KLT-Densitometri ini dapat mengukur kadar analit dalam matriks sampel secara akurat
dan seksama karena memiliki nilai CV dan yang memenuhi persyaratan.
44 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Metode KLT-densitometri dengan instrumen ' & +
CAT. No. 027.6485 SER. No.160602, fase diam silika gel 60 F254, fase gerak
n-heksan : toluen : dietilamin (15,25 : 5,75 : 4), volume penotolan 1,0 µL, dan jarak
pengembangan 10 cm memiliki selektivitas yang baik dengan resolusi pada 3 kali
replikasi sampel berturut-turut adalah 1,58; 1,89; dan 1,88; linearitas yang baik
pada konsentrasi 1-5 ppm dengan r = 0,999; nilai dan CV berturut-turut
untuk konsentrasi nikotin 1 ppm, 3 ppm, dan 5 ppm yaitu 98,72-102,46% dan
1,50%; 99,90-101,80% dan 0,78%; 98,23-100,55% dan 0,96%. Berdasarkan hasil
tersebut, maka metode KLT-densitometri ini memiliki validitas yang baik untuk
menetapkan kadar nikotin dalam ekstrak etanolik daun tembakau.
B. Saran
Metode analisis yang telah divalidasi ini perlu diaplikasikan pada