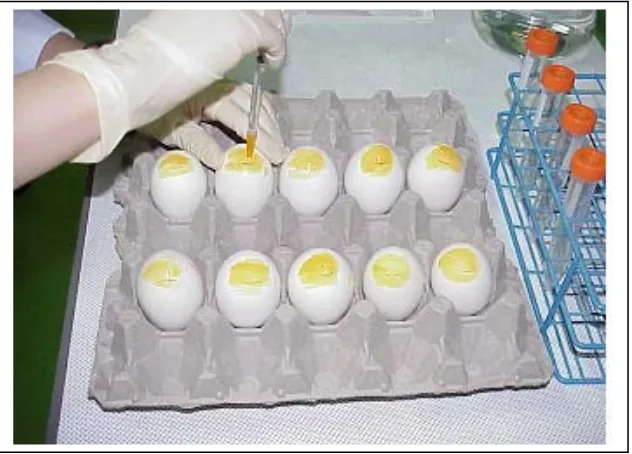
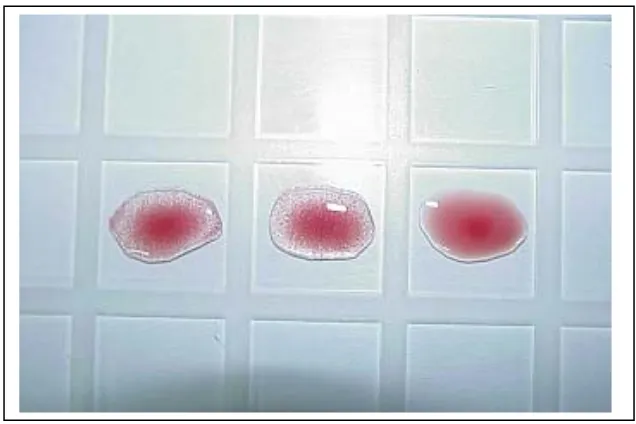
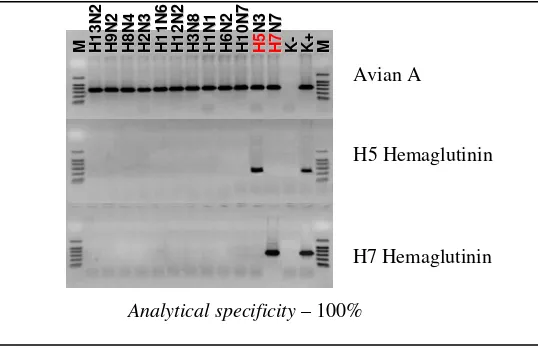
Characterisation and Identification of Avian Influenza Virus (AI)
Teks penuh
Gambar
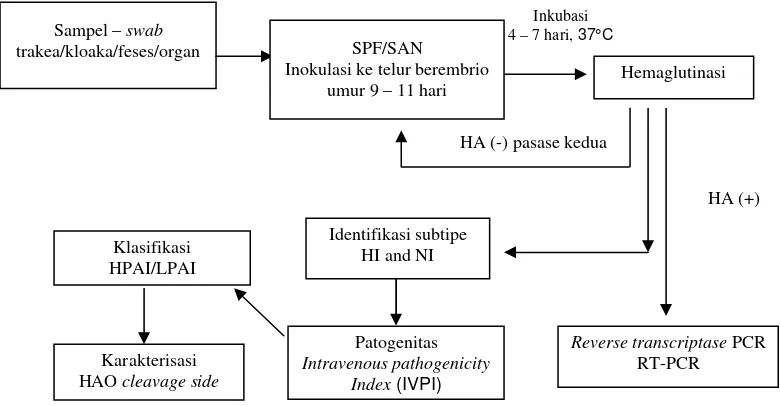

Dokumen terkait
Analisis Sidik Ragam menunjukkan laju pertumbuhan diameter tunas pada perlakuan persemaian menunjukkan hasil berbeda nyata pada taraf 0,05 dan uji lanjutan Beda Nyata
Dalam stability of consociational settlement yang akan disinggung dalam pembahasan konflik di Irlandia Utara ini meliputi agenda kebijakan politik dan kebijakan
Berdasarkan hasil kuesioner yang telah dilakukan tersebut, Penulis menggunakan dan mengembangkan 2 gaya gambar yang mendapatkan perolehan suara terbanyak yaitu gaya
Kedudukan, Susunan Organisasi, Uraian Tugas dan Tata Kerja Dinas Perhubungan Kabupaten Lumajang mengalami perubahan, sehingga Rencana strategis Dinas Perhubungan
keunggulan estetik dibandingkan pasak yang terbuat dari logam.. -- Pa Pasa sak k y yan ang g te terb rbua uat t da dari ri b bah ahan an lo loga gam m te terd rdap apat at
Bila gejala klinis sudah tidak ada dan BB anak sudah mencapai 80% BB/U, dapat dak ada dan BB anak sudah mencapai 80% BB/U, dapat dikatakan anak sembuh.Pola pemberian makan yang baik
5.2.2 Kepala seksi menetapkan jadwal Pelaksanaan Diklat selama satu tahun berdasarkan program kerja yang ada dalam DIPA Balai Diklat Industri Jakarta.. Jadwal
Pada jenis serangan ini, penyerang tidak terlibat dalam komunikasi antara pengirim dan penerima, namun penyerang menyadap semua pertukaran pesan antara kedua entitas