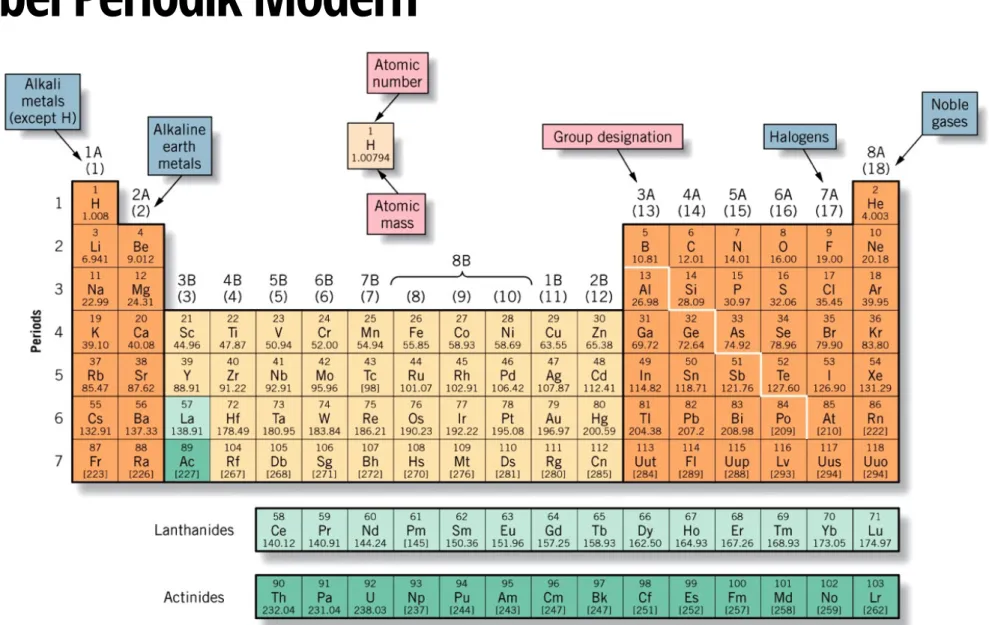
1. Unsur, senyawa dan tabel periodik
Kimia Dasar 1A
Dr. Rukman Hertadi
De nisi:
Kimia adalah disiplin ilmu yang
mempelajari komposisi, sifat-sifat dan
transformasi materi
Eksperimen menemukan bahwa proton dan netron merupakan partikel penyusun inti atom yang mengisi volume sangat kecil dan masif, sementara elektron berada di luar inti mengisi volume yang lebih besar.
Atom
Atom adalah satuan dasar materi yang mengemban sifat unsur.
Atom terbentuk dari gabungan partikel subatom: proton, netron dan elektron. Diantara ketiga partikel ini elektron memiliki massa yang paling kecil.
PARTIKEL MASSA (G) MUATAN LISTRIK SIMBOL
Elektron
Proton ,
Neutron
9.1093897 × 10−28 −1 −10 e
1.6726231 × 10−24 +1 11H+ 11p
1.6749286 × 10−24 0 10n
3/59
Unsur
Unsur adalah zat dimana semua atomnya yang memiliki jumlah proton yang sama.
Setiap unsur memiliki identitas unik yang disebut sebagai nomor atom ( ) yang nilainya sama dengan jumlah proton dari inti dari setiap atomnya.
Sebagain besar unsur merupakan campuran atom yang mirip yang disebut sebagai isotop, yaitu atom-atom yang memiliki jumlah proton yang sama tetapi jumlah netronnya berbeda.
Jumlah proton dan netron dalam atom dari isotop tertentu disebut sebagai nomor massa ( ). Oleh karena itu setiap isotop dide nisikan dengan nomor atom dan nomor massa.
Lengkapi tabel berikut:
SIMBOL Z A MUATAN
14 14 14
32
34
15 15 16
Latihan-1 Solusi-1
Σp Σe− Σn
Si … … …
S2 − … … … … −2
Cu2 + … … … … +2
… … … …
5/59
Massa atom relatif
Untuk menetapkan skala massa untuk atom perlu ditetapkan acuan baku dimana massa atom relatif dapat ditentukan.
Telah disepakati bahwa isotop paling melimpah di bumi, yaitu karbon-12, sehingga digunakan sebagai massa acuan.
Massa atom tepat 12 satuan massa atom (sma), sehingga massa satu satuan atom adalah
1 sma = 1.6605 x 10 kg = 1 Dalton (Da) Massa 1 mol = 12.000 g
Mengapa dipilih massa atom karbon-12 sebagai 1 sma?
12
C
12
C (m C)
121 12
-27
12
C
121
Karbon adalah unsur yang melimpah dan dikenal luas
Massa atom hampir semua unsur mendekati bilangan bulat bila pembaginya adalah massa atom karbon. Contoh hidrogen, memiliki massa hampir 1 sma.
121
1. Aluminum memiliki massa 2.24845 kali massa atom . Tentukan massa atom aluminum.
2. Massa atom relatif pada sistem periodik, menggunakan massa sebagai 1 sma. Berdasarkan acuan ini, massa rata-rata karbon dan oksigen di sistem periodik adalah 12.011 sma dan 15.9994 sma. Bila sistem periodik tidak didasarkan pada massa acuan ini, tetapi menggunakan massa 12.000 g dari 1 mol karbon, tentukan massa untuk 1 mol oksigen berdasarkan acuan ini.
Latihan-2 Solusi-2
12
C
× massa C
121 12
12
C
7/59
Massa atom rata-rata dari kelimpahan isotop
Di alam klor adalah campuran dari dua isotop dan . Dalam setiap sampel klor terdapat 75.77% atom dan 24.23% . Massa atom adalah 34.9689 sma dan massa atom adalah 36.9659. Berdasarkan data ini tentukan massa atom rata-rata dari klor.
Solusi:
Latihan:
Boron hanya memiliki dua isotop alam, yaitu dan . Massa isotop = 10.01294 sma dan massa = 11.00931 sma. Diketahui massa atom rata-rata boron adalah 10.811 sma, tentukan kelimpahan kedua isotop boron di alam.
35
Cl
37Cl
35
Cl
37Cl
35Cl
37
Cl
= ( × 34.9689 sma
) +
( × 36.9659 sma
) = 35.453 sma m
Cl75.77% Cl
35100%
24.23% Cl
37100%
10
B
11B
10B
11
B
Tabel Periodik Modern
9/59
Logam, nonlogam dan metaloid
Latihan-3
Klasi kasikan tiga unsur berikut sebagai logam, nonlogam atau mataloid:
silicon (Si), vanadium (V), bromine (Br) A. nonlogam, logam, nonlogam B. logam, metaloid, nonlogam C. nonlogam, logam, metaloid D. metaloid, logam, metaloid E. metaloid, logam, nonlogam
Submit Show Hint Show Answer Clear
11/59
Latihan-4
Strontium (Sr) adalah ..., ruthenium (Ru) adalah ..., dan Yod (I) adalah ...
A. logam alkali, logam transisi, halogen
B. logam transisi, logam alkali tanah, halogen C. logam alkali tanah, logam transisi, halogen D. logam transisi, logam alkali, gas mulia
E. logam alkali, aktinida, halogen
Submit Show Hint Show Answer Clear
Sifat sik logam: Sifat kimia logam:
Logam
Sebagian besar unsur dalam tabel periodik adalah logam
mengkilap atau memantulkan cahaya dapat ditempa menjadi lembaran tipis
sebagian bersifat keras: besi dan krom, tetapi sebagian bersifat lunak: natrium, timbal, tembaga
menghantarkan panas dan listrik (konduktif)
padat pada suhu kamar, kecuali raksa (Hg)
reakti tas logam bervariasi. Contoh: Au dan Pt sangat tidak reaktif, sementara Na dan K sangat reaktif
13/59
Non logam
Terdiri dari 17 unsur pada posisi kanan dari tabel periodik
Sebagian besar ditemukan sebagai senyawa dari pada sebagai unsur
Wujud bervariasi:
Sifat lainnya:
gas monoatom: He, Ne, Ar, Kr, Xe, Rn (gas mulia)
gas diatom:
padatan: , C(gra t,intan) cairan:
, , , , H
2O
2N
2F
2Cl
2, , ,
I
2Se
8S
8P
4Br
2rapuh insulator
Sifat kimia:
Inert: gas mulia Reaktif:
Bereaksi dengan logam membentuk senyawa ion
, ,
F
2O
2H
2Metaloid
Terdiri dari 8 unsur: B, Si, Ge, As, Sb, Te, Po, At yang terletak pada posisi diagonal antara logam dan nonlogam dalam tabel periodik unsur.
Sifat metaloid:
mengkilap seperti logam tetapi rapuh seperti nonlogam
bersifat semikonduktor (Si dan Ge) menghantarkan listrik tetapi tidak sebaik logam
15/59
Molekul
Atom bergabung membentuk zat yang lebih kompleks yang disebut molekul Rumus molekul menentukan komposisi unsur-unsur dalam senyawa.
Rumus molekul terdiri dari simbol unsur dan subskrip yang menyatakan jumlah relatif setiap unsur dalam senyawa
Contoh:
Molekul oksigen, karbon dioksida, Amonia,
Sukrosa,
O
2CO
2NH
3C
12H
22O
11Menggambar molekul
Gambar molekul berfungsi untuk:
Ada 3 cara untuk memvisualkan molekul:
1. Struktur formula 2. Model Ball-and-stick 3. Model Space lling
memperlihatkan posisi atom ketika terikat dalam senyawa memperlihatkan bentuk 3D dari molekul
17/59
Struktur formula
Digunakan untuk memperlihatkan bagaimana atom-atom terikat
Atom diwakili dengan simbol unsur
Ikatan kimia untuk mengikat atom digambarkan dengan garis
Model ball-stick
19/59
Space filling model
menggunakan bola berfusi untuk menunjukkan molekul warna berbeda memperlihatkan unsur yang berbeda
ukuran relatif bole mencerminkan perbedaan ukuran atom
Space filling model
21/59
Apa formula dari senyawa pada gambar?
A.
B.
C.
D.
E.
Submit Show Hint Show Answer Clear
Latihan-5
, ,
C
3H
8CH
3NH
2C
3H
6O
2, Cl,
C
3H
7CH
5CH
6O
2, ,
C
3H
8CH
3NH
2C
3H
6Br
2, ,
C
3H
8CH
3SiH
2C
3H
6O
2, ,
N
3H
8CH
3BH
2C
3H
6O
2Ion dan Senyawa Ion
Ion:
Partikel bemuatan yang terbentuk dari hasil transfer satu atau lebih elektron dari satu atom netral ke atom netral lainnya.
Senyawa ion
Senyawa ion yang terdiri dari ion-ion yang terbentuk dari unsur logam dan nonlogam. Contoh:
NaCl yang merupakan kombinasi dari ion
Na
+ danCl
−.23/59
Satuan rumus
Senyawa ion, seperti NaCl, merupakan kristal garam dimana ion dan ion mengisi kisi kristal secara selang seling membentuk struktur raksasa.
Oleh karena itu, simbol NaCl merupakan satuan rumus, yaitu komposisi paling sederhana untuk merepresentasikan senyawa ion. Jadi NaCl bukan rumus molekul.
Na
+Cl
−Bukti eksperimen terbentuknya ion
Senyawa ion:
Senyawa molekul:
Senyawa ion tidak dapat menghantarkan listrik dalam wujud apapun, karena molekul terbentuk dari partikel-partikel tidak bermuatan.
Hantaran listrik memerlukan gerak partikel bermuatan.
Senyawa ion tidak bisa menghantarkan listrik dalam wujud padatan
Senyawa ion hanya dapat menghantarkan listrik dalam wujud cair atau ketika terlarut dalam air dimana pada keadaan tersebut ion dapat bebas bergerak
25/59
Ion dari beberapa wakil unsur
Kation dari logam transisi
Unsur golongan transisi tidak sereaktif unsur pada golongan 1 dan 2
Unsur ini masih dapat mentransfer elektron ke unsur nonlogam membentuk senyawa ion, tetapi jumlah ion yang ditransfer tidak pasti seperti unsur logam pada golongan 1 dan 2.
Unsur transisi dapat membentuk lebih dari satu ion positif, sehingga dapat membentuk lebih dari satu senyawa ion. Contoh:
Fe(s) + Cl
2(g) ⟶ FeCl
2(s) dan FeCl
3(s)
27/59
Kation dari logam post-transisi
Logam post-transisi: Ga, In, Sn, Tl, Pb, Bi, Uut, Uuq, Uub
Pada sistem periodik logam ini setelah golongan transisi tetapi sebelum metaloid
Ada dua logam yang penting diketahui, yaitu timah (Sn) dan timbal (Pb)
Kedua unsur ini memiliki dia bilangan oksidasi sehingga dapat membentuk dua senyawa dengan unsur nonlogam. Contoh: and
Bismuth (Bi) satu-satunya unsur yang hanya memiliki satu muatan, +3.
SnO SnO
2Daftar ion transisi dan post-transisi
29/59
Senyawa ion poliatom
Tatanama senyawa ion
Kation:
Logam yang hanya membentuk satu kation diberi nama sesuai nama unsurnya. Contoh:
Logam yang dapat membentuk lebih dari satu kation setelah nama logam diberi tanda romawi untuk menyatakan muatannya. Contoh:
= natrium = kalsium
Na
+Ca
2 += kromium(II) = kromum(III)
Cr
2 +Cr
3 +31/59
Tatanama senyawa ion
Anion:
Ion monoatom diberi nama dengan menambahkan akhiran -ida.
Nama anion poliatom
33/59
Latihan tatanama
Beri nama senyawa berikut:
1.
2.
3.
4.
5.
Submit Show Hint Show Answer Clear
O K
2NH
4ClO
3Mg( C
2H
3O
2 2) Cr
2O
3ZnBr
2Latihan tatanama
Tuliskan rumus untuk senyawa berikut 1. Kalsium hidroksida
2. Mangan(II) bromida
3. Amonium fosfat
4. Merkuri(I) nitrida
Submit Show Hint Show Answer Clear
35/59
Latihan tatanama
Nama yang benar untuk adalah A. tembaga sul da
B. tembaga(II) sul da C. tembaga(II) sulfat D. tembaga(I) sul da E. tembaga(I) sul t
Submit Show Hint Show Answer Clear
S
Cu
2Latihan tatanama
Rumus yang tepat untuk amonium sul t adalah A.
B.
C.
D.
E.
Submit Show Hint Show Answer Clear
NH
4SO
3( NH
4 2) SO
3( NH
4 2) SO
4S NH
4S ( NH
4 2)
37/59
Hidrat
Hidrat adalah kristal yang mengandung air, contoh:
Air tidak terikat dengan kuat, sehingga dapat dihilangkan dengan proses dehidrasi menyisakan padatan anhidrat.
⋅ 2 O
CaSO
4H
2Penamaan hidrat
Senyawa ion hidrat adalah senyawa ion ketika dalam bentuk padatan kristal mengikat molekul air dengan proporsi tetap tertentu.
Senyawa ion hidrat ini diberi nama mengikuti tatanama senyawa ion yang diikuti dengan jumlah molekul air yang terikat. Jumlah molekul air dinyatakan dalam: mono-, di-, tri-, tetra-, penta- dst. Contoh:
= kalsium sulfat dihidrat
= kobal(II) klorida heksahidrat = besi(III) yodida trihidrat
CaS .2 O O
4H
2CoC .6 O l
2H
2Fe .3 O I
3H
239/59
Latihan
Nama yang benar untuk A. besi nitrat nonahidrat B. besi(III) nitrat nonahidrat C. Ferium(III) nitrat dekahidrat D. besi(III) nitrit nonahidrat E. besi(III) nitrat heptahidrat
Submit Show Hint Show Answer Clear
Fe(N O
3)
3.9 O H
2Senyawa Molekul
Molekul:
Ikatan kimia:
Rumus molekul:
Pembentukan senyawa molekul:
Partikel netral yang terdiri dari dua atom atau lebih.
Interaksi yang mengikat atom-atom bersama-sama dalam molekul.
Sekelompok atom yang membentuk molekul akan berperilaku seperti partikel tunggal
Menerangkan komposisi dari setiap atom yang membentuk molekul
Senyawa molekul dibentuk dari kombinasi nonlogam
C + O
2⟶ CO
22 H
2+ O
2⟶ 2 H
2O
41/59
Perbedaan senyawa ion dan molekul
Senyawa molekul merupakan unit diskrit. Contoh: satu unit molekul air: terdiri dari 2 atom H yang terikat pada 1 atom O
Pada senyawa ion, setiap ion berlawanan muatan dikemas saling berdekatan sehingga tidak dapat dijelaskan satu ion milik ion yang mana. Contoh pada NaCl. Setiap satu ion Na berikatan dengan 6 ion Cl , begitu pula sebaliknya.
+ -
Senyawa molekul yang mengandung hidrogen
Jumlah hidrogen yang terikat sama dengan jumlah elektron yang diperlukan oleh unsur nonlogam untuk mencapai kon gurasi gas mulia.
43/59
Senyawa hidrokarbon
45/59
Tatanama senyawa biner
Jumlah atom diberi awalan: mono-, di-, tri-, dst. Kecuali untuk unsur pertama yang jumlahnya hanya satu atom awalan mono ditiadakan.
Awalan mono-, di-, tri-, dst. juga tidak digunakan terhadap hidrogen Contoh:
= hidrogen bromida = hidrogen sul da = karbon monoksida
= karbon dioksida
= triselenium dinitrida = dinitrogen tetraoksida
HBr
S
H
2CO
CO
2Se
3N
2N
2O
4Latihan
1. Tuliskan rumus molekul untuk disulfur deka uorida
2. Tuliskan struktur untuk nitrogen triyodida
3. Beri nama
Submit Show Hint Show Answer Clear
P
4O
1047/59
Tutorial
Soal 1
Pernyataan di bawah ini menjelaskan tentang informasi yang benar tentang unsur-unsur gas mulia, kecuali:
A. Dikenal sebagai gas inert
B. He, Ne, Ar, Kr, Xe, Rn, dan Uuo are termasuk unsur-unsur gas mulia C. Unsur lebih berat bereaksi dengan unsur lain
D. Terdapat pada golongan VIIIA (atau golongan 18) E. Mengandung setidaknya satu unsur metaloid
Submit Show Hint Show Answer Clear
49/59
Soal 2
Manakah pernyataan berikut yang tidak termasuk sifat dari logam?
A. Mengkilap
B. Bersifat konduktor
C. Sifat konduktornya melemah ketika dipanaskan D. Dapat ditempa
E. Sebagian logam keras dan sebagian lagi lunak
Submit Show Hint Show Answer Clear
Soal 3
Unsur yang di alam dalam keadaan molekul diatom adalah ....
A. C B. N C. Ga D. Ge E. P
Submit Show Hint Show Answer Clear
51/59
Soal 4
Jumlah atom oksigen dalam satuan rumus adalah ....
A. 2 B. 3 C. 5 D. 6 E. 11
Submit Show Hint Show Answer Clear
Cu(N O
3)
2.5 O H
2Soal 5
Seorang mahasiswa mencoba menyetarakan persamaan reaksi dan memberikan hasil berikut:
Bila diperiksa dengan seksama persamaan reaksi di atas belum setara. Unsur manakah yang belum setara?
A. Cl B. O C. H
D. O dan H E. C
Submit Show Hint Show Answer Clear
8 KClO
3+ C
12H
22O
10⟶ 8 KCl + 12 CO
2+ 11 H
2O
53/59
Soal 6
Rumus manakah yang tepat untuk senyawa ionik?
A.
B.
C.
D.
E.
Submit Show Hint Show Answer Clear
Br Li
2Pb
2I
2KBr
2Rb
2Se
4Al
2S
3Soal 7
Pilih mana diantara rumus senyawa ionik berikut yang tidak tepat penulisannya (atau tidak mungkin ditemukan seperti yang dituliskan).
A. I saja B. II dan III C. III dan IV D. I dan IV E. I, II, dan IV
Submit Show Hint Show Answer Clear
I.
II.
III.
IV.
As ( NH
4 2)
CuO
Mg( C
2H
3O)
2Na
3( HCO
3 2)
55/59
Soal 8
Jumlah proton, neutron, dan elektron dalam ion adalah ....
A. 27 proton, 30 neutron, dan 30 elektron B. 26 proton, 31 neutron, dan 23 elektron C. 29 proton, 28 neutron, dan 26 elektron D. 26 proton, 31 neutron, dan 29 elektron E. 25 proton, 32 neutron, dan 22 elektron
Submit Show Hint Show Answer Clear
57
F e
3+Soal 9
Manakah senyawa yang termasuk kelompok hidrida?
A.
B.
C.
D.
E.
Submit Show Hint Show Answer Clear
· 6 O CoCl
2H
2HC
2H
3O
2NaOH
CaH
2C
6H
12O
657/59
Soal 10
Nama yang tepat untuk senyawa adalah ....
A. divanadium pentoksida B. vanadat oksida
C. vanadium(V) oksida
D. vanadium(V) pentoksida E. vanadous oksida
Submit Show Hint Show Answer Clear
V
2O
5Soal 11
Pilih senyawa yang penamaannya tidak sesuai dengan rumusnya
A. II saja B. II dan IV C. III dan IV D. I dan IV E. I, II, dan IV
Submit Show Hint Show Answer Clear
I. Natrium klorat
II. Amonium(I) karbonat
III. Cadmium dihidrogen fosfat IV. Kalium-mangan(VII) oksida
NaClO
3( NH
4 2) CO
3Cd( H
2PO
4 2) KMnO
459/59