PENETAPAN KADAR KALSIUM DAN MAGNESIUM DALAM BIJI NANGKA MUDA DAN BIJI NANGKA TUA (Artocarpus integra Merr.) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
OLEH:
AYU DEWIANI YUHARNANDA PUTRI NIM 111524011
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2013
PENETAPAN KADAR KALSIUM DAN MAGNESIUM DALAM BIJI NANGKA MUDA DAN BIJI NANGKA TUA (Artocarpus integra Merr.) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
AYU DEWIANI YUHARNANDA PUTRI NIM 111524011
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2013
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALSIUM DAN MAGNESIUM DALAM BIJI NANGKA MUDA DAN BIJI NANGKA TUA (Artocarpus integra Merr.) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM OLEH:
AYU DEWIANI YUHARNANDA PUTRI NIM 111524011
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal: 27 Agustus 2013
Pembimbing I, Panitia Penguji,
Drs. Chairul Azhar D., M.Sc., Apt. Prof. Dr. rer. nat. E. De Lux Putra, S.U., Apt.
NIP 194907061980021001 NIP 195306191983031001
Pembimbing II, Drs. Chairul Azhar D., M.Sc., Apt.
NIP 194907061980021001
Drs. Fathur Rahman Harun, M.Si., Apt. Dra. Siti Nurbaya, M.Si., Apt.
NIP 195201041980031002 NIP 195008261974122001
Dra. Sudarmi, M.Si., Apt.
NIP 195409101983032001
Medan, Oktober 2013 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
Prof. Dr. Sumadio Hadisahputra, Apt.
NIP 195311281983031002
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas segala limpahan berkat, rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini serta shalawat beriring salam untuk Rasulullah Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Penetapan Kadar Kalsium dan Magnesium dalam Biji Nangka Muda dan Biji Nangka Tua (Artocarpus integra Merr.) Secara Spektrofotometri Serapan Atom.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr.
Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara Medan, yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Bapak Drs. Chairul Azhar Dalimunthe, M.Sc., Apt., dan Bapak Drs. Fathur Rahman Harun, M.Si., Apt., yang telah membimbing dan memberikan petunjuk serta saran-saran selama penelitian hingga selesainya skripsi ini. Bapak Prof. Dr. rer. nat. Effendy de Lux Putra, S.U., Apt., Ibu Dra. Siti Nurbaya, M.Si., Apt., dan Ibu Dra. Sudarmi, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik, saran dan arahan
kepada penulis dalam menyelesaikan skripsi ini. Bapak dan Ibu staff pengajar Fakultas Farmasi USU Medan yang telah mendidik selama perkuliahan dan Ibu Dra. Djendakita Purba, M.Si., Apt., selaku penasehat akademik yang selalu memberikan bimbingan kepada penulis selama perkuliahan. Ibu Dra. Masfria, M.Si., Apt., selaku kepala Laboratorium Kimia Farmasi Kualitatif USU dan Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., selaku kepala Laboratorium Penelitian Fakultas Farmasi USU yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada Ayahanda Drs. Harun Al Rasyid dan Ibunda Juliani yang telah memberikan cinta kasih yang tidak ternilai, doa yang tulus, serta pengorbanan baik materi maupun non materi. Sahabat terbaikku kak Ajeng, bang Surya, Ucok, Rudi, Kiteng, kak Rahman, serta seluruh teman-teman ekstensi 2011, terimah kasih untuk dorongan, semangat dan kebersamaannya selama ini, serta seluruh pihak yang telah ikut membantu penulis.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, 4 Agustus 2013 Penulis,
Ayu Dewiani Y. Putri
PENETAPAN KADAR KALSIUM DAN MAGNESIUM DALAM BIJI NANGKA MUDA DAN BIJI NANGKA TUA (Artocarpus integra Merr.)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM ABSTRAK
Pohon nangka (Artocarpus integra), sehari-hari disebut nangka adalah tanaman yang telah dikenal hampir seluruh masyarakat Indonesia. Tanaman nangka termasuk tanaman serbaguna karena buah yang muda dapat disayur (gudeg), sedangkan buah yang tua enak dimakan segar. Bijinya dapat dimakan setelah direbus, daunnya dapat digunakan untuk pakan ternak. Unsur gizi yang terkandung dalam biji nangka muda berbeda dengan yang terkandung dalam biji nangka tua fisiologis (masak di pohon). Buah maupun biji nangka merupakan sumber kalori, protein, lemak, karbohidrat, kalsium, fosfor, magnesium, kalium, besi, vitamin A, vitamin B, dan vitamin C. Tujuan penelitian ini adalah untuk mengetahui perbedaan kandungan kalsium dan magnesium pada biji nangka tua dan biji nangka muda.
Penentuan kadar kalsium dan magnesium dilakukan secara spektrofotometri serapan atom dengan menggunakan nyala udara – asetilen pada panjang gelombang 422,7 nm untuk kalsium dan 285,2 nm untuk magnesium. Sebelum dilakukan penentuan kadar, terlebih dahulu dilakukan analisis kualitatif dengan menggunakan pereaksi asam sulfat encer dan amonium oksalat untuk kalsium, sedangkan untuk magnesium menggunakan pereaksi kuning titan dan natrium hidroksida.
Hasil penelitian menunjukkan kandungan kalsium dan magnesium dalam biji nangka tua masing-masing adalah (17,7813 ± 1,2756) mg/100 g dan (62,9777 ± 4,2948) mg/100 g, sedangkan kandungan kalsium dan magnesium dalam biji nangka muda masing-masing adalah (23,7865 ± 0,6937) mg/100 g dan (29,0621 ± 0,3830) mg/100 g. Dari hasil uji statistik, yaitu uji beda rata- rata yang dilanjutkan dengan uji t, diperoleh kandungan kalsium pada biji nangka muda lebih tinggi dari biji nangka tua dan kandungan magnesium pada biji nangka tua lebih tinggi dari biji nangka muda.
Kata kunci: biji nangka, kalsium, magnesium, spektrofotometri serapan atom
DETERMINATION OF CALCIUM AND MAGNESIUM CONTENT IN YOUNG JACKFRUIT SEEDS AND OLD JACKFRUIT SEEDS
(Artocarpus integra Merr.) BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Jackfruit tree (Artocarpus integra), a known as jackfruit is a plant that has been recognized by almost all Indonesian people. This plant belong multipurpose plant, because the young fruit can be a side dish as a cury, while the old fruit is fresh and delicious eaten. The seeds can be eaten after boiling, the leaves can be used for animal feed. Nutrients contained in young jackfruit seeds and old jackfruit seeds is different. Fruit and jackfruit seeds are a source of calories, protein, fat, carbohydrates, calcium, phosphorus, magnesium, potassium, iron, vitamin A, vitamin B, and vitamin C. The purpose of this study was to determine differences in the content of calcium and magnesium on an old jackfruit seeds and young jackfruit seeds.
Determination of calcium and magnesium is done by atomic absorption spectrophotometry using flame air - acetylene at a wavelength of 422.7 nm for calcium and 285.2 nm for magnesium. Before the determination of levels, first performed a qualitative analysis using dilute sulfuric acid reagent and ammonium oxalate for calcium, whereas for magnesium using titan yellow reagent and sodium hydroxide.
The results showed the content of calcium and magnesium in the old jackfruit seeds, respectively (17.7813 ± 1.2756) mg/100 g and (62.9777 ± 4.2948) mg/100 g, while calcium and magnesium in young jackfruit seeds respectively (23.7865 ± 0.6937) mg/100 g and (29.0621 ± 0.3830) mg/100 g.
From the results of statistical tests, that is the average difference test followed by a test t, obtained calcium content in young jackfruit seeds is higher than the old jackfruit seeds and magnesium content of the old jackfruit seeds is higher than young jackfruit seeds.
Keywords: jackfruit seed, calcium, magnesium, atomic absorption spectrophotometry
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Nangka ... 5
2.1.1 Taksonomi Tumbuhan ... 5
2.1.2 Deskripsi Tumbuhan ... 5
2.1.3 Manfaat Tumbuhan Nangka ... 6
2.2 Biji Nangka ... 6
2.2.1 Bagian-Bagian Biji Nangka ... 6
2.2.2 Manfaat Biji Nangka ... 7
2.3 Kandungan Gizi Nangka ... 7
2.4 Mineral ... 8
2.4.1 Kalsium ... 9
2.4.2 Magnesium ... 10
2.5 Spektrofotometri Serapan Atom ... 12
2.5.1 Prinsip Dasar Spektrofotometri Serapan Atom ... 12
2.5.2 Instrumentasi Spektrofotometri Serapan Atom ... 13
2.6 Validasi Metode Analisis ... 15
BAB III METODE PENELITIAN ... 20
3.1 Tempat dan Waktu Penelitian ... 20
3.2 Bahan-bahan ... 20
3.2.1 Sampel ... 20
3.2.2 Pereaksi ... 20
3.3 Alat-alat ... 21
3.4 Identifikasi sampel ... 21
3.5 Pembuatan Pereaksi ... 21
3.5.1 Larutan HNO3 (1:1) v/v ... 21
3.5.2 Larutan H2SO4 10% v/v ... 21
3.5.3 Larutan Amonium Oksalat 3,5% b/v ... 21
3.5.4 Larutan Kuning Titan 0,1% b/v ... 22
3.5.5 Larutan Natrium Hidroksida 2 N ... 22
3.6 Prosedur Penelitian ... 22
3.6.1 Pengambilan Sampel ... 22
3.6.2 Penyiapan Bahan ... 22
3.6.3 Proses Destruksi Kering ... 22
3.6.4 Pembuatan Larutan Sampel ... 23
3.6.5 Analisis Kualitatif ... 23
3.6.5.1 Analisis Kualitatif Kalsium ... 23
3.6.5.1.1 Uji Mikroskop Kalsium Sulfat .... 23
3.6.5.1.2 Reaksi dengan Amonium Oksalat 3,5% b/v ... 24
3.6.5.2 Analisis Kualitatif Magnesium ... 24
3.6.5.2.1 Reaksi dengan Larutan Kuning Titan 0,1% b/v ... 24
3.6.6 Analisis Kuantitatif ... 24
3.6.6.1 Analisis Kuantitatif Kalsium ... 24
3.6.6.1.1 Pembuatan Larutan Induk Baku Kalsium ... 24
3.6.6.1.2 Penentuan Kurva Kalibrasi Kalsium ... 25
3.6.6.1.3 Penentuan Kadar Kalsium dalam sampel ... 25
3.6.6.1.4 Perhitungan Kadar Kalsium dalam Sampel ... 25
3.6.6.2 Analisis Kuantitatif Magnesium ... 26
3.6.6.2.1 Pembuatan Larutan Induk Baku Magnesium ... 26
3.6.6.2.2 Penentuan Kurva Kalibrasi
Magnesium ... 26
3.6.6.2.3 Penentuan Kadar Magnesium dalam Sampel ... 26
3.6.6.2.4 Perhitungan Kadar Magnesium dalam Sampel ... 27
3.6.7 Penentuan Batas Deteksi dan Batas Kuantitasi ... 27
3.6.8 Uji Perolehan Kembali (Recovery) ... 28
3.6.9 Simpangan Baku Relatif ... 29
3.6.10 Analisis data Secara Statistik ... 29
3.6.11 Pengujian Beda Nilai Rata-rata ... 30
BAB IV HASIL DAN PEMBAHASAN ... 32
4.1 Analisis Kualitatif ... 32
4.2 Analisis Kuantitatif ... 33
4.2.1 Kurva Kalibrasi Kalsium dan Magnesium ... 33
4.2.2 Penetapan Kadar Kalsium dan Magnesium dalam Biji Nangka ... 34
4.2.3 Pengujian Beda Nilai Rata-rata Kadar Kalsium dan Magnesium pada Biji Nangka Tua dan Biji Nangka Muda ... 36
4.2.4 Batas Deteksi dan Batas Kuantitasi ... 37
4.2.5 Uji Perolehan Kembali (Recovery) ... 37
4.2.6 Simpangan Baku Relatif ... 38
BAB V KESIMPULAN DAN SARAN ... 39
5.1 Kesimpulan ... 39
5.2 Saran ... 39
DAFTAR PUSTAKA ... 40 LAMPIRAN ... 42
DAFTAR TABEL
Halaman Tabel 2.1 Kandungan Unsur Gizi dalam Buah dan Biji Nangka ... 8 Tabel 4.1 Hasil Analisis Kualitatif ... 32 Tabel 4.2 Hasil Analisis Kuantitatif Kalsium dan Magnesium pada
Sampel ... 35 Tabel 4.3 Hasil Uji Beda Nilai Rata-rata Kadar Kalsium dan
Magnesium pada Biji Nangka Tua dan Biji Nangka
Muda ... 36 Tabel 4.4 Batas Deteksi dan Batas Kuantitasi Kalsium dan
Magnesium ... 37 Tabel 4.5 Persen uji Perolehan Kembali (recovery) Kalsium dan
Magnesium dalam Sampel ... 37 Tabel 4.6 Nilai Simpangan Baku dan Simpangan Baku Relatif
Kalsium dan Magnesium ... 38
DAFTAR GAMBAR
Halaman Gambar 2.1 Sistem Peralatan Spektrofotometri Serapan Atom ... 13 Gambar 4.1 Kurva Kalibrasi Kalsium ... 33 Gambar 4.2 Kurva Kalibrasi Magnesium ... 33
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil Identifikasi Sampel ... 42
Lampiran 2. Gambar Sampel Biji Nangka ... 43
Lampiran 3. Gambar Alat-alat yang Digunakan ... 44
Lampiran 4. Gambar Hasil Pengarangan dan Hasil Pengabuan Sampel ... 46
Lampiran 5. Gambar Hasil Analisis Kualitatif ... 47
Lampiran 6. Bagan Alir Proses Dekstruksi Kering ... 49
Lampiran 7. Bagan Alir Pembutan Larutan Sampel ... 50
Lampiran 8. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ... 51
Lampiran 9. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ... 53
Lampiran 10. Hasil Analisis Kadar Kalsium dan Magnesium dalam Sampel ... 55
Lampiran 11. Contoh Perhitungan Kadar Kalsium dan Magnesiumdalam Sampel ... 57
Lampiran 12. Perhitungan Statistik Kadar Kalsium dalam Sampel ... 58
Lampiran 13. Perhitungan Statistik Kadar Magnesium dalam Sampel ... 62
Lampiran 14. Pengujian Beda Nilai Rata-Rata Kalsium dalam Biji Nangka ... 65
Lampiran 15. Pengujian Beda Nilai Rata-Rata Magnesium dalam
Biji Nangka ... 67 Lampiran 16. Validasi Metode Analisis ... 69 Lampiran 17. Perhitungan Batas Deteksi dan Batas Kuantitasi ... 71 Lampiran 18. Contoh Perhitungan Uji Perolehan Kembali
Kalsium dan Magnesium dalam Biji Nangka Tua ... 73 Lampiran 19. Perhitungan Simpangan Baku Relatif (RSD)
Kalsium dan Magnesium dalam Sampel ... 75 Lampiran 20. Tabel Distribusi t ... 77 Lampiran 21. Tabel Distribusi F ... 78
BAB I PENDAHULUAN
1.1 Latar Belakang
Pohon nangka (Artocarpus integra), sehari-hari disebut nangka adalah tanaman yang telah dikenal hampir seluruh masyarakat Indonesia. Tanaman ini tumbuh baik di daerah dataran rendah sampai daerah pegunungan dengan ketinggian 1.000 m di atas permukaan laut (Soetanto, 1998).
Tanaman nangka termasuk tanaman serbaguna, karena buah yang muda dapat disayur, sedangkan buah yang tua enak dimakan segar. Bijinya dapat dimakan setelah direbus, daunnya dapat digunakan untuk pakan ternak. Batangnya yang telah tua dapat digunakan untuk bahan bangunan (Sunarjono, 2004).
Kebanyakan masyarakat di Indonesia memanfaatkan buah nangka tanpa memanfaatkan bijinya, karena tidak mengetahui ternyata biji nangka merupakan sumber kalori, protein, lemak, karbohidrat, kalsium, fosfor, magnesium, besi, vitamin B, dan vitamin C. Biji nangka muda dapat dikonsumsi bersama buah nangka muda yang umumnya disayur, sedangkan biji nangka tua dapat diolah menjadi berbagai macam produk seperti tepung biji nangka, dodol biji nangka, kecap biji nangka, dan susu biji nangka (Suprapti, 2004).
Mineral adalah bagian tubuh yang memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara keseluruhan. Kalsium, fosfor, dan magnesium merupakan bagian dari tulang, besi dari hemoglobin dalam sel darah merah, dan iodium dari hormon tiroksin. Mineral digolongkan ke dalam mineral makro dan
mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari (Almatsier, 2004).
Unsur gizi yang terkandung dalam biji nangka muda berbeda dengan yang terkandung dalam biji nangka tua. Biji nangka mengandung 165 kalori, protein 4,2 g, lemak 0,1 g, karbohidrat 36,7 g, kalsium 33 mg, fosfor 200 mg, magnesium 150,7 mg – 210 mg, besi 1 mg, vitamin B 0,2 mg, dan vitamin C 10 mg masing-masing tiap 100 g bahan (Abedin, 2012; Suprapti, 2004). Di dalam literatur tersebut, tidak dijelaskan kandungan gizi yang terdapat di dalam biji nangka muda dan biji nangka tua.
Di Yogyakarta, biji nangka diolah menjadi susu biji nangka. Susu biji nangka mengandung fosfor dan karbohidrat yang lebih tinggi daripada susu kedelai, serta kandungan lemak yang lebih rendah. Susu dan hasil olahannya seperti keju adalah sumber utama kalsium yang dapat meningkatkan kekuatan tulang. Susu diyakini dapat mencukupi kebutuhan kalsium harian, hal itulah yang mendasari mengapa susu dianggap sebagai strategi terbaik untuk pencegahan osteoporosis. Selain kalsium, terdapat zat gizi lain seperti vitamin D, magnesium, fosfor dan fitonutrien yang tidak kalah penting dalam pencegahan dan pengendalian osteoporosis (Almatsier, 2004; Nuraini, 2011).
Kalsium merupakan mineral yang paling banyak terdapat didalam tubuh. Mineral ini memegang peranan penting dalam mengatur fungsi sel, seperti untuk transmisi saraf, kontraksi otot, penggumpalan darah dan menjaga permeabilitas membran sel, serta mengatur pekerjaan hormon-hormon dan faktor pertumbuhan. Magnesium merupakan mineral nomor dua paling banyak
setelah natrium di dalam cairan intraselular. Sekitar 60% dari 20 mg – 28 mg magnesium di dalam tubuh terdapat di dalam tulang dan gigi, 26% di dalam otot dan selebihnya di dalam jaringan lunak serta cairan tubuh. Sumber utama magnesium adalah sayuran hijau, serelia tumbuk, biji-bijian dan kacang- kacangan (Almatsier, 2004).
Analisis kuantitatif kalsium dan magnesium dapat dilakukan secara, gravimetri, kompleksometri dan spektrofotometri serapan atom. Metode yang dipilih dalam penelitian ini adalah spektrofotometri serapan atom yang didasarkan pada ketelitian alat, kecepatan analisis, tidak memerlukan pemisahan pendahuluan, dan dapat menetukan kadar suatu unsur dengan konsentrasi yang rendah (Khopkar, 1990).
Berdasarkan uraian di atas, penulis tertarik untuk meneliti kandungan kalsium dan magnesium yang terdapat dalam biji nangka muda dan biji nangka tua (Artocarpus integra).
1.2 Perumusan Masalah
1. Berapakah kadar kalsium dan magnesium pada biji nangka muda dan biji nangka tua.
2. Apakah terdapat perbedaan kadar kalsium dan magnesium pada biji nangka muda dan biji nangka tua.
1.3 Hipotesis
1. Biji nangka muda dan biji nangka tua mengandung kalsium dan magnesium dalam jumlah tertentu.
2. Terdapat perbedaan kadar kalsium dan magnesium pada biji nangka muda dan biji nangka tua.
1.4 Tujuan Penelitian
1. Untuk mengetahui kadar kalsium dan magnesium pada biji nangka muda dan biji nangka tua.
2. Untuk mengetahui perbedaan kadar kalsium dan magnesium pada biji nangka muda dan biji nangka tua.
1.5 Manfaat Penelitian
Dari hasil penelitian ini, dapat diinformasikan kepada masyarakat tentang kandungan kalsium dan magnesium yang terdapat di dalam biji nangka tua dan biji nangka muda, sehingga masyarakat dapat menjadikan biji nangka sebagai sumber kalsium dan magnesium alternatif yang sangat ekonomis.
BAB II
TINJAUAN PUSTAKA
2.1 Nangka
2.1.1 Taksonomi Tumbuhan
Menurut Meda (2013), taksonomi nangka adalah sebagai berikut:
Kerajaan : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Ordo : Urticales Famili : Moraceae Genus : Artocarpus
Spesies : Artocarpus integra Merr.
2.1.2 Deskripsi Tumbuhan
Pohon nangka (Artocarpus integra) telah dikenal hampir seluruh masyarakat Indonesia. Tanaman ini tumbuh baik di daerah dataran rendah sampai daerah pegunungan dengan ketinggian 1000 m di atas permukaan laut.
Tumbuhan ini dapat diperbanyak dengan bijinya, okulasi, dan cangkok. Jarak tanam yang baik untuk budi daya tanaman nangka adalah 12 m x 12 m (Sunarjono, 2004).
Nangka merupakan tanaman hutan yang pohonnya dapat mencapai tinggi 25 m. Kayunya keras dan bergetah, bila telah tua berwarna kuning hingga kemerahan. Daunnya bergetah, lonjong, lebar, tebal, dan agak kaku.
Permukaan daun berbulu halus hingga kasar. Cabangnya sedikit, pertumbuhannya cenderung keatas (Soetanto, 1998).
Buah nangka relatif besar dan berbiji banyak. Kulitnya berduri lunak dan bewarna hijau hingga kuning kemerahan. Setiap biji dibalut oleh daging buah yang tipis hingga tebal. Setelah matang, daging buah bewarna kuning merah, lunak, manis, dan aromanya spesifik (Soetanto, 1998).
2.1.3 Manfaat Tumbuhan
Buah nangka muda atau biasa disebut gori sering dimanfaatkan sebagai bahan sayuran. Sedangkan buah nangka yang sudah masak atau buah nangka tua dapat langsung dikonsumsi sebagai buah segar atau untuk campuran minuman. Buah nangka tua juga dapat dijadikan makanan olahan, misalnya sirup nangka, keripik nangka, manisan nangka, dan sebagainya. Batangnya dapat dipakai untuk bahan bangunan atau bahan perabot rumah tangga (Sunarjono, 2004).
2.2 Biji Nangka
2.2.1 Bagian-Bagian Biji Nangka
Pada umumnya, biji nangka terdiri dari kulit biji (spermodermis) dan inti biji atau isi biji (nukleus seminis). Biji nangka mempunyai tiga lapisan kulit, yaitu kulit luar (sarcotesta), kulit tengah (sclerotesta), dan kulit dalam (endotesta). Kulit luar biasanya tebal berdaging dan kulit tengah merupakan suatu lapisan yang kuat dan keras, sedangkan kulit dalam biasanya tipis seperti selaput, seringkali merekat erat pada inti biji. Inti biji merupakan semua bagian
biji yang terdapat di dalam kulit biji, oleh sebab itu, inti biji juga dapat dinamakan sebagai isi biji (Tjitrosoepomo, 2001).
2.2.2 Manfaat Biji Nangka
Kegunaan dari biji nangka adalah untuk sebagai sumber karbohidrat (biji nangka yang dikukus dan dimakan dapat menjadi sumber karbohidrat tambahan), dan sebagai bahan pembuatan alkohol. Biji buah nangka tua dapat dikonsumsi setelah direbus, dibakar, digoreng, atau diolah menjadi dodol.
Selain itu, biji nangka dapat dibuat menjadi tepung biji nangka yang digunakan sebagai bahan baku industri makanan dengan kandungan gizi yang tinggi, kecap biji nangka, dan susu biji nangka. Susu biji nangka mengandung fosfor dan karbohidrat yang lebih tinggi daripada susu kedelai, serta kandungan lemak yang lebih rendah (Nuraini, 2011).
2.3 Kandungan Gizi Nangka
Menurut Abedin, et al., (2012), biji nangka mengandung kalium sebesar 1300 mg/100 g – 1423 mg/100 g bahan, dan magnesium sebesar 150 mg/100 g – 210 mg/100 g bahan. Selain itu, biji nangka juga mengandung mineral mikro lain seperti sulfur sebesar 30 mg/100 g - 81 mg/100 g, tembaga sebesar 1,467 mg/100 g – 4,133 mg/100 g, dan seng sebesar 1,50 mg/100 g – 3,1 mg/100 g bahan.
Unsur gizi yang terkandung dalam buah nangka muda berbeda dengan yang terkandung dalam buah nangka tua, demikian pula dengan bijinya. Biji nangka muda mempunyai kandungan gizi yang berbeda dengan kandungan
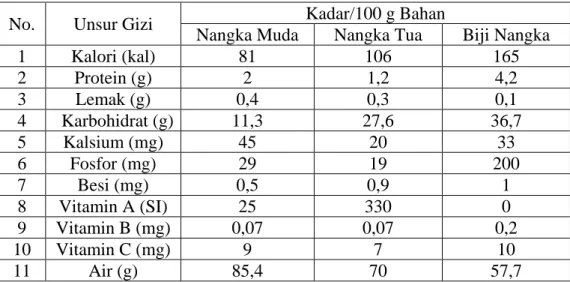
gizi yang terdapat pada biji nangka tua. Adapun kandungan gizi yang terdapat dalam buah dan biji nangka dapat dilihat pada Tabel 2.1 (Suprapti, 2004).
Tabel 2.1 Kandungan Unsur Gizi dalam Buah dan Biji Nangka
No. Unsur Gizi Kadar/100 g Bahan
Nangka Muda Nangka Tua Biji Nangka
1 Kalori (kal) 81 106 165
2 Protein (g) 2 1,2 4,2
3 Lemak (g) 0,4 0,3 0,1
4 Karbohidrat (g) 11,3 27,6 36,7
5 Kalsium (mg) 45 20 33
6 Fosfor (mg) 29 19 200
7 Besi (mg) 0,5 0,9 1
8 Vitamin A (SI) 25 330 0
9 Vitamin B (mg) 0,07 0,07 0,2
10 Vitamin C (mg) 9 7 10
11 Air (g) 85,4 70 57,7
2.4 Mineral
Mineral adalah bagian dari tubuh yang memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan. Kalsium, fosfor, dan magnesium adalah bagian dari tulang, besi dari hemoglobin dalam sel darah merah, dan iodium dari hormon tiroksin. Di samping itu, mineral berperan dalam berbagai tahap metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim (Almatsier, 2004).
Mineral digolongkan kedalam mineral makro dan mineral mikro.
Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari. Jumlah mineral mikro dalam tubuh kurang dari 15 mg. Yang termasuk mineral makro adalah natrium, klorida, kalium, kalsium, fosfor, magnesium,
dan sulfur. Adapun yang termasuk mineral mikro adalah besi, seng, mangan, dan tembaga (Almatsier,2004).
Sumber mineral yang paling baik adalah makanan hewani, kecuali magnesium yang lebih banyak terdapat di dalam makanan nabati. Hewan memperoleh mineral dari tumbuh-tumbuhan dan menumpuk didalam jaringan tubuhnya (Almatsier, 2004).
2.4.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaitu 1,5%-2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Dari jumlah ini, sebanyak 99% berada di dalam jaringan keras, yaitu tulang dan gigi, selebihnya tersebar luas didalam tubuh. Didalam cairan ekstraselular dan intraselular, kalsium memegang peranan penting dalam mengatur fungsi sel, seperti untuk transmisi saraf, kontraksi otot, penggumpalan darah, dan menjaga permeabilitas membran sel. Mineral ini juga mengatur pekerjaan hormon-hormon dan faktor pertumbuhan (Almatsier, 2004).
Angka kecukupan rata-rata sehari untuk kalsium bagi orang Indonesia yang ditetapkan adalah 300 mg – 400 mg pada bayi, 500 mg pada anak-anak, 600 mg – 700 mg pada remaja, 500 mg – 800 mg pada orang dewasa, serta lebih besar 400 mg pada ibu hamil dan menyusui. Kekurangan kalsium pada masa pertumbuhan dapat menyebabkan gangguan pertumbuhan seperti tulang kurang kuat, mudah bengkok, dan rapuh. Selain itu, kekurangan kalsium juga
dapat menyebabkan mineralisasi matriks tulang terganggu serta dapat menyebabkan kejang atau tetani (Almatsier, 2004).
Sumber kalsium utama adalah susu dan hasil olahan susu seperti keju.
Ikan yang dimakan dengan tulang, termasuk ikan kering merupakan sumber kalsium yang baik. Serealia, kacang-kacangan dan hasil kacang-kacangan, tahu, tempe, serta sayuran hijau merupakan sumber kalsium yang baik (Almatsier, 2004).
2.4.2 Magnesium
Magnesium merupakan mineral nomor dua paling banyak setelah natrium di dalam cairan intraselular. Mineral ini di alam merupakan bagian dari klorofil daun. Peranan magnesium dalam tumbuh-tumbuhan sama dengan peranan zat besi dalam ikatan hemoglobin di dalam darah manusia, yaitu untuk pernapasan. Selain itu, magnesium juga terlibat dalam berbagai proses metabolisme (Almatsier, 2004).
Sekitar 60% dari 20 mg – 28 mg magnesium didalam tubuh terdapat didalam tulang dan gigi, 26% di dalam otot, dan selebihnya didalam jaringan lunak lainnya serta cairan tubuh. Magnesium didalam tulang merupakan cadangan yang siap dikeluarkan apabila bagian lain dari tubuh membutuhkan.
Kecukupan magnesium rata-rata sehari untuk Indonesia ditetapkan sekitar 4,5 mg/kg berat badan. Ini berarti kecukupan magnesium untuk orang dewasa laki- laki adalah 280 mg/hari dan untuk wanita dewasa adalah 250 mg/hari (Almatsier, 2004).
Sumber magnesium utama adalah sayuran hijau, serelia tumbuk, biji- bijian dan kacang-kacangan. Daging, susu dan hasil olahannya serta cokelat juga merupakan sumber magnesium yang baik. Kekurangan magnesium dapat terjadi pada kekurangan protein dan energi serta sebagai komplikasi penyakit- penyakit yang menyebabkan gangguan absorpsi dan atau penurunan fungsi ginjal, terlalu lama mendapat makanan tidak melalui mulut, serta penggunaan diuretik. Kekurangan magnesium berat dapat menyebabkan kurang nafsu makan, gangguan dalam pertumbuhan, mudah tersinggung, gugup, kejang tetanus, gangguan sistem saraf pusat, halusinasi, koma, dan gagal jantung (Almatsier, 2004).
Magnesium bertindak di dalam semua sel jaringan lunak sebagai katalisator dalam reaksi-reaksi biologik termasuk reaksi-reaksi yang berkaitan dengan metabolisme energi, karbohidrat, lipid, protein, dan asam nukleat.
Didalam cairan sel ekstraselular, magnesium berperan dalam transmisi saraf, kontraksi otot, dan pembekuan darah. Dalam hal ini, peranan magnesium berlawanan dengan kalsium dimana kalsium merangsang kontraksi otot sedangkan magnesium mengendorkan otot. Kalsium merangsang penggumpalan darah, sedangkan magnesium mencegah. Kalsium menyebabkan ketegangan saraf sedangkan magnesium melemaskan saraf.
Selain itu, magnesium mencegah kerusakan gigi dengan cara menahan kalsium didalam email gigi (Almatsier, 2004).
2.5 Spektrofotometri Serapan Atom
2.5.1 Prinsip Dasar Spektrofotometri Serapan Atom
Spektroskopi serapan atom digunakan untuk analisis kuantitatif unsur- unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace).
Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok untuk analisis logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan interferensinya sedikit (Gandjar dan Rohman, 2009).
Spektroskopi serapan atom didasarkan pada absorbsi cahaya oleh atom.
Atom-atom akan menyerap cahaya pada panjang gelombang tertentu. Cahaya pada panjang gelombang ini mempunyai cukup energi untuk mengubah tingkat elektronik suatu atom. Dengan menyerap suatu energi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat dinaikkan tingkat energinya ke tingkat eksitasi. Unsur Ca dengan nomor atom 20 mempunyai konfigurasi elektron 1s22s22p63s23p64s2, tingkat dasar untuk elektron valensi 4s, artinya tidak memiliki kelebihan energi. Elektron ini dapat tereksitasi ke tingkat 4p dengan menyerap energi pada panjang gelombang 422,7 nm. Begitu juga dengan unsur Mg dengan nomor atom 12 mempunyai konfigurasi elektron 1s22s22p63s2, tingkat dasar untuk elektron valensi 3s, artinya tidak memiliki kelebihan energi. Elektron ini dapat tereksitasi ke tingkat 3p dengan menyerap energi pada panjang gelombang 285,2 nm (Khopkar, 1990).
Interaksi materi dengan berbagai energi seperti energi panas, energi radiasi, energi kimia, dan energi listrik selalu memberikan sifat-sifat yang spesifik untuk setiap unsur. Besarnya perubahan yang terjadi biasanya sebanding dengan jumlah unsur atau persenyawaan yang terdapat didalamnya.
Proses interaksi ini mendasari analisis spektrofotometri atom yang dapat berupa emisi dan absorpsi (Gandjar dan Rohman, 2009).
2.5.2 Instrumentasi Spektrofotometri Serapan Atom
Sistem peralatan spektrofotometer serapan atom dapat dilihat pada Gambar 2.1 (Gandjar dan Rohman, 2009).
Gambar 2.1 Sistem Peralatan Spektrofotometri Serapan Atom a. Sumber sinar
Sumber sinar yang umum dipakai adalah lampu katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari unsur atau dilapisi unsur yang sama dengan unsur yang akan dianalisis. Tabung logam ini diisi dengan gas mulia dengan tekanan rendah yang jika diberikan tegangan pada arus tertentu, katoda akan memancarkan elektron-elektron yang bergerak menuju anoda dengan kecepatan dan energi
yang tinggi. Elektron dengan energi tinggi ini akan bertabrakan dengan gas mulia sehingga gas mulia kehilangan elektron dan menjadi ion bermuatan positif. Ion gas mulia bermuatan positif akan bergerak menuju katoda dengan kecepatan dan energi yang tinggi sehingga menabrak unsur-unsur yang terdapat pada katoda. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar permukaan katoda dan mengalami eksitasi ke tingkat energi elektron yang lebih tinggi.
b. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala (flame) dan tanpa nyala (flameless).
Teknik atomisasi dengan nyala bergantung pada suhu yang dapat dicapai oleh gas-gas yang digunakan. Untuk gas batubara-udara suhunya kira- kira sebesar 1800ºC, gas alam-udara 1700ºC, gas asetilen-udara 2200ºC, dan gas asetilen-dinitrogen oksida sebesar 3000ºC. Sumber nyala yang paling banyak digunakan adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi.
Teknik atomisasi tanpa nyala dapat dilakukan dengan meletakkan sejumlah sampel didalam tungku dari grafit kemudian dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada tabung grafit. Akibat pemanasan ini, zat yang akan dianalisis akan berubah menjadi atom-atom
netral dan dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadi proses penyerapan energi.
c. Monokromator
Pada spektrofotometri serapan atom, monokromator berfungsi untuk memisahkan dan memilih panjang gelombang yang digunakan untuk analisis.
Di dalam monokromator, terdapat suatu alat yang digunakan untuk memisahkan panjang gelombang yang disebut dengan chopper.
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman. Biasanya, detektor yang digunakan adalah tabung penggandaan foton (photomultiplier tube).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai sistem pencatatan hasil. Pencatatan hasil dilakukan dengan suatu alat yang telah terkalibrasi untuk pembacaan suatu transmisi atau absorbsi. Hasil pembacaan dapat berupa angka atau kurva dari suatu alat perekam yang menggambarkan absorbansi atau intensitas emisi.
2.6 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya.
Tindakan ini dilakukan untuk menjamin bahwa metode analisis akurat,
spesifik, reprodusibel, dan tahan akan kisaran analit yang akan dianalisis (Gandjar dan Rohman, 2009; Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut (Harmita, 2004).
1. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan hasil analis sangat tergantung kepada sebaran galat sistematik di dalam keseluruhan tahapan analisis. Untuk mencapai kecermatan yang tinggi, dapat dilakukan dengan berbagai cara seperti menggunakan peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik, pengontrolan suhu, dan pelaksanaannya yang cermat, taat asas sesuai prosedur. Kecermatan ditentukan dengan dua cara yaitu:
− Metode simulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke dalam campuran bahan pembawa sediaan farmasi lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya).
− Metode penambahan baku (standard addition method)
Dalam metode penambahan baku, sampel dianalisis lalu sejumlah tertentu analit yang diperiksa ditambahkan ke dalam sampel, dicampur dan
dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang diharapkan).
Persen perolehan kembali dalam kedua metode tersebut dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Persen perolehan kembali dapat ditentukan dengan cara membuat sampel plasebo (eksepien obat, cairan biologis) kemudian ditambah analit dengan konsentrasi tertentu (biasanya 80% sampai 120% dari kadar analit), kemudian dianalisis dengan metode yang akan divalidasi. Tetapi bila tidak memungkinkan membuat sampel plasebo karena matriksnya tidak diketahui seperti obat-obatan paten, atau karena analitnya berupa suatu senyawa metabolit sekunder, maka dapat dipakai metode adisi. Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut. Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan tadi dapat ditemukan.
2. Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata- rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen. Presisi merupakan ukuran keterulangan metode analisis dan biasanya dinyatakan sebagai simpangan baku relatif dari sejumlah sampel yang berbeda signifikan secara statistik.
3. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuan suatu metode mengukur zat tertentu saja secara cermat dan seksama dengan adanya komponen lain yang mungkin ada dalam matriks sampel. Selektivitas biasanya dinyatakan sebagai derajat penyimpangan metode yang dilakukan terhadap sampel yang mengandung bahan yang ditambahkan berupa cemaran, hasil urai, senyawa sejenis, dan senyawa lain yang dibandingkan terhadap hasil analisis sampel yang tidak mengandung bahan lain yang ditambahkan.
4. Linearitas dan Rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon yang secara langsung atau dengan bantuan perhitungan matematik yang baik, proporsional terhadap konsentrasi analit dalam sampel. Rentang metode adalah pernyataan batas terendah dan tertinggi analit yang sudah ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan, dan linearitas yang dapat diterima.
5. Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah jumlah analit terkecil dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan blangko. Batas kuantitasi merupakan parameter pada analisis dan diartikan sebagai kuantitas analit terkecil dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
6. Ketangguhan Metode (Ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang diperoleh dari analisis sampel yang sama dalam berbagai kondisi uji normal, seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu, dan hari yang berbeda.
Ketangguhan metode dinyatakan sebagai tidak adanya pengaruh perbedaan operasi atau lingkungan kerja terhadap hasil uji.
7. Kekuatan (Robustness)
Kekuatan merupakan kemampuan metode untuk tetap tidak terpengaruh oleh adanya variasi parameter metode yang kecil. Kekuatan suatu metode adalah dengan membuat variasi parameter-parameter penting dalam suatu metode secara sistematis lalu mengukur pengaruhnya pada pemisahan (Gandjar dan Rohman, 2009).
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif dan di Laboratorium Penelitian Farmasi Fakultas Farmasi Universitas Sumatera Utara pada bulan April 2013 - Juni 2013.
3.2 Bahan-bahan 3.2.1 Sampel
Sampel yang digunakan adalah biji dari nangka (Artocarpus integra) muda dan nangka tua beserta kulit dalam (endotesta) yang diambil secara purposif di Jalan Sisingamangaraja Km 8,5 Kelurahan Timbang Deli, Kecamatan Medan Amplas, Medan (Gambar dapat dilihat pada Lampiran 2, halaman 43).
3.2.2 Pereaksi
Pereaksi yang digunakan dalam penelitian ini jika tidak dinyatakan lain mempunyai kualitas pro analis produksi E. Merck yaitu Larutan baku kalsium 1000 µg/ml, larutan baku magnesium 1000 µg/ml, H2SO4 96% b/v, etanol 96% v/v, HNO3 65% b/v, ammonium oksalat 100,25%, NaOH 99,5%, kuning titan, dan akuabides (PT. Ikapharmindo Putramas).
3.3 Alat-alat
Alat yang digunakan antara lain, Spektrofotometer Serapan Atom Hitachi Z-2000 lengkap dengan lampu katoda kalsium dan magnesium, Neraca analitik (AND GF-200), Tanur (Philips Harris Ltd.Shenstone), Hot plate (Shott), blender, krus porselen, botol kaca, dan alat-alat gelas (Pyrex dan Oberoi).
3.4 Identifikasi Sampel
Identifikasi tumbuhan nangka dilakukan oleh Laboratorium Taksonomi Tumbuhan Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Hasil identifikasi sampel dapat dilihat pada Lampiran 1, halaman 42).
3.5 Pembuatan Pereaksi 3.5.1 Larutan HNO3 (1:1) (v/v)
Larutan HNO3 (1: 1) dibuat dengan cara mengencerkan 50 ml HNO3 65% (b/v) dengan air suling hingga 100 ml(Isaac, 1990).
3.5.2 Larutan H2SO4 10%
Ditambahkan secara hati-hati 57 ml H2SO4 96% (b/v) ke dalam lebih kurang 100 ml air suling, didinginkan hingga suhu kamar dan encerkan dengan air suling hingga 1000 ml (Ditjen POM, 1995).
3.5.3 Larutan Amonium Oksalat 3,5% b/v
Sebanyak 3,4913 g ammonium oksalat 100,25% dilarutkan di dalam 100 ml air suling (Ditjen POM, 1995).
3.5.4 Larutan Kuning Titan 0,05% b/v
Sebanyak 0,05 g kuning titan dilarutkan di dalam 100 ml air suling (Ditjen POM, 1995).
3.5.5 Larutan NaOH 2 N
Sebanyak 80,4221 gram NaOH 99,5% dilarutkan di dalam 100 ml air suling (Ditjen POM, 1995).
3.6 Prosedur Penelitian 3.6.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif yang dikenal juga sebagai sampling pertimbangan dimana sampel ditentukan atas pertimbangan bahwa populasi sampel adalah homogen dan sampel yang tidak diambil mempunyai karakteristik yang sama dengan sampel yang sedang diteliti (Sudjana, 2005).
3.6.2 Penyiapan Bahan
Diambil biji dari buah nangka muda dan buah nangka tua beserta kulit dalam (endotesta) yang telah dipisahkan dari daging buahnya, kemudian dicuci dan ditiriskan, lalu dipotong kasar dan dihaluskan dengan menggunakan blender.
3.6.3 Proses Destruksi Kering
Sampel yang telah dihaluskan ditimbang sebanyak ± 25 g dalam krus porselen, dipanaskan di atas hot plate untuk menguapkan kandungan air yang terdapat pada biji nangka sampai kering dan mengarang. Diabukan di tanur
dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan menjadi 500oC dengan interval 25oC setiap 5 menit. Pengabuan dilakukan selama 14 jam dan dibiarkan dingin (Isaac, 1990). Bagan alir proses dekstruksi kering dapat dilihat pada Lampiran 6, halaman 49.
3.6.4 Pembuatan Larutan Sampel
Hasil destruksi dilarutkan dalam 5 ml HNO3 (1:1) kemudian dipanaskan di atas hot plate hingga larutan menjadi bening. Hasilnya dimasukkan ke dalam labu tentukur 50 ml dan krus porselen dibilas dengan akuabides sebanyak 3 kali. Dicukupkan volumenya dengan akuabides hingga garis tanda, lalu disaring dengan kertas Whatman No. 42 dengan membuang 5 ml filtrat pertama, kemudian filtrat selanjutnya ditampung didalam botol kaca.
Larutan ini digunakan untuk analisis kualitatif dan analisis kuantitatif (Isaac, 1990). Perlakuan yang sama diulang sebanyak 6 kali untuk masing-masing sampel. Bagan alir pembuatan larutan sampel dapat dilihat pada Lampiran 7, halaman 50.
3.6.5 Analisis Kualitatif
3.6.5.1 Analisis Kualitatif Kalsium 3.6.5.1.1 Uji Mikroskop Kalsium Sulfat
Diletakkan 2-3 tetes larutan sampel di atas object glass dan ditambahkan 1 tetes larutan H2SO4 10% v/v, kemudian diamati di bawah mikroskop, akan terbentuk kristal seperti kumpulan jarum atau prisma yang memanjang (Svehla, 1979).
3.6.5.1.2 Reaksi dengan Ammonium Oksalat 3,5% b/v
Dipekatkan sebanyak 5 ml larutan sampel hingga tersisa 2 ml larutan sampel, lalu dimasukkan kedalam tabung reaksi, kemudian ditambahkan beberapa tetes larutan ammonium oksalat 3,5% b/v dan akan terbentuk endapan putih kalsium oksalat. Endapan diamati di bawah mikroskop, akan terbentuk kristal seperti amplop (Svehla,1979).
3.6.5.2 Analisis Kualitatif Magnesium
3.6.5.2.1 Reaksi dengan Larutan Kuning Titan 0,05% b/v
Dimasukkan kedalam tabung reaksi 1 ml larutan sampel, ditambah 5-6 tetes NaOH 2 N dan 3 tetes pereaksi kuning titan 0,05% b/v. Dihasilkan endapan merah terang (Svehla, 1979).
3.6.6 Analisis Kuantitatif
3.6.6.1 Analisis Kuantitatif Kalsium
3.6.6.1.1 Pembuatan Larutan Induk Baku Kalsium
Larutan baku kalsium (1000 µg/ml) dipipet sebanyak 5 ml, di masukkan ke dalam labu tentukur 50 ml. Ditambahkan 5 ml HNO3 (1:1), dicukupkan dengan akuabides hingga garis tanda. Diperoleh konsentrasi kalsium pada Larutan Induk Baku (LIB) I adalah 100 µg/ml.
Dari LIB I dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml, kemudian dicukupkan dengan akuabides hingga garis tanda. Diperoleh konsentrasi kalsium pada Larutan Induk Baku (LIB) II adalah 10 µg/ml.
3.6.6.1.2 Penentuan Kurva Kalibrasi Kalsium
Dari LIB II dipipet 1,25 ml; 2,5 ml; 5,0 ml; 7,5 ml; dan 10,0 ml kemudian di masukkan ke dalam labu tentukur 25 ml dan dicukupkan volumenya dengan akuabides hingga garis tanda sehingga diperoleh konsentrasi 0,5 µg/ml; 1,0 µg/ml; 2,0 µg/ml; 3,0 µg/ml; dan 4,0 µg/ml. Diukur serapan pada panjang gelombang 422,7 nm dengan nyala udara-asetilen.
3.6.6.1.3 Penentuan Kadar Kalsium dalam Sampel
Larutan sampel dipipet sebanyak 1 ml di masukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akuabides hingga garis tanda (faktor pengenceran: 50/1 = 50 kali), kemudian diukur absorbansinya dengan spektrofotometer serapan atom pada panjang gelombang 422,7 nm. Nilai absorbansi yang diperoleh berada di dalam rentang nilai kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.6.6.1.4 Perhitungan Kadar Kalsium dalam Sampel
Menurut Isaac (1990), perhitungan kadar kalsium dalam sampel dapat dihitung dengan cara sebagai berikut:
Kadar (µg/g) = 𝐶𝐶 𝑥𝑥 𝑉𝑉 𝑥𝑥 𝐹𝐹𝐹𝐹 𝐵𝐵𝐵𝐵 Keterangan:
C = Konsentrasi logam dalam larutan sampel (µg/ml) V = Volume larutan sampel (ml)
Fp = Faktor pengenceran BS= Berat sampel (g)
3.6.6.2 Analisis Kuantitatif Magnesium
3.6.6.2.1 Pembuatan Larutan Induk Baku Magnesium
Larutan baku magnesium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml. Ditambahkan 5 ml HNO3 (1:1), dicukupkan dengan akuabides hingga garis tanda. Diperoleh konsentrasi magnesium pada Larutan Induk Baku (LIB) I adalah 100 µg/ml.
Dari LIB I dipipet sebanyak 2,5 ml, dimasukkan ke dalam labu tentukur 50 ml, kemudian dicukupkan dengan akuabides hingga garis tanda. Diperoleh konsentrasi magnesium pada Larutan Induk Baku (LIB) II adalah 5 µg/ml.
3.6.6.2.2 Penentuan Kurva Kalibrasi Magnesium
Dari LIB II dipipet sebanyak (1,0; 2,0; 3,0; 4,0; 5,0; dan 6,0) ml kemudian dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan dengan akuabides hingga garis tanda. Larutan ini mengandung (0,1; 0,2; 0,3; 0,4; 0,5;
dan 0,6) µg/ml dan diukur pada panjang gelombang 285,2 nm dengan tipe nyala udara-asetilen.
3.6.6.2.3 Penentuan Kadar Magnesium dalam Sampel
Larutan sampel biji nangka tua dipipet sebanyak 1 ml dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akuabides hingga garis tanda. Dari larutan tersebut, dipipet sebanyak 1 ml lalu dimasukkan ke dalam labu tentukur 25 ml dan diencerkan dengan akuabides hingga garis tanda (faktor pengenceran: 50 x 25 = 1250 kali). Untuk biji nangka muda, dipipet sebanyak 2,5 ml larutan sampel lalu dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akuabides hingga garis tanda. Dari larutan tersebut,
dipipet sebanyak 1 ml lalu dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akuabides hingga garis tanda (faktor pengenceran: 20 x 50
= 1000 kali). Diukur absorbansi dari masing-masing larutan sampel dengan spektrofotometer serapan atom pada panjang gelombang 285,2 nm dengan tipe nyala udara-asetilen. Nilai absorbansi yang diperoleh berada di dalam rentang nilai kurva kalibrasi larutan baku magnesium. Konsentrasi magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.6.6.2.4 Perhitungan Kadar Magnesium dalam Sampel
Menurut Isaac (1990), perhitungan kadar magnesium dalam sampel dapat dihitung dengan cara sebagai berikut:
Kadar (µg/g) =𝐶𝐶 𝑥𝑥 𝑉𝑉 𝑥𝑥 𝐹𝐹𝐹𝐹 𝐵𝐵𝐵𝐵 Keterangan :
C = Konsentrasi logam dalam larutan sampel (µg/ml) V = Volume larutan sampel (ml)
Fp = Faktor pengenceran BS= Berat sampel (g)
3.6.7 Penentuan Batas Deteksi dan Batas Kuantitasi
Menurut Harmita (2004), batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sebaliknya batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan baku �𝐵𝐵𝑆𝑆𝑋𝑋� =
�
∑(𝑆𝑆−𝑆𝑆𝑌𝑌)𝑛𝑛−2 2Batas Deteksi (LOD) = 3𝑥𝑥 �
𝐵𝐵𝑆𝑆𝑋𝑋 � 𝑠𝑠𝑠𝑠𝑠𝑠𝐹𝐹𝑠𝑠
Batas Kuantitasi (LOQ) = 10 𝑥𝑥 �
𝐵𝐵𝑆𝑆 𝑋𝑋 � 𝑠𝑠𝑠𝑠𝑠𝑠𝐹𝐹𝑠𝑠
3.6.8 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar logam dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar logam dalam sampel yang sudah ditambahkan larutan standar dengan konsentrasi tertentu, kemudian dihitung kembali berapa jumlah analit yang ditambahkan (Harmita, 2004).
Sampel biji nangka tua ditimbang sebanyak ± 25 g, lalu ditambahkan 1 ml larutan baku kalsium (konsentrasi 1000 µg/ml) dan 1 ml larutan baku magnesium (konsentrasi 1000 µg/ml), kemudian dilanjutkan dengan prosedur dekstruksi kering seperti yang telah dilakukan sebelumnya. Prosedur pengukuran uji perolehan kembali dilakukan sama dengan prosedur penetapan kadar sampel.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
Persen Perolehan Kembali = 𝐶𝐶𝐹𝐹− 𝐶𝐶𝐴𝐴
𝐶𝐶𝐴𝐴∗
𝑥𝑥
100%Keterangan :
CA = Kadar logam dalam sampel sebelum penambahan baku (µg/g) CF = Kadar logam dalam sampel setelah penambahan baku (µg/g) C*A = Kadar larutan baku yang ditambahkan (µg/g)
3.6.9 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah sebagai berikut:
RSD = ×100%
X SD
Keterangan :
−
X = Kadar rata-rata sampel (µg/g) SD = Standar Deviasi (µg/g)
RSD = Relative Standard Deviation 3.6.10 Analisis Data Secara Statistik
Menurut Gandjar dan Rohman (2009), kadar kalsium dan magnesium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik dengan cara menghitung standar deviasi menggunakan rumus sebagai berikut:
SD =
( )
1 - n
X -
Xi 2
∑
Keterangan : SD = Standar Deviasi (mg/100 g) Xi = Kadar sampel (mg/100 g)
X = Kadar rata-rata sampel (mg/100 g) n = Jumlah pengulangan
Kadar kalsium dan magnesium yang diperoleh dari hasil pengukuran masing-masing ke enam larutan sampel, diuji secara statistik dengan uji T.
Untuk mengetahui data ditolak atau diterima dilakukan dengan uji T yang dapat dihitung dengan rumus:
thitung = �(Xi − X )𝐵𝐵𝑆𝑆
�√𝑛𝑛 �
Hasil pengujian atau nilai thitung yang diperoleh ditinjau terhadap tabel distribusi t, apabila thitung > ttabel maka data tersebut ditolak.
Menurut Sudjana (2005), untuk menentukan kadar kalsium dan magnesium di dalam sampel dengan tingkat kepercayaan 99%, α = 0,01, dk = n-1, dapat digunakan rumus:
µ = X ± t (½α,dk) x (SD/ √𝑛𝑛)
Keterangan : µ = kadar sebenarnya (mg/100 g) X = kadar rata-rata sampel (mg/100 g) t = harga t tabel sesuai dengan dk = n-1 α = tingkat kepercayaan
SD = standar deviasi (mg/100 g) n = jumlah pengulangan
3.6.11 Pengujian Beda Nilai Rata-rata
Menurut Sudjana (2005), sampel yang dibandingkan adalah independen dan jumlah pengamatan masing-masing lebih kecil dari 30 dan varians (σ) tidak diketahui sehingga dilakukan uji F untuk mengetahui apakah varians kedua populasi sama (σ1 = σ 2) atau berbeda (σ1 ≠ σ 2) dengan menggunakan rumus:
F0 = 𝐵𝐵1
2
𝐵𝐵22
Keterangan : F0 = Beda nilai yang dihitung
S1 = Standar Deviasi sampel 1 (mg/100 g) S2 = Standar Deviasi sampel 2 (mg/100 g)
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka dilanjutkan uji dengan distribusi t dengan rumus:
to = (𝑋𝑋1− 𝑋𝑋2) 𝐵𝐵𝐹𝐹 �1/𝑛𝑛1+ 1/𝑛𝑛 2
Sp
= �
(𝑛𝑛1−1)𝐵𝐵1 +2 (𝑛𝑛2−1)𝐵𝐵22𝑛𝑛1+ 𝑛𝑛2−2
Keterangan : X1 = kadar rata-rata sampel 1 (mg/100 g) X2 = kadar rata-rata sampel 2 (mg/100 g) Sp = simpangan baku (mg/100 g)
n1 = jumlah pengulangan sampel 1 n2 = jumlah pengulangan sampel 2 S1 = Standar Deviasi sampel 1 (mg/100 g) S2 = Standar Deviasi sampel 2 (mg/100 g)
Dan jika Fo melewati nilai kritis F maka dilanjutkan uji dengan distribusi t dengan rumus:
to = (𝑋𝑋1− 𝑋𝑋2) 𝐵𝐵𝐹𝐹 �𝐵𝐵12/𝑛𝑛1+ 𝐵𝐵22/𝑛𝑛 2
Keterangan : X1 = kadar rata-rata sampel 1 (mg/100 g) X2 = kadar rata-rata sampel 2 (mg/100 g) Sp = simpangan baku (mg/100 g)
n1 = jumlah pengulangan sampel 1 n2 = jumlah pengulangan sampel 2 S1 = Standar Deviasi sampel 1 (mg/100 g) S2 = Standar Deviasi sampel 2 (mg/100 g)
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif
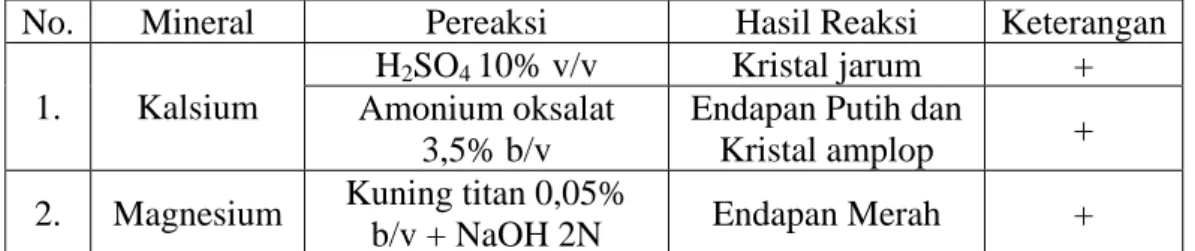
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya kalsium dan magnesium dalam sampel. Data dan Gambar dapat dilihat pada Tabel 4.1 dan Lampiran 5, halaman 47.
Tabel 4.1 Hasil Analisis Kualitatif Biji Nangka Muda
No. Mineral Pereaksi Hasil Reaksi Keterangan
1. Kalsium
H2SO4 10% v/v Kristal jarum + Amonium oksalat
3,5% b/v
Endapan Putih dan
Kristal amplop + 2. Magnesium Kuning titan 0,05%
b/v + NaOH 2N Endapan Merah + Keterangan : + = Mengandung mineral
Tabel 4.1 menunjukkan bahwa biji nangka mengandung kalsium dan magnesium. Sampel positif mengandung kalsium karena menghasilkan kristal jarum dengan penambahan H2SO4 10% v/v serta menghasilkan kristal amplop dengan penambahan ammonium oksalat 3,5% b/v, dan mengandung magnesium karena menghasilkan endapan merah terang dengan penambahan larutan kuning titan 0,05% b/v dan natrium hidroksida 2 N (Svehla, 1979).
Hasil absorbansi dengan spektrofotometer serapan atom menunjukkan adanya absorbansi pada panjang gelombang kalsium yaitu 422,70 nm dan magnesium 285,20 nm, hal ini membuktikan hasil dengan reaksi warna maupun reaksi kristal benar adanya, bahwa sampel mengandung kalsium dan magnesium.
4.2 Analisis Kuantitatif
4.2.1 Kurva Kalibrasi Kalsium Dan Magnesium
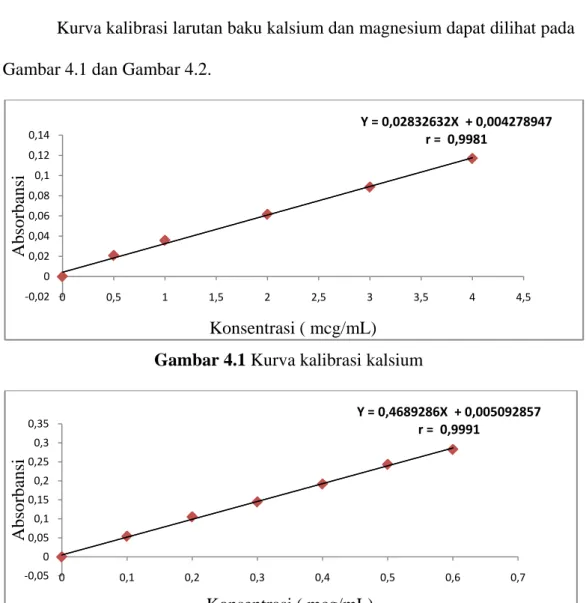
Kurva kalibrasi kalsium dan magnesium diperoleh dengan cara mengukur absorbansi dari larutan baku kalsium dan magnesium pada panjang gelombang 422,7 nm dan 285,2 nm. Dari pengukuran kurva kalibrasi untuk kalsium dan magnesium diperoleh persamaan garis regresi yaitu Y = 0,02832632X + 0,004278947 untuk kalsium dan Y = 0,4689286X + 0.005092857 untuk magnesium.
Kurva kalibrasi larutan baku kalsium dan magnesium dapat dilihat pada Gambar 4.1 dan Gambar 4.2.
Gambar 4.1 Kurva kalibrasi kalsium
-0,02 0 0,02 0,04 0,06 0,08 0,1 0,12 0,14
0 0,5 1 1,5 2 2,5 3 3,5 4 4,5
Absorbansi
Konsentrasi ( mcg/mL)
Y = 0,02832632X + 0,004278947 r = 0,9981
-0,05 0 0,05 0,1 0,15 0,2 0,25 0,3 0,35
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7
Absorbansi
Konsentrasi ( mcg/mL)
Y = 0,4689286X + 0,005092857 r = 0,9991
Berdasarkan kurva di atas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi, dimana koefisien korelasi (r) untuk kalsium sebesar 0,9981 dan magnesium 0,9991. Nilai r ≥ 0,95 menunjukkan adanya korelasi yang linier antara X dan Y (Ermer, 2005).
4.2.2 Penetapan Kadar Kalsium Dan Magnesium dalam Biji Nangka
Sampel yang digunakan dalam penetapan kadar kalsium dan magnesium adalah biji nangka muda dan biji nangka tua beserta kulit dalam (endotesta). Adapun karakteristik buah nangka muda adalah buah nangka yang digunakan sebagai bahan sayur, yang dipanen saat masih muda yaitu saat berumur ± 3 bulan sejak pembungaan atau saat daging buah, dami, serta biji nangka masih bewarna putih. Karakteristik buah nangka tua adalah buah nangka yang dapat langsung dimakan, yang dipanen saat berumur ± 8 bulan sejak pembungaan atau pada saat duri-duri buah nangka berukuran besar dan rata, warna kulit buah dan daging buah kuning, serta menebarkan bau harum.
Karakteristik biji nangka muda yang digunakan adalah biji nangka yang kulit luarnya bewarna putih, kulit tengah bewarna putih dan lunak, kulit dalam bewarna putih dan melekat kuat pada biji, serta inti biji yang belum terlalu keras. Adapun karakteristik dari biji nangka tua adalah biji nangka yang kulit luarnya bewarna kuning, kulit tengah bewarna putih dan keras, kulit dalam bewarna cokelat dan tidak melekat kuat pada biji, serta inti biji yang keras.
Penetapan kadar kalsium dan magnesium dilakukan secara spektrofotometri serapan atom. Konsentrasi kalsium dan magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi Hasil
analisis kuantitatif kalsium dan magnesium pada sampel dapat dilihat pada Tabel 4.2.
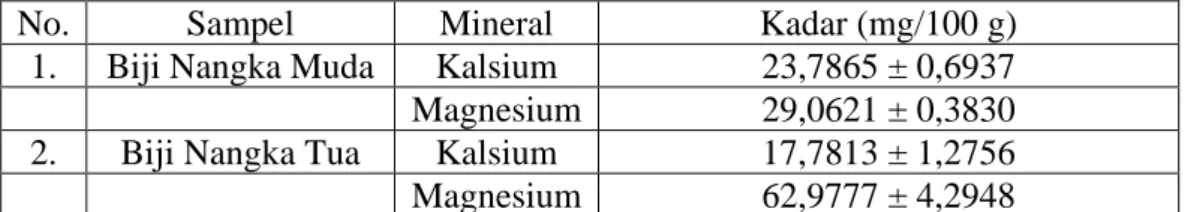
Tabel 4.2 Hasil Analisis Kuantitatif Kalsium dan Magnesium pada Bij Nangka
No. Sampel Mineral Kadar (mg/100 g)
1. Biji Nangka Muda Kalsium 23,7865 ± 0,6937 Magnesium 29,0621 ± 0,3830 2. Biji Nangka Tua Kalsium 17,7813 ± 1,2756 Magnesium 62,9777 ± 4,2948
Dari hasil analisis kuantitatif kalsium dan magnesium, sesuai yang tercantum pada tabel, biji nangka muda mengandung kadar kalsium yang lebih tinggi dibandingkan dengan biji nangka tua. Biji nangka tua mengandung kadar magnesium yang lebih tinggi dibandingkan dengan biji nangka muda.
Kalsium dalam tumbuhan berperan sebagai pengikat antara molekul- molekul fosfolipid dengan protein penyusun membran sehingga akan memperkuat dinding sel. Selain itu, kalsium juga berperan dalam pengambilan nitrat dan mereduksinya menjadi nitrit yang merupakan penyusun asam amino pada tumbuhan. Mineral ini juga berfungsi untuk merangsang perkembangan akar dan daun, serta sangat dibutuhkan dalam perkembangan biji. Hal inilah yang menyebabkan kandungan kalsium lebih banyak terdapat pada jaringan tumbuhan yang masih muda (Winarso, 2005).
Magnesium dalam tumbuhan berperan sebagai unsur penyusun klorofil dan memegang peranan penting dalam pertukaran zat fosfat. Mineral ini dapat bergabung dengan ATP sehingga dapat berfungsi dalam berbagai reaksi. Selain itu, magnesium juga berfungsi sebagai aktivator dari berbagai enzim seperti enzim transfosforilase, dehidrogenase, dan karboksilase, serta ikut
mempengaruhi proses pernapasan dan pembentukan DNA maupun RNA. Hal inilah yang menyebabkan kandungan magnesium lebih banyak terdapat pada jaringan tumbuhan yang tua (Dwijoseputro, 1980).
4.2.3 Pengujian Beda Nilai Rata-rata Kadar Kalsium dan Magnesium pada Biji Nangka Tua dan Biji Nangka Muda
Pengujian nilai beda rata-rata kadar kalsium dan magnesium pada sampel bertujuan untuk melihat apakah ada perbedaan yang signifikan pada rata-rata kadar kalsium dan magnesium antara biji nangka tua dan biji nangka muda. Uji statistik yang digunakan yaitu uji beda nilai rata-rata kadar kalsium dan magnesium antara biji nangka tua dan biji nangka muda yang dilanjutkan dengan menggunakan uji t pada taraf kepercayaan 99%. Perbedaan kadar yang signifikan antara kedua sampel diperoleh jika to atau thitung lebih tinggi atau lebih rendah dari range ttabel. Hasil uji beda nilai rata-rata kadar kalsium dan magnesium dalam biji nangka tua dan biji nangka muda dapat dilihat pada Tabel 4.3.
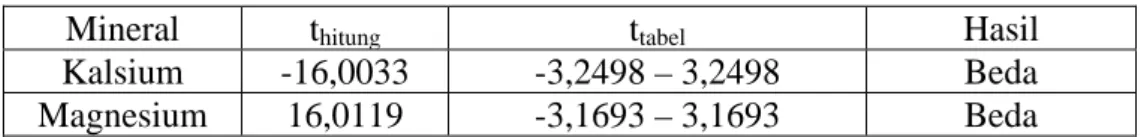
Tabel 4.3 Hasil Uji Beda Nilai Rata-rata Kadar Kalsium dan Magnesium dalam Biji Nangka Tua dan Biji Nangka Muda
Mineral thitung ttabel Hasil
Kalsium -16,0033 -3,2498 – 3,2498 Beda
Magnesium 16,0119 -3,1693 – 3,1693 Beda
Setelah dilakukan uji statistik terhadap kadar sampel maka dapat dilihat bahwa kadar kalsium dan magnesium yang terdapat dalam biji nangka muda dan biji nangka tua (Autocarpus integra) mempunyai perbedaan yang signifikan. Hal ini dipengaruhi oleh faktor perbedaan tua dan mudanya sampel yang diperiksa (Rosmarkam dan Yuwono, 2002).
4.2.4 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalsium dan magnesium diperoleh batas deteksi dan batas kuantitasi untuk kedua mineral tersebut. Batas deteksi dan batas kuantitasi kalsium dan magnesium dapat dilihat pada Tabel 4.4.
Tabel 4.4 Batas Deteksi dan Batas Kuantitasi Kalsium dan Magnesium Mineral Batas Deteksi (µg/ml) Batas Kuantitasi (µg/ml)
Kalsium 0,2372 0,7906
Magnesium 0,0294 0,0979
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi.
Perhitungan batas deteksi dan batas kuantitasi dapat dilihat pada Lampiran 17, halaman 71.
4.2.5 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (Recovery) kalsium dan magnesium setelah penambahan larutan baku dalam sampel dapat dilihat pada Lampiran 16, halaman 68. Perhitungan persen recovery kalsium dan magnesium dalam sampel dapat dilihat pada Lampiran 18, halaman 73. Persen recovery kalsium dan magnesium dalam sampel dapat dilihat pada Tabel 4.5.
Tabel 4.5. Persen Uji Perolehan Kembali (recovery) Kalsium dan Magnesium dalam Biji Nangka Tua
No Mineral yang dianalisis
Recovery (%) Syarat rentang persen Recovery (%)
1. Kalsium 94,97 80-120
2. Magnesium 95,49 80-120
Berdasarkan Tabel 4.5 di atas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) untuk kalsium 94,97% dan untuk magnesium 95,49%. Persen perolehan kembali tersebut menunjukkan kecermatan kerja
yang memuaskan pada saat pemeriksaan kadar kalsium dan magnesium dalam sampel. Hasil yang diperoleh dari uji perolehan kembali memberikan ketepatan pada pemeriksaan kadar kalsium dan magnesium dalam sampel. Menurut Harmita (2004), suatu metode dikatakan teliti jika nilai recovery nya antara 80 – 120%.
4.2.6 Simpangan Baku Relatif
Nilai simpangan baku dan simpangan baku relatif untuk kalsium dan magnesium pada biji nangka tua dapat dilihat pada Tabel 4.6, sedangkan perhitungannya dapat dilihat pada Lampiran 19, halaman 75.
Tabel 4.6 Nilai Simpangan Baku dan Simpangan Baku Relatif Kalsium dan Magnesium pada Biji Nangka Tua
No. Mineral Simpangan Baku Simpangan Baku Relatif
1. Kalsium 0,0242 0,11%
2. Magnesium 0,0457 0,07%
Berdasarkan Tabel 4.6 di atas, dapat dilihat nilai simpangan baku (SD) untuk kalsium adalah sebesar 0,0242 dan untuk magnesium adalah sebesar 0,0457, sedangkan nilai simpangan baku relatif (RSD) sebesar 0,11% untuk kalsium dan 0,07% untuk magnesium. Menurut Harmita (2004), nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per billion (ppb) RSD nya adalah tidak lebih dari 32%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki presisi yang baik.