i
EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill.
TERHADAP AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI
KARBON TETRAKLORIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh:
Ni Luh Putu Dian Prawita Putri NIM: 108114079
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
"Lakukan apa yang menjadi kewajibanmu dan jangan pikirkan hasilnya"
---Bhagawadgita---“Happiness and sadness, this too, will pass…”
---Pesan dari seorang pengajar yang luar
biasa---“
“The greatest prayer is a patience”
---Buddha---Ku persembahkan karya kecil ini untuk…
Ida Sang Hyang Widhi Wasa yang senantiasa memampukanku untuk melewati segala proses kehidupan dan menjadi sandaran terakhirku bila aku terlalu letih dan bahagia, Terimakasih untuk Bapak dan Ibu yang sejak awal membawa namaku dalam doa dan
mengijinkanku pergi untuk menemukan jalan pulang,
Setiap orang yang telah hadir membawa makna dan warna dalam hidupku, Almamaterku
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang berjudul
EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill.
TERHADAP AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI
KARBON TETRAKLORIDA, tidak memuat karya atau bagian karya orang
lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 30 September 2013 Penulis
(Ni Luh Putu Dian Prawita Putri)
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang berjudul
EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill.
TERHADAP AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI
KARBON TETRAKLORIDA, tidak memuat karya atau bagian karya orang
lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 30 September 2013 Penulis
(Ni Luh Putu Dian Prawita Putri)
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang berjudul
EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill.
TERHADAP AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI
KARBON TETRAKLORIDA, tidak memuat karya atau bagian karya orang
lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 30 September 2013 Penulis
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan dibawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Ni Luh Putu Dian Prawita Putri
Nomor Mahasiswa : 108114079
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill. TERHADAP AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI
KARBON TETRAKLORIDA
Beserta perangkat yang diperlukan (bila ada). Demikian saya memberikan kepada Perpustakaan Universitas Sana Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalty kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya, Dibuat di Yogyakarta
Pada tanggal: 30 September 2013
Yang menyatakan
(Ni Luh Putu Dian Prawita Putri)
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan dibawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Ni Luh Putu Dian Prawita Putri
Nomor Mahasiswa : 108114079
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill. TERHADAP AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI
KARBON TETRAKLORIDA
Beserta perangkat yang diperlukan (bila ada). Demikian saya memberikan kepada Perpustakaan Universitas Sana Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalty kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya, Dibuat di Yogyakarta
Pada tanggal: 30 September 2013
Yang menyatakan
(Ni Luh Putu Dian Prawita Putri)
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan dibawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Ni Luh Putu Dian Prawita Putri
Nomor Mahasiswa : 108114079
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill. TERHADAP AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI
KARBON TETRAKLORIDA
Beserta perangkat yang diperlukan (bila ada). Demikian saya memberikan kepada Perpustakaan Universitas Sana Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalty kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya, Dibuat di Yogyakarta
Pada tanggal: 30 September 2013
Yang menyatakan
vii
PRAKATA
Puji syukur kepada Tuhan Yang Maha Kasih atas berkat yang tiada henti, sehingga penulis dapat menyelesaikan skripsi berjudul “EFEK HEPATOPROTEKTIF INFUSA BIJI Persea americana Mill. TERHADAP
AKTIVITAS ALT-AST SERUM PADA TIKUS TERINDUKSI KARBON
TETRAKLORIDA” dengan baik.
Skripsi ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S.Farm) program studi Farmasi Universitas Sanata Dharma.
Penulis menyadari bahwa dalam pelaksanaan dan penyusunan skripsi ini tentunya tidak lepas dari bantuan dan campur tangan dari berbagai pihak. Oleh karena itu, pada kesempatan ini penulis mengucapkan terimakasih kepada:
1. Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Phebe Hendra, M.Si., Ph.D., Apt. sebagai Dosen Pembimbing skripsi atas waktu dan segala kesabaran dalam membimbing, memberi masukan dan motivasi kepada penulis selama penelitian dan penyusunan skripsi ini. 3. Bapak Prof. Dr. C. J. Soegihardjo, Apt. sebagai Dosen Penguji skripsi atas
bantuan dan masukan demi kemajuan skripsi ini.
4. Bapak Ipang Djunarko, M.Sc.,Apt. sebagai Dosen Penguji skripsi atas bantuan dan masukan demi kemajuan skripsi ini
5. Ibu Rini Dwiastuti, M.Si., Apt. sebagai Kepala Laboratorium Fakultas Farmasi yang telah memberikan ijin dalam penggunaan semua fasilitas laboratorium untuk kepentingan penelitian ini.
viii
6. Bapak Yohanes Dwiatmaka, M.Si., yang telah memberikan bantuan dalam determinasi tanaman P. americana Mill.
7. Bapak Heru Purwanto dan Bapak Suparjiman selaku laboran Laboratorium Farmakologi dan Toksikologi, Bapak Kayatno selaku laboran Laboratorium Biokimia dan Fisiologi Manusia, Bapak Wagiran selaku laboran Laboratorium Farmakognosi Fitokimia dan Bapak Otok selaku pengelola gudang farmasi.
8. Teman-teman “Tim Persea americana Ceria” Lydia Setiawan, Inneke Devi Permatasari, Gidion Krisnadi Yoseph, Irene, Ike Kumalasari, Angelia Rosari, Yudytha Anggarhaeni, Liana Risha, Robert Dwijantara Putra, Priscilla Diana Vivi Vionita, Maria Malida Vernandes Sasadara, Rotua Winata Nopelia Silitonga, Komang Ayu Nopitasari dan Adrienne Roma atas kerja sama, bantuan, suka duka dan perjuangan dalam menyelesaikan skripsi ini sampai akhir.
9. Teman-teman FSM B 2010, FKK A 2010 dan seluruh angkatan 2010 atas kebersamaan kita.
10. Teman-teman relawan di Pos Kesehatan St. Antonius Kota Baru yang senantiasa mengingatkan saya akan cinta kasih dan berbagi tidak akan mengurangi apa yang kita miliki.
11. Teman-teman PKMP PO-TA-TO 2013 Gidion Krisnadi Yoseph, Christiana Destia Anggraeni dan Abednego Dwi Yoga P atas kerjasamanya dan kekompakannya.
ix
12. Sahabat-sahabat terbaik sejak SMA hingga kini Ayu Tyas Febiyanti Wangsa, Yully Trisna Dewi dan Desak Putu Siska Dewi yang senantiasa menghapus tetesan air mata yang mengalir disela derai tawa kita dan berjalan bersama meraih mimpi dari tempat yang berbeda.
13. Kakak Asti, Oswaldine Heraolia Pramesthi, dan segenap anak kos 99999, terimakasih atas kebersamaan suka dan duka sebagai anak rantauan yang meraih mimpi dan cita-cita.
14. Semua pihak yang penulis tidak dapat sebutkan satu per satu yang turut membantu selama penyusunan skripsi ini berlangsung.
Penulis menyadari bahwa setiap manusia tidak ada yang sempurna. Oleh karena itu, penulis mengharapkan adanya kritik dan saran yang membangun demi kemajuan di masa yang akan datang.
Akhir kata, penulis berharap bahwa skripsi ini dapat bermanfaat bagi semua pihak, mahasiswa, lingkungan akademis, masyarakat serta memberikan sumbangan kecil bagi perkembangan ilmu pengetahuan khususnya di bidang kefarmasian.
Yogyakarta, 30 September 2013
Penulis
ix
12. Sahabat-sahabat terbaik sejak SMA hingga kini Ayu Tyas Febiyanti Wangsa, Yully Trisna Dewi dan Desak Putu Siska Dewi yang senantiasa menghapus tetesan air mata yang mengalir disela derai tawa kita dan berjalan bersama meraih mimpi dari tempat yang berbeda.
13. Kakak Asti, Oswaldine Heraolia Pramesthi, dan segenap anak kos 99999, terimakasih atas kebersamaan suka dan duka sebagai anak rantauan yang meraih mimpi dan cita-cita.
14. Semua pihak yang penulis tidak dapat sebutkan satu per satu yang turut membantu selama penyusunan skripsi ini berlangsung.
Penulis menyadari bahwa setiap manusia tidak ada yang sempurna. Oleh karena itu, penulis mengharapkan adanya kritik dan saran yang membangun demi kemajuan di masa yang akan datang.
Akhir kata, penulis berharap bahwa skripsi ini dapat bermanfaat bagi semua pihak, mahasiswa, lingkungan akademis, masyarakat serta memberikan sumbangan kecil bagi perkembangan ilmu pengetahuan khususnya di bidang kefarmasian.
Yogyakarta, 30 September 2013
Penulis
ix
12. Sahabat-sahabat terbaik sejak SMA hingga kini Ayu Tyas Febiyanti Wangsa, Yully Trisna Dewi dan Desak Putu Siska Dewi yang senantiasa menghapus tetesan air mata yang mengalir disela derai tawa kita dan berjalan bersama meraih mimpi dari tempat yang berbeda.
13. Kakak Asti, Oswaldine Heraolia Pramesthi, dan segenap anak kos 99999, terimakasih atas kebersamaan suka dan duka sebagai anak rantauan yang meraih mimpi dan cita-cita.
14. Semua pihak yang penulis tidak dapat sebutkan satu per satu yang turut membantu selama penyusunan skripsi ini berlangsung.
Penulis menyadari bahwa setiap manusia tidak ada yang sempurna. Oleh karena itu, penulis mengharapkan adanya kritik dan saran yang membangun demi kemajuan di masa yang akan datang.
Akhir kata, penulis berharap bahwa skripsi ini dapat bermanfaat bagi semua pihak, mahasiswa, lingkungan akademis, masyarakat serta memberikan sumbangan kecil bagi perkembangan ilmu pengetahuan khususnya di bidang kefarmasian.
Yogyakarta, 30 September 2013
x
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ...ii
HALAMAN PENGESAHAN ...iii
HALAMAN PERSEMBAHAN ...iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ...vi
PRAKATA ...vii
DAFTAR ISI... x
DAFTAR TABEL...xiv
DAFTAR GAMBAR ...xvi
DAFTAR LAMPIRAN...xvii INTISARI ...xix ABSTRACT... xx BAB I. PENGANTAR... 1 A. Latar Belakanng ... 1 1. Perumusan masalah... 4 2. Keaslian penelitian... 4 3. Manfaat penelitian ... 5 B. Tujuan Penelitian ... 6
xi
A. Hati... 7
1. Anatomi dan fisiologi hati ... 7
2. Kerusakan sel-sel hati ... 10
3. Hepatotoksin ... 11
4. Alanin transaminase (ALT) dan Aspartat transaminase (AST)…...12
B. Karbon Tetraklorida... 13
C. Curliv®... 14
D. Tanaman Persea americana Mill... 15
1. Sinonim ... 15
2. Nama daerah ... 15
3. Taksonomi... 16
4. Penyebaran ... 16
5. Morfologi ... 17
6. Kandungan dan kegunaan ... 17
E. Infusa... 18
F. Keterangan Empiris ... 19
BAB III. METODE PENELITIAN ... 20
A. Jenis dan Rancangan Penelitian ... 20
B. Variabel dan Definisi Operasional ... 20
1. Variabel utama ... 20
2. Variabel pengacau... 20
3. Definisi operasional ... 21
xii
D. Alat dan Instrumen Penelitian... 23
1. Alat pembuatan infusa biji P. americana... 23
2. Alat uji kadar ALT-AST ... 23
E. Tata Cara Penelitian ... 23
1. Determinasi serbuk biji P. americana ... 23
2. Pengumpulan bahan ... 24
3. Penetapan kadar air serbuk kering biji P. americana ... 24
4. Pembuatan infusa biji P. americana 8%... 24
5. Penetapan dosis infusa biji P. americana ... 24
6. Pembuatan larutan karbon tetraklorida konsentrasi 50%... 25
7. Penetapan dosis kontrol positif Curliv®... 25
8. Uji pendahuluan ... 26
9. Pengelompokkan dan perlakuan hewan uji... 27
10. Pembuatan serum ... 27
11. Penetapan aktivitas serum kontrol, serum ALT dan serum AST.... 28
F. Tata Cara Analisis Hasil ... 28
BAB IV. HASIL DAN PEMBAHASAN ... 30
A. Penyiapan Bahan... 30
1. Hasil determinasi serbuk ... 30
2. Penetapan kadar air serbuk biji P. americana... 30
B. Uji Pendahuluan... 31
1. Penentuan dosis hepatotoksik karbon tetraklorida... 31
xiii
3. Penetapan lama pemejanan infusa biji P. americana ... 35
4. Penetapan dosis infusa biji P. americana ... 35
C. Hasil Uji Efek Hepatoprotektif Infusa Biji P. americana... 36
1. Kontrol negatif olive oil dosis 2 mL/kgBB... 39
2. Kontrol hepatotoksin karbon tetraklorida dosis 2 mL/kgBB ... 42
3. Kontrol infusa biji P. americana dosis 1142,86 mg/kgBB... 43
4. Kontrol positif Curliv®dosis 4,05 mL/kgBB ... 44
5. Kelompok perlakuan infusa biji P. americana dosis 360,71; 642,06; 1142,86 mg/kgBB pada tikus jantan galur Wistar terinduksi karbon tetraklorida dosis 2 mL/KgBB ………45
D. Rangkuman Pembahasan ... 49
BAB V. KESIMPULAN DAN SARAN ... 53
A. Kesimpulan ... 53
B. Saran ... 53
DAFTAR PUSTAKA ... 54
LAMPIRAN... 58
xiv DAFTAR TABEL Tabel I. Tabel II. Tabel III. Tabel IV. Tabel V. Tabel VI. Tabel VII. Tabel VIII. Tabel IX.
Komposisi dan konsentrasi reagen serum ALT ………..
Komposisi dan konsentrasi reagen serum AST ………...
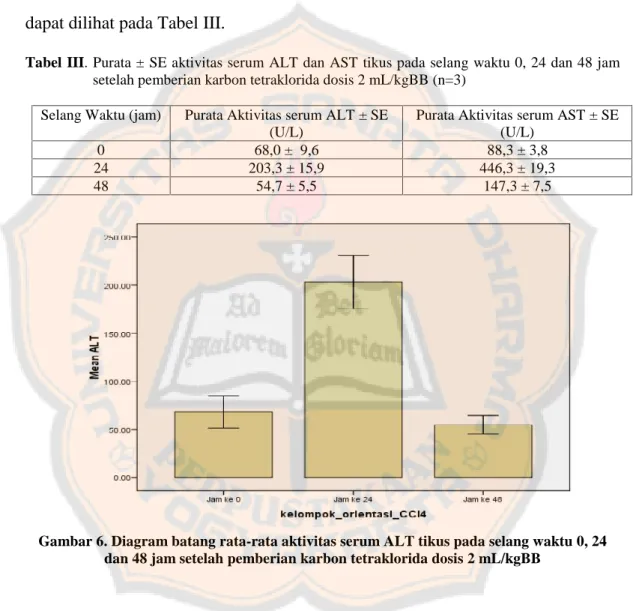
Purata ± SE aktivitas serum ALT dan AST tikus pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB ………. Hasil uji Scheffe aktivitas serum ALT tikus pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB………. Hasil uji Scheffe aktivitas serum AST tikus pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB……… Purata ± SE aktvitas serum ALT dan AST tikus praperlakuan infusa biji P. americana terinduksi karbon tetraklorida dosis 2 mL/kgBB……… Hasil uji Mann-Whitney aktivitas serum ALT tikus setelah pemberian karbon tetraklorida dosis 2 mL/kgBB pada kelompok perlakuan………. Hasil uji Mann-Whitney aktivitas serum AST tikus setelah pemberian karbon tetraklorida dosis 2 mL/kgBB pada kelompok perlakuan………. Purata ± SE aktvitas serum ALT dan AST tikus setelah pemberian olive oil dosis 2 mL/kgBB pada selang waktu 0
22 23 32 33 34 37 38 39
xv Tabel X.
dan 24 jam ………... Hasil uji T berpasangan aktivitas serum ALT dan AST tikus setelah pemberian olive oil dosis 2 mL/kgBB pada selang waktu 0 dan 24 jam………..
41
xvi DAFTAR GAMBAR Gambar 1. Gambar 2. Gambar 3. Gambar 4. Gambar 5. Gambar 6. Gambar 7. Gambar 8. Gambar 9. Gambar 10. Gambar 11. Anatomi hati ……… Struktur mikroskopik hati……….. Struktur karbon tetraklorida……….. Mekanisme biotransformasi dan oksidasi karbon tetraklorida….. Buah Persea americana Mill……… Diagram batang rata-rata aktivitas serum ALT tikus pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB……… Diagram batang rata-rata aktivitas serum AST tikus pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB……… Diagram batang rata-rata aktivitas serum ALT tikus praperlakuan infusa biji P. americana satu kali sehari selama enam hari berturut-turut terinduksi karbon tetraklorida………… Diagram batang rata-rata aktivitas serum AST tikus praperlakuan infusa biji P. americana satu kali sehari selama enam hari berturut-turut terinduksi karbon tetraklorida………… Diagram batang rata-rata aktivitas serum ALT tikus setelah pemberian olive oil dosis 2 mL/kgBB pada selang waktu 0 dan 24 jam……….. Diagram batang rata-rata aktivitas serum AST tikus setelah pemberian olive oil dosis 2 mL/kgBB pada 0 dan 24 jam………
7 9 13 14 15 32 33 37 38 41 41
xvii DAFTAR LAMPIRAN Lampiran 1. Lampiran 2. Lampiran 3. Lampiran 4. Lampiran 5. Lampiran 6. Lampiran 7. Lampiran 8. Lampiran 9. Lampiran 10. Lampiran 11. Lampiran 12. Lampiran 13. Lampiran 14
Foto biji P. americana …..………... Foto serbuk biji P. americana……… Foto infusa biji P. americana ……… Foto hasil determinasi organoleptis dan mikroskopik serbuk biji P. americana………. Surat pengesahan determinasi tanaman P. americana ……….. Surat pengesahan Medical and Health Research Ethics
Committee (MHREC)……….. Analisis statistik aktivitas serum ALT pada uji pendahuluan penentuan dosis hepatotoksin karbon tetraklorida 2 mL/kgBB Analisis statistik aktivitas serum AST pada uji pendahuluan penentuan dosis hepatotoksin karbon tetraklorida 2 mL/kgBB Analisis statistik aktivitas serum ALT perlakuan infusa biji P. americana setelah induksi karbon tetraklorida 2 mL/kgBB Analisis statistik aktivitas serum AST perlakuan infusa biji P. americana setelah induksi karbon tetraklorida 2 mL/kgBB Analisis statistik aktivitas serum ALT dan AST perlakuan kontrol negatif olive oil 2 mL/kgBB……… Perhitungan penetapan peringkat dosis infusa biji P. americana pada kelompok perlakuan……… Perhitungan Konversi Dosis untuk Manusia………... Perhitungan Dosis Curliv®……….
59 59 59 60 61 62 63 66 69 86 104 111 112 112
xviii Lampiran 15
Lampiran 16.
Lampiran 17. Lampiran 18.
Perhitungan Efek Hepatoprotektif……….. Perbandingan daya hepatoprotektif dosis IBPA perlakuan
dengan Curliv®………..
Penetapan kadar air serbuk biji P. americana……….. Hasil pengukuran validitas dan reabilitas……….
113
113 114 115
xix
INTISARI
Penelitian ini bertujuan untuk mengetahui efek hepatoprotektif infusa biji Persea americana Mill. pada tikus jantan galur Wistar yang terinduksi karbon tetraklorida dengan melihat penurunan aktivitas serum ALT dan AST, serta mendapatkan dosis efektifnya.
Penelitian ini termasuk eksperimental murni dengan rancangan acak lengkap pola searah. Tikus yang digunakan memiliki kisaran bobot 150-250 g sebanyak 35 ekor dan dibagi menjadi tujuh kelompok perlakuan. Kelompok I (kontrol hepatotoksin) diinduksikan karbon tetraklorida 2 mL/kgBB secara ip. Kelompok II (kontrol negatif) diberikan olive oil 2 mL/kgBB secara ip. Kelompok III (kontrol infusa) diberikan infusa biji P. americana dosis 1142,86 mg/kgBB secara po. Kelompok IV (kontrol positif) diberikan Curliv®4,05 mL/kgBB secara po selama enam hari berturut-turut dan hari ketujuh diinduksikan CCl4 2 mL/kgBB. Kelompok V, VI dan VII diberikan preperlakuan infusa berturut-turut dengan dosis 360,71; 640,06; dan 1142,86 mg/kgBB selama enam hari dan pada hari ketujuh diinduksikan CCl4 2 mL/kgBB. Dua puluh empat jam setelah perlakuan tersebut dilakukan pencuplikan darah melalui sinus orbitalis mata. Efek hepatoprotektif dari ketiga kelompok peringkat dosis dievaluasi melalui penurunan aktivitas serum ALT dan AST yang dihasilkan dan dianalisis menggunakan statistik Kruskal Wallis dan Mann-Whitney.
Hasil yang diperoleh menggambarkan bahwa hubungan dosis dengan respon yang dihasilkan tidak berbanding lurus dan ketiga dosis infusa biji P. americana memiliki efek hepatoprotektif. Jadi, efek hepatoprotektif yang paling tinggi ditunjukkan oleh infusa biji P. americana dosis 360,71 mg/kgBB sebesar 98,82%, yang diikuti dengan dosis 1142,86 mg/kgBB sebesar 87,02% dan dosis 642,06 mg/kgBB sebesar 61,50%.
Kata kunci: Persea americana, infusa, karbon tetraklorida, aktivitas serum ALT dan AST, efek hepatoprotektif
xx
ABSTRACT
The infusion of seed of Persea americana Mill. at dose 360.71; 642.06; and 1142.86 mg/kg body weight per oral was studied for the hepatoprotective effect using Carbon tetrachloride 2 mL/kg body weight induced liver damaged in rats. Male Wistar rats 150-250 g were divided in to seven groups.
Group I was given carbontetrachloride 2 mL/kg BW i.p. Group II was given olive oil 2 mL/kgBW i.p. The rats in the group III were given infusion of P. americana seed 1142.86 mg/kgBW p.o for six days. In the group IV, the rats were given Curliv® 4.05 mL/kgBW p.o for six days. Then, group V, VI and VII were given 360.71; 642.06; and 1142.86 mg/kg BW doses of infusion of Persea americana seed for six days p.o and on 7th day, the rats were given carbon tetrachloride 2 mL/kg BW. The hepatoprotective effect from dose 360.71; 642.06; and 1142.86 mg/kg body weight was evaluated by measuring activity of alanine transaminase (ALT) and aspartate aminotransferase (AST) from blood which taken from sinus orbitalis on 8thday.
The three doses of infusion P.americana seed showed significant (p<0,05) hepatoprotective effect by lowering the serum levels of ALT and AST. Based of the result, aqueous extract P. americana seed has not showed a linier relationship between doses and responses. Dose 360.71 mg/kg body weight has given the highest hepatoprotective effect 98.82%, and followed by dose 1142.86 and 642.06 mg/kg body weight (87.02% dan 61.50%).
Keywords: Persea americana, infusion, carbon tetrachloride, ALT-AST serum activities, hepatoprotective effect
1
BAB I
PENGANTAR
A. Latar Belakang
Metabolisme adalah segala proses kimia yang terjadi di dalam tubuh organisme hidup yang meliputi pemanfaatan bahan makanan untuk kebutuhan energi, pertumbuhan dan perbaikan sel. Selain itu, metabolisme juga menyangkut proses pembongkaran (katabolisme) dan proses penyusunan (anabolisme) suatu senyawa seperti karbohidrat, protein dan lemak (Sumardjo, 2009). Organ yang berperan penting dalam proses metabolisme ini adalah hati. Hati memiliki kapasitas cadangan yang membantu fungsi jaringan. Bila organ hati telah mengalami kerusakan melebihi 80%, maka kerusakan hati akan tampak. Ada banyak penyebab kerusakan hati diantaranya infeksi virus, imunologi, dan induksi suatu senyawa atau obat (Williamson, David, dan Fred, 1996).
Data dari Riset Kesehatan Dasar (Riskesdas) Departemen Kesehatan RI tahun 2007 menjelaskan bahwa penyakit gangguan fungsi hati dengan golongan umur 15 – 44 tahun menduduki urutan pertama sebagai penyebab kematian di daerah pedesaan, sedangkan untuk daerah perkotaan penyakit ini menduduki urutan ketiga. Perlemakan hati merupakan salah satu gangguan fungsi hati yang sering terjadi selain hepatitis, dimana pada kondisi ini terjadi penumpukan zat lemak di dalam sel hati, terutama trigliserida. Dilihat dari penyebabnya, perlemakan hati ada dua macam yaitu disebabkan oleh konsumsi alkohol berlebih dan non alkoholik (sindrom metabolik). Dari data epidemiologi, angka kejadian
perlemakan hati non alkoholik mencapai 30-100% pada obesitas di dunia (Angulo, 2002).
Perlemakan hati merupakan penyakit dengan penyebab yang multi faktorial, sehingga faktor risiko perlu dipertimbangkan dalam upaya pencegahan. Faktor risiko yang memiliki hubungan erat dengan perlemakan hati adalah umur, hiperlipidemia, diabetes melitus dan kegemukan. Kontribusi faktor risiko menunjukkan bila kegemukan dapat dihilangkan pada populasi tersebut maka perlemakan hati akan turun 30,6% menjadi 11,7% (Machmud, 2000).
Pengobatan kerusakan hati hingga kini belum ada yang bersifat spesifik. Namun, hingga saat ini obat komplementer maupun alternatif untuk gangguan fungsi hati masih terus dikembangkan guna memperoleh hasil yang lebih memuaskan ditinjau dari manfaat pengobatan maupun efek sampingnya. Pengobatan penyakit hati dapat dilakukan dengan terapi suportif seperti diet dan pengeluaran racun. Pengobatan dilanjutkan dengan terapi aktif baik dengan menggunakan obat konvensional maupun obat tradisional dari bahan alam yang dapat memberikan efek yang menguntungkan untuk perbaikan hati (Williamson, et al., 1996).
Di tengah pengembangan dunia kesehatan, back to nature merupakan isu yang tengah mendunia dan berdampak besar pada peningkatan penggunaan bahan alam sebagai obat. Di Indonesia, obat bahan alam dibagi menjadi tiga kategori yaitu jamu merupakan ramuan tradisional yang belum teruji secara klinis, obat herbal terstandar yaitu obat tradisional yang sudah melewati tahap uji pra klinis dengan hewan uji, dan fitofarmaka yaitu obat tradisional yang sudah melewati uji
praklinis dan klinis (Herdiani, 2012). Beragam flora yang tumbuh di Indonesia mendorong untuk terus melakukan eksplorasi tanaman terkait dengan manfaat bagi dunia kesehatan. Penggunaan bahan alam dalam dunia pengobatan bersifat empirik yang telah diwariskan secara turun temurun dan telah menjadi bagian penting dari kehidupan masyarakat.
Alpukat (Persea americana Mill) merupakan tumbuhan tropis, dimana bagian buahnya sangat umum untuk dikonsumsi menjadi aneka minuman segar dan makanan di Indonesia. Beberapa keterangan empiris menyebutkan bahwa biji alpukat dapat digunakan dalam pengobatan tradisional sebagai antidiabetik dengan cara dikeringkan dan dihaluskan, kemudian air seduhannya dapat diminum. Berdasarkan penelitian Malangngi, Sangi, dan Paendong (2012), dilaporkan bahwa kandungan total tanin dan tanin terkondesasi tertinggi dihasilkan pada ekstrak etanol biji alpukat biasa kering yaitu berturut-turut sebesar 117 mg/kg dan 20,855 mg/kg, dibandingkan dengan biji alpukat biasa segar, biji alpukat mentega kering dan biji alpukat mentega segar. Selain itu, biji alpukat kering juga memiliki aktivitas antioksidan tertinggi yang diukur dengan metode DPPH yaitu sebesar 93,045%. Adanya aktivitas antioksidan yang tinggi, biji alpukat kering diduga memiliki kemampuan hepatoprotektif terhadap kerusakan hati yang disebabkan oleh senyawa-senyawa model seperti karbon tetraklorida (CCl4). Mekanisme hepatotoksik dari senyawa CCl4 dengan terbentuknya radikal bebas triklorometil (CCl3*̇) dan triklorometil peroksil (CCl3O2*) yang merupakan hasil biotransformasi di hati oleh enzim sitokrom P450 reduktase dan kofaktor NADPH. Radikal bebas yang terbentuk akan berikatan dengan membran hepatosit
dan organel sel sehingga terjadi peroksidasi lipid serta ketidakseimbangan kalsium yang memicu kematian sel (Timbrell, 2008). Informasi mengenai kemampuan hepatoprotektif dari infusa biji P. americana belum banyak tersedia, apalagi cara pembuatan rebusan biji P. americana di masyarakat mirip dengan pembuatan sediaan infusa. Dengan demikian penelitian lebih lanjut mengenai efek hepatoprotektif infusa biji P. americana pada tikus jantan yang terinduksi karbon tetraklorida dengan melihat perubahan kadar serum AST dan ALT dalam darah akan sangat menarik untuk dilakukan.
1. Perumusan masalah
a. Apakah pemberian infusa biji P. americana mempunyai pengaruh hepatoprotektif dengan menurunkan kadar ALT dan AST serum pada tikus jantan galur Wistar yang terinduksi karbon tetraklorida?
b. Berapa besar nilai dosis infusa biji P. americana yang memiliki efek hepatoprotektif yang paling besar pada tikus jantan galur Wistar terinduksi karbon tetraklorida ?
2. Keaslian penelitian
Penelitian dengan menggunakan biji P. americana pernah dilakukan oleh Malangngi et al. (2012) yang melaporkan mengenai kandungan total tanin dan tanin terkondesasi tertinggi dihasilkan pada ekstrak etanol biji P. americana kering yaitu berturut-turut sebesar 117 dan 20,855 mg/kg. Pada penelitian tersebut juga melaporkan bahwa biji P. americana juga memiliki aktivitas antioksidan tertinggi yang diukur dengan metode DPPH yaitu sebesar 93,045%.
Kandungan senyawa kimia pada biji P. americana juga pernah diteliti oleh Leite, et al. (2009). Dari penelitian tersebut dilaporkan bahwa ekstrak heksan dan methanol dari biji P. americana menghasilkan LC50 berturut-turut 2,37 dan 24,13 mg mL-1dari uji toksisitas dengan menggunakan Artemia salina. Selain itu, pada ekstrak heksan biji P. americana menunjukkan kandungan dari asam palmitat (21,3%), asam palmitoleat (1,6%), asam stearat (2,2%), asam oleat (24,1%) dan asam linoleat (27,6%) yang diidentifikasi sebagai
1,2,4-trihidroksi-nonadekana dan β-sitosterol. Ding, Chin, Kinghorn, dan Ambrosio (2007)
mengidentifikasi kandungan metabolit sekunder yang ada pada buah alpukat diantaranya flavonoid, tanin, kumarin, dan alkanol. Flavonoid merupakan antioksidan larut air yang sangat kuat dan merupakan penangkap radikal bebas.
Sejauh penelusuran pustaka, penelitian yang dilakukan penulis berbeda dengan penelitian-penelitian sebelumnya, karena pada penelitian ini melihat dari aspek lain yaitu pengaruh pemberian infusa biji P. americana jangka panjang terhadap kadar AST dan ALT pada tikus jantan yang terinduksi CCl4.
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian efek hepatoprotektif jangka panjang dari infusa biji P. americana diharapkan mampu membantu pengembangan eksplorasi tanaman yang bersifat hepatoprotektor.
b. Manfaat praktis. Penelitian efek hepatoprotektif jangka panjang dari infusa biji P. americana diharapkan mampu memberikan informasi kepada masyarakat mengenai dosis efektif infusa biji P. americana yang memberikan proteksi terhadap hati.
B. Tujuan Penelitian
Penelitian yang dilakukan ini bertujuan untuk :
1. Membuktikan bahwa infusa biji P. americana memiliki kemampuan hepatoprotektif pada tikus jantan galur Wistar yang terinduksi karbon tetraklorida dengan menurunkan aktivitas AST dan ALT.
2. Mengetahui dosis infusa biji P. americana yang memiliki kemampuan hepatoprotektif yang paling besar pada tikus galur Wistar yang terinduksi karbon tetraklorida.
7
BAB II
PENELAAHAN PUSTAKA
A. Hati
1. Anatomi dan fisiologi hati
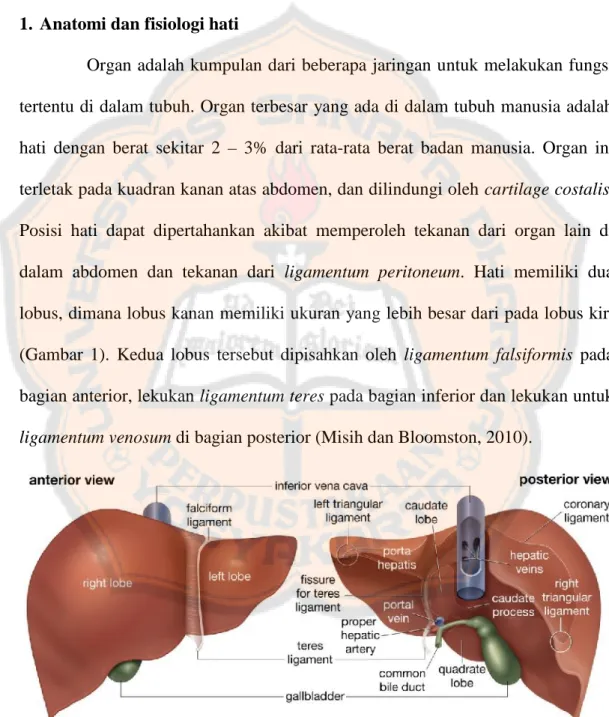
Organ adalah kumpulan dari beberapa jaringan untuk melakukan fungsi tertentu di dalam tubuh. Organ terbesar yang ada di dalam tubuh manusia adalah hati dengan berat sekitar 2 – 3% dari rata-rata berat badan manusia. Organ ini terletak pada kuadran kanan atas abdomen, dan dilindungi oleh cartilage costalis. Posisi hati dapat dipertahankan akibat memperoleh tekanan dari organ lain di dalam abdomen dan tekanan dari ligamentum peritoneum. Hati memiliki dua lobus, dimana lobus kanan memiliki ukuran yang lebih besar dari pada lobus kiri (Gambar 1). Kedua lobus tersebut dipisahkan oleh ligamentum falsiformis pada bagian anterior, lekukan ligamentum teres pada bagian inferior dan lekukan untuk ligamentum venosum di bagian posterior (Misih dan Bloomston, 2010).
Gambar 1. Anatomi hati (Misih dan Bloomston, 2010).
Pembuluh yang berperan dalam menyuplai darah untuk hati yaitu arteri hepatika dan vena porta. Arteri hepatika membawa darah yang kaya akan oksigen (kejenuhan oksigen 95-100%) dengan kecepatan aliran ±500 mL/menit. Vena porta membawa darah yang mengandung oksigen (kejenuhan oksigen 70%), lebih banyak nutrient dan sisa bakteri atau zat toksin dari saluan pencernaan (lambung, usus, pankreas dan limpa) dengan kecepatan aliran darah ±1000 mL/menit. Kedua pembuluh darah tersebut selanjutnya mengalirkan darah menuju kapiler hati yang disebut sinusoid, diteruskan ke vena sentralis pada tiap lobulus (Tso dan McGill, 2003).
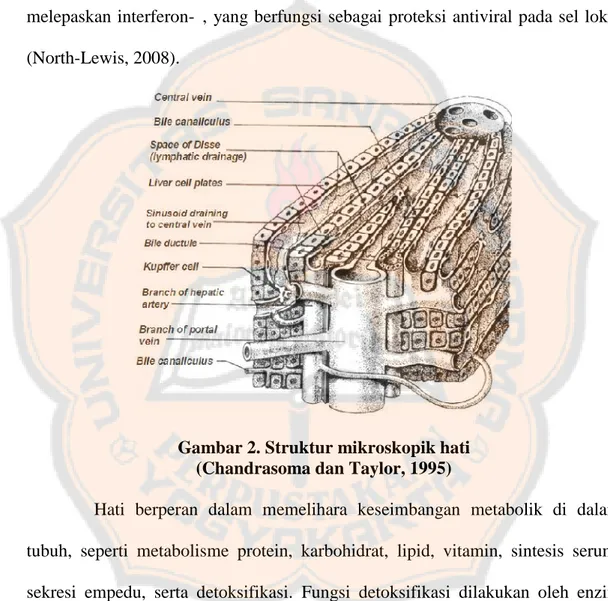
Struktur mikroskopik hati menggambarkan suatu sistem yang komplek yang terdiri dari beberapa sel dan pembuluh darah (Gambar 2). Sel hati berbentuk polihedral dan diameternya kira-kira 20-30 µm. Sebagian besar sel hati memiliki satu nukleus, namun ditemui juga yang memiliki nukleus ganda yang membagi diri dengan cara mitosis. Usia sel hati diperkirakan 150 hari dan memiliki daya regenerasi yang tinggi (North-Lewis, 2008). Kerusakan hati yang mengakibatkan hanya 10-20% jaringan hati yang masih berfungsi sudah cukup untuk mempertahankan hidup individu. Dalam tiap milligram jaringan hati ditemukan kira-kira 202.000 sel yang terdiri atas 171.000 sel parenkim hati dan 31.000 sel-sel lain termasuk sel-sel Kupffer (Price and Wilson, 2005). Hepatosit atau sel-sel parenkim hati berperan dalam proses metabolisme yang merupakan fungsi hati yang utama. Hepatosit terletak diantara sinusoid yang terdiri atas darah dan saluran empedu. Sel Kupffer adalah sel makrofag pada hati yang terletak di lumen sinusoid dan berperan penting dalam sistem kekebalan tubuh (Tso dan McGill,
2003). Makrofag akan teraktivasi oleh bakteri atau antigen asing yang masuk ke dalam hati atau sitokin yang dihasilkan oleh sel T helper. Kupffer sel akan mensekresikan sitokin yang dapat memicu sel proinflamatori ke hati dan melepaskan interferon-γ, yang berfungsi sebagai proteksi antiviral pada sel lokal (North-Lewis, 2008).
Gambar 2. Struktur mikroskopik hati (Chandrasoma dan Taylor, 1995)
Hati berperan dalam memelihara keseimbangan metabolik di dalam tubuh, seperti metabolisme protein, karbohidrat, lipid, vitamin, sintesis serum, sekresi empedu, serta detoksifikasi. Fungsi detoksifikasi dilakukan oleh enzim hati dengan cara oksidasi, hidrolisis, reduksi atau konjugasi senyawa-senyawa berbahaya bagi tubuh yang selanjutnya diubah menjadi bentuk tidak aktifnya. Kapasitas hati untuk mengubah obat induk menjadi metabolitnya sangat dipengaruhi oleh aktivitas enzim pemetabolisme yang terdapat pada retikulum endoplasma halus dan sitosol pada hepatosit. Selain itu, jumLah protein pengikat 2003). Makrofag akan teraktivasi oleh bakteri atau antigen asing yang masuk ke dalam hati atau sitokin yang dihasilkan oleh sel T helper. Kupffer sel akan mensekresikan sitokin yang dapat memicu sel proinflamatori ke hati dan melepaskan interferon-γ, yang berfungsi sebagai proteksi antiviral pada sel lokal (North-Lewis, 2008).
Gambar 2. Struktur mikroskopik hati (Chandrasoma dan Taylor, 1995)
Hati berperan dalam memelihara keseimbangan metabolik di dalam tubuh, seperti metabolisme protein, karbohidrat, lipid, vitamin, sintesis serum, sekresi empedu, serta detoksifikasi. Fungsi detoksifikasi dilakukan oleh enzim hati dengan cara oksidasi, hidrolisis, reduksi atau konjugasi senyawa-senyawa berbahaya bagi tubuh yang selanjutnya diubah menjadi bentuk tidak aktifnya. Kapasitas hati untuk mengubah obat induk menjadi metabolitnya sangat dipengaruhi oleh aktivitas enzim pemetabolisme yang terdapat pada retikulum endoplasma halus dan sitosol pada hepatosit. Selain itu, jumLah protein pengikat 2003). Makrofag akan teraktivasi oleh bakteri atau antigen asing yang masuk ke dalam hati atau sitokin yang dihasilkan oleh sel T helper. Kupffer sel akan mensekresikan sitokin yang dapat memicu sel proinflamatori ke hati dan melepaskan interferon-γ, yang berfungsi sebagai proteksi antiviral pada sel lokal (North-Lewis, 2008).
Gambar 2. Struktur mikroskopik hati (Chandrasoma dan Taylor, 1995)
Hati berperan dalam memelihara keseimbangan metabolik di dalam tubuh, seperti metabolisme protein, karbohidrat, lipid, vitamin, sintesis serum, sekresi empedu, serta detoksifikasi. Fungsi detoksifikasi dilakukan oleh enzim hati dengan cara oksidasi, hidrolisis, reduksi atau konjugasi senyawa-senyawa berbahaya bagi tubuh yang selanjutnya diubah menjadi bentuk tidak aktifnya. Kapasitas hati untuk mengubah obat induk menjadi metabolitnya sangat dipengaruhi oleh aktivitas enzim pemetabolisme yang terdapat pada retikulum endoplasma halus dan sitosol pada hepatosit. Selain itu, jumLah protein pengikat
obat di dalam darah dan aliran darah di hati juga mempengaruhi jumLah obat bebas yang akan di bawa ke hepatosit (DiPiro, Robert, Gary, Gary, Barbara, Michael, 2008).
2. Kerusakan sel-sel hati
Kerusakan hati disebabkan karena adanya kerusakan yang parah pada sel-sel hepatosit atau kerusakan berulang sel parenkim. Hati memiliki kapasitas cadangan, sehingga manifestasi klinis dari kerusakan hati baru akan muncul ketika telah terjadi kerusakan hati yang mencapai 80%-90%. Kerusakan hati dibagi menjadi tiga kategori, yaitu kerusakan hati akut, kerusakan hati kronis dan disfungsi hati tanpa nekrosis yang tampak (Crawford dan Liu, 2010).
Kerusakan hati akut disebabkan karena nekrosis hati yang parah dan umumnya disebabkan karena virus (hepatitis), obat (parasetamol), dan senyawa kimia (karbon tetraklorida). Kerusakan hati akut dapat digolongkan menjadi jaundice (kuning), hepatik enselopati, kegagalan sintesis protein yang berperan dalam pembekuan darah, dan kenaikan serum enzim yang berhubungan dengan kasus nekrosis sel hati (Crawford dan Liu, 2010). Penderita umumnya mengalami sakit selama 2-3 minggu. Kerusakan hati banyak diderita pada usia muda dan menunjukkan peningkatan morbiditas dan mortalitas (Polson dan Lee, 2005).
Kerusakan hati kronis disebabkan karena terjadinya nekrosis sel hati yang parah, fibrosis, regenerasi nobular dan kerusakan yang terakhir yaitu sirosis. Sirosis ditandai dengan akumulasi sejumLah jaringan fibrosa yang luas, khususnya serabut kolagen, sebagai respon terhadap kerusakan atau peradangan (Crawford dan Liu, 2010). Sirosis masuk ke dalam sepuluh besar penyakit yang
menyebabkan kematian di negara barat. Sirosis bersifat irreversible dan pada umumnya memiliki harapan hidup yang kecil. Faktor yang memicu terjadinya sirosis meliputi penggunaan minuman beralkohol, infeksi kronis, hepatitis autoimun, dan gangguan empedu (Kumar, Abbas, Fausto, Mitchel, 2007).
Kerusakan hati tanpa nekrosis yang tampak disebabkan karena hepatosit yang normal, namun tidak dapat menjalankan fungsi metaboliknya. Hal tersebut dapat disebabkan oleh pengaruh dari toksisitas tetrasiklin, steatosis saat kehamilan dan sindrom Reye (Kumar, et al., 2007).
3. Hepatotoksin
Hepatotoksin adalah senyawa kimia atau obat yang menyebabkan kerusakan sel hati akibat sifat toksik yang dimiliki atau mengalami perubahan struktur menjadi metabolit toksik. Obat dan senyawa yang dapat menyebabkan kerusakan hati dapat dibedakan menjadi dua, yaitu hepatotoksin teramalkan (tipe A) atau hepatotoksin tak teramalkan (tipe B) (Forrest, 2006).
Hepatotoksin teramalkan adalah senyawa kimia atau obat yang dapat menimbulkan efek toksik pada hati bila diberikan dalam jumLah yang besar. Hepatotoksin tipe ini sangat dipengaruhi oleh dosis pemberian. Contoh dari hepatotoksin teramalkan adalah parasetamol, karbon tetraklorida dan kloroform (Forrest, 2006).
Hepatotoksin tak teramalkan adalah senyawa kimia yang tidak menimbulkan efek toksik pada hati, namun bila diberikan pada orang tertentu dapat menimbulkan efek toksik. Frekuensi terjadinya sangat jarang pada 1 : 1000 orang dan hepatotoksin tipe ini tidak bergantung pada dosis pemberian. Contoh
dari hepatotoksin tak teramalkan adalah isoniazid, halothane, dan chlorpromazine (Forrest, 2006).
4. Alanin transaminase (ALT) dan Aspartat transaminase (AST)
Sel hepatosit mengandung beberapa enzim yang dapat dilepaskan ke sistem sirkulasi apabila sel hepatosit mengalami kerusakan. Alanin transaminase atau alanin aminotransferase (ALT) dan aspartat transaminase atau aspartat aminotransferase (AST) merupakan dua enzim yang banyak digunakan untuk menguatkan diagnosis adanya kerusakan hati. Enzim ALT lebih spesifik menggambarkan fungsi kerja hati dibandingkan AST (Waldmann, Soni, dan Rhodes, 2008). AST terdapat dalam konsentrasi tinggi pada hati, pankreas, ginjal, paru paru, otot dan sel darah merah. ALT juga ditemukan pada jaringan lain, namun jumlah yang dihasilkan di hati lebih banyak, sehingga dapat secara spesifik menggambarkan fungsi hati. Kadar normal ALT dan AST pada orang dewasa berkisar antara 0-40 IU/L (North-Lewis, 2008).
Beberapa enzim lainnya yang dapat digunakan sebagai penanda untuk mengetahui adanya kerusakan hati adalah enzim-enzim golongan hidrogenase seperti laktat dehidrogenase (LDH), glutamate dehidrogenase, isositrat dehidrogenase, dan malat dehidrogenase. Namun, enzim tersebut jarang digunakan untuk mendeteksi adanya kerusakan hati dan sifatnya kurang sensitif dan spesifik dibandingkan dengan kombinasi ALT dan AST (Hodgson dan Levi, 2000).
B. Karbon Tetraklorida
Organoleptis dari karbon tetraklorida berupa cairan jernih yang mudah menguap, tidak berwarna dan memiliki bau yang khas. Struktur karbon tetraklorida terdiri dari satu atom C yang mengikat tiga atom Cl (Gambar 3). Berat molekul senyawa ini 153,82 dan bersifat sangat sukar larut dalam air (Direktorat Jenderal Pengawasan Obat dan Makanan, 1995).
Gambar 3. Struktur karbon tetraklorida
(Direktorat Jenderal Pengawasan Obat dan Makanan, 1995).
Karbon tetraklorida adalah molekul sederhana yang dapat menyebabkan nekrosis hepatik sentrilobular dan perlemakan hati (steatosis). Senyawa ini banyak digunakan dalam penelitian kerusakan hati. Sifat karbon tetraklorida yaitu mudah larut dalam lemak sehingga efek toksik karbon tetraklorida sangat mudah terdistribusi ke seluruh tubuh. Hati menjadi target utama ketoksikan dari karbon tetraklorida dikarenakan enzim P450 paling banyak terdapat pada organ ini, terutama pada bagian sentrilobular. Mayoritas efek hepatotoksik dari karbon tetraklorida berasal dari metabolitnya (Gambar 4). Metabolit selanjutnya diaktivasi oleh sitokrom P450, khususnya sitokrom P450 2E1, sehingga menghasilkan radikal triklorometil yang bersifat toksik (Johnston dan Kroening, 1998). Radikal bebas ini selanjutnya menghasilkan metabolit kloroform akibat penambahan satu atom hidrogen. Produk lainnya yaitu radikal lipid atau radikal
thiol, bergantung pada sumber atom hidrogen. Radikal triklorometil dapat juga bereaksi dengan oksigen menyebabkan terjadinya lipid peroksidasi yang menghasilkan ketoksikan terhadap sel hati (Timbrell, 2008).
Gambar 4. Mekanisme biotransformasi dan oksidasi karbon tetraklorida (Timbrell, 2008).
Peroksidasi lipid dapat menyebabkan kerusakan membran sel dan mitokondria yang menyebabkan keluarnya substansi-substansi yang terdapat pada sitoplasma sel seperti enzim ALT dan AST. Selain itu, gangguan keluarnya lipid juga mengakibatkan penghambatan produksi protein dan sekresi lipoprotein. Hal tersebut berkaitan dengan adanya hambatan pada sintesis dan sekresi lipoprotein yang berfungsi membawa trigliserida meninggalkan hati. Hal inilah yang akhirnya menyebabkan hati mengalami perlemakan (Poli, Gravela, Albano dan Dianzani, 1979).
C. Curliv®
Produk Curliv® (Soho Industri Pharmacy) memiliki khasiat dan kegunaan sebagai suplemen makanan untuk memelihara kesehatan fungsi hati. Setiap 5 mL Curliv® mengandung ekstrak Silymarin 8,75 mg, Schisandrae
Fructus 33,75 mg, Curcuma xanth. Rhizoma 37,5 mg, Liquiritiae Radix 33,75 mg dan vitamin B6 sebesar 0,5 mg. Sediaan Curliv® tersedia dalam bentuk sirup 120 mL per botol. Aturan pakai untuk dewasa yaitu tiga kali sehari, dimana tiap pemakaiannya sebanyak tiga sendok teh (15 mL), sehingga dalam satu hari Curliv® diminum sebanyak 45 mL. Pemberian pada anak-anak yaitu tiga kali sehari, dimana tiap pemberiannya yaitu dua sendok teh (10 mL). Jadi total pemberian pada anak-anak yaitu 30 mL per hari.
D. Tanaman Persea americana Mill.
1. Sinonim
Persea gratissima Gaertn. f. (Departemen Kesehatan Republik Indonesia, 1978), Laurus persea L, Persea drymifolia Schlecht. and cham, Persea edulis Raf., Persea nubigena, Persea steyermarkii C.K. Allen (Lim, 2012).
2. Nama daerah
Avokat, advokat, apokat (Sumatra), adpokat (Melayu), apuket, alpuket (Sunda), apokat, avokat (Jawa) (Direktorat Jenderal Pengawasan Obat dan Makanan Republik Indonesia, 1978).
3. Taksonomi
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh) Super Divisi : Spermatophyta (Menghasilkan biji) Divisi : Magnoliophyta (Tumbuhan berbunga) Kelas : Magnoliopsida (berkeping dua / dikotil) Sub Kelas : Magnoliidae
Ordo : Laurales
Famili : Lauraceae
Genus : Persea
Spesies : Persea americana Mill.
(Proseanet, 2012)
4. Penyebaran
Tanaman P. americana berasal dari Amerika Tengah, tumbuh di daerah tropik dan subtropik dengan curah hujan antara 1.800 mm sampai 4.500 mm tiap tahun. Pada umumnya, tumbuhan ini cocok dengan iklim yang sejuk dan basah. Tumbuhan tidak tahan terhadap suhu rendah maupun tinggi, kelembaban rendah pada saat berbunga dan pada saat pembentukan buah serta angin yang keras. Di Indonesia, tanaman ini tumbuh pada tempat dengan ketinggian antara 1- 1.000 m di atas permukaan laut (Direktorat Jenderal Pengawasan Obat dan Makanan Republik Indonesia, 1978).
5. Morfologi
Tanaman P. americana merupakan tanaman periodik yang pertumbuhannya dipengaruhi oleh kondisi lokal tempat tumbuh. Tanaman ini berukuran sedang sampai besar, dengan tinggi mencapai 20 m. Karakteristik daun berupa daun tunggal, tersusun spiral, dengan tepi daun rata. Daun berbentuk elips hingga lanset, bulat telur hingga bulat telur sungsang, panjang daun 5-40 cm dan lebar 3-15 cm, permukaan atas daun diselaputi lilin. Panjang tangkai daun 1.5-5 cm (Proseanet, 2012).
Tanaman P. americana memiliki ribuan bunga per tanaman. Kelopak bunganya akan terbuka dalam kurun waktu mingguan atau bulanan. Bentuk bunga berupa tongkol majemuk (malai) yang muncul di ujung cabang. Bunga banci tersusun atas 3 daun mahkota. Perhiasan bunga tersusun atas dua lingkaran, benang sari 9 di dalam 3 lingkaran, kumpulan benang sari di bagian dalam mengeluarkan 2 nektar di bagian dasarnya. Putik terdiri atas satu ruang bakal buah, tangkai kepala putik ramping dengan kepala putik tunggal (simple papillate stigma) (Ospina, 2004). Pada Gambar 5, menggambarkan buah alpukat berukuran besar berdaging dan berair, berbiji tunggal, permukaan buah halus, panjang 7-20 cm. Buah besar dan bulat, dilapisi dua lapisan dan dua kotiledon besar yang melindungi embrio kecil (Proseanet, 2012).
6. Kandungan dan kegunaan
Kandungan fitokimia pada P. americana sangat beragam, diantaranya alkanol atau asetogenin alifatik, glikosida terpenoid, turunan cincin furan, flavonoid, dan kumarin. Senyawa alkanol berfungsi sebagai anti-inflamasi.
Senyawa turunan cincin furan memiliki aktivitas antibakterial, antifungal dan insektisidal. Beberapa senyawa flavonoid yang terkandung dalam tanaman ini diisolasi dari biji dan daun, memiliki aktivitas antiviral (Ding, et al, 2007). Flavonoid merupakan antioksidan larut air yang sangat kuat dan merupakan penangkap radikal bebas. Flavonoid dapat mencegah kerusakan oksidatif sel, mempunyai aktifitas perlindungan dan anti kanker yang kuat melawan tahap-tahap dalam karsinogenesis (Salah, Miller, Pangauga, Bolwell, Rice, dan Evans, 1995). Prinsip fungsi antioksidan adalah menghambat inisiasi atau propagasi dari rantai reaksi oksidasi oleh radikal bebas, sehingga mengurangi terjadinya kerusakan oksidatif (Frankel dan Meyer, 2000).
Penelitian Alhassan, et al. (2012) menunjukkan adanya indikasi potensi antidiabetes pada biji alpukat. Selain itu, biji alpukat juga berpotensi sebagai antioksidan berdasarkan penelitian dari Malangngi, dkk (2012). Di Nigeria, ekstrak biji P. americana digunakan untuk mengobati hipertensi. Hal ini kemudian diteliti oleh Anaka, Raymond, dan Stephen (2009) dan diperoleh kesimpulan bahwa ekstrak biji P. americana dapat menurunkan tekanan darah sedangkan ekstrak kulit kayunya digunakan secara tradisional sebagai pengobatan penyakit kulit yang disebabkan oleh parasit di Nigeria (Owolabi, Jaja, dan Coker, 2005).
E. Infusa
Infusa didefinisikan sebagai sediaan cair yang dibuat dengan mengekstraksi simplisia nabati dengan air pada suhu 90°C selama 15 menit (Badan Pengawas Obat dan Makanan, 2010). Infusa dapat dibuat dengan cara
mencampur simplisia dengan derajat halus yang sesuai dalam panci dengan air secukupnya. Pemanasan dilakukan di atas penangas air selama 15 menit terhitung sejak mencapai suhu 90°C yang disertai dengan pengadukan. Penyerkaian dilakukan menggunakan kain flannel yang disertai dengan menambahkan air panas secukupnya melalui ampas hingga diperoleh volume infus yang dikehendaki (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995).
F. Keterangan Empiris
Penelitian ini merupakan penelitian eksploratif untuk mengetahui adanya efek hepatoprotektif dari pemberian jangka panjang infusa biji P. americana pada hati berdasarkan aktivitas serum ALT-AST darah tikus terinduksi karbon tetraklorida.
20
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan rancangan acak lengkap pola searah.
B. Variabel dan Definisi Operasional
1. Variabel utama
a. Variabel bebas. Variabel bebas penelitian ini adalah variasi dosis dalam pemberian infusa biji P. americana.
b. Variabel tergantung. Variabel tergantung penelitian ini adalah efek hepatoprotekif infusa biji P. americana.
2. Variabel pengacau
a. Variabel pengacau terkendali. Vaiabel pengacau terkendali dalam penelitian ini adalah kondisi hewan uji, yaitu tikus jantan galur Wistar dengan berat badan 150-250 g dan umur 2-3 bulan, frekuensi pemberian infusa biji P. americana Mill satu kali sehari selama enam hari berturut-turut dengan waktu pemberian yang sama, cara pemberian senyawa pada tikus dilakukan secara per oral (infusa P. americana) dan intraperitoneal (karbon tetraklorida), dan bahan uji yang digunakan berupa biji P. americana yang diperoleh dari Padang, Sumatera Barat yang diambil pada bulan Januari 2013.
b. Variabel pengacau tak terkendali. Variabel pengacau tak terkendali dalam penelitian ini adalah kondisi patologis dari tikus jantan galur Wistar yang digunakan.
3. Definisi operasional
a. Dosis infusa biji P. americana. Didefinisikan sebagai volume (mL) infusa biji P. americana tiap kg berat badan subjek uji yang digunakan.
b. Infusa biji P. americana 8%. Infusa serbuk kering biji P. americana Mill 8% didapatkan dari dengan menginfundasi 8,0 g serbuk kering biji P. americana Mill dalam 100,0 mL air pada suhu 90°C selama 15 menit.
c. Efek hepatoprotektif infusa biji P. americana. Didefinisikan sebagai kemampuan infusa biji P. americana Mill untuk melindungi hepar dari hepatotoksin berupa penurunan ALT dan AST.
C. Bahan Penelitian
Penelitian ini menggunakan bahan uji sebagai berikut:
1. Hewan uji yang digunakan berupa tikus jantan galur Wistar dengan umur 2-3 bulan dan berat badan 150 hingga 250 g yang diperoleh dari Laboratorium Imono Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Serbuk biji P. americana Mill. yang diperoleh dari Padang, Sumatera Barat pada bulan Januari 2013.
3. Bahan hepatotoksin yang digunakan adalah karbon tetraklorida (Merck®) yang diperoleh dari Laboratorium Kimia Analisis Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
4. Kontrol negatif berupa olive oil (Bertoli®) yang diperoleh dari Supermarket Mirota Kampus, Yogyakarta.
5. Kontrol serum Cobas (PreciKontrol ClimChem Multi 1) Roche/ Hitachi Analyzer
6. Pelarut untuk infusa dengan aquadest yang diperoleh dari Laboratorium Farmakognosi-Fitokimia Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
7. Blanko pengujian ALT dan AST menggunakan aqua bidestilata yang diproduksi dari Laboratorium Kimia Analisis dan Instrumental Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
8. Reagen ALT
Reagen serum yang digunakan adalah reagen ALT Dyasis. Komposisi dan konsentrasi dari reagen ALT adalah sebagai berikut.
Tabel I. Komposisi dan konsentrasi reagen serum ALT
Komposisi pH Konsentrasi
R1 : TRIS 7,15 140 mmol/L
L-Alanine 700 mmol/L
LDH (lactate dehydrogenase) ≥2300 U/L
R2 : 2-Oxoglutarate 85 mmol/L NADH 1 mmol/L Pyridoxal-5 phosphate FS : Good’s buffer Pyridoxal-5-phosphate pH 9,6 100 mmol/L 13 mmol/L 9. Reagen AST
Reagen serum yang digunakan adalah reagen AST Dyasis. Komposisi dan konsentrasi dari reagen AST adalah sebagai berikut.
Tabel II. Komposisi dan konsentrasi reagen serum AST
Komposisi pH Konsentrasi
R1 : TRIS 7,65 140 mmol/L
L-Aspartate 320 mmol/L
MDH (malate dehydrogenase) ≥800 U/L
LDH (lactate dehydrogenase) ≥ 1200 U/L
R2 : 2-Oxoglutarate 65 mmol/L NADH 1 mmol/L Pyridoxal-5 phosphate FS : Good’s buffer Pyridoxal-5-phosphate pH 9,6 100 mmol/L 13 mmol/L
D. Alat dan Instrumen Penelitian
1. Alat pembuatan infusa biji P. americana
Panci lapis enamel, termometer, stopwatch, Beker glass, gelas ukur, cawan porselen, batang pengaduk, kompor listrik, timbangan analitik, dan kain flannel.
2. Alat uji aktivitas ALT-AST
Peralatan gelas, seperti Beker glass, labu ukur, batang pengaduk, gelas ukur, tabung reaksi, timbangan analitik, spuit injeksi intraperitoneal, pipa kapiler, mikro-vitalab 200, stopwatch, vortex, sentrifuge, Eppendorf.
E. Tata Cara Penelitian
1. Determinasi serbuk biji P. americana
Determinasi biji P. americana dilakukan dengan cara mencocokkan karakteristik organoleptis dan mikroskopis serbuk biji yang akan digunakan dengan serbuk biji P. americana Mill. yang telah diidentifikasi sebelumnya (standar). Determinasi dilakukan oleh Bapak Yohanes Dwiatmaka, M.Si, dosen Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Pengumpulan bahan
Bahan uji yang digunakan adalah biji P. americana yang sudah dalam bentuk serbuk berwarna kecoklatan, diperoleh dari wilayah Padang, Sumatera Barat pada bulan Januari 2013.
3. Penetapan kadar air serbuk kering biji P. americana
Serbuk kering biji P. americana yang sudah diayak dengan ayakan no. 40, selanjutnya dimasukkan ke dalam alat moisture balance ± 5 g dan diratakan. Bobot serbuk kering biji P. americana tersebut ditimbang sebagai bobot serbuk sebelum dilakukan pemanasan (bobot I). Serbuk dipanaskan pada suhu 105°C selama 15 menit, kemudian dilakukan penimbangan kembali bobot serbuk biji P. americana sebagai bobot serbuk setelah pemanasan (bobot II). Selisih bobot I dan bobot II yang diperoleh merupakan kadar air serbuk biji P. americana.
4. Pembuatan infusa biji P. americana 8%
Serbuk kering biji P. americana ditimbang sebanyak 8 g dan dibasahi dengan aquadest sebanyak dua kali berat serbuk yaitu 16 mL. Sebanyak 100 mL pelarut aquadest ditambahkan ke dalam panci enamel berisi serbuk yang telah dibasahi tersebut. Pemanasan dilakukan pada suhu 90°C dan dijaga tetap dalam suhu tersebut selama 15 menit. Campuran kemudian diambil, diperas menggunakan kain flannel dan ditambahkan aquadest hingga didapatkan volume perasan 100,0 mL infusa biji P. americana.
5. Penetapan dosis infusa biji P. americana
Dasar penetapan peringkat dosis adalah bobot tertinggi tikus dan pemberian cairan secara intraperitonial yaitu 5 mL. Maksimal pemberian
intraperitonial untuk tikus 5 mL (Nebendahl, 2000). Penetapan dosis tertinggi infusa biji P. americana adalah sebagai berikut.
D x BB = C x V
D x 350 gBB = 8 g/100 mL x 5 mL D = 1142,86 mg/kgBB
Penentuan dosis rendah infusa biji P. americana didasarkan pada keterangan empiris penggunaan rebusan serbuk biji P. americana di masyarakat, dan untuk dosis tengah berdasarkan faktor kelipatan dari dua dosis tersebut. Adapun faktor kelipatan yang digunakan sebesar 1,78. Dengan demikian, dosis yang digunakan dalam penelitian ini yaitu 360,71; 642,06; 1142,86 mg/kgBB.
6. Pembuatan larutan karbon tetraklorida konsentrasi 50%
Pembuatan larutan tetraklorida dengan konsentrasi 50% berdasarkan penelitian Janakat dan Al-Merie (2002), dilakukan dengan mencampurkan olive oil dan karbon tetraklorida masing-masing sebanyak 12,5 mL dengan perbandingan 1:1.
7. Penetapan dosis kontrol positif Curliv®
Penetapan dosis Curliv® berdasarkan informasi cara penggunaan di masyarakat yang tertera pada kemasan. Dosis untuk manusia 70 kgBB/hari sebesar 45 mL. Dosis untuk tikus setelah dikonversi dari dosis manusia menjadi 4,05 mL/kgBB.
Dosis Curliv® untuk manusia 70 kgBB = 45 ml
Dosis untuk tikus 200 gBB = 45 ml/70 kgBB x 0,018 = 0,81 ml/200gBB = 4,05 ml/kgBB
8. Uji pendahuluan
a. Penetapan dosis hepatotoksik karbon tetraklorida. Penetapan dosis hepatotoksik karbon tetraklorida ini mengacu pada penelitian yang dilakukan oleh Janakat dan Al-Merie (2002) yaitu sebesar 2 mL/kgBB yang diberikan secara intraperitoneal (i.p). Pada dosis ini dilaporkan telah dapat menyebabkan kerusakan sel-sel hati pada tikus jantan galur Wistar yang ditandai dengan peningkatan ALT dan AST, namun belum menyebabkan kematian. Windrawati (2013) melaporkan induksi CCl4 2 mL/kgBB mampu meningkatkan ALT dan AST tiga kali dari kadar awalnya. Penelitian Rajendran, et al (2009) menginformasikan peningkatan kadar ALT dan AST akibat induksi CCl4 sebesar 2 kali dari kadar awalnya juga menandakan telah terjadinya kerusakan sel hati tikus.
b. Penetapan waktu pencuplikan darah. Berdasarkan hasil penelitian Janakat dan Al-Merie (2002) dan Windrawati (2013) kenaikan serum ALT dan AST akan terjadi pada waktu 24 jam dan terjadi penurunan pada waktu 48 jam setelah pemejanan karbon tetraklorida. Pada penelitian ini dilakukan orientasi yang bertujuan untuk melihat profil kenaikan ALT dan AST serum. Orientasi dilakukan dengan tiga kelompok perlakuan waktu, dimana kelompok I-III masing-masing menggunakan cuplikan darah yang diambil pada 0, 24, dan 48 jam setelah pemejanan karbon tetraklorida. Setiap kelompok terdiri dari 5 ekor tikus dan darah diambil melalui sinus orbitalis mata. Darah yang telah diambil, kemudian diukur aktivitas serum ALT dan AST pada setiap kelompok perlakuan waktu tersebut.
9. Pengelompokkan dan perlakuan hewan uji
Hewan uji yang dibutuhkan sebanyak tiga puluh lima ekor tikus jantan yang dibagi secara acak dalam tujuh kelompok perlakuan masing-masing sejumLah lima ekor tikus. Kelompok I merupakan kelompok hepatotoksin, diberikan campuran karbon tetraklorida dan olive oil dengan perbandingan volume 1:1 dan dosis 2,0 mL/kg BB secara intraperitonial. Kelompok II merupakan kelompok kontrol negatif, diberikan olive oil dengan dosis 2 mL/kgBB secara intraperitonial. Kelompok III merupakan kontrol infusa, diberi infusa biji P. americana dosis 1142,86 mg/kgBB selama enam hari berturut-turut secara per oral. Kelompok IV merupakan kontrol positif (Curliv®) dosis 4,05 mL/kgBB selama enam hari berturut-turut secara per oral dan pada hari ketujuh diberikan larutan karbon tetraklorida 2 mL/kgBB secara intraperitonial. Kelompok V, VI dan VII merupakan kelompok perlakuan yang diberi infusa biji P. americana dengan tiga peringkat dosis yaitu 360,71; 642,06; 1142,86 mg/kgBB selama enam hari berturut-turut. Pada hari ketujuh kelompok V-VII diberi larutan karbon tetraklorida dosis 2 mL/kgBB secara intraperitonial. Dua puluh empat jam kemudian diambil darahnya melalui sinus orbitalis mata, lalu diukur kadar serum ALT dan AST.
10. Pembuatan serum
Darah diambil melalui bagian sinus orbitalis mata tikus, kemudian ditampung dalam tabung Eppendorf. Darah didiamkan selama ±15 menit, selanjutnya disentrifugasi selama 15 menit dengan kecepatan 10.000 rpm. Lapisan yang diambil yaitu lapisan supernatan yang terletak pada bagian atas.
11. Penetapan aktivitas serum kontrol, serum ALT dan serum AST
Alat yang digunakan untuk menganalisis aktivitas serum ALT dan AST adalah Mikrolab 200 Merck®. Aktivitas enzim dinyatakan dengan satuan U/L. pengukuran aktivitas serum ALT dan AST dilakukan di Laboratorium Biokimia Fisiologi Manusia, Fakultas Farmasi, Universitas Sanata Dharma Yogyakarta.
a. Penetapan aktivitas serum kontrol. Penetapan ini bertujuan untuk validitas dan reliabilitas alat yang digunakan.. Analisis serum kontrol dilakukan dengan cara mencampur 100 µL serum kontrol dengan 1000 µL reagen I, kemudian divortex selama 5 detik dan didiamkan selama 2 menit. Reagen II dicampurkan sebanyak 250 µL, kemudian divortex selama 5 detik dan dibaca serapannya setelah 1 menit (rentang nilai ALT = 26,2-41,8 U/L dan AST = 35,4-56,6 U/L).
b. Penetapan aktivitas serum ALT dan AST. Analisis serum ALT dilakukan dengan cara mencampur 100 µL serum dengan 1000 µL reagen I, kemudian divortex selama 5 detik dan didiamkan selama 2 menit. Reagen II dicampurkan sebanyak 250 µL, kemudian divortex selama 5 detik dan dibaca serapannya setelah 1 menit. Analisis serum AST dilakukan dengan cara mencampur 100 µL serum dengan 1000 µL reagen I, kemudian divortex selama 5 detik dan didiamkan selama 2 menit. Reagen II dicampurkan sebanyak 250 µL, kemudian divortex selama 5 detik dan dibaca serapannya setelah 1 menit.
F. Tata Cara Analisis Hasil
Pengujian data aktivitas serum ALT-AST untuk lebih dari dua kelompok dilakukan menggunakan Kolmogorov-Smirnov untuk mengetahui distribusi data
dan analisis varian untuk melihat homogenitas varian antar kelompoknya sebagai syarat analisis parametrik. Jika data terdistribusi normal dan variansi data homogen, maka dilanjutkan dengan analisis variansi pola searah (ANOVA one way) dengan taraf kepercayaan 95% untuk mengetahui perbedaan masing-masing kelmpok. Pengujian dilanjutkan menggunakan uji Scheffe untuk melihat perbedaan antar kelompok bermakna (signifikan) (p<0,05) atau tidak bermakna (tidak signifikan) (p>0,05). Jika data memiliki distribusi tidak normal dilakukan analisis dengan Kruskal Wallis untuk mengetahui perbedaan aktivitas serum ALT-AST antar kelompok. Pengujian dilanjutkan menggunkaan uji Mann Whitney untuk melihat kebermaknaan perbedaan tiap kelompok.
Pengujian data aktivitas serum ALT-AST untuk dua kelompok berpasangan dilakukan menggunakan Kolmogorov-Smirnov untuk mengetahui distribusi data dan analisis varian untuk melihat homogenitas variansi data antar kelompoknya sebagai syarat analisis parametrik. Jika data terdistribusi normal maka dilanjutkan dengan uji T berpasangan untuk melihat kebermaknaan dari perbedaan yang dihasilkan.
Perhitungan persen hepatoprotektif terhadap hepatotoksin karbon tetraklorida diperoleh dengan rumus:
(Aktivitas ALT CCl − aktivitas kontrol olive oil) − (Aktivitas ALT perlakuan − aktivitas kontrol olive oil) (Aktivitas ALT kontrol CCl − aktivitas kontrol olive oil) x 100% Daya hepatoprotektif kelompok perlakuan infusa biji P. americana terhadap
kontrol positif Curliv®diperoleh dengan rumus:
(Aktivitas ALT CCl − aktivitas kontrol ®) − (Aktivitas ALT perlakuan − aktivitas kontrol ®) (Aktivitas ALT kontrol CCl − aktivitas kontrol ®) x 100
30
BAB IV
HASIL DAN PEMBAHASAN
Tujuan dari penelitian ini yaitu untuk mengetahui pengaruh pemberian dan besar dosis efektif hepatoprotektif infusa biji P. americana pada tikus jantan galur Wistar terinduksi karbon tetraklorida dengan melihat aktivitas serum ALT dan AST. Serangkaian pengujian dilakukan untuk mencapai tujuan tersebut.
A. Penyiapan Bahan
1. Hasil determinasi serbuk
Determinasi serbuk bertujuan untuk memastikan bahwa serbuk yang digunakan dalam penelitian ini adalah serbuk biji P. americana, sehingga tidak terjadi kesalahan dalam penyiapan bahan yang akan digunakan. Determinasi dilakukan di Laboratorium Farmakognosi-Fitokimia, Fakultas Farmasi, Universitas Sanata Dharma Yogyakarta.
Proses determinasi ini dilakukan dengan cara mencocokkan kesamaan organoleptis dan mikroskopis dari serbuk yang digunakan dalam penelitian ini dengan serbuk standar biji P. americana (Lampiran 4). Hasil determinasi membuktikan bahwa memang benar serbuk yang digunakan dalam penelitian ini adalah serbuk biji P. americana.
2. Penetapan kadar air serbuk biji P. americana
Serbuk yang baik dapat terpenuhi bila kadar airnya masuk dalam persyaratan yang telah ditentukan Farmakope Indonesia IV yaitu kurang dari 10%. Penetapan kadar air serbuk biji P. americana menggunakan metode Gravimetri dengan alat moisture balance. Serbuk yang akan diukur kadar airnya dimasukkan
ke dalam alat moisture balance dan dipanaskan pada suhu 105°C. Pencatatan bobot serbuk dilakuan tiap lima menit hingga menit ke-15, dimana pada menit ini bobot serbuk dianggap sudah tetap. Dari hasil pengukuran tersebut, serbuk biji P. americana memiliki kadar air sebesar 7,4% sehingga dapat dikatakan telah memenuhi syarat serbuk yang baik.
B. Uji Pendahuluan
1. Penentuan dosis hepatotoksik karbon tetraklorida
Dosis hepatotoksik karbon tetraklorida merupakan dosis dimana senyawa model karbon tetraklorida mampu menyebabkan kerusakan hati ringan berupa steatosis pada tikus. Adanya kerusakan hati ditandai dengan meningkatnya aktivitas ALT dan AST tikus akibat induksi karbon tetraklorida. Menurut Ziemmerman (1999) dan Windrawati (2013) menyebutkan bahwa karbon tetraklorida dosis 2 mL/kgBB telah mampu meningkatkan aktivitas ALT kurang lebih sebesar tiga kali dan AST tikus empat kali lipat dari semula. Penelitian Janakat dan Al-Merie (2002) serta Windrawati (2013) menyebutkan bahwa karbon tetraklorida dosis 2 mL/kgBB telah mampu menginduksi terjadinya hepatotoksik. Berdasarkan hasil studi pustaka yang dilakukan, dosis senyawa karbon tetraklorida yang digunakan sebesar 2 mL/kgBB.
2. Penentuan waktu pencuplikan darah
Penentuan waktu pencuplikan darah dilakukan untuk mengetahui waktu yang menunjukkan efek hepatotoksik yang maksimal dari senyawa model karbon tetraklorida (CCl4). Efek hepatotoksik ditandai dengan peningkatan aktivitas serum ALT dan AST tikus pada selang waktu tertentu setelah penginduksian