EVALUASI
KETERSEDIAAN
HAYATI SEDIAAN
PENGERTIAN
Ketersediaan hayati adalah pengukuran
kecepatan (rate) dan jumlah (amount)
atau derajat(extent) zat aktif yang masuk
ke sirkulasi sistemik dalam keadaan
tidak berubah setelah pemberian suatu
bentuk sediaan.
Mencakup dua pengertian :
➢
Kecepatan
PENGERTIAN
Sirkulasi sitemik :
Peredaran darah vena dan arteri, tidak
termasuk vena porta
Istilah ketersediaan hayati ketersediaan
biologi ketersediaan sistemik ada
karena, tidak adanya kesetaraan
terapetik diantara sediaan bermerek
dagang tidak sama denganzat aktif
sama dalam bentuk sediaan sama dan
diberikan dengan dosis yang sama
PENGERTIAN
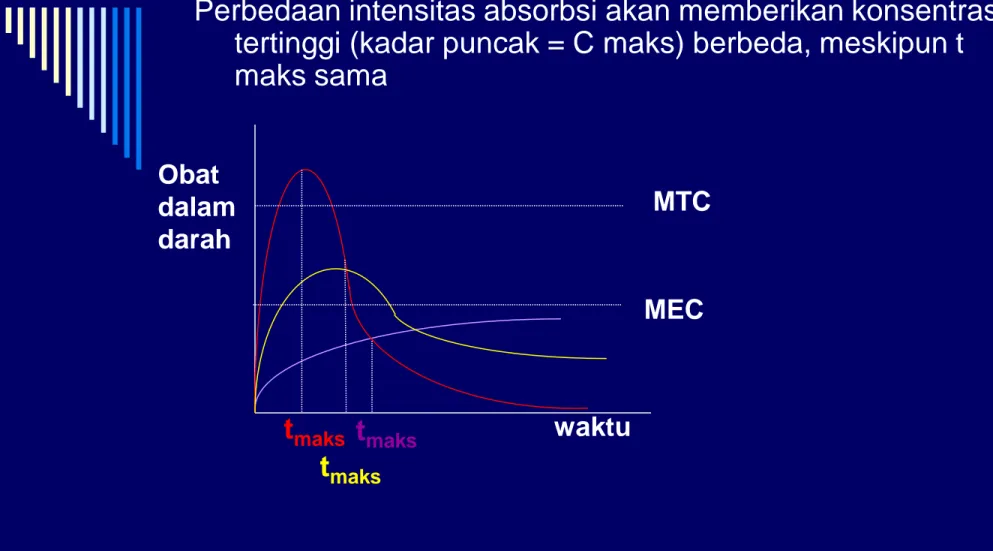
Kurva berikut memperlihatkan
ketidak-setaraan terapetik tersebut :
Obat dalam plasma t maks waktu cmaks cmaks cmaks
Gambar1 . Pengaruh intensitas penyerapan terhadap perubahan konsentrasi obat dalam darah
MEC MTC
Perbedaan intensitas absorbsi akan memberikan konsentrasi tertinggi (kadar puncak = C maks) berbeda, meskipun t maks sama
Perbedaan disposisi akan memberikan t maks maupun C maks yang berbeda Obat dalam darah tmaks tmaks tmaks MTC MEC waktu
gambar 2. Pengaruh disposisi terhadap perubahan konsentrasi obat dalam darah
KESETARAAN
Kesetaraan farmakoklinik
kesetaraan antara 2 obat dengan mol kimia berbeda
mempunyai aktivitas intrisik sama dan secara in vivo
bekerja pada mol substrat yang sama.
contoh : bentuk garam atau ester suatu zat aktif
Kesetaraan Kimia
kesetaraan antara 2 obat yang sama dengan dosis dan
cara yang sama dengan bentuk sediaan sejenis.
contoh : tablet dengan kaplet
Kesetaraan Farmasetik
kesetaraan antara 2 bentuk sediaan yang sama serta
memenuhi persyaratan farmakope secara in vivo
KESETARAAN
Kesetaraan Biologik atau Bioekivalen
obat yang mempunyai kesetaraan kimia atau farmasetik,
bila diberikan dengan aturan yang sama akan
memberikan ketersediaan hayati yang sama pada setiap
individu
Kesetaraan Klinik atau Terapetik
obat dengan kesetaraan farmakologi, kimia atau
farmasetik, jika diberikan pada subyek dengan aturan
pakai sama akan memberikan efektivitas terapetik sama
serta toksisitas yang sama.
Perbedaan ketersediaan hayati
disebabkan oleh :
❖
Sifat fisiko-kimia zat aktif yang
digunakan (bentuk kristal, ukuran
partikel, bentuk garam/ ester, dsb)
❖
Komposisi dan kualitas bahan baku
❖
Cara pencampuran
Perbedaan – perbedaan tersebut
menyebabkan perbedaan kecepatan
pelepasan & kecepatan melarut zat aktif
dari sediaan (untuk sediaan padat)
Mempengaruhi kecepatan & efisiensi
absorpsi zat aktif
Gambar 3. Kadar rata-rata dalam plasma pada pemberiaan 4 jenis sediaan kapsul kloramifenikol 0,5 gram pada subyek manusia
Obat dalam plasma (mg/ml)
Tujuan penelitian ketersediaan
hayati:
Dalam rangka pengembangan obat baru : untuk
menentukan cara pemberian & bentuk sediaan
yang sesuai suatu obat baru
Setelah diputuskan pembuatan obat baru,
menetapkan mutu & pengaturan pemberiannya
berkaitan dengan penderita (regiaira dosis =
frekwensi pemberian & besarnya dosis)
Untuk membandingkan kesetaraan mutu obat
sejenis yang dihasilkan pabrik lain (produk
inovator) untuk kepentingan pendaftaran
Parameter ketersediaan hayati
( menggunakan data darah )
i. Kadar puncak ( C maks )
- menunjang kadar obat tertinggi di dalam sirkulasi sistemik
- umumnya di nyatakan dalam µg / ml )
- C maks sering kali di hubungkan terhadap
intensitas aktivitas biologis & sebaiknya melebihi MEC, tapi kurang dari MTC
ii. Waktu untuk mencapai C maks ( t maks )
- menyatakan lamanya waktu yang di perlukan untuk mencapai C maks.
- t maks menunjang onsert ( mula kerja ) & merupakan
perkiraan kasar terhadap kecepatan abs. ( satuan t maks : jam )
iii. Luas di bawah kurva ( AUC = area under the
curve )
- menyatakan luas di bawah kurva
konsentrasi Vs waktu.
- Secara total & integral, di nyatakan dengan
satuan µg / ml x jam.
-
Merupakan perkiraan kasar terhadap
jumlah obat yang di absorpsi
- merupakan derajat ( extent ) ketersediaan
hayati.
Jika menggunakan data urin :
i. Dv
~: jumlah obat kumulatif yang di ekskresikan
ke
dalam urin
ii. dDv / dt : kecepatan ekskresi obat ke dalam
urin
iii.
t
~: waktu yang diperlukan untuk
mencapai ekskresi uriner maks
Pengukuran ketersediaan hayati
Ada 2 cara yang dapat di lakukan yaitu : 1. Cara absolut
2. Cara relatif
Cara absolut = cara mutlak
- ketersediaan hayati Z.a sediaan yang akan di
tentukan ( misal : sediaan tablet di berikan per oral ) di ukur dengan membandingkan parameter ketersediaan hayatinya terhadap sediaan Z.a yang sama yang di berikan I . V pada cara ini yang di tentukan hanya efisiensi abs memakai parameter AUCmenggunakan pers sbb :
Untuk data darah
F = AVC s x Di.v
AUC s = luas di bawah kurva yang diperoleh setelah pemberian sediaan obat yang di periksa
AUC I .V= luas di bawah kurva yang diperoleh setelah pemberian obat secara I . V
F = efisiensi abs ≈ fraksi dosis yang di abs Untuk data urin :
F = Dv~ . s x D I . V
Dv ~
I . V D s
Dv = jumlah obat total yang di ekskresi melalui urin
Nilai efisiensi abs yang diperoleh dengan cara ini berkisar 0 – 1 :
Cara relatif = Cara komparatif
Membandingkan parameter ketersediaan hayati dari suatu bentuk sediaan yang akan di tentukan terhadap parameter ketersediaan hayati sediaan inovator ( standar ). Pada cara ini selain membandingkan F ( efisiensi abs ) juga C maks & T maks dapat di bandingkan.
Untuk data darah :
F rel = AUC uji x Dosis st AUC st Dosisuji Untuk data urin :
F rel = Dv ~ uji x Dosis st
Dv ~ st Dosis uji
Keterangan = cara absolut
Nilai efisiensi abs yang diperoleh dengan cara ini bisa > 1 atau > 100 %
F < 1 > 1 atau F < 100 % > 100% Kerugiannya : karena kadar obat dalam darah jauh lebih
Keterangan = cara absolut
Nilai efisiensi abs yang diperoleh
dengan cara ini bisa > 1 atau > 100 %
F < 1 > 1 atau
F < 100 % > 100%
Kerugiannya : karena kadar obat dalam
darah jauh lebih besar kemungkinan
toksik
4. Protokol pemberian obat & waktu sampling
- subjek harus di puasakan selama 12 jam sebelum pemberian obat yaitu untuk menghindari pengaruh makanan terhadap disposisi obat
- Waktu pemberian obat yang paling baik adalah pukul 08.00 yaitu karena subjek harus di puasakan
- Interval waktu pemberian antara 1 sediaan dengan sediaan lainnya harus panjang . Idealnya penberian
sediaan berikutnya setelah semua Z.a / metabolitnya sah di eliminasi sempurna
Untuk pemberian dosis tunggal biasanya 6 x t ½
eliminasisah cukup, sebaiknya 10 – 20 x t ½ eliminasi ( terutama untuk metabolitnya )
- Frekuensi sampling : untuk data darah idealnya 15 kali tddr. 5 titik pada fase absorpsi, 5 titik pada fase sekitar puncak & 5 titk pada fase elimiasi, julah ini dapat
diperkecil yaitu 9 x masing – masing 3 titik tiap fase.
- Lamanya sampling 2- 3 x t ½ eliminasi sejak konsentrasi obat mulai turun
5. Senyawa yang akan di analisa & metode analisa
- senyawa asalnya, metabolit atau campran keduanya
bisa saja di lakukan
- Untuk mendapatkan gambaran knsentrasi efektif minimum sebaiknya senyawa aktif yang ditentukan ( senyawa aktif bisa berupa senyawa asal atau
metabolitnya )
- Metode analisa yang di gunakan harus peka & spesifik
6. Analisis cairan biologis
- Darah : penentuan kadar obat dalam darah adalah
pilihan ideal
- Tergantung dari mol yang di analisis & afinitasnya terhadap substrat biologis, maka penentuan kadar dapat di lakukan terhadap darah legkap / total atau plasma.
- Ekskresi yaiu Urin : dapat encerminkan keadaan
darah yang melalui ginjal yaitu pengeluaran kumulatif zat aktif atau metabolit )
- sulit untuk mendapat gambaran kecepatan absorbsinya