EKSTRAKSI PADAT-CAIR
I.
Pendahuluan
Ekstraksi padat-cair adalah proses transfer difusi (pemisahan) komponen yang mudah terlarut (solute) dari suatu padatan dengan menggunakan suatu larutan (pelarut) pada temperatur dan proses alir tertentu. Proses ini merupakan proses yang bersifat fisik karena komponen terlarut kemudian dikembalikan lagi ke keadaan semula tanpa mengalami perubahan kimiawi.
Unit proses ini adalah salah satu diantara unit operasi tertua dalam industri teknik kimia, yang sekarang mempunyai beberapa sebutan. Proses ini merupakan proses yang penting dari industri metalurgi dan farmasi, misalnya pada proses pemisahan biji emas dan tembaga dari biji-bijian logam lainnya. Proses ini dapat dilakukan untuk mendapatkan bagian yang mudah terlarut karena lebih berharga dari padatannya, misalnya pada bahan tambang, minyak nabati dan lain-lain, ataupun untuk menghilangkan bahan kontaminan yang mudah terlarut dari padatan yang lebih berharga, misalnya pigmen dari kontaminan kimiawi yang bisa atau
mudah dilarutkan.
Potassium Sulphate (ZK) atau biasa disebut Sulphate of Potash (SOP) telah dikenal sejak abad ke-14 yang merupakan garam berwarna putih dan memiliki sifat tidak mudah terbakar serta larut di dalam air. ZK digunakan sebagai pupuk yakni sumber senyawa kalium dan sulfur pada tanaman perkebunan seperti rami, kapas, dan tembakau.
Di Indonesia pupuk ini tidak disubsidi sehingga harganya relatif tinggi di pasaran. Bahan baku alami untuk pembuatan ZK yang berasal dari pertambangan antara lain adalah lanbeinite (K2SO4.2MgSO4), leonite (K2SO4.MgSO4.4H2O), schoenite (K2SO4.MgSO4.6H2O), dan glaserite (K3Na(SO4)2). Pertambangan sumber batuan tersebut banyak terdapat di negara Rusia, Kanada, benua Eropa, Israel, negara-negara timur tengah, Cina, Thailand, Kongo, dan Amerika Serikat.
Abu merupakan salah satu sumber Potash yang ada di Indonesia. Sumber Potash yang paling mudah ditemukan ialah pada tanaman, yaitu pada tanaman Pisang, Alpukat, Tomat, Jeruk, Melon, Kentang, Kacang-kacangan , Bayam dan sayuran berdaun hijau lainnya , Kacang-kacangan , Air kelapa , #angka , Kembang kol , Apel merah. Abu merupakan sisa pembakarang dari tanaman. Sehingga pada percobaan kali ini akan diuji, kadar Potash yang terdapat pada abu tanaman dapat menjadi peluang penyelesaian masalah kebutuhan akan Potash di Indonesia.
II.
Tujuan
a. Melakukan ekstraksi padat cair dengan metoda Counter Current 3 tahap dan Cross Current 5 tahap untuk mengekstrak Pottash (Kalium) dari abu gosok yang di beli di pasar.
b. Menentukan massa jenis larutan ekstraksi
c. Mendeteksi adanya ion SO42- di dalam larutan ekstrak
III.
Sasaran
a. Praktikan dapat menentukan massa jenis larutan ekstraksi
b. Praktikan dapat menentukan kandungan potash yang terdapat pada abu c. Praktikan dapat menentukan banyaknya kandungan SO42- pada abu
IV.
Tinjauan Pustaka
IV.1. Operasi Ekstraksi Padat Cair
Operasi ekstraksi padat cair terdiri atas dua langkah, yaitu kontak antara padatan dan pelarut untuk mendapatkan perpindahan solute ke dalam pelarut kemudian pemisahan larutan yang terbentuk dari padatan sisa. Sedangkan alat pengontak padatan dengan pelarut dibagi menjadi dua, yaitu:
1. Alat dengan unggun tetap (fixed bed), dimana pelarut dilewatkan melalui partikel padatan yang tersusun dalam suatu unggun tetap. Alat ini paling sederhana, terdiri dari tangki terbuka dengan dasar berlubang-lubang.
2. Alat dengan kontak terdispersi (dispersed contact), dimana partikel padatan didispersikan dalam pelarut, sehingga di samping terjadi pergerakan relatif antara partikel padatan dan pelarut terdapat juga pergerakan relatif antara partikel padatan itu sendiri.
IV.2. Metode Operasi
Ada empat jenis metode operasi ekstraksi padat cair, yaitu:
IV.2.1 Operasi sistem bertahap tunggal
Dalam metode ini, pengontakan antara padatan dan pelarut dilakukan secara bersamaan, kemudian disusul dengan pemisahan larutan dari padatan sisa. Metode ini jarang digunakan dalam operasi industri karena perolehan solute-nya rendah.
Gambar 2.1. Sistem operasi ekstraksi bertahap tunggal
(Sumber: Jurnal Ekstraksi Padat Cair, Laboratorium Operasi Teknik Kimia)
IV.2.2 Operasi sistem bertahap banyak dengan aliran sejajar atau aliran silang
Operasi ini dimulai dengan pencampuran umpan padatan dan pelarut dalam tahap pertama, kemudian aliran bawah dari tahap ini dikontakkan dengan pelarut baru pada tahap berikutnya, dan demikian seterusnya. Larutan yang diperoleh sebagai aliran atas dapat dikumpulkan menjadi satu seperti yang terjadi pada sistem dengan aliran sejajar, atau ditampung secara terpisah, seperti pada sistem dengan aliran silang.
Gambar 2.2. Sistem bertahap banyak dengan aliran sejajar
(Sumber: Jurnal Ekstraksi Padat Cair, Laboratorium Operasi Teknik Kimia)
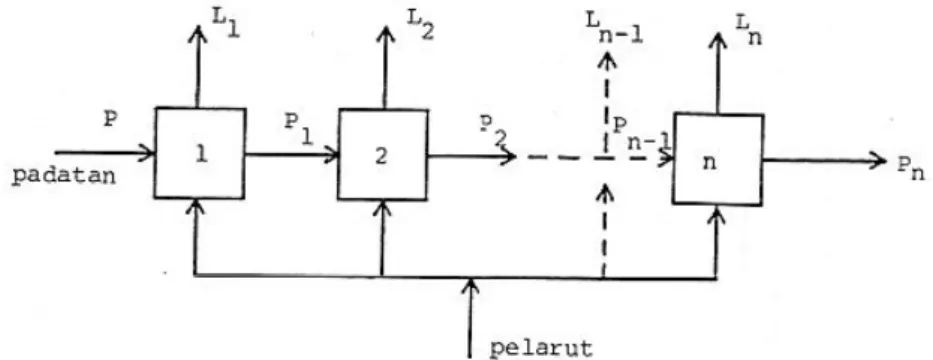
Gambar 2.3. Sistem bertahap banyak dengan aliran silang
(Sumber: Jurnal Ekstraksi Padat Cair, Laboratorium Operasi Teknik Kimia)
IV.2.3 Operasi kontinu dengan aliran berlawanan
Dalam sistem ini, aliran bawah dan atas mengalir secara berlawanan. Operasi dimulai pada tahap pertama dengan mengontakkan larutan pekat yang merupakan aliran atas tahap kedua, dan padatan baru. Operasi berakhir pada tahap ke-n (tahap terakhir), ketika terjadi pencampuran antara pelarut baru dan padatan yang berasal dari tahap ke-n (n-1). Pada operasi ini, sistem memungkinkan memperoleh hasil solute yang tinggi, sehingga banyak digunakan di dalam industri.
Gambar 2.4. Sistem bertahap banyak dengan aliran berlawanan (Sumber: Jurnal Ekstraksi Padat Cair, Laboratorium Operasi Teknik Kimia)
IV.2.4 Operasi batch sistem bertahap banyak dengan aliran berlawanan
Sistem ini terdiri dari beberapa unit pengontak batch yang disusun berderet atau dalam lingkaran yang dikenal sebagai rangkaian ekstraksi (extraction battery). Dalam sistem ini, padatan dibiarkan tetap
dalam setiap tangki dan dikontakkan dengan beberapa larutan yang konsentrasinya makin menurun. Padatan yang hampir tidak mengandung solute meninggalkan rangkaian setelah dikontakkan dengan pelarut baru, sedangkan larutan pekat sebelum keluar dari rangkaian terlebih dahulu dikontakkan dengan padatan baru di dalam tangki yang lain.
Langkah pertama Langkah kedua
Gambar 2.5. Operasi batch bertahap empat dengan aliran berlawanan (Sumber: Jurnal Ekstraksi Padat Cair, Laboratorium Operasi Teknik Kimia)
IV.3. Perhitungan Ekstraksi Padat Cair
Operasi ekstraksi padat cair terdiri atas dua langkah, yaitu kontak antara padatan dan pelarut untuk mendapatkan perpindahan solute ke dalam pelarut kemudian pemisahan larutan yang terbentuk dari padatan sisa. Sedangkan alat pengontak padatan dengan pelarut dibagi menjadi dua, yaitu:
1. Alat dengan unggun tetap (fixed bed), dimana pelarut dilewatkan melalui partikel padatan yang tersusun dalam suatu unggun tetap. Alat ini paling sederhana, terdiri dari tangki terbuka dengan dasar berlubang-lubang.
2. Alat dengan kontak terdispersi (dispersed contact), dimana partikel padatan didispersikan dalam pelarut, sehingga di samping terjadi pergerakan relatif antara partikel padatan dan pelarut terdapat juga pergerakan relatif antara partikel padatan itu sendiri.
IV.4. Titrasi
Titrasi adalah proses pengujian kuantitatif secara analitik untuk menentukan konsentrasi dari reaktan yang sudah diketahui. Disebut juga volumetric analysis karena pengukuran volume memegang peranan penting didalamnya. Sebuah reagen, yang disebut titran dengan konsentrasi yang diketahui (larutan standar) digunakan untuk menitrasi analit yang tidak diketahui konsentrasinya.
Alat yang digunakan untuk menambahkan titran, yaitu buret yang sudah dikalibrasi memungkinkan untuk menentukan jumlah volume yang digunakan untuk mencapai endpoint secara eksak. Endpoint adalah titik dimana titrasi dianggap sempurna sesuai didefinisikan oleh indikator. Titrasi memang umumnya menggunakan indikator secara visual atau perubahan warna. Dalam titrasi asam basa sederhana, phenolphthalein yang berubah menjadi pink saat pH 8,2 dan metil jingga yang menjadi merah dalam suasana asam dan kuning dalam suasana basa dapat menjadi indikator yang baik.
Gambar 2.6 Skema Alat Titrasi
(Sumber: http://www.bsieducation.org/Education/14-19/topic-areas/applied-science/images/titration-equipment.jpg)
IV.5. Penentuan Ion SO
42-dalam sampel
Penentuan sulfat secara potensiometrik. Telah dilakukan penelitian penentuan sulfat secara potensiometrik dengan metoda back titration, contoh larutan diendapkan sebagai barium sulfat dengan
cara menambahkan barium klorida berlebihan, kelebihan Barium dititrasi dengan larutan NaEDTA menggunakan elektroda ion selektif kalsium. Perbedaan antara barium klorida yang ditambahkan dengan kelebihan barium yang dititrasi merupakan barium sulfat yang diendapkan.
IV.6. Penentuan Posphate
dalam sampel
Penentuan kadar Phosphate dengan metoda gravimetri dapat dilakukan, prinsip metoda ini ialah
mengubah sampel ke dalam bentuk Mg2P2O7, dimana Mg2P2O7 akan berbentuk padatan setelah dibiarkan
dingin, Tahapan sampel yang diubah menjadi Mg2P2O7 mengikuti diagram dibawah ini,
Gambar 2.7 Skema tahapan sampel menjadi Mg2P2O7
(Sumber:http://download.fa.itb.ac.id/filenya/Handout%20Kuliah/Inorganic%20Pharmaceutical%20Analy sis%202008/Versi%20Bhs.%20Indonesia/03a.%20Analisis%20Gravimetri.pdf)
V.
Rancangan Percobaan
V.1.
Alat dan Bahan
i. Alat
- Gelas ukur 10 mL dan 100 mL, 1000 mL. - Piknometer - Timbangan digital - Pipet ukur 10 mL, 25 mL ii. Bahan - Abu gosok - NaOH 0,1 M - HCl 0,1 M - Aqua dm - Air - Indikator penoftalein - Indikator metil jingga - Larutan BaCl2
- Labu Erlenmeyer - Gelas kimia 400 mL
- Kompor pendidih dan stirrer - Perangkat titrasi - Labu ukur 1 L - Pipet tetes - Batang pengaduk - Kertas saring - Sarung tangan - Corong - Spatula - Tabung reaksi
V.2.
Prosedur Kerja
V.2.1 Pengenceran HCLo Masukkan aqua dm ke dalam labu takar 1 L terlebih dahulu sampai setengah penuh. o Pindahkan HCl 12 M sejumlah 8,33 ml kedalam labu takar 1 liter
o Masukkan aqua dm hingga batas dalam labu takar. o Campurkan larutan dalam labu takar.
V.2.2 Kalbrasi HCL
o Timbang NaOH pada timbangan digital, lalu catat massanya.
o Larutkan NaOH tersebut dalam gelas kimia dengan volume tertentu air, lalu catat volume air yang digunakan.
o Pisahkan larutan NaOH ke dalam dua gelas ukur yang lain, masing-masing dengan volume yang identik.
o Siapkan perangkat titrasi dan masukkan HCl yang sudah diencerkan.
o Pada larutan NaOH di gelas yang pertama, masukkan tiga tetes penofalein ke dalam laruran NaOH yang sudah dibuat.
o Titrasi dengan HCl hingga warna larutan berubah dari pink jadi bening, catat volume HCl yang digunakan.
o Lakukan kegiatan penitrasian yang serupa dengan indikator penoftalein pada NaOH gelas kedua. o Hitung konsentrasi NaOH dan konsentrasi HCl
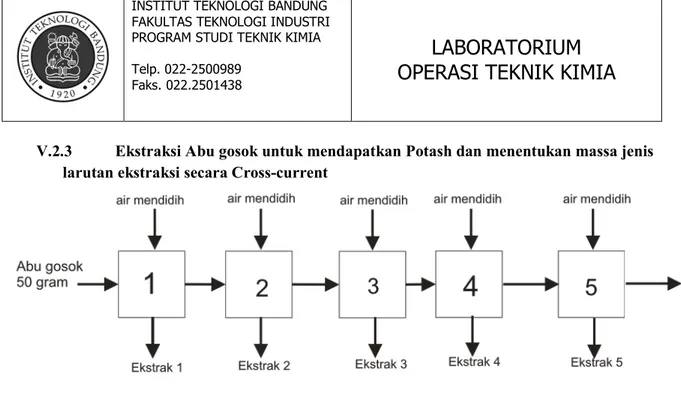
V.2.3 Ekstraksi Abu gosok untuk mendapatkan Potash dan menentukan massa jenis larutan ekstraksi secara Cross-current
Gambar V.1 Diagram Alat Ekstraksi Padat Cair Cross Current Lima Tahap
o Aqua dm sebanyak 375 mL disiapkan dan dididihkan di dalam gelas kimia o Abu gosok sebesar 50 gram ditimbang dengan menggunakan timbangan digital o Abu gosok yang telah terukur massanya dimasukkan ke dalam gelas kimia yang telah
berisi aqua dm mendidih
o Campuran di aduk hingga panas mencapai 110-120oC
o Setelah campuran tercampur merata, gelas kimia diangkat dari pemanas o Campuran dipisahkan dengan mengunakan kertas saring
o Ekstrak yang dihasilkan diukur volume cairan totalnya, dititrasi, dan diukur massanya dengan neraca digital di dalam sebuah piknometer
o Titrasi dilakukan dua kali, pertama digunakan indikator PP, awalnya ekstrak berwarna kemerahan, lalu ditrasi dengan HCl menjadi warna orange muda.
o Setelah ekstrak menjadi warna orange muda, ekstrak diberikan indikator Mo dimana warna ekstrak akan mengalami perubahan ke warna orange yang lebih pekat. Titrasi dengan HCl dilanjutkan sampai warna ekstrak menjadi jingga.
o Catat volume HCl yang telah digunakan
o Rafinat sisa filtrasi digunakan kembali sebagai feed pada ekstrasi tahap 2, dengan menggunakan aqua dm yang sama banyaknya dan perlakuan yang sama dengan di atas. Proses ini diulang sebanyak 5 kali.
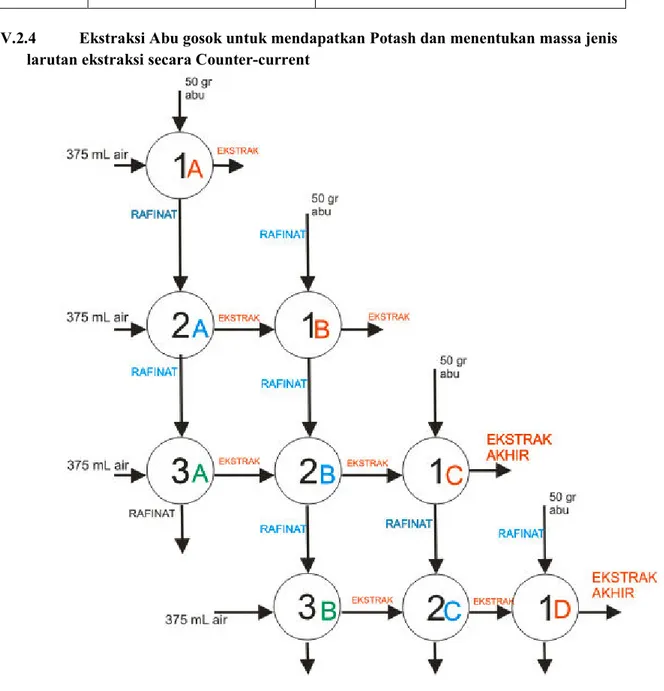
V.2.4 Ekstraksi Abu gosok untuk mendapatkan Potash dan menentukan massa jenis larutan ekstraksi secara Counter-current
Gambar Diagram Alat Ekstraksi Padat Cair Counter-Current 3 Tahap Tahap 1A
o Aqua dm sebanyak 375 mL disiapkan dan dididihkan di dalam gelas kimia o Abu gosok sebesar 50 gram ditimbang dengan menggunakan timbangan digital o Abu gosok yang telah terukur massanya dimasukkan ke dalam gelas kimia yang telah
o Campuran di aduk hingga panas mencapai 110-120oC
o Setelah campuran tercampur merata, gelas kimia diangkat dari pemanas o Campuran dipisahkan dengan mengunakan kertas saring
o Rafinat sisa filtrasi digunakan kembali sebagai feed pada ekstrasi tahap 2A o Pada tahap 1A ini ekstrak tidak perlu diukur.
Tahap 2A
o Aqua dm sebanyak 375 mL disiapkan dan dididihkan di dalam gelas kimia
o Hasil rafinat dari tahap 1A dimasukkan ke dalam gelas kimia yang telah berisi aqua dm mendidih
o Campuran di aduk hingga panas mencapai 110-120oC
o Setelah campuran tercampur merata, gelas kimia diangkat dari pemanas o Campuran dipisahkan dengan mengunakan kertas saring
o Rafinat sisa filtrasi digunakan kembali sebagai feed pada ekstrasi tahap 3A o Pada tahap 2A ini kembali digunakan untuk menjadi solvent pada tahap 1B Dan seterusnya sesuai dengan diagram XX yang telah disajikan diatas
Hasil akhir yang akan diukur adalah hasil ekstrak dari tahap 1C dan 1D
o Ekstrak yang dihasilkan diukur volume cairan totalnya, dititrasi, dan diukur massanya dengan neraca digital di dalam sebuah piknometer
o Titrasi dilakukan dua kali, pertama digunakan indikator PP, awalnya ekstrak berwarna kemerahan, lalu ditrasi dengan HCl menjadi warna orange muda.
o Setelah ekstrak menjadi warna orange muda, ekstrak diberikan indikator Mo dimana warna ekstrak akan mengalami perubahan ke warna orange yang lebih pekat. Titrasi dengan HCl dilanjutkan sampai warna ekstrak menjadi jingga.
o Catat volume HCl yang telah digunakan, lakukan titrasi dilakukan duplo untuk kedua hasil akhir.
V.2.5 Mendeteksi ion SO42- dalam hasil ekstrak pada metoda Cross-current dan Counter-current
a. Hasil ekstrak di tiap tahap yang telah dititrasi HCl dipindahkan ke dalam tabung reaksi b. Ekstrak yang telah ditempatkan dalam tabung reaksi tersebut dinetralken dengan NaOH
c. NaOH diberikan sampai larutan kembali berwarna merah muda d. Larutan tersebut diberikan BaCl2 sebanyak 3 tetes
e. Larutan dipanaskan dengan pemanas f. Endapan akan muncul bila ion SO4
2-
terdapat pada larutan tersebut
V.3.
Contoh Perhitungan
A. Standarisasi HCl ሾܪܥ݈ሿ =ሾܱܰܽܪሿݔ ܸ݈ݑ݉݁ ܱܰܽܪ (ݐ݅ݐݎܽ݊) ݒ݈ݑ݉݁ ܪܥ݈ ݕܽ݊݃ ݀݅ݐ݅ݐݎܽݏ݅ contoh : ሾܪܥ݈ሿ =0,103 ݔ 24,2 25 = 0,1 MB. Penentuan Jumlah Kalium dan Kalium Oksida dalam Abu
Contoh perhitungan diambil pada tahap ekstraksi 1 dengan metode cross-current 1. Jumlah mol karbonat
݊ ܥܱଷଶି = ሾܪܥ݈ሿݔܸ݈ݑ݉݁ ܪܥ݈ ݎܽݐܽ − ݎܽݐܽ ݀݁݊݃ܽ݊ contoh :
݊ ܥܱଷଶି = 0,1 ݔ 0,35 = 0,035 mmol
2. massa K2CO3 dalam 25 mL ekstrak ݉ܽݏݏܽ ܭଶܥܱଷ =݊ ܥܱଷ
ଶି ݔ ܯ
ܭଶܥܱଷ
1000 contoh :
݉ܽݏݏܽ ܭଶܥܱଷ = 0,035 ݔ 138 1000 = 0,005 gram 3. Massa K2CO3 dalam ekstrak
݉ܽݏݏܽ ܭଶܥܱଷ =݉ܽݏݏܽ ܭଶܥܱଷ݈݀ܽܽ݉ 25 ݉ܮ ݁݇ݏݐݎܽ݇ ݔ ݒ݈ݑ݉݁ ݁݇ݏݐݎܽ݇ 25 ݉ܮ contoh : ݉ܽݏݏܽ ܭଶܥܱଷ =0,005 ݔ 255 ݉ܮ 25 ݉ܮ = 0,049 gram 4. massa K2O dalam K2CO3 ݉ܽݏݏܽ ܭଶO = ܯ ܭଶO ܯ ܭଶܥܱଷݔ ݉ܽݏݏܽ ܭଶܥܱଷ݈݀ܽܽ݉ ݁݇ݏݐݎܽ݇ contoh : ݉ܽݏݏܽ ܭଶO = ଽସ ଵଷ଼ݔ 0,049 = 0,034 gram 5. massa K dalam K2CO3 ݉ܽݏݏܽ ܭଶO = 2ݔܯ ܭ ܯ ܭଶܥܱଷݔ ݉ܽݏݏܽ ܭଶܥܱଷ݈݀ܽܽ݉ ݁݇ݏݐݎܽ݇ contoh : ݉ܽݏݏܽ ܭଶO = 2 ݔ 39 138 ݔ 0,049 = 0,028 gram
6. Jumlah mol bikarbonat ݊ ܥܱଷଶି = ሾܪܥ݈ሿݔ(ܸ ܪܥ݈ ݀݁݊݃ܽ݊ ݉݁ݐ݈݅ ݎܽ݊݃݁ − ܸ ܪܥ݈ ݀݁݊݃ܽ݊ ) contoh : ݊ ܥܱଷଶି = 0,1 ݔ(1,4 − 0,35) = 0,1 x 1,05 = 0,105 mmol
7. Massa KHCO3 dalam 25 mL ekstrak
݉ܽݏݏܽ ܭܪܥܱଷ =݊ ܪܥܱଷ ି ݔ ܯ ܭܪܥܱଷ 1000 contoh : ݉ܽݏݏܽ ܭܪܥܱଷ =0,105 ݔ 100 1000 = 0,011 gram 8. Massa KHCO3 dalam ekstrak
݉ܽݏݏܽ ܭܪܥܱଷ =݉ܽݏݏܽ ܭܪܥܱଷ݈݀ܽܽ݉ 25 ݉ܮ ݁݇ݏݐݎܽ݇ ݔ ݒ݈ݑ݉݁ ݁݇ݏݐݎܽ݇ 25 ݉ܮ contoh : ݉ܽݏݏܽ ܭܪܥܱଷ =0,011 ݔ 255 25 ݉ܮ = 0,107 gram 9. Massa K2O dalam KHCO3 ݉ܽݏݏܽ ܭଶO = ܯ ܭଶO
2 ݔ ܯ ܭܪܥܱଷݔ ݉ܽݏݏܽ ܭܪܥܱଷ݈݀ܽܽ݉ ݁݇ݏݐݎܽ݇
݉ܽݏݏܽ ܭଶO = 94
200ݔ 0,107 = 0,050 gram 10. Massa K dalam KHCO3
݉ܽݏݏܽ ܭ = ܯ ܭ ܯܭܪܥܱଷݔ ݉ܽݏݏܽ ܭܪܥܱଷ݈݀ܽܽ݉ ݁݇ݏݐݎܽ݇ contoh : ݉ܽݏݏܽ ܭ = ଷଽ ଵݔ 0,107 = 0,042 gram 11. Massa K2O dalam abu
ܯܽݏݏܽ ܭଶO dalam abu = massa ܭଶO dalam ܭଶܥܱଷ+ ݉ܽݏݏܽܭଶO dalam ܭܪܥܱଷ contoh :
ܯܽݏݏܽ ܭଶO dalam abu = 0,034 + 0,050 = 0,084 gram 12. Persentase K2O dalam abu
%ܭଶO dalam abu = ܯܽݏݏܽ ܭଶO dalam abu
݉ܽݏݏܽ ܾܽݑ ݕܽ݊݃ ݀݅݁݇ݏݐݎܽ݇ݏ݅ ݔ 100%
contoh :
%ܭଶO dalam abu =0,084
50 ݔ 100%
= 0,168% 13. Massa K dalam abu
ܯܽݏݏܽ ܭ dalam abu = massa ܭ dalam ܭଶܥܱଷ+ ݉ܽݏݏܽ K dalam ܭܪܥܱଷ
ܯܽݏݏܽ ܭ dalam abu = 0,028 + 0,042 = 0,070 gram 14 Persentase K dalam abu
% ܭ dalam abu = ܯܽݏݏܽ ܭ dalam abu
݉ܽݏݏܽ ܾܽݑ ݕܽ݊݃ ݀݅݁݇ݏݐݎܽ݇ݏ݅ ݔ 100%
contoh :
% ܭ dalam abu =0,07
50 ݔ 100%
= 0,139%
C. Massa Jenis Ekstrak
ߩ ݁݇ݏݐݎܽ݇ = (݉ܽݏݏܽ ݁݇ݏݐݎܽ݇ + ݉ܽݏݏܽ ݅݃݊݉݁ݐ݁ݎ) − ݉ܽݏݏܽ ݅݃݊݉݁ݐ݁ݎ ݒ݈ݑ݉݁ ݅݃݊݉݁ݐ݁ݎ contoh : ߩ ݁݇ݏݐݎܽ݇ = 12,707 − 7,848 5 = 0,972 g/mL
Daftar Pustaka
Douglas, J.S. 1985. Advanced guide to hydrophonics (Soilless cultivation). Pelham Books Ltd, London. p.368
Geankoplis, Christie J.1993.Transport Processes and Unit Operations.USA : Prentice Hall.p.727-728
Harvey, David.2000.Modern Analytical Chemistry. USA : McGraw Hill.p 289 Li, Wenping, Carl Kiser, Quintin Richard.2005.Quality Test of Rice Hull Ash Filter