BAB 3
BAHAN DAN METODE PENELITIAN
3.1 Alat dan Bahan 3.1.1 Alat-Alat
Alat-alat yang digunakan adalah:
Nama Alat Merek
- Alat-alat Gelas Pyrex
- Neraca Analitis Ohaus
- Termometer Fisher
- Hot Plate Cimarec
- Magnetic Stirer -
- Oven Carbolite
- Indikator pH Universal Sartorius
- Desikator -
- Seperangkat alat SEM JSM-35 C Shumandju
- Seperangkat alat FTIR Shimadzu
3.2 Bahan-Bahan
Bahan-bahan yang digunakan adalah:
Bahan Merek
3.3.1 Pembuatan Larutan Pereaksi 3.3.1.1 Larutan HNO3 3,5%
Sebanyak 54,6 mL HNO3 64% ditambahkan 10 mg NaNO3 lalu diencerkan dengan akuades dalam labu ukur 1000 mL hingga garis tanda lalu dihomogenkan.
3.3.1.2 Larutan NaSO3 2%
Sebany ak 10 g NaSO3 dilarutkan dengan akuades dalam labu ukur 500 mL hingga garis tanda lalu dihomogenkan.
3.3.1.3 Larutan NaOH 2%
3.3.1.4 Larutan NaOH 17,5%
Sebanyak 87,5 g NaOH pellet dilarutkan dengan akuades dalam labu ukur 500 mL hingga garis tanda lalu dihomogenkan.
3.3.1.5 Larutan Na-Hipoklorit 1,75%
Sebanyak 72,9 mL Na-Hipoklorit 12% diencerkan dengan akuades dalam labu ukur 500 mL hingga garis tanda lalu dihomogenkan.
3.3.1.6 Larutan H2O2 10%
Sebanyak 167 mL H2O2 30%diencerkan dengan akuades dalam labu ukur 500 mL hingga garis tanda lalu dihomogenkan.
3.3.2 Penyiapan Serbuk Tandan Kosong Sawit (TKS)
Tandan kosong sawit dibersihkan dan dicuci dengan air bersih. Dikeringkan dibawah sinar matahari sampai kering. Tandan kosong sawit yang sudah kering dipotong-potong hingga menjadi serat halus.
3.3.3Isolasi α-selulosa dari Tandan Kosong Sawit (TKS)
disimpan dalam desikator (Ohwoavworhua, et. al., 2005). Selanjutnya α-selulosa dikarakterisasi dengan analisa FT-IR.
3.3.4 Pembuatan Nanoserat selulosa dari α selulosa
Sebanyak 4 gram alfa selulosa dimasukkan kedalam beaker glass yang berisi 300 ml aquadest, kemudian ditambahkan NaBr sebanyak 2 gr, selanjutnyaa ditambahkan TEMPO sebanyak 1 gr dibiarkan beberapa menit hingga terbentuk suspensi. Dan ditambahkan larutan buffer 10 sambil Dilakukan pengadukan selama 3 jam dan diukur pHnya 10,5 dan disesuaikan pH dengan menambahkan larutan buffer 10 secukupnya, kemudian dilakukan penyaringan. Diperoleh filtrat dan residu, filtrat dibuang dan kemudian residu ditambahkan aquadest sebanyak 500 mL, dihomogenizer selama 6 menit dengan kecepatan 7500 rpm kemudian disonifikasi selama 4 menit, dan selanjutnya disentrifugasi dengan kecepatan 8400 rpm selama 10 menit, setelah itu diperoleh nanoserat selulosa.
3.3.5 Analisis Gugus Fungsi Dengan Spektroskopi FTIR
Sampel diletakkan pada plat kea rah sinar infra merah lalu dijepit. Hasilnya akan diperoleh spectrum puncak absorbs infra merah dari sampel berupa plot bilangan gelombang (cm-1) dan persen transmitansi (%T) dimonitor dengan rentang bilangan gelombang 4000-500 cm-1
3.3.6 Analisis Permukaan Dengan SEM
pada mesin SEM (JSM-35C) untuk dilakukan pemotretan. Hasil pemotretan dapat diesuaikan dengan pembesaran yang diinginkan.
3.3.7 Analisis Permukaan Dengan TEM
Analisis morfologi nanoserat selulosa dilakukan dengan menggunakan alat TEM JEOL 1400 dengan tegangan sebesar 120 kV. Pertama-tama nanoserat selulosa ditetesi dengan cairan ammonium molibdat 2%, kemudian cairan yang terbentuk diperangkap dalam resin. Selanjutnya dilakukan pemotongan dengan menggunakan mikrogrid untuk memperoleh nanoserat selulosa tunggal. Nanoserat selulosa yang terbentuk dimasukkan ke dalam kisi karbon untuk dilakukan pengujian TEM. Dari analisis permukaan megunakan TEM dapat dihitung ukuran nanoserat selulosa dengan menggunakan persamaan 3.1 (Lu and Hseish, 2012).
������� �����
������� �������� ������=
3.4 Bagan penelitian
3.4.1 Penyiapan Tandan Kosong Sawit
Dicuci dengan air bersih
Direndam dengan air selama 2 jam
Dikeringkan di bawah sinar matahari selama 1 hari Digunting-gunting hingga menjadi serat halus Dihaluskan
Tandan Kosong Sawit
3.4.2 Isolasi Selulosa dari Tandan Kosong Sawit
Dimasukkan ke dalam beaker glass
Ditambahkan 1 L campuran HNO3 3,5% dan 10 mg NaNO2
Dipanaskan diatas hot plate sambil di aduk selama 2 jam pada suhu 90oC
Disaring dan residu dicuci hingga filtrat netral
Ditambahkan 375 NaOH 2% dan 375 mL Na2SO3 2% dan Dipanaskan selama 1 jam pada suhu 50oC
Disaring dan dicuci hingga filtrat netral
Diputihkan dengan 500 mL Na-Hipoklorit 1,75% selama 30 menit sambil di aduk
Disaring dan dicuci hingga filtrat netral
Ditambahkan 500mL NaOH 17,5% dan Dipanaskan selama 30 menit pada suhu 80oC Disaring dan dicuci hingga filtrate netral
Diputihkan dengan H2O2 10% selama 15 menit pada suhu 60oC
Disaring dan dicuci dengan aquadest
Dikeringkan didalam oven pada suhu 60oC
Disimpan dalam desikator (Ohwoavworhua, 2005)
3.4.3 Pembuatan Nanoserat Selulosa dari α-selulosa
Dimasukkan kedalam beaker glass yang berisi air sebanyak 300 ml
Ditambahkan NaBr sebanyak 2 g Ditambahkan NaOCl sebanyak 12,5 ml Ditambahkan TEMPO sebanyak 1 g Ditambahkan larutan buffer
Distirer selama 3 jam Disaring
Ditambahkan aqudest sebanyak 500 mL
Dihomogenisasi dengan kecepatan 7500 rpm selama 6 menit
Disonifikasi selama 4 menit
Disentrifugasi dengan kecepatan 8400 rpm selama 10 menit
Dikarakterisasi
BAB 4 4 g alfa selulosa
Residu
Nanoserat Selulosa
FTIR SEM TEM
BAB IV
HASIL DAN PEMBAHASAN 4.1. Hasil Penelitian
4.1.1 Hasil Isolasi α-Selulosa dari Tandan Kosong Sawit
Setelah melalui proses delignifikasi, pemutihan, dan pemurnian maka diperoleh α-selulosa yang berwarna putih. Dari 75 g serbuk tandan kosong sawit yang digunakan diperoleh 18,78 g selulosa. Hasil isolasi α-selulosa yang diperoleh dari penelitian ini dapat dilihat pada Gambar 4.1.
4.1.2 Hasil Nanoserat Selulosa dari α-Selulosa
Selulosa yang diperoleh selanjutnya disentrifugasi sehingga menghasilkan nanoserat selulosa yang berbentuk serbuk berwarna putih. Dari 4 g α-selulosa yang disentrifugasi pada waktu 10 menit diperoleh nanoserat selulosa sebanyak 1,5 g. Nanoserat selulosa yang dihasilkan tersebut dapat dilihat pada Gambar 4.2.
4.1.3 Hasil Analisis Gugus Fungsi Menggunakan FTIR
Spektroskopi FT-IR merupakan suatu teknik analisis yang dilakukan untuk mengetahui gugus fungsi dari suatu molekul dalam satu sampel. Pada penelitian ini telah dilakukan analisis gugus fungsi menggunakan spektroskopi FT-IR. Hasil analisis gugus fungsi α-selulosa dan nanoserat selulosa menggunakan spektroskopi FTIR dapat dilihat pada Tabel 4.1, Gambar 4.3.
Tabel 4.1 Bilangan Gelombang dari Gugus Fungsi Pada α - selulosa dan
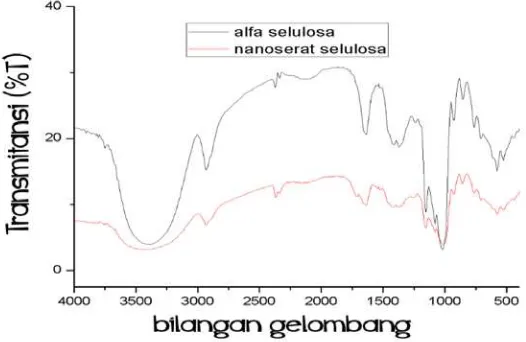
Gambar 4.3 Spektrum FTIR dari α-selulosa dan Nanoserat Selulosa 4.1.4 Hasil Analisis Morfologi Menggunakan SEM (Scanning Electron Microscopy)
Gambar 4.5 Hasil SEM dari Selulosa Tandan Kosong Sawit
Gambar 4.6 Hasil SEM dari nanoserat Selulosa 4.1.5 Hasil Analisa Morfologi Menggunakan TEM
4.2 Pembahasan
4.2.1 Isolasi α-selulosa dari Tandan Kosong Sawit
Sebelum dilakukan proses isolasi α-selulosa, pertama-tama tandan kosong sawit dibersihkan dan dicuci dengan air hingga bersih dan direndam selama 2 jam. Kemudian dikeringkan dibawah sinar matahari selama 1 hari. Selanjutnya dipotong kecil-kecil hingga menjadi serat halus.
Tahapan selanjutnya adalah proses isolasi α-selulosa dari tandan kosong sawit. Tahapan pertama dari proses isolasi ini adalah delignifikasi menggunakan NaOH 2%. Proses ini dilakukan untuk melarutkan lignin dan hemiselulosa. Pada tahap ini akan dihasilkan bubur selulosa yang berwarna coklat kehitaman sehingga perlu dilakukan proses pemutihan.
Pada proses pemutihan digunakan NaOCl 1,75%, proses ini juga dilakukan untuk menghilangkan sisa-sisa lignin (Silverio et al. 2012). Pada proses ini akan dihasilkan selulosa yang berwarna putih.
4.2.2 Isolasi Nanoserat Selulosa dari α-selulosa
Tahapan pertama pada proses isolasi nanoserat selulosa dari α-selulosa dengan penambahan TEMPO/NaBr/NaoCl diaduk dengan stirer selama 3 jam diukur pHnya dengan menambahkan Larutan Buffer yang berfungsi untuk menjaga pHnya agar tetap stabil. Selama oksidasi selulosa dengan penambahan TEMPO/NaBr/NaoCl terjadi penurunan pH, sehingga stabilitas pH dengan larutan buffer perlu dilakukan. Oksidasi penggunaan TEMPO yang larut dalam air mengkonversi hidroksil primer menjadi kelompok karboksilat. Dalam percobaan 1-3 jam larutan buffer digunakan untuk menstabilkan pH dari larutan antara 10,6 dan 10,4 (Thomas, 2014).
Tahapan selanjutnya adalah proses dihomogenisasi dengan kecepatan 7500 rpm selama 6 menit untuk menghomogenkan agar distribusinya merata. Dan kemudian disonifikasi selama 4 menit untuk memecah partikel lebih kecil (Griser et al. 1999).
Tahapan terakhir dari proses isolasi nanoserat selulosa adalah proses sentrifugasi dengan kecepatan 8400 rpm selama 10 menit untuk memisahkan residu dari filtratnya, yang berisi nanoserat selulosa berukiran 0-100 nm hingga diperoleh nanoserat selulosa kering berbentuk bening dengan massa sebesar 10% dari massa awal α-selulosa yang diisolasi.
4.2.3 Analisis Selulosa dan Nanoserat Selulosa Gugus Fungsi Menggunakan Spektroskopi FTIR
Dari spectrum FTIR selulosa terdapat pita yang melebar pada daerah serapan 3425 cm-1 yang menunjukkan adanya vibrasi regangan O-H dari alcohol dalam molekul selulosayang diikuti oleh vibrasi regangan C-H dari rantai alkane pada daerah serapan 2931 cm-1. Selain itu, puncak vibrasi juga terlihat pada serapan 1018 cm-1 yang menunjukkan adanya regangan C-O di dalam cincin selulosa. Puncak serapan pada daerah 1157 cm-1 menunjukkan adanya regangan C-O-C dari gugus eter pada ikatan glikosidik dan cincin piranosa dari selulosa. Sedangkan vibrasi ayunan C-H dari selulosa terdapat pada daerah serapan 856 cm-1.
C=O karbonil yang berasal dari gugus ester, yang diperkuat dengan vibrasi regangan C-O daeri ester pada daerah serapan 1018. Dari hasil analisa tersebut menunjukkan bahwa senyawa nanoserat selulosa telah terbentuk. Hal ini dibuktikan dengan munculnya puncak serapan untuk gugus C=O dan C-O yang merupakan ciri khas dari ester.
4.2.4 Analisis Morfologi menggunakan SEM dari Selulosa danNanoserat Selulosa
Adapun hasil SEM dari selulosa hasil isolasi dari tandan kosong sawit dari Gambar 4.4, menunjukkan morfologi permukaan sebelum dimodifikasi. Permukaan pada perbesaran 500 kali tampak serat lebih halus dan memiliki permukaan serat yang kecil.
Sedangkan hasil SEM dari Nanoserat selulosa TEMPO hasil dari isolasi dari tandan kosng sawit dari Gambar 4.5 , menunjukkan telah terjadi perubahan morfologi permukaan. Permukaan pada perbesaran 500 kali tampak serat lebih kasar, dan memiliki permukaan serat yang lebih besar daripada selulosa. Ini menunjukkan perubahan morfologi yang mendukung telah terjadi interaksi antara gugus hidroksil (OH) dari selulosa dan gugus karboksil dari TEMPO.
4.2.5 Analisis Morfologi menggunakan TEM
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Hasil Nanoserat selulosa dari α-selulosa dengan menggunakan oksidator TEMPO adalah berupa serat dan berwarna putih.
2. Penelitian ini memberikan karakteristik :
a. Pada analisis gugus fungsi FT-IR gugus menunjukkan adanya puncak serapan gugus O-H pada daerah bilangan gelombang 3425 cm-1 dan didukung oleh vibrasi gugus karbonil C=O pada daerah bilangan geombang 1743 cm-1.
b. Pada analisis permukaan menggunakan SEM menunjukkan bahwa permukaan selulosa tampak homogen, lebih teratur dan nanoserat selulosa telah bercampur.
c. Pada analisis ukuran partikel menggunakan TEM menunjukkan bahwa nanoserat selulosa memiliki ukuran diameter sekitar 31,04 nm.
5.2. Saran
1. Disarankan untuk peneliti selanjutnya melakukan sintesis selulosa dengan melakukan sejumlah variasi perbandingan massa selulosa dengan nanoserat selulosa