INTISARI
Terapi alternatif yang mulai digunakan untuk penyakit kanker adalah dengan daun mimba (Azadirachta indica A. Juss). Hasil penelitian sebelumnya fraksi protein daun mimba hasil pengendapan dengan amonium sulfat 30% dan 60% memiliki efek sitotoksik terhadap kultur sel HeLa. Tujuan dari penelitian ini adalah untuk mengetahui sitotoksisitas fraksi protein daun mimba FP10, FP20, FP30
dan FP40 terhadap kultur sel HeLa dan sel Vero.
Penelitian ini adalah penelitian eksperimental murni rancangan acak lengkap pola satu arah. Fraksi protein diendapkan menggunakan amonium sulfat dalam berbagai tingkat kejenuhan dan konsentrasi. Uji sitotoksisitas dilakukan terhadap sel HeLa dan sel Vero secara in vitro menggunakan metode MTT (3-(4,5-dimetil-tiazol-2-il)-2,5-dipheniltetrazolium bromide). Hasil uji berupa prosentase kematian sel. Analisis statistik dengan analisis probit dilakukan untuk mengetahui nilai LC50 dan uji t-independent sample untuk membandingkan
sitotoksisitas fraksi protein daun mimba terhadap sel HeLa dan sel Vero.
Hasil uji sitotoksisitas menunjukkan bahwa FP10, FP20, FP30 dan FP40
sitotoksik terhadap sel HeLa dan sel Vero. Nilai LC50 FP10, FP20, FP30 dan FP40
terhadap sel HeLa berturut-turut sebesar 1,5.107 µg/ml; 6.10-3 µg/ml; 3,7.10-13 µg/ml dan 1,8.10-2 µg/ml; sedangkan terhadap sel Vero berturut-turut sebesar 1,2.10-3 µg/ml; 1,2.104 µg/ml; 1,2.10-2 µg/ml dan 2,3.1011 µg/ml. Uji
t-independent sample menunjukkan bahwa seluruh fraksi protein daun mimba memiliki perbedaan sitotoksisitas yang tidak signifikan antara sel HeLa dan sel Vero. FP10, FP20, FP30 dan FP40 daun mimba tidak berpotensi untuk
dikembangkan sebagai antikanker.
Kata kunci : daun mimba, sitotoksisitas, fraksi protein, LC50,sel HeLa, sel Vero
ABSTRACT
Neem leaves (Azadirachta indica A. Juss) is now being used as alternative therapy for cancer. Previous research showed that protein fraction of neem leaves which were precipitated using ammonium sulphate in concentration of 30% and 60% had cytotoxic activity against HeLa cells. This research aim to investigate the cytotoxicity of protein fraction of neem leaves PF10, PF20, PF30, and PF40
against HeLa and Vero cells (normal cells).
This research was pure experimental research with the complete random and one way design. Protein fractions were precipitated with ammonium sulphate in various saturation grades. The cytotoxicity test was determined against HeLa cells and Vero cells in vitro using MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide) method. Data collected was cell death percentage. Data were statistically analysis by probit analysis to determined the LC50 values
and independent samples t-test was used to identify whether the protein fractions have selectivity to HeLa cells.
The result indicated that PF10, PF20, PF30, and PF40 of neem leaves show
cytotoxic activity to HeLa and Vero cells. LC50 of PF20, PF30, and PF40 against
HeLa cells are 1,5.107 µg/ml; 6.10-3 µg/ml; 3,7.10-13 µg/ml and 1,8.10-2 µg/ml respectively; whereas LC50 of PF10, PF20, PF30 and PF40 against Vero cells are
1,2.10-3 µg/ml; 1,2.104 µg/ml; 1,2.10-2 µg/ml and 2,3.1011 µg/ml. The results of independent samples t-test showed that all protein fraction of neem leaves have no significant difference of cytotoxicity between HeLa and Vero cells. In conclusion, PF10, PF20, PF30, and PF40 of neem leaves were not recommended to be developed
as anticancer.
Keywords: neem leaves, cytotoxicity, protein fraction, LC50, HeLa cells, Vero
cells
SITOTOKSISITAS FRAKSI PROTEIN DAUN MIMBA (Azadirachta indica A. Juss) FP10, FP20, FP30, DAN FP40 TERHADAP
KULTUR SEL HeLa
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Lestarining Wahyu Ndadari
NIM: 038114029
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2007
SITOTOKSISITAS FRAKSI PROTEIN DAUN MIMBA (Azadirachta indica A. Juss) FP10, FP20, FP30, DAN FP40 TERHADAP
KULTUR SEL HeLa
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Lestarining Wahyu Ndadari
NIM: 038114029
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2007
HALAMAN PERSEMBAHAN
Ia membuat segala sesuatu indah pada waktunya, bahkan
Ia memberi kekekalan dalam hati mereka. Tetapi manusia
tidak dapat menyelami pekerjaan yang dilakukan Allah
dari awal sampai akhir. Pengkhotbah 3 : 11
Ku persembahkan karyaku ini kepada: Tuhan Yesus Kristus atas Kasih dan KaryaNya yang luar biasa dalam
hidupku Bapak dan Ibu yang menyayangiku dengan seluruh dukungan, restu dan doa yang selalu menyertaiku Semua teman-teman dan Almamaterku
PRAKATA
Puji dan syukur kepada Tuhan Yang Maha Esa atas karunia dan
anugerahNya sehingga penulis dapat menyelesaikan skripsi yang berjudul
“Sitotoksisitas Fraksi Protein Daun Mimba (Azadirachta indica A. Juss) FP10,
FP20, FP30, dan FP40 terhadap Kultur Sel HeLa” sebagai salah satu syarat untuk
memperoleh gelar sarjana pada Fakultas Farmasi Universitas Sanata Dharma.
Penulisan skripsi ini tidak mungkin terwujud tanpa adanya bimbingan,
bantuan dan dukungan dari berbagai pihak yang senantiasa meluangkan waktu
dan pikirannya. Oleh karena itu, pada kesempatan ini penulis ingin mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Rita Suhadi, M.Si., Apt., selaku dosen dan dekan Fakultas Farmasi Universitas
Sanata Dharma yang bersedia berbagi ilmu dan pengalaman klinis.
2. Drs. A. Yuswanto, Ph.D., S.U., Apt., yang telah memberikan bimbingan,
pengarahan, dan semangat selama penelitian dan penyusunan skripsi.
3. Drs. Mulyono, Apt., yang bersedia berdiskusi dan memberikan saran sebagai
dosen penguji skripsi. yang bersedia meluangkan waktu dan memberikan
masukan dalam menyelesaikan permasalahan.
4. dr. Luciana Kuswibawati, M. Kes., yang memberikan saran sebagai dosen
penguji skripsi.
5. Ign. Y. Kristio Budiasmoro, M.Si. yang membantu dalam pengolahan statistik
dan determinasi tanaman.
6. Dosen dan karyawan Fakultas Farmasi yang telah banyak memberikan
sumbangan ilmu dan tenaga.
7. Kedua orang tua, Bapak Wahjudi dan Ibu J. Endang Lestari serta keluarga
besar atas doa, cinta, nasehat, semangat dan perhatian kepada penulis.
8. Bapak Rajiman, Mbak Yuli, Mbak Istini, Heni, Mas Dwi, segenap karyawan
dan staf Laboratorium Ilmu Hayati UGM yang telah banyak membantu dan
membimbing selama penelitian skripsi ini.
9. Nike, yang telah menjadi teman dan sahabat yang berharga yang Tuhan Yesus
anugerahkan bagi penulis dalam suka, duka, tangis dan tawa ceria.
10. Teman-teman PMK Apostolos yang menjadi keluarga untuk berbagi suka dan
keluh kesah, kekuatan yang menopang dan menarik kembali saat jauh
dariNya, dan semangat dalam pelayanan, dalam mereka kelembutan kasih
Tuhan terpancar.
11. Teman-teman Komunitas Tari Genta Rakyat atas kebersamaan yang indah
dalam perjalanan yang mengagumkan untuk menemukan jati diri. Dance with our Soul.
12. Leea, Vita, Sari, Lucy, Melon, Ana, Jenny (kelompok Mimba) dan Mila, Wati,
Ratih, Agnes (kelompok Teki) untuk diskusi, kerjasama, dan sebagai teman
seperjuangan suka maupun duka dalam menyelesaikan penyusunan skripsi ini.
13. Seluruh angkatan 2003 Fakultas Farmasi Universitas Sanata Dharma
khususnya kelas A kelompok B atas kebersamaan kita dalam setiap belajar di
kelas maupun di luar kelas dan praktikum yang penuh dengan tantangan,
ketegangan dan keceriaan.
14. Semua pihak yang telah memberikan dukungan baik moral maupun material
yang tidak dapat disebutkan satu persatu.
Penulis menyadari masih banyak kekurangan baik dalam isi, bahasa maupun
penulisan skripsi ini. Untuk itu, penulis mengharapkan koreksi dan saran dari
seluruh pembaca untuk lebih menyempurnakan tulisan ini. Penulis berharap
semoga skripsi ini bermanfaat dan memberikan sumbangan bagi ilmu
pengetahuan.
Penulis
INTISARI
Terapi alternatif yang mulai digunakan untuk penyakit kanker adalah dengan daun mimba (Azadirachta indica A. Juss). Hasil penelitian sebelumnya fraksi protein daun mimba hasil pengendapan dengan amonium sulfat 30% dan 60% memiliki efek sitotoksik terhadap kultur sel HeLa. Tujuan dari penelitian ini adalah untuk mengetahui sitotoksisitas fraksi protein daun mimba FP10, FP20, FP30
dan FP40 terhadap kultur sel HeLa dan sel Vero.
Penelitian ini adalah penelitian eksperimental murni rancangan acak lengkap pola satu arah. Fraksi protein diendapkan menggunakan amonium sulfat dalam berbagai tingkat kejenuhan dan konsentrasi. Uji sitotoksisitas dilakukan terhadap sel HeLa dan sel Vero secara in vitro menggunakan metode MTT (3-(4,5-dimetil-tiazol-2-il)-2,5-dipheniltetrazolium bromide). Hasil uji berupa prosentase kematian sel. Analisis statistik dengan analisis probit dilakukan untuk mengetahui nilai LC50 dan uji t-independent sample untuk membandingkan
sitotoksisitas fraksi protein daun mimba terhadap sel HeLa dan sel Vero.
Hasil uji sitotoksisitas menunjukkan bahwa FP10, FP20, FP30 dan FP40
sitotoksik terhadap sel HeLa dan sel Vero. Nilai LC50 FP10, FP20, FP30 dan FP40
terhadap sel HeLa berturut-turut sebesar 1,5.107 µg/ml; 6.10-3 µg/ml; 3,7.10-13 µg/ml dan 1,8.10-2 µg/ml; sedangkan terhadap sel Vero berturut-turut sebesar 1,2.10-3 µg/ml; 1,2.104 µg/ml; 1,2.10-2 µg/ml dan 2,3.1011 µg/ml. Uji
t-independent sample menunjukkan bahwa seluruh fraksi protein daun mimba memiliki perbedaan sitotoksisitas yang tidak signifikan antara sel HeLa dan sel Vero. FP10, FP20, FP30 dan FP40 daun mimba tidak berpotensi untuk
dikembangkan sebagai antikanker.
Kata kunci : daun mimba, sitotoksisitas, fraksi protein, LC50,sel HeLa, sel Vero
ABSTRACT
Neem leaves (Azadirachta indica A. Juss) is now being used as alternative therapy for cancer. Previous research showed that protein fraction of neem leaves which were precipitated using ammonium sulphate in concentration of 30% and 60% had cytotoxic activity against HeLa cells. This research aim to investigate the cytotoxicity of protein fraction of neem leaves PF10, PF20, PF30, and PF40
against HeLa and Vero cells (normal cells).
This research was pure experimental research with the complete random and one way design. Protein fractions were precipitated with ammonium sulphate in various saturation grades. The cytotoxicity test was determined against HeLa cells and Vero cells in vitro using MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide) method. Data collected was cell death percentage. Data were statistically analysis by probit analysis to determined the LC50 values
and independent samples t-test was used to identify whether the protein fractions have selectivity to HeLa cells.
The result indicated that PF10, PF20, PF30, and PF40 of neem leaves show
cytotoxic activity to HeLa and Vero cells. LC50 of PF20, PF30, and PF40 against
HeLa cells are 1,5.107 µg/ml; 6.10-3 µg/ml; 3,7.10-13 µg/ml and 1,8.10-2 µg/ml respectively; whereas LC50 of PF10, PF20, PF30 and PF40 against Vero cells are
1,2.10-3 µg/ml; 1,2.104 µg/ml; 1,2.10-2 µg/ml and 2,3.1011 µg/ml. The results of independent samples t-test showed that all protein fraction of neem leaves have no significant difference of cytotoxicity between HeLa and Vero cells. In conclusion, PF10, PF20, PF30, and PF40 of neem leaves were not recommended to be developed
as anticancer.
Keywords: neem leaves, cytotoxicity, protein fraction, LC50, HeLa cells, Vero
cells
DAFTAR ISI
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xvi
DAFTAR GAMBAR ... xviii
DAFTAR LAMPIRAN ... xix
ARTI SINGKATAN DAN ISTILAH ASING ... xx
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Permasalahan ... 3
2. Keaslian penelitian ... 3
3. Manfaat penelitian ... 4
B. Tujuan Penelitian ... 4
Tujuan umum ... 4
Tujuan khusus ... 4
BAB II PENELAAHAN PUSTAKA ... 5
A. Tanaman Mimba (Azadirachta indica A. Juss.) ... 5
1. Nama daerah ... 5
2. Deskripsi tanaman ... 5
3. Kandungan kimia ... 6
4. Penelitian terhadap tanaman mimba ... 6
B. Protein ... 7
1. Pengertian protein ... 7
2. Jenis protein berdasarkan kelarutan ... 8
3. Pemurnian protein ... 9
4. Pengukuran konsentrasi protein ... 11
C. Kanker ... 11
1. Definisi ... 11
2. Proses terjadinya kanker ... 13
3. Kanker leher rahim ... 18
D. Kultur Sel ... 19
1. Sel HeLa ... 20
2. Sel Vero ... 21
E. Uji Sitotoksisitas In vitro ... 21
F. Landasan Teori ... 23
G. Hipotesis ... 24
BAB III METODOLOGI PENELITIAN ... 25
A. Jenis dan Rancangan Penelitian ... 25
B. Variabel-variabel Penelitian ... 25
C. Definisi Operasional ... 26
D. Bahan atau Materi Penelitian ... 26
E. Alat-alat Penelitian ... 27
F. Tatacara Penelitian ... 28
1. Determinasi tanaman ... 28
2. Pengumpulan daun mimba ... 28
3. Sterilisasi alat dan bahan ... 28
4. Pembuatan fraksi protein dari daun mimba ... 28
5. Pengukuran konsentrasi protein total ... 31
6. Propagasi dan panen sel HeLa ... 31
a. Propagasi sel HeLa ... 31
b. Panen sel HeLa ... 32
7. Propagasi dan panen sel Vero ... 32
a. Propagasi sel Vero ... 32
b. Panen sel Vero ... 33
8. Uji sitotoksisitas terhadap sel HeLa dan sel Vero ... 33
a. Uji sitotoksisitas dengan metode MTT terhadap sel HeLa ... 33
b. Uji sitotoksisitas dengan metode MTT terhadap sel Vero ... 34
G. Analisis Hasil ... 35
BAB IV HASIL DAN PEMBAHASAN ... 36
A. Preparasi Fraksi Protein Daun Mimba ... 36
B. Penetapan Konsentrasi Fraksi Protein ... 38
C. Uji Sitotoksisitas Fraksi Protein ... 39
BAB V KESIMPULAN DAN SARAN ... 53
A. Kesimpulan ... 53
B. Saran ... 53
DAFTAR PUSTAKA ... 54
LAMPIRAN ... 58
BIOGRAFI PENULIS ... 102
DAFTAR TABEL
Halaman
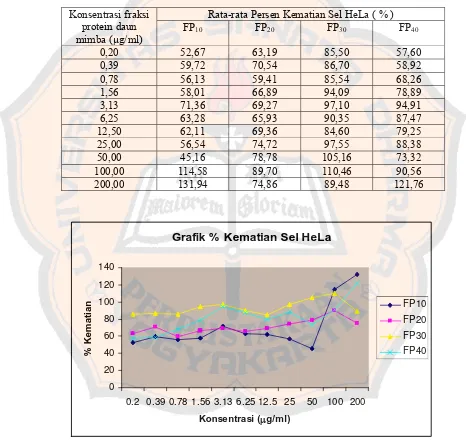
Tabel I. Prosentase kematian dari uji sitotoksisitas fraksi protein
terhadap sel HeLa ... 44
Tabel II. Prosentase kematian dari uji sitotoksisitas fraksi protein
terhadap sel Vero ... 46
Tabel III. Volume larutan ekstrak gubal protein daun mimba ... 58
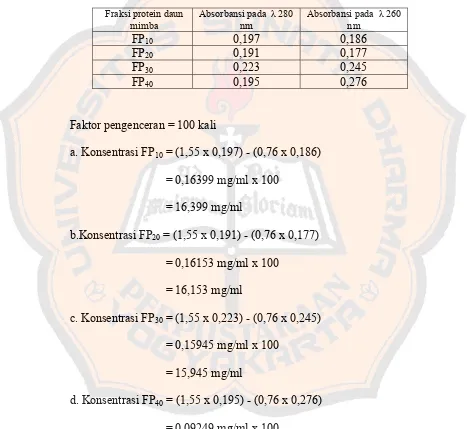
Tabel IV. Absorbansi fraksi protein pada panjang gelombang
280 nm dan 260 nm ... 60
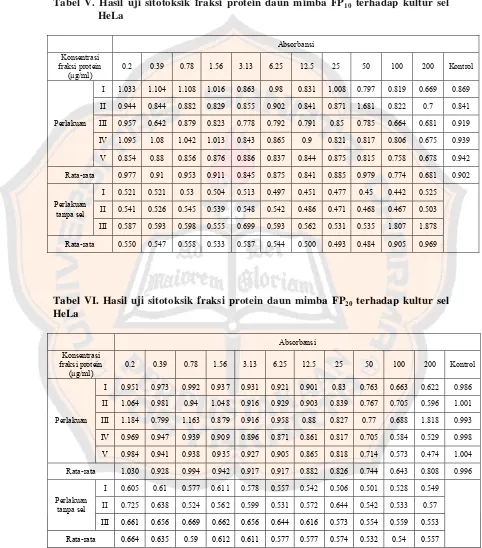
Tabel V. Hasil uji sitotoksik fraksi protein daun mimba FP10
terhadap kultur sel HeLa ... 61
Tabel VI. Hasil uji sitotoksik fraksi protein daun mimba FP20
terhadap kultur sel HeLa ... 61
Tabel VII. Hasil uji sitotoksik fraksi protein daun mimba FP30
terhadap kultur sel HeLa ... 62
Tabel VIII. Hasil uji sitotoksik fraksi protein daun mimba FP40
terhadap kultur sel HeLa ... 62
Tabel IX. Hasil uji sitotoksik fraksi protein daun mimba FP10
terhadap kultur sel Vero ... 63
Tabel X. Hasil uji sitotoksik fraksi protein daun mimba FP20
terhadap kultur sel Vero ... 63
Tabel XI. Hasil uji sitotoksik fraksi protein daun mimba FP30
terhadap kultur sel Vero ... 64
Tabel XII. Hasil uji sitotoksik fraksi protein daun mimba FP40
terhadap kultur sel Vero ... 64
DAFTAR GAMBAR
Halaman
Gambar 1. Reaksi reduksi MTT menjadi formazan ... 22
Gambar 2. Foto sel HeLa dan sel Vero tanpa perlakuan ... 41
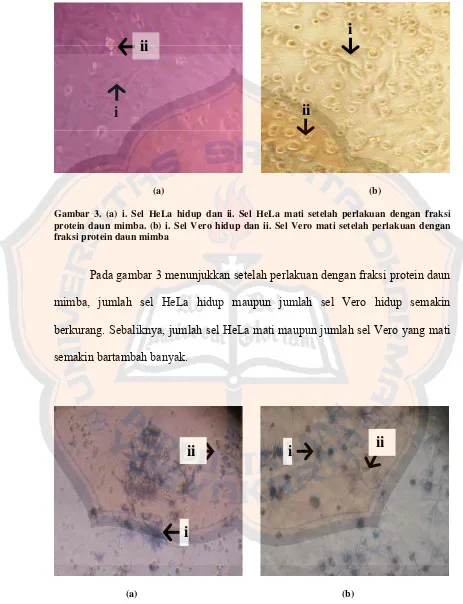
Gambar 3. Foto sel HeLa dan sel Vero setelah perlakuan ... 42
Gambar 4. Foto kristal formazan ungu ... 42
Gambar 5. Grafik prosentase kematian sel HeLa ... 44
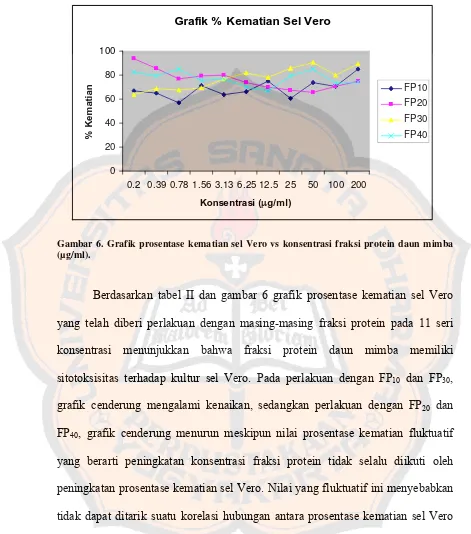
Gambar 6. Grafik prosentase kematian sel Vero ... 47
Gambar 7. Foto tanaman Azadirachta indica A. Juss ... 98
Gambar 8. Foto daun Azadirachta indica A. Juss ... 98
Gambar 9. Foto Hi-Mac Sentrifuge HITACHI SCP85 ... 99
Gambar 10. Foto ELISA reader SLT 340ATC ... 99
Gambar 11. Foto Mikroskop (Olympus IMT-2) ... 99
Gambar 12. Foto perlakuan dengan sel HeLa dalam 96 well plate 100
Gambar 13. Foto perlakuan dengan sel Vero dalam 96 well plate 100
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Jumlah penambahan amonium sulfat ... 58
Lampiran 2. Perhitungan konsentrasi protein ... 60
Lampiran 3. Absorbansi sel dengan metode MTT ... 61
Lampiran 4. Hasil analisis probit LC50 fraksi protein terhadap sel
HeLa ... 66
Lampiran 5. Hasil analisis probit LC50 fraksi protein terhadap sel
Vero ... 78
Lampiran 6. Hasil distribusi data dengan Uji Kolmogorov-Smirnov 90
Lampiran 7. Hasil analisis Uji t-independent sample ... 94 Lampiran 8. Foto tanaman dandaun mimba
(Azadirachta indica A. Juss) ... 98 Lampiran 9. Foto Hi-Mac Sentrifuge HITACHI SCP85H, ELISA
reader SLT 340ATC dan mikroskop
(Olympus IMT-2) ... 99
Lampiran 10. Foto hasil uji sitotoksik fraksi protein daun mimba
FP40 terhadap kultur sel HeLa dan sel Vero dalam
96 well plate ... 100 Lampiran 11. Surat determinasi tanaman ... 101
ARTI SINGKATAN DAN ISTILAH ASING
continous cell lines : sel yang berasal dari sel primer yang ditumbuhkan terus menerus
ELISA : Enzyme Link Immunosorbent Assay
FP10 (PF10) : fraksi protein (protein fraction) daun mimba hasil
pengendapan dengan amonium sulfat 10% jenuh
FP20(PF20) : fraksi protein (protein fraction) daun mimba hasil
pengendapan dengan amonium sulfat 20% jenuh
FP30(PF30) : fraksi protein (protein fraction) daun mimba hasil
pengendapan dengan amonium sulfat 30% jenuh
FP40(PF40) : fraksi protein (protein fraction) daun mimba hasil
pengendapan dengan amonium sulfat 40% jenuh
FBS : Foetal Bovine Serum
MTT : 3-(4,5-dimetil-tiazol-2-il)-2,5-dipheniltetrazolium bromide)
reagen stopper : reagen yang terdiri dari larutan SDS 10% dalam HCl 0,01N RPMI : Rosswell Park Memorial Institute
SDS : Sodium Dodesil Sulfat
tissue culture flask : tempat untuk menumbuhkan sel, berbentuk botol dengan leher bengkok
96 well plate : sumuran mikro yang terdiri dari 96 lubang tempat menanam sel pada uji sitotoksisitas
BAB I PENGANTAR
A. Latar Belakang
Kanker memiliki reputasi sebagai penyakit yang mematikan (Anonim,
2005b). Dalam daftar Badan Kesehatan Dunia penyakit kanker masuk dalam
urutan teratas dari kelompok penyakit. Di seluruh dunia penyakit kanker
menempati urutan kedua setelah penyakit jantung, sedangkan di Indonesia masuk
urutan keenam sebagai penyakit penyebab kematian. Penyakit kanker
diperkirakan diidap oleh 15 orang per 100.000 penduduk di dunia (Mulyadi,
1996). Sampai saat ini penyakit kanker masih menjadi ancaman, sementara obat
spesifik untuk menghentikan perkembangan sel kanker belum juga ditemukan
(Hartono, 1999).
Upaya pencegahan terus diusahakan dengan berbagai terapi seperti
pembedahan, radiasi dan sitostatika. Namun terapi-terapi tersebut membutuhkan
biaya yang besar dan menimbulkan efek samping yang merugikan bagi penderita
sehingga sebagian penderita lebih memilih terapi alternatif. Guna menakar
besarnya manfaat dan risiko terapi alternatif, sangat diperlukan pemahaman
tentang cara kerja terapi alternatif, termasuk penggunaan suplemen makanan
(senyawa antioksidan serta vitamin mineral) dan preparat herbal yang dapat
bekerja melawan kanker (Hartono, 1999).
Pada umumnya antineoplastik menekan pertumbuhan atau proliferasi sel
dan menimbulkan toksisitas. Suatu antikanker diharapkan memiliki toksisitas
selektif artinya menghancurkan sel kanker tanpa merusak sel jaringan normal
(Ganiswarna, 1995). Oleh sebab itu, penelitian-penelitian menggunakan
bahan-bahan yang berasal dari alam misalnya tanaman, diharapkan dapat menjadi terapi
antikanker alternatif yang bersifat selektif. Daun yang berasal dari tanaman
mimba (Azadirachta indica A. Juss) telah lama diketahui memiliki banyak manfaat dalam dunia kesehatan antara lain, sebagai antiinflamasi, antirematik,
antipiretik, penurun gula darah, antitukak lambung, hepatoprotektor,
imunopotensiasi, antifertilitas, antivirus, dan antikanker (Sukrasno, 2003).
Penelitian tentang efek sitotoksik fraksi protein daun mimba terhadap
kultur sel kanker telah dilakukan antara lain, fraksi total protein daun mimba
terhadap kultur sel Raji (Ariyani, 2004), terhadap kultur sel SiHa (Lusia, 2004),
terhadap kultur sel HeLa (Febriani, 2004), fraksi protein daun mimba hasil
pengendapan dengan amonium sulfat 30%; 60% dan 100% jenuh terhadap kultur
sel Myeloma (Hariadi, 2006), terhadap kultur sel SiHa (Candra, 2006), terhadap
kultur sel Raji (Robbyono, 2006), dan terhadap kultur sel HeLa (Suwanto, 2006).
Suatu senyawa dapat dinyatakan memiliki potensi untuk dikembangkan
sebagai antikanker apabila mempunyai nilai LC50 ≤ 20 µg/ml (Suffness and
Pezzuto, 1991) dan bersifat toksik selektif (Ganiswarna, 1995). Berdasarkan
penelitian yang dilakukan oleh Suwanto (2006) diketahui bahwa fraksi protein
daun mimba (Azadirachta indica A. Juss) hasil pengendapan dengan amonium sulfat 30%; 60% dan 100% jenuh memiliki efek sitotoksik terhadap kultur sel
HeLa terutama pada fraksi 30% dan 60% dengan nilai LC50 sebesar 1,0 µg/ml dan
antikanker. Namun, penelitian yang dilakukan oleh Suwanto (2006) tersebut perlu
dilakukan penelitian dengan fraksinasi yang lebih kecil dan seri konsentrasi yang
lebih banyak untuk mengetahui secara lebih spesifik fraksi protein yang bersifat
sitotoksik terhadap sel HeLa serta keselektifan efek sitotoksiknya terhadap sel
normal. Oleh karena itu, pada penelitian kali ini akan dilakukan fraksinasi
proteinnya dengan pengendapan menggunakan amonium sulfat dengan fraksi
yang lebih kecil yaitu 10% (FP10), 20%(FP20), 30% (FP30) dan 40% (FP40) jenuh
dengan harapan dapat diperoleh hasil yang lebih spesifik dan membandingkan
sitotoksisitasnya terhadap sel Vero (sel normal).
1. Permasalahan
a. Diantara fraksi protein daun mimba FP10, FP20, FP30 dan FP40, manakah
yang mempunyai sitotoksisitas terhadap sel HeLa dan sel Vero ?
b. Berapakah nilai LC50 dari fraksi protein daun mimba FP10, FP20, FP30 dan
FP40 terhadap sel HeLa dan sel Vero ?
c. Apakah fraksi protein daun mimba FP10, FP20, FP30 dan FP40 dapat
dikembangkan sebagai antikanker ?
2. Keaslian penelitian
Sebelumnya pernah dilakukan penelitian mengenai sitotoksisitas fraksi
protein daun mimba (Azadirachta indica A. Juss.) hasil pengendapan dengan amonium sulfat 30%, 60% dan 100% jenuh terhadap kultur sel HeLa (Suwanto,
2006). Sejauh yang diketahui penulis belum pernah dilakukan penelitian
3. Manfaat penelitian a. Manfaat teoritis
Penelitian ini dapat melengkapi dan memperkaya teori yang telah ada
mengenai khasiat, penggunaan, dan efek sitotoksisitas fraksi protein daun
mimba terhadap sel HeLa dan sel Vero yang berguna dalam kemajuan
bidang ilmu kefarmasian.
b. Manfaat praktis
Penelitian ini diharapkan dapat digunakan sebagai acuan yang mendukung
penemuan obat alternatif antikanker dari daun mimba.
B. Tujuan Penelitian Tujuan umum:
untuk mengetahui apakah fraksi protein daun mimba FP10, FP20, FP30 dan FP40
memiliki potensi untuk dikembangkan sebagai senyawa antikanker baru.
Tujuan khusus:
a. untuk mengetahui fraksi protein daun mimba FP10, FP20, FP30 dan FP40
yang mempunyai daya sitotoksisitas terhadap sel HeLa dan sel Vero
b. untuk mengetahui nilai LC50 dari fraksi protein daun mimba FP10, FP20,
FP30 dan FP40 terhadap sel HeLa dan sel Vero
c. untuk mengetahui apakah fraksi protein daun mimba FP10, FP20, FP30 dan
BAB II
PENELAAHAN PUSTAKA
A. Tanaman Mimba (Azadirachta indica A. Juss) 1. Keterangan botani tanaman mimba (Azadirachta indica A. Juss)
Tanaman mimba (Azadirachta indica A. Juss.) termasuk dalam divisi Spermatophyta, sub divisi Angiospermae, kelas Dicotyledonae, bangsa Meliales,
suku Meliaceae, marga Azadirachta, jenis Azadirachta indica A. Juss. Tanaman mimba memiliki sinonim yaitu Melia azadirachta Linn. Dalam bahasa Inggris atau Belanda tanaman ini dikenal dengan nama Margosa tree, Neem tree, atau Margosier.
(Backer and Backuizen van den Brink, 1963; 1965; Hutapea, 1993)
2. Nama daerah
Tanaman mimba (Azadirachta indica A. Juss.) memiliki nama daerah Jawa yaitu Imba, mimba, membha, mempheuh. Di wilayah Pasundan (Sunda)
dikenal dengan nama nimba, di Bali dan Nusa Tenggara dikenal dengan nama
intaran, dan di Madura dikenal dengan nama mimba, membha, atau mempheuh
(Sukrasno, 2003).
3. Deskripsi tanaman
Tanaman mimba berupa pohon dengan tinggi 10-15 meter. Batang tegak,
berkayu, bulat, permukaan kasar, percabangan simpodial, coklat. Daun majemuk,
berhadapan, lonjong, melengkung, tepi bergerigi, ujung lancip, pangkal
meruncing, pertulangan menyirip, panjang 5-7 cm, lebar 3-4 cm, tangkai panjang
8-20 cm, hijau. Bunga majemuk, berkelamin dua, di ujung cabang, tangkai
silindris, panjang 8-15 cm, kelopak hijau, benang sari silindris, putih kekuningan,
putik lonjong, coklat muda, mahkota halus, putih. Buah buni, bulat telur, hijau.
Biji bulat, diameter kurang lebih 1 cm, putih. Akar tunggang, coklat (Hutapea,
1993). Pohon mimba dapat tumbuh di berbagai ketinggian tempat, tetapi di atas
ketinggian 500 meter diatas permukaan laut sulit menghasilkan biji, hanya
daunnya yang tumbuh lebat (Kardinan dan Taryono, 2003).
4. Kandungan kimia
Sampai saat ini, setidaknya ada sembilan senyawa yang telah diisolasi dan
diidentifikasi dari daun mimba yaitu nimonol, nimbolida, 28-deoksi nimbolida, α
-linolenat, 14-15-epoksinimonol, 6-K-O-asetil-7-deasetil-mimosinol, melrasinol,
dan nimbotalin. Penelitian terhadap senyawa-senyawa yang terkandung dalam
daun mimba tersebut mendukung pemanfaatannya dalam dunia kesehatan
(Sukrasno, 2003).
5. Penelitian terhadap tanaman mimba
Beberapa penelitian untuk membuktikan kebenaran khasiat daun mimba
terutama protein daun mimba sebagai antikanker telah dilakukan antara lain,
penelitian sitotoksisitas fraksi total protein daun mimba terhadap kultur sel Raji
(Ariyani, 2004), terhadap kultur sel SiHa (Lusia, 2004), terhadap kultur sel HeLa
(Febriani, 2004), dengan kesimpulan bahwa fraksi protein daun mimba
mempunyai efek sitotoksik terhadap ketiga jenis sel kanker tersebut walaupun
belum dapat dinyatakan sebagai senyawa yang berpotensi untuk dikembangkan
µg/ml. Penelitian lebih lanjut yaitu sitotoksisitas fraksi protein daun mimba hasil
pengendapan dengan amonium sulfat 30%; 60% dan 100% terhadap sel Raji
(Robbyono, 2006) dengan kesimpulan fraksi 30% berpotensi untuk dikembangkan
sebagai antikanker karena nilai LC50 < 20 µg/ml, sedangkan pada penelitian
serupa terhadap sel HeLa (Suwanto, 2006), terhadap sel Myeloma (Hariadi, 2006)
dan terhadap sel SiHa (Candra, 2006) menyimpulkan bahwa fraksi 30% dan 60%
berpotensi untuk dikembangkan sebagai antikanker sebab nilai LC50 yang
diperoleh juga < 20 µg/ml.
B. Protein 1. Pengertian protein
Kata protein berasal dari protos atau proteos yang berarti pertama atau
utama. Protein merupakan komponen penting atau komponen utama sel hewan
atau manusia. Oleh karena sel itu merupakan pembentuk tubuh hewan maupun
manusia, maka protein yang terdapat dalam makanan berfungsi sebagai zat utama
dalam pembentukan dan pertumbuhan tubuh. Tumbuhan membentuk protein dari
CO2, H2O dan senyawa nitrogen. Protein adalah suatu polipeptida yang
mempunyai molekul besar dengan bobot molekul bervariasi antara 5000 sampai
jutaan (Poedjiadi, 1994). Protein terdapat dalam semua jenis zat hidup: tumbuhan,
hewan, dan jasad renik. Semua protein, selain mengandung karbon, hidrogen, dan
oksigen juga mengandung nitrogen dan sering mengandung belerang dan fosfor
Protein merupakan polimer kondensasi asam amino dengan penghilangan
unsur air dari gugus amino dan gugus karboksil. Asam amino pada protein
mempunyai konfigurasi-L dan ikatan amida hanya terbentuk antara gugus
amino-alfa dan gugus karboksil-amino-alfa dari asam amino yang bersangkutan. Beberapa
protein beracun mempunyai peran ekologi dalam melindungi tumbuhan dari
serangan mikroba. Protein beracun lain memberi harapan dalam pengobatan
kanker dan penyakit yang disebabkan virus. Fraksinasi ekstrak protein dapat
dilakukan dengan cara pengendapan menggunakan amonium sulfat (Robinson,
1991).
2. Jenis protein berdasarkan kelarutan
Beberapa jenis protein yang diklasifikasikan berdasarkan kelarutannya
antara lain:
1. albumin merupakan protein yang dapat larut dalam air dan larutan garam,
dapat terkoagulasi oleh panas. Larutan albumin di dalam air dapat
diendapkan dengan penambahan amonium sulfat hingga jenuh.
2. globulin memiliki sifat sukar larut dalam air murni, tetapi dapat larut
dalam larutan garam netral, misalnya larutan NaCl encer. Larutan globulin
dapat diendapkan oleh penambahan garam ammonium sulfat hingga
setengah jenuh. Globulin dapat diperoleh dengan jalan mengekstraksinya
dengan larutan garam (5%-10%) NaCl kemudian ekstrak yang diperoleh
diencerkan dengan penambahan air. Globulin akan mengendap dan dapat
3. histon merupakan protein yang mempunyai sifat basa dan dapat larut
dalam air. Pada proses hidrolisis menghasilkan banyak arginin dan lisin.
Histon terdapat di dalam inti sel dalam bentuk ikatan dengan asam nukleat.
4. protamin merupakan protein yang bersifat basa seperti histon, tidak
mengandung tirosin dan triptofan, tetapi mengandung banyak arginin
sehingga mempunyai kadar nitrogen antara 25%-30%. Protamin berikatan
dengan asam nukleat. Protamin larut dalam etanol 70%-80% tetapi tidak
larut dalam air serta etanol absolut.
5. skleroprotein tidak larut dalam air atau larutan garam, banyak
mengandung asam amino Glysin, Alanin dan Prolin.
(Poedjiadi, 1994; Murray dkk, 1995)
3. Pemurnian protein
Suatu jenis protein dari bahan alam dalam keadaan murni tidak mudah
diperoleh sebab molekul protein tidak stabil terhadap pemanasan serta pelarut
organik. Pemurnian protein diawali dengan pemilihan bahan alam yang akan
diproses berdasarkan kadar protein yang terkandung didalamnya yaitu yang
berkadar protein tinggi dan mudah diperoleh. Selanjutnya mengeluarkan protein
dari dalam bahan alam tersebut dengan cara memecahkan sel-sel jaringan secara
mekanik misal dengan cara menghancurkan dan melumatkannya dalam suatu alat
tertentu dan beberapa jenis protein dapat diperoleh dengan melarutkannya dalam
air atau pelarut lain. Dalam proses ini perlu dijaga agar temperatur dan pH larutan
tidak merusak protein. Pada temperatur 40°C protein mudah terdenaturasi, maka
beku pelarut yang digunakan. Disamping itu, protein juga sensitif terhadap asam
atau basa dengan konsentrasi tinggi, dan biasanya pemurnian protein dilakukan
pada pH mendekati netral dengan menggunakan larutan buffer tertentu (Poedjiadi,
1994).
Setelah diperoleh larutan yang berisi beberapa macam protein maka proses
selanjutnya ialah fraksinasi yaitu memisahkan masing-masing protein dalam
campuran secara fraksi demi fraksi. Dua cara yang biasa digunakan untuk proses
fraksinasi ini yaitu pengendapan dan kromatografi. Proses pengendapan protein
dapat dilakukan menggunakan amonium sulfat berkonsentrasi tinggi atau larutan
jenuh. Beberapa protein berbeda kelarutannya dalam konsentrasi garam yang
berbeda. Cara ini digunakan terutama bila diinginkan satu macam protein saja
sedangkan protein lain tidak diperlukan. Selain dengan garam proses pengendapan
protein dapat dilakukan dengan menyesuaikan pH titik isoelektrik protein yang
diinginkan. Pada titik isoelektrik kelarutan protein berkurang hingga minimum
dan protein yang diinginkan akan mengendap, sedangkan protein lain yang tidak
diinginkan tetap di dalam larutan. Protein dapat dipisahkan satu dari yang lain
dengan cara kromatografi. Kromatografi adsorpsi untuk pemurnian protein
dilakukan dengan menggunakan alumina atau kalsium fosfat sebagai adsorben.
Selain itu kromatografi penukar ion dapat digunakan pula untuk pemurnian
protein. Kolom kromatografi diisi dengan DEAE-selulosa, suatu penukar ion yang
mempunyai gugus dietilaminoetil yang terikat pada selulosa atau dengan penukar
kation yaitu CM-selulosa yang mempunyai gugus karboksimetil terikat pada
4. Pengukuran konsentrasi protein
Pada umumnya, metode pemurnian protein harus dilakukan pada
temperatur rendah, pada range 0-4°C. Temperatur rendah meminimalkan
degradasi protein selama pemurnian dengan menghalangi aktifitas protease
(enzim yang memecah ikatan peptida) dan mengurangi kemungkinan protein akan
terdenaturasi, atau membuka ikatannya (banyak protein yang sangat sensitif
terhadap panas). Pada pH netral tirosin, triptofan dan fenilalanin mengabsorpsi
sinar ultraviolet (UV) pada panjang gelombang 280 nm (Moran dkk, 1994;
Murray dkk, 1995).
C. Kanker 1. Definisi
Kanker adalah penyakit yang disebabkan adanya perbanyakan dan
penyebaran yang tidak terkontrol menjadi bentuk tubuh abnormal dari sel tubuh
itu sendiri. Kanker merupakan salah satu penyebab utama kematian di Negara
berkembang, setidaknya satu dari lima pada populasi di Eropa dan Amerika Utara
diperkirakan meninggal karena kanker (Rang dkk, 2003). Kanker ditandai oleh
pembelahan sel yang tidak terkontrol dan kemampuannya untuk menyerang
jaringan lain, baik melalui pertumbuhan langsung pada jaringan (invasi) atau
dengan migrasi sel ke jaringan yang lain (metastasis). Pertumbuhan yang tidak
sesuai aturan ini disebabkan oleh kerusakan DNA, menghasilkan mutasi pada gen
dari mutasi ini, baik yang diturunkan atau didapatkan, dapat menuntun ke
pembelahan sel yang tak terkendali dan pembentukan tumor (Anonim, 2005b).
Tumor menunjukkan suatu massa yang abnormal di jaringan, baik berupa
malignan (kanker) atau benigna (nonkanker). Tumor benigna tidak menyebar ke
bagian lain tubuh atau menyerang jaringan lain, dan jarang perawatannya untuk
bertahan hidup jika tidak secara kebetulan menekan struktur utama (vital). Tumor
malignan dapat menyerang organ lain, menyebar ke lokasi yang jauh (metastasis)
dan menjadi perawatan untuk bertahan hidup (Anonim, 2005b). Istilah kanker,
neoplasma malignan dan tumor malignan merupakan sinonim. Keduanya
dibedakan dari tumor benigna oleh dediferensiasi, keinvasifan dan kemampuan
metastasis (penyebaran ke bagian lain dari tubuh). Kedua tumor baik benigna
maupun malignan menunjukkan proliferasi yang tidak terkendali. Sel kanker
memiliki karakteristik yang membedakannya dari sel normal, yaitu sel kanker
mengalami pertumbuhan dan pembelahan sel yang tidak terkendali oleh regulasi
pembelahan sel dan pertumbuhan jaringan yang normal, adanya gangguan
diferensiasi dan kehilangan fungsi pada sel kanker, sel kanker mampu melakukan
invasif dan metastasis (Rang dkk, 2003).
Untuk menghambat metastasis kanker, perlu diketahui cara sel tersebut
menyebar. Ada dua cara sel kanker ber-metastasis: melalui angiogenesis
(pembentukan pembuluh darah yang baru) dan penghancuran kolagen yang
merupakan kerangka sel normal. Dengan demikian metastasis akan dapat
diperbaiki oleh tubuh sendiri dengan memanfaatkan makanan tertentu (Hartono,
1999).
Pendekatan utama dalam pengobatan kanker yaitu pembedahan, irradiasi,
dan kemoterapi. Penggunaan masing-masing pengobatan tersebut tergantung pada
tipe tumor dan tingkat perkembangannya (Rang dkk, 2003).
2. Proses terjadinya kanker
Sel normal berubah menjadi sel kanker karena satu atau lebih mutasi pada
DNA-nya baik secara diturunkan, bukan kanker itu sendiri yang diturunkan
melainkan gen yang telah termutasi dan mudah berkembang menjadi kanker
maupun dengan cara didapat dari luar sel akibat pemaparan zat kimia,
ko-karsinogen, dan lain-lain. Perkembangan kanker merupakan proses yang rumit,
melibatkan tidak hanya satu perubahan genetik tetapi juga yang lain, seperti
faktor-faktor epigenetik (aksi hormonal, ko-karsinogen dan efek pemacu tumor)
yang tidak hanya menghasilkan kanker itu sendiri melainkan dengan
meningkatkan kemungkinan mutasi genetik yang akan menimbulkan kanker
(Rang dkk, 2003).
Sel kanker mempunyai antigen pada permukan sel yang dapat dikenali dan
bereaksi dengan sistem imun inang sehingga mampu mencegah pertumbuhan
tumor yang tak terkendali. Teori ini dikenal sebagai immunosurveillance (pemantauan imun). Teori ini bermula dari percobaan yang dilakukan oleh Paul
Ehrlich yang mengamati bahwa hewan dengan pertumbuhan tumor bervirulensi
rendah mengalami penurunan pertumbuhan tumor setelah dilakukan inokulasi sel
yang dapat dikenali sebagai sesuatu yang abnormal oleh inang. Penelitian
dilanjutkan oleh Lewis Thomas yang memberikan teori penolakan allograft menggambarkan mekanisme utama dalam pertahanan alami terhadap neoplasia.
Berdasarkan penelitian-penelitian tersebut, Macfarlane Burnet memberikan teori
immunosurveillance yang berpusat adanya antigen yang tergabung pada sel tumor (Schwartz, 1991; Dasgupta, 1992).
Teori tersebut menyatakan bahwa sel efektor pada sistem imun secara aktif
beredar di dalam tubuh untuk mengenali dan membasmi sel-sel tumor yang mulai
terbentuk. Penelitian pada tahun 1970 mampu menemukan dan mengidentifikasi
adanya sel T, sel ini menjadi sel efektor yang diduga memperantarai dalam
immunosurveillance. Lebih dari dua dekade terakhir, data-data memunculkan pendapat bahwa konstituen sistem imun seperti sel natural killer (NK) dan jaringan cytokine mampu memberi pertahanan terhadap kanker (Ichim, 2005).
Aktivitas sel NK menjadi tanda penunjuk pada beberapa tipe tumor.
Sel-sel NK terlibat baik secara langsung maupun tidak langsung dalam pemantauan
kemunculan tumor dan mikrometastasis. Teori ini kemudian dibuktikan dengan
data yang menunjukkan bahwa onkogen tertransfeksi fibroblas dapat lisis secara
selektif oleh sel NK bila dibandingkan dengan kontrol yang tidak tertransfeksi.
Mekanisme secara tepat sel NK dalam immunosurveillance belum diketahui secara pasti. Berkaitan dengan efek sitotoksik secara langsungnya, kemungkinan
sel NK mengaktifkan sel lain dalam sistem imun dengan cara memperlengkapinya
(TNF)-α, interferon (IFN)- dan granulocyte-macrophage colony-stimulating factor (GM-CSF). Pada kenyataanya, sekresi IFN- oleh sel NK dapat mempengaruhi pembentukan respon imun tipe Th1 terhadap agen patogen
maupun tumor terinduksi 3-methylcholanthrene (MCA) (Ichim, 2005).
Langkah awal respon imun memerlukan cytokine yang dihasilkan oleh
sel-sel T-helper. Perbedaan cytokine yang dihasilkan oleh sel-sel menentukan tipe respon
imun. Respon imun yang diperantarai sel membutuhkan cytokine Th1, sedangkan
respon imun yang diperantarai antibodi membutuhkan cytokine Th2. Sel T-helper
yang terdiferensiasi menjadi sel Th1 mensekresikan IFN- dan sedikit interleukin (IL)-2 dan IL-12, sedangkan sel Th2 mensekresikan IL-10, IL-4, dan sedikit IL-5.
Namun, tumor memiliki beberapa cara baik spesifik maupun non-spesifik untuk
menghindari respon Th1. Tumor mensekresikan sejumlah agen, termasuk
transforming growth factor (TGF)- , IL-10 dan prostaglandin E-2, yang menunjukkan meningkatkan respon imun Th2 ketika menekan respon imun Th1.
Hal ini telah ditunjukkan bahwa jaringan cytokine dari beberapa pasien kanker
cenderung mengarah ke Th2. Pasien-pasien tersebut menunjukkan peningkatan
cytokine Th2 atau penurunan cytokine Th1 baik tumor sistemik maupun lokal.
Penelitian mengenai tumor yang mengembangkan beberapa cara untuk
menghindari respon Th1 sesuai dengan pengertian immunosurveillance. Fakta bahwa malignan memiliki banyak cara dalam menghindari respon Th1
menunjukkan bahwa kemampuan untuk menghindari respon ini memberikan
keuntungan pertahanan pada sel malignan, yang selanjutnya menunjukkan bahwa
Cytokine Th1 IFN- berfungsi sebagai antitumor baik secara langsung
maupun tidak langsung. Serangkaian penelitian menunjukkan arti penting IFN-
dalam membasmi tumor awal dengan adanya peningkatan keberhasilan
karsinogenesis saat tidak ada IFN- . IFN- menghambat pertumbuhan tumor
dengan mempengaruhi proliferasi, apoptosis dan angiogenesis. IFN- juga
mempunyai efek antitumor tidak langsung dengan memacu respon imun
antitumor yang efektif. Sebagai tambahan dalam mempengaruhi keseimbangan
cytokine Th1-Th2, IFN- mampu mengaktifkan makrofag sitotoksik, sel-sel NK
dan sel-sel T NK (Ichim, 2005).
Bukti dari prinsip tipe respon imun yang tidak tepat akan meningkatkan
pertumbuhan tumor telah dibuktikan pada awal 1907 oleh Flexner dan Jobling,
yang menunjukkan bahwa injeksi sel tumor autologous mati meningkatkan pertumbuhan tumor yang ada lebih dulu. Secara umum, Th2 membawa respon
antibodi ke tumor yang tidak terlindungi dan mendukung perkembangan tumor
dengan menghambat respon imun yang diperantarai sel Th1. Namun, paham
bahwa respon imun yang diperantarai antibodi dapat merugikan pada kanker telah
diusulkan lama sebelum Mossman dan Coffman menunjukkan paradigma
Th1-Th2 pada tahun 1986. Pada tahun 1950-an Kaliss mempopulerkan istilah
”immunological enhancement” untuk menggambarkan peningkatan pertumbuhan tumor oleh antibodi non-sitotoksik. Teori ini menyebutkan bahwa antibodi
berikatan dengan sel tumor, melapisi atau menutup epitop sel tumor dan kemudian
dengan imun dan tetap bisa tumbuh dan berkembang, meskipun hal ini belum
pernah dibuktikan dengan percobaan (Ichim, 2005).
Ada dua kategori utama perubahan genetik yang dapat mengakibatkan
munculnya kanker, yaitu:
Aktivasi proto-onkogen menjadi onkogen
Proto-onkogen adalah gen yang secara normal mengendalikan pembelahan sel,
apoptosis, dan diferensiasi tetapi dapat berubah menjadi onkogen oleh adanya aksi
virus atau karsinogen.
Inaktivasi gen penekan tumor
Sel normal mengandung gen yang mempunyai kemampuan untuk menekan
perubahan malignan yang disebut gen penekan tumor (anti-onkogen) dan
sekarang terdapat bukti bahwa mutasi terhadap gen ini terlibat dalam
pembentukan kanker yang berbeda-beda. Kehilangan fungsi dari gen penekan
tumor dapat menjadi peristiwa penting dalam karsinogenesis (Rang dkk, 2003).
Kanker akan muncul bila DNA sel normal mengalami kerusakan sehingga
menyebabkan mutasi genetik. Kalau ini tidak segera dikoreksi, perbanyakan sel
yang DNA-nya rusak tersebut potensial menghasilkan sel kanker. Padahal
perbanyakan sel dimaksudkan untuk pemulihan sel-sel yang aus atau rusak
(Hartono, 1999).
Tingkatan perubahan sel pada pertumbuhan kanker adalah sebagai berikut:
b. metaplasi yaitu perubahan epitel suatu jenis jaringan dewasa menjadi jaringan lain yang juga dewasa.
c. displasi yaitu perubahan sel dewasa ke arah kemunduran dalam hal bentuk, besar dan orientasinya. Masih bersifat reversibel.
d. anaplasi yaitu perubahan serupa displasi yang menyimpang lebih jauh dari normal. Merupakan suatu ciri tumor ganas yang sangat ireversibel.
e. karsinoma insitu yaitu gambaran sel menjadi sangat atipik namun belum terdapat pertumbuhan infiltratif.
f. invasi yaitu sel kanker telah menembus lapisan basal jaringan (Kuswibawati, 2000).
3. Kanker leher rahim
Kanker servik merupakan suatu bentuk malignan pada leher rahim
(servik). Kanker leher rahim merupakan jenis kanker paling banyak kedua di
dunia yang menyerang wanita dan peringkat ketiga kanker yang dapat
menyebabkan kematian setelah kanker payudara dan kanker paru-paru. Kanker ini
menyerang 16 per 100.000 orang wanita dan menyebabkan kematian 9 per
100.000 setiap tahunnya (Anonim, 2007a). Uji sitologi cervical (Pap smear) menunjukkan identifikasi dan penghilangan lesi prekanker (Anonim, 2005b).
Gejala klinik kanker leher rahim adalah keputihan yang tidak gatal, nyeri dan
perdarahan sehabis senggama, anemia serta gejala-gejala lain yang ditimbulkan
pada metastasis jauh (Fenty, 2000).
Virus (HPV) pada stadium ini merupakan virus yang beresiko rendah dalam arti tidak selalu berkembang menjadi kanker tetapi bisa juga menjadi virus beresiko
tinggi menyebabkan kanker leher rahim. Apabila kanker leher rahim dideteksi
lebih dini, maka kanker ini dapat diobati tanpa mempengaruhi kesuburan
(Anonim, 2007a).
Kanker leher rahim atau karsinoma servik uteri paling sering ditemukan di
antara tumor ganas ginekologik, dan umumnya paling banyak ditemukan pada
wanita berusia 31-60 tahun (Fenty, 2000). Lebih dari 90% kasus kanker leher
rahim disebabkan oleh Human Papilloma Virus (HPV) terutama tipe 16 dan 18. Human Papilloma Virus (HPV) tipe 16 dan 18 mengandung dua macam gen yaitu E6 dan E7 yang menghambat p53 dan Rb. Gen p53 dan Rb merupakan gen
penekan tumor yang ada di dalam tubuh manusia. Gen p53 terlibat dalam regulasi
apoptosis (bunuh diri sel) dan Rb bertanggung jawab untuk menghentikan siklus
sel pada fase G1. Pada saat fungsi Rb melemah, sel melanjutkan siklus ke fase S
dan mengalami mitosis sempurna, kemudian menghasilkan proliferasi sel dan dari
hal ini menyebabkan adanya pembentukan neoplastik (Anonim, 2007a).
D. Kultur Sel
Kultur sel yang baru diisolasi dari suatu jaringan dan kemudian
cell line) atau berubah menjadi continuous cell line. Sel normal dapat mengalami perubahan menjadi continuous cell line tanpa menjadi malignan, sedangkan tumor malignan dapat tumbuh pada media kemudian mengalami perubahan dan menjadi
lebih atau kurang tumorigenik. Keuntungan penggunaan continuous cell line adalah lebih cepat tumbuh sehingga kepadatan populasi sel lebih tinggi,
membutuhkan serum yang lebih rendah dan cukup mudah perawatannya pada
media sederhana, serta memiliki kemampuan untuk tumbuh dalam suspensi.
Kerugiannya meliputi ketidakstabilan kromosomal yang lebih besar, adanya
penyimpangan dari fenotip donor, dan terjadi kehilangan penanda khusus jaringan
(Freshney, 1986).
1. Sel HeLa
HeLa cell line merupakan continouous cell line yang tumbuh sebagai sel yang semi melekat. HeLa cell line diturunkan dari sel epitel kanker leher rahim (cervix) manusia. Sel ini diisolasi dari seorang wanita penderita kanker leher rahim bernama Henrietta Lacks berusia 31 tahun, yang meninggal pada tahun
1951 akibat kanker yang dideritanya. HeLa cell line ini cukup aman dan umum digunakan untuk kepentingan kultur sel. Sel HeLa merupakan cell line cervix intraepitel (Cervical Intraepithelial Carcinoma) akibat infeksi HPV 18 (Widiyani, 2005).
Sel HeLa diketahui dapat hidup dan berkembang dengan sangat baik
dalam kultur buatan di laboratorium. Kultur sel HeLa mengalami proliferasi yang
sangat cepat, bahkan jika dibandingkan dengan jenis sel kanker yang lain. Sel-sel
bertambah pendeknya telomer-telomer yang mengakibatkan penuaan dan bahkan
kematian sel. Sel HeLa mudah menginvasi atau mengkontaminasi kultur sel lain
dalam satu laboratorium yang sama (Anonim, 2007b).
HeLa cell line merupakan immortal cell line yang digunakan dalam penelitian dibidang kesehatan seperti uji antitumor, uji sitotoksisitas, biologi sel,
dan kemampuan invasi bakteri. Sel ini dapat dikultur menggunakan media RPMI
1640. Media RPMI 1640 mengandung nutrisi yang dibutuhkan oleh sel seperti
asam amino, vitamin, garam-garam anorganik dan glukosa (Freshney, 1986).
2. Sel Vero
Vero epithelial cell line ditemukan pertama pada tahun 1962 oleh Y. Yasumura dan Y. Kawakita di Universitas Chiba di Chiba, Jepang. Sel Vero
diambil dari ginjal kera dewasa (jenis African Green Monkey) yang sehat. Walaupun sering digunakan dalam tranfections dan produksi vaksin, sel Vero juga sering digunakan untuk mendeteksi verotoksin (sekelompok toksin yang
berhubungan yang dihasilkan oleh beberapa strain Escherichia coli yang merupakan penyebab utama hemorrhagic colitic dan sindrom hemolytic uremic pada manusia) (Anonim, 2006b).
E. Uji Sitotoksisitas In Vitro
Uji untuk identifikasi agen kemoterapetik kanker yang baru biasanya
dilakukan pada hewan percobaan yang mempunyai kesamaan sifat dengan
manusia. Namun, ada beberapa pertimbangan yang menyebabkan kecenderungan
lain, tes in vitro lebih murah dibanding in vivo, ada perbedaan proses fisiologis antara hewan percobaan dan manusia, dan adanya pertimbangan moral di dalam
penggunaan hewan sebagai objek penelitian (Freshney, 1986).
Uji MTT (3-(4,5-dimetil-tiazol-2-il)-2,5-dipheniltetrazolium bromide)
didasarkan pada aktivitas mitokondria, yang diinterpretasikan sebagai tolok ukur
kelangsungan hidup sel. Pada uji MTT, garam tetrazolium,
3-(4,5-dimetil-tiazol-2-il)-2,5-dipheniltetrazolium bromide secara aktif akan diabsorpsi ke dalam sel
hidup dan direduksi dalam mitokondria sel membentuk suatu produk formazan
berwarna ungu. Produk tersebut terakumulasi di dalam sel karena tidak bisa keluar
menembus membran sel. Dengan penambahan DMSO, isopropanil, atau solven
lain yang cocok, produk formazan ungu yang terbentuk tadi baru dapat larut atau
dibebaskan dan siap diukur dengan metode kolorimetri (Barile, 1997).
N
Gambar 1. Reaksi reduksi MTT menjadi formazan
Kematian sel merupakan respon uji sitotoksisitas maka konsentrasi yang
menimbulkan kematian pada 50% populasi pada sel dalam waktu yang spesifik
concentration atau LC50 (Cassaret and Doull, 2001). Semakin kecil harga LC50 suatu senyawa berarti senyawa tersebut semakin besar sitotoksisitasnya.
F. Landasan Teori
Penyakit kanker merupakan penyakit yang telah menjadi ancaman di
seluruh dunia, sementara obat spesifik untuk menghentikan perkembangan sel
kanker belum juga ditemukan. Tetapi upaya pencegahan terus diusahakan dengan
terapi alternatif obat antikanker yang berasal dari tanaman.
Tanaman mimba merupakan salah satu tanaman yang diyakini mempunyai
khasiat untuk mengobati kanker. Fraksi protein daun mimba ternyata dapat
memberikan efek sitotoksik terhadap beberapa tipe sel kanker termasuk sel HeLa.
Sel HeLa dapat hidup dan berkembang sangat baik dalam kultur buatan di
laboratorium, diakui aman untuk digunakan dalam kultur sel, dan mampu
memberikan respon yang cukup baik terhadap aktivitas dari senyawa-senyawa
yang diujikan.
Beberapa penelitian tentang sitotoksisitas fraksi protein daun mimba
terhadap sel HeLa sebagai subyek uji telah banyak dilakukan. Dari penelitian
Suwanto (2006) diketahui bahwa fraksi protein hasil pengendapan amonium sulfat
30% dan 60% memiliki nilai LC50 yang berpotensi untuk dikembangkan sebagai
senyawa antikanker. Diduga bahwa protein yang berperan sebagai antikanker
berada terutama antara kedua fraksi protein tersebut sehingga dimungkinkan
untuk memfraksinasi protein kedalam konsentrasi yang lebih kecil lagi dengan
(FP10), 20%(FP20), 30% (FP30) dan 40% (FP40). Dengan demikian, diharapkan
dapat diketahui pada fraksi mana protein yang memiliki potensi sebagai
antikanker tersebut paling banyak terendapkan dan kespesifikan protein yang
bersifat antikanker. Namun, fraksi protein daun mimba belum pernah dicobakan
pada sel normal (sel Vero). Jika ternyata tidak menimbulkan kerusakan pada sel
normal (sel Vero), fraksi protein daun mimba dapat diajukan sebagai alternatif
obat antikanker baru. Hal-hal tersebutlah yang mendasari dilakukan penelitian
fraksinasi protein daun mimba menjadi lebih kecil lagi untuk dilihat keberadaan
protein yang berpotensi untuk dikembangkan menjadi senyawa antikanker.
G. Hipotesis
Fraksi protein daun mimba (Azadirachta indica A. Juss) FP10, FP20, FP30 dan FP40 memiliki efek sitotoksik terhadap sel HeLa dan berpotensi untuk
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian eksperimental murni sederhana tunggal dengan rancangan
penelitian acak lengkap pola searah.
B. Variabel-variabel Penelitian 1. Variabel bebas
Konsentrasi fraksi protein daun Azadirachta indica A. Juss FP10, FP20, FP30 dan FP40.
2. Variabel tergantung
Prosentase kematian sel HeLa dan sel Vero pada masing-masing kultur sel.
3. Variabel pengacau terkendali
a. Medium tumbuh sel dikendalikan dengan menggunakan medium RPMI
1640 untuk sel HeLa dan medium M199 untuk sel Vero.
b. Tempat tumbuh dan waktu pemanenan daun mimba dikendalikan dengan
memanen daun pada tempat dan waktu yang sama.
c. pH dan suhu pembuatan fraksi protein, dikendalikan pada pH 7,2 dan suhu
4oC.
4. Variabel pengacau tak terkendali
Kematian sel HeLa dan sel Vero secara alami.
C. Definisi Operasional
1. Uji sitotoksisitas adalah uji toksisitas secara in vitro menggunakan kultur sel. 2. Fraksi protein adalah protein yang didapat dari ekstrak gubal daun mimba
dengan pengendapan menggunakan amonium sulfat.
3. Lethal Concentration (LC50) adalah konsentrasi fraksi protein daun mimba yang dapat mengakibatkan kematian 50% populasi sel HeLa maupun sel Vero.
D. Bahan atau Materi Penelitian
1. Bahan utama yang digunakan dalam penelitian ini adalah daun segar tanaman
mimba (Azadirachta indica A. Juss). Daun mimba diambil dari tanaman mimba (Azadirachta indica A. Juss) yang tumbuh di pekarangan Laboratorium Hayati LPPT Unit III, Universitas Gadjah Mada, Yogyakarta,
pada bulan Juni 2006. Daun mimba diambil pada saat tanaman mimba belum
berbunga dan berbiji.
2. Kultur sel HeLa dari stok Laboratorium Ilmu Hayati Universitas Gadjah Mada
3. Kultur sel Vero dari stok Laboratorium Ilmu Hayati Universitas Gadjah Mada
4. Pereaksi untuk isolasi dan penetapan konsentrasi protein dari daun
Azadirachta indica A. Juss dengan bahan p.a (Merck): a. larutan dapar natrium fosfat 5mM pH 7,2
b. larutan dapar natrium fosfat 5mM pH 7,2 yang mengandung 0,14 M NaCl
c. amonium sulfat
5. Pereaksi untuk uji sitotoksisitas pada sel HeLa dan sel Vero
b. Media penumbuh sel HeLa : RPMI 1640 (Sigma), Foetal Bovine Serum (FBS) 10% (Gibco), Penisilin-Streptomisin 2% (Gibco), dan Fungison
0,5% (Gibco)
c. Media penumbuh sel Vero : M199 (Sigma), Foetal Bovine Serum (FBS) 10% (Gibco), Penisilin-Streptomisin 2% (Gibco), dan Fungison 0,5%
(Gibco)
d. Reagen Stopper : natrium dodeksil sulfat 10% dalam HCl 0,01 N (Merck) e. MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide)
5 mg/ml (Sigma)
f. Trypsin 0,25% (Sigma)
E. Alat-alat Penelitian
Peralatan yang digunakan dalam penelitian ini antara lain: alat-alat gelas
(Pyrex), mortir dan stamper, kain monel, sentrifuge (Sigma K PLC series), spektrofotometer UV (CECIL Serie 2) dan kuvet 1 ml, mikroskop (Olympus
Model IMT-2), haemocytometer (Nebauer), laminar air flow (Nuraire Class II type A/B3), inkubator 37ºC, aliran 5% CO2 (Nuraire IR Airflow), 96-well plate (Nunc), ELISA Reader SLT 340ATC, tissue culture flask, pipet Pasteur, membran / tabung dialisis (Sigma), tangki nitrogen cair, penangas air, almari es (National),
F. Tatacara Penelitian 1. Determinasi tanaman
Bahan utama yang akan digunakan dalam penelitian yaitu daun mimba,
telah dideterminasi terlebih dahulu di laboratorium Farmakognosi Fitokimia,
Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta dan dipastikan juga
kebenarannya menggunakan acuan baku (Backer and Backuizen van den Brink,
1963; 1965).
2. Pengumpulan daun mimba
Daun mimba yang digunakan diambil dari pohon mimba yang tumbuh di
pekarangan Laboratorium Hayati, Universitas Gadjah Mada, Yogyakarta, pada
bulan Juni 2006.
3. Sterilisasi alat dan bahan
Untuk mencegah terjadinya kontaminasi oleh organisme, maka alat-alat
yang digunakan dalam penelitian ini harus disterilkan terlebih dahulu. Alat-alat
tersebut dicuci dengan larutan sabun hingga bersih dan dikeringkan, setelah itu
dibungkus dengan alumunium foil dan disterilkan dalam autoklaf selama 20 menit
pada suhu 121oC (Gennaro, 2000).
4. Pembuatan fraksi protein dari daun mimba
Daun segar tanaman Azadirachta indica A. Juss dikumpulkan, diseleksi, dan dicuci bersih dengan air mengalir. Daun dipotong kecil-kecil, tulang daun
dibuang dan ditimbang sebanyak 450 gram. Daun kemudian dibungkus dengan
untuk proses selanjutnya dimana bahan-bahan tersebut sebelumnya telah
disterilkan.
Daun ditumbuk halus dengan penambahan sesedikit mungkin dapar
natrium fosfat 5mM pH 7,2 yang mengandung 0,14 M NaCl dalam mortir yang
ditempatkan dalam baskom berisi air es. Hasil tumbukan diperas dengan kain
monel, ditampung dalam tabung conical yang bersih dan steril. Cairan yang diperoleh disentrifus pada 8000 rpm selama 30 menit. Supernatan dikumpulkan
dalam labu ukur 500 ml yang bersih dan steril.
Supernatan yang diperoleh kemudian diendapkan proteinnya dengan
menambahkan 27,45 gram amonium sulfat perlahan-lahan sambil terus diaduk
menggunakan magnetic stirrer dan dijaga suhunya, kemudian didiamkan selama semalam di dalam lemari es sambil terus diaduk.
Supernatan kemudian disentrifus lagi pada 8000 rpm selama 25 menit.
Supernatan (1) ditampung dalam labu ukur 500 ml sedang pelet yang yang
diperoleh dilarutkan dengan larutan dapar natrium fosfat 5mM pH 7,2 hingga
volumenya mencapai 3 ml.
Supernatan (1) yang telah ditampung ditambahkan dengan 27,47 gram
amonium sulfat perlahan-lahan sambil terus diaduk menggunakan magnetic stirrer selama semalam dan dijaga suhunya dalam lemari es. Selanjutnya supernatan (1) disentrifus 8000 rpm selama 25 menit. Supernatan (2) ditampung
dalam labu ukur 500 ml sedang pelet yang diperoleh dilarutkan dengan larutan
Supernatan (2) yang ditampung ditambah dengan 28,35 gram amonium
sulfat perlahan-lahan sambil terus diaduk menggunakan magnetic stirrer selama semalam dan dijaga suhunya dalam lemari es. Selanjutnya supernatan (2)
disentrifus 8000 rpm selama 25 menit. Supernatan (3) ditampung dalam labu ukur
500 ml sedang pelet yang diperoleh dilarutkan dengan larutan dapar natrium
fosfat 5mM pH 7,2 hingga volumenya mencapai 3 ml.
Supernatan (3) ditambah dengan 29,28 gram amonium sulfat
perlahan-lahan sambil terus diaduk menggunakan magnetic stirrer selama semalam dan dijaga suhunya dalam lemari es. Selanjutnya supernatan (3) disentrifus 8000 rpm
selama 25 menit. Supernatan (4) ditampung dalam labu ukur 500 ml sedang pelet
yang diperoleh dilarutkan dengan larutan dapar natrium fosfat 5mM pH 7,2
hingga volumenya mencapai 3 ml.
Langkah selanjutnya dilakukan dialisis dengan memasukkan keempat
sampel fraksi protein yang diperoleh tadi ke dalam tabung dialisis dan direndam
dalam larutan dapar natrium fosfat 5mM pH 7,2, diaduk menggunakan magnetic stirrer selama semalam dalam lemari es. Hasil dialisis ditambahkan larutan dapar natrium fosfat 5mM pH 7,2 yang mengandung 0,14 M NaCl hingga volumenya
mencapai 10 ml, sentrifus 8000 rpm selama 20 menit. Pelet dibuang sedang
supernatan diambil sebagai sampel fraksi protein dengan konsentrasi 10% jenuh,
sampel fraksi protein dengan konsentrasi 20% jenuh, sampel fraksi protein dengan
5. Pengukuran konsentrasi protein total
Fraksi protein 10%, 20%, 30% dan 40% jenuh yang diperoleh,
masing-masing sebanyak 10 μl kemudian ditambah larutan dapar natrium fosfat 5mM
hingga volumenya mencapai 1 ml. Ambil dan masukkan ke dalam kuvet. Ukur
serapan dengan spektrofotometer UV pada panjang gelombang 260 nm dan 280
nm dengan blanko larutan dapar natrium fosfat 5mM pH 7,2.
Concentration = [1.55E(280)] – [0.76E(260)] mg ml-1
(Layne cit., Richterich and Colombo, 1981) 6. Propagasi dan panen sel HeLa
a. Propagasi sel HeLa
Sel diambil dari tangki nitrogen cair, lalu dengan segera dicairkan diatas
penangas air 37ºC. Ampul disemprot dengan etanol 70% dan dibuka. Sel
kemudian dipindahkan ke dalam tabung conical steril yang berisi medium RPMI 1640. Suspensi sel disentrifus 8000 rpm selama 5 menit, supernatan yang didapat
dibuang, kemudian medium RPMI diganti dengan yang baru, disuspensikan
secara perlahan-lahan. Suspensi sel kemudian disentrifus lagi selama 5 menit.
Supernatan dibuang sedang pelet ditambah dengan 1 ml medium penumbuh yang
mengandung 20% FBS. Disuspensikan perlahan hingga homogen, kemudian sel
ditumbuhkan dalam 3-4 tissue culture flask kecil, diinkubasi dalam inkubator pada suhu 37ºC dengan aliran 5% CO2. Setelah 24 jam, medium diganti dan sel
b. Panen sel HeLa
Setelah jumlah sel cukup, medium RPMI 1640 kemudian diganti dengan
medium RPMI 1640 yang baru sebanyak 5 ml. Sel dilepaskan dari dinding flask dengan cara diresuspensikan menggunakan pipet Pasteur. Sel kemudian
dipindahkan ke dalam tabung conical steril, ditambah medium RPMI 1640 sampai volume 10 ml dan kemudian disentrifus 8000 rpm selama 5 menit. Supernatan
yang didapat dibuang sedang pelet diresuspensi kembali secara perlahan dengan 1
ml media. Jumlah sel dihitung menggunakan haemocytometer. Suspensi sel kemudian ditambahkan sejumlah medium sehingga diperoleh konsentrasi sel
sebesar 5 x 104 sel / 200 μl yang akan digunakan untuk penelitian.
7. Propagasi dan panen sel Vero a. Propagasi sel Vero
Sel diambil dari tangki nitrogen cair, lalu dengan segera dicairkan diatas
penangas air 37ºC. Ampul disemprot dengan etanol 70% dan dibuka. Sel
kemudian dipindahkan ke dalam tabung conical steril yang berisi medium M199. Suspensi sel disentrifus 8000 rpm selama 5 menit, supernatan yang didapat
dibuang, kemudian medium M199 diganti dengan yang baru, disuspensikan
secara perlahan-lahan. Suspensi sel kemudian disentrifus lagi selama 5 menit.
Supernatan dibuang sedang pelet ditambah dengan 1 ml medium penumbuh yang
mengandung 20% FBS. Disuspensikan perlahan hingga homogen, kemudian sel
ditumbuhkan dalam 3-4 tissue culture flask kecil, diinkubasi dalam inkubator pada suhu 37ºC dengan aliran 5% CO2. Setelah 24 jam, medium diganti dan sel
b. Panen sel Vero
Setelah jumlah sel cukup (kurang lebih setelah berumur 7 hari), sel dicuci
dengan FBS 10% sebanyak 3 ml. Untuk melepaskan sel-sel dari dinding flask,
diberi trypsin 0,25% sebanyak 1 ml. Sel dipindahkan dalam tabung conical steril yang sudah berisi M199 sebanyak 7 ml. Kemudian sel dibilas kembali dengan
FBS 10% sebanyak 3 ml. Hasil bilasan dituang ke dalam tabung conical yang sama dan disentrifus selama 5 menit. Untuk menghilangkan sisa trypsin, sel dicuci sekali lagi dengan menggunakan medium yang sama. Kemudian pelet ditambah
media kultur sebanyak 1 ml. Selanjutnya lakukan perhitungan jumlah sel dengan
menggunakan haemocytometer. Suspensi sel ditambah sejumlah medium sehingga memperoleh konsentrasi sel sebesar 2,5x104/100 μl dan siap dipakai untuk
penelitian (Freshney, 1986; Jacoby and Pastan, 1979; Sambrook et al, 1989). 8. Uji sitotoksisitas terhadap sel HeLa dan sel Vero
a. Uji sitotoksisitas dengan metode MTT terhadap sel HeLa
Seratus μl suspensi sel HeLa dengan konsentrasi 5 x 104 sel / 200 μl
dimasukkan ke dalam sumuran-sumuran pada 96-well plate dan diinkubasi bersama fraksi protein satu seri kadar selama 24 jam. Replikasi dilakukan
sebanyak 5 kali dengan memberikan perlakuan yang sama terhadap 11 baris
sumuran. Sebagai kontrol, 100 μl suspensi sel ditambahkan ke dalam sumuran
yang berisi medium RPMI 1640 dan dapar natrium fosfat 5mM pH 7,2 sedangkan
untuk faktor koreksi, 100 μl sampel ditambahkan ke dalam sumuran yang berisi
medium RPMI 1640 dan dapar natrium fosfat 5mM pH 7,2. Selanjutnya sel
inkubasi, pada masing-masing sumuran ditambahkan 10 μl MTT 5 mg/ml, dan
diinkubasi lagi semalam pada suhu 37ºC. Sel yang hidup akan bereaksi dengan
MTT membentuk kristal formazan berwarna ungu. Reaksi MTT dihentikan
dengan penambahan reagen stopper, diinkubasi lagi selama semalam pada suhu kamar. Kemudian serapan dapat dibaca dengan ELISA Reader pada panjang gelombang 550 nm.
b. Uji sitotoksisitas dengan metode MTT terhadap sel Vero
Seratus μl suspensi sel Vero dengan konsentrasi 5 x 104 sel / 200 μl
dimasukkan ke dalam sumuran-sumuran pada 96-well plate dan diinkubasi bersama fraksi protein satu seri kadar selama 24 jam. Replikasi dilakukan
sebanyak 5 kali dengan memberikan perlakuan yang sama terhadap 11 baris
sumuran. Sebagai kontrol, 100 μl suspensi sel ditambahkan ke dalam sumuran
yang berisi medium M199 dan dapar natrium fosfat 5mM pH 7,2 sedangkan untuk
faktor koreksi, 100 μl sampel ditambahkan ke dalam sumuran yang berisi medium
M199 dan dapar natrium fosfat 5mM pH 7,2. Selanjutnya sel diinkubasikan dalam
inkubator dengan aliran 5% CO2 pada suhu 37ºC. Pada akhir inkubasi, pada
masing-masing sumuran ditambahkan 10 μl MTT 5 mg/ml, dan diinkubasi lagi
semalam pada suhu 37ºC. Sel yang hidup akan bereaksi dengan MTT membentuk
kristal formazan berwarna ungu. Reaksi MTT dihentikan dengan penambahan
G. Analisis Hasil
Prosentase kematian sel pada metode MTT adalah selisih absorbansi
kontrol dengan absorbansi perlakuan dibagi absorbansi kontrol dikalikan 100%
atau :
Persen kematian =
kontrol
sel) tanpa perlakuan
-(perlakuan
-kontrol
x 100%
(Meyer, Ferrigni, Putnam, Jacobsen, Nochols, Mc Laughlin, 1982)
Hasil uji berupa prosentase kematian sel tersebut kemudian dianalisis
secara statistik menggunakan analisis probit untuk mengetahui konsentrasi protein
yang dapat mengakibatkan kematian 50% populasi sel HeLa maupun sel Vero
(LC50). Analisis statistik menggunakan uji t-independent sample dilakukan untuk membandingkan daya sitotoksisitas fraksi protein daun mimba terhadap sel HeLa