KATA PENGANTAR
Assalamu’alaikum Wr,WbPertama-tama kami panjatkan puji syukur kehadirat Allah SWT, atas limpahan rahmat dan karunia-Nya sehingga kami dapat menyelesaikan makalah yang berjudul “Aldehid dan Keton”. Dan tak lupa shalawat beserta salam tetap
terlimpah curahkan kepada Nabi Muhammad SAW karena berkat perjuangannya kami bisa berada dalam zaman yang penuh ilmu pengetahuan ini.
Kami mengucapkan terimakasih kepada semua pihak yang telah membantu terselesaikannya makalah ini. Diantaranya ucapan terima kasih kepada Dosen mata kuliah Teori Kimia Dasar yaitu Dadan Ridwanuloh,M.Si dan juga rekan-rekan yang telah menyusun makalah ini. Dan kami berharap semoga makalah yang kami buat ini dapat bermanfaat.
Kami menyadari bahwa makalah ini sangat jauh dari sempurna, masih banyak kekurangan dalam makalah ini. Setiap saran, kritik, dan komentar yang bersifat membangun dari pembaca demi kemajuan dimasa yang akan datang.
Wassalamu’alaikum Wr,Wb
Karawang, 20 Desember 2016
BAB I
PENDAHULUAN
1.1 Latar Belakang
Adanya gugus fungsi dalam suatu senyawa dapat diperkirakan dari hasil analisa unsur senyawa tersebut. Aldehid berasal dari alkohol primer yang teroksidasi, sedangkan keton berasal dari alkohol sekunder yang teroksidasi.
Aldehid dan keton adalah contoh senyawa-senyawa karbonil yang banyak ditemukan di alam bebas. Aldehid adalah senyawa organik yang karbon karbonilnya selalu berikatan dengan paling sedikit satu atom hidrogen. Sedangkan keton adalah senyawa organik yang karbon karbonilnya dihubungkan dengan 2 karbon lain.
Aldehid dan keton memiliki banyak manfaat. Contoh senyawa aldehid adalah formalin yang sering digunakan dalam pengawetan zat organik. Sedangkan contoh senyawa keton adalah aseton yang dapat digunakan untuk pembersih kuteks.
Gugus karbonil ialah satu atom karbon dan satu atom oksigen yang dihubungkan dengan ikatan ganda dua. Gugus ini merupakan salah satu gugus fungsi yang paling lazim di alam dan terdapat dalam karbohidrat, lemak, protein, dan steroid. Gugus fungsi ini dijumpai dalam senyawa aldehid dan keton.
1.2 Rumusan Masalah
1. Apa pengertian dari senyawa aldehid dan keton? 2. Bagaimana struktur dari senyawa aldehid dan keton? 3. Bagaimana tata nama dari senyawa aldehid dan keton? 4. Bagaimana isomer dari senyawa aldehid dan keton?
5. Apa saja kegunaan aldehid dan keton dalam kehidupan sehari-hari?
1. Untuk mengetahui pengertian dari senyawa aldehid dan keton 2. Untuk mengetahui struktur dari senyawa aldehid dan keton 3. Untuk mengetahui tata nama dari senyawa aldehid dan keton 4. Untuk mengetahui isomer dari senyawa aldehid dan keton
5. Untuk mengetahui kegunaan aldehid dan keton dalam kehidupan sehari-hari
2.1 Aldehida (Alkanal)
Nama aldehida merupakan singkatan dari alkoholdehidrogeneratus,yang berasal dari bahasa latin yang berarti alkohol yang kehilangan hidrogen. Senyawa yang mengandung gugus aldehida disebut golongan alkanal. Aldehida atau alkanal merupakan senyawa karbon turunan alkana dari keluarga aldehida yang memiliki
gugus fungsi (-CHO). Rumus struktur aldehida adalah (RCHO).
a. Rumus Umum Aldehida
Contoh senyawa aldehida pada tabel
Dari contoh – contoh di atas, maka dapat disimpulkan rumus umum aldehida / alkanal adalah CnH2nO . Pada aldehid gugus fungsi selalu terletak di salah satu ujung rantai C.
b. Tata nama Aldehida - Sistem IUPAC
Nama IUPAC untuk aldehida adalah alkanal. Adapun tata nama aldehida menurut sistem IUPAC adalah sebagai berikut:
1. Nama aldehid sebagai turunan dari alkana diturunkan dari nama alkana dengan mengganti akhiran -a dengan -al.Contoh:
CH4 (metana) dan metanal
4. Pemberian nama dimulai dari nama cabang – cabang yang disusun menurut abjad, kemudian nama rantai induk. Posisi gugus fungsi tidak perlu disebutkan karena selalu terletak pada atom C nomor 1.
Contoh :
3-metil pentanal 2,4-dimetil heksanal
- Sistem Trivial
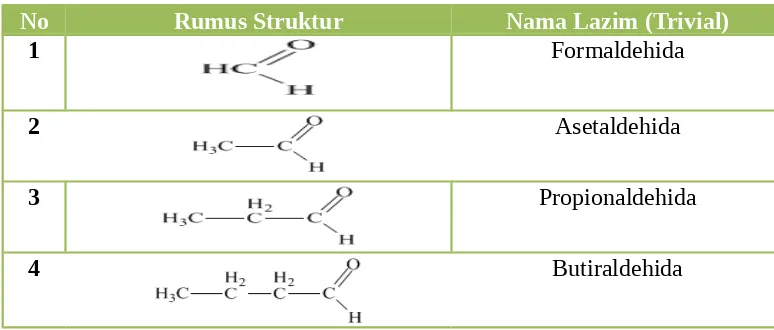
Nama lazim (trivial) aldehid diturunkan dari nama asam karboksilat induk dengan mengubah asam oat / asam –at menjadi aldehid. Contoh penamaan aldehida secara trivial diperlihatkan dalam tabel berikut:
c. Sifat-sifat pada aldehida
- Sifat fisis aldehida
No Rumus Struktur Nama Lazim (Trivial)
1 Formaldehida
2 Asetaldehida
3 Propionaldehida
Aldehida mempunyai molekul-molekul yang bersifat polar karena adanya gugus karbonil Cδ+ = Oδ-dengan dipol-dipol δ+ dan δ-. Oleh karena itu, jenis gaya antar molekulnya adalah gaya tarik menarik dipol-dipol. Selain itu, aldehida juga memiliki gaya London (gaya tarik-menarik dipole sesaat dipol terimbas). Sebagai catatan, aldehida tidak memiliki ikatan hydrogen seperti halnya alkohol, karena atom H-nya yang bersifat asam yang terikat ke atom O. H-nya yang bersifat asam yang terikat ke atom O.
Adanya gaya tarik-menarik dipol-dipol menyebabkan titik didih aldehida lebih tinggi dibandingkan alkana yang tidak memiliki gaya ini. Namun, tidak adanya ikatan hydrogen pada aldehida menyebabkan titik didih aldehida masih rendah dibandingkan alkohol. Namun, dengan pertambahan panjang rantai karbon, gaya antar molekul yang lebih berperan adalah gaya London. Hal ini ditunjukkan oleh kenaikan titik didih dari metanal ke butanal.
Untuk isomer-isomer aldehida, sifat fisis seperti titik didih dari isomer rantai lurus lebih tinggi dibanding isomer rantai bercabang. Hal ini dikarenakan molekul-molekul dengan rantai lurus dapat mendekat dengan mudah. Dengan demikian, gaya antar molekul dari isomer rantai lurus lebih kuat dan lebih banyak dibandingkan gaya serupa dari isomer rantai bercabang.
Kelarutan aldehida
Aldehida memiliki gugus –CO– yang bersifat polar dan rantai alkyl (R-) yang bersifat non polar. Jadi, aldehida dapat bercampur dengan senyawa ion, senyawa kovalen polar, dan non polar. Kelarutan aldehida dalam pelarut polar seperti air akan berkurang dengan pertambahan panjang rantai karbon karena aldehida semakin bersifat non polar.
- Sifat Kimia aldehida
Reaksi Identifikasi Aldehida
Pembuatan aldehida
Aldehida dapat dibuat dari reaksi oksidasi alkohol primer dengan suatu oksidator. Simak mekanisme reaksinya berikut ini.
2.2 Keton (Alkanon)
a. Rumus Umum Keton
Contoh senyawa keton pada tabel
Dari contoh – contoh di atas, maka dapat disimpulkan rumus umum keton / alkanon adalah CnH2nO.
b. Tata nama Keton - Sistem IUPAC
Nama keton diturunkan dari alkana induknya, huruf akhir –a diubah menjadi –on. Bila perlu digunakan nomor. Penomoran dilakukan sehingga gugus karbonil mendapat nomor kecil.
Contoh :
Propanon Butanon
- Sistem Trivial
Keton mengandung gugus karbonil Cδ = Cδ yang sangat polar seperti halnya aldehida. Dengan demikian, jenis gaya antar molekul keton juga sama dengan aldehida, yakni gaya tarik menarikdipol-dipol disamping gaya London. Tidak mengherankan apabila sifat fisis keton, seperti titik didihnya mirip dengan aldehida. Juga, bahwa titik dididh keton lebih tinggi dari alkana, tetapi masih lebh rendah dari alkohol.
Dengan pertambahan panjang rantai karbon, gaya antar molekul yang lebih berperan adalahgaya London. Hal ini ditunjukkan oleh kenaikan titik didih dari propanon ke 2-pentanon pada tabel
Disamping itu, untuk menunjukkan isomer-isomer keton, sifat fisis seperti titik didih dari isomer rantai lurus lebih tinggi dibanding isomer rantai bercabang. Untuk jelasnya, bandingkan titik didih 2-pentanon dan 3-metil2-butanon, seperti tampak pada tabel
Kelarutan keton
Keton memiliki gugus karbonil –CO- yang bersifat polar dan rantai alkyl (R-) yang bersifat non polar. Jadi, keton dapat bercampur dengan senyawa ion, senyawa kovalen polar, dan non polar. Kelarutan keton dalam pelarut polar seperti air akan berkurang dengan pertambahan panjang rantai karbon karena keton semakin bersifat non-polar.
- Sifat kimia keton
Pembuatan keton
Keton dapat dibuat dari reaksi oksidasi alcohol skunder dengan suatu oksidator. Simak contoh berikut.
Seperti halnya aldehida, pembuatan keton di laboratorium menggunakan oksidator K2Cr2O7 dalam suasana asam. Sedangkan di industri, digunakan oksidator O2 dari udara dengan katalis seperti Cu dan Ag.
2.3 Isomer
1. Isomer Struktur pada aldehid
Keisomeran alkanal mulai terdapat pada butanal yang mempunyai dua isomer, yaitu butanal dan 2–metil–propanal (isobutanal).
Butanal 2–metil–propanal (isobutanal)
2. Isomer posisi pada keton
Isomer posisi yang terjadi pada keton disebabkan oleh adanya perubahan dalam kedudukan gugus karbonil dalam rantai Contoh :
3. Isomer Fungsi
Keisomeran fungsi, yaitu keisomeran yang terjadi karena perbedaan gugus fungsi di antara dua senyawa yang mempunyai rumus molekul sama. Aldehida dengan rumus struktur R-CHO berisomer fungsi dengan keton yang memiliki rumus struktur R-O-R`.
Contoh :
2.4 Kegunaan
a. Aldehid
1. Larutan formaldehida atau metanal 40% dikenal sebagai formalin yang digunakan untuk antiseptik dan pengawet mayat.
2. Formaldehida juga dimanfaat sebagai bahan baku untuk industri plastik melamin dan bakelit.
4. Beberapa jenis aldehida lain, misalnya sinamaldehida merupakan zat yang memberi aroma khas pada kayu manis, dan vanilin merupakan senyawa aldehida yang memberi aroma khas pada buah vanili.
b. Keton
1. Senyawa keton yang paling banyak dikenal adalah propanon atau aseton. Aseton banyak dimanfaatkan sebagai pelarut (misalnya pelarut cat kuku) dan pembersih kaca. Aseton juga merupakan bahan baku untuk membuat senyawa bahan industri, misalnya perspex (sejenis plastik) dan bispenol (plastik).
2. Hormon dalam tubuh manusia, misalnya testosteron, progesteron, kortikosteron, dan sejenisnya merupakan senyawa keton.
3. Bahan baku pembuatan zat organic lain seperti chlaroform yang digunakan sebagai obat bius.
BAB III
PENUTUP
3.2 Kesimpulan
Aldehid dan keton merupakan senyawa turunan alkana yang memiliki rumus umum CnH2nO
1. Gugu karbonil aldehid terikat pada hidrogen dari satu ujung, tetapi dalam keton, gugus karbonil terikat pada atom karbon dari kedua belah pihak.
2. Oleh karena itu, gugus fungsional keton selalu terlihat di tengah molekul, dan gugus aldehid selalu di ujung.
3. Dalam nomenklatur tersebut, aldehid memiliki akhiran -al dan keton akhiran adalah -on.
dengan cara memberikan nomor serendah mungkin pada karbon karbonil (tidak akan mendapatkan nomor satu di setiap kesempatan).
5. Aldehid dapat dengan mudah teroksidasi dibandingkan dengan keton.
3.2 Saran
Gugus aldehid dan keton memiliki berbagai macam kegunaan baik kegunaan positif maupun negatif bagi manusia. Seperti formalin yang dipergunakan dalam pengawetan mayat. Penggunaan senyawa ini mestinya lebih diawasi dalam kehidupan masyarakat.