SKRINING AKTIVITAS ANTIMIKROBA DAN UJI FITOKIMIA DARI KAPANG
ENDOFITIK TANAMAN DAHLIA (DAHLIA VARIABILIS
)
Dina Fitriyah, Christine Jose, Saryono
Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Riau Kampus Binawidya Pekanbaru, 28293, Indonesia
Abstract
Dahlia variabilis has many beneficial effects to human health, such as antibacterial and antifungi. This research was to discover the potency of endophytes from Dahlia as antimicrobial agents. A total number of four endophytic molds were isolated from Dahlia’s tuber. The screenings were carried out using the agar diffusion method againts pathogens with concentrations 50 µL/disc. The inhibition zone of amoxsan was (12,55 ± 0,38) mm and ketoconazole was (17,67 ± 0,57) mm. The crude extract of endophytic mold, LBKURCC 41 (Aureobasidium sp) showed the most significant of inhibition zones. The Inhibition zone of crude extract of LBKURCC 41 to Eschericia colli and Staphylococcus aureus were (19,33±1,15) mm and (17,00±1,00) mm respectively. The crude extract of LBKURCC 41 was identified by phytochemical screenings method. The result showed the presence of saponin. Three other isolates LBKURCC 40 (Monilia sp) and LBKURCC 42 (Moniliella sp) and LBKURCC 43 (Sporothrix sp) showed no activity as an antimicrobial. These results indicated that endophytic mold could be a promising source for antimicrobial agents.
Kata kunci: Jamur endofit, Antimikroba, Tanaman Dahlia, Escherichia
coli, Staphylococcus aureus
PENDAHULUAN
Penyakit infeksi di Indonesia masih mengkhawatirkan kehidupan masyarakat. Salah satu penyebabnya adalah semakin meluasnya resistensi mikroorganisme ter- hadap obat-obatan yang ada. Keadaan ter- sebut mendorong upaya penggalian obat-obatan antimikroorganisme yang baru (Suciatmih, 2010).
Salah satu jenis tanaman yang dapat digunakan sebagai obat adalah tanaman dahlia (Dahlia variabilis). Umbi dahlia ini diketahui mengandung senyawa yang me-miliki bioaktitas yang tinggi. Ekstrak metanol umbi dahlia berbunga merah menunjukkan adanya aktivitas antimikroba terhadap
Escherichia coli, Basillus subtilis,
Staphy-lococcus aureus, Candida utilis dan
Penicillium sp (Suryadi, 2007).
Produksi senyawa antimikroba dari tanaman dalam jumlah massal membutuhkan tanaman dahlia dalam jumlah yang sangat besar, diperlukan lahan yang luas dan masa tumbuh tanaman yang lama. Oleh sebab itu perlu dilakukan isolasi senyawa antimikroba
dari mikroorganisme endofitik yang hidup dalam jaringan tanaman dahlia.
Pada penelitian sebelumnya didapatkan empat isolat jamur endofitik dari umbi tanaman dahlia, antara lain: Aureobasidium
sp (LBKURCC 41) dari umbi dahlia berbunga
kuning, Moniliella sp (LBKURCC 42) dari umbi dahlia berbunga merah hati, Monilia sp (LBKURCC 40) dari umbi dahlia berbunga jingga, dan Sporothrix sp (LBKURCC 43) dari umbi dahlia berbunga ungu (Maria, 2011). Oleh karena itu perlu dilakukan skrining awal aktivitas antimikroba dari jamur endofitik tanaman Dahlia variabilis.
BAHAN DAN METODA
a. Persiapan Media Fermentasi (Huang
et. al.,2007)
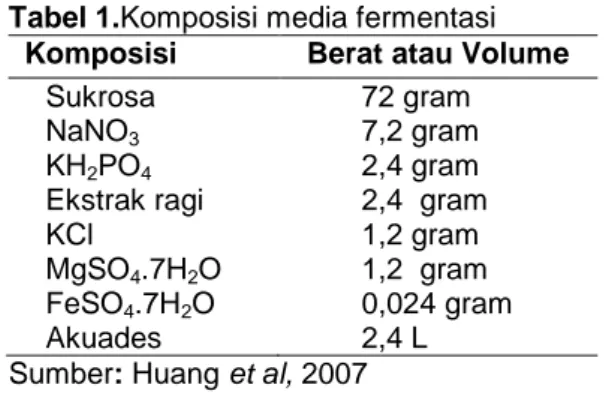
Media ini digunakan sebagai media fermentasi produksi senyawa antimikroba. Komposisi pembuatan media ini dapat dilihat pada Tabel 1. Semua bahan dilarutkan ke dalam 2400 mL akuades dan dipanaskan hingga larut, setelah larut media dibagi ke- dalam 12 erlemeyer masing-masing 200 mL. Kemudian disterilisasi dengan autoklaf pada
121oC (tekanan uap 15 lbs) selama 20 menit. Media dibiarkan sehari untuk melihat ada atau tidaknya kontaminasi. Jika tidak terlihat tanda–tanda kontaminasi, maka media siap digunakan.
Tabel 1.Komposisi media fermentasi
Sumber: Huang et al, 2007
b. Fermentasi Jamur Endofitik
Sebanyak 1ml inokulum jamur endo-fitik (5%) diinokulasikan kedalam 200 mL media (Huang et al. 2007), kemudian diinkubasi selama 20 hari pada suhu ruang dengan kecepatan 150 rpm. Tiap selang 5 hari, dilakukan uji antimikroba. Kultur jamur hasil fermentasi diambil dan disentrifus dengan kecepatan 5000 rpm selama 20 menit. Untuk memisahkan supernatan dan massa selnya, kultur hasil fermentasi ini disaring dengan menggunakan millipore
syringe filter 0,2 µm, sehingga didapatkan
ekstrak kasar jamur endofit tanaman dahlia. Ekstrak kasar jamur endofitik inilah yang akan digunakan untuk uji antimikroba.
c. Peremajaan bakteri Patogen
Bakteri uji (Escherichia coli dan
Staphylococcus aureus) dari agar miring
dipindahkan ke media Nutrien Agar yang baru secara aseptik dan diinkubasi selama 24 jam. Koloni yang tumbuh diinokulasikan ke media Nutrient Broth dan diinkubasi se-lama 24 jam pada suhu 37oC. Setelah 24 jam, absorbansi bakteri diukur. Bakteri siap digunakan untuk uji antibakteri apabila OD telah mencapai 0,08 0,1 (setara 107 CFU/mL). Jika OD lebih besar dari 0,1 maka dilakukan pengenceran dengan mengguna-kan larutan NaCl 0,85%.
d. Peremajaan khamir patogen
Isolat Candida albicans dari agar miring dipindahkan ke media PDA yang baru secara aseptik dan diinkubasi selama 4x24 jam. Selanjutnya diinokulasikan kembali ke media Sabouroud Dextrose Broth (SDB) dan diinkubasi selama 48 jam. Khamir siap digunakan untuk uji antikhamir apabila OD telah mencapai 0,08 0,1 (setara dengan 107 CFU/mL). Jika OD lebih besar dari 0,1 maka
dilakukan pengenceran dengan mengguna-kan larutan NaCl 0,85%.
e. Uji antibakteri
Inokulum patogen (OD600nm 0,1) setara
107 CFU/mL (Martin, 2011) diinokulasikan sebanyak 1 mL ke dalam tabung reaksi yang mengandung media NA cair sebanyak 15 mL (suhu 50oC) dan divortex, kemudian agar cair ini dituangkan ke dalam cawan petri dan dibiarkan memadat.
Masing-masing ekstrak kasar steril jamur endofitik sebanyak 50 L diteteskan pada kertas cakram steril (diameter 6 mm) dan dibiarkan mengering. Kontrol positif yang digunakan adalah Amoxsan 30 g dan kontrol negatif yang digunakan adalah media fermentasi steril. Kemudian kertas cakram diletakkan di atas media NA yang mengan-dung bakteri uji (Escherichia coli atau
Staphylococcus aureus). Selanjutnya cawan
petri diinkubasi pada suhu 37oC dengan kondisi cawan petri dibalikkan. Diameter zona bening disekitar kertas cakram diukur setelah inkubasi selama 24 jam.
f. Uji antikhamir
Inokulum khamir patogen (OD600nm 0,1)
setara 107 CFU/mL (Martin, 2011) diinoku-lasikan sebanyak 1 mL ke dalam tabung reaksi yang mengandung media PDA cair sebanyak 15 mL (suhu 50oC) dan divortex, kemudian dituangkan ke dalam cawan petri dan dibiarkan memadat.
Masing-masing ekstrak kasar steril isolat endofitik sebanyak 50 L diteteskan pada kertas cakram steril (diameter 6 mm) dan dibiarkan mengering. Kontrol positif yang digunakan adalah Ketoconazole konsentrasi 30 g dan kontrol negatif yang digunakan adalah media fermentasi steril. Kemudian kertas cakram diletakkan di atas media PDA yang mengandung Candida albicans. Selan-jutnya cawan petri diinkubasi pada suhu ruang. Diameter zona bening disekitar kertas cakram diukur setelah inkubasi selama 2x24 jam.
g. Uji Fitokimia
Ekstrak kasar fermentasi steril jamur endofitik yang menunjukkan adanya aktivitas antimikroba dilakukan uji fitokimia (Devi et
al., 2012) untuk mengetahui kandungan
senyawa metabolit sekunder yang dihasilkan.
1. Uji terpenoid/steroid
Ekstrak kasar fermentasi jamur endofit dimasukkan ke dalam tabung reaksi dan ditambahkan kloroform beramoniak. Kemudi-an ditambahkKemudi-an H2SO4 2 N ke dalam tabung
Komposisi Berat atau Volume
Sukrosa 72 gram
NaNO3 7,2 gram
KH2PO4 2,4 gram
Ekstrak ragi 2,4 gram
KCl 1,2 gram
MgSO4.7H2O 1,2 gram
FeSO4.7H2O 0,024 gram
dan dikocok kuat. Campuran ini didiamkan hingga terbentuk dua lapisan yaitu lapisan asam (atas) dan lapisan kloroform (bawah). Lapisan kloroform diletakkan di plat tetes dan dibiarkan menguap lalu ditambahkan asam asetat anhidrat dan asam sulfat pekat (pereaksi Lieberman-Burchard). Apabila ter-bentuk warna hijau-biru menandakan adanya senyawa steroid dan warna merah menan-dakan adanya senyawa terpenoid.
2. Uji alkaloid
Lapisan asam diambil dan dimasukkan ke dalam tabung reaksi. Kemudian ditambah-kan pereaksi Dragendorff dan pereaksi Mayer. Apabila terjadi perubahan warna menjadi jingga setelah penambahan pereaksi Dragendorff dan warna putih setelah penam-bahan pereaksi Mayer berarti ekstrak positif mengandung alkaloid.
3. Uji fenolik
Ekstrak kasar fermentasi diletakkan di atas plat tetes dan ditambahkan larutan besi (III) klorida. Hasil positif dinyatakan dengan adanya perubahan warna larutan menjadi biru-hitam.
4. Uji flavonoid
Ekstrak kasar fermentasi dimasukkan ke dalam tabung reaksi dan ditambahkan etanol 70% kemudian dipanaskan. Campur-an ini ditambahkCampur-an lempeng logam magne-sium dan setetes asam klorida pekat. Apabila terjadi perubahan warna larutan menjadi merah muda, hasil dinyatakan positif.
5. Uji saponin
Ekstrak kasar ditambahkan akuades kemudian dipanaskan hingga mendidih. Kemudian larutan dikocok kuat dan apabila terbentuk busa yang stabil selama ±10 menit maka sampel dinyatakan mengandung saponin.
Hasil dan Pembahasan
1. Skrining aktivitas antimikroba jamur
endofit tanaman dahlia
Media Huang et al (2007) merupakan media produksi ketiga yang digunakan dalam penelitian ini. Hasil skrining aktivitas anti-mikroba ekstrak kasar jamur endofitik yang difermentasi menggunakan media yang dapat dilihat pada tabel berikut:
Tabel 2. Hasil skrining terhadap Eschericia coli pada media Huang et al, 2007
Ekstrak Rata-rata diameter hambat (mm)
Hari ke-5 Hari ke-10 Hari ke-15 Hari ke-20
Amoxsan (12,55 ± 0,38) (11,67 ± 0,33) (12,00 ± 0,33) (11,66 ± 1,45) Kontrol (-) - - - - LBKURCC 40 - - - - LBKURCC 41 - - (19,33 ± 1,15) (15,56±0,50) LBKURCC 42 - - - - LBKURCC 43 - - - -
Catatan: * harga rata-rata diameter hambat ekstrak kasar jamur endofitik sebanyak tiga kali pengulangan.
Tabel 3. Hasil skrining terhadap Staphylococcus aureus pada media Huang et al, 2007
Ekstrak Rata-rata diameter hambat (mm)
Hari ke-5 Hari ke-10 Hari ke-15 Hari ke-20
Amoxan (11,55 ± 0,50) (11,66 ± 0,57) (11,67 ± 0,33) (11,77 ± 0,50) Kontrol (-) - - - - LBKURCC 40 - - - - LBKURCC 41 - - (17,00 ± 1,00) (15,11±0,19) LBKURCC 42 - - - - LBKURCC 43 - - - -
Catatan: * harga rata-rata diameter hambat ekstrak kasar jamur endofitik sebanyak tiga kali pengulangan.
Ekstrak kasar jamur endofitik LBKURCC 41 menunjukkan aktivitas antimikroba pada media Huang et al (2007) di hari inkubasi ke-15 dan hari ke-20, baik terhadap E.coli (Tabel 2) maupun S.aureus (Tabel 3). Pada hari ke-15, zona hambat terhadap E.coli dan
S.aureus sebesar (19,33±1,15) mm dan
(17,00±1,00) mm. Sedangkan, zona hambat untuk E.coli dan S.aureus pada hari ke 20 sebesar (15,56±0,50) mm dan (15,11±0,19) mm. Hasil menunjukkan bahwa zona bening yang dihasilkan pada hari ke-15 lebih besar dibandingkan dengan hari ke-20.
Skrining ekstrak kasar jamur endofitik terhadap aktivitas antikhamir terhadap khamir patogen Candida albicans tidak menunjukkan hasil yang positif terhadap aktivitas antimikroba (Tabel 4).
2. Uji Fitokimia jamur endofit tanaman
dahlia
Uji fitokimia dilakukan terhadap ekstrak kasar jamur endofitik tanaman dahlia yang
memiliki aktivitas antimikroba. Uji fitokimia ini dilakukan untuk mengetahui adanya kesama-an senyawa metabolit sekunder ykesama-ang dihasil-kan oleh jamur endofitik, dengan senyawa metabolit sekunder yang dihasilkan oleh tanaman inangnya (Agusta, 2009).
Tabel 4. Hasil skrining terhadap Candida albicans pada media Huang et al (2007)
Ekstrak Rata-rata diameter hambat (mm)
Hari ke-5 Hari ke-10 Hari ke-15 Hari ke-20
Nizoral (15,77 ± 0,69) (16,44 ± 0,38) (16,77 ± 0,38) (17,67 ± 0,57) Kontrol (-) - - - - LBKURCC 40 - - - - LBKURCC 41 - - - - LBKURCC 42 - - - - LBKURCC 43 - - - -
Tabel 5 . Hasil uji fitokimia jamur endofit tanaman dahlia pada media Huang et al., (2007).
Alkaloid Flavonoid Terpenoid Fenolik Saponin
LBKURCC 40 - - - - -
LBKURCC 41 - - - - +
LBKURCC 42 - - - - -
LBKURCC 43 - - - - -
PEMBAHASAN
Media Huang et al (2007) terdiri dari sukrosa sebagai sumber karbon, NaNO3
sebagai sumber nitrogen, KH2PO4 sebagai
sumber posfor dan berperan sebagai buffer, Ekstrak ragi berperan sebagai sumber nitrogen, KCl berperan sebagai sumber kalium, MgSO4.7H2O dan FeSO4.7H2O
berperan sebagai sumber Mg dan Fe. Sukrosa merupakan disakarida yang dibentuk dari sebuah molekul α-D-glukosa dan molekul β-D-fruktosa yang dihubungkan oleh ikatan 1,2 glikosidik. Ketika ikatan β-1,2 glikosidik terputus oleh reaksi hidrolisis, akan terbentuk campuran glukosa dan fruktosa. Campuran monosakarida-mono-sakarida tersebut disebut sebagai gula invert (invert sugar), yang merupakan turunan dari sukrosa. Sukrosa dapat dihidrolisis dengan bantuan enzim yang disebut sebagai invertase atau sukrase (Rahma, 2006).
Sukrosa merupakan sumber karbon kompleks. Media yang dapat memproduksi senyawa metabolit sekunder pada umumnya yaitu media yang mengandung sumber karbon yang komplek karena salah satu faktor yang mempengaruhi mikroorganisme dalam menghasilkan metabolit sekunder adalah kekomplekskan medium. Komplek-sitas suatu medium pada hakekatnya
me-rupakan kondisi kritis dimana mikroba umumnya akan menghasilkan senyawa metabolit sekunder untuk mempertahankan hidupnya (Kumala et al, 2006).
Menurut Berg et al. (2000),
Aureo-basidium sp. dapat menghasilkan senyawa aureoquinone yang memiliki aktivitas
anti-mikroba terhadap bakteri Gram positif seperti Bacillus subtilis ATCC 6633. A. pullulans juga dapat menghasilkan senyawa aureobasidins yang berpotensi sebagai antikhamir.
Aureo-basidium pullulans yang diisolasi dari daun Santalum album memiliki kemampuan
anti-mikroba terhadap bakteri Gram negatif dan
Pseudomonas sp. namun tidak terhadap S. aureus (Kalantar et al., 2006).
Ada beberapa dugaan mengapa ekstrak kasar endofit LBKURCC 40 dan LBKURCC 43 tidak dapat menghasilkan senyawa anti-mikroba. Pertama, kedua isolat tersebut me-miliki gen yang mengkode pembentukan senyawa metabolit sekunder, namun tidak terekspresi pada media produksi yang telah digunakan. Gen tersebut baru terekspresi ketika diinduksi terlebih dahulu (Nofiani et al, 2009). Mungkin pada tiga media produksi yang digunakan, tidak ada induser yang dapat mengekspresikan gen pembentukan senyawa metabolit untuk isolat LBKURCC 40 dan LBKURCC 43, kemungkinan ini juga menjawab mengapa keempat ekstrak kasar
jamur endofit ini tidak memiliki aktivitas antikhamir terhadap Candida albicans.
Hasil uji fitokimia ekstrak kasar jamur endofitik tanaman dahlia menunjukkan bahwa jamur Aureobasidium sp. positif mengandung saponin.
Senyawa saponin memiliki peran alami dalam tanaman sebagai pelindung terhadap patogen dan hama (Turk, 2005). Lebih dari
90%, dinding sel bakteri pada bagian membran luar dilindungi oleh lipopolisakarida (LPS). Saponin akan bereaksi dengan lipopolisakarida sehingga menurunkan te-gangan permukaan membran, yang akhirnya akan menyebabkan kehancuran sel (Arabski
et al, 2012).
Gambar 1. Skrining aktivitas antimikroba terhadap E.coli (a), Staphylococcus aureus (b) dan
Candida albicans (c) pada hari ke-15
Keterangan : (1) = kontrol positif, (2) = kontrol negatif, (3) = LBKURCC 40, (4) = LBKURCC 41, (5) = LBKURCC 42 dan (6) = LBKURCC 43
KESIMPULAN
Kesimpulan yang dapat diambil dari penelitian ini yaitu skrining keempat jamur endofitik menunjukkan bahwa ekstrak kasar jamur endofit LBKURCC 41 (Aureobasidium
sp) menunjukkan aktivitas antimikroba dengan media produksi Huang et al. (2007) pada hari ke-15 dan 20. Aktivitas antimikroba
yang ditunjukkan pada hari ke-15 lebih besar dibandingkan aktivitas antimikroba di hari ke-20.
UCAPAN TERIMAKASIH
Penelitian ini dibiayai oleh “Hibah Pasca DIKTI 2011 atas nama Prof. Saryono
DAFTAR PUSTAKA
Agusta. A, 2009. Biologi dan Kimia Jamur Endofitik. ITB University Press, Bandung
Arabski. M, Aneta, W & Kaca, W, 2012. Effect of saponin againts Clinical E.coli strains and eukaryotic cell lines. Journal of Biomedicine and Biotechnology
Berg, A., Gorls, H., Dorfelt, H., Walther, G., Schlegel, B., & Grafe, U. 2000. Aureoquinone, a new protease inhibitor from Aureobasium sp. The Journal of Antibiotics 53 (11):1293-1295. Devi, N.N., Prabakaran, J.J., & Wahab, F. 2012. Phytochemical analysis and enzyme analysis of
endophytic fungi from Centella asiatica. Asian Pacific Journal of Tropical Biomedicine (2012):1-5.
Huang, W.Y., Cai, Y.Z., Hyde, K.D., Corke, H., & Sun, M. 2007. Endophytic fungi from Nerium
oleander L (Apocynaceae) main constituents and antioxidant activity. World Journal of Microbiology and Biotechnology 23(9)1253-1263.
Kalantar, E., Deopurkar, R., & Kapadnis, B. 2006. Antimicrobial Activity of Indigenous Strains of Aureobasidium Isolated from Santalum Album Leaves. Iranian Journal of Pharmaceutical
Research 1: 59-64.
Kumala, S., Agustina, E., dan Wahyudi, P. 2006. Uji aktivitas antimikroba metabolit sekunder kapang endofit tanaman trengguli (Cassia fistula L). Jurnal Bahan Alam Indonesia ISSN. 2 (6):46-48.
Lorenita, M. 2011. Isolasi jamur Endofitik dari Tanaman Dahlia (Dahlia Variabilis) Padang Luar, Sumatera Barat. FMIPA Kimia. Universitas Riau
Martins, I.M., Cortes, J.C.G., Munoz, J. Moreno, B., Ramos, M., Clemente, J.A., Duran, A., & Ribas, J.C. 2011. Differential activities of three families of specific (1,3)glucan synthase inhibitors in wild-type and resistant strains of fission yeast. The Journal of Biological
Chemistry 286(5): 3484-3496.
Nofiani, R., Nurbetty, S., & Sapar, A. 2009. Aktivitas Antimikroba Ekstrak Methanol Bakteri Berasosiasi Spons dari Pulau Lemukutan, Kalimantan Barat. Jurnal Ilmu dan Teknologi
Kelautan Tropis 1(2):33-41.
Suciatmih. 2010. Pengaruh Konsentrasi Antimikroorganisme, Media Fermentasi, dan Waktu Inkubasi Terhadap Pertumbuhan Absidia corymbifera (Cohn) Sacc. & Trotter dari jamur
Endofit Fusarium nivale (Fr.) Ces. Media Litbang Kesehatan Volume XX:1.
Suryadi, A.E. 2007. Ekstraksi dan Uji Aktivitas Antimikroba Ekstrak Umbi Dahlia (Dahlia variabilis). Skripsi FMIPA Universitas Riau. Pekanbaru.
Turk, F.M. 2006. Saponins versus plant fungal pathogens. Journal of Cell and Molecular Biology 5:13-17.