i
EFEK HEPATOPROTEKTIF JANGKA PENDEK EKSTRAK
METANOL - AIR DAUN Macaranga tanarius L. TERHADAP
TIKUS TERINDUKSI KARBON TETRAKLORIDA
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Ilmu Farmasi
Diajukan Oleh:
M. R. Biri Koni Tiala
NIM : 098114088
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
ii
iii
iv
PERSEMBAHAN
“Dont wait for the perfect moment, just take the moment
and make it perfect”
Kupersembahkan skripsi ini untuk……
vii
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa atas
berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul
“Efek Hepatoprotektif Jangka Pendek Ekstrak Metanol-Air Daun Macaranga
tanariusL. Terhadap Tikus Terinduksi Karbon Tetraklorida” ini dengan baik. Skripsi
ini disusun untuk memenuhi salah satu syarat untuk memperoleh gelar Sarjana
Farmasi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Penyelesaian skripsi ini tentunya tidak lepas dari bantuan dari berbagai pihak,
baik secara langsung maupun secara tidak langsung. Oleh karena itu penulis hendak
mengucapkan terima kasih kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Phebe Hendra, M.Si., Ph.D., Apt., selaku Dosen Pembimbing skripsi ini atas
segala kesabaran untuk selalu membimbing, memberi motivasi, dan memberi
masukan kepada penulis dalam menyusun skripsi ini.
3. Ibu dr. Fenty, M. Kes., Sp. PK, selaku Dosen Penguji skripsi atas bantuan dan
masukkan kepada penulis demi kemajuan skripsi ini.
4. Bapak Prof., Dr. CJ Soegihardjo, Apt., selaku Dosen Penguji skripsi atas bantuan
dan masukkan, kepada penulis demi kemajuan skripsi ini.
5. Ibu Rini Dwiastuti, M.Si., Apt., selaku Kepala Penanggung Jawab Laboratorium
Fakultas Farmasi yang telah memberi izin dalam penggunaan fasilitas
laboratorium Farmakologi-Toksikologi, Farmakognosi-Fitokimia dan Farmasi
viii
6. Pak Parjiman selaku laboran Laboratorium Farmakologi-Toksikologi, Pak Heru
selaku laboran Laboratorium Biofarmasetika-Farmakokinetika, Pak Kayat selaku
laboran Laboratorium Biokimia dan Pak Ratijo selaku laboran Laboratorium
Hayati, Pak Wagiran, selaku laboran Laboratorium Farmakognosi-Fitokimia, Pak
Agung selaku laboran Laboratorium Farmasi Fisika, serta Pak Andri selaku
laboran di kebun obat, atas segala bantuan dan kerja sama selama di
laboratorium.
7. Papa, mama, kakak, adik, dan saudara yang telah membantu dari awal sampai
akhir penelitian ini, atas doa, dukungan semangat dan perhatiannya.
8. Aloysius Gonzaga Jati Panantya sebagai teman seperjalanan, sahabat setia, yang
tak pernah kurang dan tak pernah habis, atas doa, kasih sayang, perhatian,
bantuan, motivasi dan waktunya yang telah membantu dari awal sampai akhir
penelitian ini.
9. Rekan-rekan penelitian tim macaranga, Nanda Chris Nurcahyanti, Theresia Garri
Windrawati, Fransisca Devita Risti W., Christine Herdyana Febrianti, Bernadetta
Amilia, A.M. Inggrid Silli dan Luluk Rahendra Martha atas bantuan, kerjasama,
perjuangan dan suka duka yang telah kita alami bersama selama penelitian.
10. Teman-teman FKK B atas kebersamaan kita.
11. Pihak-Pihak lain yang turut membantu penulis namun tidak dapat disebutkan
satu persatu.
Penulis menyadari bahwa setiap manusia tidak ada yang sempurna. Oleh
karena itu, penulis mengharapkan adanya kritik, saran dan masukan demi kemajuan
ix
bagi perkembangan ilmu pengetahuan khususnya di bidang kefarmasian, serta semua
pihak, baik mahasiswa, lingkungan akademis, maupun masyarakat.
Yogyakarta, 19 Desember 2012
x
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH.. v
PERNYATAAN KEASLIAN KARYA ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xvii
INTISARI ... xviii
ABSTRACT ... xix
BAB I. PENDAHULUAN ... 1
A.Latar Belakang... 1
B.Rumusan Masalah ... 4
C.Keaslian Penelitian ... 4
D.Manfaat Penelitian ... 5
xi
BAB II. PENELAAHAN PUSTAKA ... 7
A. Tanaman Macaranga tanarius L. ... 7
1. Sinonim... 7
2. Nama daerah ... 7
3. Taksonomi ... 7
4. Kandungan tanaman ... 7
B. Hepar ... 10
1. Anatomi dan fisiologi hati ... 10
2. Kerusakan hati ... 12
C. Hepatotoksin ... 15
D. Karbon Tetraklorida ... 17
E. Metanol ... 20
F. Metode Ekstraksi ... 20
G. Pengukuran Serum ALT dan AST ... 22
H. Landasan Teori ... 23
I. Hipotesis ... 24
BAB III. METODE PENELITIAN ... 25
A.Jenis dan Rancangan Penelitian... 25
B.Variabel Penelitian dan Definisi Operasional... 25
1. Variabel Penelitian ... 25
2. Definisi Operasional ... 26
C. Bahan Penelitian ... 27
xii
2. Bahan Kimia ... 27
D. Alat Penelitian ... 29
E. Tata Cara Penelitian ... 30
1. Determinasi daun M. tanarius ... 30
2. Pengumpulan bahan... 30
3. Pembuatan serbuk ... 30
4. Pembuatan ekstrak metanol : air daun M. tanarius ... 30
5. Penetapan konsentrasi pekat ekstrak ... 30
6. Pembuatan dosis ekstrak metanol : air daun M. tanarius ... 32
7. Pembuatan larutan karbon tetraklorida dalam olive oil ... 32
8. Uji pendahuluan ... 32
9. Pengelompokan dan perlakuan hewan uji ... 33
10. Pengukuran aktivitas ALT dan AST serum ... 34
11. Perhitungan efek hepatoprotektif ... 35
F. Tata Cara Analisis Hasil ... 35
BAB IV. HASIL DAN PEMBAHASAN ... 36
A.Penyiapan Bahan ... 36
1. Hasil determinasi tanaman ... 36
2. Pembuatan serbuk daun M. tanarius ... 37
3. Penetapan kadar air serbuk daun M. tanarius ... 37
xiii
C.Uji Pendahuluan ... 40
1. Penentuan dosis hepatotoksik ... 40
2. Penentuan dosis ekstrak metanol-air daun M. tanarius ... 40
3. Penentuan waktu pencuplikan darah ... 40
D.Efek Hepatoprotektif Jangka Pendek Ekstrak Metanol-Air Daun M. tanarius Terhadap Tikus Jantan Terinduksi Karbon Tetraklorida ... 45
1. Kontrol negatif... 46
2. Kontrol hepatotoksin ... 48
3. Kontrol perlakuan ... 49
4. Perlakuan Jangka Pendek Ekstrak Metanol-Air Daun M. tanarius Terhadap Tikus Terinduksi Karbon Tetraklorida ... 50
E. Rangkuman Pembahasan ... 57
BAB V. KESIMPULAN DAN SARAN ... 59
A.Kesimpulan ... 59
B.Saran ... 59
DAFTAR PUSTAKA ... 60
LAMPIRAN ... 65
xiv
DAFTAR TABEL
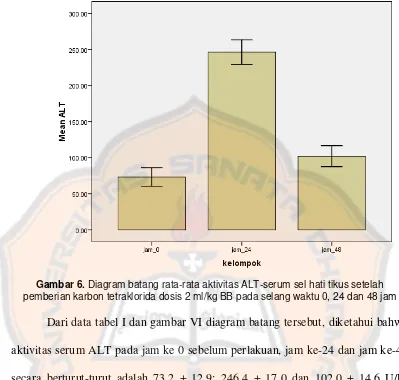
Tabel I. Aktivitas serum ALT setelah pemberian karbon tetraklorida dosis
2 ml/kg BB pada selang waktu 0, 24 dan 48 ... 41
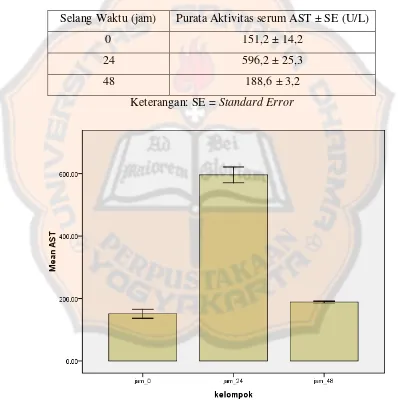
Tabel II. Aktivitas serum AST setelah pemberian karbon tetraklorida dosis
2 ml/kg BB pada selang waktu 0, 24 dan 48 ... 43
Tabel III. Perbedaan kenaikan aktivitas serum ALT setelah pemberian karbon
tetraklorida dosis 2 ml/kg BB pada waktu pencuplikan darah jam ke 0,
24 dan 48 ... 44
Tabel IV. Perbedaan kenaikan aktivitas serum AST setelah pemberian karbon
tetraklorida dosis 2 ml/kg BB pada waktu pencuplikan darah jam ke 0
24 dan 48 ... 45
Tabel V. Pengaruh perlakuan jangka pendek ekstrak metanol-air daun M. tanarius
3840 mg/kg BB berdasarkan aktivitas serum ALT dan AST pada
beberapa variasi waktu terhadap hepatotoksin karbon tetraklorida ... 46
Tabel VI. Perbandingan aktivitas serum ALT jam ke-0 dengan perlakuan
kontrol negatif olive oil ... 47
Tabel VII. Perbandingan aktivitas serum AST jam ke-0 dengan perlakuan
kontrol negatif olive oil ... 47
Tabel VIII. Perbandingan aktivitas serum ALT kontrol perlakuan dengan
kontrol hepatotoksin dan kontrol negatif... 50
Tabel IX. Perbandingan aktivitas serum AST kontrol perlakuan dengan
kontrol hepatotoksin dan kontrol negatif... 50
xv
pada perlakuan jangka pendek ekstrak metanol-air daun M. tanarius
3840 mk/kg BB berdasarkan aktivitas serum ALT pada beberapa
variasi waktu ... 51
Tabel XI. Perbandingan data berbeda bermakna dan berbeda tidak bermakna
pada perlakuan jangka pendek ekstrak metanol-air daun M. tanarius
3840 mk/kg BB berdasarkan aktivitas serum AST pada beberapa
xvi
DAFTAR GAMBAR
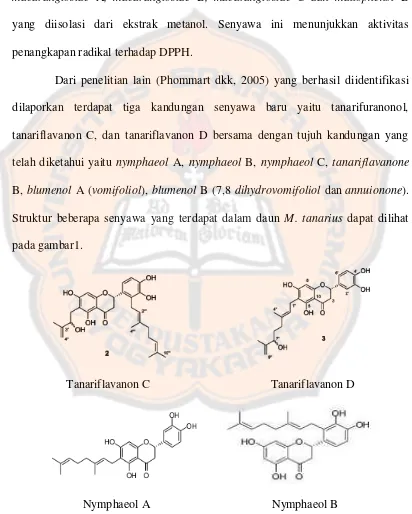
Gambar 1. Struktur senyawa yang terdapat pada daun M. tanarius... ... 8
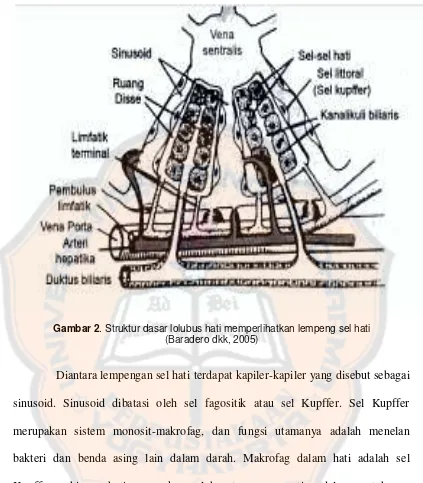
Gambar 2. Struktur dasar lolubus hati memperlihatkan lempeng sel hati... 11
Gambar 3. Struktur kimia karbon tetraklorida... 17
Gambar 4. Kenaikan relatif aktivitas serum ALT dan AST... 18
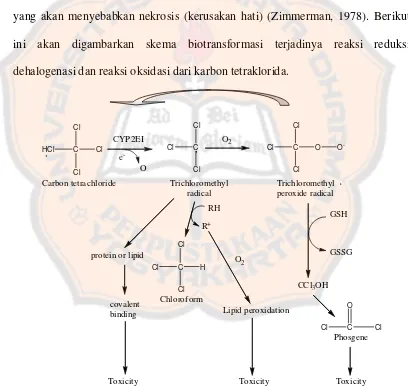
Gambar 5. Mekanisme biotrasformasi dan oksidasi karbon tetrakloria... 19
Gambar 6. Diagram batang rata-rata aktivitas ALT serum sel hati tikus setelah pemberian karbon tetraklorida dosis 2 ml/kg BB pada selang waktu 0, 24 dan 48 jam... 42
Gambar 7. Diagram batang rata-rata aktivitas AST serum sel hati tikus setelah pemberian karbon tetraklorida dosis 2 ml/kg BB pada selang waktu 0, 24 dan 48 jam... 43
Gambar 8. Diagram batang rata-rata pengaruh perlakuan jangka pendek pemberian ekstrak metanol-air terhadap hepatotoksin karbon tetraklorida dilihat dari aktivitas serum ALT... 51
xvii
DAFTAR LAMPIRAN
Lampiran 1. Foto daun M. tanarius ... 66
Lampiran 2. Foto ekstrak metanol-air daun M. tanarius ... 66
Lampiran 3. Surat pengesahan determinasi tanaman M. tanarius ... 67
Lampiran 4. Surat Etikal Clearance ... 68
Lampiran 5. Hasil Uji Kolmogorov-Smirnov dilanjutka Anova One-Way data ALT pada orientasi waktu pengambilan pencuplikan darah setelah pemberian karbon tetraklorida dengan dosis 3840 mg/kgBB... 69
Lampiran 6. Hasil Uji Kolmogorov-Smirnov dilanjutka Anova One-Way data AST pada orientasi waktu pengambilan pencuplikan darah setelah pemberian karbon tetraklorida dengan dosis 3840 mg/kgBB... 76
Lampiran 7. Hasil rendemen ekstrak metanol-air daun M. tanarius ... 82
xviii
INTISARI
Penelitian ini bertujuan untuk mengetahui efek pemberian jangka pendek ekstrak metanol-air daun Macaranga tanarius L., untuk menurunkan aktivitas ALT
dan AST serum sehingga dapat digunakan sebagai hepatoprotektor. Dari penelitian ini juga dapat diketahui lama waktu efektif yang diperlukan untuk memberikan efek hepatoprotektif.
Penelitian ini bersifat eksperimental murni dengan rancangan acak lengkap pola searah. Penelitian ini menggunakan tikus jantan galur Wistar, umur 2-3 bulan, dan berat ± 150-200 gram. Kelompok I merupakan kontrol hepatotoksin CCl4 dengan
dosis 2,8 ml/kg BB secara intra peritonial. Kelompok II merupakan kontrol negatif yaitu pemberian olive oil 2 ml/kg BB secara intra peritonial. Kelompok III merupakan
kontrol perlakuan yaitu pemberian ekstrak metanol-air daun M. tanarius dosis 5 g/kg BB secara per oral. Kelompok IV-VIII diberikan ekstrak metanol-air daun M. tanarius dengan dosis 3840 mg/kg BB, kemudian secara berturut-turut pada ½, 1, 2, 4
dan 6 jam setelah perlakuan diberikan dosis hepatotoksik CCl4 dengan dosis 2 ml/kg
BB. Pada jam ke-24 setelah diberi CCl4, semua kelompok diambil darahnya pada
daerah sinus orbitalis di mata tikus. Data ALT dan AST serum yang didapat, dianalisis dengan uji Kolmogorov-Smirnov untuk melihat distribusi datanya kemudian
dilanjutkan analisis dengan uji Scheffe untuk mengetahui perbedaan aktivitas ALT dan AST serum antar kelompok.
Dari data pengukuran aktivitas serum ALT dan AST yang diperoleh waktu paling efektif menunjukkan efek hepatoprotektif adalah pada jam ke-½.
xix
ABSTRACT
This study is aimed to determine the effects of short-term administration of methanol-water extract of Macaranga tanarius L. leave; to decrease the activity of
ALT and AST serum, as a result, it can be used as a hepatoprotector. This study also measures the effective time allocation in providing effective hepatoprotective effects.
This is pure experimental study using completely randomized design. This study uses male Wistar rats, attain the age of 2-3 months and ±150-200 grams weight. Group I was the hepatotoxins CCl4 control at a dose of 2.8 ml/kg body weight which
was injected intraperitoneally. Group II was the negative control which was given olive oil 2 ml/kg body weight intraperitoneally. Group III was the control treatment given methanol-water extract of M. tanarius leave orally at a dose of 5 g/kg body
weight. Group IV-VIII were given the methanol-water extract of M. tanarius leave at
a dose of 3840 mg/kg, afterward, the treatment was given hepatotoxic dose of CCl4 at
a dose of 2 ml/kg at ½, 1, 2, 4 and 6 hours successively. At the 24th hour after being
given CCl4, all groups have blood drawn at the orbital sinus region in the rats’ eyes.
ALT data and AST serum which were obtained were analyzed using
Kolmogorov-Smirnov test to look at the data distribution, after that, the data were analyzed using
Scheffe test to determine the differences in ALT activities and AST serum in each
group.
From the data measurement of serum ALT activities and serum AST activities which were obtained, the most effective time showing hepatoprotective effect was shown at the beginning of the ½ hour.
1
BAB I
PENGANTAR
A. Latar Belakang Penelitian
Hati merupakan organ vital yang berfungsi vaskuler untuk menyimpan dan
menyaring darah, metabolisme dan sekresi atau eksresi, yang berperan dalam
pembentukan empedu yang mengalir melalui saluran empedu ke pencernaan, serta
fungsi pertahanan tubuh melalui detoksifikasi dan fungsi perlindungan (Guyton
dan Hall, 2010). Adanya kerusakan pada hati dapat disebabkan oleh
mikroorganisme maupun senyawa kimia (obat-obatan) (Donatus, 1992). Menurut
WHO (2012), kanker hati yang disebaban oleh adanya virus (mikoorganisme)
seperti virus HBV dan HCV menyebabkan kematian sebesar 20% di negara maju
dan negara berkembang, sedangkan di negara dengan kondisi menengah kebawah
memiliki tingkat resiko kematian lebih besar, sekitar 70%. Pada tahun 2008,
Kanker hati memiliki tingkat kematian ketiga setelah kanker paru dan lambung.
Obat dan zat beracun dapat menyebabkan sekitar 10% dari seluruh kasus hepatitis,
atau sekitar 20-30% dari kasus penyakit hati akut (Cadman, 2000).
Salah satu senyawa yang dapat digunakan sebagai senyawa model yang
dapat menyebabkan kerusakan hati adalah karbon tetraklorida (CCl4). Karbon
tetraklorida merupakan yang biasa digunakan sebagai pelarut, cairan pencuci, dan
digunakan dalam pembuatan bahan-bahan plastik, tinta, bahan semikonduktor
karsinogen dan berpengaruh pada penipisan lapisan ozon di atmosfer (Bruckner
dan Warren, 2001).
Banyak orang di dunia ini yang terpapar karbon tetraklorida di lingkungan
kerja. Kazanthis, Bomford, Oxon (1960) melaporkan bahwa 17 karyawan pabrik
pengolahan kuarsa dievakuasi karena terpapar uap karbon tetraklorida dan 15
pekerjanya mengeluhkan gejala mual, anoreksia, muntah perut kembung,
ketidaknyamanan epigastrium, pusing sampai 4 bulan sebelum evaluasi.
Dampak dari terkena paparan karbon tetraklorida jangka panjang ini dapat
menyebabkan terjadinya kerusakan hati. Menurut data yang ada di WHO (2012)
pada tahun 2008 kanker hati mengakibatkan 695.000 kematian. Kanker ini dapat
diakibatkan senyawa kimia karsinogen ataupun karsinogen biologi seperti infeksi
virus, bakteri, maupun parasit. Pada tahun 2008 (WHO, 2008a; 2008b) dilaporkan
kejadian hepatitis akibat virus seperti VHA terjadi 1,4 juta kasus dan 2 milyar
orang terinfeksi VHB dengan 350 juta orang diantaranya menderita hepatitis
kronis.
Dengan adanya tumbuh-tumbuhan dapat menjadi suatu alternatif
pengobatan yang dilakukan untuk mencegah bahkan mengobati penyakit
(Donatus, 1992). Salah satu tumbuhan yang dapat berpotensi sebagai
hepatoprotektor adalah Macaranga tanarius L. Berdasarkan penelitian terakhir
mengenai M. tanarius., dilaporkan oleh Nugraha (2010) dan Mahendra (2010)
bahwa infusa daun M. tanarius dapat digunakan sebagai hepatoprotektor. Pada
penelitian tersebut, digunakan model senyawa hepatotoksin parasetamol dosis
tanarius, dapat digunakan untuk sebagai hepatoprotektor dengan senyawa model
yang digunakan adalah parasetamol.
Berdasarkan penelitian Matsunami, Takamori, Shinzato, Aramoto, Kondo,
Otsuka (2006), tanaman M. tanarius, mempunyai aktivitas sebagai antioksidan
yang sangat bermanfaat untuk kesehatan, yaitu macarangiosida A-D, dan
malofenol B yang didapat dari isolasi ekstrak metanol daun M. tanarius, yang
mana mempunyai aktivitas penangkapan terhadap DPPH.
Dari hasil penelitian yang dilakukan oleh Matsunami, dkk (2006) meneliti
bahwa senyawa antioksidan yang dapat didapatkan dari daun M. tanarius adalah
dari hasil isolasi ekstrak metanol yang bersifat polar. Oleh karena itu, maka
metanol-air, diharapkan dapat diperoleh senyawa antioksidan yang mencegah
aktivitas radikal bebas dari karbon tetraklorida. Dari uraian diatas, maka
penelitian ini dilakukan untuk mengetahui efek hepatoprotektif jangka pendek
ekstrak metanol-air daun M. tanarius pada tikus jantan terinduksi karbon
tetraklorida.
Penelitian efek hepatoprotektif jangka pendek ekstrak metanol-air daun M.
tanarius terhadap tikus yang terinduksi karbon tetraklorida ini dilakukan untuk
membandingkan dengan penelitian efek hepatoprotektif jangka panjang ekstrak
metanol-air daun M. tanarius terhadap tikus yang terinduksi karbon tetraklorida
(Windrawati, 2012) yang juga dilaksanakan bersamaan. Oleh karena itu,
penelitian ini menarik untuk diteliti karena penelitian menggunakan ekstrak
metanol-air daun M. tanarius jangka pendek dan belum pernah dilakukan
B. Rumusan Masalah
1. Apakah praperlakuan jangka pendek ekstrak metanol-air daun Macaranga
tanarius L. mempunyai efek hepatoprotektif pada tikus yang terinduksi
karbon tetraklorida yang dengan melihat adanya penurunan aktivitas serum
Alanine Aminotransferase (ALT) dan serum Aspartate Transaminase
(AST)?
2. Berapakah waktu paling efektif ekstrak metanol-air daun Macaranga
tanarius L. untuk menimbulkan efek hepatoprotektif pada tikus yang
terinduksi karbon tetraklorida?
C. Keaslian Penelitian
Penelitian yang menggunakan M. tanarius pernah dilakukan oleh Phommart, Sutthivaiyakit, Chimnoi, Ruchirawat, Sutthivaiyakit (2005) dan Matsunami dkk
(2006), Matsunami dkk ( 2009). Phommart, dkk (2005) melaporkan kandungan
tanaman M. tanarius. Mahendra (2010) bahwa infusa daun M. tanarius dapat
digunakan sebagai hepatoprotektor jangka panjang dan Nugraha (2010
melaporkan bahwa infusa daun M. tanarius dapat digunakan sebagai
hepatoprotektor jangka pendek. Selain itu, Adrianto (2010) melaporkan ekstrak
metanol-air daun M. tanarius, dapat digunakan untuk sebagai hepatoprotektor
dengan senyawa model parasetamol. Kurniawati (2010) melaporkan ekstrak
metanol-air daun M. tanarius sebagai antiinflamasi. Dari hasil penelitian Andini
(2010), ekstrak metanol-air daun M. tanarius memiliki efek analgesik. Dari
metanol-air daun M. Tanarius dengan metformin memiliki efek antidiabetik.
Selain itu, berdasarkan hasil penelitian yang dilakukan oleh Windrawati (2013)
bahwa daun M. tanarius memiliki efek hepatoprotektif jangka panjang.
Berdasarkan penelusuran pustaka, efek hepatoprotektif jangka pendek ekstrak
metanol-air daun M. tanarius terhadap tikus terinduksi karbon tetraklorida belum
pernah dilakukan.
D. Manfaat Penelitian
1. Manfaat teoritis
Penelitian ini diharapkan dapat bermanfaat bagi pengembangan ilmu
pengetahuan khususnya ilmu kefarmasian mengenai pemberian ekstrak
metanol-air daun M. tanarius yang memiliki efek hepatoprotektif jangka
pendek.
2. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi kepada masyarakat
mengenai manfaat daun M. tanarius yang memiliki efek hepatoprotektif
jangka pendek.
E. Tujuan Penelitian
1. Tujuan umum
Untuk membuktikan adanya efek hepatoprotektif pemberian ekstrak
karbon tetraklorida dengan cara melihat adanya pernurunan aktivitas serum
ALT dan serum AST.
2. Tujuan khusus:
Secara khusus penelitian ini bertujuan untuk mengetahui waktu paling efektif
yang dapat memberikan efek hepatoprotektif dari ekstrak metanol-air jangka
pendek daun M. tanarius untuk menimbulkan efek hepatoprotektif pada tikus
7
BAB II
PENELAAHAN PUSTAKA
A. Tanaman Macaranga tanarius L.
1. Sinonim
Ricinus tanarius L., Macaranga molliuscula Kurz, Macaranga tanarius
var. Glabra F. Muell. (Asian Plant, 2012).
2. Nama Daerah
Mara, Tutup merah, Sapat (Plantamor, 2008)
3. Taksonomi
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh)
Superdevisi : Spermatophyta (Menghasilkan biji)
Divisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping dua / dikotil)
Subkelas : Rosidae
Ordo : Euphorbiales
Famili : Euphorbiaceae
Genus : Macaranga
Spesies : Macaranga tanarius L. (Plantamor, 2008).
4. Kandungan
Penelitian mengenai tanaman Macaranga tanarius L. sudah banyak
diisolasi dan diidentifikasi. Pada penelitian Matsunami dkk. (2006), Matsunami
dkk. (2009) diketahui bahwa dalam daun M. tanarius, yaitu macarangiosida D,
dan laurosida E, metil brevifolin karboksilat, dan larutan hiperin dan isokuercitin,
macarangioside A, macarangioside B, macarangioside C dan mallophenol B
yang diisolasi dari ekstrak metanol. Senyawa ini menunjukkan aktivitas
penangkapan radikal terhadap DPPH.
Dari penelitian lain (Phommart dkk, 2005) yang berhasil diidentifikasi
dilaporkan terdapat tiga kandungan senyawa baru yaitu tanarifuranonol,
tanariflavanon C, dan tanariflavanon D bersama dengan tujuh kandungan yang
telah diketahui yaitu nymphaeol A, nymphaeol B, nymphaeol C, tanariflavanone
B, blumenol A (vomifoliol), blumenol B (7,8 dihydrovomifoliol dan annuionone).
Struktur beberapa senyawa yang terdapat dalam daun M. tanarius dapat dilihat
pada gambar1.
Tanariflavanon C Tanariflavanon D
Nymphaeol A Nymphaeol B
5. Khasiat dan kegunaan
Daun M. tanarius juga memiliki banyak kegunaan, penelitian yang
dilakukan oleh Phommart dkk. (2005) akar tanaman M. tanarius digunakan
sebagai antipiretik dan antitusif, sedangkan daun M. tanarius memiliki efek
antiinflamasi. Daun M. tanarius yang kaya akan tanin, dapat digunakan sebagai
obat diare, luka dan antiseptik (Lin, Nonaka, Nishioka, 1990).
Berdasarkan penelitian lainnya yang dilakukan oleh Ardianto (2010),
ekstrak metanol-air daun tanaman Macaranga tanarius L. memiliki khasiat
sebagai hepatoprotektif jangka panjang. Infusa infusa daun M. tanarius dapat
digunakan sebagai hepatoprotektor jangka panjang yang dilaporkan oleh
Mahendra (2010). Selain itu, Nugraha (2010) melaporkan bahwa infusa daun M.
tanarius juga memiliki khasiat sebagai efek hepatoprotektif jangka pendek.
Dari penelitian lain, dilaporkan oleh Andini (2010) ekstrak metanol-air
daun M. tanarius memiliki efek analgesik. Selain itu, pada tahun 2010,
Kurniawati melaporkan hasil penelitian bahwa ekstrak metanol-air daun M.
tanarius memiliki efek antiinflamasi. Daun M. tanarius secara tradisional
digunakan untuk fermentasi tempe dan pakan hewan (Puteri dan Kawabata, 2010).
Khasiat lain yang diteliti pada daun M. tanarius adalah melalui penelitian terbaru
mengenai daun M. tanarius, dilaporkan oleh Oktavia (2012), bahwa kombinasi
ekstrak metanol-air daun M. tanarius dengan metformin dapat digunakan sebagai
antidiabetes. Penelitian terbaru yang dilakukan oleh Windrawati (2013) mengenai
efek hepatoprotektif jangka panjang ekstrak metanol-air daun M. tanarius
B. Hepar
1. Anatomi dan Fisiologi Hati
Hepar adalah kelenjar yang paling besar dalam tubuh manusia dengan
berat 1500 g (Baradero, Dayrit, Siswadi, 2005). Fungsi hati adalah pembentukan
empedu, penyimpanan karbohidrat, pembentukan benda keton, pengaturan
metabolisme karbohidrat, reduksi dan konjugasi hormon steroid adrenal dan
kelenjar kelamin, detoksikasi obat-obatan dan toksin, membentuk protein-protein
plasma dan banyak fungsi penting dalam metabolisme lemak (Ganong, 2001).
Unit dasar fungsional dasar hati adalah lolubus hati, yang berbentuk
silindris dengan panjang dan diameter tertentu. Hati manusia mengandung 50.000
sampai 100.000 lolubus (Guyton dan Hall, 2007). Hati memiliki dua lobus utama
yaitu kanan dan kiri. Setiap lobus hati terbagi menjadi struktur-struktur yang
disebut sebagai lobulus, setiap lobulus merupakan badan heksagonal yang terdiri
atas lempeng-lempeng sel hati berbentuk kubus, tersusun radial mengelilingi vena
sentralis yang mengalirkan darah dari lobulus (Price dan Wilson, 2005).
Lolubus hati terbentuk mengelilingi sebuah vena sentralis yang mengalir
ke vena hepatika dan kemudian ke vena cava. Lolubus sendiri dibentuk terutama
dari banyak lempeng sel hati yang menyebar dari vena sentralis seperti jeruji roda.
Masing-masing lempeng sel hati tebalnya dua sel, dan diantara sel yang
berdekatan terdapat kanalikuli biliaris kecil yang mengalir ke duktus biliaris di
dalam septum fibrosa yang memisahkan lolubus hati yang berdekatan (Guyton
Gambar 2. Struktur dasar lolubus hati memperlihatkan lempeng sel hati (Baradero dkk, 2005)
Diantara lempengan sel hati terdapat kapiler-kapiler yang disebut sebagai
sinusoid. Sinusoid dibatasi oleh sel fagositik atau sel Kupffer. Sel Kupffer
merupakan sistem monosit-makrofag, dan fungsi utamanya adalah menelan
bakteri dan benda asing lain dalam darah. Makrofag dalam hati adalah sel
Kupffer, sehingga hati merupakan salah satu organ penting dalam pertahanan
melawan invasi bakteri dan agen toksik (Price dan Wilson, 2005).
Hati dalam kondisi normal memiliki kapasitas fungsional yang besar.
Kemampuan hati di dalam tubuh antara lain untuk sintesis, eksresi dan berfungsi
dalam proses metabolisme. Hati merupakan sumber dari plasma albumin, globulin
dikeluarkan oleh hati melalui empedu. Komponen utama dari empedu adalah
bilirubin, selain itu kolesterol, urobilinogen dan asam empedu juga terdapat dalam
empedu. Pada fungsi metabolisme, hati memetabolisme lemak, karbohidrat,
protein dan detoksifikasi. Hati memegang peranan penting dalam
menawar-racunkan racun berbahaya turunan senyawa nitrogen yang berasal dari usus,
obat-obatan dan senyawa kimia. (Candrasoma dan Taylor, 1995).
Selain itu, hati memiliki kemampuan untuk mengembalikan dirinya
sendiri setelah kehilangan jaringan hati. Proses ini disebut regenerasi sel hati.
Selama regenerasi sel hati, hepatosoit diperkirakan mengalami replikasi sebanyak
satu sampai dua kali dan setelah tercapai ukuran dan volume hati sebelumnya,
hepatosit kembali kepada keadaan sebelumnya (Guyton dan Hall, 2007).
Peran penting hati dalam eliminasi obat adalah untuk memetabolisme
obat induk dan merubahnya menjadi senyawa metabolit. Kapasitas dari hati untuk
mengubah obat induk menjadi metabolit sangat dipengaruhi oleh aktivitas enzim
pemetabolisme yang terdapat pada retikulum endoplasma halus dan sitosol pada
hepatosit (DiPiro dkk, 2008).
2. Kerusakan Hati
Hati merupakan organ penting yang dapat mengubah struktur dari senyawa
kimia dan obat-obatan. Beberapa hasil dari proses terjadinya metabolisme secara
biologis dapat menjadi tidak aktif, beberpa menjadi metabolit yang aktif dan
Konsekuensi klinis paling parah penyakit hati akibat terjadinya kerusakan
hati adalah gagal hati. Hal ini dapat terjadi akibat kerusakan hati yang mendadak
dan masif. Gagal hati umumnya merupakan titik akhir kerusakan progresif hati
sebagai bagian dari penyakit hati kronik. Umumnya, sekitar 80%-90% kapasitas
fungsional hati sudah rusak sebelum gagal hati timbul (Kumar, Abbas, Fausto,
Mitchell, 2007).
Senyawa toksik dapat menyebabkan berbagai jenis efek toksik pada
berbagai organel dalam sel hati. Jenis kerusakannya, antara lain:
1. Steatosis (Perlemakan hati).
Perlemakan hati adalah hati yang mengandung berat lipid lebih dari 5%.
Adanya kelebihan lemak dalam hati dapat dibuktikan secara histokimia (Lu,
1995). Ketika senyawa toksin seperti alkohol masuk ke dalam tubuh dengan
jumlah yang cukup, maka akan menimbulkan terbentuknya lipid yang
terakumulasi dalam hepatosit. Ketika jumlah senyawa toksin yang terpapar ke
dalam tubuh jumlahnya semakin banyak maka lipid akan semakin terakumulasi
dan menciptakan gelembung-gelembung besar, dan meluas hingga ke tepi hati
(Kumar dkk, 2007).
Berbagai macam toksikan menyebabkan terjadinya penimbunan lemak di
dalam hati, mekanisme yang mendasari sangat beragam. Mekanisme yang paling
umum adalah terjadinya pelepasan trigliserid hati ke plasma, karena trigliserid
hati hanya disekresi bila dalam keadaan tergabung dengan lipoprotein.
Penimbunan lipid juga melalui beberapa mekanisme, seperti penghambatan
etionin); penekanan konjugasi trigliserid dengan lipoprotein (misalnya karbon
tetraklorida); rusaknya oksidasi lipid oleh mitokondria (misalnya etanol) (Lu,
1995).
2. Nekrosis hati
Nekrosis hati adalah kematian hepatosit. Nekrosis dapat bersifat fokal
(sentral, tengah dan perifer) atau masif. Biasanya nekrosis merupakan kerusakan
akut. Beberapa zat kimia telah dilaporkan menyebabkan nekrosis akut. Nekrosis
hati merupakan suati manifestasi toksik yang berbahaya tetapi tidak selalu kritis
karena hati mempunyai kapasitas pertumbuhan kembali yang luar biasa. Kematian
sel terjadi bersama dengan pecahnya membran plasma. Perubahan biokimia pada
nekrosis hati bersifat kompleks (Lu, 1995).
3. Sirosis
Sirosis ditandai oleh adanya septa kolagen yang tersebar di sebagian besar
hati. Patogenesis terjadinya sirosis hati dalam sebagian kasus tampaknya berasal
dari nekrosis sel tunggal karena kurangnya mekanisme perbaikan sel dari hati.
Keadaan ini menyebabkan aktivitas fibroblastik dan pembentukan jaringan parut.
Karsinogen kimia dan pemberian CCl4 jangka panjang dapat menyebabkan sirosis
hati pada hewan. Pada manusia, terjadinya sirosis hati karena konsumsi kronis
minuman beralkohol (Lu, 1995).
4. Kanker hati
Karsinoma hepatoseluler merupakan terjadinya kerusakan hati yang paling
berat. Sejumlah besar senyawa toksik dapat menyebabkan kanker hati pada hewan
Kerusakan sel hati dibagi menjadi dua, yaitu:
a. Kerusakan sel hati akut
Kerusakan sel hati akut dapat terjadi karena nekrosis besar pada hati, yang
disebabkan karena infeksi viral, obat-obat yang merusak hati, maupun induksi
senyawa kimia. Kerusakan sel hati akut ditandai dengan adanya penyakit kuning,
hipoglikemia, gangguan elektrolit dan asam-basa, enselophati hati, dan kenaikan
serum enzim (alanin transferase dan aspartate transaminase) pada kasus terjadinya
nekrosis hati (Chandrasoma dan Taylor, 1995).
b. Kerusakan sel hati kronik
Kerusakan sel hati kronik biasanya merupakan hasil dari sirosis yang
merupakan tahap lanjut dari nekrosis, fibrosis, dan regenerasi nodular
(Chandrasoma dan Taylor, 1995). Pada keadaan nekrosis terjadi pemecahan sel
hepatosit sehingga enzim alanin transferase (ALT) yang terdapat dalam sel hati
keluar dan masuk ke aliran darah dan ditandai dengan peningkatan aktivitas ALT
(Zimmerman, 1978).
C. Hepatotoksin
Banyak kerusakan hati seperti yang diuraikan diatas yaitu steatosis,
nekrosis, sirosis yang disebabkan oleh paparan senyawa toksik (hepatotoksin).
Contohnya adalah paparan CCl4, kloroform, aflatoksin dan fosfor (Lu, 1995).
Hepatotoksin merupakan zat toksik yang dapat menyebabkan rusaknya sel hati
(Poppy, Komala, Santoso, Sulaiman, Rienita, Nuswantari, 1998). Obat dan
a. Hepatotoksin teramalkan (tipe A).
Merupakan obat atau senyawa yang bila diberikan dapat mempengaruhi
sebagian besar orang yang menelan senyawa tersebut dalam jumlah yang cukup
untuk menimbulkan efek toksik. Hepatotoksin teramalkan bergantung kepada
dosis pemberian (Forrest, 2006). Contoh hepatotoksin teramalkan adalah racun
jamur (Amanita phalloides), karbon tetraklorida, kloroform, parasetamol
(Chandrasoma dan Taylor, 1995).
Prosesnya dikenal sebagai toksisitas-intrinsik, dan aksinya dapat terjadi
secara langsung atau tidak langsung. Secara langsung, obat induk atau bentuk
metabolitnya langsung berikatan dengan komponen membran sel dan merusak sel
hati beserta seluruh organelnya, seperti ditunjukkan oleh karbon tetraklorida dan
parasetamol. Secara tidak langsung, obat induk atau bentuk metabolitnya dalam
menimbulkan luka hepatik dengan cara mengganggu jalur metabolik-khas atau
mengganggu jalur ekskresi hepatik (Donatus,1992).
b. Hepatotoksin takteramalkan (tipe B).
Merupakan obat atau senyawa yang tidak bersifat toksik pada hati tetapi
jika diberikan kepada orang tertentu akan dapat menimbulkan efek toksik.
Hepatotoksin jenis ini tidak bergantung pada dosis pemberian. Contoh obat-obat
D. Karbon tetraklorida
Gambar 3. Struktur kimia karbon tetraklorida (Pustakalaya, 2005)
Karbon tetraklorida merupakan senyawa kimia yang dengan rumus
molekul CCl4 dan memiliki rumus bangun seperti pada gambar 3. Karbon
tetraklorida merupakan cairan bening yang tidak mudah terbakar dan memiliki
bau yang khas, larut dalam etanol, aseton, benzen, karbon disulfida dan memiliki
kelarutan rendah dalam air (Oehha, 2000). Karbon tetraklorida pada masa lalu
digunakan sebagai cairan pemebersih, bahan yang digunakan untuk pemadam
kebakaran (Departement of Health and Human Services, 2005). Karbon
tetraklorida merupakan cairan bening yang sangat mudah menguap dan tidak
mudah terbakar Karbon tetraklorida merupakan senyawa kimia yang
dikhawatirkan dapat menyebabkan karsinogen dan dibuktikan melalui penelitian
terhadap hewan uji (Departement of Health and Human Services, 2011).
Hal ini dibuktikan dengan adanya beberapa penelitian. Frezza dkk (1994)
meneliti bahwa sekelompok tikus galur Sprague Dawley yang diinduksi karbon
tetraklorida mengalami kematian dan terjadi kanker hati. Pada tahun 1995,
penelitian mengenai hepatotoksin karbon tetraklorida dilakukan oleh Rosnalini
Penelitian lainnya mengenai karbon tetraklorida sebagai hepatotoksin dilaporkan
oleh Bulan, Pramono (2009) yang meneliti adanya perubahan kadar SGOT dan
SGPT setelah diberikan rebusan daun putri malu (Mimosa pudica, Linn) pada
tikus yang terinduksi karbon tetraklorida.
Karbon tetraklorida telah diketahui sebagai senyawa model yang dapat
menimbulkan nekrosis hepar dan perlemakan hati pada berbagai macam spesies.
Senyawa ini mudah larut dalam komponen lemak, yang mengakibatkan senyawa
ini terdistribusi ke seluruh tubuh, meskipun begitu efek utama ketoksikannya
adalah di hepar dengan cara pemberian apapun (Timbrell, 2008). Kerusakan hati
yang ditimbulkan oleh karbon tetraklorida dapat menaikkan aktivitas serum ALT
dan AST sebesar sekitar 4 kali dan 3 kali dari aktivitas serum normal. Berikut
adalah tingkat kenaikan relatif dari beberapa serum enzim dari terjadinya
keracunan hati.
Gambar 4. Kenaikan relatif aktivitas serum ALT dan AST (Zimmerman, 1999)
Karbon tetraklorida merupakan senyawa yang bersifat toksik karena akan
mengalami reaksi reduksi dehalogenasi membentuk radikal bebas yaitu radikal
triklormetil (CCl3). Radikal ini kemudian akan bereaksi dengan oksigen dan
dan Elstner, 1999). Kemudian radikal tersebut menginisiasi terjadinya radikal
lipid yang menyebabkan terbentuknya lipid hidroperoksidase (LOOH) dan radikal
lipid alkoksil (LO). Melalui proses fragmentasi, radikal lipid alkoksi tersebut
akan diubah menjadi malondialdehid (Gregus dan Klaaseen, 2001). Senyawa
aldehid inilah yang akan menyebabkan kerusakan pada membran plasma dan
meningkatkan permeabilitas membran (Bruckner dan Warren, 2001).
Senyawa radikal ini juga mengakibatkan kerusakan pada organela lain
yang akan menyebabkan nekrosis (kerusakan hati) (Zimmerman, 1978). Berikut
ini akan digambarkan skema biotransformasi terjadinya reaksi reduksi
dehalogenasi dan reaksi oksidasi dari karbon tetraklorida.
C
E. Metanol
Metanol (metil alkohol) yang memiliki struktur molekul CH3OH. Metanol
bersifat racun dan dapat mematikan bila ditelan. Kebutaan dapat pula terjadi
karena kontak dengan kulit atau penghirupan uapnya terlalu lama. Kebutaan orang
yang mencerna metanol disebabkan terbentuknya formaldehid (H2CO) yang dapat
merusakkan retina (Keenan, 1992).
Metanol adalah golongan senyawa alkohol yang paling sederhana, yang
berisi satu atom karbon. Kharakteristik dari metanol adalah berupa cairan, tidak
berwarna dan memiliki bau khas alkohol (Environmental Protection Agency,
1994). Metanol memiliki nilai indeks polaritas sebesar 5,1 dan termasuk senyawa
yang bersifat polar (Byers, 2003). Metanol banyak digunakan sebagai larutan
penyari yang digunakan pada saat maserasi. Pelarut ini diduga mampu melarutkan
hampir semua komponen, baik yang bersifat polar, semi polar maupun non polar
(Al-Ash’ary, Supriyanti, Zackiyah, 2010).
F. Metode Ekstraksi
Ekstraksi cair-cair digunakan sebagai cara untuk praperlakuan sampel
untuk memisahkan analit-analit dari komponen-komponen matriks yang mungkin
mengganggu pada saat pendeteksian analit. Disamping itu, ekstraksi pelarut juga
digunakan untuk memekatkan analit yang ada di dalam sampel dengan jumlah
kecil sehingga tidak menyulitkan proses pendeteksiannya. Analit-analit yang
mudah terekstraksi dalam pelarut organik adalah molekul-molekul netral yang
polar. Sementara itu, senyawa-senyawa polar dan juga senyawa-senyawa yang
mudah mengalami ionisasi akan tertahan dalam fase air (Sudjadi, 2007).
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang
tersisa diperlakukan sedemikian rupa hingga memenuhi baku yang telah
ditetapkan (Departemen Kesehatan RI , 1995).
Metode ekstraksi memilik beberapa metode ekstraksi, yang paling
sederhana adalah ekstraksi dingin. Dengan cara ini bahan kering hasil gilingan
diekstraksi pada suhu kamar secara berturut-turut dengan pelarut yang
kepolarannya makin tinggi: pertama heksana (atau petroleum eter), kemudian
kloroform (atau diklorometana), etil asetat, aseton, metanol dan akhirnya air
(Heinrich dan Barnes, 2009).
Keuntungan utama metode ini merupakan metode ekstraksi yang mudah
karena ekstrak tidak dipanaskan sehingga kemungkinan kecil bahan alam menjadi
terurai. Penggunaan pelarut dengan peningkatan kepolaran secara berurutan
memungkinkan pemisahan bahan-bahan alam berdasarkan kelarutannya
(polaritasnya) dalam pelarut ekstraksi. Ekstraksi dingin memungkinkan banyak
senyawa terekstraksi, meskipun beberapa senyawa memiliki kelarutan terbatas
dalam pelarut ekstraksi suhu kamar (Heinrich dan Barnes, 2009).
Metode maserasi merupakan cara penyarian sederhana yang dilakukan
dengan cara merendam serbuk simplisia dalam cairan penyari selama beberapa
digunakan untuk menyari simplisia yang mengandung komponen kimia yang
mudah larut dalam cairan penyari tidak mengandung benzoin, tiraks dan lilin.
(Sudjadi, 1986).
G. Pengukuran Serum ALT dan AST
Sejumlah pemeriksaan sering digunakan untuk menilai cedera hati.
Aspartat aminotransferase (AST) dan alanin aminotransferase (ALT) serum, yang
sering disebut uji fungsi hati, merupakan pengukuran kadar enzim-enzim yang
normalnya terletak di dalam hepatosit. Oleh karena itu keberadaan keduanya
dalam serum adalah tanda nekrosis sel hati dan bukan merupakan indikasi sejati
fungsi hati (McPhee dan Ganong, 2010).
Kerusakan sel-sel hati dapat dilihat dari peningkatan serum
aminotransferase secara signifikan yang mendahului terjadinya kenaikan jumlah
bilirubin total dan alkaline phospatase. Kebanyakan dari kerusakan hati dapat
terjadi satu tahun setelah pemaparan agen hepatotoksik (DiPiro dkk.,2008).
Saat terjadi nekrosis pada hepatosit, kebocoran pada associated plasma
membran dapat dideteksi secara biokimia dengan cara menganalisa plasma atau
serum untuk melihat enzim turunan sitosol yakni, lactate dehydrogenase (LDH),
alanine aminotransferase (ALT atau SGPT), aspartate aminotransferase (AST atau
H. Landasan Teori
Di dalam hati, terdapat bermacam-macam bentuk kerusakan hati.
Kerusakan hati akibat induksi obat yang biasa terjadi yaitu nekrosis (Forrest,
2006). Pada keadaan nekrosis terjadi pemecahan sel hepatosit sehingga enzim
ALT yang terdapat dalam sel hati keluar dan masuk ke aliran darah. Kerusakan ini
ditandai dengan adanya peningkatan aktivitas ALT (Zimmerman, 1978).
Karbon tetraklorida telah diketahui sebagai senyawa model yang dapat
menimbulkan toksisitas (Timbrell, 2008). Karbon tetraklorida ini bersifat toksik
karena akan mengalami reaksi reduksi dehalogenasi membentuk radikal bebas
yaitu radikal triklormetil (CCl3) (Gregus dan Klaaseen, 2001). Dengan bereaksi
dengan oksigen akan membentuk radikal triklorometil peroksi menginisiasi
terjadinya radikal lipid. Radikal lipid ini akan menyebabkan terbentuknya lipid
radikal lipid alkoksil (LO). Melalui proses fragmentasi, radikal lipid alkoksi
tersebut akan diubah menjadi malondialdehid (Gregus dan Klaaseen, 2001).
Senyawa aldehid ini yang akan menyebabkan kerusakan pada membran plasma
yang dapat mengakibatkan kerusakan pada sel-sel lainya termasuk sel hati.
Berdasarkan penelitian yang dilakukan Phommart (2005) menemukan
adanya senyawa flavonoid dari ekstrak n-heksana dan kloroform dari daun
Macaranga tanarius L. yang memiliki aktivitas antioksidan terhadap DPPH dan
berfunsi mencegah terjadinya oksidasi. Pada tahun 2010, Adrianto melaporkan
penelitian mengenai M. tanarius bahwa, ekstrak metanol-air daun tanaman M.
tanarius memiliki khasiat sebagai hepatoprotektif dengan senyawa penginduksi
hepatoprotektif, hal ini berdasarkan penelitian yang dilakukan oleh Mahendra
(2010) yang melaporkan bahwa infusa daun M. tanarius memiliki efek
hepatoprotektif jangka panjang dengan senyawa hepatotoksin parasetamol.
Nugraha (2010) juga melaporkan bahwa infusa daun M. tanarius juga memiliki
khasiat sebagai efek hepatoprotektif jangka pendek dengan menginduksi
parasetamol. Pada tahun 2012, Windrawati meneliti dari ekstrak metanol-air daun
M. tanarius yang memiliki efek hepatoprotektif jangka panjang.
I. Hipotesis
Ekstrak metanol-air daun Macaranga tanarius L., memiliki efek
25
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian mengenai efek hepatoprotektif ekstrak metanol-air daun
Macaranga tanarius L., terhadap tikus jantan merupakan jenis penelitian
eksperimental murni diberikan pelakuan terhadap sejumlah variabel penelitian.
Rancangan penelitian ini termasuk rancangan acak lengkap dengan menggunakan
rancangan acak lengkap pola searah.
B. Variabel dan Definisi Operasional
Variabel-variabel yang digunakan pada percobaan ini ialah:
1. Variabel penelitian
a. Variabel utama
1. Variabel bebas
Lama pemberian ekstrak metanol-air daun M. tanarius, yaitu
variasi jam pemberian ekstrak.
2. Variabel tergantung
Efek hepatoprotektif jangka pendek ekstrak metanol-air daun M.
tanarius, terhadap sel hati tikus yang terinduksi karbon tetraklorida,
dengan tolok ukur kuantitatif berdasarkan penurunan aktivitas serum ALT
b. Variabel pengacau
1. Variabel pengacau terkendali
Kondisi hewan uji yaitu subyek uji yang digunakan adalah tikus
galur Wistar, jenis kelamin jantan, berat badan 150-200 gram, dan umur
2-3 bulan. Frekuensi pemberian ekstrak metanol-air daun M. tanarius dan
cara pemberian ekstrak secara per oral. Bahan daun M. tanarius yang
dipanen dari Kebun Obat Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta pada bulan Mei 2012, cara penyimpanan serbuk daun M.
tanarius.
2. Variabel pengacau tak terkendali
Kondisi patologis hewan uji.
2. Definisi operasional
Definisi operasional penelitian ini adalah:
a. Ekstrak metanol-air daun M. tanarius
Ekstrak daun Macaranga tanarius L. adalah ekstrak kental yang
diperoleh dengan mengekstraksi serbuk kering daun M. tanarius seberat
10,0 gram yang dilarutkan dalam 100 ml pelarut metanol 50% secara
maserasi selama 72 jam, dengan putaran 140 rpm. Kemudian disaring
dengan kertas saring dan diuapkan di oven selama 24 jam pada suhu 50 C,
b. Efek hepatoprotektif
Efek hepatoprotektif adalah kemampuan ekstrak metanol-air daun M.
tanarius pada dosis tertentu dapat melindungi hepar dari hepatotoksin.
c. Jangka pendek, yaitu penelitian dilakukan dalam selang waktu ½, 1, 2, 4,
dan 6 jam.
C. Bahan Penelitian
1. Bahan utama
a. Hewan uji yang digunakan berupa tikus jantan galur Wistar, umur 2-3
bulan dengan berat badan berkisar antara 150-200 gram yang diperoleh
dari Laboratorium Imono Fakultas Farmasi, Universitas Sanata Dharma
Yogyakarta.
b. Bahan uji berupa daun M. tanarius yang dipanen dari Kebun Obat Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta pada bulan Mei 2012.
2. Bahan kimia
a. Pelarut ekstrak yang digunakan adalah metanol dan air yang diperoleh dari
Laboratorium Farmakognosi Fitokimia Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
b. Karbon tetraklorida (Merck) sebagai hepatotoksin yang berupa cairan,
tidak berwarna, berbau khas yang diperoleh dari Laboratorium Kimia
c. CMC-Na sebagai pelarut ekstrak kental dari daun M. tanarius berupa
sebuk, berwarna putih yang diperoleh dari Laboratorium
Farmakologi-Toksikologi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
d. Bahan pensuspensi karbon tetraklorida adalah olive oil (Bertolli) yang
berupa minyak.
e. Olive oil sebagai kontrol negatif.
f. Blanko pengujian ALT dan AST menggunakan aqua bidestilata (PT.
Ikapharmindo Putramas, Jakarta) yang diperoleh dari Laboratorium Kimia
Dasar Fakultas Farmasi Universitas Sanata Dharma.
g. Reagen DyaSyss untuk mengukur aktivitas serum ALT dan AST berupa
reagen SGPT dan SGOT.
h. Serum ALT
Reagen serum yang digunakan adalah reagen serum ALT DyaSyss.
Komposisi dan konsentrasi dari reagen serum ALT adalah sebagai berikut:
R1: TRIS pH 7,15 140 mmol/L
L-Alanine 700 mmol/L
LDH (lactatedehydrogenase) 2300 U/L
R2: 2-Oxoglutarate 85 mmol/L
NADH 1 mmol/L
Pyridoxal-5-phosphate
FS: Good’s buffer pH 9,6 100 mmol/L
i. Serum AST
Reagen serum yang digunakan adalah reagen serum AST DyaSyss.
Komposisi dan konsentrasi dari reagen serum AST adalah sebagai berikut:
R1: TRIS pH 7,65 110 mmol/L
L-Aspartate 320 mmol/L
MDH(malatedehydrogenase) 800 U/L
LDH(lactatedehydrogenase) 1200 U/L
R2: 2-Oxoglutarate 65 mmol/L
NADH 1mmol/L
Pyridoxal-5-phosphate
FS: Good’s buffer pH 9,6 100 mmol/L
Pyridoxal-5-phosphate 13mmol/L
D. Alat Penelitian
1. Peralatan pembuatan serbuk kering daun M. tanarius antara lain: oven
(Memmert), mesin penyerbuk (Retsch) timbangan elektrik.
2. Peralatan pembuatan ekstrak metanol-air daun M. tanarius antara lain:
timbangan elektrik, seperangkat alat gelas berupa Erlenmeyer, labu ukur,
Bekker glass, gelas ukur, pipet tetes, batang pengaduk (Pyrek Iwaki Glass),
cawan porselin, shaker (maserator), kertas saring, corong Buchner, vaccum
pump, vaccum rotary evaporator, oven.
3. Peralatan uji hepatoprotektif antara lain: peralatan gelas, seperti Bekker glass,
pipa kapiler, effendorf, spuit injeksi per oral 5 ml dan 10 ml untuk tikus, spuit
injeksi intra peritonial 3 ml, stopwatch, vortex, sentrifuge, mikro pipet, mikro
vitalab (Microlab 200, Merck).
E. Tata Cara Penelitian
1. Determinasi Tanaman Macaranga tanarius L.
Determinasi tanaman M. tanarius dilakukan dengan mencocokan
ciri-ciri tanaman M. tanarius dengan buku acuan batang yang dilakukan secara
benar sesuai dengan buku acuan. Determinasi tanaman dilakukan di
Laboratorium Farmakognosi Fitokimia, Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta.
2. Pengumpulan bahan
Bahan uji yang digunakan adalah daun M. tanarius yang masih segar
dan berwarna hijau, tidak berlubang yang dipetik dari Kebun Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta pada bulan Mei 2012.
3. Pembuatan serbuk
Daun M. tanarius dicuci bersih dibawah air mengalir. Setelah bersih
daun diangin-anginkan hingga daun tidak tampak basah kemudian dilakukan
pengeringan menggunakan oven pada suhu 50° C selama 24 jam. Setelah
kering daun dibuat serbuk dan diayak dengan ayakan nomor 40 supaya
kandungan fitokimia yang terkandung dalam daun M. tanarius lebih mudah
terekstrak karena luas permukaan serbuk yang kontak dengan pelarut semakin
4. Pembuatan ekstrak metanol : air daun M. tanarius
Sebanyak 10 gram serbuk kering daun M. tanarius diekstraksi secara
maserasi dengan melarutkan serbuk dalam 100 ml pelarut metanol 50% pada
suhu kamar selama 3x24 jam dengan kecepatan 140 rpm. Setelah dilakukan
perendaman, hasil maserasi disaring dengan kertas saring. Larutan hasil
saringan dipindahkan dalam cawan porselen yang telah ditimbang
sebelumnya, agar mempermudah perhitungan randemen ekstrak yang akan
diperoleh. Cawan porselen yang berisi larutan hasil maserasi, dimasukkan
dalam vaccum rotary evaporator untuk menguapkan metanol dan
mendapatkan ekstrak kemudian dimasukkan dalam oven untuk diuapkan
selama 24 jam dengan suhu 50° C untuk mendapatkan ekstrak metanol-air
daun M. tanarius yang kental dengan bobot pengeringan ekstrak yang tetap
agar mendapatkan ekstrak metanol-air daun M. tanarius yang kental dengan
bobot pengeringan ekstrak yang tetap yaitu sebesar 3,77 g.
5. Penetapan konsentrasi pekat ekstrak
Menghitung rata-rata rendemen enam replikasi ekstrak metanol : air
daun M. tanarius kental yang telah dibuat.
Rendemen ekstrak = berat cawan ekstrak kental – berat cawan kosong
𝑅𝑎𝑡𝑎 − 𝑟𝑎𝑡𝑎𝑟𝑒𝑛𝑑𝑒𝑚𝑒𝑛=𝑟𝑒𝑝. 1 +𝑟𝑒𝑝. 2 +𝑟𝑒𝑝. 3 +𝑟𝑒𝑝. 4 +𝑟𝑒𝑝. 5 +𝑟𝑒𝑝. 6 6
Konsentrasi ekstrak didapat dari hasil rata-rata rendemen ekstrak.
percawannya yaitu 3,77 g dalam labu ukur terkecil dengan pelarut yang
sesuai. Konsentrasi yang dapat digunakan adalah konsentrasi pekat yang
dikeluarkan dari spuit oral. Cara pembuatannya adalah dengan melarutkan
ekstrak percawannya (gram) dalam labu ukur dengan pelarut yang sesuai
CMC Na 1%. Labu ukur terkecil yang tersedia adalah labu ukur 5 ml
sehingga konsentrasi ekstrak dapat ditetapkan yaitu sebesar 0,384 g/ml atau
384 mg/ml atau 38,4%b/v (Andini, 2010).
6. Penetapan dosis ekstrak metanol : air daun M. tanarius
Dasar penetapan peringkat dosis adalah bobot tertinggi tikus dan pemberian
cairan secara peroral separuhnya yaitu 2,5 ml. Penetapan dosis tertinggi
ekstrak metanol : air daun M. tanarius adalah :
D x BB = C x V
D x BB tertinggi tikus ( kg/BB) = C ekstrak (mg/ml) x 2,5 ml
D = x mg/kg BB
Dua dosis lainnya diperoleh dengan menurunkan 3 dan 6 kalinya dari dosis
tertinggi.
7. Pembuatan larutan karbon tetraklorida dalam olive oil
Larutan karbon tetraklorida dalam olive oil dibuat dengan cara
mengambil volume karbon tetraklorida secara seksama, kemudian diencerkan
dengan olive oil dengan perbandingan 1:1 sampai volume tertentu sehingga
8. Uji pendahuluan
a. Penetapan dosis hepatotoksin karbon tetraklorida
Pemilihan dosis karbon tetraklorida dilakukan untuk mengetahui pada
dosis berapa karbon tetraklorida mampu menyebabkan kerusakan hati
tikus yang ditandai dengan peningkatan aktivitas GPT-serum paling tinggi
tetapi tidak menimbulkan kematian. Dosis hepatotoksik yang digunakan
dalam penelitian ini mengacu pada penelitian Janakat, Al-Merie (2003),
bahwa dosis 2 ml/kg BB karbon tetraklorida dalam olive oil dengan
perbandingan karbon tetraklorida : oilve oil 1:1, terbukti mampu
meningkatkan aktivitas ALT-AST serum pada tikus bila diberikan secara
intra peritonial (i.p).
b. Penetapan waktu pencuplikan darah
Berdasarkan penelitian Janakat, Al-Merie (2003) meunjukkan bahwa
aktivitas GPT serum tikus terangsang karbon tetraklorida 2 mg/kg BB
mencapai maksimal pada jam ke-24 setelah pemberiannya, kemudian pada
jam ke-48 berangsur-angsur menurun. Pengukuran ada jam ke-24
dilakukan untuk mengetahui profil kenaikan serum GPT sebelum jam
ke-48.
c. Penetapan lama pemejanan ekstrak metanol : air daun M. tanarius
Lama waktu pemejanan ekstrak metanol : air daun M. tanarius dilakukan
pada waktu jam ke-½, 1, 2, 4 dan 6 kemudian setelah ½, 1, 2, 4 dan 6 jam
aktivitas ALT dan AST-nya sesuai hasil orientasi waktu penetapan
pencuplikan darah.
9. Pengelompokkan dan perlakuan hewan uji
Hewan percobaan yang dibutuhkan sebanyak 40 ekor tikus jantan
dibagi secara acak dalam delapan kelompok sama banyak. Kelompok I
merupakan kontrol negatif yaitu pemberian olive oil secara intra peritonial.
Kelompok II merupakan kontrol negatif yaitu hepatotoksin karbon
tetraklorida dengan dosis 3840 mg/kg BB secara intra peritonial. Kelompok
III merupakan kontrol perlakuan yaitu pemberian ekstrak metanol-air daun M.
tanarius dosis 3840 mg/kg BB secara per oral. Kelompok IV-VIII diberikan
ekstrak metanol-air daun M. tanarius dengan dosis 3840 mg/kg BB,
kemudian secara berturut-turut pada ½, 1, 2, 4, dan 6 jam setelah perlakuan
diberikan dosis hepatotoksik karbon tetraklorida dengan dosis 2 ml/kg BB.
Pada jam ke-24 setelah diberi karbon tetraklorida semua kelompok diambil
darahnya pada daerah sinus orbitalis pada mata tikus, kemudian ditampung
dalam Effendorf untuk penetapan aktivitas serum ALT dan AST. Darah
disentrifugasi selama 15 menit dengan kecepatan 3500 rpm dan bagian
supernatannya diambil.
10.Penetapan aktivitas ALT-AST serum
Alat yang digunakan untuk menganalisis aktivitas ALT dan AST serum
adalah Mikro vitalab 200. Aktivitas enzim diukur pada panjang gelombang
Biokimia Fisiologi Manusia, Fakultas Farmasi, Universitas Sanata Dharma,
Yogyakarta. Analisis aktivitas serum ALT dilakukan dengan cara mencampur
100 µL serum atau plasma dengan 800 µL reagen I, kemudian dicampurkan
200 µL reagen II dan didiamkan selama operating time selama satu menit
kemudian divortex dan dibaca resapan setelah dua menit. Untuk analisis
fotometri dengan AST serum dilakukan dengan cara mencampur 100 µL
serum atau plasma dengan 800 µL reagen I, kemudian dicampurkan 200 µL
reagen II dan didiamkan selama operating time selama satu menit kemudian
divortex dan dibaca resapan setelah dua menit.
11.Perhitungan Efek Hepatoprotektif
Hasil resapan aktivitas serum ALT dan AST yang dilakukan pengujian
besarnya efek hepatoprotektif yang dinyatakan dalam persen (%).
Perhitungan mengenai besarnya efek hepatoprotektif dapat dihitung
menggunakan rumus:
𝑝𝑢𝑟𝑎𝑡𝑎 𝐴𝐿𝑇/𝐴𝑆𝑇ℎ𝑒𝑝𝑎𝑡𝑜𝑡𝑜𝑘𝑠𝑖𝑛 −𝑝𝑢𝑟𝑎𝑡𝑎 𝐴𝐿𝑇/𝐴𝑆𝑇𝑝𝑒𝑟𝑙 𝑎𝑘𝑢𝑎𝑛
𝑝𝑢𝑟𝑎𝑡𝑎 𝐴𝐿𝑇/𝐴𝑆𝑇ℎ𝑒𝑝𝑎𝑡𝑜𝑡𝑜𝑘𝑠𝑖𝑛
x 100%
F. Tata Cara Analisis Hasil
Data aktivitas ALT-AST diuji dengan Kolmogorov-Smirnov untuk
mengetahui distribusi data dan analisis varian untuk melihat homogenitas varian
antar kelompoknya sabagai syarat analisis parametrik. Jika data terdistribusi
normal maka dilanjutkan dengan analisis variansi pola searah (ANOVA one way)
dengan taraf kepercayaan 95% untuk mengetahui perbedaan masing-masing
antar kelompok bermakna (signifikan) (p<0,05) atau tidak bermakna (tidak
signifikan) (p>0,05). Tetapi bila distribusi tidak normal dilakukan analisis dengan
Kruskal Wallis untuk mengetahui perbedaan aktivitas ALT-AST serum antar
kelompok. Kemudian dilanjutkan uji dengan Mann Whitney untuk melihat
36
BAB IV
HASIL DAN PEMBAHASAN
Penelitian ini bertujuan untuk mengetahui dan membuktikan khasiat
ekstrak metanol-air daun Macaranga tanarius L. sebagai hepatoprotektor tikus
yang terinduksi karbon tetraklorida (CCl4) dengan pemberian jangka pendek.
Selain itu penelitian ini sebagai kelanjutan dari penelitian sebelumnya mengenai
efek hepatoprotektif jangka panjang ekstrak metanol-air daun M.tanarius namun
menggunakan hepatotoksin karbon tetraklorida. Untuk mencapai tujuan penelitian
tersebut maka dilakukan beberapa pengujian. Aktivitas ALT dan AST dari serum
tikus yang diteliti dijadikan sebagai tolak ukur pengujian kuantitatif.
A. Penyiapan Bahan
1. Hasil determinasi tanaman
Penelitian dengan tema penggunaan tanaman sebagai hepatoprotektor ini
menggunakan serbuk dari daun tanaman M. tanarius. Daun tanaman M. tanarius
yang didapat dari kebun obat Fakultas Farmasi Universitas Sanata Dharma ini
dilakukan determinasi. Tujuan determinasi tanaman ini supaya diketahui secara
pasti tanaman yang digunakan dalam penelitian ini benar merupakan tanaman M.
tanarius supaya tidak terjadi kesalahan dalam penyiapan bahan.
Pendeterminasian ini dilakukan di Laboratorium Farmakognosi Fitokimia
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta. Bagian tanaman yang
dideterminasi adalah daun, batang, bunga dan buah menggunaan buku acuan
untuk mendeterminasi tanaman hingga ke tingkat spesies. Hasil yang diperoleh
2. Pembuatan serbuk daun M. tanarius
Pembuatan serbuk daun M. tanarius diawali dengan pengambilan daun M.
tanarius, kemudian dilakuan pencucian dan pensortiran daun sesuai dengan
langkah-langkah pembuatan simplisia. Pencucian bertujuan supaya daun yang
diperoleh bebas dari kotoran dan debu. Penyortiran dilakukan supaya daun yang
digunakan daun yang hijau dan tidak berlubang. Kemudian daun dikeringkan
dibawah sinar matahari yang ditutupi kain hitam. Hal ini dilakukan supaya daun
menjadi layu, namun kandungan klorofilnya tidak rusak akibat sinar matahari.
Setelah daun menjadi rapuh, dipanaskan menggunakan oven sekitar 15 menit,
kemudian dipisahkan daun dari tulang daun, sehingga diperoleh serpihan daun.
Potongan kecil daun-daun ini kemudian diserbukkan penggunakan penyerbuk dan
disaring menggunakan pengayak dengan nomor mess 40. Hal ini sesuai dengan
ketentuan yang ditetapkan oleh BPOM RI.
3. Penetapan kadar air serbuk daun M. tanarius
Penetapan kadar air dari serbuk daun M. tanarius bertujuan untuk menguji
serbuk yang dihasilkan memenuhi persyaratan serbuk yang baik, yakni kadar air
kurang dari 10% (Departemen Kesehatan RI, 1995). Penetapan kadar air serbuk
daun M. tanarius dilakukan dengan metode Gravimetri dengan menggunakan alat
moisture balance. Serbuk dipanaskan pada suhu 110°C selama 15 menit.
Penetapan suhu sebesar 110°C dimaksudkan agar supaya kandungan air telah
menguap dan waktu 15 menit dianggap bahwa kadar air telah memenuhi
kadar air menunjukkan bahwa serbuk daun M. tanarius memiliki rata-rata kadar
air sebesar 7,59%. Hasil pengujian ini, menunjukkan bahwa kadar air sebuk daun
M. tanarius telah memenuhi persyaratan kadar air untuk serbuk yang baik, yaitu
kurang dari 10% (Departemen Kesehatan RI, 1995).
B. Hasil Penimbangan Bobot Ekstrak Metanol-Air Daun M. tanarius
Pembuatan ekstrak metanol-air dilakukan dengan metode penyarian yaitu
dengan maserasi. Maserasi merupakan metode penyarian yang dilakukan dengan
cara memasukkan serbuk simplisia ke dalam labu erlenmeyer, yang kemudian di
aduk dengan kecepatan kostan menggunakan shaker, selama kurang lebih 72 jam.
Metode ini dipilih dalam metode penyarian karena peralatan yang digunakan
sederhana dan cara pengerjaan serta pengoperasian alat yang mudah. Metode ini
dilakukan untun menyari simplisia yang dilarutkan menggunakan pelarut tertentu.
Pemilihan pelarut ini didasarkan pada jenis kandungan zat aktif digunakan,
hal ini supaya ada kecocokan antara zat akif dengan larutan penyari, sehingga zat
aktif akan larut dan bercampur dengan cairan penyari. Dalam daun M. tanarius
mengandung senyawa golongan glikosida fenolik yang dapat larut di dalam air,
sehingga dalam larutan penyari juga menggunakan air. Pada penelitian ini
digunakan cairan penyari, yaitu campuran metanol dengan air dengan
perbandingan 1:1 atau 50 ml air dan 50 ml metanol.
Menurut standar, proses ekstraksi metanol-air serbuk daun M. tanarius
menghasilkan ekstrak kental. Ekstrak kental didapatkan dengan mengikuti
dengan susut pengeringan sebesar 0%. Tujuan dilakukan pengukuran parameter
non spesifik yaitu parameter susut pengeringan adalah untuk menghitung sisa zat
setelah dilakukan pengeringan pada temperatur ± 50°C. Ekstrak yang berada
dalam cawan ditimbang setiap waktu tertentu selama 24 jam atau hingga berat
menjadi konstan (dinyatakan dalam persen). Tujuannya adalah untuk menentukan
batasan atau rentang mengenai seberapa banyak senyawa yang hilang selama
proses pengeringan, dimana hal ini dapat mempengaruhi bobot ekstrak yang
didapatkan sehingga akan mempengaruhi konsentrasi dan dosis ekstrak. Hasil dari
proses pengeringan didapatkan bahwa tidak ada perubahan bobot ekstrak sehingga
diperoleh bobot pengeringan tetap yaitu pada jam ke-23 dan ke-24.
Untuk susut pengeringan ekstrak metanol air daun M. tanarius pada jam
ke-23 dan ke-24 sebesar 0% sehingga dapat diketahui pelarut penyari ekstrak
sudah tidak ada atau tidak ada sisa. Dengan demikian, pada penelitian ini, waktu
pengeringan 24 jam yang digunakan untuk memperoleh bobot pengeringan tetap
ekstrak metanol air daun M. tanarius. Dari hasil penimbangan bobot ekstrak
didapat rendemen ekstrak metanol-air daun M. tanarius sebesar 3,77% yang
dihasilkan dari 63 cawan ekstrak kental. Untuk pembuatan ekstrak kental,
digunakan 1 kg serbuk kering daun M. tanarius, sehingga dapat dihasilkan ekstrak