5 BAB II
TINJAUAN PUSTAKA
2.1 Minuman Energi
Menurut BadanStandarisasi Nasional (2002), Minuman energi adalah minuman yang mengandung satu atau lebih bahan yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi dengan atau tanpa bahan tambahan
makanan yang diizinkan.
Energi Drink (minuman berenergi) termasuk salah satu suplemen makanan
yang terdiri dari komponen multivitamin, makronutrien (karbohidrat, protein), taurin dengan atau tanpa kafein dan biasanya ditambahkan herbal seperti ginseng, jahe, dan sebagainya dengan bentuk sediaan cairan Obat Dalam (COD) dalam
kemasan botol bervolume 150 mL, 250 mL atau serbuk dan tablet yang dilarutkan menjadi minuman, yang dalam setiap kemasannya mengandung energi minimal
100 kkal, dengan indikasi untuk menambah tenaga, kesegaran, stimulasi metabolisme, memelihara kesehatan dan stamina tubuh, yang dapat diminum pada saat bekerja keras atau setelah berolah raga (Anonim, 2014).
2.2 Kandungan Minuman berenergi
Minuman berenergi mengandung sumber energi dari sukrosa (gula) atau
maltodextrin. Minuman berenergi juga mengandung vitamin-vitamin yang terlibat dalam metabolisme tubuh antara lain sebagai berikut:
a) Vitamin B atau tiamin (Vitamin B1, aneurin)
Vitamin B berfungsi sebagai koenzim atau membantu kerja enzim, penting dalam metabolisme tubuh untuk menghasilkan energi, mengatur sirkulasi
6 b) Vitamin B3 (niasin, asam nikotinat)
Vitamin B3 berhubungan dengan aktivitas saraf dan sebagai koenzim dari NAD, dan NADP yang berperan dalam reaksi metabolisme karbohidrat,
lemak dan protein.
c) Vitamin B5 (asam pantotenat)
Vitamin B5 berperan dalam sistem imun dan proses pencernaan, serta
berperan dalam produksi hormon adrenalin dan sel-sel darah merah. d) Vitamin B6 (piridoksin)
Vitamin B6 berperan dalam pembentukan protein tubuh, sel-sel darah merah, prostaglandin, dan senyawa struktural yang berfungsi sebagai transmiter kimia pada sistem saraf.
e) Vitamin B12 (sianokobalamin)
Vitamin B12 berperan dalam mengatur pembentukan sel darah merah, memelihara sistem saraf, sintesa DNA, mengubah karbohidrat lemak dan
protein menjadi energi. f) Taurin
Taurin berperan dalam membantu meningkatkan toleransi terhadap glukosa, menghambat pembentukkan kolestrol dan meningkatkan ekskresi kolestrol.
g) Kafein
Kafein berfungsi sebagai stimulan susunan saraf pusat (SSP), jantung dan
7 h) Ginseng
Ginseng adalah herbal yang sering ditambahkan didalam minuman berenergi dengan tujuan untuk dapat meningkatkan stamina tubuh.
i) Jahe (Zingiber officinale)
Jahe dalam minuman berenergi berkhasiat sebagai stimulan, meningkatkan nafsu makan, dan tonik.
Selain kandungan bahan-bahan tersebut diatas, minuman berenergi juga mengandung natrium bikarbonat (soda) dan asam sitrat.Natrium bikarbonat dapat
memberikan efek karminatif (mengeluarkan gas) dan sebagai antacid sistemik.Campuran keduanya dengan adanya air dapat menimbulkan gelembung CO2 dan meningkatkan kelarutannya (Anonim, 2014).
Konsumsi minuman berenergi yang berlebihan dapat menyebabkan gangguan pada ginjal dan hati sehingga harus dikonsumsi dengan batas yang telah dicantumkan (Anonim, 2014).
2.3 Bahan Tambahan Makanan
Bahan Tambahan Makanan (BTM) atau food additives adalah bahan yang
ditambahkan ke dalam makanan untuk mempengaruhi sifat atau bentuk makanan (Yuliarti, 2007). Bahan Tambahan Makanan mempunyai atau tidak mempunyai
nilai gizi, yang sengaja ditambahkan kedalam makanan untuk meningkatkan nilai gizi makanan, memperbaiki nilai sensori makanan, dan memperpanjang umur simpan makanan (Cahyadi, 2009).Bahan Tambahan Makanan yang diizinkan
8 2.3.1 Bahan pengawet
Pengawet adalah bahan tambahan makanan yang mencegah atau menghambat fermentasi, pengasaman atau peruraian lain terhadap makanan yang
disebabkan oleh mikroorganisme. Pemakaian bahan pengawet menguntungkan karena dengan bahan pengawet, bahan pangan dapat dibebaskan dari kehidupan mikroba, baik yang bersifat patogen yang dapat menyebabkan keracunan atau
gangguan kesehatan lainnya maupun mikrobial yang nonpatogen yang dapat menyebabkan kerusakan bahan pangan, misalnya pembusukan.Tanpa bahan
tambahan pangan, khususnya bahan pengawet maka bahan pangan yang tersedia di pasar atau swalayan akan menjadi kurang menarik, tidak dapat dinikmati secara layak dan tidak awet (Cahyadi, 2009).
Menurut Cahyadi (2009), terdapat beberapa persyaratan untuk bahan pengawet kimiawi lainnya, antara lain sebagai berikut:
1. Memberikan arti ekonomis dari pengawetan
2. Digunakan hanya apabila cara-cara pengawetan yang lain tidak mencukupi 3. Memperpanjang umur simpan dalam pangan
4. Aman dalam jumlah yang diperlukan 5. Mudah dilarutkan
6. Menunjukkan sifat-sifat antimikroba
7. Tidak mengalami dekomposisi atau tidak bereaksi untuk membentuk suatu senyawa kompleks yang bersifat lebih toksik
8. Tidak Menurunkan kualitas (warna, cita rasa, dan bau) bahan pangan yang diawetkan
9
10.Mempunyai spektra antimikro yang luas, meliputi macam-macam
pembusukkan oleh mikroba yang berhubungan dengan bahan pangan yang diawetkan.
Berdasarkan bahan asalnya maka bahan pengawet dibagi menjadi dua jenis, yaitu bahan pengawet organik dan bahan pengawet anorganik.
2.3.1.1 Bahan Pengawet Organik
Zat pengawet organik lebih banyak digunakan daripada zat pengawet anorganik karena bahan ini lebih mudah larut dan mudah untuk dibuat.Bahan
organik digunakan baik dalam bentuk asam maupun dalam bentuk garamnya.Zat kimia yang sering digunakan sebagai bahan pengawet adalah asam sorbat, asam propionat, asam benzoat, asam asetat dan epoksida (Cahyadi, 2009).
2.3.1.2 Bahan Pengawet Anorganik
Zat pengawet anorganik yang masih sering dipakai adalah sulfit, hidrogen peroksida, nitrat dan nitrit. Sulfit digunakan dalam bentuk gas SO2, garam Na atau K sulfit, bisulfit dan metabisulfit. Garam nitrat dan nitrit umumnya digunakan pada proses pengolahan daging (seperti sosis, kornet, ham, dan hambuger) Selain
digunakan pada produk daging, nitrat dan nitrit juga digunakan pada ikan dan keju untuk memperoleh warna yang baik, mencegah pertumbuhan mikroba, juga berfungsi sebagai pembentuk faktor sensori lain, yaitu aroma dan cita rasa
(flavor)(Cahyadi, 2009).
2.4 Natrium Benzoat
10 2.4.1 Sifat Fisikokimia
Menurut Ditjen POM (1995), monografi dari Natrium benzoat adalah sebagai berikut:
a. Rumus bangun:
Gambar 1.Rumus bangun natrium benzoat b. Rumus molekul: C
7H5NaO2 c. Berat molekul : 144,11
d. Nama kimia : Natrium benzoat
e. Kandungan : tidak kurang dari 99,0% dan tidak lebih dari 100,5%.
f. Pemerian : Granul atau serbuk hablur, putih; tidak berbau atau praktis tidak
berbau; stabil di udara.
g. Kelarutan : Mudah larut dalam air, agak sukar larut dalam etanol, lebih mudah larut dalam etanol 90%.
2.4.2 Mekanisme Kerja sebagai Pengawet
Parameter pH sangat menentukan jumlah asam yang
terdisosiasi.Penambahan asam berarti menurunkan pH yang disertai dengan naiknya kosentrasi ion hidrogen (H+), dan dikatakan bahwa pH rendah lebih besar penghambatannya pada pertumbuhan mikroorganisme.Asam digunakan sebagai
11
mikroba dalam bahan pangan dengan pH rendah, seperti minuman penyegar
(Cahyadi, 2009).
2.4.3 Efek terhadap Kesehatan
Pada penderita asma dan orang yang menderita urtikaria sangat sensitif terhadap asam benzoat, jika dikonsumsi dalam jumlah besar akan mengiritasi lambung (Cahyadi, 2009).
2.5 Vitamin C
Vitamin C merupakan molekul yang menyerupai glukosa kecil yang aktif dalam 2 bentuk, yaitu asam askorbat dan dehidro askorbat dan berguna sebagai antioksidan (Tjokronegoro, 1985).
2.5.1 Sifat Fisikokimia
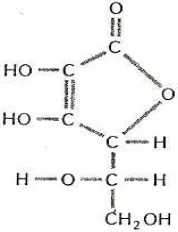
Menurut Ditjen POM (1995), monografi Vitamin C adalah sebagai berikut: a. Rumus bangun:
Gambar 2.Rumus bangun vitamin C b. Rumus molekul : C
6H8O6 c. Berat molekul : 176,13
d. Nama kimia : Asam askorbat
12
f. Pemerian : Hablur atau serbuk putih atau agak kuning. Oleh pengaruh
cahaya lambat laun menjadi berwarna gelap.Dalam keadaan kering stabil diudara, dalam larutan cepat teroksidasi.
g. Kelarutan : Mudah larut dalam air; agak sukar larut dalam etanol; tidak larut dalam kloroform, dalam eter dan dalam benzene.
2.5.2 Fungsi Vitamin C
Fungsi vitamin C didalam tubuh bersangkutan dengan sifat alamiahnya
sebagai antioksidan yang berperan serta didalam banyak proses metabolisme yang berlangsung didalam jaringan tubuh, menurunkan kadar LDL, menaikkan HDL serta mencegah terjadinya kanker dengan meningkatkan sistem kekebalan tubuh
terhadap infeksi dan virus, mengurangi pembentukan nitrosamin yang dapat menyebabkan kanker di perut dan menjaga koenzim folat utuh. Vitamin C dan vitamin E bekerja sama sebagai penangkal radikal bebas. Vitamin C juga dapat
membantu mengaktifkan kembali vitamin E yang teroksidasi sehingga dapat digunakan kembali.Studi populasi menunjukkan bahwa vitamin C efektif dalam
membantu mencegah kanker tertentu (seperti kanker esofagus, mulut dan kanker pada perut), penyakit kardiovaskular, dan katarak pada mata, yang mungkin disebabkan oleh kemampuan antioksidannya (Silalahi, 2006; Wardlaw, 2003).
Vitamin C dibutuhkan untuk menghasilkan norepinefrin (noradrenalin), yang dapat dikonversikan menjadi bentuk epinefrin (adrenalin) (William dan
Caliendo, 1984).
13
Kebutuhan harian vitamin C sesuai dengan yang dirusak oleh oksidasi atau
yang diekskresi. Pada manusia sehat kebutuhan vitamin C 3-4 % dari persediaan tubuh (1500 mg), yaitu berkisar 60 mg/hari (Tjokronegoro, 1985).
2.5.4 Defisiensi Vitamin C
Gejala defisiensi vitamin C termasuk kelelahan, lemas, dan lesu yang lebih parah yaitu terjadi nyeri otot, sendi, kulit menjadi kering, gusi berdarah, gigi
melonggar dan dapat mencapai kehilangan rambut (William dan Caliendo, 1984). Dalam kasus-kasus skorbut atau sariawan spontan, biasanya dikaitkan
dengan gigi mudah tanggal, gingivitis, dan anemia, yang disebabkan oleh adanya fungsi spesifik asam askorbat dalam sintesis hemoglobin (Gilman, dkk., 1996).
2.5.5 Efek Samping
Vitamin C dengan dosis tinggi dapat menyebabkan diare, keluhan nyeri perut pada penderita dengan gastritis, juga meningkatkan absorpsi besi pada saluran cerna sehingga dapat menimbulkan hemosiderosis. Dosis besar tersebut
juga meningkatkan bahaya terbentuknya batu ginjal, karena sebagian besar vitamin C akandimetabolisme dan diekskresi sebagai oksalat(Tjokronegoro, 1985).
2.6 Teori Kromatografi Cair Kinerja Tinggi 2.6.1 Sejarah Kromatografi
Kromatografi adalah suatu istilah umum yang digunakan untuk bermacam-macam teknik pemisahan, yaitu berdasarkan absorbsi sampel diantara suatu fase
14
untuk melukiskan daerah-daerah yang berwarna yang bergerak ke bawah
kolom.Pada waktu yang hampir bersamaan, Day juga menggunakan kromatografi untuk memisahkan fraksi-fraksi petroleum, namun Tswett adalah yang pertama
diakui sebagai penemu yang pertama kali mengenali dan menafsirkan proses kromatografi (Johnson dan Stevenson, 1978).
2.6.2 Pembagian Kromatografi
Kromatografi dapat dibedakan atas berbagai macam, tergantung pada pengelompokannya. Berdasarkan pada mekanisme pmisahannya, kromatografi
dibedakan menjadi: (a) kromatografi adsorbsi; (b) kromatografi partisi; (c) kromatografi pasangan ion; (d) kromatografi penukar ion (e) kromatografi eksklusi ukuran dan (f) kromatografi afinitas (Johnson dan Stevenson, 1978;
Rohman, 2007).
Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas: (a) kromatografi kertas; (b) kromatografi lapis tipis, yang kedua sering disebut
kromatografi planar; (c) kromatografi cair kinerja tinggi (KCKT) dan (d) kromatografi gas (KG) (Johnson dan Stevenson, 1978; Rohman, 2007).
2.6.3 Kromatografi Cair Kinerja Tinggi
Kromatografi Cair Kinerja Tinggi (KCKT) merupakan teknik pemisahan yang didukung oleh kemajuan teknologi yang canggih untuk menganalisis
berbagai analit secara kualitatif maupun kuantitatif, baik dalam komponen tunggal maupun campuran, senyawa bahan aktif obat, menganalisis kemurnian suatu
senyawa didalam suatu cuplikan (Ditjen POM, 1995).
15
(impurities) dan analisis senyawa-senyawa yang tidak mudah menguap
(nonvolatile). KCKT sering digunakan untuk menetapkan kadar senyawa-senyawa
tertentu seperti asam-asam amino, asam-asam nukleat, dan protein-protein dalam
cairan fisiologis, menentukan kadar senyawa-senyawa aktif obat dan lain-lain (Rohman, 2007).
2.6.4 Jenis Kromatografi Cair Kinerja Tinggi
Berdasarkan pada mekanisme pemisahannya KCKT dapat dikelompokkan menjadi KCKT fase normal dan KCKT fase terbalik.Untuk fase normal (fase
gerak lebih polar daripada fase gerak), sementara untuk fase terbalik (fase diam kurang polar daripada fase gerak).Fase terbalik menggunakan fase diam silika yang dimodifikasi secara kimiawi seperti oktadesilsilan (ODS atau C18) dan fase gerak campuran metanol atau asetonitril dengan air atau dengan larutan buffer. Untuk solut yang bersifat asam lemah,peranan pH sangat krusial karena bila pH fase gerak tidak diatur maka solut akan mengalami ionisasi atau protonisasi.
Terbentuknya bagian yang terionisasi ini menyebabkan ikatannya dengan fase diam menjadi lebih lemah dibanding jika solut dalam bentuk yang tidak
terionisasi akan terelusi lebih cepat (Rohman, 2007).
2.6.5 Proses Pemisahan dalam Kolom Kromatografi Cair
Pemisahan analit dalam kolom kromatografi berdasarkan pada aliran fase
gerak yang membawa campuran analit melalui fase diam dan perbedaan interaksi analit dengan permukaan fase diam sehingga terjadi perbedaan waktu perpindahan
setiap komponen dalam campuran (Meyer, 2010).
16
fase diam dan komponen ● lebih cenderung di dalam fase gerak. Ilustrasi proses
pemisahan dalam kolom kromatografi dapat dilihat pada Gambar 3 berikut.
Gambar3 .Ilustrasi proses pemisahan yang terjasi di dalam kolom KCKT (Sumber: Meyer, 2010).
Masuknya eluen (fase gerak) yang baru ke dalam kolom akan menimbulkan kesetimbangan baru, molekul sampel dalam fase gerak diadsorpsi
sebagian oleh permukaan fase diam berdasarkan pada koefisien distribusinya, sedangkan molekul yang sebelumnya diadsorpsi akan muncul kembali di fase gerak (Gambar 4c). Setelah proses ini terjadi berulang kali, kedua komponen akan
terpisah. Komponen ● yang lebih suka dengan fase gerak akan berpindah lebih cepat daripada komponen ▲ yang cenderung menetap di fase diam, sehingga
komponen ● akan muncul terlebih dahulu dalam kromatogram, kemudian diikuti oleh komponen ▲ (Meyer, 2010).
2.7 Parameter Penting dalam Kromatografi Cair 2.7.1 Waktu tambat/retention time
Waktu tambat/retention time(tR) merupakan waktu antara penyuntikan sampel dan puncak maksimum yang terekam oleh detektor. Waktu tambat dari suatu komponen yang tidak ditahan/dihambat oleh fase diam disebut sebagai waktu hampa/void time.Waktu tambat merupakan fungsi dari laju alir fase gerak
Fase gerak
17
dan panjang kolom. Jika fase gerak mengalir lebih lambat atau kolom semakin
panjang, waktu hampa dan waktu tambat akan semakin besar, dan sebaliknya bila fase gerak mengalir lebih cepat atau kolom semakin pendek, maka waktu hampa
dan waktu tambat akan semakin kecil (Meyer, 2010). 2.7.2 Faktor Kapasitas
Faktor kapasitas atau faktor tambat (k) merupakan suatu ukuran derajat
tambatan dari suatu analit didalam kolom. K didefinisikan sebagai waktu zat terlarut berada dalam fase diam (tR) dibagi dengan waktu zat terlarut dalam fase
gerak (tM) rumusnya ditulis sebagai berikut ini (Dong, 2006).
Retention factor, k=
tR −t M
tM
Faktor tambat yang baik berada diantara nilai 1 hingga 10.Jika nilai k
terlalu kecilmenunjukkan tingkat pemisahan yang tidak bagus karena analit terlalu cepatmelewati kolom sehingga tidak terjadi interaksi dengan fase diam dan tidak muncul kromatogram. Sebaliknya nilai k yang terlalu besar mengindikasikan
waktu analisis akan panjang (Meyer, 2010).
Faktor kapasitas dipengaruhi oleh perbandingan komposisi fase gerak
yang digunakan sehingga akan menghasilkan resolusi dan waktu retensi dari puncak-puncak kromatogram yang berbeda pada setiap perbandingan komposisi fase gerak (Snyder, dkk., 2010).
2.7.3 Selektivitas
Selektivitas disebut juga sebagai faktor tambahan relatif.Selektivitas (α)
18
Selektivitas bergantung pada banyak faktor umumnya tergantung pada
sifat analit itu sendiri, interaksinya dengan permukaan fase diam serta jenisdan komposisi fase gerak yang digunakan. Selektivitas yang didapatkan dalam sistem
KCKT harus
α
>1 agar pemisahan terjadi dengan baik (Dong, 2006).2.7.4 Efisiensi Kolom
Solusi untuk memperbaiki masalah daya pisah adalah efisiensi kolom.
Efisiensi kolom disebut sebagai nilai lempeng/plate number (N). Kolom yang efisien adalah kolom yang mencegah pelebaran pita serta menghasilkan puncak yang sempit dan memisahkan analit dengan baik.Jumlah nilai lempeng berbanding
lurus dengan panjang kolom. Nilai lempeng akan semakin tinggi jika ukuran kolom semakin panjang, hal ini berarti proses pemisahan yang terjadi semakin
baik. Hubungan proporsionalitas antara nilai lempeng dengan panjang kolom disebut sebagai nilai HETP/High Equivalent of a Theoritical Plate. Praktik HPLC yang baik adalah mendapatkan nilai HETP yang kecil untuk nilai N yang
maksimum dan efisiensi kolom yang tertinggi (Johnson dan Stevenson,1978).
𝑁𝑁
=
�
𝑡𝑡𝑅𝑅Nilai lempeng sangat dipengaruhi oleh waktu tambat puncak, ukuran partikel kolom, laju alir fase gerak, suhu kolom, viskositas fase gerak dan berat
molekul analit (Jhonson dan Stevenson, 1978).FDA merekomendasikan agar tiap analisis KCKT yang valid mempunyai nilai lempeng lebih besar dari 2000 (Meyer, 2010).
2.7.5 Resolusi
19
Resolusi merupakan derajat pemisahan dari dua puncak analit yang saling
bersebelahan (Meyer, 2010).
R =tR 2 − tR 1
w 1+ w 2
Harga resolusi yang semakin besar memiliki arti proses pemisahan semakin bagus dan sebaliknya resolusi yang kecil merupakan pertanda proses
pemisahan yang buruk. Dua puncak yang tidak terpisah dengan sempurna namun sudah dapat terlihat memiliki resolusi 1. Sedangkan bila kedua puncak yang saling berdekatan terpisah sempurna tepat pada garis alas, resolusi bernilai 1,5. Oleh
karena itu pada analisis kuantitatif, resolusi yang ditunjukkan harus lebih besar dari 1,5. Sementara bila kedua puncak memiliki perbedaan yang signifikan, maka
diperlukan nilai resolusi yang lebih besar (Meyer, 2010).
Pemisahan yang kurang baik dalam kromatografi fase balik biasanya disebabkan oleh tahanan yang lemah untuk senyawa yang sangat polar, sensitifitas
deteksi yang kurang bagus dan ukuran molekul terutama dalam senyawa kompleks. Puncak yang tumpang tindih biasanya ditemukan bila satu puncak
lebih besar dari puncak yang lain (Snyder, dkk., 2010). 2.7.6 Faktor Ikutan dan Faktor Asimetri
Kondisi ideal dari puncak kromatogram akan memperlihatkan bentuk
Gaussian dengan derajat simetris yang sempurna. Namun kenyataannya dalam praktik kromatografi, puncak yang simetris secara sempurna jarang dijumpai.Jika
20
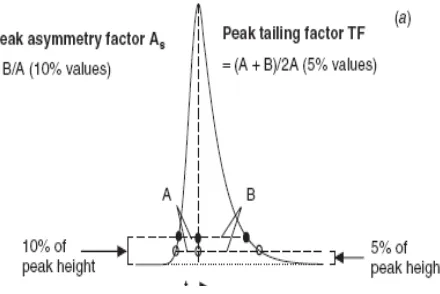
Gambar 4.Contoh gambar puncak yang asimetris (Sumber: Dolan, 2003). Pengukuran derajat asimetris puncak ini dapat diukur dengan faktor ikatan dan faktor asimetri.Faktor ikatan atau lebih dikenal tailing factordilambangkan
dengan simbol (Tf) yang dapat dihitung dengan menggunakan lebar puncak pada ketinggian 5% (W0,05), rumusnya dituliskan sebagai berikut:
Dengan nilai a dan b merupakan setengah lebar puncak pada ketinggian 5% seperti yang ditunjukkan pada Gambar 5.
Gambar 5.Pengukuran derajat asimetris puncak (Sumber: Snyder, 2010). Sementara itu, faktor asimetri/asymmetry factor(As) dihitung dengan rumus sebagai berikut:
As =
ba
Tf =
a + b
21
Namun nilai a dan b dalam perhitungan faktor asimetri merupakan
setengah lebar puncak pada ketinggian 10% seperti yang ditunjukkan di Gambar. Jika nilai a sama dengan b, maka faktor ikutan dan asimetri bernilai 1. Kondisi ini
menunjukkan bentuk puncak yang simetris sempurna (Dolan, 2003).
Bila harga TF > 1 menunjukkan bahwa kromatogram mengalami pengekoran (tailing) dan sebaliknya bila puncak berbentuk fronting, maka faktor
ikatan dan asimetri akan bernilai lebih kecil dari 1. Semakin besar harga TF maka kolom yang dipakai akansemakin kurang efisien. Dengan demikian harga TF
dapat digunakan sebagai acuan untuk melihat efisiensi kolom kromatografi (Rohman, 2007).
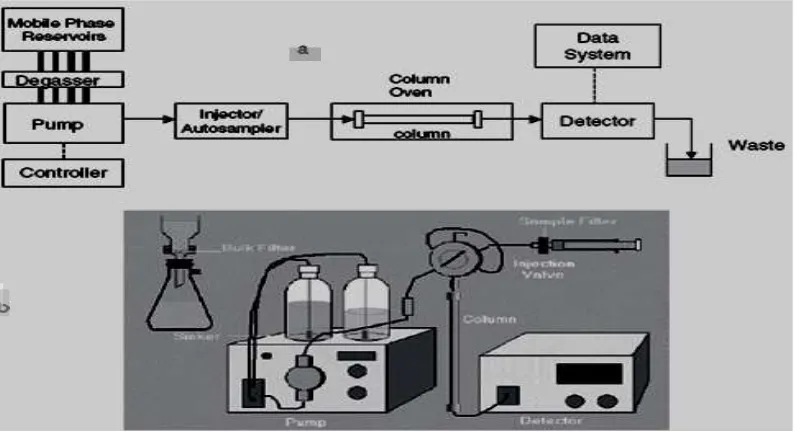
2.8 Instrumen Kromatografi Cair Kinerja Tinggi
Komponen-komponen penting sertaskematik sistem dari KCKT dapat dilihat pada Gambar 6.
22 2.8.1Wadah Fase Gerak
Wadah fase gerak merupakan sebuah bagian penting namun sederhana dari sistem HPLC. Untuk aplikasi isokratik menggunakan pencampuran fase gerak
dalam wadah tunggal, sedangkan untuk aplikasi gradien pencampuran fase gerak dapat menggunakan lebih dari satu wadah fase gerak. Fase gerak harus bebas dari partikel sehingga fase gerak harus disaring terlebih dahulu sebelum digunakan.
Wadah fase gerak yang digunakan dapat berupa botol kaca berdinding tebal atau labu laboratorium yang harus inert dan bersih, sedangkan penutup wadah
diperbolehkan dengan berbagai bahan namun harus dapat menjaga agar debu tidak masuk dan bercampur dengan fase gerak serta meminimalkan penguapan dari fase gerak (Snyder, dkk., 2010).
2.8.2 Pompa
Pompa yang cocok digunakan untuk KCKT adalah pompa yang mempunyai syarat sebagaimana syarat wadah pelarut yakni : pompa harus inert terhadap fase
gerak. Bahan yang umum dipakai untuk pompa adalah gelas, baja tahan karat, teflon, dan batu nilam. Pompa yang digunakan sebaiknya mampu memberikan
tekanan sampai 5000 psi dan mampu mengalirkan fase gerak dengan kecepatan alir 3 ml/menit.Aliran pelarut dari pompa harus tanpa denyut untuk menghindari hasil yang menyimpang pada detektor (Rohman, 2007).
2.8.3 Tempat Injeksi Sampel
Menurut Jhonson dan Stevenson (1978), Cuplikan harus dimasukkan
23
a. Aliran-henti: Aliran dihentikan, penyuntikkan dilakukan pada tekanan
atmosfir, sistem tertutup, dan aliran dilanjutkan lagi. Cara ini dapat dipakai karena difusi didalam zat cair kecil dan daya pisah tidak dipengaruhi.
b. Septum: Ini adalah injektor langsung pada aliran, yang sama dengan injektor yang umum dipakai pada kromatografi gas. Injektor ini dapat dipakai pada tekanan sampai sekitar 60 -70 atmosfir. Tetapi septum ini
tidak dapat dipakai untuk semua pelarut kromatografi cair. Selain itu, partikel kecil terlepas dari septum dan cenderung menyumbat
mengakibatkan gangguan pada kolom.
c. Katup putaran (loop valve): dikenal dengan sebutan katup jalan-kitar. Jenis injektor ini umumnya digunakan untuk menginjeksi volume lebih besar
daripada 10 µl dan sekarang digunakan dengan cara otomatis. Volume yang lebih kecil dapat diinjeksikan secara manual memakai adaptor khusus. Pada saat fase gerak dialirkan, katup putaran pada tekanan
atmosfir. Jika katup dijalankan (dibuka), maka cuplikan di dalam putaran akan bergerak menuju kolom. Automatic injector atau disebut juga
autosampler memiliki prinsip yang mirip, hanya saja sistem penyuntikannya bekerja secara otomatis.
2.8.4 Kolom
Menurut Jhonson dan Stevenson, (1978) Kolom merupakan jantung kromatograf.Keberhasilan atau kegagalan analisis bergantung pada pilihan kolom
dan kondisi kerja yang tepat.Kolom dapat dibagi menjadi dua kelompok:
24
kolom 50- 100 cm, sedangkan untuk kemasan mikropartikel berpori
biasanya 10-30 cm.
b. Kolom preparatif: diameter 6 mm atau lebih besar dan panjang 25-100
cm.Kolom umumnya terbuat dari stainlesteel dan biasanya dipakai pada suhu kamar, tetapi suhu yang lebih tinggi dapat juga dipakai. Pengepakan kolom tergantung pada model KCKT yang digunakan KCP, KCC,
pertukaran ion, atau eksklusi ukuran.
2.8.5 Detektor
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen cuplikan dalam aliran yang keluar dari kolom. Detektor-detektor yang baik memiliki
sensitifitas yang tinggi, gangguan (noise) yang rendah, kisar respons linier yang luas, dan memberi tanggapan/respon untuk semua tipe senyawa. Suatu kepekaan yang rendah terhadap aliran dan fluktuasi temperatur sangat diinginkan, tetapi
tidak selalu dapat diperoleh (Johnson dan Stevenson, 1978).
Detektor yang paling banyak digunakan adalah detektor spektrofotometer
UV 254 nm. Detektor lainnya, antara lain: detektor fluometer, detektor ionisasi nyala, detektor elektrokimia dan lain-lain juga telah digunakan (Johnson dan Stevenson, 1978).
2.8.6 Perekam Data
25 2.9 Validasi Metode
Validasi merupakan persyaratan mendasar yang diperlukan untuk menjamin kualitas dan hasil dari semua aplikasi analitik. Validasi metode meliputi
akurasi (ketepatan), presisi, spesifisitas/selektifitas , batas deteksi, batas kuantitasi, linieritas, rentang/kisaran dan kekuatan/ketahanan dan ketangguhan (Ermer dan McB. Miller, 2005).
2.9.1 Akurasi
Akurasi merupakan ketepatan metode analisis atau kedekatan antara nilai
terukur dengan nilai sebenarnya.Kecermatan dinyatakan sebagai persen perolehan kembali analit yang ditambahkan. Akurasi dapat ditentukan dengan dua metode, yakni spiked placebo recovery dan standard addition method. Pada spiked
placebo recovery atau metode simulasi, analit murni ditambahkan (spiked)
kedalam campuran bahan pembawa sediaan farmasi, lalu campuran tersebut dianalisis dan jumlah analit hasil analisis yang dibandingkan dengan jumlah
analit teoritis yang diharapkan. Jika placebo tidak memungkinkan untuk disiapkan, maka sejumlah analit yang telah diketahui kosentrasinya dapat
ditambahkan secara langsung kedalam sediaan farmasi. Metode ini dapat kita dinamakan standard addition method atau lebih dikenal metode penambahan baku (Harmita, 2004).
2.9.2 Presisi
Presisi merupakan ukuran keterulangan metode analisis yang diperoleh
26 2.9.3 Spesifisitas
Spesifisitas/selektifitas adalah kemampuan untuk mengukur analit yang dituju secara tepat dan spesifik dengan adanya komponen lain dalam matriks
sampel seperti ketidakmurnian, produk degradatif dan komponen matriks (Ermer dan McB. Miller, 2005).
2.9.4 Batas Deteksi dan Batas Kuantitasi
Batas deteksi (limit of detection, LOD) adalah konsentrasi analit terendah dalam sampel yang masih dapat dideteksi, meskipun tidak selalu dapat
dikuantifikasi. Sedangkan batas kuantitasi ( limit of quantification, LOQ) adalah konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan
(Rohman,2007).
2.9.5 Linearitas
Linieritas adalah kemampuan suatu metode untuk memperoleh hasil uji
yang secara langsung proposional dengan konsentrasi analit pada kisaran yang telah diberikan. Linieritas dapat ditentukan secara langsung dengan pengukuran
sampel (analit) yang ditambahkan baku pada sekurang-kurangnya lima titik konsentrasi yang mencakup pada seluruh rentang konsentrasi kerja (Ermer dan McB. Miller, 2005).
2.9.6 Rentang
Rentang/kisaran adalah konsentrasi terendah dan tertinggi yang mana
27 2.9.7 Kekuatan
Kekuatan/ketahanan merupakan pengujian kemampuan dari suatu metode untuk tidak terpengaruh oleh adanya variasi parameter metode yang kecil.
Ketahanan dievaluasi dengan melakukan variasi parameter-parameter metode seperti persentase kandungan pelarut organik dalam fase gerak, pH larutan dapar, suhu, waktu pengekstraksian analit, komposisi pengekstraksi dan perbandingan
konsentrasi fase gerak (Rohman,2007).
2.9.8 Kekasaran
Kekasaran/ketangguhan merupakan tingkat reprodusibilitas hasil yang diperoleh dengan kondisi yang bervariasi dan dinyatakan sebagai simpangan baku relatif/relative standard deviation (RSD). Kondisi ini meliputi laboratorium,