BAB II
TINJAUAN PUSTAKA
2.1 Ulkus Peptikum
Ulkus peptikum adalah luka yang berkembang di dalam lapisan mukosa pada saluran pencernaan, khususunya pada bagian atas saluran pencernaan usus halu (doedenum), esofagus, dan lambung (Dufton, 2012).Secara klinis, ulkus peptikum adalah keadaan hilangnya epitel superfisian atau lapisan lebih dalam dengan diameter ≥ 5 mm yang dapat diamati secara endoskopis d an radiologis (Akil, 2009).
Penyakit ulkus peptikum kebanyakan disebabkan karena adanya asam lambung dan enzim pepsin ketika bakteri Helicobacter pylori, obat anti inflamasi nonsteroid (AINS), atau faktor lainnya mengganggu sistem pertahanan mukosa dan penyembuhan mukosa. Hipersekresi dari asam lambung dan pepsin ini yang menghambat mekanisme pertahanan mukosa dan proses penyembuhannya (Berardi dan Welage, 2005).
Menurut Robbins dan kawan-kawan (1995), ulkus peptikum terjadi karena adanya ketidakseimbangan antara mekanisme pertahanan mukosa lambung (faktor defensif) dengan tekanan yang merusak lambung (faktor agresif).
a) Faktor agresifyang merusak pertahanan mukosa adalah Helicobacter pylori, obat anti inflamasi non-steroid, asam lambung/pepsin serta faktor-faktor lingkungan serta kelainan satu atau beberapa faktor pertahanan yang berpengaruh pada kejadian tukak lambung.
a. Faktor preepitel, terdiri dari:
- Mukus dan bikarbonat yang berguna untuk menahan pengaruh asam lambung/pepsin
- Lapisan mukoid, yaitu suatu struktur yang yang terdiri dari mukus dan fibrin, yang terbentuk sebagai respon terhadap ransangan inflamasi
- Permukaan aktif fosfolipid, yang berperan untuk meningkatkan hidrofobisitas membran sel dan meningkatkan viskositas mukus
b. Faktor epitel
- Kecepatan perbaikan mukosa yang rusak, dimana terjadi migrasi sel –sel yang sehat ke daerah yang rusak untuk perbaikan
- Pertahanan selpengauler, kemampuan untuk memelihara elektrik gradien dan mencegah pengasaman sel.
- Kemampuan transporter asam-basa untuk mengangkut bikarbonat kedalam lapisan mukus dan jaringan subepitel dan untuk mendorong asam keluar jaringan.
- Faktor pertumbuha, prostaglandin dan nitrit oksida. c. Faktor subepitel
- Aliran darah (mikrosirkulasi) yang berperan mengangkut nutrisi, oksigen dan bikarbonat ke epitel sel.
- Prostaglandin endogen menekan perlekatan dan ekstravariasi leukosit yang merangsang reaksi inflamasi jaringan.
bentuk gastritis akut pada kronik. Organisme ini melekat pada epitel lambung dan merusak lapisan mukosa perlindungan dan meninggalkan daerah-daerah epitel yang rusak (Mc Guigan, 2001).
2.2 Helicobacter pylori
Helicobacter pylori adalah suatu basilus Gram-negatif, spiral dengan
flagela multipel lebih menyukai lingkungan mikroaerofilik. Helicobacter pylori tidak menyerang jaringan tetapi menghuni bagian gel lendir yang melapisi sel epitelial, dengan bagian kecil dari Helicobacter pylori melekat langsung pada sel epitelial. Kebanyakan orang yang terinfeksi Helicobacter pylori mempunyai neutrofil- neutrofil dalam lamina propia dan kelenjar epitel dan suatu peningkatan dalam sel radang kronik pada lamina propia.Kolonisasi Helicobacter pylori dalam duodenum terbatas pada daerah metaplasia lambung dan ditemukan dalam epitelium pasien dengan ulkus duodeni (Mc Guigan, 2001). BakteriHelicobacter
pylori bersifat mikroaerofilik dan hidup di lingkungan yang unik, di bawah mukus
dinding lambung yang bersuasana asam. Bakteri ini mempunyai enzim urease yang dapat memecah ureum menjadi amonia yang bersifat basa, sehingga tercipta lingkungan memungkinkan bakteri ini dapat bertahan hidup di dalam lambung (Rani dan Fauzi, 2009).
Bakteri Helicobacter pylori adalah bakteri yang sangat suka pada kondisi
kelembapan yang tinggi, memerlukan karbondioksida yang lumayan banyak, butuh
sedikit oksigen, dan bersifat sangat patogenik. Infeksi Helicobacter pylori pada
saluran cerna bagian atas mempunyai variasi klinis yang luas, mulai dari kelompok
asimtomatik sampai tukak peptik, bahkan dihubungkan dengan keganasan dilambung
Bakteri ini juga mempunyai keunggulan yakni bertahan dan berkembang biak
dalam lambung. Secara umum, ada 3 mekanisme infeksi bakteri H. pylori yang
menyebabkan tukak lambung. Pertama, H. pylori menginfeksi bagian bawah
lambung antrum. Kedua, setelah infeksi akan terjadi peradangan bakteri yang
mengakibatkan peradangan lendir lambung (gastritis), peristiwa ini seringkali
terjadi tanpa penampakan gejala (asimptomotik). Ketiga, terjadinya peradangan
dapat berimplikasi terjadinya tukak lambung atau usus 12 jari. Hal ini bisa terjadi
komplikasi akut, yaitu luka dengan pendarahan dan luka berlubang (Ranidan Fauzi,
2009).
2.3 Terapi Eradikasi Helicobacter pylori
Sasaran terapi adalah menghilangkan nyeri tukak, mengobati ulkus,
mencegah kekambuhan dan mengurangi komplikasi yang berkaitan dengan tukak.
Pada penderita dengan Helicobacter pylori positif, tujuan terapi adalah mengatasi
mikroba dan menyembuhkan penyakit dengan obat yang efektif secara ekonomi
(Sukandar, et.al., 2008).
Terapi eradikasi Helicobacter pylori direkomendasikan untuk semua pasien
yang terinfeksi Helicobacter pylori dengan tukak aktif, tukak yang sudah ada
sebelumnya, atau dengan komplikasi tukak.Regimen individual harus diseleksi
berdasarkan efikasi, toleransi, interaksi obat yang potensial, resistensi antibiotik,
biaya dan kepatuhan pasien.Pengobatan harus diawali dengan regimen 3 obat, karena
pengobatan dengan regimaen 2 obat kurang efektif dan dapat menyebabkan resistensi.
Pengobatan dengan regimen 3 terapi yaitu menggunakan kombinasi dari dua
antibiotik klaritomisin, amoksisilin dan pompa proton inhibitor. Amoksisilin diganti
dengan metroniazol atau pun kombinasi antara metronidazol dan amoksisilin yang
2.4 Amoksisillin trihidrat 2.4.1 Uraian bahan
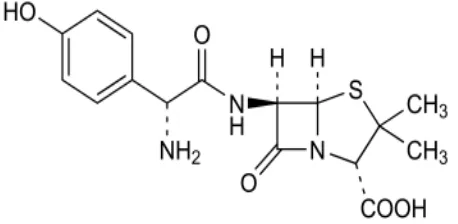
Gambar 2.1Struktur amoksisilin(Ditjen POM, 2014)
Amoksisilin mengandung tidak kurang dari 90,0% C16H19N3O5S.3H20, dihitung terhadap zat anhidrat. Mempunyai potensi setara dengan tidak kurang dari 900 μg dan tidak lebih dari 1050 μg per mg C16H19N3O5S, dihitung terhadap
zat anhidrat.
Nama Kimia : Asam (2S,5R,6R)-(-)-2-amino-2-(p-hidroksifenil) asetamido]-3,3 dimetil-7-okso-4-tia-1-azabisiklo[3.2.0]-heptan-2-karboksilat trihidrat
Berat Molekul : 419,45
Pemerian : Serbuk hablur; putih; praktis tidak berbau
2.4.2 Farmakologi
Amoksisilin adalah antibiotika golongan β-laktam dengan spektrum luas,
digunakan untuk pengobatan infeksi pada saluran napas, saluran empedu dan saluran
seni, gonorhu, gastroenteritis, meningitis dan infeksi karena Salmonella sp., seperti
demam tipoid. Amoksisilin merupakan turunan penisilin yang tahan asam tetapi tidak
tahan terhadap penisilanase (Siswandono dan Soekardjo, 1995).
Amoksisilin antibakteri berisifat bakterisid yang sensitif terhadap mikroorganisme dengan mekanisme kerja yaitu menghabat sintesis mukopeptida dinding sel bakteri selama proses multipikasi bakteri. Dengan cara berikatan dangan penisilin-binding-protein 1A (PBP-1A) yang berlokasi di dalam dinding sel bakteri. Amoksisilin lebih efektif menghambat mikroorganisme Gram positif dibandingkan dengan bakteri Gram negatif (Kaur, et al., 2011). Menurut Neal (2005) amoksisilin lebih efektif melawan bakteri Gram-positif yang tidak menghasilkan β-laktamase sedangkan pada bakteri Gram-negatif, amoksisilin
melawan dengan cara menembus pori–pori dalam membran fosfolipid luar. 2.4.3 Farmakokinetik
hati, prostad, empedu, dan cairan senovial, cairan okular, tetapi penetrasinya buruk terhadap sistem saraf pusat kecuali jika terjadi inflamasi. Kadar obat sangat rendah ditemukan di dalam cairan aqueous humor, dan kadar obat rendah di mata, keringat dan ludah. Sekitar 17-20% obat berikatan dengan protein plasma manusia, secara umum albumin. Amoksisilin diekskresikan atau dibuang terutama melalui ginjal, dalam air kemih terdapat dalm bentuk aktif. Waktu paruh (t1/2) nya
adalah 1-1,5 jam (Kaur, et al., 2011).
2.5 Sistem Penghantaran Obat Tertahan di Lambung
Sistem gastroretentifadalah sistem yang dapat tertahan didalam lambung untuk beberapa jam dan oleh karena itu secara siknifikan dapat memperpanjang waktu tinggal obat. Perpanjangan waktu tinggal obat didalam lambung dapat mempengaruhi bioavabilitas, mengurangi obat yang terbuang, dan mempengaruhi kelarutan untuk obat-obat yang memiliki kelarutan rendah di lingkungan dengan pH yang tinggi, juga dapat digunakan untuk penghantaran obat yang bekerja lokal di lambung dan bagian proksimal usus halus (Sharma, et al.,2011).
Banyak teknik yang telah dikembangkan untuk mendapatkan sistem penghantaran obat yang dapat tertahan dilambung.Beberapa teknik seperti sistem pengapungan, sistem pengembangan dan pembesaran, sistem bioadhesif, dan sistem yang berdensitas tinggi merupakan teknik yang banyak dikembangkan untuk mendapatkan sistem gastroretentif ini (Sharma, et al.,2011).
Kandidat obat yang sesuai untuk sediaan yang tertahan di lambung (Garg dan Gupta, 2008; Swetha, et al., 2012):
b. Obat-obat yang kelarutan rendah dalam pH alkalis misalnya: furosemida, diazepam, verapamil, dan klordiazepoksida.
c. Obat-obat yang terutama diabsorbsi dalam lambung atau bagian atas dari saluran pencernaan misalnya: amoksisilin.
d. Obat-obat yang mempunyai rentang absorpsi yang sempit di dalam saluran pencernaan misalnya seperti: siklosporin, metotreksat, levodopa, dan riboflavin.
e. Obat-obat yang diabsorbsi cepat dari saluran pencernaan misalnya: metronidazol, dan tetrasikilin.
f. Obat-obat yang tidak stabil dan terdegradasi didalam kolon misalnya ranitidin, metronidazol, dan metformin HCl.
g. Obat-obat yang mengganggu mikroba kolon misalnya antibiotik untuk
Helicobacter pylori.
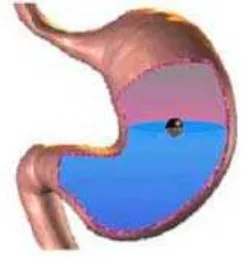
2011).Sistem penghantaran mengapungdalam lambung dapat dilihat pada Gambar 2.2.
Gambar 2.2Sistem mengapung di dalam lambung (Bardonnet, et al., 2006) Sistem penghantaran obat mengapung diklasifikasikan dalam tiga variabel mekanisme yaitu sistem effervescent, sistem non-effervescent, dan sistem pembentuk rakit (Murthy, et al, 2015).
a. Sistem effervescent
Sistem ini dibuat dalam bentuk matriks dengan menggunakan polimer yang dapat mengembang seperti HPMC, senyawa polisakarida lain, kitosan, dan berbagai komponen effervescent seperti natrium bikarbonat, kalsium karbonat, asam sitrat atau asam tartrat. Sediaan ini dirancang sedemikian rupa, sehingga ketika kontak dengan cairan lambung, maka gas karbondioksida (CO2) akan terlepas dan terperangkap dalam sistem hidrokoloid yang mengembang. Hal ini membantu sediaan untuk mengapung (Goyal, et al., 2011).
b. Sistem non-effervescent
Sistem non-effervescent ini mengembang apabila terjadi kontak yang cukup lama dengan cairan lambung sehingga mencegah keluarnya obat dari lambung.Sistem ini cenderung menyangkut di daerah mendekati spinkter pilori.Salah satu metode formulasi yang dilakukan untuk membuat sistem ini adalah dengan mencampurkan obat dengan gel, yang mengembang ketika kontak dengan cairan lambung.Contoh dari tipe sistem penghantaran obat ini adalah sistem koloid gel, sistem kompartemen mikroporos, beadsalginat, dan mikrobalon (Murthy, et al., 2015).
Pada umumnya dalam formulasi sistem non-effervescent ini menggunakan bahan yang mampu membentuk gel atau memiliki kemampuan mengembang yang baik seperti senyawa hidrokoloid, polisakarida. Juga biasa digunakan bentuk matriks dari polimer-polimer seperti polimetaakrilat, poliakrilat, polistiren dan bioadesif polimer yaitu: kitosan dan karbopol (Gopalakrishnan dan Chenthilnathan, 2011).
c. Sistem pembentuk rakit
2.6.1 Keuntungan sistem penghantaran obat mengapung
Sistem penghantaran obat melalui sistem mengapung ini merupakan teknologi penghantaran obat dengan retensi lambung yang lebih lama dan memiliki beberapa keuntungan dalam pemberian obat. Menurut Sharma dan kawan-kawan (2011) beberapa keuntungan tersebut meliputi:
a. Peningkatan penyerapan obat, karena peningkatan waktu tinggal di lambung dan peningkatan waktu kontak obat dengan daerah penyerapan.
b. Penghantaran obat yang dapat dikendalikan pelepasannya. c. Penghantaran obat secara lokal untuk daerah kerja di lambung.
d..Meminimalkan terjadinya iritasi pada mukosa lambung karena obat-obatan tertentu, dengan cara melepaskan obat secara lambat pada tingkat terkendali. e. Digunakan untuk pengobatan gangguan pencernaan.
f. Menggunakan peralatan yang sederhana dan konvensional dalam formulasinya. g. Kemudahan dalam penggunaannya dan meningkatkan faktor kepatuhan pasien
menjadi lebih baik.
h. Penghantaran obat pada daerah tertentu
2.6.2 Kekurangan sistem penghantaran obat mengapung
Disamping memiliki banyak keuntungan sistem penghantaran obat mengapungini, terdapat pula kekurangan dari sistem ini yaitu (Sharma, et al., 2011):
a. Retensi lambung dipengaruhi oleh banyak faktor seperti makanan, pH dan motilitas lambung. Faktor-faktor ini tidak pernah tetap dan karenanya daya apung sediaan tidak dapat diprediksi.
c. Variabilitas tinggi dalam waktu pengosongan lambung serta membutuhkan cairan lambung yang cukup untuk mempertahankan sediaan tetap berada di lambung.
d. Pengosongan lambung untuk pasien dalam keadaan tidur tidak dapat diprediksi dan bergantung pula pada diameter dan ukuran sediaan
floatingtersebut. Oleh karena itu sebaiknya tidak diberikan sediaan ini saat
pasien akan tidur.
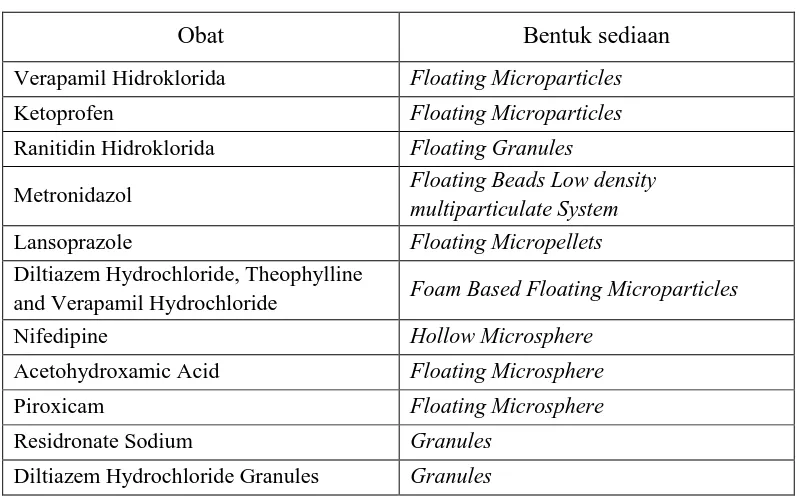
Daftar beberapa obat yang diformulasi dalam bentuk sistem penghantaran obat mengapung dapat dilihat pada tabel di bawah ini:
Tabel 2.1 Daftar obat dalam bentuksistem penghantaran obat mengapung (Sharma, et al., 2011)
Obat Bentuk sediaan
Verapamil Hidroklorida Floating Microparticles
Ketoprofen Floating Microparticles
Ranitidin Hidroklorida Floating Granules
Metronidazol Floating Beads Low density
multiparticulate System
Lansoprazole Floating Micropellets
Diltiazem Hydrochloride, Theophylline
and Verapamil Hydrochloride Foam Based Floating Microparticles
Nifedipine Hollow Microsphere
Acetohydroxamic Acid Floating Microsphere
Piroxicam Floating Microsphere
Residronate Sodium Granules
Diltiazem Hydrochloride Granules Granules
2.7 Kapsul
juga keras.Kebanyakan kapsul-kapsul yang diedarkan di pasaran adalah kapsul yang semuanya dapat ditelan oleh pasien, untuk keuntungan dalam pengobatan.Kapsul gelatin yang keras merupakan jenis yang digunakan oleh ahli farmasi masyarakat dalam menggabungkan obat-obat secara mendadak dan di lingkungan para pembuat sediaan farmasi dalam memproduksi kapsul pada umumnya (Ansel, 2008).
2.8 Natrium Alginat
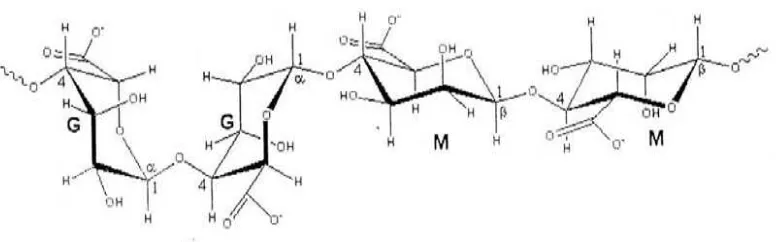
Gambar 2.4Struktur kimia alginat (Thom, et al., 1981)
Asam alginat adalah kopolimer biner yang terdiri dari residu β
-D-mannuronat (M) dan α-L-asam guluronat (G) yang tersusun dalam blok-blok yang membentuk rantai linear. Kedua unit tersebut berikatan pada atom C1 dan C4 dengan susunan homopolimer dari masing-masing residu (MM dan GG) dan suatu blok heteropolimer dari dua residu (MG) (Thom, et al., 1981).
buatan pH 1,2 disebabkan komponen penyusun cangkang kapsul alginat yaitu kalsium guluronat (Bangun, et.al., 2005).
2.9 Uji Pelepasan
Uji pelepasan dilakukan dengan uji disolusi menggunakan seperangkat alat uji disolusi. Disolusi merupakan proses dimana suatu bahan kimia atau bahan obat menjadi terlarut dalam suatu pelarut. Dalam sistem biologik, pelarut atau disolusi obat dalam media air merupakan suatu bagian penting sebelum kondisi absorpsi sistemik (Shargel dan Yu, 1988).
Pelepasan obat dari bentuk sediaan dan absorbsi dalam tubuh dikontrol oleh sifat fisika kimia dari obat dan bentuk yang diberikan, serta sifat-sifat fisika kimia dan fisiologis dari sistem biologis. Konsentrasi obat, kelarutan dalam air, ukuran molekul, bentuk kristal, ikatan protein, dan pKa adalah faktor-faktor fisiko kimia yang harus dipahami untuk mendesain sediaan pelepasan terkontrol atau terkendali (Martin, et al., 2008).
Sejumlah metode untuk menguji disolusi secara in vitro telah dilakukan.Bila suatu sediaan obat dimasukkan kedalam beaker glass yang berisi air atau dimasukkan kedalam saluran cerna (saluran gastrointestin), obat tersebut mulai masuk kedalam larutan dari bentuk padatnya.Disintegrasi, deagregasi dan disolusi bisa berlangsung secara serentak dengan melepasnya suatu obat dari bentuk dimana obat tersebut diberikan (Martin, et al., 2008).
Faktor-faktor yang mempengaruhi disolusi dibagi atas 3 kategori yaitu: a. Faktor-faktor yang berhubungan dengan sifat fisikokimia obat, meliputi:
ii. Efek ukuran parrtikel, ukuran partikel berkurang dapat memperbesar luas permukaan obat yang berhubungan dengan medium, sehingga laju disolusi akan meningkat.
b. Faktor-faktor yang berhubungan dengan sediaan obat, meliputi:
i. Efek formulasi, laju disolusi suatu bahan obat dapat dipengaruhi bila dicampur dengan bahan tambahan. Bahan pengisi, pengikat dan penghancur yang bersifat hidrofil dapat memberikan sifat hidrofil pada bahan obat yang hidrofob, oleh karena itu disolusi bertambah. Sedangkan bahan tambahan yang hidrofob dapat mengurangi laju disolusi. Hal ini kaitannya dengan kelarutan bahan tambahan yang digunakan.
ii. Efek faktor pembuatan sediaan, metode granulasi dapat mempercepat laju disolusi obat-obat yang kurang larut. Penggunaan bahan pengisi yang bersifat hidrofil seperti laktosa dapat menambah hidrofilisitas bahan aktif dan dapat menambah laju disolusi.
c. Faktor-faktor yang berhubungan dengan uji disolusi, meliputi:
i. Tegangan permukaan medium disolusi, tegangan permukaan mempunyai pengaruh nyata terhadap laju disolusi bahan obat. Surfaktan dapat menurunkan sudut kontak, sehingga dapat meningkatkan proses penetrasi medium disolusi ke matriks. Formulasi tablet dan kapsul konvensional juga menunjukkan penambahan laju disolusi obat-obat yang sukar larut dengan penambahan surfaktan kedalam medium disolusi.
ii. Viskositas medium, semakin tinggi viskostas medium, semakin kecil laju disolusi bahan obat.
Farmakope Indonesia edisi V (2014) menuliskan beberapa alat yang dapat digunakan untuk melakukan uji disolusi yaitu:
a. Tipe keranjang
Alat terdiri dari sebuah wadah bertutup yang terbuat dari kaca atau bahan transparan lain yang inert; sebuah motor; batang logam yang digerakkan oleh motor dan keranjang berbentuk silinder.Wadah tercelup sebagian di dalam suatu tangas air yang sesuai, berukuran sedemikian sehingga dapat mempertahankan suhu didalam wadah (37o±0,5o) selama pengujian berlangsung dan menjaga agar gerakan air dalam tangas air halus dan tetap. Wadah disolusi memiliki kapasitas 1000 ml, memiliki tinggi 160-210 mm, diameter 98-106 mm. Untuk mencegah penguapan dapat digunakan suatu penutup yang sesuai. Suatu alat pengatur kecepatan digunakan untuk mengatur kecepatan putaran yang dikehendaki dan mempertahankan kecepatan sesuai dengan yang tertera di monografi dalam batas kurang lebih 4%.
b. Tipe dayung
Sama seperti alat tipe keranjang, kecuali pada alat ini digunakan dayung yang terdiri dari daun dan batang sebagai pengaduk. Batang berada pada posisi sedemikian sehingga sumbunya tidak lebih dari 2 mm pada setiap titik dari sumbu vertikal wadah dan berputar dengan halus tampa goyangan yang berarti. Jarak 25±2 mm antara daun dan bagian dalam dasar wadah dipertahankan selama pengujian berlangsung.
c. Silinder kaca bolak-balik
tidak mengabsorbsi, dirancang untuk menyambungkan bagian atas dan alas silinder yang bergerak bolak balik, dan sebuah motor yang berfungsi menggerakkan silinder. Labu tercelup sebagian di dalam suatu tangas air yang sesuai dengan ukuran sedemikian sehingga dapat mempertahankan suhu di dalam wadah selama pengujian berlangsung.
d. Sel yang dapat dialiri
Alat terdiri dari sebuah wadah dan sebuah pompa untuk media disolusi; sebuah sel yang dapat dialiri, sebuah tangas air yang dapat mempertahankan suhu media. Pompa mendorong media disolusi ke atas melalui pompa sel. Pompa memiliki kapasitas aliran 240 ml per jam dan 960 ml per jam, dengan laju aliran baku 4 ml, 8 ml dan 16 ml per menit. Alat memberikan aliran yang konstan; profil aliran adalah sinusoidal dengan 120±10 pulsa/denyut per menit. Sel terbuat dari bahan yang inert dan transparan, dipasang vertikal dengan suatu sistem penyaringan yang mencegah lepasnya partikel tidak larut dari bagian atas sel bagian bawah yang meruncing umumnya diisi dengan butiran kaca kecil dengan diameter lebih kurang 5 mm yang diletakkan pada bagian ujung untuk mencegah cairan masuk ke dalam tabung, terdapat suatu alat pemengang untuk meletakkan bentuk sediaan tertentu, misalnya tablet.
2.10 Uji Aktivitas Antibakteri
mengontrol kemoterapi obat. Kegunaan uji antimikroba adalah diperolehnya susatu sistem pengobatan yang efektif dan efisien.Beberapa macam metode uji antimikroba dijelaskan berikut ini (Pratiwi, 2008).
2.10.1 Metode difusi
- Metode agar cakram difusi
Metode ini merupakan metode yang paling sering digunakan, lazim dikenal dengan cara Kirby-Bauer. Metode ini telah dikembangkan sejak tahun 1940, digunakan dalam banyak uji klinis mikrobiologi untuk pengujian sensitivitas antimikroba. Sekarang ini, banyak santandar umum dan diakui telah dipublikasikan oleh Clinical Laboratory Standart Institute(2012) untuk menguji bakteri dan jamur, meskipun tidak semua bakteri tertentu dapat diuji menggunakan metode ini.Salah satu contoh gambar hasil pengujian ativitas antibakteri menggunakan metode difusi agar dapat dilihat pada Gambar 2.5.
Gambar 2.5 Metode difusi cakram agar (tes Kirby & Bauer) terhadap bakteri C.albicas (Balouiri, et al., 2016)
kondisi yang sesuai. Umumnya, agen antimikroba akan berdifusi ke agar dan menghambat pertumbuhan dari mikroorganisme uji dan diameter dari daerah hambat diukur (Balouiri, et al., 2016). Antimikroba memberikan hasil kualitatif dengan kategori sensitif, intermediat, dan resisten(Jorgensen dan Ferraro, 2009).
- Metode E-test
Metode E-test digunakan untuk mengestimasi konsentrasi hambat minimum (KHM), yaitu konsentrasi minimal suatu agen antimikroba untuk menghambat pertummbuhan mikroorganisme. Pada metode ini digunakan stip plastik yang mengandung agen antimikroba dari kadar yang terendah hingga kadar yang tertinggi dan diletakkan pada permukaan media agar yang telah ditanami mikroorganisme. Metode pengujian ini dapat dilihat pada Gambar 2.6. Pengamatan dilakukan pada area jernih yang telah ditimbulkannya yang menunjukkan kadar agen antimikroba yang menghambat pertumbuhan mikroorganisme pada media agar (Pratiwi, 2008).
Gambar 2.6Metode E-test (Pratiwi, 2008)
- Metode difusi lain
mikroorganisme.Beberapa diantara metode tersebut yang paling umum digunakan adalah metode difusi sumur agar, metode difusi penyumbat agar, metode goresan menyilang, dan metode makanan kuno.(Balouiri, et al., 2016).
2.10.2 Metode dilusi
Metode dilusi (metode pengenceran) merupakan metode yang dilakukan dengan mengencerkan zat antimikroba dan dimasukkan kedalam tabung-tabung reaksi steril.Masing-masing tabung tersebut ditambahkan sejumlah mikroba uji yang telah diketahui jumlahnya.Pada interval tertentu, dilakukan pemindahan dari tabung reaksi ke dalam tabung-tabung berisi media steril kemudian diinkubasi dan diamati penghambatan pertumbuhan.Metode dilusi dibedakan menjadi dua yaitu dilusi cair dan dilusi padat (Pratiwi, 2008).
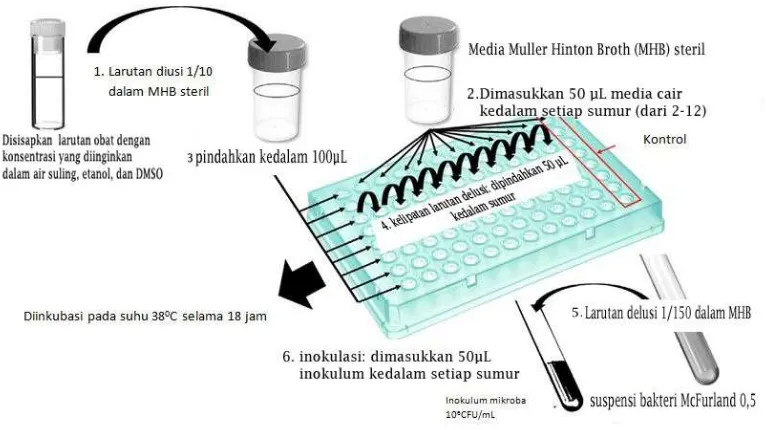
- Metode dilusi cair
Gambar 2.7 Mikrodilusi cair untuk uji antibakteri berdasarkan CLSI (Balouiri, et al., 2016)
- Metode dilusi padat
Metode ini sama dengan metode dilusi cair namaun menggunakan media padat, keuntungan dari metode ini adalah satu konsentrasi dari agen antimikroba yang diuji dapat digunakan untuk menguji beberapa mikroba uji (Pratiwi, 2008). 2.10.3 Media pertumbuhan bakteri
Menurut Irianto (2006) media pertumbuhan bakteri berdasarkan kegunaannya dapat di bagi atas:
1. Media selektif yaitu media biakan yang mengandung paling sedikit satu bahan yang dapat menghambat perkembangbiakan mikroorganisme yang tidak diinginkan dan membolehkan perkembangbiakan mikroorganisme tertentu yang ingin diisolasi.
2. Media difrensial yaitu media yang digunakan untuk menyeleksi suatu mikroorganisme dari berbagai jenis dalam suatu lempengan agar
2.10.4 Fase pertumbuhan bakteri
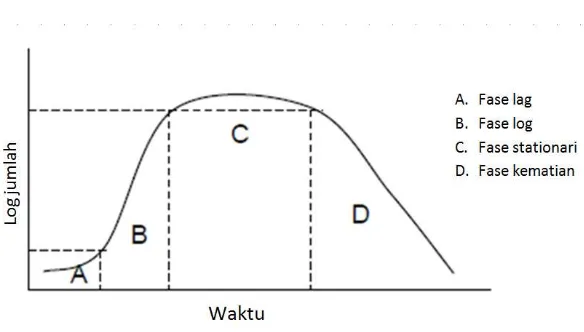
Ada empat macam fase pertumbuhan bakteri menurut Pratiwi (2008), yaitu:
1. Fase lag merupakan fase adaptasi dimana tidak adanya peningkatan jumlah sel, yang ada hanya peningkatan ukuran sel. Lama fase ini tergantung pada kondisi dan jumlah awal mikroorganisme dan media pertumbuhan.
2. Fase log atau fase eksponensial merupakan fase dimana mikroorganisme tumbuh dan membelah pada kecepatan maksimum, tergantung pda genetika mikroorganisme, sifat media, dan kondisi pertumbuahan. Untuk organisme aerob yang membatasi pertumuhan adalah oksigen.
3. Fase stationer merupakan fase dimana pertumbuhana mikrooranisme terthenti dan terjadi keseimbangan antara jumlah sel yang membelah dengan jumlah sel yang mati dan terjadi akumulasi produk buangan yang bersifat toksik. 4. Fase kamatian merupakan fase dimana jumlah sel yang mati meningkat
karena ketidaktersediaan nutrisi dan akumulasi produk buangan yang bersifat toksik.
Gambar kurva pertumbuhan bakteri dapat dilihat pada gambar dibawah ini: