LAPORAN PRAKTIKUM FISIKA DASAR II HUBUNGAN KONSENTRASI LARUTAN DENGAN KAPASITAS KALOR JENISNYA
Kelompok : I Putu Wesa Angga Jaya (2108521010) Ruben Hamonangan S. (2108521014) Dosen : I Putu Tedy Indrayana, S. Pd,.M. Sc.
PROGRAM STUDI FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS UDAYANA
2022
I. TUJUAN
1. Mengetahui Kapasistas Kalor Jenis Larutan Garam
2. Membuat Grafik Konsentrasi Larutan Terhadap Kapasitas Kalor Jenis 3. Mengetahui Hubungan Konsentrasi Larutan dengan Kapasitas Kalor
Jenisnya
II. DASAR TEORI
Larutan garam dapur atau yang nama kimianya Natrium klorida adalah bubuk atau kristal zat tak berwarna (cenderung tampak berwarna putih dalam kehidupan sehari-hari), tidak berbau, dengan cita rasa asin. Dalam kehidupan sehari-hari, Natrium klorida dikenal sebagai garam meja. Rumus kimianya adalah NaCl.
Larutan NaCl adalah garam yang terbentuk sebagai hasil dari reaksi antara senyawa asam kuat dan basa kuat, umumnya dibuat dengan pencampuran asam kuat Asam Klorida (HCl) dan basa kuat Natrium Hidroksida (NaOH), (Hardjono, 2018).
Kalor didefinisikan sebagai energi panas yang dimiliki oleh suatu zat. Secara umum untuk mendeteksi adanya kalor yang dimiliki oleh suatu benda yaitu dengan mengukur suhu benda tersebut. Jika suhunya tinggi maka kalor yang dikandung oleh benda sangat besar, begitu juga sebaliknya jika suhunya rendah maka kalor yang dikandung sedikit. secara matematis Kalor dapat dirumuskansebagai berikut:
𝑄 = 𝑚. 𝐶. ∆𝑇 (2.1)
Keterangan
𝑄 = 𝐾𝑎𝑙𝑜𝑟 𝑏𝑒𝑛𝑑𝑎 (𝐽𝑜𝑢𝑙𝑒) 𝑚 = 𝑚𝑎𝑠𝑠𝑎 𝑏𝑒𝑛𝑑𝑎 (𝑘𝑔)
𝐶 = 𝑘𝑎𝑝𝑎𝑠𝑖𝑡𝑎𝑠 𝑘𝑎𝑙𝑜𝑟 𝑗𝑒𝑛𝑖𝑠 𝑏𝑒𝑛𝑑𝑎 ( 𝐽 𝑘𝑔. 𝐾)
∆𝑇 = 𝑝𝑒𝑟𝑢𝑏𝑎ℎ𝑎𝑛 𝑠𝑢ℎ𝑢 (𝐾)
Perpindahan kalor (heat transfer) adalah ilmu untuk perpindahan energi yang terjadi karena adanya perbedaan suhu diantara benda atau material. Dimana energi yang pindah itu dinamakan kalor. Kalor telah diketahui dapat berpindah dari tempat dengan temperatur lebih tinggi ke tempat dengan temperatur lebih rendah.
Hukum pencampuran kalor juga terjadi karena kalor itu berpindah, sedangkan pada kalorimeter, perpindahan kalor dapat terjadi dalam bentuk pertukaran kalor dengan luar sistem. Jadi pemberian atau pengurangan kalor tidak saja mengubah temperatur atau fasa zat suatu benda secara lokal, melainkan kalor itu merambat ke atau dari bagian lain benda atau tempat lain. Bila dalam suatu sistem terdapat gradien suhu atau bila dua buah benda yang suhunya berbeda dalam kontak ternal, maka panas akan mengalir dari benda yang suhunya lebih tinggi ke benda yang suhunya lebih rendah atau akan terjadi perpindahan energi. Proses tersebut disebut perpindahan panas (Zemansky, 1986).
Kesetimbangan termal tercapai bila dua benda atau sistem mencapai suhu yang sama dan berhenti untuk bertukar energi melalui panas. Ketika dua benda ditempatkan bersama-sama, objek dengan energi panas-lebih akan kehilangan energi ke objek dengan energi panas yang lebih sedikit. Akhirnya, suhu mereka akan sama dan mereka akan berhenti pertukaran energi panas sebagai objek tidak lebih hangat atau lebih dingin dari yang lain. Pada titik ini, mereka berada dalam keadaan kesetimbangan termal. Kontak termal merupakan konsep penting yang berkaitan dengan kesetimbangan termal. Beberapa sistem yang dianggap berada dalam kontak termal jika mereka mampu mempengaruhi suhu yang lain (Yohanes, 2009).
Kalor jenis adalah banyaknya kalor yang dibutuhkan untuk menaikkan suhu 1 kg zat sebesar 1 derajat celcius. Alat yang digunakan untuk menentukan besar kalor jenis adalah kalorimeter. Menurut asas Black apabila ada dua benda yang suhunya berbeda kemudian disatukan atau dicampur maka akan terjadi aliran kalor dari benda yang bersuhu tinggi menuju benda yang bersuhu rendah. Aliran ini akan berhenti sampai terjadi keseimbangan termal (suhu kedua benda sama).
Secara matematis dapat dirumuskan sebagai berikut:
𝑄𝑙𝑒𝑝𝑎𝑠= 𝑄𝑡𝑒𝑟𝑖𝑚𝑎 (2.2)
Sehingga kapasitas kalor jenis dari suatu bahan dapat diketahui dengan membandingkan dengan kapasitas kalor jenis air. Secara matematis dapat dirumuskan sebagai berikut:
𝐶𝑠 = 𝐶𝑎.(𝑚𝑛(𝑇𝑓− 𝑇𝑖)) (𝑚𝑠(𝑇𝑠− 𝑇𝑓))
(2.3) Keterangan
𝐶𝑎 = 𝑘𝑎𝑝𝑎𝑠𝑖𝑡𝑎𝑠 𝑘𝑎𝑙𝑜𝑟 𝑗𝑒𝑛𝑖𝑠 𝑎𝑖𝑟 (4190 𝐽 𝑘𝑔. 𝐾) 𝐶𝑠 = 𝑘𝑎𝑝𝑎𝑠𝑖𝑡𝑎𝑠 𝑘𝑎𝑙𝑜𝑟 𝑏𝑎ℎ𝑎𝑛 ( 𝐽
𝑘𝑔. 𝐾) 𝑚𝑠 = 𝑚𝑎𝑠𝑠𝑎 𝑏𝑎ℎ𝑎𝑛 (𝑘𝑔)
𝑚𝑛 = 𝑚𝑎𝑠𝑠𝑎 𝑎𝑖𝑟 (𝑘𝑔) 𝑇𝑠 = 𝑠𝑢ℎ𝑢 𝑏𝑎ℎ𝑎𝑛 (𝐾) 𝑇𝑓= 𝑠𝑢ℎ𝑢 𝑐𝑎𝑚𝑝𝑢𝑟𝑎𝑛 (𝐾) 𝑇𝑖 = 𝑠𝑢ℎ𝑢 𝑎𝑖𝑟 (𝐾)
(Halliday, 2015) III. ALAT DAN BAHAN
1. Neraca 2. Termometer 3. Garam 4. Air
5. Kalorimeter 6. Pemanas 7. Gelas ukur 8. Pengaduk 9. Penyangga
IV. PROSEDUR PERCOBAAN
1. Kalorimeter + termometer ditimbang
2. Air 100 ml ditambahkan ke kalorimeter lalu ditimbang 3. Suhu air didalam kalorimeter diukur
4. Garam ditimbang 10gram dan dicampur dengan 100 ml air 5. Larutan garam dipanaskan sampai 100º C
6. Setelah mencapai 100º C larutan garam dituangkan ke kalorimeter
7. Suhu campuran diukur
8. Kalorimeter yang telah ditambahkan larutan garam ditimbang 9. Tabel Data Pengamatan dibuat
10. Langkah 2-9 dilakukan untuk 20g, 30g, 40g, 50g garam
V. DATA PENGAMATAN
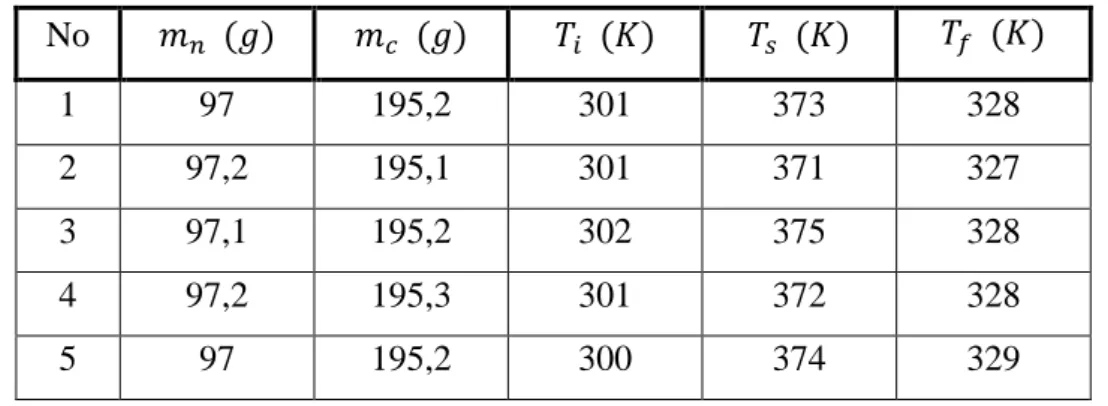
Tabel 5.1 Data Pengamatan Percobaan 1 10gram
No 𝑚𝑛 (𝑔) 𝑚𝑐 (𝑔) 𝑇𝑖 (𝐾) 𝑇𝑠 (𝐾) 𝑇𝑓 (𝐾)
1 97 195,2 301 373 328
2 97,2 195,1 301 371 327
3 97,1 195,2 302 375 328
4 97,2 195,3 301 372 328
5 97 195,2 300 374 329
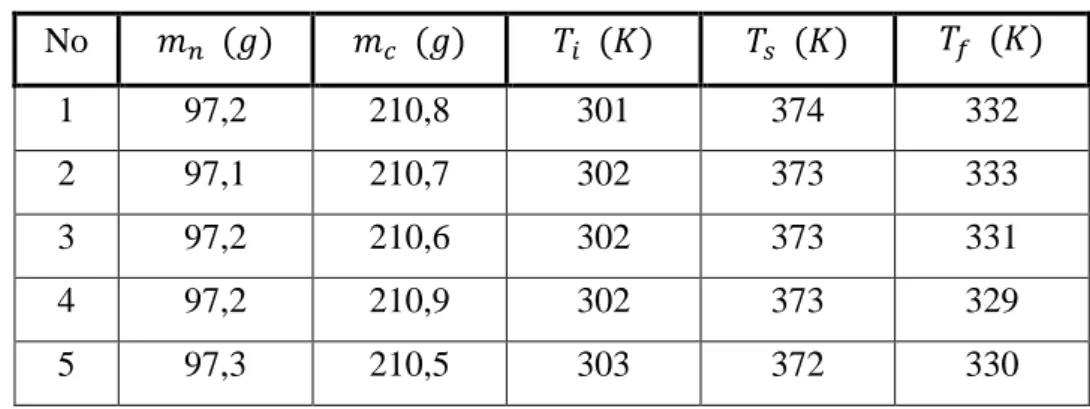
Tabel 5.2 Data Pengamatan Percobaan 2 20gram
No 𝑚𝑛 (𝑔) 𝑚𝑐 (𝑔) 𝑇𝑖 (𝐾) 𝑇𝑠 (𝐾) 𝑇𝑓 (𝐾)
1 97,2 210,8 301 374 332
2 97,1 210,7 302 373 333
3 97,2 210,6 302 373 331
4 97,2 210,9 302 373 329
5 97,3 210,5 303 372 330
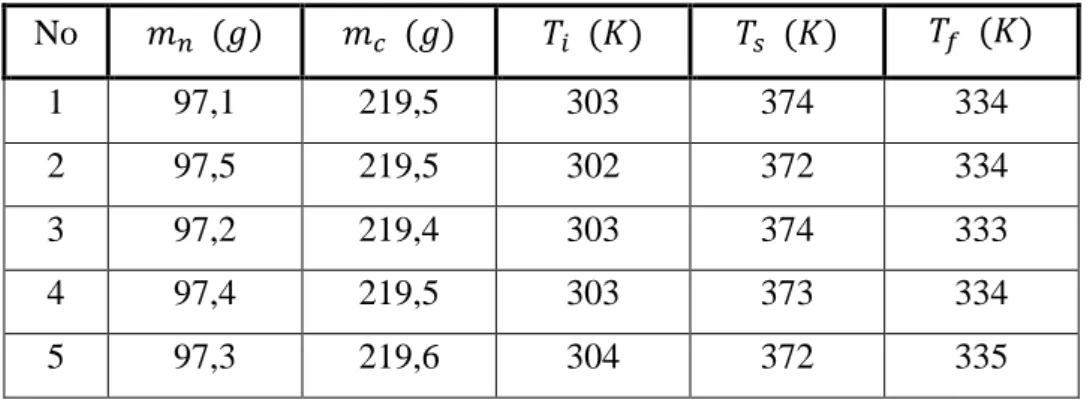
Tabel 5.3 Data Pengamatan Percobaan 3 30gram
No 𝑚𝑛 (𝑔) 𝑚𝑐 (𝑔) 𝑇𝑖 (𝐾) 𝑇𝑠 (𝐾) 𝑇𝑓 (𝐾)
1 97,1 219,5 303 374 334
2 97,5 219,5 302 372 334
3 97,2 219,4 303 374 333
4 97,4 219,5 303 373 334
5 97,3 219,6 304 372 335
Tabel 5.4 Data Pengamatan Percobaan 4 40gram
No 𝑚𝑛 (𝑔) 𝑚𝑐 (𝑔) 𝑇𝑖 (𝐾) 𝑇𝑠 (𝐾) 𝑇𝑓 (𝐾)
1 97,3 230,3 304 374 337
2 97,2 230 305 372 339
3 97,2 230,2 303 373 337
4 97,2 230,4 306 373 335
5 97,1 230,1 302 373 337
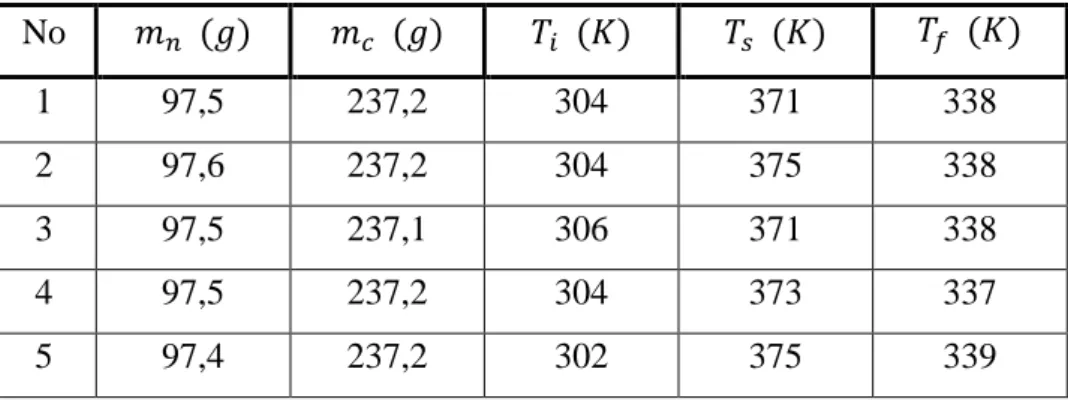
Tabel 5.5 Data Pengamatan Percobaan 5 50gram
No 𝑚𝑛 (𝑔) 𝑚𝑐 (𝑔) 𝑇𝑖 (𝐾) 𝑇𝑠 (𝐾) 𝑇𝑓 (𝐾)
1 97,5 237,2 304 371 338
2 97,6 237,2 304 375 338
3 97,5 237,1 306 371 338
4 97,5 237,2 304 373 337
5 97,4 237,2 302 375 339
VI. ANALISIS DATA 6.1 Ralat Nisbi
Tabel 6.1.1 Ralat Nisbi massa air 10 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,0970 0,0975 -0,0001 1 × 10−8
0,0972 0,0975 0,0001 1 × 10−8
0,0971 0,0975 0 0
0,0972 0,0975 0,0001 1 × 10−8
0,0970 0,0975 -0,0001 1 × 10−8
∑(𝑚 − 𝑚̅ )2 4 × 10−8
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √4 × 10−8
5(5 − 1) = √4 × 10−8 20 = √2 × 10−9 = (4,472 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,0971 ± 4,472 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =4,472 × 10−5
0,0971 × 100%
= 0,046%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,046% = 99,954%
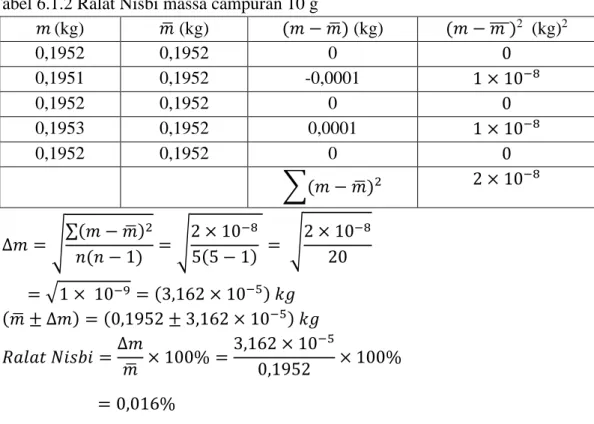
Tabel 6.1.2 Ralat Nisbi massa campuran 10 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,1952 0,1952 0 0
0,1951 0,1952 -0,0001 1 × 10−8
0,1952 0,1952 0 0
0,1953 0,1952 0,0001 1 × 10−8
0,1952 0,1952 0 0
∑(𝑚 − 𝑚̅ )2 2 × 10−8
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √2 × 10−8
5(5 − 1) = √2 × 10−8 20 = √1 × 10−9 = (3,162 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,1952 ± 3,162 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =3,162 × 10−5
0,1952 × 100%
= 0,016%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,016% = 99,984%
Tabel 6.1.3 Ralat Nisbi T air 10 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
301 301 0 0
301 301 0 0
302 301 1 1
301 301 0 0
300 301 -1 1
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √1 × 10−1 = (3,162 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (301 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =3,162 × 10−1
301 × 100%
= 0,105%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,105% = 99,895%
Tabel 6.1.4 Ralat Nisbi T sampel 10 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
373 373 0 0
371 373 -2 4
375 373 2 4
372 373 -1 1
374 373 1 1
∑(𝑇 − 𝑇̅)2 10
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 10
5(5 − 1) = √10 20 = √5 × 10−1 = (7.071 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (373 ± 7.071 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =7.071 × 10−1
373 × 100%
= 0,190%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,190% = 99,810%
Tabel 6.1.5 Ralat Nisbi T campuran 10 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
328 328 0 0
327 328 -1 1
328 328 0 0
328 328 0 0
329 328 1 1
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √1 × 10−1 = (3,162 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (328 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =3,162 × 10−1
328 × 100%
= 0,096%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,096% = 99,904%
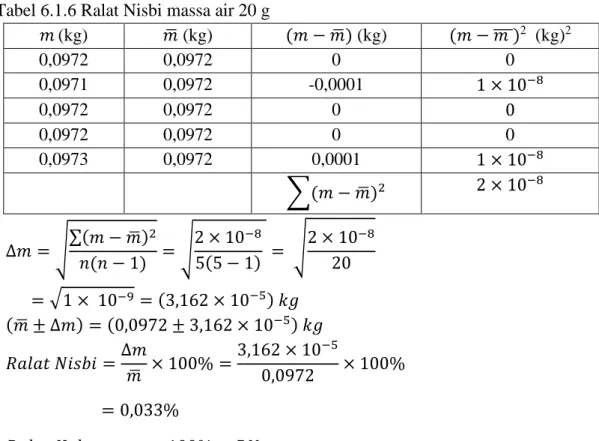
Tabel 6.1.6 Ralat Nisbi massa air 20 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,0972 0,0972 0 0
0,0971 0,0972 -0,0001 1 × 10−8
0,0972 0,0972 0 0
0,0972 0,0972 0 0
0,0973 0,0972 0,0001 1 × 10−8
∑(𝑚 − 𝑚̅ )2 2 × 10−8
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √2 × 10−8
5(5 − 1) = √2 × 10−8 20 = √1 × 10−9 = (3,162 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,0972 ± 3,162 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =3,162 × 10−5
0,0972 × 100%
= 0,033%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,033% = 99,967%
Tabel 6.1.7 Ralat Nisbi massa campuran 20 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,2108 0,2107 0,0001 1 × 10−8
0,2107 0,2107 -0 0
0,2106 0,2107 -0,0001 1 × 10−8
0,2109 0,2107 0,0002 4 × 10−8
0,2105 0,2107 -0,0002 4 × 10−8
∑(𝑚 − 𝑚̅ )2 1 × 10−7
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √1 × 10−7
5(5 − 1) = √1 × 10−7 20 = √5 × 10−9 = (7,071 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,2107 ± 7,071 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =7,071 × 10−5
0,2107 × 100%
= 0,034%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,034% = 99,966%
Tabel 6.1.8 Ralat Nisbi T air 20 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
301 302 -1 1
302 302 0 0
302 302 0 0
302 302 0 0
303 302 1 1
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √2 × 10−1 = (3,162 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (302 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =3,162 × 10−1
302 × 100%
= 0,105%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,105% = 99,895%
Tabel 6.1.9 Ralat Nisbi T sampel 20 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
374 373 1 1
373 373 0 0
373 373 0 0
373 373 0 0
372 373 -1 1
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √2 × 10−1 = (3,162 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (373 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =3,162 × 10−1
373 × 100%
= 0,085%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,085% = 99,915%
Tabel 6.1.10 Ralat Nisbi T campuran 20 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
332 331 1 1
333 331 2 4
331 331 0 0
329 331 -2 4
330 331 -1 1
∑(𝑇 − 𝑇̅)2 10
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 10
5(5 − 1) = √10 20 = √5 × 10−1 = (7,071 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (331 ± 7,071 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =7,071 × 10−1
331 × 100%
= 0,214%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,214% = 99,786%
Tabel 6.1.11 Ralat Nisbi massa air 30 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,0971 0,0973 -0,0002 4 × 10−8
0,0975 0,0973 0,0002 4 × 10−8
0,0972 0,0973 -0,0001 1 × 10−8
0,0974 0,0973 0,0001 1 × 10−8
0,0973 0,0973 0 0
∑(𝑚 − 𝑚̅ )2 1 × 10−7
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √1 × 10−7
5(5 − 1) = √1 × 10−7 20 = √5 × 10−9 = (7,071 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,0973 ± 7,071 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =7,071 × 10−5
0,0973 × 100%
= 0,073%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,073% = 99,927%
Tabel 6.1.12 Ralat Nisbi massa campuran 30 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,2195 0,2195 0 0
0,2195 0,2195 0 0
0,2194 0,2195 -0,0001 1 × 10−8
0,2195 0,2195 0 0
0,2196 0,2195 0,0001 1 × 10−8
∑(𝑚 − 𝑚̅ )2 2 × 10−8
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √2 × 10−8
5(5 − 1) = √2 × 10−8 20 = √1 × 10−9 = (3,162 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,2195 ± 3,162 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =3,162 × 10−5
0,2195 × 100%
= 0,014%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,014% = 99,986%
Tabel 6.1.13 Ralat Nisbi T air 30 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
303 303 0 0
302 303 -1 1
303 303 0 0
303 303 0 0
304 303 1 1
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √1 × 10−1 = (3,162 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (303 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =3,162 × 10−1
303 × 100%
= 0,104%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,104% = 99,896%
Tabel 6.1.14 Ralat Nisbi T sampel 30 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
374 373 1 1
372 373 -1 1
374 373 1 1
373 373 0 0
372 373 -1 1
∑(𝑇 − 𝑇̅)2 4
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 4
5(5 − 1) = √4 20 = √2 × 10−1 = (4,472 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (373 ± 4,472 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =4,472 × 10−1
373 × 100%
= 0,120%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,120% = 99,880%
Tabel 6.1.15 Ralat Nisbi T campuran 30 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
334 334 0 0
334 334 0 0
333 334 -1 1
334 334 0 0
335 334 1 1
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √1 × 10−1 = (3,162 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (334 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =3,162 × 10−1
334 × 100%
= 0,095%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,095% = 99,905%
Tabel 6.1.16 Ralat Nisbi massa air 40 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,0973 0,0972 0,0001 1 × 10−8
0,0972 0,0972 0 0
0,0972 0,0972 0 0
0,0972 0,0972 0 0
0,0971 0,0972 -0,0001 1 × 10−8
∑(𝑚 − 𝑚̅ )2 2 × 10−8
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √2 × 10−8
5(5 − 1) = √2 × 10−8 20 = √1 × 10−9 = (3,162 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,0972 ± 3,162 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =3,162 × 10−5
0,0972 × 100%
= 0,033%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,033% = 99,967%
Tabel 6.1.17 Ralat Nisbi massa campuran 40 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,2303 0,2302 0,0001 1 × 10−8
0,23 0,2302 -0,0002 4 × 10−8
0,2302 0,2302 0 0
0,2304 0,2302 0,0002 4 × 10−8
0,2301 0,2302 -0,0001 1 × 10−8
∑(𝑚 − 𝑚̅ )2 1 × 10−7
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √1 × 10−7
5(5 − 1) = √1 × 10−7 20 = √5 × 10−9 = (7,071 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,2302 ± 7,071 × 10−5) 𝑘𝑔
𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =7,071 × 10−5
0,2302 × 100%
= 0,031%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,031% = 99,969%
Tabel 6.1.18 Ralat Nisbi T air 40 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
304 304 0 0
305 304 -1 1
303 304 -1 1
306 304 2 4
302 304 2 4
∑(𝑇 − 𝑇̅)2 10
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 10
5(5 − 1) = √10 20 = √5 × 10−1 = (7,071 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (304 ± 7,071 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =7,071 × 10−1
304 × 100%
= 0,233%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,233% = 99,767%
Tabel 6.1.19 Ralat Nisbi T sampel 40 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
374 373 1 1
372 373 -1 1
373 373 0 0
373 373 0 0
373 373 0 0
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √1 × 10−1 = (3,162 × 10−1) 𝐾
(𝑇̅ ± ∆𝑇) = (373 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =4,472 × 10−1
373 × 100%
= 0,085%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,085% = 99,15%
Tabel 6.1.20 Ralat Nisbi T campuran 40 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
337 337 0 0
339 337 2 4
337 337 0 0
335 337 -2 4
337 337 0 0
∑(𝑇 − 𝑇̅)2 8
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 8
5(5 − 1) = √8 20 = √4 × 10−1 = (6,325 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (337 ± 6,325 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =6,325 × 10−1
337 × 100%
= 0,188%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,188% = 99,812%
Tabel 6.1.21 Ralat Nisbi massa air 50 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,0975 0,0975 0 0
0,0976 0,0975 -0,0001 1 × 10−8
0,0975 0,0975 0 0
0,0975 0,0975 0 0
0,0974 0,0975 -0,0001 1 × 10−8
∑(𝑚 − 𝑚̅ )2 2 × 10−8
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √2 × 10−8
5(5 − 1) = √2 × 10−8 20
= √1 × 10−9 = (3,162 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,0975 ± 3,162 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =3,162 × 10−5
0,0975 × 100%
= 0,032%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,032% = 99,968%
Tabel 6.1.22 Ralat Nisbi massa campuran 50 g
𝑚(kg) 𝑚̅ (kg) (𝑚 − 𝑚̅ ) (kg) (𝑚 − 𝑚 ̅̅̅)2 (kg)2
0,2372 0,2372 0 0
0,2373 0,2372 0,0001 1 × 10−8
0,2371 0,2372 0,0001 1 × 10−8
0,2372 0,2372 0 0
0,2372 0,2372 0 0
∑(𝑚 − 𝑚̅ )2 2 × 10−8
∆𝑚 = √∑(𝑚 − 𝑚̅ )2
𝑛(𝑛 − 1) = √2 × 10−8
5(5 − 1) = √2 × 10−8 20 = √1 × 10−9 = (3,162 × 10−5) 𝑘𝑔 (𝑚̅ ± ∆𝑚) = (0,2372 ± 3,162 × 10−5) 𝑘𝑔 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑚
𝑚̅ × 100% =3,162 × 10−5
0,2372 × 100%
= 0,013%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,013% = 99,987%
Tabel 6.1.23 Ralat Nisbi T air 50 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
304 304 0 0
304 304 0 0
306 304 2 4
304 304 0 0
302 304 -2 4
∑(𝑇 − 𝑇̅)2 8
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 8
5(5 − 1) = √8 20 = √4 × 10−1 = (6,325 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (304 ± 6,325 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =6,325 × 10−1
304 × 100%
= 0,208%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,208% = 99,792%
Tabel 6.1.24 Ralat Nisbi T sampel 50 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
371 373 -2 4
375 373 2 4
371 373 -2 4
373 373 0 0
373 373 2 4
∑(𝑇 − 𝑇̅)2 16
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 16
5(5 − 1) = √16 20 = √8 × 10−1 = (8,944 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (373 ± 8,944 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =8,944 × 10−1
373 × 100%
= 0,240%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,240% = 99,760%
Tabel 6.1.25 Ralat Nisbi T campuran 50 g
𝑇(K) 𝑇̅ (K) (𝑇 − 𝑇 ̅ ) (K) (𝑇 − 𝑇 ̅ )2 (K)2
338 338 0 0
338 338 0 0
338 338 0 0
337 338 -1 1
339 338 1 1
∑(𝑇 − 𝑇̅)2 2
∆𝑇 = √∑(𝑇 − 𝑇̅)2
𝑛(𝑛 − 1) = √ 2
5(5 − 1) = √2 20 = √1 × 10−1 = (3,162 × 10−1) 𝐾 (𝑇̅ ± ∆𝑇) = (338 ± 3,162 × 10−1) 𝐾 𝑅𝑎𝑙𝑎𝑡 𝑁𝑖𝑠𝑏𝑖 =∆𝑇
𝑇 × 100% =3,162 × 10−1
338 × 100%
= 0,094%
𝑅𝑎𝑙𝑎𝑡 𝐾𝑒𝑏𝑒𝑛𝑎𝑟𝑎𝑛 = 100% − 𝑅𝑁
= 100% − 0,094% = 99,906%
6.2 Perhitungan
6.2.1 Perhitungan Kalor Jenis Larutan Garam 10 g
Dik: m air = (𝑚̅ ± ∆𝑚) = (0,0971 ± 4,472 × 10−5) 𝑘𝑔
m campuran = (𝑚̅ ± ∆𝑚) = (0,1952 ± 3,162 × 10−5) 𝑘𝑔 Suhu air = (𝑇̅ ± ∆𝑇) = (301 ± 3,162 × 10−1) 𝐾
Suhu sampel = (𝑇̅ ± ∆𝑇) = (373 ± 7.071 × 10−1) 𝐾 Suhu campuran = (𝑇̅ ± ∆𝑇) = (328 ± 3,162 × 10−1) 𝐾 Dit: m sampel =
Cs = Jawab:
m sampel = m campuran – m air
(𝑚̅ ± ∆𝑚) = (0,1952 ± 3,162 × 10−5) − (0,0971 ± 4,472 × 10−5)
(𝑚̅ ± ∆𝑚) = (0,1952 − 0,0975) ± √(3,162 × 10−5)2+ (4,472 × 10−5)2 (𝑚̅ ± ∆𝑚) = (0,0981 ± 5,477 × 10−5) 𝑘𝑔
𝐶𝑠 = 𝐶𝑎.(𝑚𝑛(𝑇𝑓− 𝑇𝑖)) (𝑚𝑠(𝑇𝑠− 𝑇𝑓))
= 4190.((0,0971 ± 4,472 × 10−5) ((328 ± 3,162 × 10−1) − (301 ± 3,162 × 10−1))) ((0,0981 ± 5,477 × 10−5)((373 ± 7.071 × 10−1) − (328 ± 3,162 × 10−1)))
= 4190.((0,0971 ± 4,472 × 10−5) (27 ± 4,472 × 10−1)) ((0,0981 ± 5,477 × 10−5)(45 × 7,746 × 10−1))
= 4190.(2,622 ± 9,505 × 10−2) (4,415 ± 7,603 × 10−2)
= 4190 × (0,594 ± 1,045 × 10−2)
= (𝟐𝟒𝟖𝟖, 𝟑𝟕𝟔 ± 𝟒, 𝟑𝟕𝟗 × 𝟏𝟎+𝟏) 𝑱 𝒌𝒈. 𝑲
6.2.2 Perhitungan Kalor Jenis Larutan Garam 20 g
Dik: m air = (𝑚̅ ± ∆𝑚) = (0,0972 ± 3,162 × 10−5) 𝑘𝑔
m campuran = (𝑚̅ ± ∆𝑚) = (0,2107 ± 7,071 × 10−5) 𝑘𝑔 Suhu air = (𝑇̅ ± ∆𝑇) = (302 ± 3,162 × 10−1) 𝐾
Suhu sampel = (𝑇̅ ± ∆𝑇) = (373 ± 3,162 × 10−1) 𝐾 Suhu campuran = (𝑇̅ ± ∆𝑇) = (331 ± 7,071 × 10−1) 𝐾 Dit: m sampel =
Cs = Jawab:
m sampel = m campuran – m air
(𝑚̅ ± ∆𝑚) = (0,2107 ± 7,071 × 10−5) − (0,0972 ± 3,162 × 10−5)
(𝑚̅ ± ∆𝑚) = (0,2107 − 0,0972) ± √(7,071 × 10−5)2+ (3,162 × 10−5)2 (𝑚̅ ± ∆𝑚) = (0,1135 ± 7,746 × 10−5) 𝑘𝑔
𝐶𝑠 = 𝐶𝑎.(𝑚𝑛(𝑇𝑓− 𝑇𝑖)) (𝑚𝑠(𝑇𝑠− 𝑇𝑓))
= 4190.((0,0972 ± 3,162 × 10−5)((331 ± 7,071 × 10−1) − (302 ± 3,162 × 10−1))) ((0,1135 ± 7,746 × 10−5)((373 ± 3,162 × 10−1) − (331 ± 7,071 × 10−1)))
= 4190.((0,0972 ± 3,162 × 10−5)(29 ± 7,456 × 10−1)) ((0,1135 ± 7,746 × 10−5)(42 ± 7,456 × 10−1))
= 4190.(2,819 ± 7,529 × 10−2) (4,767 ± 8,797 × 10−2)
= 4190 × (0,591 ± 1,920 × 10−2)
= (𝟐𝟒𝟕𝟕, 𝟕𝟖𝟕 ± 𝟖, 𝟎𝟒𝟓 × 𝟏𝟎+𝟏) 𝑱 𝒌𝒈. 𝑲
6.2.3 Perhitungan Kalor Jenis Larutan Garam 30 g
Dik: m air = (𝑚̅ ± ∆𝑚) = (0,0973 ± 7,071 × 10−5) 𝑘𝑔
m campuran = (𝑚̅ ± ∆𝑚) = (0,2195 ± 3,162 × 10−5) 𝑘𝑔 Suhu air = (𝑇̅ ± ∆𝑇) = (303 ± 3,162 × 10−1) 𝐾
Suhu sampel = (𝑇̅ ± ∆𝑇) = (373 ± 4,472 × 10−1) 𝐾 Suhu campuran = (𝑇̅ ± ∆𝑇) = (334 ± 3,162 × 10−1) 𝐾 Dit: m sampel =
Cs = Jawab:
m sampel = m campuran – m air
(𝑚̅ ± ∆𝑚) = (0,2195 ± 3,162 × 10−5) − (0,0973 ± 7,071 × 10−5)
(𝑚̅ ± ∆𝑚) = (0,2195 − 0,0973) ± √(3,162 × 10−5)2+ (7,071 × 10−5)2 (𝑚̅ ± ∆𝑚) = (0,1222 ± 7,746 × 10−5) 𝑘𝑔
𝐶𝑠 = 𝐶𝑎.(𝑚𝑛(𝑇𝑓− 𝑇𝑖)) (𝑚𝑠(𝑇𝑠− 𝑇𝑓))
= 4190.((0,0973 ± 7,071 × 10−5) ((334 ± 3,162 × 10−1) − (303 ± 3,162 × 10−1))) ((0,1222 ± 7,746 × 10−5)((373 ± 4,472 × 10−1) − (334 ± 3,162 × 10−1)))
= 4190.((0,0973 ± 7,071 × 10−5)(31 ± 4,472 × 10−1)) ((0,1222 ± 7,746 × 10−5)(39 ± 5,477 × 10−1))
= 4190.(3,016 ± 4,357 × 10−2) (4,766 ± 6,700 × 10−2)
= 4190 × (0,633 ± 1,276 × 10−2)
= (𝟐𝟔𝟓𝟏, 𝟒𝟗𝟖 ± 𝟓, 𝟑𝟒𝟔 × 𝟏𝟎+𝟏) 𝑱 𝒌𝒈. 𝑲
6.2.4 Perhitungan Kalor Jenis Larutan Garam 40 g
Dik: m air = (𝑚̅ ± ∆𝑚) = (0,0972 ± 3,162 × 10−5) 𝑘𝑔
m campuran = (𝑚̅ ± ∆𝑚) = (0,2302 ± 7,071 × 10−5) 𝑘𝑔 Suhu air = (𝑇̅ ± ∆𝑇) = (304 ± 7,071 × 10−1) 𝐾
Suhu sampel = (𝑇̅ ± ∆𝑇) = (373 ± 3,162 × 10−1) 𝐾 Suhu campuran = (𝑇̅ ± ∆𝑇) = (337 ± 6,325 × 10−1) 𝐾 Dit: m sampel =
Cs = Jawab:
m sampel = m campuran – m air
(𝑚̅ ± ∆𝑚) = (0,2302 ± 7,071 × 10−5) − (0,0972 ± 3,162 × 10−5)
(𝑚̅ ± ∆𝑚) = (0,0,2302 − 0,0972) ± √(3,162 × 10−5)2+ (7,071 × 10−5)2 (𝑚̅ ± ∆𝑚) = (0,1330 ± 7,746 × 10−5) 𝑘𝑔
𝐶𝑠 = 𝐶𝑎.(𝑚𝑛(𝑇𝑓− 𝑇𝑖)) (𝑚𝑠(𝑇𝑠− 𝑇𝑓))
= 4190.((0,0972 ± 3,162 × 10−5)((337 ± 6,325 × 10−1) − (304 ± 7,071 × 10−1))) ((0,1330 ± 7,746 × 10−5)((373 ± 3,162 × 10−1) − (337 ± 6,325 × 10−1)))
= 4190.((0,0972 ± 3,162 × 10−5)(33 ± 9,487 × 10−1)) ((0,1330 ± 7,746 × 10−5)(36 ± 7,071 × 10−1))
= 4190.(3,208 ± 9,222 × 10−2) (4,788 ± 9,409 × 10−2)
= 4190 × (0,670 ± 2,333 × 10−2)
= (𝟐𝟖𝟎𝟕, 𝟑𝟑𝟓 ± 𝟗, 𝟕𝟕𝟓 × 𝟏𝟎+𝟏) 𝑱 𝒌𝒈. 𝑲
6.2.5 Perhitungan Kalor Jenis Larutan Garam 50 g
Dik: m air = (𝑚̅ ± ∆𝑚) = (0,0975 ± 3,162 × 10−5) 𝑘𝑔
m campuran = (𝑚̅ ± ∆𝑚) = (0,2372 ± 3,162 × 10−5) 𝑘𝑔 Suhu air = (𝑇̅ ± ∆𝑇) = (304 ± 6,325 × 10−1) 𝐾
Suhu sampel = (𝑇̅ ± ∆𝑇) = (373 ± 8,944 × 10−1) 𝐾 Suhu campuran = (𝑇̅ ± ∆𝑇) = (338 ± 3,162 × 10−1) 𝐾 Dit: m sampel =
Cs = Jawab:
m sampel = m campuran – m air
(𝑚̅ ± ∆𝑚) = (0,2372 ± 3,162 × 10−5) − (0,0975 ± 3,162 × 10−5)
(𝑚̅ ± ∆𝑚) = (0,2372 − 0,0975) ± √(3,162 × 10−5)2+ (3,162 × 10−5)2 (𝑚̅ ± ∆𝑚) = (0,1397 ± 4,472 × 10−5) 𝑘𝑔
𝐶𝑠 = 𝐶𝑎.(𝑚𝑛(𝑇𝑓− 𝑇𝑖)) (𝑚𝑠(𝑇𝑠− 𝑇𝑓))
= 4190.((0,0975 ± 3,162 × 10−5)((338 ± 3,162 × 10−1) − (304 ± 6,325 × 10−1))) ((0,1397 ± 4,472 × 10−5)((373 ± 8,944 × 10−1) − (338 ± 3,162 × 10−1)))
= 4190.((0,0975 ± 3,162 × 10−5)(34 ± 7071 × 10−1)) ((0,1397 ± 4,472 × 10−5)(35 ± 9,486 × 10−1))
= 4190.(3,315 ± 6,895 × 10−2) (4,890 ± 1,325 × 10−1)
= 4190 × (0,678 ± 2,316 × 10−2)
= (𝟐𝟖𝟒𝟎, 𝟒𝟔𝟎 ± 𝟗, 𝟕𝟎𝟒 × 𝟏𝟎+𝟏) 𝑱 𝒌𝒈. 𝑲
6.3 Grafik
6.3.1 Grafik Hubungan Konsentrasi Larutan Garam terhadap Kalor Jenisnya
Grafik 6.1 Hubungan Konsentrasi Garam dengan Kalor Jenisnya
VII. PEMBAHASAN
Pada praktikum kali ini bertujuan untuk mengukur kapasitas kalor jenis larutan garam dan mengetahui hubungan konsentrasi larutan garam dengan kapasitas kalorjenisnya. Praktikum ini didasari dengan konsep bahwa, ketika dua buah benda berinteraksi maka akan terjadi perpindahan kalor antara kedua benda tersebut. Perpindahan kalor ini terjadi sampai kedua benda mengalami kesetimbangan termal. Sesuai dengan hukum Black dimana kalor yang dilepaskan benda bertemperatur tinggi sama dengan kalor yang diterima benda bertempratur rendah. Selain itu praktikum ini didasari oleh pernyataan bahwa semakin pekat konsentrasi larutan maka semakin lama waktu yang dibutuhkan untuk meningkatkan temperaturnya.
Pada praktikum kali ini mengunakan konsentrasi larutan garam yang sebagai variable bebasnya dan volume air dan suhu larutan sebagai variable kontrolnya.
Pada percobaan pertama dilakukan dengan menggunakan 10gram garam dapur dicampurkan dengan 100 ml air didapatkan hasil data pengamatan berupa massa air pada kalorimeter (𝑚̅̅̅̅ ± ∆𝑚𝑛 𝑛) sebesar (0,0971 ± 4,472 × 10−5) 𝑘𝑔, massa campuran (𝑚̅̅̅̅ ± ∆𝑚𝑐 𝑐) sebesar (0,1952 ± 3,162 × 10−5) 𝑘𝑔, suhu air (𝑇̅ ±𝑖
2400 2450 2500 2550 2600 2650 2700 2750 2800 2850 2900
0 10 20 30 40 50 60
Kalor Jenis (J/kg.K)
Konsentrasi Garam (gram)
Kalor Jenis
∆𝑇𝑖) sebesar (301 ± 3,162 × 10−1) 𝐾, suhu larutan garam (𝑇̅ ± ∆𝑇𝑠 𝑠) sebesar (373 ± 7.071 × 10−1) 𝐾 ,dan suhu campuran (𝑇̅ ± ∆𝑇𝑓 𝑓) sebesar (328 ± 3,162 × 10−1) 𝐾. Selain itu didapatkan dari perhitungan berupa massa larutan garam (𝑚̅̅̅̅ ± ∆𝑚𝑠 𝑠) sebesar (0,0981 ± 5,477 × 10−5) 𝑘𝑔, dan kapasitas kalor jenis larutan garam (𝐶̅ ± ∆𝐶𝑠 𝑠) sebesar (2488,376 ± 4,379 × 10+1) 𝐽
𝑘𝑔.𝐾. Pada percobaan kedua dilakukan dengan menggunakan 20gram garam dapur dicampurkan dengan 100 ml air didapatkan hasil data pengamatan berupa massa air pada kalorimeter (𝑚̅̅̅̅ ± ∆𝑚𝑛 𝑛) sebesar (0,0972 ± 3,162 × 10−5) 𝑘𝑔, massa campuran (𝑚̅̅̅̅ ± ∆𝑚𝑐 𝑐) sebesar (0,2107 ± 7,071 × 10−5) 𝑘𝑔, suhu air (𝑇̅ ±𝑖
∆𝑇𝑖) sebesar (302 ± 3,162 × 10−1) 𝐾, suhu larutan garam (𝑇̅ ± ∆𝑇𝑠 𝑠) sebesar (373 ± 3,162 × 10−1) 𝐾,dan suhu campuran (𝑇̅ ± ∆𝑇𝑓 𝑓) sebesar (331 ± 7,071 × 10−1) 𝐾. Selain itu didapatkan dari perhitungan berupa massa larutan garam (𝑚̅̅̅̅ ± ∆𝑚𝑠 𝑠) sebesar (0,1135 ± 7,746 × 10−5) 𝑘𝑔, dan kapasitas kalor jenis larutan garam (𝐶̅ ± ∆𝐶𝑠 𝑠) sebesar (2477,787 ± 8,045 × 10+1) 𝐽
𝑘𝑔.𝐾 . Pada percobaan ketiga dilakukan dengan menggunakan 30gram garam dapur dicampurkan dengan 100 ml air didapatkan hasil data pengamatan berupa massa air pada kalorimeter (𝑚̅̅̅̅ ± ∆𝑚𝑛 𝑛) sebesar (0,0973 ± 7,071 × 10−5) 𝑘𝑔, massa campuran (𝑚̅̅̅̅ ± ∆𝑚𝑐 𝑐) sebesar (0,2195 ± 3,162 × 10−5) 𝑘𝑔, suhu air (𝑇̅ ±𝑖
∆𝑇𝑖) sebesar (303 ± 3,162 × 10−1) 𝐾, suhu larutan garam (𝑇̅ ± ∆𝑇𝑠 𝑠) sebesar (373 ± 4,472 × 10−1) 𝐾,dan suhu campuran (𝑇̅ ± ∆𝑇𝑓 𝑓) sebesar (334 ± 3,162 × 10−1) 𝐾. Selain itu didapatkan dari perhitungan berupa massa larutan garam (𝑚̅̅̅̅ ± ∆𝑚𝑠 𝑠) sebesar (0,1222 ± 7,746 × 10−5) 𝑘𝑔, dan kapasitas kalor jenis larutan garam (𝐶̅ ± ∆𝐶𝑠 𝑠) sebesar (2651,498 ± 5,346 × 10+1) 𝐽
𝑘𝑔.𝐾 . Pada percobaan keempat dilakukan dengan menggunakan 40gram garam dapur dicampurkan dengan 100 ml air didapatkan hasil data pengamatan berupa massa air pada kalorimeter (𝑚̅̅̅̅ ± ∆𝑚𝑛 𝑛) sebesar (0,0972 ± 3,162 × 10−5) 𝑘𝑔, massa campuran (𝑚̅̅̅̅ ± ∆𝑚𝑐 𝑐) sebesar (0,2302 ± 7,071 × 10−5) 𝑘𝑔, suhu air (𝑇̅ ±𝑖
∆𝑇𝑖) sebesar (304 ± 7,071 × 10−1) 𝐾, suhu larutan garam (𝑇̅ ± ∆𝑇𝑠 𝑠) sebesar (373 ± 3,162 × 10−1) 𝐾,dan suhu campuran (𝑇̅ ± ∆𝑇𝑓 𝑓) sebesar (337 ± 6,325 × 10−1) 𝐾. Selain itu didapatkan dari perhitungan berupa massa larutan
garam (𝑚̅̅̅̅ ± ∆𝑚𝑠 𝑠) sebesar (0,1330 ± 7,746 × 10−5) 𝑘𝑔, dan kapasitas kalor jenis larutan garam (𝐶̅ ± ∆𝐶𝑠 𝑠) sebesar (2807,335 ± 9,775 × 10+1) 𝐽
𝑘𝑔.𝐾 . Pada percobaan kelima dilakukan dengan menggunakan 50gram garam dapur dicampurkan dengan 100 ml air didapatkan hasil data pengamatan berupa massa air pada kalorimeter (𝑚̅̅̅̅ ± ∆𝑚𝑛 𝑛) sebesar (0,0975 ± 3,162 × 10−5) 𝑘𝑔, massa campuran (𝑚̅̅̅̅ ± ∆𝑚𝑐 𝑐) sebesar (0,2372 ± 3,162 × 10−5) 𝑘𝑔, suhu air (𝑇̅ ±𝑖
∆𝑇𝑖) sebesar (304 ± 6,325 × 10−1) 𝐾, suhu larutan garam (𝑇̅ ± ∆𝑇𝑠 𝑠) sebesar (373 ± 8,944 × 10−1) 𝐾,dan suhu campuran (𝑇̅ ± ∆𝑇𝑓 𝑓) sebesar (338 ± 3,162 × 10−1) 𝐾. Selain itu didapatkan dari perhitungan berupa massa larutan garam (𝑚̅̅̅̅ ± ∆𝑚𝑠 𝑠) sebesar (0,1397 ± 4,472 × 10−5) 𝑘𝑔, dan kapasitas kalor jenis larutan garam (𝐶̅ ± ∆𝐶𝑠 𝑠) sebesar (2840,460 ± 9,704 × 10+1) 𝐽
𝑘𝑔.𝐾. Dari data di atas dapat dilihat bahwa kapasitas kalor jenis semakin besar ketika konsentrasi larutan garamnya semakin pekat. Hal ini sesuai dengan pernyataan yang menyatakan bahwa semakin pekat konsentrasi larutan semakin lama waktu yang diperlukan untuk meningkatkan temperaturnya. Namun terjadi anomaly pada larutan garam 20gram. Disebabkan karena pada saat pengambilan data alat yang digunakan seadanya serta kekurang telitian pengamat pada saat menimbang dan mengukur suhu.
VIII. KESIMPULAN
Dari hasil pengamatan dan pengukuran didapatkan kesimpulan sebagai berikut:
1. Kapasitas Kalor Jenis larutan garam dengan konsentrasi garam 10gram, 20gram, 30gram, 40gram dan 50gram secara berturut turut sebesar (2488,376 ± 4,379 × 10+1) 𝐽
𝑘𝑔.𝐾, (2477,787 ± 8,045 × 10+1) 𝐽
𝑘𝑔.𝐾, (2651,498 ± 5,346 × 10+1) 𝐽
𝑘𝑔.𝐾, (2807,335 ± 9,775 × 10+1) 𝐽
𝑘𝑔.𝐾, (2840,460 ± 9,704 × 10+1) 𝐽
𝑘𝑔.𝐾.
2. Dari grafik dapat dilihat bahwa kapasitas kalor jenis larutan garam meningkat seiringnya dengan meningkatnya konsentrasi larutan garam tersebut.
3. Semakin pekat konsentrasi larutan garam maka semakin tinggi kapasitas kalor jenisnya dan semakin encer konsentrasi larutan garam semakin kecil kapasitas kalor jenisnya.
DAFTAR PUSTAKA
David Halliday, 2015, Fisika Dasar Jilid 1, Jakarta: Erlangga
Hardjono Sastrohamidjojo, 2018, KIMIA DASAR, Yogyakarta: UGM PRESS
Mark W. Zemansky, 1986, KALOR DAN TERMODINAMIKA, Bandung:
Penerbit ITB
Yohanes Surya, 2009, Suhu dan Termodinamika, Tanggerang: PT Kandel
Lampiran 1. Doumentasi