PENGARUH PEMBERIAN EKSTRAK KENCUR (Kaempferia
galanga L) TERHADAP PROFIL FARMAKOKINETIKA
NATRIUM DIKLOFENAK
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
MUTIA MUSTIKA
NIM 111524073
\
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGARUH PEMBERIAN EKSTRAK KENCUR (Kaempferia
galanga L) TERHADAP PROFIL FARMAKOKINETIKA
NATRIUM DIKLOFENAK
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas SumateraUtara
OLEH:
MUTIA MUSTIKA
NIM 111524073
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Dr. Edy Suwarso, S.U., Apt.
PENGESAHAN SKRIPSI
PENGARUH PEMBERIAN EKSTRAK KENCUR (Kaempferia
galanga L) TERHADAP PROFIL FARMAKOKINETIKA
NATRIUM DIKLOFENAK
OLEH:
MUTIA MUSTIKA
NIM 111524073
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal: 17 Desember 2014
Disetujui oleh:
Pembimbing I, Panitia Penguji,
Dr. Edy Suwarso, S.U., Apt. Prof. Dr. Karsono, Apt. NIP 130935857 NIP 195409091982011001
Pembimbing II,
NIP 130935857
Prof. Dr. M. T. Simanjuntak, M.Sc., Apt. Dr. Kasmirul Ramlan Sinaga, M.Si., Apt. NIP 195212041980021001 NIP 195504241983031003
Dra. Azizah Nasution, M.Sc., Ph.D., Apt. NIP 195503121983032001
Medan, Januari 2015 Fakultas Farmasi
Universitas Sumatera Utara Pembantu Dekan 1,
Prof. Dr. Julia Reveny, M.Si., Apt.
KATA PENGANTAR
Puji dan syukur kepada Allah SWT yang telah melimpahkan rahmat dan anugerah-Nya sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini yang berjudul “Pengaruh Pemberian Ekstrak Kencur (Kaemferia
galangal, L) Terhadap Profil Farmakokinetika Natrium Diklofenak”. Skripsi ini
diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada
Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyampaikan terimakasih kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU yang telah memberikan
bantuan dan fasilitas selama masa pendidikan. Bapak Dr. Edy Suwarso, S.U., Apt dan Bapak Prof. Dr. M. T. Simanjuntak, M.Sc., Apt. yang telah membimbing
penulis dengan penuh kesabaran, tulus dan ikhlas selama penelitian hingga selesainya penulisan skripsi ini. Bapak Drs. Panal Sitorus M.Si., Apt., selaku dosen wali yang telah membimbing penulis selama masa pendidikan. Bapak Prof.
Dr. Karsono, Apt., Bapak Dr. Kasmirul Ramlan Sinaga, M.Si., Apt., Ibu Dra. Azizah Nasution, M.Sc., Ph.D., Apt., sebagai dosen penguji yang telah memberikan saran dan kritikan kepada penulis hingga selesainya penulisan skripsi ini. Ibu Marianne, S.Si., M.Si., Apt., selaku kepala Laboratorium Farmakologi dan Toksikologi, Ibu Dra. Suwarti Aris, M.Si., Apt., selaku Kepala Laboratorium Farmakognosi dan
Bapak Prof. Dr. M.T. Simanjuntak, M.Sc., Apt., selaku Koordinator Laboratorium
Ucapan terimakasih dan penghargaan yang tulus tiada terhingga kepada Ayahanda Syafaruddin dan Ibunda Herliya, S.Pd., tercinta serta Kakak Rafika
Handayani S.E, Arwita naela AM.Keb dan Adik Nurul FiQih atas doa, dorongan dan semangat baik moril maupun materil kepada penulis selama perkuliahan hingga selesainya penyusunan skripsi ini. Kepada seluruh Staf Pengajar, Pegawai
Tata Usaha dan sahabat-sahabat (Riandi, Agnes, Ari, Ira, Fitri, Rina, Nita, Rizha, Fika) yang telah membantu selama penelitian hingga selesainya penulisan skripsi
ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih memiliki banyak kekurangan, oleh karena itu sangat diharapkan kritikan dan saran yang
dapat menyempurnakan skripsi ini.
Medan, Januari 2015 Penulis,
PENGARUH PEMBERIAN EKSTRAK KENCUR
(Kaempferia galanga
L)
TERHADAP PROFIL FARMAKOKINETIKANATRIUM DIKLOFENAK
Abstrak
Pemberian natrium diklofenak kepada manusia yang telah mengkonsumsi ekstrak kencur (Kaempferia galanga L) sebelumnya dapat menimbulkan interaksi pada fase farmakokinetika, terutama pada metabolisme natrium diklofenak. Tujuan penelitian ini adalah untuk mengetahui apakah ekstrak kencur berpengaruh terhadap profil farmakokinetika dari natrium diklofenak.
Penelitian dilakukan dengan menggunakan 20 ekor tikus jantan yang beratnya 150 – 200 gram, yang terbagi dalam empat kelompok, kelompok pertama diberikan larutan natrium diklofenak baku 2,25 mg/kg bb. Selanjutnya kelompok 2, 3 dan 4 diberi ekstrak kencur dengan dosis 20, 40, 80 mg/kg bb selama 7 hari berturut-turut. Selanjutnya diberikan larutan natrium diklofenak 2,25 mg/kg bb setelah 4 jam pemberian ekstrak kencur. Kadar obat dalam urin pada masing-masing tikus dikumpulkan dengan selang waktu waktu 6; 12; 18; 24; 30 jam lalu di vortex dan disentrifuge. Pengukuran kadar Natrium diklofenak dalam urin tikus dilakukan dengan menggunakan alat spektrofotometer ultra violet.
Hasil penelitian diperoleh nilai laju eliminasi (Kel) perlakuan tanpa ekstrak kencur sebesar 0,1121 ± 0,0055 jam-1 menjadi 0,1029 ± 0,0185 jam-1; 0,0891 ± 0,0109 jam-1 dan 0,0821 ± 0,0232 jam-1 setelah pemberian ekstrak kencur 20 mg/kg bb, 40 mg/kg bb, 80 mg/kg bb. Nilai laju metabolisme (Km) sebesar 0,1035 ± 0,0060 jam-1 menjadi 0,0960 ± 0,0197 jam-1; 0,0814 ± 0,0112 jam-1 dan 0,0696 ± 0,0183 jam-1 setelah pemberian ekstrak kencur 20 mg/kg bb, 40 mg/kg bb, 80 mg/kg bb dan nilai paruh (t1/2eliminasi)dengan nilai 6,18 ± 0,30 jam pada perlakuan tanpa ekstrak kencur menjadi 6,91 ± 1,26 jam; 7,86 ± 0,93 jam dan 9,14 ± 3,22 jam pada pemberian ekstrak kencur 20 mg/kg bb, 40 mg/kg bb, 80 mg/kg bb. Penurunan nilai laju metabolisme (Km), nilai laju eliminasi (Kel) dan peningkatan t1/2eliminasi menggambarkan kemampuan ekstrak kencur sebagai penghambat enzim pemetabolisme dalam hati.
THE INFLUENCE OF ADMINISTRATION
(Kaempferia galanga L)
EXTRACT ON THE PHARMACOKINETIC PROFILE OF SODIUM DICKLOFENAC
Abstract
The administrasion of sodium diklofenak to human previously consumed Kaempferia galanga L extract can lead to the possibility of pharmacokinetic interactions, especially in the metabolism of sodium diclofenac. The purpose of this study was to determine whether the Kaempferia galanga L extract affects the pharmacokinetics profile of sodium diclofenac.
The research was conducted using 20 male rats weighing of 150-200 gram, were divided into four groups, the first groups was given sodium diclofenac standard solution of 2.25 mg/kg body weight of extract. Groups 2. 3 and 4 were orally given kaemferia galanga L ekstract with doses 20 mg/kg body weight, 40 mg/kg body weight, 80 mg/kg body weight for 7 days. The next 4 hours each of the 3 groups was administrered standard solution of sodium diclofenac with doses of 2.25 mg/kg body weight. The urin drug levels for each rats is recorded in the interval of 6; 12; 18; 24; 30 hours. The measurement of the sodium diclofenac content in urin is measured by using ultra violet spectrophotometry.
The result obtained that elimination rate (Kel) values the treatment without extracts Kaempferia galanga L decreased from 0.1121 ± 0.0055 hour-1 to 0.1029 ± 0.0185 hour-1; 0.0891 ± 0.0109 hour-1 and 0.0821 ± 0.0232 hour-1 after the treatment of extracts Kaempferia galanga L. Metabolism rate (Km) value also showed decrease from 0.1035 ± 0.0060 hour-1 to 0.0960 ± 0.0197 hour-1; 0.0814 ± 0.0112 hour-1 and 0.0696 ± 0.0183 hour-1 after the treatment of extracts Kaempferia galanga L and the elimination half life value (t1/2elimination)the value 6.18 ± 0.30 hour for treatment without extracts Kaempferia galanga L and 6.91 ± 1.26 hour; 7.86 ± 0.93 hour and 9.14 ± 3.22 hour for the treatment of extracts Kaempferia galanga L. Decrease of metabolism rate (Km), elimination rate (Kel) and increase the elimination half life value (t1/2elimination), describe the ability of extracts Kaempferia galanga L as inhibitors of metabolic enzymes in the liver.
DAFTAR ISI
Halaman
JUDUL ……… i
HALAMAN PENGESAHAN………. ii
KATA PENGANTAR ……… iv
ABSTRAK ……….. vi
ABSTRACT ……….... vii
DAFTAR ISI ………... viii
DAFTAR TABEL……… xii
DAFTAR GAMBAR ……….. xiii
DAFTAR LAMPIRAN ……….. xiv
BAB I PENDAHULUAN ……….. 1
1.1 Latar belakang ……… 1
1.2 Perumusan masalah ……… 3
1.3 Hipotesis ………. 3
1.4 Tujuan penelitian ………... 4
1.5 Manfaat penelitian ………. 4
1.6 Kerangka pikir ……… 5
BAB II TINJAUAN PUSTAKA ……… 6
2.1 Uraian Tumbuhan ……… 6
2.1.1 Sistematika tumbuhan ………... 6
2.1.2 Morfologi tumbuhan ………. 6
2.1.3 Kandungan kimia ……….. 8
2.1.4 Khasiat tumbuhan ………. 9
2.2 Natrium Diklofenak ……… 10
2.3.1 Absorpsi ……… ... 11
2.3.2 Distribusi ……… .. 11
2.3.3 Metabolisme ……… . 12
2.3.4 Ekskresi ……… .... 12
2.4 Parameter Farmakokinetika Ekskresi Urin Kumulatif Obat ……… ... 13
BAB III METODE PENELITIAN ………. 16
3.1 Alat ……… 16
3.2 Bahan ……… 16
3.3 Penyiapan sampel ……… 17
3.3.1 Pengambilan tumbuhan ……… 17
3.3.2 Identifikasi tumbuhan ………. 17
3.3.3 Pengolahan sampel ……….. 17
3.4 Pemeriksaan karakterisasi simplisia ……… 17
3.4.1 Pemeriksaan makroskopik ……….. 18
3.4.2 Pemeriksaan makroskopik ……….. 18
3.4.3 Penetapan kadar air simplisia ……… 18
3.4.4 Penetapan kadar sari yang larut dalam air …………. 19
3.4.5 Penetapan kadar sari yang larut dalam etanol ……… 19
3.4.6 Penetapan kadar abu total ……….. 20
3.4.7 Penetapan kadar abu tidak larut asam ……… 20
3.5 skrining fitokimia serbuk simplisia ……… 20
3.5.1 Pemeriksaan flavonoida ………. 20
3.5.2 Pemeriksaan alkaloida ……….. 21
3.5.5 Pemeriksaan glikosida ……….. 22
3.5.6 Pemeriksaan steroida/triterpenoida ……… 22
3.6 Pembuatan ekstrak etanol rimpang kencur ………. 23
3.7 Pembuatan diklofenak baku ……… 23
3.7.1 Pembuatan larutan induk baku I ……… 23
3.7.2 pembuatan induk baku II ……… 24
3.7.3 Pengukuran panjang gelombang absorpsi ………… 24
3.7.4 Pembuatan kurva baku ……….. 24
3.8 Pembuatan suspensi dan larutan ………. 25
3.8.1 Pembuatan suspensi CMC 1% ………. 25
3.8.2 Pembuatan suspensi natrium diklofenak ………. 25
3.8.3 Pembuatan suspensi ekstrak ………. 25
3.9 Perlakuan terhadap hewan percobaan ……… 26
3.9.1 Perlakuan pada hewan percobaan dengan pemberian natrium diklofenak tanpa pemberian ekstrak etanol rimpang kencur (EERK) ………. 26
3.9.2 Perlakuan pada hewan percobaan dengan pemberian natrium diklofenak dengan pemberian EERK selama 7 hari berturut-turut ……….…… 27
3.10 Analisis data ……….……….……….…… 28
BAB IV HASIL DAN PEMBAHASAN ……….……….…. 29
4.1 Simplisia dan ekstrak …….……….……….….. 29
4.2 Skrining fitokimia ………….……….……….… 31
4.3 Analisis parameter farmakokinetik ……….……… 32
BAB V KESIMPULAN DAN SARAN….……….……… 37
5.1Kesimpulan….……….……….…….……… 37
DAFTAR PUSTAKA ….……….……….…….………. 38
DAFTAR TABEL
Tabel Halaman 4.1 Pemeriksaan karakterisasi simplisia rimpang kencur….………….. 31 4.2 Hasil pemeriksaan skrining fitokimia serbuk simplisia
Rimpang kencur ….……….……….…….………... 31 4.3 Penentuan parameter farmakokinetika data ekskresi urin
DAFTAR GAMBAR
Gambar Halaman
DAFTAR LAMPIRAN
Lampiran Halaman
1 Surat hasil identifikasi tumbuhan ………….……….……… 40
2 Sertifikat analisis natrium diklofenak ……….……….……. 41
3 Gambar hasil makroskopik ………….……….………. 42
4 Perhitungan kadar air serbuk simplisia …….……….……… 44
5 Perhitungan hasil kadar sari larut dalam air .……….……… 45
6 Perhitungan hasil kadar sari larut dalam etanol ………….……… 46
7 Perhitungan abu total serbuk simplisia .……….……… 47
8 Perhitungan hasil penetapan kadar abu tidak larut asam ……….. 49
9 Tabel konversi dosis hewan dengan manusia ……….………… .. 51
10 Bagan perlakuan pada hewan percobaan ……….…………. 52
11 Bagan perlakuan pada hewan percobaan dengan EERK ……….. 53
12 Contoh perhitungan dosis ………….……….……… 54
13 Panjang gelombang natrium diklofenak ………….……… 56
14 Hasil perhitungan parameter farmakokinetik urin kumlatif …….. 59
15 Nilai parameter farmakokinetik natrium diklofenak dalam urin Kumulatif ……….……….……….……….……….……….……. 64
16 Contoh perhitungan nilai parameter farmakokinetika dalam urin Kumulatif natrium diklofenak …….……….……….……….……. 68
PENGARUH PEMBERIAN EKSTRAK KENCUR
(Kaempferia galanga
L)
TERHADAP PROFIL FARMAKOKINETIKANATRIUM DIKLOFENAK
Abstrak
Pemberian natrium diklofenak kepada manusia yang telah mengkonsumsi ekstrak kencur (Kaempferia galanga L) sebelumnya dapat menimbulkan interaksi pada fase farmakokinetika, terutama pada metabolisme natrium diklofenak. Tujuan penelitian ini adalah untuk mengetahui apakah ekstrak kencur berpengaruh terhadap profil farmakokinetika dari natrium diklofenak.
Penelitian dilakukan dengan menggunakan 20 ekor tikus jantan yang beratnya 150 – 200 gram, yang terbagi dalam empat kelompok, kelompok pertama diberikan larutan natrium diklofenak baku 2,25 mg/kg bb. Selanjutnya kelompok 2, 3 dan 4 diberi ekstrak kencur dengan dosis 20, 40, 80 mg/kg bb selama 7 hari berturut-turut. Selanjutnya diberikan larutan natrium diklofenak 2,25 mg/kg bb setelah 4 jam pemberian ekstrak kencur. Kadar obat dalam urin pada masing-masing tikus dikumpulkan dengan selang waktu waktu 6; 12; 18; 24; 30 jam lalu di vortex dan disentrifuge. Pengukuran kadar Natrium diklofenak dalam urin tikus dilakukan dengan menggunakan alat spektrofotometer ultra violet.
Hasil penelitian diperoleh nilai laju eliminasi (Kel) perlakuan tanpa ekstrak kencur sebesar 0,1121 ± 0,0055 jam-1 menjadi 0,1029 ± 0,0185 jam-1; 0,0891 ± 0,0109 jam-1 dan 0,0821 ± 0,0232 jam-1 setelah pemberian ekstrak kencur 20 mg/kg bb, 40 mg/kg bb, 80 mg/kg bb. Nilai laju metabolisme (Km) sebesar 0,1035 ± 0,0060 jam-1 menjadi 0,0960 ± 0,0197 jam-1; 0,0814 ± 0,0112 jam-1 dan 0,0696 ± 0,0183 jam-1 setelah pemberian ekstrak kencur 20 mg/kg bb, 40 mg/kg bb, 80 mg/kg bb dan nilai paruh (t1/2eliminasi)dengan nilai 6,18 ± 0,30 jam pada perlakuan tanpa ekstrak kencur menjadi 6,91 ± 1,26 jam; 7,86 ± 0,93 jam dan 9,14 ± 3,22 jam pada pemberian ekstrak kencur 20 mg/kg bb, 40 mg/kg bb, 80 mg/kg bb. Penurunan nilai laju metabolisme (Km), nilai laju eliminasi (Kel) dan peningkatan t1/2eliminasi menggambarkan kemampuan ekstrak kencur sebagai penghambat enzim pemetabolisme dalam hati.
THE INFLUENCE OF ADMINISTRATION
(Kaempferia galanga L)
EXTRACT ON THE PHARMACOKINETIC PROFILE OF SODIUM DICKLOFENAC
Abstract
The administrasion of sodium diklofenak to human previously consumed Kaempferia galanga L extract can lead to the possibility of pharmacokinetic interactions, especially in the metabolism of sodium diclofenac. The purpose of this study was to determine whether the Kaempferia galanga L extract affects the pharmacokinetics profile of sodium diclofenac.
The research was conducted using 20 male rats weighing of 150-200 gram, were divided into four groups, the first groups was given sodium diclofenac standard solution of 2.25 mg/kg body weight of extract. Groups 2. 3 and 4 were orally given kaemferia galanga L ekstract with doses 20 mg/kg body weight, 40 mg/kg body weight, 80 mg/kg body weight for 7 days. The next 4 hours each of the 3 groups was administrered standard solution of sodium diclofenac with doses of 2.25 mg/kg body weight. The urin drug levels for each rats is recorded in the interval of 6; 12; 18; 24; 30 hours. The measurement of the sodium diclofenac content in urin is measured by using ultra violet spectrophotometry.
The result obtained that elimination rate (Kel) values the treatment without extracts Kaempferia galanga L decreased from 0.1121 ± 0.0055 hour-1 to 0.1029 ± 0.0185 hour-1; 0.0891 ± 0.0109 hour-1 and 0.0821 ± 0.0232 hour-1 after the treatment of extracts Kaempferia galanga L. Metabolism rate (Km) value also showed decrease from 0.1035 ± 0.0060 hour-1 to 0.0960 ± 0.0197 hour-1; 0.0814 ± 0.0112 hour-1 and 0.0696 ± 0.0183 hour-1 after the treatment of extracts Kaempferia galanga L and the elimination half life value (t1/2elimination)the value 6.18 ± 0.30 hour for treatment without extracts Kaempferia galanga L and 6.91 ± 1.26 hour; 7.86 ± 0.93 hour and 9.14 ± 3.22 hour for the treatment of extracts Kaempferia galanga L. Decrease of metabolism rate (Km), elimination rate (Kel) and increase the elimination half life value (t1/2elimination), describe the ability of extracts Kaempferia galanga L as inhibitors of metabolic enzymes in the liver.
BAB I
PENDAHULUAN
1.1Latar Belakang
Farmakokinetika dapat didefenisikan sebagai setiap proses yang dilakukan
tubuh terhadap obat, yaitu absorpsi, distribusi, metabolisme dan ekskresi. Dalam arti sempit farmakokinetika khususnya mempelajari perubahan-perubahan
konsentrasi dari obat dan metabolitnya di dalam darah dan jaringan sebagai fungsi dari waktu (Tan, 2002).
Menurut Hussar (1995), interaksi farmakokinetika merupakan suatu
interaksi manakala senyawa pertama dapat mengubah absorpsi, distribusi, metabolisme/biotransformasi atau ekskresi (ADME) dari senyawa kedua dengan
konsekuensi terjadi perubahan konsentrasi senyawa kedua dalam plasma/darah. Oleh karena interaksi dapat membawa dampak terhadap perubahan kadar obat maka mengakibatkan perubahan efek obat tersebut. Sifat perubahan efek obat
tersebut dapat bersifat merugikan atau menguntungkan.
Natrium diklofenak merupakan derivate sederhana fenil asetat yang
termasuk NSAIDs yang terkuat anti radang nya, tetapi mempunyai efek samping pada pemakaian sediaan obat yang konvensional dalam jangka waktu lama dapat menyebabkan pendarahan pada saluran cerna (Insel, 1996). Obat ini banyak
Alam sudah menjadi sumber bahan berkhasiat selama ribuan tahun. Dalam beberapa tahun terakhir banyak kalangan akademisi serta
perusahaan-perusahan farmasi yang tertarik dengan produk alam, karena berpotensi sebagai sumber obat baru. Pada kurun waktu 1983-1994 telah ditemukan 520 obat baru yang legal, 39% dari penemuan tersebut merupakan produk alam serta
turunannya, dan 60-80% obat antibakteri dan antikanker berasal dari alam, sehingga pada saat ini penggunaan obat herbal menjadi lebih popular dalam
bentuk suplemen makanan, nutraceutical, obat tambahan dan obat pengganti (Sarker, et al., 2006).
Kencur merupakan tanaman obat yang bernilai ekonomis cukup tinggi
sehingga banyak dibudidayakan. Bagian rimpangnya digunakan sebagian bahan baku industri obat tradisional, bumbu dapur, bahan makanan, maupun minuman
penyegar lainnya (Rostiana, dkk., 2003).
Sulaiman, dkk., (2007), menyatakan bahwa rimpang kencur dapat digunakan untuk hipertensi, rematik, dan asma. Menurut Hasanah, dkk., (2011),
bahwa ekstrak rimpang kencur berkhasiat sebagai antiradang dimana semakin tinggi dosis ekstrak rimpang kencur yang diberikan maka semakin kecil
Oleh karena itu, perlu dilakukan penelitian untuk mengetahui sejauh mana pengaruh ekstrak rimpang kencur terhadap profil farmakokinetik natrium
diklofenak yang dilakukan pada tikus sebagai hewan uji menggunakan data urin.
1.2Perumusan masalah
Berdasarkan latar belakang diatas, maka perumusan masalah dalam
penelitian ini adalah apakah ada pengaruh pemberian ekstrak kencur terhadap perubahan parameter farmakokinetik natrium diklofenak menggunakan data urin
kumulatif.
1.3Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis penelitian ini
1.4Tujuan penelitian
Tujuan penelitian ini adalah untuk mengetahui pengaruh pemberian
ekstrak kencur selama 7 hari berturut-turut terhadap parameter farmakokinetik natrium diklofenak pada hewan uji tikus data urin kumulatif.
1.5Manfaat Penelitian
Hasil penelitian ini diharapkan dapat digunakan sebagai informasi terhadap penggunaan kombinasi ekstrak kencur dan natrium diklofenak apakah
1.6Kerangka Pikir Penelitian
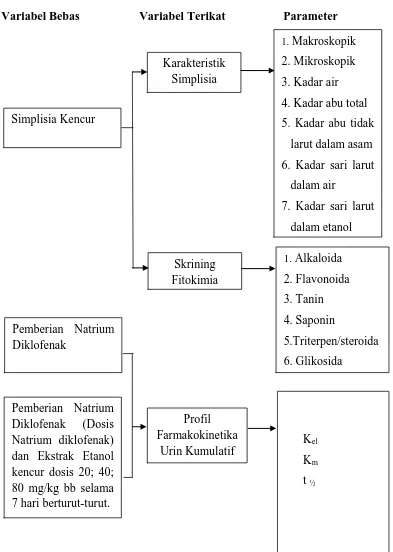
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Diagram Kerangka pikir penelitian
Simplisia Kencur Pemberian Natrium Diklofenak Karakteristik Simplisia Profil Farmakokinetika Urin Kumulatif
1. Makroskopik 2. Mikroskopik 3. Kadar air 4. Kadar abu total 5. Kadar abu tidak
larut dalam asam 6. Kadar sari larut
dalam air
7. Kadar sari larut dalam etanol
Skrining Fitokimia
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
2.1.1 Sistematika tumbuhan
Sistematika tumbuhan kencur adalah sebagai berikut (MEDA, 2013). Kingdom/kerajaan : Plantae (tumbuh-tumbuhan)
Divisi : Spermatophyta (tumbuhan berbunga) Kelas : Monocotyledoneae (biji berkeping tunggal)
Ordo : Zingiberales
Famili : Zingiberaceae
Genus : Kaempferia
Spesies : Kaempferia galangal L
2.1.2 Morfologi tumbuhan
Kencur merupakan tumbuhan dengan batang lunak tidak berkayu atau
hanya mengandung sedikit jaringan kayu. Ia tumbuh di daratan rendah sampai sedang, ia juga dapat tumbuh dengan baik pada musim penghujan. Tanaman
kencur cocok ditanam di tanah yang relatif gembur dan tidak terlalu banyak air, namun ia juga dapat ditanam pot atau di kebun yang cukup mendapat sinar. Kencur termasuk tanaman yang dapat hidup dimana pun pada tanah yang gembur
dan subur dengan sedikit naungan. Ia adalah salah satu jenis tanaman obat yang tergolong dalam suku temu-temuan (zingiberaceae) yang masih satu keluarga
Tanaman kencur memiliki batang semu yang sangat pendek. Batang tersebut terbentuk dari pelepah-pelepah daun yang saling menutupi.
Daun-daunnya tumbuh tunggal, melebar dan mendatar atau menurun mendekati permukaan tanah. Bentuk daun elip melebar lebar 3 - 6 cm, dan panjangnya 7 - 12 cm. Bunga tanaman kencur berwarna putih, bibir bunga bewarna ungu, dan
baunya wangi. Bunga-bunga ini tumbuh diantara helaian daun. Setiap tangkai bunga berjumlah 4 - 12 kuntum bunga. Buah kencur termasuk buah kotak beruang
3, dengan bakal buah yang letaknya tenggelam. Tapi buah kencur ini amat sulit menghasilkan biji. Akar kencur merupakan akar tinggal, yang bercabang halus dan menempel pada umbi akar, yang biasanya disebut rimpang. Rimpang ini
tumbuh memanjang kebawah, berdiamater sampai 1,5 cm, dan tidak berserat. Bila rimpang tersebut dipotong melintang, tampak bewarna putih dan pinggir nya
bewarna coklat kekuningan, aroma rimpang kencur sangat khas dan lembut (Santoso, 2013).
Kencur diduga berasal dari india lalu dibudayakan secara luas di asia
tenggara, cina selatan, dan australia utara. Nama kencur dipinjam dari bahasa sansakerta, kachora, yang berarti temu putih. Istilah kencur dalam bahasa inggris
sering disebut lesser galanggal (alphinia officinarum) maupun zedoary (temu putih) padahal kedua nya merupakan spesies yang berbeda dan bukan rempah pengganti. Nama-nama lainnya untuk kencur adalah cekur (malaysia) dan prohom
(thailand). Kencur sudah sangat dikenal masyarakat kemampuannya sebagai bumbu masakan dan membuat masakan lebih sedap. Kencur dikenal dengan nama
tekur, keciwer (karo), kopuk, cakuwe, cokur, atau kencur (sumatra). Tanaman kencur bisa juga dijadikan sebagai tanaman hias atau tumpang sari (Utami, 2013).
2.1.3 Kandungan Kimia
Kandungan senyawa kimia dalam kencur antara lain minyak atsiri yang tersusun atas etil ester asam sinamat, etil aster asam parametoksi sinamat, borneol,
campfen, p-metoksitiren, karen, n-pentadekan, dan golongan senyawa flavanoid (Utami, 2013).
Berdasarkan hasil riset di laboratorium tananam kencur mengandung lebih
dari 23 senyawa dan tujuh diantaranya mengandung senyawa monoterpena, senyawa aromatik, serta senyawa seskuiterpena. Komposisi kimianya adalah:
- Pati (4,14%) - Mineral (13,73%)
- Minyak atsiri (0,02% berupa sineol, asam metil kanil dan penta dekaan, asam cinamic, etil ester, kamphen, paraeumarin, asam anisic, alkaloid dan gom)
Ekstrak metanol dari tanaman kencur menunjukkan aktivitas melawan toxocaracanis (sejenis cacing parasit yang menyebabkan penyakit toxocariasis) dan efektif melawan 3 spesies yang menyebabkan granulomatous amoebic encephalitis (penyakit sistem syarat pusat) dan amoebic keratitis (bakteri yang menyebabkan infeksi dikornea mata). Ekstrak rimpang nya juga menghalangi aktivitas virus epstein-barr bahkan riset lebih lanjut menunjukkan bahwa ekstrak rimpang secara efektif dapat membunuh larva nyamuk culex dan aedes aegypti (Sina, 2012).
2.1.4 Khasiat tumbuhan
Sejak zaman dahulu kencur dijadikan sebagai obat untuk menyembuhkan
influenza, astma, reumatik, tetanus dan menghilangkan jerawat. Kencur termasuk tanaman obat yang tidak mengandung efek samping yang bahaya dibanding
obat-obatan kimia. Berikut ini ramuan-ramuan berbahan kencur yang patut dicoba untuk menyembuhkan berbagai penyakit (Sina, 2012).
- Kencur bersifat stimulan sehingga bisa digunakan sebagai penambah
tenaga.
- Kencur bersifat karminatif atau meluruhkan angin sehingga mampu
menghilangkan kembung diperut, ia bahkan mampu mengobati radang lambung, radang anak telingga, influenza pada anak bayi, masuk angin, sakit kepala, batuk, diare, menghilangkan darah kotor, memperlancar haid,
mata pegel, dan keseleo.
- Di indonesia, jamu beras kencur populer sebagai minuman penyegar.
2.2 Natrium Diklofenak
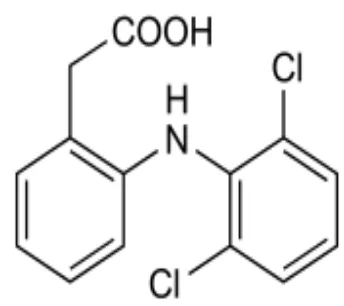
Rumus Struktur
Gambar 2.1 Rumus struktur Natrium diklofenak
Rumus molekul : C14H10Cl2NO2Na
Nama Kimia : (2- (2,6-diklorophenyl) amino benzeneacetic acid)
Berat Molekul : 318,13
Pemerian : Serbuk hablur, berwarna putih, tidak berasa (USP 30, 2007).
Kelarutan : Sedikit larut dalam air, larut dalam alkohol; praktis tidak larut dalam kloroform dan eter; bebas larut dalam alkohol
metil. pH larutan 1% b/v dalam air adalah antara 7.0 dan 8. Diklofenak merupakan derivat fenil asetat efek samping terjadi kira-kira 20% penderita dan meliputi distress saluran cerna, perdarahan saluran cerna sering
menyebabkan kerusakan gastrointestinal (dyspepsia, mual, dan gastritis). Efek samping yang paling serius adalah perdarahan gastrointestinal dan perforasi (Neal,
2.3 Farmakokinetika
Farmakokinetika dapat didefenisikan sebagai setiap proses yang dilakukan
tubuh terhadap obat, yaitu absorpsi, distribusi, metabolisme dan ekskresi. Dalam arti sempit farmakokinetika khususnya mempelajari perubahan-perubahan konsentrasi dari obat dan metabolitnya di dalam darah dan jaringan sebagai fungsi
dari waktu (Tan, 2002).
2.3.1 Absorpsi
Obat-obat yang diberikan peroral akan diabsorpsi bila molekul obat berada dalam bentuk terlarut. Molekul obat mula-mula berikatan dengan mukosa lambung atau usus, kemudian obat mencapai lapisan yang lebih dalam dari
membran sel tapi belum sampai ke pembuluh darah. Penyerapan obat dapat terjadi di lambung atau usus halus. Penyerapan obat dilambung tergantung pada keadaan
lambung yang penuh atau kosong. Saat saluran pencernaan berada dalam keadaan istirahat, spincter pylorus agak membuka dan obat yang diberikan peroral dapat melintas dengan mudah dan akan diserap di usus halus. Selanjutnya obat akan
menembus dinding pembuluh darah dan masuk kedalam sirkulasi darah (Aiache, 1993).
2.3.2 Distribusi
Setelah obat diserap dari dalam usus menuju ke aliran darah, obat akan diikat oleh protein darah dan akan dilepaskan sedikit demi sedikit ke plasma
dalam bentuk bebas menuju target kerja (target sel) (Tan, 2002).
Setelah molekul zat aktif masuk ke dalam peredaran darah, maka
penyebaran ini sangat peka terhadap berbagai pengaruh yang terkait dengan tahap penyerapan dan tahap yang terjadi sesudahnya yaitu peniadaan, serta terkait pula
dengan komposisi biokimia serta keadaan fisiopatologi subyeknya, disamping itu perlu diingat kemungkinan adanya interaksi dengan molekul lainnya (Aiache, 1993).
2.3.3 Metabolisme
Metabolisme obat terbesar adalah pada hati, juga terjadi di ginjal, jaringan
otot, dinding usus dan saluran darah. Obat yang mengalami metabolisme pada epitel saluran pencernaan dan hati sebelum mencapai sirkulasi sistemik dikenal dengan metabolisme lintas pertama. Obat-obat dapat mengalami metabolisme
sebagian sebelum diekskresi (Ritschel, 1980).
2.3.4 Ekskresi
Pengeluaran obat atau metabolitnya dari tubuh terutama dilakukan oleh ginjal melalui air seni disebut ekskresi. Lazimnya tiap obat diekskresi berupa metabolitnya dan hanya sebagian kecil dalam keadaan asli yang utuh. Tapi ada
pula beberapa cara lain yaitu melalui kulit bersama keringat, paru-paru melalui pernafasan dan melalui hati dengan empedu (Tan, 2002).
Obat dapat diekskresikan melalui berbagai rute (Aiache, 1993) yaitu:
a. Ginjal, organ utama untuk mengeliminasi obat dari tubuh melalui urine. b. Fases, khususnya untuk obat-obat yang sukar diabsorpsi dan tinggal dalam
saluran lambung-usus.
c. Empedu, bila reabsorpsi obat dari saluran lambung-usus kecil.
d. Paru-paru, tempat keluar obat-obat yang mudah menguap melalui ekspirasi
pernapasan.
2.4 Parameter Farmakokinetika Ekskresi Urin Kumulatif Obat
Dalam farmakokinetik, urin dapat digunakan sebagai salah satu objek
pemeriksaan selain plasma darah, untuk penentuan beberapa parameter farmakokinetik.Data eksresi obat lewat urin dapat dipakai untuk memperkirakan
bioavailabilitas. Agar dapat diperkirakan yang sahih, obat harus dieksresi dengan jumlah yang bermakna di dalam urin dan cuplikan urin harus dikumpulkan secara lengkap. Jumlah kumulatif obat yang dieksresi dalam urin secara langsung
berhubungan dengan jumlah total obat yang terabsorbsi (Shargel, 2005).
Jumlah obat total yang masih dapat ditemukan kembali dalam urin pada
waktu tak terhingga “Ae∞”, dapat ditentukan melalui jumlah urin yang dikumpulkan selama 7 sampai 10 kali waktu paruh. Penentuan parameter Farmakokinetika terhadap metabolit dan obat tak berubah yang dieliminasi
Jumlah obat yang diekskresikan tiap sampel urin yaitu “Aei”, ditentukan dengan
mengalikan nilai Cu dan V, sebagaimana terlihat pada persamaan 2. 1
Aei = Cu x V ... (2.1)
Jumlah kumulatif obat yang diekskresikan sampai dengan waktu tak terhingga “Ae∞”, ditentukan dengan menjumlahkan nilai Ae hasil penentuan dari persamaan
2.1, dapat dilihat pada persamaan 2.2
Ae∞= ∑∞�=1��� ... (2.2)
K
el=
��(��∞−��3)−��(��∞−��5)
�5−�3
... (2.3)
Laju ekskresi obat dari sampel yang diambil dilambangkan dengan “Ku“, dapat ditentukan yaitu dengan persamaan 2.4
�
�=
��∞�� ��
� ... (2.4)
Nilai konstanta laju metabolisme “ Km” dapat ditentukan yaitu dengan
persamaan 2.5
K
m= K
el+ K
uNilai fraksi obat yang dieliminasi “ Fel ” dapat ditentukan yaitu dengan persamaan
2.6
F
el = ��∞� ... (2.6)
Turunnya kadar plasma obat dan lama efeknya tergantung pada kecepatan metabolisme dan ekskresi. Kedua faktor ini menentukan kecepatan eliminasi obat yang dinyatakan dengan pengertian plasma half-life eliminasi (waktu paruh) yaitu
sampai separuhnya.. Obat dengan metabolisme cepat half life-nya juga pendek. Sebaliknya zat yang tidak mengalami biotransformasi atau yang resorpsi kembali
oleh tubuli ginjal, dengan sendirinya t1/2-nya panjang (Waldon, 2008).
Waktu paruh eliminasi “t1/2 eliminasi ” dapat ditentukan dengan persamaan 2.7
t1/2 eliminasi =
0,693
��� ... (2.7)
BAB III
METODELOGI PENELITIAN
Penelitian ini dilakukan terhadap rimpang kencur berdasarkan metode eksperimental dengan tahapan penelitian yaitu pengumpulan tumbuhan,
pengolahan simplisia, pembuatan pereaksi, pemeriksaan karakteristik simplisia, Pemeriksaan skrining fitokimia simplisia, pembuatan ekstrak, penyiapan hewan
percobaan, perlakuan pemberian obat terhadap hewan percobaan, pengambilan urin, urin yang diperoleh divorteks dan disentrifuge dan di ambil supernatan kemudian diukur dengan spektrofotometer ultraviolet.
3.1 Alat
Alat-alat yang digunakan adalah alat-alat gelas laboratorium, blender
(National), lemari pengering, perkolator, oven, cawan penguap, Rotary evaporator
(Heidolph VV-300), oral sonde, timbangan hewan (GW-1500), neraca analitik
(Mettler Toledo), tabung sentrifuge, rak tabung, alat vortex, alat
sentrifuge(Velocity 18R), spuit, labu tentukur, pipet tetes, spektrofotometer UV (shimadzu UV 1800), stamfer, mortir dan stopwatch.
3.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah natrium diklofenak (bahan baku obat, PT. Dexa Medica), ekstrak kencur, etanol 96%,
3.3 Penyiapan Sampel
3.3.1 Pengambilan Tumbuhan
Pengambilan tumbuhan yang digunakan dalam penelitian ini adalah rimpang kencur yang masih segar yang diperoleh dari pasar pagi Tanjung Sari, Medan, Provinsi Sumatera Utara.
3.3.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di “Laboratorium Herbarium”
Laboratorium Penelitian Biologi Fakultas MIPA Universitas Sumatera Utara, Medan.
3.3.3 Pengolahan Sampel
Rimpang kencur yang masih segar dibersihkan dari kotoran atau bahan asing lainnya kemudian dicuci dengan air bersih lalu ditiriskan dan ditimbang
sebagai berat basah. Lalu dirajang kecil-kecil dan dikeringkan pada temperatur ruangan hingga kering ditandai dengan rimpang mudah dipatahkan dan ditimbang sebagai berat kering. Irisan rimpang kencur kering diblender hingga menjadi
serbuk dan ditimbang sebagai berat serbuk simplisia. Lalu disimpan dalam wadah plastik, diberi etiket dan disimpan ditempat kering.
3.4 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam air, penetapan
3.4.1 Pemeriksaan Makroskopik dan Organoleptik
Pemeriksaan makroskopik dan organolepik dilakukan dengan mengamati
bentuk, bau dan rasa dari rimpang kencur segar dan serbuk simplisia rimpang kencur.
3.4.2 Pemeriksaan Mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia rimpang kencur. Serbuk simplisia rimpang kencur diletakkan di atas kaca objek yang telah
ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup, selanjutnya diamati di bawah mikroskop.
3.4.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluena). Alat terdiri dari labu alas bulat 500 ml, pendingin, tabung penyambung,
tabung penerima 10 ml, alat penampung dan pemanas listrik. Cara kerja:
Dimasukkan 200 ml toluena dan 2 ml air suling ke dalam labu alas bulat, lalu
didestilasi selama 2 jam. Setelah itu, toluena dibiarkan mendingin selama 30 menit, dan dibaca volume air pada tabung penerima dengan ketelitian 0,05 ml.
Kemudian ke dalam labu tersebut dimasukkan 5 g serbuk simplisia yang telah ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluena mendidih, kecepatan tetesan diatur lebih kurang 2 tetes tiap detik sampai sebagian
besar air terdestilasi, kemudian kecepatan tetesan dinaikkan hingga 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan
sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang
diperiksa. Kadar air dihitung dalam persen (WHO, 1992; Ditjen POM, 1995).
3.4.4 Penetapan Kadar Sari Larut dalam Air
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml
air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan
selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah ditara dan sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang
larut dalam air dihitung terhadap bahan yang telah dikeringkan (WHO, 1992; Ditjen POM, 1995).
3.4.5 Penetapan Kadar Sari Larut dalam Etanol
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama,
kemudian dibiarkan selama 18 jam. Kemudian disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan
penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam etanol 96% dihitung terhadap bahan yang telah dikeringkan (WHO, 1992; Ditjen
3.4.6 Penetapan Kadar Abu Total
Sebanyak 2 g serbuk simplisia dimasukkan dalam krus porselin yang telah
dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, jika arang masih tidak dapat dihilangkan, ditambahkan air panas, saring melalui kertas saring bebas abu. Pijarkan sisa dan kertas saring dalam krus yang
sama. Masukkan filtrat ke dalam krus, uapkan, pijarkan hingga bobot tetap, timbang. Kadar abu dihitung terhadap bahan yang telah dikeringkan (WHO, 1992;
Ditjen POM, 1995).
3.4.7 Penetapan Kadar Abu Tidak Larut dalam Asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml
asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu, cuci dengan air panas,
dipijarkan, kemudian didinginkan dan ditimbang sampai bobot tetap. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan (WHO, 1992; Ditjen POM, 1995).
3.5 Skrining Fitokimia
Skrining fitokimia serbuk simplisia meliputi pemeriksaan senyawa
golongan flavonoid, alkaloid, saponin, tanin, glikosida dan steroid/triterpenoid.
3.5.1 Pemeriksaan Flavanoid
Sebanyak 10 g simplisia ditambahkan 10 ml air panas, dididihkan selama
5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok
3.5.2 Pemeriksaan Alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml
asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk tes alkaloid. Diambil 3 tabung reaksi, lalu ke dalamnya dimasukkan 0,5 ml filtrat. Pada
masing-masing tabung reaksi
a. Ditambahkan 2 tetes pereaksi Mayer b. Ditambahkan 2 tetes pereaksi Bouchardat c. Ditambahkan 2 tetes pereaksi Dragendorff
Alkaloid positif jika terjadi endapan atau kekeruhan pada dua dari tiga percobaan
diatas (Ditjen POM, 1995).
3.5.3 Pemeriksaan Saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukkan ke dalam tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan, kemudian dikocok kuat-kuat selama 10 menit. Jika terbentuk busa setinggi 1 - 10 cm yang stabil
tidak kurang dari 10 menit dan buih tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Ditjen POM, 1995).
3.5.4 Pemeriksaan Tanin
Simplisia ditimbang sebanyak 1 g, dididihkan selama 30 menit dalam 100 ml air suling lalu didinginkan dan disaring. Pada filtrat ditambahkan 1 – 2 tetes
3.5.5 Pemeriksaan Glikosida
Serbuk simplisia ditimbang sebanyak 3 g, lalu disari dengan 30 ml
campuran etanol 96%-air (7:3) dan 10 ml asam klorida 2 N, direfluks selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat, ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5 menit, lalu
disaring. Filtrat disari dengan 20 ml campuran kloroform-isopropanol (3:2) sebanyak 3 kali. Pada kumpulan sari lapisan isopropanol diuapkan pada suhu
tidak lebih dari 50oC. Sisanya dilarutkan dengan 2 ml metanol untuk larutan percobaan. 0,1 ml larutan percobaan diuapkan di atas penangas air, pada sisa ditambahkan 2 ml air dan 5 tetes Molish, kemudian ditambahkan hati-hati 2 ml
asam sulfat, terbentuk cincin berwarna ungu pada batas cairan, menunjukkan adanya ikatan gula (Ditjen POM, 1995).
3.5.6 Pemeriksaan Steroid/Triterpenoid
Serbuk simplisia ditimbang sebanyak 1 g, dimaserasi dengan 20 ml nheksan selama 2 jam, disaring. Filtrat diuapkan dalam cawan penguap dan pada
sisanya ditambahkan pereaksi Liebermann-Burchard melalui dinding cawan. Apabila terbentuk warna ungu atau merah yang berubah menjadi biru ungu atau
3.6 Pembuatan Ekstrak Etanol Rimpang Kencur (EERK)
Pembuatan ekstrak etanol rimpang kencur dilakukan dengan metode
perkolasi. Caranya 350 gram serbuk simplisia direndam dengan etanol 96% selama 3 jam. Selanjutnya dipindahkan. Massa dipindahkan sedikit demi sedikit ke dalam perkolator, tambahkan etanol 96% secukupnya hingga simplisia
terendam dan terdapat cairan penyari di atasnya, perkolator ditutup dengan aluminium foil dan dibiarkan selama 24 jam. Kemudian kran perkolator dibuka
dan dibiarkan cairan ekstrak menetes dengan kecepatan 20 tetes per menit dan ditambahkan etanol 96% berulang-ulang secukupnya dan diatur kecepatan penetesan cairan penyari sama dengan kecepatan tetesan perkolat, sehingga selalu
terdapat selapis cairan penyari di atas simplisia. Perkolasi dihentikan perkolat yang keluar terakhir diuapkan dan tidak meninggalkan sisa. Perkolat yang
diperoleh dipekatkan dengan alat rotary evaporator. Kemudian dikeringkan dengan freeze dryer selama lebih kurang 24 jam (Depkes RI, 1974).
3.7. Pembuatan Diklofenak Baku
3.7.1 Pembuatan Larutan Induk Baku I Natrium Diklofenak
Timbang seksama sejumlah 50 mg natrium diklofenak baku, dimasukan ke
3.7.2 Pembuatan Larutan Induk Baku II Natrium Diklofenak
Pipet dari LIB I sebanyak 10 ml, dimasukan ke dalam labu tentukur 50 ml,
dicukupkan dengan NaOH 0,1 N hingga garis tanda. Dikocok sampai homogen sehingga diperoleh larutan dengan konsentrasi 100 mcg/ml.
3.7.3 Pengukuran panjang gelombang absorpsi maksimum didalam larutan
NaOH 0,1 N
Larutan natrium diklofenak dibuat dengan konsentrasi 13 mcg/mL dengan
memipet 6,5 ml dari LIB II dimasukan ke dalam labu tentukur 50 ml, lalu di tambahkan larutan NaOH 0,1 N. Serapan larutan tersebut diukur pada panjang gelombang 200 - 400 nm dengan alat spektrofotometer ultraviolet.
3.7.4 Pembuatan Kurva Baku Natrium diklofenak pada panjang gelombang
maksimum
Pembuatan kurva baku natrium diklofenak pada panjang gelombang maksimum dilakukan dengan cara:
Dipipet larutan dari LIB II berturut-turut 0,4 ml; 0,6 ml; 0,8 ml; 1,2 ml; 1,4 ml;
1,6 ml dan1,8 ml larutan kemudian dimasukan ke dalam labu takar 10 ml dan di adkan hingga 10 ml dengan larutan NaOH 0,1 N. Diperoleh larutan dengan
3.8 Pembuatan Suspensi dan larutan
3.8.1 Pembuatan Suspensi CMC 1%
Sebanyak 1 gram CMC yang telah ditimbang seksama ditaburkan dalam lumpang yang berisi 20 ml akuades panas. Didiamkan selama 15 menit hingga diperoleh massa yang transparan, lalu digerus sampai homogen, diencerkan
dengan aquadest dan dimasukkan ke dalam labu tentukur 100 ml, kemudian dicukupkan volumenya dengan akuadest hingga 100 ml.
3.8.2 Pembuatan Suspensi Natrium diklofenak 0,05%
Sebanyak 50 mg natrium diklofenak baku, digerus di dalam lumpang. Kemudian ditambahkan CMC 1 % digerus sampai homogen. Dituang kedalam
labu tentukur 100 ml, ditambah CMC 1 % sampai batas tanda, kocok hingga homogen.
3.8.3 Penyiapan suspensi ekstrak etanol rimpang kencur 1%
Sebanyak 250 mg ekstrak etanol rimpang kencur, dimasukkan ke dalam lumpang, digerus. Ditambahkan sedikit suspensi CMC 1% kemudian
3.9 Perlakuan Terhadap Hewan Percobaan
3.9.1 Perlakuan Pada Hewan Percobaan dengan Pemberian Natrium Diklofenak tanpa Ekstrak Etanol Rimpang Kencur (EERK).
Perlakuan Pada Hewan Percobaan dengan Pemberian Natrium Diklofenak
tanpa EERK adalah sebagai berikut:
1. Hewan percobaan (tikus) diadaptasikan selama 2 minggu.
2. Kemudian hewan percobaan diberikan larutan Natrium Diklofenak dengan
dosis yang telah dikonversikan (dosis manusia ke dosis tikus) terhadap dosis lazim 25 mg.
3. Masing-masing hewan percobaan diambil urinnya dengan interval waktu 6; 12; 18; 24 dan 30 jam.
4. Setiap waktu pengambilan cuplikan, volume urin yang diekskresikan dicatat
dan disimpan dalam vial.
5. jika urin tidak segera dianalisis, disimpan dalam lemari es sampai analisis
dikerjakan, urin dapat ditambahkan toluen (toluen mencegah oksidasi urin). 6. Dipipet 0,5 ml urin yang telah ditampung dalam vial, lalu dimasukkan dalam
tabung sentrifuge yang telah berisi 1 ml TCA 20%, lalu divorteks dan
3.9.2 Perlakuan Pada Hewan Percobaan dengan Pemberian Natrium Diklofenak dengan Pemberian EERK selama 7 Hari Berturut-turut
Perlakuan Pada Hewan Percobaan dengan Pemberian Natrium Diklofenak dengan Pemberian EERK selama 7 Hari Berturut-turut adalah sebagai berikut:
1. Pada kelompok perlakuan masing-masing hewan diberi ekstrak rimpang kencur dengan dosis 20 mg/kg bb, 40 mg/kg bb, 80 mg/kg bb selama 7 hari berturut-turut.
2. Kemudian hewan uji diatas pada hari ke-7 setelah 4 jam pemberian ekstrak rimpang kencur diberi larutan obat natrium diklofenak dengan dosis yang telah
dikonversikan (dosis manusia ke dosis tikus) terhadap dosis lazim 25 mg. 3. Masing-masing hewan uji diambil urinnya dengan interval waktu 6; 12; 18; 24
dan 30 jam.
4. Setiap waktu pengambilan cuplikan, volume urin yang diekskresikan dicatat dan disimpan dalam vial.
5. jika urin tidak segera dianalisis, disimpan dalam lemari es sampai analisis dikerjakan, urin dapat ditambahkan toluene (toluen mencegah oksidasi urin). 6. Dipipet 0,5 ml urin yang telah ditampung dalam vial, lalu dimasukkan dalam
tabung sentrifuge yang telah berisi 1 ml TCA 20%, lalu divorteks dan disentrifuge pada 3000 rpm selama 10 menit, ambil supernatant kemudian
3.10 Analisis data
Data hasil penelitian ini dianalisis secara statistik menggunakan metode
BAB IV
HASIL DAN PEMBAHASAN
4.1 Simplisia dan Ekstrak
Berdasarkan identifikasi yang dilakukan di “Laboratorium Herbarium” Laboratorium Penelitian Biologi Fakultas MIPA Universitas Sumatera Utara,
Medan identitas sampel tumbuhan yang diteliti adalah Kaempferia galanga, L Suku Zingiberaceae yang dikenal masyarakat dengan nama Kencur. Hasil
identifikasi tumbuhan dapat dilihat pada Lampiran 1.
Hasil pemeriksaan makroskopik simplisia rimpang kencur yaitu, bentuk pipih, bagian luar berwarna coklat kemerahan, bagian dalam berwarna putih
kekuningan sampai kecoklatan, bagian tepi berombak dan berkeriput. Hasil pemerikasaan mikroskopik terhadap serbuk simplisia tumbuhan rimpang kencur
mempunyai warna putih kecoklatan sampai coklat dimana terdapat parenkim, parenkim yang berisi sel minyak, pembuluh kayu dengan penebalan spiral, terdapat periderm, periderm dengan parenkim, serta pembuluh kayu dengan
1.
2. 3. 4.
4
[image:46.595.111.456.126.392.2]5.
Gambar 4.1 Hasil Pemeriksaan Mikroskopik Serbuk Rimpang Kencur. Keterangan:
1. Parenkim
2. Pembuluh kayu dengan penebalan spiral 3. Parenkim dengan sel minyak
Tabel 4.1 Hasil pemeriksaan karakteristik simplisia rimpang kencur
No. Parameter Hasil
(%)
Persyaratan MMI (%)
1. Kadar air 5,99 10
2. Kadar sari yang larut dalam air 15,8 >14
3. Kadar sari yang larut dalam
etanol 7,03 >4
4. Kadar abu total 6,98 < 8
5. Kadar abu tidak larut dalam asam 1,36 < 2,2
4.2 Skrining Fitokimia
Tujuan dilakukannya skrining fitokimia adalah untuk mengetahui senyawa
[image:47.595.112.516.474.576.2]metabolit sekunder yang terdapat dalam simplisia (Harborne, 1996). Hasil skrining fitokimia dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil Skrining Fitokimia Simplisia Rimpang Kencur
No Skrining Hasil
1. 2. 3. 4. 5. 6. Alkaloid Flavonoid Glikosida Saponin Tanin Tripenoid/steroid - + + - - +
Rimpang kencur yang digunakan pada penelitian ini sebanyak 8 kg, yang
selanjutnya dikeringkan dalam lemari pengering dengan temperatur ± 40oC
Hasil penyarian 350 g serbuk simplisia rimpang dengan pelarut etanol 96% diperoleh ekstrak kental yang kemudian diuapkan dengan menggunakan
rotary evaporator dan kemudian dikeringkan dengan menggunakan freeze dryer
diperoleh 56,87 g ekstrak (rendemen 16,24%).
4.3 Analisis Parameter Farmakokinetik
Penentuan kadar natrium diklofenak dilakukan dengan menggunakan urin tikus. Hasil pengukuran kadar untuk perlakuan pemberian natrium diklofenak
[image:48.595.111.514.360.577.2]tanpa EERK dan perlakuan pemberian natrium diklofenak dengan EERK dosis 20, 40, 80 mg/kg bb selama 7 hari berturut-turut.
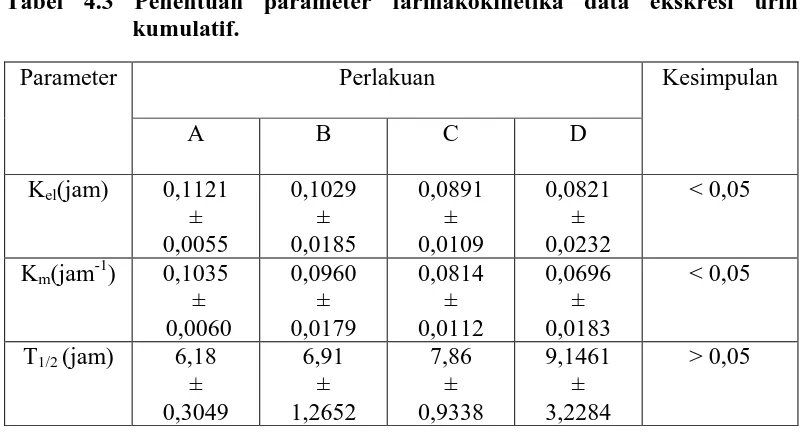
Tabel 4.3 Penentuan parameter farmakokinetika data ekskresi urin kumulatif.
Parameter Perlakuan Kesimpulan
A B C D
Kel(jam) 0,1121 ± 0,0055 0,1029 ± 0,0185 0,0891 ± 0,0109 0,0821 ± 0,0232 < 0,05
Km(jam-1) 0,1035 ± 0,0060 0,0960 ± 0,0179 0,0814 ± 0,0112 0,0696 ± 0,0183 < 0,05
T1/2 (jam) 6,18 ± 0,3049 6,91 ± 1,2652 7,86 ± 0,9338 9,1461 ± 3,2284 > 0,05 Keterangan:
A : Tanpa pemberian ekstrak rimpang kencur
B : Dengan pemberian ekstrak rimpang kencur 20 mg/kg bb C : Dengan pemberian ekstrak rimpang kencur 40 mg/kg bb D : Dengan pemberian ekstrak rimpang kencur 80 mg/kg bb (*) = Kesimpulan hasil uji statistika, beda antara empat rata-rata
Dari tabel 4.3 dapat dilihat penurunan nilai laju eliminasi Natrium diklofenak (Kel) pada perlakuan tanpa pemberian EERK yaitu 0,1121 ± 0,0055
dan untuk perlakuan dengan pemberian EERK 20; 40; 80 mg/kg bb selama 7 hari berturut-turut yaitu nilai 0,1029 ± 0,0185; 0,0891 ± 0,0109 dan 0,0821 ± 0,0232. Penurunan nilai Kel ini cukup bermakna (p < 0,05), dengan menurunnya nilai Kel
menunjukkan bahwa kecepatan eliminasi natrium diklofenak menurun sesuai dengan peningkatan dosis. Dengan kata lain EERK memperpanjang masa kerja
[image:49.595.110.498.343.499.2]natrium diklofenak sehingga proses peniadaannya dalam tubuh juga berlangsung lama.
Gambar 4.2 Penurunan nilai Kel (jam-1) terhadap rata-rata tiap perlakuan
Penurunan nilai laju eliminasi Natrium diklofenak (Kel) juga diikuti dengan penurunan laju metabolisme Natrium diklofenak (Km) yaitu untuk perlakuan tanpa pemberian EERK 0,1035 ± 0,0060 dan untuk perlakuan dengan
pemberian EERK 20; 40; 80 mg/kg bb selama 7 hari berturut-turut yaitu 0,0960 ± 0,0197; 0,0814 ± 0,0112 dan 0,0696 ± 0,0183. Penurunan nilai Km ini cukup
bermakna (p < 0,05). 0
0.02 0.04 0.06 0.08 0.1 0.12
K
el(j
a
m
-1
)
Perlakuan
Tanpa EERK
Dengan EERK 20 mg/kgbb
Dengan EERK 40 mg/kgbb
Gambar 4.3 Penurunan nilai Km (jam-1) terhadap rata-rata tiap perlakuan
Penurunan nilai laju eliminasi Natrium diklofenak (Kel), diikuti dengan
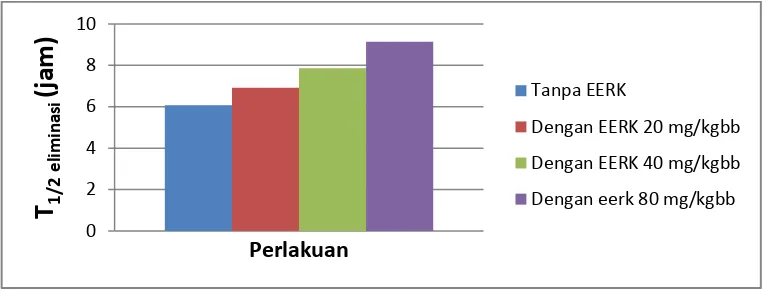
peningkatan Untuk waktu paruh tanpa pemberian EERK 6,18 ± 0,30 dan untuk perlakuan dengan pemberian EERK 20; 40; 80 mg/kgbb selama 7 hari
berturut-turut yaitu 6,91 ± 1,26; 7,86 ± 0,93 dan 9,14 ± 3,22.
Gambar 4.4 Peningkatan nilai T1/2eliminasi (jam) terhadap rata-rata tiap
perlakuan
Penurunan nilai laju metabolism (Km), laju eliminasi (Kel) dan peningkatan nilai waktu paruh (T1/2eliminasi) menggambarkan tentang penghambatan enzim
pemetabolisme yang terjadi di hati. Penurunan yang cukup nyata terlihat pada 0 0.02 0.04 0.06 0.08 0.1 0.12
K
m(j
a
m
-1)
Perlakuan Tanpa EERKDengan EERK 20 mg/kgbb
Dengan EERK 40 mg/kgbb
Dengan EERK 80 mg/kgbb
0 2 4 6 8 10
T
1/2e li m in a si
(j
a
m
)
Perlakuan Tanpa EERKDengan EERK 20 mg/kgbb
Dengan EERK 40 mg/kgbb
[image:50.595.113.500.439.589.2]penurunan nilai laju metabolisme (Km) perlakuan tanpa pemberian EERK 0,1035 ± 0,0060 dan untuk perlakuan dengan pemberian EERK 20; 40; 80 mg/kg bb
selama 7 hari berturut-turut yaitu 0,0960 ± 0,0197; 0,0814 ± 0,0112 dan 0,0696 ± 0,0183. Penurunan nilai Km ini cukup bermakna (p < 0,05). menurunnya nilai (Km) menunjukkan kemampuan memetabolisme nya menurun, hal ini
menggambarkan tentang penghambatan enzim pemetabolisme dihati, sehingga obat bebas akan berada lebih lama di dalam tubuh dan dalam jumlah yang tinggi
(Shargel, 1988). Untuk nilai laju eliminasi natrium diklofenak (Kel) juga mengalami penurunan yaitu pada pada perlakuan tanpa pemberian EERK yaitu 0,1121 ± 0,0055 dan untuk perlakuan dengan pemberian EERK 20; 40; 80 mg/kg
bb selama 7 hari berturut-turut yaitu nilai 0,1029 ± 0,0185; 0,0891 ± 0,0109 dan 0,0821 ± 0,0232. Penurunan nilai Kel ini cukup bermakna (p < 0,05). Dengan
penurunan nilai laju eliminasi (Kel) tentunya nilai waktu paruh (T1/2eliminasi) mengalami peningkatan yaitu dengan tanpa pemberian EERK 6,18 ± 0,30 dan untuk perlakuan dengan pemberian EERK 20; 40; 80 mg/kgbb selama 7 hari
berturut-turut yaitu 6,91 ± 1,26; 7,86 ± 0,93 dan 9,14 ± 3,22. Dengan meningkat nilai waktu paruh (T1/2eliminasi) maka obat dalam tubuh bertahan lama sehingga
jumlah obat dalam tubuh makin banyak.
Penelitian lain menunjukkan bahwa flavonoid terbukti dapat menghambat metabolisme obat lain (Dayong, et al., 2008). Flavonoid berperan dalam
penghambat enzyme CYP 450 dimana enzyme CYP 450 adalah salah satu enzyme pemetabolisme utama yang mempengaruhi penghambatan obat (Jiawang, et al.,
terkandung dalam ekstrak rimpang kencur yang dapat membuat laju metabolisme menjadi menurun. Senyawa CYP 450 memberikan kontribusi paling luas untuk
biotranformasi menjadi metabolit yang lebih polar dan mudah untuk dieksresikan (Jiawang, et al., 2013).
Secara teoritis hasil dari penelitian parameter farmokinetika dengan
menggunakan data urin harus sesuai dengan data darah, karena pada akhirnya obat yang berada di dalam darah akan terkumpul ke dalam ginjal dan obat serta
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Pemberian ekstrak rimpang kencur dapat mempengaruhi parameter farmakokinetika natrium diklofenak yang ditandai dengan penurunan nilai
Km dan Kel secara bermakna (p < 0,05), dan peningkatan nilai T1/2eliminasi. Penurunan nilai Km, Kel dan peningkatan nilai T1/2eliminasi menunjukkan
kemampuan ekstrak kencur sebagai penghambat enzim pemetabolisme di hati.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk menguji profil farmakokinetika data urin menggunakan alat yang lebih canggih seperti
DAFTAR PUSTAKA
Aiache, M. (1993), Farmasetika 2 Biofarmasi. Edisi Kedua. Surabaya: Airlangga University Press. Hal 7-11, 39.
Dayong, S., Ying, W., Yi-Han, Z., Yingjie, G., Juan, W., Hu,i Z., Ze-Sheng, L., and paul, F., (2008). Mechanism OF CYP2C9 Inhibition by Flavonoid. New Zealand; Changchun, China; Institute by Theoretical Chemistry, Jilin University, ang school of Pharmacy, University of Otago.
Ditjen POM. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan Republik Indonesia. Hal. 300-304, 306.
Ditjen POM. (1979). Farmakope Indonesia. Edisi ke III. Jakarta: Departemen Kesehatan Republik Indonesia. Hal. 512.
Fansworth, N.R. (1966). Biological and Phytochemical Screenning of Plants. Journal of Pharmaceutical Science. 55(3): 257.
Goodman, L.S., dan Gilman, A. (2012). Dasar Farmakologi Terapi. Penerjemah: Widjajakusumah, Dewi Irawati, Minarma Siagian, Dangsina Moeloek, dan Brahm U, Edisi XXVII, Jakarta: Penerbit ECGC. Hal. 485.
Gunawan, G.S. (2009). Farmakologi dan Terapi. Edisi ke V. Jakarta: Balai Penerbit FKUI. Hal. 232.
Hakim, L. (2002). Farmakokinetik. Yogyakarta: Bursa Ilmu. Hal. 21-22.
Hussar, D.A. (1995). Drug Interactions. Pennsylvania: Mack Publishing Company Easton. Hal. 1822-1836.
Insel, P.A. (1996). Analgesic-Antipiretic and Antiinflammatory Agen and of Drugs Employed In The Treatment of Gout. Dalam: Goodman and Gilman’s The Pharmalogical Basis of Therapeutics. Edisi ke IX. Diedit Oleh: BerryMolinoff dan Raymond Ruddon. New York: Mc Graw-Hill Company. Hal. 617-635.
Katzung, B. (2010). Farmakologi Dasar dan Klinik. Edisi ke VIII. Penerjemah: Bagian Farmakologi FKUI. Jakarta: Penerbit Salemba Medika. Hal. 36.
Lazuardi, M. (2010). Biofarmasetik dan Farmakokinetik Klinik Medis Veteriner. Cetakan I. Bogor: Ghalia Indonesia. Hal. 16-17.
Mutscler, E. (1985). Dinamika Obat. Edisi kelima. Penerjemah: Mathilda Widianto. Bandung: Penerbit ITB. Hal. 82-89.
Neal, M.J. (2006). Farmakologi Medis. Edisi Kelima, Jakarta : Penerbit Erlangga. Hal. 70-71.
Ritschel, W.A (2004). Handbook of Basic Pharmacokinetic. Edisi kedua. Hamilton: Drug Intelligence Publication. Inc : Hal. 125-241.
Sandhar, K.K. (2011). A Review of pytochemistry and pharmacology of Flavanoids. Phagwara Punjab India: University Jalandhar Deli G-T Road. Hal. 28-30.
Santoso, H. (2013). Tumpas Penyakit Dengan 40 Daun dan 10 Akar Rimpang. Yogyakarta: Cahaya Jiwa. Hal. 265-267.
Sarker, S.D., Latif, Z., dan Gray, A.I, (2006). Natural Products Isolation. Edisi 2, New Jersey: Humana Press lnc. Hal. 5.
Shargel, L., dan Yu, A.B. (2005). Biofarmasetika dan Farmakokinetika Terapan. Edisi Kedua. Surabaya: Airlangga University Press. Hal. 63.
Sina, M. (2013). Khasiat Super Minuman Alami Tradisional “BERAS KENCUR DAN KUNYIT ASAM” Menyehatkan dan Menyegarkan Tubuh tanpa Efek Samping. Yogyakarta: Diandra Pustaka Indonesia. Hal. 2-7.
Tan, H.T., dan Raharja, K. (2002). Obat-Obat Penting. Edisi ke V. Jakarta: PT. Alex Media Komputindo. Hal. 295, 313.
Tobyn, G., Denham, A., dan Whitelegg, M. (2011). The Western Herbal Tradition. Chicago: Elsevier Ltd. Hal 36.
USP Pharmacopiea. (2007). The National Formulary. Edisi 30. The United States Pharmacopeial Convention. Hal. 541, 1765-1766.
Utami, P. (2013). Diet Aman dan Sehat Berkat Herbal. Jakarta: Fmedia. Hal. 72-73.
Lampiran 2. Sertifikat Pengujian Natrium Diklofenak
Lampiran 3. Gambar Hasil Makroskopik
a. Rimpang kencur segar
Simplisia Rimpang Kencur
Lampiran 4. Perhitungan Hasil Penetapan Kadar Air Serbuk Simplisia Rimpang Kencur
Persen kadar air = Volume air (ml) Berat sampel (g)
x 100%
- Berat sampel I = 5,010 g
Volume penjenuhan toluen = 2,0 ml
Volume air I = 2,3 ml
Persen kadar air I = 2,3 – 2,0 5,011
x 100% = 5,9868%
- Berat sampel II = 5,004 g Volume air I = 2,3 ml
Volume air II = 2,6 ml Persen kadar air II = 2,6 – 2,3
5,007
x 100% = 5,9916%
- Berat sampel III = 5,007 g
Volume air II = 2,6 ml Volume air III = 2,9 ml Persen kadar air III = 2,9 – 2,6
5,005
x 100% = 5,9940%
Persen rata-rata kadar air serbuk simplisia =
3
Lampiran 5. Perhitungan Hasil Penetapan Kadar Sari Larut dalam Air Serbuk Simplisia Rimpang Kencur
Berat Cawan Berat Cawan + Sari Berat Sampel
K1 = 26,592 26,751 5,014
K2 = 45,100 45,260 5,003
K3 = 43,067 43,227 5,007
Persen kadar sari larut air = berat sari (g) x 100 berat sampel(g) 20
x 100%
1.Persen kadar sari larut dalam air I = 26,751 – 26,592 x 100 5,014 20
x 100%
= 15,8 %
2.Persen kadar sari larut dalam air II = 45,260 – 45,100 x 100 5,003 20
x 100%
=15,9 %
3.Persen kadar sari larut dalam air III = 43,227 – 43,067 x 100
5,007 20 x 100%
= 15,9 %
Persen rata-rata kadar sari larut air = 1
3
Lampiran 6. Perhitungan Hasil Penetapan Kadar Sari Larut dalam Etanol Serbuk Simplisia Rimpang Kencur
Beratcawan (g) Beratcawan + sari (g) Beratsampel (g)
K1 = 47,819 47,889 5,011
K2 = 43,241 43,313 5,005
K3 = 45,137 43,209 5,004
Persen kadar sari larut etanol = berat sari (g) x 100 berat sampel(g) 20
x 100%
1.Persen kadar sari larut dalam etanol = 47,889 – 47,819 x 100 5,011 20
x 100%
= 6,9%
2.Persen kadar sari larut dalam etanol= 43,313 -43,241 x 100
5,00520 20 x 100%
= 7,1%
3.Persen kadar sari larut dalam etanol= 43,209 – 43,137 x 100 5,00420 20
x 100%
= 7,1%
Persen rata-rata kadar sari larut etanol =
3
6,9 % + 7,1 % + 7,11 %
Lampiran 7. Perhitungan Hasil Penetapan Kadar Abu Total Serbuk Simplisia Rimpang Kencur
Persen kadar abu total = berat abu (g) berat sampel(g)
x 100%
I. a.berat kurs porselin setelah dipijar 1 = 27,511 g b.berat kurs porselin setelah dipijar 2 = 24,505 g c.berat kurs porselin setelah dipijar 3 = 27,515 g
II. a.berat sampel1 = 2,005 g b.berat sampel2 = 2,003 g c.berat sampel3 = 2,001 g
III.a.berat kurs porselin + sampel 1 setelah dipijar 1 = 27,653
b.berat kurs porselin + sampel 2 setelah dipijar 2 = 24,644 c.berat kurs porselin + sampel 3 setelah dipijar 3 = 27,661
- berat simplisia = 2,005 g
berat abu = 0,142 g
persen kadar abu total I = 0,142 2,005
x 100%
- berat simplisia = 2,003 g berat abu = 0,139 g
persen kadar abu total II = 0,139 2,003
x 100%
= 6,939 %
- berat simplisia = 2,001 g berat sampel = 0,139 g
persen kadar abu total III = 0,139 2,001
x 100%
= 6,946 %
Persen rata-rata kadar abu total =
3
7,082 % + 6,939 % + 6,946 %
Lampiran 8. Perhitungan Hasil Penetapan Kadar Abu Tidak Larut Asam
Serbuk Simplisia Rimpang Kencur
Persen kadar abu tidak larut asam = berat sari (g) berat sampel(g)
x 100%
1. a.berat kurs porselin setelah dipijar I = 27,511 g
b.berat kurs porselin setelah dipijar II = 24,505 g c.berat kurs porselin setelah dipijar III = 27,515 g
2. a.berat sampel I = 2,005 g
b.berat sampel II = 2,003 g c.berat sampel III = 2,001 g
3. a.berat kurs porselen + sampel setelah dipijar I = 27,540 g
b.berat kurs porselin + sampel setelah dipijar II = 24,532 g c.berat kurs porselin + sampel setelah dipijar III = 27,541 g
- berat abu I = 0,029 g
berat sampel = 2,005 g
persen kadar abu tidak larut asam I = 0,029 2,005
x 100%
= 1.446 % - berat abu II = 0,027 gr
berat sampel = 2,003 gr
persen kadar abu tidak larut asam II = 0,027 2,003
x 100% = 1,347%
persen kadar abu tidak larut asam III = 0,026 2,001
x 100%
= 1,299 %
persen rata-rata kadar abu tidak larut asam = 3
1,446 % + 1,347 % + 1,299 %
Lampiran 9. Tabel Konversi Dosis Hewan dengan Manusia
Konversi dosis antara jenis hewan dengan manusia (Laurence and Bacharach,
1964).
Mencit 20 g
Tikus 200 g
Marmut 400 g
Kelinci 1,2 kg
Kera 4 kg
Anjing 12 kg
Manusia 70 kg Mencit
20g 1,0 7,0 12,25 27,8 64,1 124,2 387,9
Tikus
200g 0,14 1,0 1,74 3,9 9,2 17,8 56,0
Marmut
400 g 0,08 0,57 1,0 2,25 5,2 10,2 31,5
Kelinci
1,2 kg 0,04 0,25 0,44 1,0 2,4 4,5 14,2
Kera
4 kg 0,016 0,11 0,19 0,42 1,0 1,9 6,1
Anjing
12 kg 0,008 0,06 0,10 0,22 0,52 1,0 3,1 Manusia
Lampiran 10 . Bagan Perlakuan Pada Hewan Percobaan dengan Pemberian Natrium Diklofenak Tanpa EERK
Dipuasakan minimal 8 jam sebelum percobaan Ditimbang
Diberikan natrium diklofenak dengan dosis yang telah dikonversikan terhadap dosis lazim 25 mg secara oral
Diambil urinnya dengan interval waktu 6; 12; 18; 24; 30 jam setelah pemberian natrium diklofenak
Ditambahkan TCA 20% sebanyak 1 ml
Dihomogenkan dengan vortex
Disentrifuge pada 3000 rpm selama 10 menit
Diambil supernatan dan diukur dengan alat spektrofotometri pada panjang gelo bang 276 nm
Tikus
Cuplikan urin
Lampiran 11. Bagan Perlakuan Pada Hewan Percobaan Dengan Pemberian Natrium Diklofenak Dengan EERK
Ditimbang
Diberikan EERK dosis 20; 40; 80 mg/kg BB selama 7 hari berturut-turut
Pada hari ke tujuh, 4 jam setelah pemberian EERK diberikan natrium diklofenak dengan dosis yang telah dikonversikan terhadap dosis lazim 25 mg secara oral Diambil urinnya dengan interval waktu 6; 12; 18; 24; 30 jam setelah pemberian natrium diklofenak
Ditambahkan TCA 20% sebanyak 1 ml Dihomogenkan dengan vortex
Disentrifuge pada 3000 rpm selama 10 menit
Diambil supernatan dan diukur dengan alat spektrofotometri pada panjang gelo bang 276 nm
Tikus
Cuplikan urin
Lampiran 12. Contoh Perhitungan Dosis
1. Perhitungan Dosis Ekstrak Etanol Rimpang Kencur
• Dosis suspensi ekstrak etanol rimpang kencur: 20 mg/kgbb, 40 mg/kgbb,
dan 80 mg/kgbb
• Cara pembuatan suspensi ekstrak rimpang kencur 1%
Konsentrasi suspensi ekstrak 1% = 1 g/100 ml
=1000 mg/100 ml = 10 mg/ ml
Ditimbang 250 mg ekstrak etanol rimpang kencur, dilarutkan sedikit demi sedikit
suspensi CMC 1% kemudian homogenkan. Dituang kedalam labu tentukur 25 ml ditambahkan CMC 1% sampai tanda batas.
a. Dosis = 20 mg/kgbb
berat badan tikus = 247 g
= 20 mg
1000 g× 247 g = 4,94 mg
volume ekstrak yang di suntikkan:
= 4,94 mg
10 mg /ml = 0,5 ml
b. Dosis = 40 mg/kgbb
berat badan tikus = 227 g
= 40 mg
1000 g× 227 g = 9,108 mg
Volume ekst