TESIS
PENGEMBANGAN METODE KROMATOGRAFI CAIR
KINERJA TINGGI SPEKTROMETRI MASSA UNTUK
PENETAPAN KADAR RIFAMPISIN, ISONIAZID DAN
PIRAZINAMID DARI PLASMA MANUSIA DAN SEDIAAN
TABLET
OLEH:
NERDY
NIM 107014007
PROGRAM STUDI MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGEMBANGAN METODE KROMATOGRAFI CAIR
KINERJA TINGGI SPEKTROMETRI MASSA UNTUK
PENETAPAN KADAR RIFAMPISIN, ISONIAZID DAN
PIRAZINAMID DARI PLASMA MANUSIA DAN SEDIAAN
TABLET
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister dalam Ilmu Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
NERDY
NIM 107014007
PROGRAM STUDI MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN TESIS
Nama Mahasiswa : Nerdy Nomor Induk Mahasiswa : 107014007
Program Studi : Magister Farmasi
Judul Tesis : Pengembangan Metode Kromatografi Cair Kinerja Tinggi Spektrometri Massa untuk Penetapan Kadar Rifampisin, Isoniazid dan Pirazinamid dari Plasma Manusia dan Sediaan Tablet
Tempat dan Tanggal Ujian Lisan Tesis : Medan, 21 Juli 2012
Menyetujui:
Komisi Pembimbing, Ketua,
Prof. Dr.rer.nat. Effendy De Lux Putra, S.U., Apt. NIP 19530619 198303 1 001
Anggota,
Prof. Dr. Daryono Hadi Tjahjono, M.Sc., Apt. NIP 19650709 199203 1 001
Medan, Agustus 2012
Ketua Program Studi, Dekan,
PENGESAHAN TESIS
Nama Mahasiswa : Nerdy Nomor Induk Mahasiswa : 107014007
Program Studi : Magister Farmasi
Judul Tesis : Pengembangan Metode Kromatografi Cair Kinerja Tinggi Spektrometri Massa untuk Penetapan Kadar Rifampisin, Isoniazid dan Pirazinamid dari Plasma Manusia dan Sediaan Tablet
Telah diuji dan dinyatakan LULUS di depan Tim Penguji Tesis pada hari Sabtu tanggal 21, bulan Juli, tahun 2012
Mengesahkan: Tim Penguji Tesis
Ketua Tim Penguji : Prof. Dr.rer.nat. Effendy De Lux Putra, S.U., Apt. Anggota Tim Penguji : Prof. Dr. Daryono Hadi Tjahjono, M.Sc., Apt.
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan penelitian dan penulisan tesis dengan judul “Pengembangan Metode Kromatografi Cair Kinerja Tinggi Spektrometri Massa untuk Penetapan Kadar Rifampisin, Isoniazid dan Pirazinamid dari Plasma Manusia dan Sediaan Tablet” yang merupakan salah satu syarat untuk memperoleh gelar Magister dalam Ilmu Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Selama menyelesaikan penelitian dan tesis ini penulis telah banyak mendapatkan bantuan dan dorongan dari berbagai pihak, baik moril maupun materil. Untuk itu penulis ingin menghaturkan penghargaan dan terima kasih yang tiada terhingga kepada:
1. Bapak Prof. Dr. dr. Syahril Pasaribu, DTM&H., M.Sc., (CTM)., Sp.A(K), selaku Rektor Universitas Sumatera Utara, Medan, yang telah memberikan kesempatan dan fasilitas kepada penulis untuk mengikuti dan menyelesaikan Program Studi Magister Ilmu Farmasi pada Fakultas Farmasi, Universitas Sumatera Utara, Medan.
2. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi, Universitas Sumatera Utara, Medan, yang telah menyediakan fasilitas dan kesempatan bagi penulis menjadi mahasiswa dan menyelesaikan Program Studi Magister Ilmu Farmasi pada Fakultas Farmasi, Universitas Sumatera Utara, Medan.
3. Bapak Prof. Dr. Karsono, Apt., selaku Ketua Program Studi Magister Ilmu Farmasi pada Farmasi Fakultas Farmasi, Universitas Sumatera Utara, Medan, yang telah menyediakan arahan dan bantuan bagi penulis untuk menyelesaikan Magister Ilmu Farmasi pada Fakultas Farmasi, Universitas Sumatera Utara, Medan.
4. Bapak Prof. Dr.rer.nat. Effendy De Lux Putra, S.U., Apt., dan Bapak Prof. Dr. Daryono Hadi Tjahjono, M.Sc., Apt., sebagai komisi pembimbing yang telah banyak memberikan bimbingan, arahan, masukkan, saran, dan dorongan dengan penuh kesabaran tulus dan ikhlas bagi penulis dalam menjalani pendidikan, penelitian dan penyelesaian tesis ini.
5. Bapak Prof. Dr. Matheus Timbul Simanjuntak, M.Sc., Apt., dan Bapak Dr. M. Pandapotan Nasution, MPS., Apt., sebagai komisi penguji yang telah banyak memberikan saran dan masukkan bagi penulis dalam penyelesaian tesis ini, sehingga tesis ini semakin baik.
6. Bapak Prof. Dr.rer.nat. Effendy De Lux Putra, S.U., Apt., sebagai Kepala Laboratorium Penelitian beserta staf yang telah banyak memberikan bantuan sarana penelitian bagi penulis guna kelancaran bagi penulis dalam penelitian
7. Papa Phoa Tjeng In, Mama Lina dan Abang Nardo sebagai keluarga tercinta penulis yang banyak memberikan bantuan baik dalam bentuk moril dan materil bagi penulis dalam menjalani pendidikan, penelitian dan penyelesaian tesis ini.
seperjuangan S2 angkatan 2010 dan 2011 (terutama Floriana Sundari Loung, Puji Lestari Wulandari dan Elysa) yang selalu mendukung penulis. Serta buat semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah banyak membantu dalam penelitian tesis ini. Kiranya Tuhan Yang Maha Esa memberikan balasan yang berlipat ganda atas kebaikan dan bantuan yang telah diberikan kepada penulis.
Penulis menyadari bahwa tesis ini masih jauh dari kesempurnaan, sehingga penulis mengharapkan kritik dan saran yang bersifat membangun dari semua pihak. Akhir kata semoga tulisan ini dapat menjadi sumbangan yang berarti bagi ilmu pengetahuan khususnya bagi bidang farmasi.
Medan, 21 Juli 2012 Penulis,
(Nerdy)
PENGEMBANGAN METODE KROMATOGRAFI CAIR KINERJA TINGGI SPEKTROMETRI MASSA UNTUK PENETAPAN KADAR RIFAMPISIN, ISONIAZID DAN PIRAZINAMID DARI PLASMA
MANUSIA DAN SEDIAAN TABLET ABSTRAK
Obat-obat yang digunakan dalam pengobatan tuberkulosis dapat dibagi kedalam 2 kategori, yaitu: obat anti tuberkulosis primer dan obat anti tuberkulosis sekunder. Obat anti tuberkulosis primer lebih tinggi kemanjurannya dan lebih baik keamanannya dari obat anti tuberkulosis sekunder. Obat anti tuberkulosis primer adalah rifampisin, isoniazid, pirazinamid dan etambutol. Rifampisin, isoniazid dan pirazinamid merupakan kombinasi obat anti tuberkulosis.
Menurut Undang-Undang Republik Indonesia nomor 36 tahun 2009 tentang kesehatan pasal 105 ayat 1 bahwa sediaan farmasi yang berupa obat dan bahan baku obat harus memenuhi syarat Farmakope Indonesia atau buku standar lainnya. Pemantauan terapi obat perlu dilakukan untuk mengetahui bahwa kadar obat dalam tubuh berada pada rentang terapi.
Penetapan kadar rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet dapat dilakukan dengan metode kromatografi cair kinerja tinggi. Untuk mendapatkan hasil analisis kromatografi cair kinerja tinggi yang baik memerlukan optimasi. Penelitian yang dilaksanakan ini meliputi optimasi terhadap jenis campuran fase gerak, perbandingan fase gerak, laju alir fase gerak dan suhu oven kolom pada metode kromatografi cair kinerja tinggi spektrometri massa. Penelitian ini diharapkan sebagai pengembangan metode yang dapat digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet. Penelitian ini juga meliputi pengujian validasi yang dilaksanakan dengan beberapa pengujian seperti: uji akurasi dengan parameter persentase perolehan kembali, uji presisi dengan parameter simpangan baku relatif, uji spesifitas, uji batas deteksi, uji batas kuantitasi dan uji linearitas.
Hasil penelitian menunjukkan bahwa metode kromatografi cair kinerja tinggi spektrometri massa yang telah dikembangkan dapat digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet. Kondisi optimum yang diperoleh adalah jenis campuran fase gerak larutan asam format 0,1% dalam air destilasi ganda yang telah dimurnikan (setelah dicampur kemudian disaring melalui membran penyaring nitrat selulosa 0,2 µm dan diawaudarakan/disonikasi selama 30 menit) dan larutan asam format 0,1% dalam metanol (setelah dicampur kemudian disaring melalui membran penyaring politetraflouroetilen (PTFE) 0,5 µm dan diawaudarakan/disonikasi selama 30 menit) dengan laju alir fase gerak 0,5 mL/menit, pada perbandingan fase gerak 90%:10% hingga menit 3, dimana isoniazid dan pirazinamid telah terelusi (dan memisah), kemudian diubah menjadi perbandingan fase gerak menjadi 30%:70% pada menit 3,1 dan dipertahankan hingga rifampisin terelusi (hingga menit 10) serta suhu oven kolom 35o
Kondisi optimum metode kromatografi cair kinerja tinggi spektrometri massa yang digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet memenuhi persyaratan uji validasi metode. Pengujian validitas metode meliputi uji akurasi dengan parameter
persentase perolehan kembali, uji presisi dengan parameter simpangan baku relatif, uji spesifitas, uji batas deteksi, uji batas kuantitasi dan uji linearitas. Dari hasil pemeriksaaan kadar sediaan tablet yang beredar di pasaran yang mengandung campuran rifampisin, isoniazid dan pirazinamid diketahui bahwa sediaan tablet Rimcure 3 FDC® (P.T. Sandoz) memenuhi persyaratan Farmakope Amerika Serikat edisi ke-30 tahun 2007.
HIGH PERFORMANCE LIQUID CHROMATOGRAPHY MASS SPECTROMETRY METHOD DEVELOPMENT FOR DETERMINATION
OF RIFAMPICIN, ISONIAZID AND PYRAZINAMIDE FROM HUMAN PLASMA AND TABLET PREPARATION
ABSTRACT
The drugs used in the treatment of tuberculosis can be divided into two categories, i.e.: primary anti-tuberculosis and secondary anti-tuberculosis. The primary anti-tuberculosis have a higher efficacy and better safety than those of secondary anti-tuberculosis drugs. Primary anti-tuberculosis drugs are rifampicin, isoniazid, pyrazinamide and ethambutol. In their use rifampicin, isoniazid and pyrazinamide are usually combined.
According to the Law of the Republic of Indonesia number 36 year 2009 on health of article 105 paragraph 1 that pharmaceutical preparation and pharmaceutical raw materials must meet the requirements set out by Indonesia Pharmacopoeia or other relevant standard. Therapeutic drug monitoring needs to be done to find out that the drug level in the body has to be within the therapeutic range.
The concentration of rifampicin, isoniazid and pyrazinamide in human plasma and tablet preparations can be determined by high performance liquid chromatographic method. To obtain good results of the high performance liquid chromatography analysis, the optimization of chromatographic conditions is essential. The research undertaken includes the optimization of the type of mobile phase, the composition of mobile phase, flow rate and column temperature of high performance liquid chromatography mass spectrometry. This research is expected to improve the method that can be used for the determination of a mixture of rifampicin, isoniazid and pyrazinamide in human plasma and tablet preparation. The study also includes validation procedure such as: the determination of accuracy by the recovery percentage parameter, the determination of precision by the relative standard deviation parameter, the determination of specificity, the determination of limit of detection, the determination of limit of quantitation and the determination of linearity.
The results showed that high performance liquid chromatography mass spectrometry method which has been developed in this study can be used for the determination of a mixture of rifampicin, isoniazid and pyrazinamide in human plasma and tablet preparation. Optimum conditions obtained for type of mobile phase was 0.1% formic acid solution in doubly distilled water that has been purified (after being mixed and then filtered through a cellulose nitrate membrane
filter 0.2 μm and sonicated for 30 minutes) and 0.1% formic acid solution in
methanol (after being mixed and then filtered through a polytetraflouroethylene
(PTFE) membrane filter 0.5 μm and sonicated for 30 minutes) with a flow rate 0.5
mL/min, the 90%:10% ratio up to 3 minutes, after isoniazid and pyrazinamide was eluted (and separate), then changed into 30%:70% ratio at 3.1 minutes and maintained until rifampicin eluted (up to 10 minutes) at column temperature 35o
requirements of the method validation test. The method validity testing included the accuracy test with recovery percentage parameter, the precision test with relative standard deviation parameter, the specificity test, the limit of detection test, the limit of quantitation test and the linearity test. From the results of quatitative determination of tablet preparation obtained from the marketplace that contain a mixture of rifampicin, isoniazid and pyrazinamide known that tablet preparation Rimcure 3 FDC® (P.T. Sandoz) meets the requirements of the United States Pharmacopoeia 30th edition in 2007.
DAFTAR ISI
2.2 Rifampisin, Isoniazid dan Pirazinamid ... 10
2.2.1 Rifampisin ... 12
2.2.1.1 Pengunaan dan Cara Pemberian ... 13
2.2.1.3 Efek Samping ... 14
2.3 Analisis Rifampisin, Isoniazid dan Pirazinamid ... 19
2.4 Spektrofotometri Infra Merah ... 24
2.5.1.4.1 Wadah Fase Gerak Destilasi Ganda yang telah Dimurnikan 49
3.3.1.2 Larutan Asam Format 0,1% dalam Metanol ... 49
3.3.1.4 Larutan Asam Asetat 1% dalam Isoniazid dan Baku Pirazinamid dengan Spektrofotometer Infra Merah Fourier Transform (Fourier Transform Infra Red (FTIR)) ... 52
3.3.2.2 Penyiapan Alat Kromatografi Cair Kinerja Tinggi Spektrometri Massa ... 53
3.3.2.3 Penentuan Kondisi Optimum ... 53
3.3.2.4 Analisis Kualitatif Rifampisin, Isoniazid dan Pirazinamid dalam Plasma Manusia dan Sediaan Tablet ... 55
3.3.2.5 Analisis Kuantitatif Campuran Rifampisin, Isoniazid dan Pirazinamid dalam Sediaan Tablet ... 55
3.3.2.6 Analisis Secara Statistik ... 56
3.3.3 Validasi Metode Analisis Kuantitatif Campuran Rifampisin, Isoniazid dan Pirazinamid dalam Plasma Manusia dan Sediaan Tablet ... 57
3.3.3.1 Pengujian Akurasi (Kecermatan) Metode Analisis Kuantitatif Sampel Plasma Manusia yang Mengandung Campuran Rifampisin, Isoniazid dan
Pirazinamid ... 57
Campuran Rifampisin, Isoniazid dan
Pirazinamid ... 61
3.3.3.3 Pengujian Linearitas Metode Analisis Kuantitatif Sampel Plasma Manusia yang Mengandung Campuran
Rifampisin, Isoniazid dan Pirazinamid . 61
3.3.3.4 Pengujian Batas Deteksi dan Batas Kuantitasi Metode Analisis Kuantitatif Sampel Plasma Manusia yang Mengandung Campuran Rifampisin, Isoniazid dan Pirazinamid ... 63
3.3.3.5 Pengujian Akurasi (Kecermatan) Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung Campuran
Rifampisin, Isoniazid dan Pirazinamid . 64
3.3.3.6 Pengujian Presisi (Keseksamaan) Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung Campuran
Rifampisin, Isoniazid dan Pirazinamid . 64
3.3.3.7 Pengujian Linearitas Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung Campuran Rifampisin, Isoniazid dan Pirazinamid ... 65
3.3.3.8 Pengujian Batas Deteksi dan Batas Kuantitasi Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung Campuran Rifampisin, Isoniazid dan
Pirazinamid ... 66
BAB IV HASIL DAN PEMBAHASAN ... 68
4.3 Analisis Kualitatif Rifampisin, Isoniazid dan Pirazinamid dalam Plasma Manusia dan Sediaan Tablet ... 83
4.4 Analisis Kuantitatif Sediaan Tablet Rimcure 3 FDC®
4.5 Validasi Metode Analisis Kuantitatif Campuran Rifampisin, Isoniazid dan Pirazinamid dalam Plasma Manusia dan Sediaan Tablet ... 90
(P.T. Sandoz) yang Mengandung Campuran Rifampisin, Isoniazid dan Pirazinamid ... 89
4.5.1 Pengujian Akurasi (Kecermatan) Metode Analisis Kuantitatif Sampel Plasma Manusia yang
Mengandung Campuran Rifampisin, Isoniazid dan Pirazinamid ... 90
4.5.2 Pengujian Presisi (Keseksamaan) Metode Analisis Kuantitatif Sampel Plasma Manusia yang
Mengandung Campuran Rifampisin, Isoniazid dan Pirazinamid ... 97
4.5.3 Pengujian Spesifitas Metode Analisis Kuantitatif Sampel Plasma Manusia yang Mengandung
Campuran Rifampisin, Isoniazid dan Pirazinamid 98
4.5.4 Pengujian Linearitas Metode Analisis Kuantitatif Sampel Plasma Manusia yang Mengandung
Campuran Rifampisin, Isoniazid dan Pirazinamid 98
4.5.5 Pengujian Batas Deteksi dan Batas Kuantitasi Metode Analisis Kuantitatif Sampel Plasma Manusia yang Mengandung Campuran
Rifampisin, Isoniazid dan Pirazinamid ... 103
4.5.6 Pengujian Akurasi (Kecermatan) Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung
Campuran Rifampisin, Isoniazid dan Pirazinamid 104
4.5.7 Pengujian Presisi (Keseksamaan) Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung
Campuran Rifampisin, Isoniazid dan Pirazinamid 105
4.5.8 Pengujian Spesifitas Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung Campuran
Rifampisin, Isoniazid dan Pirazinamid ... 106
4.5.9 Pengujian Linearitas Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung Campuran
4.5.10 Pengujian Batas Deteksi dan Batas Kuantitasi Metode Analisis Kuantitatif Sediaan Tablet yang Mengandung Campuran Rifampisin, Isoniazid dan
Pirazinamid ... 111
BAB V KESIMPULAN DAN SARAN ... 113
5.1 Kesimpulan ... 113
5.2 Saran ... 114
DAFTAR TABEL
Halaman
Tabel 2.1. Perubahan perbandingan fase gerak (USP XXX, 2007). ... 20
Tabel 2.2. Perubahan perbandingan fase gerak (Dorneanu, 2010). ... 21
Tabel 4.10. Data hasil perhitungan kadar campuran rifampisin,
isoniazid dan pirazinamid dari sediaan tablet Rimcure 3 FDC®
Tabel 4.11. Luas area baku rifampisin (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai konsentrasi untuk pengujian persentase perolehan kembali
(recovery percentage (% recovery)) baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku
pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 94 (P.T. Sandoz) setelah dilakukan uji statistik. ... 90
Tabel 4.12. Luas area baku isoniazid (P.T. Indofarma) dalam campuran
air dan metanol (50%:50%) pada berbagai konsentrasi untuk pengujian persentase perolehan kembali (recovery
percentage (% recovery)) baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku
pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 95
Tabel 4.13. Luas area baku pirazinamid (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai konsentrasi untuk pengujian persentase perolehan kembali
(recovery percentage (% recovery)) baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku
pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 96
Tabel 4.14. Data hasil pengujian persentase perolehan kembali
(recovery percentage (% recovery)) baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku
pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 97
Tabel 4.15. Luas area baku rifampisin (P.T. Indofarma) dalam plasma
Tabel 4.17. Luas area baku pirazinamid (P.T. Indofarma) dalam plasma
manusia pada berbagai konsentrasi untuk pengujian
linearitas. ... 102
Tabel 4.18. Data hasil pengujian persentase perolehan kembali
(recovery percentage (% recovery)) baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dari tablet Rimcure 3 FDC® (P.T. Sandoz) dengan metode penambahan bahan baku
Tabel 4.19. Luas area baku rifampisin (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai
konsentrasi untuk pengujian linearitas. ... 108
Tabel 4.20. Luas area baku isoniazid (P.T. Indofarma) dalam campuran
air dan metanol (50%:50%) pada berbagai konsentrasi untuk pengujian linearitas. ... 109
Tabel 4.21. Luas area baku pirazinamid (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai
DAFTAR GAMBAR
Halaman Gambar 1.1. Skema hubungan antara variabel bebas dan variabel
terikat pada sistem kromatografi cair kinerja tinggi. ... 6
Gambar 2.1. Rumus struktur rifampisin. ... 12
Gambar 2.2. Rumus struktur isoniazid. ... 14
Gambar 2.3. Rumus struktur pirazinamid. ... 17
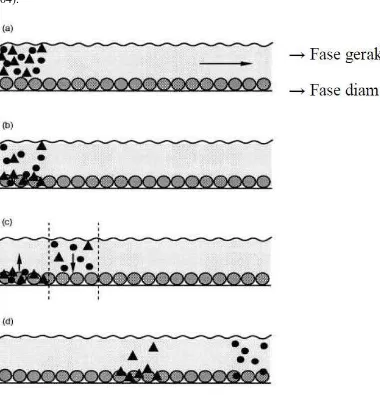
Gambar 2.4. Ilustrasi proses pemisahan yang terjadi didalam kolom kromatografi cair kinerja tinggi (Meyer, 2004). ... 29
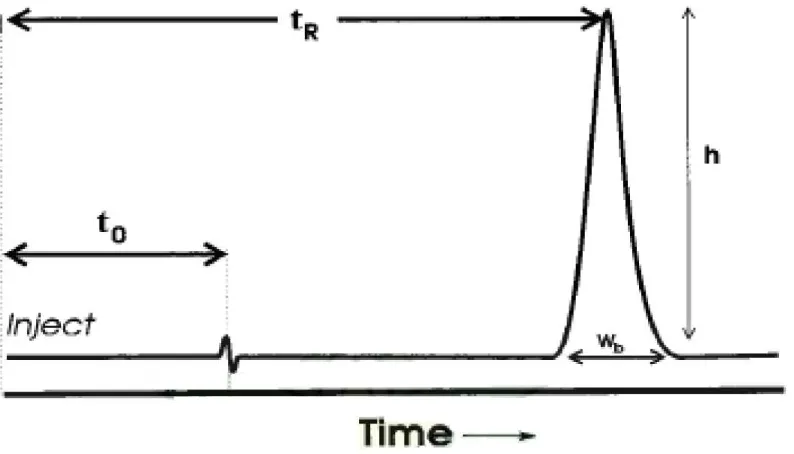
Gambar 2.5. Kromatogram puncak tunggal yang diperoleh dari analisis kromatografi cair kinerja tinggi (Ornaf dan Dong, 2005). ... 31
Gambar 2.6. Kromatogram dua puncak yang diperoleh dari analisis kromatografi cair kinerja tinggi (Meyer, 2004). ... 31
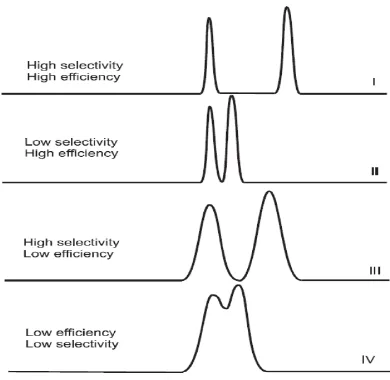
Gambar 2.7. Kromatogram hasil analisis kromatografi cair kinerja tinggi dengan berbagai selektifitas dan efisiensi (Kazakevich dan LoBrutto, 2007). ... 34
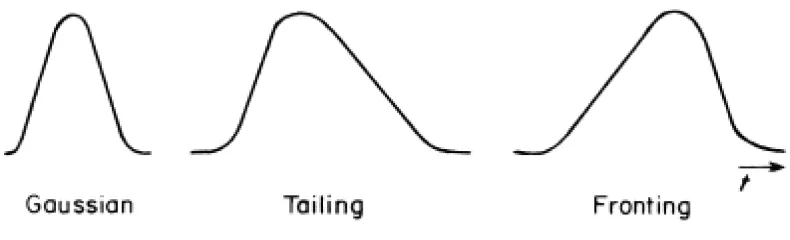
Gambar 2.8. Bentuk puncak kromatogram (Meyer, 2004). ... 36
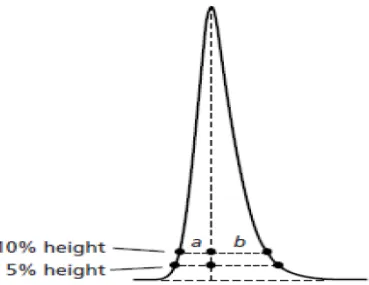
Gambar 2.9. Pengukuran derajat asimetris puncak (Dolan, 2003). ... 37
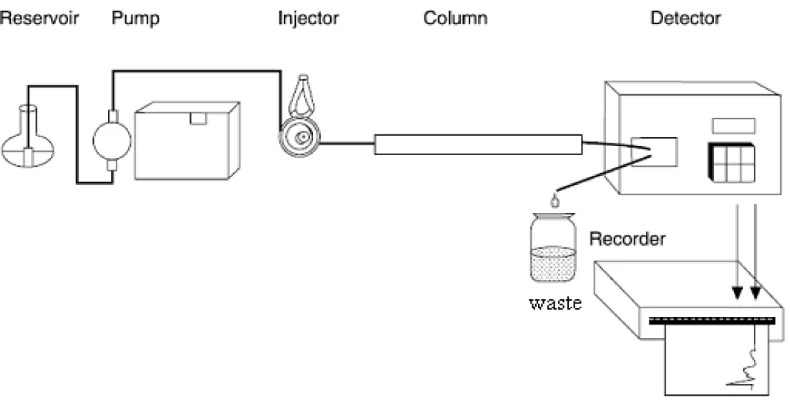
Gambar 2.10. Instrumen dasar kromatografi cair kinerja tinggi
Gambar 4.3. Spektrum infra merah baku isoniazid (P.T. Indofarma). 71
Gambar 4.5. Spektrum infra merah baku pirazinamid (P.T. baku pirazinamid (P.T. Indofarma) serta data hasil
pendeteksian spektrometri massa dengan jenis
pendeteksian pemindaian (scanning) dari setiap puncak
yang terdeteksi. ... 86
Gambar 4.8. Kromatogram hasil analisis plasma manusia yang
mengandung campuran rifampisin, isoniazid dan pirazinamid serta data hasil pendeteksian spektrometri massa dengan jenis pendeteksian pemindaian (scanning)
isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T.
Indofarma) dalam plasma manusia. ... 93
Gambar 4.11. Kurva kalibrasi baku rifampisin (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai konsentrasi untuk pengujian persentase perolehan kembali (recovery percentage (% recovery)) baku
rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 94
Gambar 4.12. Kurva kalibrasi baku isoniazid (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai konsentrasi untuk pengujian persentase perolehan kembali (recovery percentage (% recovery)) baku
Indofarma) dan baku pirazinamid (P.T. Indofarma)
baku rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 96
Gambar 4.14. Kromatogram hasil pendeteksian campuran baku
rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dalam plasma manusia pada berbagai konsentrasi untuk
pengujian linearitas. ... 100
Gambar 4.15. Kurva kalibrasi baku rifampisin (P.T. Indofarma) dalam
plasma manusia pada berbagai konsentrasi untuk
dalam plasma manusia pada berbagai konsentrasi untuk
pengujian linearitas. ... 103
Gambar 4.18. Kromatogram hasil pendeteksian campuran baku
rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dalam campuran air dan metanol (50%:50%) pada berbagai konsentrasi untuk pengujian linearitas. ... 108
Gambar 4.19. Kurva kalibrasi baku rifampisin (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai
konsentrasi untuk pengujian linearitas. ... 109
Gambar 4.20. Kurva kalibrasi baku isoniazid (P.T. Indofarma) dalam
campuran air dan metanol (50%:50%) pada berbagai
konsentrasi untuk pengujian linearitas. ... 110
Gambar 4.21. Kurva kalibrasi baku pirazinamid (P.T. Indofarma)
DAFTAR LAMPIRAN
Halaman Lampiran 1. Gambar seperangkat alat kromatografi cair kinerja
tinggi spektrometri massa (KCKTSM). ... 119
Lampiran 2. Gambar seperangkat alat spektrofotometer infra merah
(Shimadzu). ... 121
Lampiran 3. Gambar alat pendestilasi ganda air (Aquatron). ... 122 Lampiran 4. Gambar alat pemurni air (Elga). ... 123
Lampiran 8. Gambar alat membran penyaring nitrat selulosa 0,2 µm
(ukuran pori) 47 mm (diameter) (Whatman); membran penyaring politetrafluoroetilen 0,5 µm (ukuran pori) 47 mm (diameter) (Whatman); membran penyaring
politetrafluoroetilen 0,2 µm (ukuran pori) 25 mm
(diameter) (Whatman) serta syringe 5 mL (Terumo). ... 127
Lampiran 9. Gambar alat pembersih ultrasonik (Branson) dan alat
pembersih ultrasonik (Kudos). ... 130
Lampiran 10 Gambar dan spesifikasi tablet Rimcure 3 FDC®
Lampiran 13. Kromatogram rifampisin, isoniazid dan pirazinamid
dengan menggunakan kombinasi fase gerak yang terdiri dari larutan asam asetat 1% dalam air destilasi ganda yang telah dimurnikan dan larutanasam asetat 1% dalam metanol dengan perbandingan fase gerak 10%:90%;
30%:70%; 50%:50%; 70%:30%; 90%:10%. ... 144
Lampiran 14. Kromatogram optimasi laju alir fase gerak. ... 150 Lampiran 15. Kromatogram optimasi suhu oven kolom. ... 152 Lampiran 16. Perhitungan koefisien korelasi dan persamaan regresi
untuk baku rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan bakupirazinamid (P.T. Indofarma) dalam campuran air dan metanol (50%:50%) untuk pengujian persentase perolehan kembali (recovery
percentage (% recovery)) baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku
pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 154
Lampiran 17. Perhitungan koefisien korelasi dan persamaan regresi
baku rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma)
baku rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dalam campuran air dan metanol (50%:50%). ... 170
Lampiran 21. Perhitungan penimbangan tablet Rimcure 3 FDC® (P.T.
Sandoz) pada penentuan kadar campuran rifampisin, isoniazid dan pirazinamid yang sebenarnya dalam tablet Rimcure 3 FDC®
Lampiran 22. Contoh perhitungan kadar campuran rifampisin,
isoniazid dan pirazinamid pada penentuan kadar
campuran rifampisin, isoniazid dan pirazinamid yang sebenarnya dalam tablet Rimcure 3 FDC®
Lampiran 23. Contoh Perhitungan penentuan kadar campuran
Lampiran 24. Data hasil rekapitulasi dari kadar campuran rifampisin,
isoniazid dan pirazinamid yang sebenarnya dalam tablet Rimcure 3 FDC
(P.T. Sandoz). ... 177
®
Lampiran 25. Analisis data secara statistik untuk mencari kadar
campuran rifampisin, isoniazid dan pirazinamid yang sebenarnya dalam tablet Rimcure 3 FDC
(P.T. Sandoz). ... 179
®
Lampiran 26. Perhitungan kadar campuran baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) yang sebenarnya dalam plasma manusia pada penentuan perolehan kembali. .... 184
(P.T. dalam plasma manusia pada rentang spesifik 100%. ... 188
Lampiran 28. Data hasil perhitungan pengujian persentase perolehan
kembali (recovery percentage (% recovery)) baku
rifampisin (P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dalam plasma manusia. ... 190
Lampiran 29. Analisis data statistik persentase perolehan kembali
(recovery percentage (% recovery)) baku rifampisin
(P.T. Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) dalam plasma
manusia. ... 192
Lampiran 30. Perhitungan penimbangan pada penentuan persentase
perolehan kembali campuran rifampisin, isoniazid dan pirazinamid pada berbagai rentang spesifik dari tablet Rimcure 3 FDC®
Lampiran 31. Perhitungan kadar campuran rifampisin, isoniazid dan
pirazinamid yang sebenarnya pada penentuan persentase perolehan kembali campuran rifampisin,
(P.T. Sandoz) dengan metode
isoniazid dan pirazinamid pada berbagai rentang spesifik dari tablet Rimcure 3 FDC®
Lampiran 32. Perhitungan kadar campuran baku rifampisin (P.T.
Indofarma), baku isoniazid (P.T. Indofarma) dan baku pirazinamid (P.T. Indofarma) yang sebenarnya pada penentuan persentase perolehan kembali campuran rifampisin, isoniazid dan pirazinamid pada berbagai rentang spesifik dari tablet Rimcure 3 FDC
(P.T. Sandoz) dengan metode penambahan baku sebelum penambahan baku. ... 199
®
Lampiran 33. Contoh perhitungan persentase perolehan kembali
campuran rifampisin, isoniazid dan pirazinamid pada rentang spesifik 100% dari tablet Rimcure 3 FDC
(P.T. Sandoz) dengan metode penambahan baku. ... 203
®
Lampiran 34. Data hasil perhitungan persentase perolehan kembali
campuran rifampisin, isoniazid dan pirazinamid pada berbagai rentang spesifik dari tablet Rimcure 3 FDC
(P.T. Sandoz) dengan metode penambahan baku. ... 207
®
Lampiran 35. Analisis data statistik persentase perolehan kembali
campuran rifampisin, isoniazid dan pirazinamid pada berbagai rentang spesifik persentase perolehan kembali dari tablet Rimcure 3 FDC
(P.T. Sandoz) dengan metode penambahan baku. ... 210
®
Lampiran 36. Sertifikat analisis baku rifampisin (P.T. Indofarma). ... 215
(P.T. Sandoz) dengan metode penambahan baku. ... 212
PENGEMBANGAN METODE KROMATOGRAFI CAIR KINERJA TINGGI SPEKTROMETRI MASSA UNTUK PENETAPAN KADAR RIFAMPISIN, ISONIAZID DAN PIRAZINAMID DARI PLASMA
MANUSIA DAN SEDIAAN TABLET ABSTRAK
Obat-obat yang digunakan dalam pengobatan tuberkulosis dapat dibagi kedalam 2 kategori, yaitu: obat anti tuberkulosis primer dan obat anti tuberkulosis sekunder. Obat anti tuberkulosis primer lebih tinggi kemanjurannya dan lebih baik keamanannya dari obat anti tuberkulosis sekunder. Obat anti tuberkulosis primer adalah rifampisin, isoniazid, pirazinamid dan etambutol. Rifampisin, isoniazid dan pirazinamid merupakan kombinasi obat anti tuberkulosis.
Menurut Undang-Undang Republik Indonesia nomor 36 tahun 2009 tentang kesehatan pasal 105 ayat 1 bahwa sediaan farmasi yang berupa obat dan bahan baku obat harus memenuhi syarat Farmakope Indonesia atau buku standar lainnya. Pemantauan terapi obat perlu dilakukan untuk mengetahui bahwa kadar obat dalam tubuh berada pada rentang terapi.
Penetapan kadar rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet dapat dilakukan dengan metode kromatografi cair kinerja tinggi. Untuk mendapatkan hasil analisis kromatografi cair kinerja tinggi yang baik memerlukan optimasi. Penelitian yang dilaksanakan ini meliputi optimasi terhadap jenis campuran fase gerak, perbandingan fase gerak, laju alir fase gerak dan suhu oven kolom pada metode kromatografi cair kinerja tinggi spektrometri massa. Penelitian ini diharapkan sebagai pengembangan metode yang dapat digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet. Penelitian ini juga meliputi pengujian validasi yang dilaksanakan dengan beberapa pengujian seperti: uji akurasi dengan parameter persentase perolehan kembali, uji presisi dengan parameter simpangan baku relatif, uji spesifitas, uji batas deteksi, uji batas kuantitasi dan uji linearitas.
Hasil penelitian menunjukkan bahwa metode kromatografi cair kinerja tinggi spektrometri massa yang telah dikembangkan dapat digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet. Kondisi optimum yang diperoleh adalah jenis campuran fase gerak larutan asam format 0,1% dalam air destilasi ganda yang telah dimurnikan (setelah dicampur kemudian disaring melalui membran penyaring nitrat selulosa 0,2 µm dan diawaudarakan/disonikasi selama 30 menit) dan larutan asam format 0,1% dalam metanol (setelah dicampur kemudian disaring melalui membran penyaring politetraflouroetilen (PTFE) 0,5 µm dan diawaudarakan/disonikasi selama 30 menit) dengan laju alir fase gerak 0,5 mL/menit, pada perbandingan fase gerak 90%:10% hingga menit 3, dimana isoniazid dan pirazinamid telah terelusi (dan memisah), kemudian diubah menjadi perbandingan fase gerak menjadi 30%:70% pada menit 3,1 dan dipertahankan hingga rifampisin terelusi (hingga menit 10) serta suhu oven kolom 35o
Kondisi optimum metode kromatografi cair kinerja tinggi spektrometri massa yang digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet memenuhi persyaratan uji validasi metode. Pengujian validitas metode meliputi uji akurasi dengan parameter
persentase perolehan kembali, uji presisi dengan parameter simpangan baku relatif, uji spesifitas, uji batas deteksi, uji batas kuantitasi dan uji linearitas. Dari hasil pemeriksaaan kadar sediaan tablet yang beredar di pasaran yang mengandung campuran rifampisin, isoniazid dan pirazinamid diketahui bahwa sediaan tablet Rimcure 3 FDC® (P.T. Sandoz) memenuhi persyaratan Farmakope Amerika Serikat edisi ke-30 tahun 2007.
HIGH PERFORMANCE LIQUID CHROMATOGRAPHY MASS SPECTROMETRY METHOD DEVELOPMENT FOR DETERMINATION
OF RIFAMPICIN, ISONIAZID AND PYRAZINAMIDE FROM HUMAN PLASMA AND TABLET PREPARATION
ABSTRACT
The drugs used in the treatment of tuberculosis can be divided into two categories, i.e.: primary anti-tuberculosis and secondary anti-tuberculosis. The primary anti-tuberculosis have a higher efficacy and better safety than those of secondary anti-tuberculosis drugs. Primary anti-tuberculosis drugs are rifampicin, isoniazid, pyrazinamide and ethambutol. In their use rifampicin, isoniazid and pyrazinamide are usually combined.
According to the Law of the Republic of Indonesia number 36 year 2009 on health of article 105 paragraph 1 that pharmaceutical preparation and pharmaceutical raw materials must meet the requirements set out by Indonesia Pharmacopoeia or other relevant standard. Therapeutic drug monitoring needs to be done to find out that the drug level in the body has to be within the therapeutic range.
The concentration of rifampicin, isoniazid and pyrazinamide in human plasma and tablet preparations can be determined by high performance liquid chromatographic method. To obtain good results of the high performance liquid chromatography analysis, the optimization of chromatographic conditions is essential. The research undertaken includes the optimization of the type of mobile phase, the composition of mobile phase, flow rate and column temperature of high performance liquid chromatography mass spectrometry. This research is expected to improve the method that can be used for the determination of a mixture of rifampicin, isoniazid and pyrazinamide in human plasma and tablet preparation. The study also includes validation procedure such as: the determination of accuracy by the recovery percentage parameter, the determination of precision by the relative standard deviation parameter, the determination of specificity, the determination of limit of detection, the determination of limit of quantitation and the determination of linearity.
The results showed that high performance liquid chromatography mass spectrometry method which has been developed in this study can be used for the determination of a mixture of rifampicin, isoniazid and pyrazinamide in human plasma and tablet preparation. Optimum conditions obtained for type of mobile phase was 0.1% formic acid solution in doubly distilled water that has been purified (after being mixed and then filtered through a cellulose nitrate membrane
filter 0.2 μm and sonicated for 30 minutes) and 0.1% formic acid solution in
methanol (after being mixed and then filtered through a polytetraflouroethylene
(PTFE) membrane filter 0.5 μm and sonicated for 30 minutes) with a flow rate 0.5
mL/min, the 90%:10% ratio up to 3 minutes, after isoniazid and pyrazinamide was eluted (and separate), then changed into 30%:70% ratio at 3.1 minutes and maintained until rifampicin eluted (up to 10 minutes) at column temperature 35o
requirements of the method validation test. The method validity testing included the accuracy test with recovery percentage parameter, the precision test with relative standard deviation parameter, the specificity test, the limit of detection test, the limit of quantitation test and the linearity test. From the results of quatitative determination of tablet preparation obtained from the marketplace that contain a mixture of rifampicin, isoniazid and pyrazinamide known that tablet preparation Rimcure 3 FDC® (P.T. Sandoz) meets the requirements of the United States Pharmacopoeia 30th edition in 2007.
BAB I PENDAHULUAN
1.1 Latar Belakang
Tuberkulosis hingga kini masih jadi masalah kesehatan utama di dunia.
Berbagai pihak mencoba bekerja bersama untuk memeranginya. Bahkan penyakit
ini akhirnya “mampu” menggalang dana dari beberapa tokoh dunia seperti Bill
Gates dan George Soros, sehingga terbentuk GF ATM (global fund against
human immuno deficiency virus
Obat-obat yang digunakan dalam pengobatan tuberkulosis dapat dibagi
kedalam 2 kategori, yaitu: obat anti tuberkulosis primer dan obat anti tuberkulosis
sekunder. Obat anti tuberkulosis primer lebih tinggi kemanjurannya dan lebih baik
keamanannya dari obat anti tuberkulosis sekunder. Obat anti tuberkulosis primer
adalah rifampisin, isoniazid, pirazinamid dan etambutol (Muchtar, 2006).
acquired immuno deficiency syndrome,
tuberculosis, and malaria) yang juga diterima oleh program penanggulangan
tuberkulosis di negara Indonesia (Aditama, 2006).
Obat anti tuberkulosis sekunder adalah asam para amino salisilat, etionamid,
tioacetazon, fluorokuinolon, aminoglikosida, kapreomisin, sikloserin, penghambat
beta laktam, klaritromisin, rifabutin, linezolid, amikasin dan lain-lain. Pengobatan
dengan obat anti tuberkulosis sekunder memerlukan waktu yang lebih lama,
mengandung risiko efek samping yang lebih berat, sehingga ancaman
ketidakpatuhan mengikuti pengobatan adalah tinggi. Obat anti tuberkulosis
sekunder belum dapat menandingi keampuhan pasangan obat anti tuberkulosis
terhadap kuman yang dorman, sedangkan isoniazid bersifat bakterisid terhadap
kuman pada fase pembelahan. Pengobatan dengan obat anti tuberkulosis sekunder
menghasilkan konversi sputum setelah 4-7 bulan, dilanjutkan selama minimal 18
bulan dan jauh lebih lama dari pengobatan dengan menggunakan isoniazid dan
rifampisin (Muchtar, 2006).
Obat dalam bentuk kombinasi sering digunakan untuk mengobati berbagai
penyakit, termasuk diantaranya penyakit infeksi. Rifampisin, isoniazid dan
pirazinamid merupakan kombinasi obat anti tuberkulosis. Pengobatan tuberkulosis
sering dikombinasi dengan baik sebagai formulasi kombinasi dosis tetap (fixed
dose combination (FDC)) maupun diberikan dalam bentuk sediaan yang terpisah
secara bersamaan atau sekaligus (Pramudianto dan Evaria, 2010).
Sediaan tablet dalam kombinasi rifampisin, isoniazid dan pirazinamid
terdapat di pasaran, selain itu juga terdapat dalam bentuk sediaan tunggal
(Pramudianto dan Evaria, 2010). Menurut Undang-Undang Republik Indonesia
nomor 36 tahun 2009 tentang kesehatan pasal 105 ayat 1 bahwa sediaan farmasi
yang berupa obat dan bahan baku obat harus memenuhi syarat Farmakope
Indonesia atau buku standar lainnya. Persyaratan kadar untuk sediaan tablet yang
mengandung kombinasi rifampisin, isoniazid dan pirazinamid tidak tertera pada
Farmakope Indonesia. Akan tetapi dalam Farmakope Amerika Serikat edisi ke-30
(United States Pharmacopoeia) tahun 2007 tertera bahwa sediaan tablet
rifampisin, isoniazid dan pirazinamid mengandung tidak kurang dari 90,0% dan
tidak lebih dari 110,0% jumlah rifampisin (C43H58N4O12), isoniazid (C6H7N3O)
Pemantauan terapi obat (therapeutics drug monitoring (TDM)) perlu
dilakukan untuk mengetahui bahwa kadar obat dalam tubuh berada pada rentang
terapi. Adanya kemungkinan terjadinya interaksi obat anti tuberkulosis dengan
obat lain pada pasien pengguna obat anti tuberkulosis dan penggunaan obat anti
tuberkulosis pada pasien yang memiliki respon yang lambat terhadap obat anti
tuberkulosis akan dapat menurunkan efektivitas terapi dari obat anti tuberkulosis.
Sehingga dari hal-hal diatas maka perlu dilakukan pemantauan terapi obat
(therapeutics drug monitoring (TDM)) pada pengobatan tuberkulosis (Peloquin,
2002).
Penetapan kadar rifampisin, isoniazid dan pirazinamid dari plasma manusia
dan sediaan tablet dapat dilakukan dengan metode kromatografi cair kinerja
tinggi. Metode kromatografi cair kinerja tinggi mempunyai beberapa keuntungan
dibanding metode analisis lain, diantaranya: kolom dapat digunakan kembali,
memiliki berbagai jenis detektor, waktu analisis umumnya relatif singkat,
ketepatan yang relatif tinggi, ketelitian yang relatif tinggi dan dapat digunakan
untuk menganalisis kebanyakan sebagian besar senyawa kimia (Meyer, 2004).
Upaya untuk mendapatkan hasil analisis kromatografi cair kinerja tinggi
yang baik memerlukan optimasi. Tujuan optimasi metode kromatografi cair
kinerja tinggi adalah untuk memperoleh pemisahan yang lebih baik, analisis yang
lebih cepat, meningkatkan sensitifitas dan menghemat biaya. Optimasi dilakukan
terhadap beberapa variabel, diantaranya: fase gerak (mobile phase), yakni:
perbandingan fase gerak, kecepatan alir fase gerak maupun optimasi terhadap fase
diam (stationary phase) atau kolom. Adapun optimasi yang paling sederhana dan
(Kromidas, 2006). Perubahan perbandingan fase gerak dan laju alir (flow rate)
dapat mempengaruhi waktu analisis, tekanan dan efisiensi kolom (Meyer, 2004;
Ahuja dan Dong, 2005; Snyder, 1979).
Berdasarkan hal tersebut diatas, penulis tertarik untuk melakukan
pengembangan terhadap metode kromatografi cair kinerja tinggi spektrometri
massa yang akan digunakan untuk penetapan kadar campuran rifampisin,
isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet. Penelitian yang
akan dilaksanakan ini akan meliputi optimasi terhadap beberapa parameter dari
metode kromatografi cair kinerja tinggi spektrometri massa yang diharapkan
kondisi optimum yang diperoleh akan dapat digunakan untuk penetapan kadar
campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan
tablet. Optimasi dilakukan terhadap jenis campuran fase gerak, perbandingan fase
gerak, laju alir fase gerak dan suhu oven kolom.
Upaya untuk menguji validitas dari metode ini dilakukan pengujian validasi
yang dilaksanakan dengan beberapa pengujian seperti: uji akurasi dengan
parameter persentase perolehan kembali (recovery percentage (% recovery)), uji
presisi dengan parameter simpangan baku relatif (relative standard deviation
(RSD)), uji spesifitas, uji batas deteksi, uji batas kuantitasi dan uji linearitas
(Rohman, 2009).
1.2 Kerangka Pemikiran Penelitian
Pada penelitian yang akan dilaksanakan ini terdapat dua Variabel (dapat
dilihat pada Gambar 1.1), yaitu:
• Jenis campuran fase gerak.
Optimasi pada berbagai jenis campuran fase gerak, yakni:
o Air destilasi ganda (yang telah dimurnikan, disaring melalui
membran penyaring nitrat selulosa 0,2 µm dan
diawaudarakan/disonikasi selama 30 menit) dan metanol (yang
disaring melalui membran penyaring politetraflouroetilen
o Larutan asam format 0,1% dalam air destilasi ganda yang telah
dimurnikan (setelah dicampur kemudian disaring melalui
membran penyaring
(PTFE) 0,5 µm dan diawaudarakan/disonikasi selama 30 menit).
nitrat selulosa 0,2 µm dan
diawaudarakan/disonikasi selama 30 menit) dan larutan asam
format 0,1% dalam metanol (setelah dicampur kemudian
disaring melalui membran penyaring politetraflouroetilen
o Larutan asam asetat 1% dalam air destilasi ganda yang telah
dimurnikan (setelah dicampur kemudian disaring melalui
membran penyaring
(PTFE) 0,5 µm dan diawaudarakan/disonikasi selama 30 menit).
nitrat selulosa 0,2 µm dan
diawaudarakan/disonikasi selama 30 menit) dan larutan asam
asetat 1% dalam metanol (setelah dicampur kemudian disaring
melalui membran penyaring politetraflouroetilen
• Perbandingan fase gerak.
(PTFE) 0,5 µm
dan diawaudarakan/disonikasi selama 30 menit).
Optimasi pada berbagai perbandingan fase gerak, yakni: 10%:90%,
• Laju alir fase gerak.
Optimasi pada laju alir fase gerak, yakni: 0,3 mL/menit, 0,5 mL/menit
dan 0,7 mL/menit.
• Suhu oven kolom.
Optimasi pada suhu oven kolom, yakni: 30oC, 35oC dan 40o
2. Variabel terikat.
C.
Kromatogram (resolusi, lempeng teoritikal, tinggi setara dengan lempeng
teoritikal, faktor ikutan, faktor asimetri dan waktu tambat).
Gambar 1.1. Skema hubungan antara variabel bebas dan variabel terikat pada
1.3 Perumusan Masalah
1. Apakah metode kromatografi cair kinerja tinggi spektrometri massa dapat
digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan
pirazinamid dari plasma manusia dan sediaan tablet?
2. Apakah kondisi optimum metode kromatografi cair kinerja tinggi
spektrometri massa yang digunakan untuk penetapan kadar campuran
rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan
tablet memenuhi persyaratan uji validasi metode?
3. Apakah kadar sediaan tablet yang mengandung campuran rifampisin,
isoniazid dan pirazinamid yang ditetapkan dengan kondisi optimum metode
kromatografi cair kinerja tinggi spektrometri massa memenuhi persyaratan
Farmakope Amerika Serikat edisi ke-30 (United States Pharmacopoeia)
tahun 2007?
1.4 Hipotesis
1. Metode kromatografi cair kinerja tinggi spektrometri massa dapat
digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan
pirazinamid dari plasma manusia dan sediaan tablet.
2. Kondisi optimum metode kromatografi cair kinerja tinggi spektrometri
massa yang digunakan untuk penetapan kadar campuran rifampisin,
isoniazid dan pirazinamid dari plasma manusia dan sediaan tablet memenuhi
persyaratan uji validasi metode.
3. Kadar sediaan tablet yang beredar di pasaran yang mengandung campuran
optimum metode kromatografi cair kinerja tinggi spektrometri massa
memenuhi persyaratan Farmakope Amerika Serikat edisi ke-30 (United
States Pharmacopoeia) tahun 2007.
1.5 Tujuan Penelitian
1. Melakukan pengembangan metode kromatografi cair kinerja tinggi
spektrometri massa, sehingga dapat digunakan untuk penetapan kadar
campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia dan
sediaan tablet.
2. Melakukan optimasi fase gerak (jenis campuran fase gerak, perbandingan
fase gerak, laju alir fase gerak) sehingga diperoleh kondisi yang optimum
dari metode kromatografi cair kinerja tinggi spektrometri massa yang
digunakan untuk penetapan kadar campuran rifampisin, isoniazid dan
pirazinamid dari plasma manusia dan sediaan tablet.
3. Menentukan validitas kondisi optimum metode kromatografi cair kinerja
tinggi spektrometri massa yang digunakan untuk penetapan kadar campuran
rifampisin, isoniazid dan pirazinamid dari plasma manusia dan sediaan
tablet.
4. Mengetahui kesesuaian kadar sediaan tablet yang beredar di pasaran yang
mengandung campuran rifampisin, isoniazid dan pirazinamid dengan
persyaratan Farmakope Amerika Serikat edisi ke-30 (United States
1.6 Manfaat Penelitian
Diharapkan metode kromatografi cair kinerja tinggi spektrometri massa
dapat digunakan sebagai metode alternatif pada rumah sakit untuk penetapan
kadar campuran rifampisin, isoniazid dan pirazinamid dari plasma manusia secara
simultan. Disamping itu diharapkan metode kromatografi cair kinerja tinggi
spektrometri massa juga dapat digunakan sebagai metode alternatif bagi Badan
Pengawas Obat dan Makanan (BPOM) serta industri obat untuk penetapan kadar
sediaan yang mengandung campuran rifampisin dan/atau isoniazid dan/atau
BAB II
TINJAUAN PUSTAKA
2.1Tuberkulosis
Tuberkulosis merupakan suatu penyakit yang terutama disebabkan oleh
infeksi bakteri Mycobacterium tuberculosis, tetapi juga disebabkan oleh karena
infeksi Mycobacterium bovis atau Mycobacterium africanum. Infeksi awal
biasanya tanpa gejala (asymptomatic) dan lebih dari 95% tubuh manusia memiliki
imunitas. Akan tetapi imunitas tidak cukup kuat untuk melakukan eradikasi
terdahap basil tuberkulosis dan basil ini dapat memberikan peningkatan terhadap
infeksi secara progresif (cepat). Jika infeksi terjadi selama 2 tahun (dihitung
terhadap infeksi awal) maka penyakit tuberkulosis akan muncul. Anak-anak dan
pasien yang memiliki sistem kekebalan yang lemah akan semakin memudahkan
meningkatnya resiko perkembangan basil tuberkulosis. Manifestasi yang sering
dijumpai dari tuberkulosis adalah penyakit paru-paru. Pasien biasanya
menunjukkan gejala batuk, demam, berkeringat dimalam hari dan penurunan berat
badan (Sweetman, 1999).
2.2 Rifampisin, Isoniazid dan Pirazinamid
Tuberkulosis memerlukan pengobatan dengan tiga sampai lima jenis obat
yang berbeda yang diberikan secara bersama-sama (sekaligus), tergantung kepada
kategori pasiennya. Sediaan obat anti tuberkulosis ini dapat diberikan dalam
formulasi obat tunggal (dalam sediaan yang berbeda-beda) atau diberikan dalam
atau lebih obat anti tuberkulosis berada dalam perbandingan tetap (perbandingan
tertentu) dalam formulasi yang sama. Pihak organisasi kesehatan dunia (world
health organization (WHO)) dan perkumpulan internasional yang melawan
penyakit tuberkulosis dan paru-paru (international union against tuberculosis and
lung disease (IUATLD)) menyarankan agar menghindari penggunaan sediaan
obat anti tuberkulosis dalam formulasi obat tunggal (dalam sediaan yang
berbeda-beda) dan menyarankan penggunaan sediaan obat anti tuberkulosis dalam
formulasi kombinasi dosis tetap (fixed dose combination (FDC)) sebagai
pengobatan utama untuk tuberkulosis (WHO, 1999).
Merujuk kepada ketentuan organisasi kesehatan dunia (world health
organization (WHO)), 1999, beberapa latar belakang atau alasan dari penggunaan
sediaan obat anti tuberkulosis dalam formulasi kombinasi dosis tetap (fixed dose
combination (FDC)) adalah:
• Penggunaan obat monoterapi dalam pengobatan tuberkulosis dihindari,
karena beresiko untuk terjadinya resistensi mikobakterium. Dengan
penggunaan sediaan obat anti tuberkulosis dalam formulasi kombinasi dosis
tetap maka resistensi mikobakterium akan dihindari.
• Peresepan dan pemberian obat yang lebih mudah, kepatuhan pasien lebih
meningkat (karena obat berada dalam satu sediaan).
• Distribusi dan manajemen stok obat yang lebih mudah.
• Biaya sediaan obat anti tuberkulosis dalam formulasi kombinasi dosis tetap
adalah sama dan bahkan lebih rendah dari jumlah biaya penggunaan sediaan
obat anti tuberkulosis dalam formulasi obat tunggal (dalam sediaan yang
• Biaya registrasi dan pajak pada beberapa negara cukup tinggi. Sehingga bila
obat anti tuberkulosis berada dalam formulasi kombinasi dosis tetap (dalam
satu sediaan) akan menurunkan biaya.
2.2.1 Rifampisin
Gambar 2.1. Rumus struktur rifampisin.
Nama Kimia : 5, 6, 9, 17, 19, 21-Heksahidroksi-23-metoksi-2, 4, 12, 16, 18, 20,
22-heptametil-8 [N-(4-metil-1-piperazinil) formimidoil]-2,
7-(epoksipentadeka [1, 11, 13] trienimino) nafto [2, 1-b] furan- 1,
11-(2H)-dion-21-asetat.
Sinonim : Rifampicinum, Rifampin, Rivalzadin,
3-[{(4-Metil-1-piperazinil) imino} metil] rifamisin.
Rumus Molekul : C43H58N4O
Berat Molekul : 822,95.
Pemerian : Serbuk hablur, coklat merah.
Kelarutan : Sangat sukar larut dalam air, sukar larut dalam etanol, eter dan
aseton, mudah larut dalam kloroform, larut dalam etil asetat dan
dalam metanol (Depkes RI, 1995; Sweetman, 1999).
2.2.1.1 Penggunaan dan Cara Pemberian
Rifampisin adalah kelompok antimikobakterial dan digunakan untuk
pengobatan berbagai jenis infeksi. Sering digunakan dalam bentuk kombinasi
dengan antibakterial lainnya untuk menghindari resistensi dan untuk pengobatan
tuberkulosis. Penggunaan pada pasien dewasa secara umumnya adalah 600 mg
per hari melalui mulut pada keadaan lambung kosong. Sedangkan pada pasien
anak-anak diberikan dosis 10 mg/kg hingga 20 mg/kg per hari dengan batas
maksimum 600 mg per hari (Sweetman, 1999).
2.2.1.2 Farmakokinetika
Rifampisin segera diabsorbsi dari saluran pencernaan. Konsentrasi
maksimum obat dalam plasma adalah 7 µg/mL sampai 24 µg/mL setelah 2 jam
sampai 4 jam pemberian dosis 600 mg. Hal ini dapat berbeda antara individu yang
satu dengan individu yang lainnya. Rifampisin berada 80% dalam protein plasma.
Waktu paruh rifampisin berkisar antara 2 jam sampai 5 jam, dengan waktu paruh
yang lebih pendek (1 jam sampai 3 jam) pada penggunaan 2 minggu pertama
karena rifampisin menginduksi metabolisme terhadap rifampisin itu sendiri.
Rifampisin secara cepat dimetabolisme di hati menjadi 25-O-deasetilrifampisin.
melalui feses, tetapi siklus enterohepatik tetap berjalan. Sekitar 60% obat
diekskresikan melalui feses sedangkan 30% obat diekskresikan melalui urin,
setengah bagian tersebut diekskresikan dalam waktu 24 jam. Metabolit
formilrifampisin juga diekskresikan melalui urin. Pada pasien gangguan ginjal
waktu paruh rifampisin menjadi lebih panjang dari normalnya (Sweetman, 1999;
Peloquin, 2002).
2.2.1.3 Efek Samping
Efek samping dari penggunaan rifampisin adalah gangguan saluran cerna
(anoreksia, diare, mual dan muntah), gangguan darah (trombositopenia,
eosinofilia, leukopenia dan anemia), gangguan saraf (sakit kepala), udema dan
perubahan warna pada urin, feses, keringat, air liur, dahak, air mata dan cairan
tubuh lainnya menjadi jingga hingga merah (Sweetman, 1999).
2.2.2 Isoniazid
Rumus struktur :
N
N H
NH2 O
Gambar 2.2. Rumus struktur isoniazid.
Nama Kimia : Asam isonikotinat hidrazida.
Sinonim : Isoniazidum, INH, INAH, Isonikotinoilhidrazin,
Rumus Molekul : C6H7N3O
Berat Molekul : 137,14.
.
Pemerian : Hablur putih atau tidak berwarna atau serbuk hablur putih, tidak
berbau, perlahan-lahan dipengaruhi oleh udara dan cahaya.
Kelarutan : Mudah larut dalam air, agak sukar larut dalam etanol, sukar larut
dalam kloroform dan dalam eter, praktis tidak larut dalam
benzena (Depkes RI, 1995; Sweetman, 1999).
2.2.2.1 Penggunaan dan Cara Pemberian
Isoniazid adalah turunan hidrazida dan merupakan obat utama dalam
pengobatan penyakit tuberkulosis. Sering digunakan dalam bentuk kombinasi.
Penggunaan pada pasien dewasa secara umumnya adalah 300 mg per hari melalui
mulut pada keadaan lambung kosong. Sedangkan pada pasien anak-anak
bervariasi, yakni: 5 mg/kg per hari (menurut Organisasi Kesehatan Dunia (World
Health Organization/WHO)), 10 mg/kg per hari (di Inggris (United
Kingdom/UK)) dan 10 mg/kg hingga 15 mg/kg per hari (di Amerika Serikat
(United States of America/USA)) dengan semuanya mencantumkan batas
maksimum 300 mg per hari (Sweetman, 1999).
2.2.2.2 Farmakokinetika
Isoniazid segera diabsorbsi dari saluran pencernaan. Konsentrasi maksimum
obat dalam plasma adalah 3 µg/mL sampai 7 µg/mL setelah 1 jam sampai 2 jam
pemberian dosis 300 mg. Waktu paruh isoniazid berkisar antara 1 jam sampai 6
asetilator yang cepat. Rute metabolik primer adalah asetilasi dari isoniazid
menghasilkan asetilisoniazid oleh N-asetiltransferase yang ditemukan dalam hati
dan usus halus. Asetilisoniazid kemudian dihidrolisis menjadi asam isonikotinat
dan monoasetilhidrazin. Asam isonikotinat berkonjugasi dengan glisin
menghasilkan asam isonikotiurat (isonikotinil glisin), sedangkan
monoasetilhidrazin yang kemudian mengalami asetilasi menjadi diasetilhidrazin.
Beberapa bagian yang tidak dimetabolisme akan mengalami konjugasi
membentuk hidrazon. Metabolit Isoniazid tidak memiliki aktivitas tuberkulostatik.
Pada pasien dengan fungsi ginjal yang normal, lebih dari 75% dari obat
diekskresikan melalui urine selama 24 jam yang terutama sebagai metabolit.
Sejumlah kecil obat yang diekskresikan melalui feses. Isoniazid juga akan
dikeluarkan dari tubuh bila pasien menjalani dialisis (Sweetman, 1999).
2.2.2.3 Efek Samping
Efek samping dari penggunaan isoniazid adalah gangguan hati (mual,
muntah dan lelah), gangguan darah (anemia, agranulositosis, trombositopenia dan
eosinofilia), hipersensesitivitas (eritema) dan efek samping lainnya (konstipasi
2.2.3 Pirazinamid
Rumus struktur :
N N
O
NH2
Gambar 2.3. Rumus struktur pirazinamid.
Nama Kimia : Pirazinkarboksamida.
Sinonim : Pirazinamidum, Asam pirazinoat amida.
Rumus Molekul : C5H5N3O
Berat Molekul : 123,11.
.
Pemerian : Serbuk hablur, putih hingga praktis putih, tidak berbau atau
praktis tidak berbau.
Kelarutan : Agak sukar larut dalam air, sukar larut dalam etanol, dalam eter
dan dalam kloroform (Depkes RI, 1995; Sweetman, 1999).
2.2.3.1 Penggunaan dan Cara Pemberian
Pirazinamid adalah salah satu jenis obat dari terapi tuberkulosis, awal terapi
adalah selama 8 minggu. Pirazinamid biasanya diberikan per hari atau 2 kali
sampai 3 kali seminggu. Penggunaan pada pasien dewasa secara umumnya adalah
maksimum 3 g per hari melalui mulut. Sedangkan pada pasien anak-anak dosis
yang diberikan 35 mg/kg per hari di Amerika Serikat (United States of America
2.2.3.2 Farmakokinetika
Pirazinamid segera diabsorbsi dari saluran pencernaan. Konsentrasi
maksimum obat dalam plasma adalah 33 µg/mL setelah 2 jam pemberian dosis
1,5 g dan 59 µg/mL setelah 2 jam pemberian dosis 3 g. Pirazinamid secara luas
didistribusikan ke cairan tubuh. Waktu paruh pirazinamid berkisar antara 9 jam
sampai 10 jam. Produk metabolisme yang terutama di hati adalah asam pirazinoat,
selanjutnya mengalami hidroksilasi menjadi produk ekskresi asam
5-hidroksipirazinoat. Produk ekskresi ini segera diekskresikan melalui ginjal
terutama oleh filtrasi glomerulus. Sekitar 70% dari obat diekskresikan melalui
urine selama 24 jam dan 4% dalam bentuk tidak berubah yang terutama sebagai
metabolit. Pirazinamid juga akan dikeluarkan dari tubuh bila pasien menjalani
dialisis. Jalur metabolisme yang utama adalah pirazinamid mengalami deaminasi
menjadi asam pirazinoat yang kemudian mengalami hidroksilasi menjadi asam
hidroksipirazinoa, sedangkan jalur metabolisme yang lainnya adalah pirazinamid
mengalami hidroksilasi menjadi hidroksipirazinamid yang kemudian mengalami
deaminasi menjadi asam hidroksipirazinoat (Sweetman, 1999).
2.2.3.3 Efek Samping
Efek samping dari penggunaan pirazinamid adalah gangguan hati
(hepatomegali), gangguan darah (anemia) dan efek samping lainnya (mual,
2.3 Analisis Rifampisin, Isoniazid dan Pirazinamid
Menurut organisasi kesehatan dunia (world health organization (WHO))
tahun 2006, tablet campuran rifampisin, isoniazid dan pirazinamid dapat
ditentukan kadarnya secara kromatografi cair kinerja tinggi. Untuk isoniazid dan
pirazinamid dapat ditentukan kadarnya secara kromatografi cair kinerja tinggi
menggunakan kolom L1 (oktadesil silana yang terikat secara kimiawi pada
partikel mikro keramik) diameter kolom 4,6 mm, panjang kolom 15 cm, diameter
ukuran partikel 5 µm dengan campuran fase gerak, yakni: 50 g amonium asetat
dalam 1000 mL air yang kemudian ditambahkan asam asetat glasial sampai pH 5
(fase gerak A) dan metanol (fase gerak B) dengan perbandingan kedua campuran
94:6 yang laju alir (flow rate) 2 mL/menit dan deteksi dilakukan pada panjang
gelombang 240 nm. Ekstraksi sampel dilakukan dengan menggunakan air. Untuk
rifampisin ditentukan kadarnya secara terpisah secara kromatografi cair kinerja
tinggi menggunakan kolom L1 (oktadesil silana yang terikat secara kimiawi pada
partikel mikro keramik) diameter kolom 4,6 mm, panjang kolom 25 cm, diameter
ukuran partikel 5 µm dengan campuran fase gerak, yakni: dapar fosfat pH 7
(kalium dihidrogen fosfat (0,1 mol/L) yang disesuaikan pH dengan natrium
hidroksida (0,01 mol/L)) (fase gerak A) dan metanol (fase gerak B) dengan
perbandingan kedua campuran 4:6 yang laju alir (flow rate) 1 mL/menit dan
deteksi dilakukan pada panjang gelombang 254 nm. Ekstraksi sampel dilakukan
dengan menggunakan metanol.
Menurut Farmakope Amerika Serikat edisi ketiga puluh (United States
Pharmacopoeia 30th Edition (USP XXX)) tahun 2007, tablet campuran
kromatografi cair kinerja tinggi. Untuk Rifampisin, Isoniazid, Pirazinamid dapat
ditentukan kadarnya secara Kromatografi Cair Kinerja Tinggi menggunakan
kolom L1 (oktadesil silana yang terikat secara kimiawi pada partikel mikro
keramik) diameter kolom 4,6 mm, panjang kolom 25 cm, diameter ukuran partikel
5 µm dengan fase gerak campuran larutan dapar fosfat pH 6,8 dan asetonitril
(96:4) (fase gerak A) dan campuran larutan dapar fosfat pH 6,8 dan asetonitril
(55:45) (fase gerak B) dengan perbandingan kedua campuran yang berubah-ubah
(sistem gradien) (dapat dilihat pada Tabel 2.1) yang laju alir (flow rate) 1,5
mL/menit dan deteksi dilakukan pada panjang gelombang 238 nm. Ekstraksi
sampel dilakukan dengan menggunakan dapar fosfat pH 6,8.
Tabel 2.1. Perubahan perbandingan fase gerak (USP XXX, 2007).
Waktu (menit) Fase Gerak A Fase Gerak B Elusi
0 100 0 setimbang
0-5 100 0 isokratik
5-6 100→0 0→100 gradien linear
6-15 0 100 isokratik
Menurut Dorneanu tahun 2010, campuran rifampisin, isoniazid dan
etambutol dapat ditentukan dengan dapat ditentukan kadarnya secara kromatografi
cair kinerja tinggi fase balik dengan menggunakan kolom Phenomenex Luna
100-5 C18, diameter kolom 4,6 mm, panjang kolom 2100-5 cm, diameter ukuran partikel 100-5
µm dengan fase gerak campuran larutan dapar asetat pH 5 dan metanol (80:20)
(fase gerak A) dan campuran larutan asam oksalat 0,01 M dan asetonitril (30:70)
(fase gerak B) dengan perbandingan kedua campuran fase gerak tersebut yang
berubah-ubah (sistem gradien) (dapat dilihat pada Tabel 2.2) yang laju alir (flow
rate) 1 mL/menit dan deteksi dilakukan pada panjang gelombang 270 nm (untuk
rifampisin) hingga selesai analisis. Perubahan panjang gelombang dilakukan pada
waktu 9 menit hingga 9,1 menit. Analisis untuk setiap sampel memerlukan waktu
30 menit dan untuk menyetimbangkan sistem diperlukan waktu 8 menit. Sampel
diektraksi, dengan cara: sediaan dilarutkan dengan 10 mL metanol dalam labu
tentukur 50 mL, disonikasi selama 10 menit, didinginkan, ditambahkan dengan air
hingga garis tanda dan dikocok. Campuran disaring, dipipet filtrat 5 mL,
dimasukkan kedalam labu tentukur 25 mL, diencerkan dengan air hingga garis
tanda, dikocok dan kemudian sampel dapat dianalisis. Metode divalidasi dengan
beberapa pengujian, antara lain: uji akurasi dengan parameter persentase
perolehan kembali (recovery percentage (% recovery)), uji presisi dengan
parameter simpangan baku relatif (relative standard deviation (RSD)), linearitas,
batas deteksi, batas kuantitasi, rentang, selektivitas dan kekuatan.
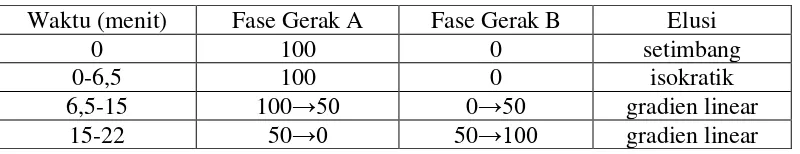
Tabel 2.2. Perubahan perbandingan fase gerak (Dorneanu, 2010).
Waktu (menit) Fase Gerak A Fase Gerak B Elusi
0 100 0 setimbang
0-6,5 100 0 isokratik
6,5-15 100→50 0→50 gradien linear
15-22 50→0 50→100 gradien linear
Menurut Dionex tahun 2010, untuk penetapan kadar rifampisin, isoniazid,
pirazinamid dan etambutol secara kromatografi cair kinerja tinggi fase normal
dengan menggunakan kolom Acclaim Polar Advantage II diameter kolom 4,6
mm, panjang kolom 15 cm, temperatur kolom 35oC, diameter ukuran partikel 3
µm dengan fase gerak campuran 8% asetonitril dalam larutan NaH2PO4 20 mM
(1,5 mL trietilamin per liter) pH 6,8 (fase gerak A) dan 50% asetonitril dalam
larutan NaH2PO4 20 mM (1,5 mL trietilamin per liter) pH 6,8 (fase gerak B)
(sistem gradien) (dapat dilihat pada Tabel 2.3) yang laju alir (flow rate) 1
mL/menit dan deteksi dilakukan pada panjang gelombang 200 nm dan 238 nm.
Sampel diektraksi, dengan cara: satu tablet dimasukkan dalam gelas beker 50 mL,
ditambahkan 5 mL asetonitil dan 20 mL fase gerak A, diaduk, disonikasi hingga
larut, dimasukkan kedalam labu tentukur 100 mL, ditambahkan dengan fase gerak
A hingga garis tanda dan dikocok. Campuran disaring, dipipet filtrat 0,75 mL,
dimasukkan kedalam labu tentukur 10 mL, diencerkan dengan fase gerak A
hingga garis tanda, dikocok dan kemudian sampel dapat dianalisis. Analisis untuk
setiap sampel memerlukan waktu 10,5 menit. Metode divalidasi dengan beberapa
pengujian, antara lain: uji akurasi dengan parameter persentase perolehan kembali
(recovery percentage (% recovery)), uji presisi dengan parameter (simpangan
baku relatif (relative standard deviation (RSD)) dan linearitas.
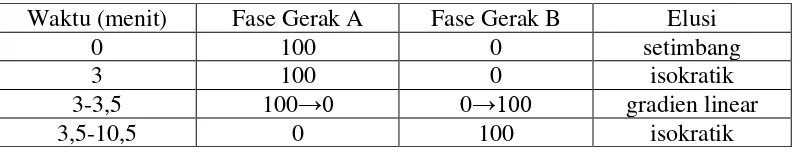
Tabel 2.3. Perubahan perbandingan fase gerak (Dionex, 2010).
Waktu (menit) Fase Gerak A Fase Gerak B Elusi
0 100 0 setimbang
3 100 0 isokratik
3-3,5 100→0 0→100 gradien linear
3,5-10,5 0 100 isokratik
Menurut Song dan kawan-kawan tahun 2007, rifampisin, isoniazid,
pirazinamid, etambutol dan dua metabolit utamanya (yakni: asetilisoniazid dan
25-desasetilrifampisin) dapat ditentukan kadarnya dari dalam darah untuk
monitoring terapi obat secara kromatografi cair kinerja tinggi tandem spektrometri
massa (KCKT/SM/SM) menggunakan kolom Hydrosphere C18, diameter kolom
3 mm, panjang kolom 5 cm, diameter ukuran partikel 3 µm dengan fase gerak
campuran asam format 0,3% dalam metanol (fase gerak A) dan asam format 0,3%