PYRROLIDONE (PVP) SEBAGAI PENGIKAT DAN PENGARUHNYA TERHADAP KADAR CD4 DALAM DARAH
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
Disusun oleh :
NAILUL HANA 106102003383
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
NAMA : NAILUL HANA NIM : 106102003383
JUDUL : FORMULASI TABLET HISAP EKSTRAK ETANOL GAMBIR (Uncaria gambir Roxb) DENGAN VARIASI
KONSENTRASI POLYVINYLPIRROLIDONE (PVP)
SEBAGAI PENGIKAT DAN PENGARUHNYA TERHADAP KADAR CD4 DALAM DARAH
Disetujui Oleh:
Pembimbing I Pembimbing II
Drs. Yanis Musdja, M.Sc, Apt Farida Sulistiawati, M.Si, Apt
NIP: 195601061985101001 NIP: 150377443
Mengetahui
Kepala Program Studi Farmasi UIN Syarif Hidayatullah Jakarta
FORMULASI TABLET HISAP EKSTRAK ETANOL GAMBIR (Uncaria gambir Roxb) DENGAN VARIASI KONSENTRASI POLYVINYL PYRROLIDONE (PVP) SEBAGAI PENGIKAT DAN PENGARUHNYA
TERHADAP KADAR CD4 DALAM DARAH
Telah disetujui, diperiksa dan dipertahankan dihadapan tim penguji oleh
Nailul Hana NIM: 106102003383
Menyetujui,
Pembimbing:
1. Pembimbing I Drs. M. Yanis Musdja, M.Sc, Apt. ...
2. Pembimbing II Farida Sulistiawati, M.Si, Apt. ...
Penguji:
1. Ketua Penguji Drs. M. Yanis Musdja, M.Sc, Apt. ...
2. Anggota Penguji I Eka Putri, M.Si, Apt. ...
3. Anggota Penguji II Azrifitria, M.Si.Apt. ...
4. Anggota Penguji III Zilhadia, M.Si, Apt. ...
Mengetahui,
Dekan Fakultas Kedokteran Dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta
Prof. Dr. (hc). dr. M.K. Tadjudin, Sp. And
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI BENAR-BENAR HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN
SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA LAIN.
Jakarta, Agustus 2010
FORMULASI TABLET HISAP EKSTRAK ETANOL GAMBIR (Uncaria gambir Roxb) DENGAN VARIASI KONSENTRASI POLYVINYLPIRROLIDONE (PVP) SEBAGAI PENGIKAT DAN
PENGARUHNYA TERHADAP KADAR CD4 DALAM DARAH
Telah dilakukan penelitian aktivitas imunomodulator ekstrak gambir (Uncaria gambir Roxb) secara in-vivo. Gambir digunakan sebagai bahan obat karena kandungan katekin dan tannin yang dapat berfungsi sebagai imunomodulator. Pada penelitian ini dilakukan pengembangan sediaan dalam bentuk tablet hisap, selanjutnya dilakukan pengukuran kadar CD4 dalam darah. Ekstrak gambir diformulasi menjadi tablet hisap dengan pengikat PVP, dilanjutkan dengan uji mutu fisik tablet hisap, uji hedonic, dan uji CD4 dalam darah panelis. Hasil evaluasi yang ditinjau dari mutu fisik tablet hisap menunjukkan bahwa dengan adanya peningkatan konsentrasi PVP, maka semakin meningkat pula mutu fisik tablet yang dihasilkan. Formula C dengan konsentrasi PVP sebesar 10% memiliki mutu fisik tablet lebih baik dibandingkan kedua formula lainnya, dengan nilai kekerasan 16,9 kg/cm2, waktu hancur 35,67 menit dan merupakan formula yang paling disukai oleh panelis dalam uji kesukaan terhadap rasa dan aroma tablet. Uji statistik terhadap %CD4 dan jumlah mutlak CD4 panelis yang mengkonsumsi tablet hisap selama 5 hari berturut-turut menunjukkan tidak adanya perbedaan bermakna (p>0,05)antara data sebelum dan sesudah perlakuan.
LOZENGE FORMULATION OF ETHANOL 70% UNCARIA GAMBIR ROXB EXTRACT WITH VARIOUS CONCENTRATION OF
POLYVINYLPIRROLIDONE (PVP) AS THE BINDING AGENT AND TO RATE THE INFLUENCE OF CD4 IN BLOOD
Research of immunomodulatory of ethanol 70% Uncaria gambir Roxb extract has been investigated in-vivo. Gambir is applied as component of drug by contents of catechin and tannin available for functioning as immunomodulator. This research is about preparation in of Lozengeand also measurement of rate CD4 in blood. Gambir extract has been formulated to Lozenge with PVP as binding agent, continued with quality of physical of Lozenge test, hedonic test, and CD4 test in panelist blood. Evaluation result which evaluated from quality of physical of Lozenge indicate that with existence of increasing of concentration of PVP, progressively increase quality of physical of the yielded tablet. Formula C with concentration of 10% PVP have better quality of physical of compared tablet both other formula, with hardness of 16,9 kg/cm2, breakdown time of 35,67 minute and is formula which very taken a fancy by panelist in hedonic test to flavor and smells. Statistical test to% CD4 and absolute counts CD4 panelists consuming Lozenge during 5 day successively show existence that there is no meaning differences (p>0,05) before and after treatment.
kepada Allah SWT. Tak ada satu pun makhluk di dunia ini yang pantas mendapatkan pujian melebihi diri- Nya. Shalawat dan Salam hanyalah untuk Muhammad Rasulullah SAW, seorang manusia luar biasa. Ia senantiasa menjadi inspirasi dan semangat semangat penulis ketika melemah dan membutuhkan dukungan.
Skripsi ini disusun untuk memenuhi salah satu syarat menempuh ujian akhir guna mendapatkan gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta. Adapun judul skripsi ini adalah ” Formulasi Tablet Hisap Ekstrak Etanol Gambir (Uncaria gambir Roxb) Dengan Variasi Konsentrasi Polyvinylpirrolidone (Pvp) Sebagai Pengikat Dan Pengaruhnya Terhadap Kadar CD4 Dalam Darah”.
Selesainya penelitian dan penyusunan skripsi ini tidak lepas dari bantuan berbagai pihak, maka dalam kesempatan ini perkenankanlah penulis menyampaikan ucapan terimakasih yang tulus dan sebesar-besarnya, khusunya kepada:
1. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp.And selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. 2. Drs. M. Yanis Musdja, M.Sc, Apt selaku Pembimbing dan Ketua
Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
3. Ibu Farida Sulistiawati, M.Si, Apt sebagai pembimbing yang senantiasa dan dengan sabar membimbing penulis dalam menyelesaikan penyusunan skripsi ini.
4. Ayahanda, Ibunda, dan keluarga tercinta yang selalu mendoakan dan mendukung penulis baik moril maupun materiil.
5. Ibu/Bapak Dosen dan Staf Akademika Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. 6. Sahabatku Gita Permata Sari, Guna Agashi, dan Fikri Syafrizal untuk
Yunita Haryati untuk kebersamaan yang sangat berharga dalam 4 tahun terakhir ini, semoga ini bukanlah perpisahan untuk kita.
8. Pak Azas “Merck”, Mas Lutfhi “Bintang Toedjoe”, dan Klik “Pharos” atas bantuan bahan-bahan penelitian yang sangat susah didapat.
9. Pak Didik dan Ibu Asih LAFIAL, atas bantuannya dalam proses penelitian
10.Teman-teman seperjuangan Farmasi Teofilin 2006 untuk kekompakan dan canda-tawa yang dihadirkan setiap hari meskipun saat kelas berlangsung.
11.Dan kepada semua pihak yang telah membantu penulis selama ini yang tidak dapat disebutkan namanya satu persatu.
Penulis meyadari bahwa skripsi ini masih jauh dari kesempurnaan karena tiada gading yang tak retak oleh karena itu penulis mengharapkan saran dan kritik yang bersifat membangun untuk lebih menyempurnakan skripsi ini serta memperbaiki kemampuan penulis dalam kesempatan lainnya.
Jakarta, Agustus 2010
LEMBAR PERSETUJUAN ……..……….… ii
LEMBAR PENGESAHAN …..…..……….… iii
LEMBAR PERNYATAAN ….………..… iv
KATA PENGANTAR ………..…..… v
DAFTAR ISI ………...……….... vii
DAFTAR TABEL ……… ix
DAFTAR GAMBAR ………..………... . x
DAFTAR LAMPIRAN ……… xi
ABSTRAK ……….………..… xii
ABSTRACT………...………..… xiii
Bab I Pendahuluan 1.1 Latar Belakang ………... 1
1.2 Perumusan Masalah ……….. 3
1.3 Hipotesa ……… 4
1.4 Tujuan Penelitian ………. 4
1.5 Manfaat Penelitian……….. 4
Bab II Tinjauan Pustaka 2.1 Tanaman Gambir ……….. 5
2.1.1 Klasifikasi Ilmiah ……….……… 5
2.1.2 Nama Daerah ………. 5
2.1.3 Deskripsi Gambir ..………. 6
2.1.4 Kandungan Kimia ……….. 6
2.1.5 Efek Farmakologis ……… 7
2.2 Simplisia ……….. 8
2.3 Ekstrak dan Ekstraksi ………..… 9
2.4 Metode Ekstraksi ……….………... 11
2.5 Tablet Hisap ……….. 13
2.5.1 Definisi Tablet Hisap ……… 13
2.5.2 Bahan Tambahan ……….. 14
2.5.3 Monografi Bahan ……….. 17
2.5.4 Metode Pembuatan……….. 21
2.5.5 Evaluasi Granul .. ………... 23
2.5.6 Evaluasi Tablet……..……….. 25
2.6 Sistem Imun ………...………. 27
2.6.1 Cluster of Differetiation ……….……… 28
2.6.2 Imunomodulator ……….……… 30
2.6.3 Kontrol Pembanding ………….………….……… 32
Bab III Kerangka Konsep ………. 34
4.2.2 Bahan Penelitian ……….. 36
4.3 Prosedur Penelitian ……….. 36
4.3.1 Penyiapan Bahan ……….. 36
4.3.2 Pembuatan Ekstrak Etanol Gambir ……….…….... 37
4.3.3 Pengujian Parameter Spesifik dan Non Spesifik Simplisia dan Ekstrak ……….……….. 37
4.3.4 Identifikasi Serbuk Gambir ……….. 39
4.3.5 Penapisan Fitokimia Serbuk dan Ekstrak Gambir……….... 40
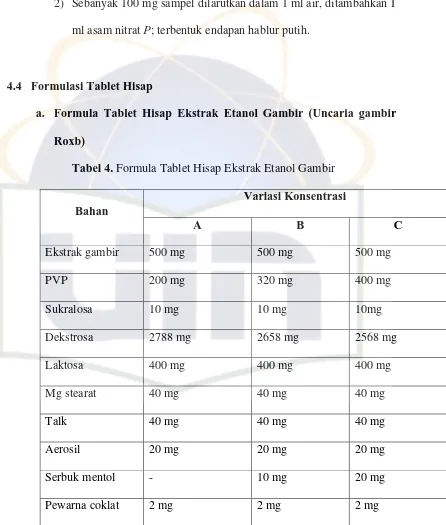
4.4 Formulasi Tablet Hisap ….………... 44
4.4.1 Evaluasi Granul ….……….……….. 45
4.4.2 Evaluasi Tablet ..………….……….. 47
4.5 Uji Kesukaan ………….…….……….. 48
4.6 Uji CD4 ……….…….………. 48
4.7 Analisa Data ………….…….……….. 50
Bab V Hasil Penelitian dan Pembahasan ……… 51
5.1 Hasil Penelitian 5.1.1 Penapisan Fitokimia Gambir ………..………. 51
5.1.2 Karakterisasi Ekstrak ………. . 52
5.1.3 Evaluasi Granul………..………. . 53
5.1.4 Evaluasi Tablet ……….………. . 55
5.1.5 Uji Kesukaan ……….………. . 56
5.1.6 Uji CD4 ……….. . 58
5.2 Pembahasan ………. 60
Bab VI Kesimpulan dan Saran ……… 71
6.1 Kesimpulan ….……….…….………. . 71
6.2 Saran ……….…….……….. 71
Daftar Pustaka ……..……… 72
Tabel I Persentase Kompresibilitas Terhadap Sifat Aliran Granul …..……. 23
Tabel 2 Nilai Sudut Henti Terhadap Sifat Alir……….. 24
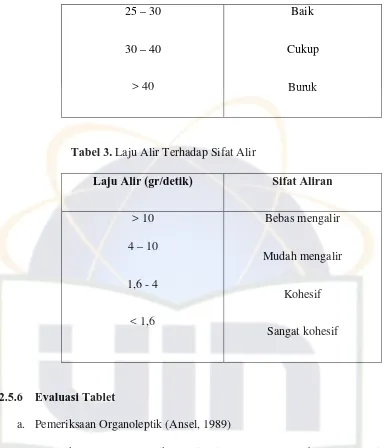
Tabel 3 Laju Alir Terhadap Sifat Alir ……..……… 25
Tabel 4 Formula Tablet Hisap Ekstrak Etanol Gambir…….………….../ 44
Tabel 5 Hasil Penapisan Serbuk & Ekstrak Etanol Gambir……..….……... 51
Tabel 6 Hasil Karakterisasi Ekstrak ……….. 52
Tabel 7 Hasil Evaluasi Granul ……….. 53
Tabel 8 Hasil Uji Distribusi Ukuran Partikel ……… 54
Tabel 9 Hasil Evaluasi Tablet ………..………. 55
Tabel 10 Hasil Uji Kesukaan Terhadap Rasa Tablet ……….. 56
Tabel 11 Hasil Uji Kesukaan Terhadap Aroma Tablet ………... 57
Tabel 12 Persentase CD4 Dalam Limfosit ……… 58
Tabel 13 Jumlah Total CD4…………..………. 59
Tabel 14 Konversi Dosis Hewan Ke HED Berdasarkan BSA …………... 77
Tabel 15 Hasil Pengukuran Kadar Air……….……….. 80
Tabel 16 Hasil Pengukuran Kadar Abu Tidak Larut Asam ………. 80
Tabel 17 Hasil Pengukuran Kadar Abu………..……… 81
Tabel 18 Uji Kadar Air ………..……….. 82
Tabel 19 Uji Kompresibilitas ………..……….. 82
Tabel 20 Uji Sudut Henti ………..……….. 83
Tabel 21 Uji Laju Alir ………..……….. 83
Tabel 22 Uji Distribusi Ukuran Partikel ………..………….... 84
Tabel 23 Uji Friabilitas ………..……….. 85
Tabel 24 Uji Kekerasan Tablet ………..……….. 85
Tabel 25 Uji Keseragaman Ukuran ……..….……….. 86
Tabel 26 Uji Keseragaman Bobot ….…..…..……….. 87
Gambar 1 Hasil Identifikasi Serbuk Gambir….….……..………. 53
Gambar 2 Simplisia Gambir ….………..………. 76
Gambar 3 Sysmex Pouch – 100i... 76
Gambar 4 Rotary Evaporator ... 76
Gambar 5 Alat Pencetak Tablet ... 76
Gambar 6 FACSCalibur ... 76
Lampiran 1 Gambar bahan-bahan dan alat-alat penelitan... 76
Lampiran 2 Rumus perhitungan dosis hewan dan tabel konfersi dosis hewan ke HED berdasarkan BSA ... 77
Lampiran 3 Perhitungan Dosis Tablet ... 78
Lampiran 4 Proses Preparasi Simplisia ……….……….. 79
Lampiran 5 Perhitungan Karakterisasi Ekstrak Gambir ………..… 80
Lampiran 6 Evaluasi Granul ……….. 82
Lampiran 7 Evaluasi Tablet …………..……… 85
Lampiran 8 Uji Kesukaan ……… 89
Lampiran 9 Hasil Uji Statistik ..……… 90
1
1.1. Latar Belakang
Indonesia adalah negara yang kaya akan hasil alam. Berbagai jenis
tanaman berkhasiat tumbuh subur di negara ini. Akan tetapi, pemanfaatan
tanaman tersebut masih relatif rendah jika dibandingkan dengan
negara-negara maju yang kebanyakan hanya memiliki hasil alam sedikit namun
pemanfaatannya dikembangkan secara maksimal.
Tanaman obat tradisional sejak zaman dahulu telah banyak
digunakan untuk pengobatan, baik dalam bentuk serbuk, rajangan, ataupun
dalam bentuk utuhnya. Berbagai bentuk bagian tanaman tersebut dapat
dikatakan sebagai hasil penyarian dari senyawa berkhasiat dengan proses
yang masih sederhana sehingga hasil ekstraksi yang didapat kurang
sempurna dan belum menjamin keseragaman mutu dan hasil yang
diperoleh.
Gambir (Uncaria gambir Roxb) adalah salah satu hasil alam
Indonesia yang terbesar didunia, selain juga banyak ditemukan di
negara-negara lain seperti di Malaysia, India, dan Pakistan. Gambir merupakan
sejenis getah berwarna coklat kehitaman yang dikeringkan, berasal dari
ekstrak remasan daun dan ranting tumbuhan bernama sama (Uncaria
gambir Roxb.). Dalam dunia pedagangan, dikenal beberapa istilah untuk
hasil tanaman gambir seperti kateku kuning, kacu, terra, & cuth dengan
kateku tannin, kuersetin, fluoresine, lender, lemak, dan lilin (Idris, 2007).
Berdasarkan banyaknya senyawa bermanfaat yang terkandung inilah yang
mendorong para peneliti untuk mengeksplorasi penggunaan gambir agar
dapat dimanfaatkan semaksimal mungkin.
Beberapa penelitian terdahulu menunjukkan bahwa tepung gambir
diketahui berguna karena dapat bersifat sebagai fungisida terhadap
golongan jamur imperfect (Fusarium sp) yang menimbulkan bercak daun
pada tanaman Clausena anisata pada konsentrasi 150-200 ppm sehingga
dapat mengurangi pertumbuhan jamur dan penambahan koloni 7,80
mm/hari dan 7,21 mm/hari (Idris, 2007). Ekstrak gambir juga dapat
berkhasiat sebagai imunomodulator, antiseptik oral, dan banyak digunakan
dalam pengobatan diare.
Imunomodulator adalah obat yang dapat mengembalikan dan
memperbaiki sistem imun yang fungsinya terganggu atau untuk menekan
sistem imun yang fungsinya berlebihan (Baratawidjaja, 2009). Sistem
imun sendiri merupakan gabungan sel, molekul, dan jaringan yang
berperan dalam resistensi terhadap berbagai penyakit terutama infeksi.
Virus yang masuk akan berikatan dengan Cluster of Differentiation-4
(CD4) kemudian menggandakan diri dan membunuh sel CD4 tersebut.
Berdasarkan penelitian sebelumnya, diketahui bahwa ekstrak
gambir dapat berkhasiat sebagai imunomodulator secara in-vivo pada dosis
400mg/kg BB (Amalia, 2009). Oleh karena itu perlu dilakukan penelitian
lebih lanjut tentang pengaruh ekstrak gambir sebagai imunomodulator
Dari pemanfaatan bahan berkhasiat dalam tanaman, seiring dengan
perkembangan zaman perlu dilakukan pula pengembangan dan modifikasi
bentuk tanaman berkhasiat yang dikemas menjadi berbagai bentuk sediaan
yang lebih modern dan beragam, seperti pil, tablet, kapsul, krim dan
suppositoria dengan tujuan agar lebih menarik dan juga lebih tepat sasaran
dalam penggunaannya.
Gambir pada umumnya digunakan dengan cara diseduh atau
digunakan untuk menyirih. Cara ini dipandang kurang efektif dalam hal
kestabilan dosis yang diterima tubuh dan rasa yang ditimbulkan sangat
pahit. Oleh karenanya diperlukan suatu pengembangan sediaan untuk
meningkatkan kenyamanan penggunaan dengan dosis yang stabil dalam
tiap pemakaian, misalnya sediaan tablet hisap.
Penelitian ini menggunakan ekstrak air gambir yang dimaserasi
menggunakan pelarut etanol 70% dan diformulasi menjadi sediaan tablet
hisap dengan rasa dan aroma yang dapat diterima oleh masyarakat. Tablet
ini kemudian diuji karakteristiknya berdasarkan persyaratan ketentuan
yang berlaku, serta diujikan terhadap manusia dengan cara diamati
perubahan kadar CD4 tiap-tiap panelis yang mengonsumsi tablet hisap
tersebut pada saat sebelum dan sesudah pemberian tablet hisap.
1.2. Perumusan Masalah
1. Apakah ekstrak tanaman gambir (Uncaria gambir Roxb) dapat dibuat
dalam sediaan tablet hisap dengan menggunakan polyvinylpyrrolidone
2. Apakah formulasi tablet hisap ekstrak etanol gambir dapat
meningkatkan kadar CD4 dalam tubuh ?
1.3. Hipotesa
1. Ekstrak etanol gambir (Uncaria gambir Roxb) dapat diformulasikan
sebagai tablet hisap dengan pengikat PVP
2. Ekstrak etanol gambir (Uncaria gambir Roxb) dapat meningkatkan
kadar CD4 dalam tubuh
1.4. Tujuan
1. Memperoleh suatu formulasi tablet hisap dari ekstrak etanol gambir
(Uncaria gambir Roxb) dengan menggunakan PVP sebagai pengikat
2. Mengetahui pengaruh ekstrak etanol gambir terhadap kadar CD4
dalam tubuh manusia
1.5. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi tentang
suatu formulasi tablet hisap dari ekstrak tanaman gambir dengan bahan
pembantu PVP sebagai pengikat, serta memberikan informasi tentang
pengaruh ekstrak gambir yang dikonsumsi dalam bentuk sediaan tablet
BAB II
TINJAUAN PUSTAKA
2.1. Tanaman Gambir 2.1.1 Klasifikasi Ilmiah
Tanaman gambir diklasifikasikan ke dalam :
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Sub Kelas : Asteridae
Ordo : Rubiales
Familia : Rubiaceae
Genus : Uncaria
Spesies : Uncaria gambir Roxb. (Haryanto, 2009)
2.1.2 Nama Daerah
Gambir (Uncaria gambir Roxb) terdapat hampir di seluruh daerah
di Indonesia. Penyebutannya pun beragam, tergantung dari kebiasaan
daerah masing-masing. Di Sumatra, gambir biasa disebut dengan
gambir/gain (Aceh); kacu (Gayo); sontang (Batak); gambe (Nias &
Minangkabau); pengilom, sepelet (Lampung). Di daerah Jawa, gambir
disebut juga dengan ghambir (Madura). Di Kalimantan, sering dikenal
dengan nama kelare (Dayak) atau abi (Kayan), sedangkan di Sulawesi
disebut dengan gambere (Sangir); gambele (Gorontalo); gambere
tagambe (Bima), gamur (Sumba); gabi (Sawu); gambe (Flores); nggame
(Roti); dan di Maluku dikenal dengan nama gabi (Halmahera); gambe
(Ternate); atau gabi (Flores) (Heyne, 1987)
2.1.3 Deskripsi Gambir
Gambir merupakan salah satu tumbuhan jenis perdu, memanjat,
batang bulat, tidak berambut, memiliki kait di antara dua tangkai daun
yang berhadapan, kecil, pipih, daun penumpu agak besar, bulat. Daun
berhadapan, tipis, bulat telur sampai lanset, ujung meruncing, dasar
tumpul membulat, panjang 8,2 – 14 cm, lebar 7,2 – 8,2 cm, tangkai daun
tidak berambut, panjang 0,5 – 0,8 cm, pertulangan primer pada permukaan
daun sebelah bawah menonjol.
Bunga majemuk, bentuk bongkol, berhadapan di ketiak daun,
tangkai pipih, panjang 0,5 – 4,2 cm, diameter bongkol 4,7 – 5 cm, tabung
mahkota pipih, merah muda atau hijau, berambut halus, kelopak bunga
pendek, lobus mahkota krem keputihan, daun pelindung tidak berambut,
lanset. Mahkota bunga berbentuk corong, benang sari 5, buah berupa
kapsul, sempit memanjang, terbagi menjadi 2 belahan. Biji banyak, kecil,
halus, berbentuk jarum dan bersayap, panjang 0,4 cm, berwarna kuning
(Haryanto, 2009).
2.1.4 Kandungan Kimia
Gambir mengandung berbagai senyawa fungsional, antara lain zat
(20-30%), catechu merah (3-5%), lendir, lemak, lilin (1-2%), dan
polifenol. Senyawa polifenol dalam gambir yang terutama adalah katekin
(50%). Polifenol alami merupakan metabolit sekunder tanaman tertentu,
termasuk golongan tanin. Tanin adalah senyawa fenolik kompleks yang
memiliki berat molekul 500-3000 (Diah, 2010; Haryanto, 2009).
2.1.5 Efek Farmakologis
a. Secara empiris
Gambir telah lama dipergunakan di kalangan masyarakat luas,
terutama untuk menyirih. Selain itu, gambir banyak digunakan untuk
ramuan berkhasiat, antara lain sebagai obat luka bakar, obat sakit kulit
serta sakit kepala.
b. Secara ilmiah
Beberapa penelitian menyimpulkan bahwa gambir dapat digunakan
sebagai astringen dan hemostatik yang menghambat pertumbuhan
bakteri. Gambir banyak dipakai sebagai penahan rasa sakit, seperti
diare, sakit gigi, gusi bengkak, tersengat lebah atau serangga, suara
parau atau sariawan mulut, tertusuk duri, dan luka luar lainnya. Oleh
sebab itu maka gambir juga digunakan sebagai bahan campuran untuk
menyirih atau menginang bagi sebagian orang (Lucida, 2007; Idris,
2.2. Simplisia
Simplisia adalah bahan alam yang digunakan sebagai obat dan
belum mengalami pengolahan apapun juga, dan kecuali dinyatakan lain,
berupa bahan yang telah dikeringkan. Simplisia dibedakan menjadi tiga
golongan, yaitu simplisia nabati, simplisia hewani, dan simplisia
pelikan/mineral. Simplisia nabati adalah simplisia yang dapat berupa
tanaman utuh, bagian tanaman, eksudat tanaman, atau gabungan antara
ketiganya. Eksudat tanaman adalah isi sel yang secara spontan keluar dari
tanaman atau dengan cara tertentu sengaja dikeluarkan dari selnya.
Eksudat tanaman dapat berupa zat-zat atau bahan-bahan nabati lainnya
yang dengan cara tertentu dipisahkan/diisolasi dari tanamannya. Simplisia
hewani adalah simplisia berupa hewan utuh atau zat-zat berguna yang
dihasilkan oleh hewan dan belum berupa bahan kimia murni. Simplisia
pelikan atau mineral adalah simplisia yang berupa bahan pelikan atau
mineral yang belum diolah dengan cara sederhana dan belum berupa
bahan kimia murni (Depkes RI, 1979).
Simplisia tidak boleh menyimpang bau dan warnanya, tidak boleh
mengandung lendir, atau menunjukkan adanya kerusakan. Sebelum
diserbukkan, simplisia nabati harus dibebaskan dari pasir, debu, atau
pengotoran lain yang berasal dari tanah maupun benda anorganik asing
2.3. Ekstrak dan Ekstraksi
Ekstrak adalah sediaan kering, kental atau cair yang diperoleh
dengan mengekstraksi senyawa aktif dari simplisia nabati atau simplisia
hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir
semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan
sedemikian hingga memenuhi baku yang telah ditetapkan (Depkes RI,
1995). Ekstrak cair adalah sediaan dari simplisia nabati yang mengandung
etanol sebagai pelarut atau sebagai pengawet. (Depkes RI, 2000).
Parameter spesifik ekstrak terdiri dari :
a. Identitas
Parameter identitas ekstrak terdiri dari :
1) Deskripsi tata nama yaitu nama ekstrak (generik, dagang, paten),
nama latin tumbuhan (sistematika botani), dan bagian tumbuhan
yang digunakan.
2) Ekstrak dapat mempunyai senyawa identitas artinya senyawa
tertentu yang menjadi petunjuk spesifik dengan metode tertentu.
b. Organoleptik
Parameter ini mendeskripsikan bentuk, warna, bau, dan rasa.
Parameter non spesifik ekstrak terdiri dari:
a. Susut pengeringan
Susut pengeringan adalah pengukuran sisa zat setelah pengeringan
pada temperatur 105oC selama 30 menit atau sampai berat konstan,
yang dinyatakan sebagai nilai persen (%). Tujuannya untuk
yang hilang pada proses pengeringan. Nilai untuk susut pengeringan
jika tidak dinyatakan lain adalah kurang dari 10%.
b. Kadar air
Kadar air adalah pengukuran kandungan air yang berada di dalam
bahan. Tujuannya untuk memberikan batasan maksimal (rentang)
tentang besarnya kandungan air di dalam bahan. Nilai untuk kadar air
sesuai dengan yang tertera dalam monografi.
c. Kadar abu
Untuk penentuan kadar abu, bahan dipanaskan pada temperatur dimana
senyawa organik dan turunannya terdestruksi dan menguap sehingga
hanya tersisa unsur mineral dan anorganik. Tujuannya adalah untuk
memberikan gambaran tentang kandungan mineral internal dan
eksternal yang berasal dari proses awal sampai terbentuknya ekstrak.
Nilai untuk kadar abu sesuai dengan yang tertera dalam monografi
(Depkes RI, 2000).
d. Kadar abu yang tidak larut asam
Kadar abu yang tidak larut asam adalah jumlah benda anorganik asing
dalam ekstrak dinyatakan sebagai kadar abu yang tidak larut asam,
dengan persyaratn tidak boleh lebih dari 2%, kecuali jika dinyatakan
lain.
e. Kadar sari larut etanol
Penetapan kadar sari larut etanol dilakukan untuk mengetahui
tidak larut dalam air. Nilai untuk kadar sari larut etanol sesuai dengan
monografinya (Depkes RI, 1995 ).
Pengertian ekstraksi adalah kegiatan penarikan kandungan kimia
yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut
dengan pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia
dapat digolongkan ke dalam golongan minyak atsiri, alkaloid, flavonoid,
dan lain-lain. Struktur kimia yang berbeda-beda akan mempengaruhi
kelarutan serta stabilitas senyawa-senyawa tersebut terhadap pemanasan,
udara, cahaya, logam berat, dan derajat keasaman. Dengan diketahuinya
senyawa aktif yang dikandung simplisia akan mempermudah pemilihan
pelarut dan cara ekstraksi yang tepat.(Depkes RI, 2000).
2.4. Metode Ekstraksi
Metode ekstraksi dengan menggunakan pelarut terdiri dari dua
cara, yaitu cara dingin dan cara panas.
a. Cara dingin
1) Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan
menggunakan pelarut dengan beberapa kali pengocokan atau
pengadukan pada temperatur ruang (kamar). Maserasi kinetik
berarti dilakukan pengadukan yang kontinu (terus-menerus),
sedangkan remaserasi berarti dilakukan pengulangan penambahan
pelarut setelah dilakukan penyaringan maserat pertama dan
2) Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna (exhaustive extraction) yang umumnya dilakukan pada
temperatur ruang.
b. Cara panas
1) Refluks
Refluks adalah ekstraksi dengan pelarut sampai pada temperatur
titik didihnya selama waktu tertentu dan jumlah pelarut terbatas
yang relatif konstan dengan adanya pendingin balik. Umumnya
dilakukan pengulangan proses pada residu pertama sampai 3-5 kali
sehingga dapat termasuk proses ekstraksi sempurna.
2) Sokhletasi
Sokhletasi adalah ekstraksi menggunakan pelarut yang selalu baru
yang umumnya dilakukan dengan alat khusus sehingga terjadi
ekstraksi berkelanjutan dengan jumlah pelarut yang relatif konstan
dengan adanya pendingin balik.
3) Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinyu)
pada temperatur yang lebih tinggi dari temperatur ruangan, secara
umum dilakukan pada temperatur 40o-50oC.
4) Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas
air (bejana infus tercelup dalan penangas air mendidih), temperatur
5) Dekok
Dekok adalah infus ada waktu yang lebih lama (≥30oC) dan
temperatur sampai titik didih air (Depkes RI, 2002).
2.5. Tablet Hisap
2.5.1 Definisi Tablet Hisap
Tablet hisap adalah suatu sediaan padat yang mengandung satu
atau lebih bahan obat, umumnya dengan bahan dasar beraroma dan manis,
yang dapat melarut atau hancur perlahan-lahan di dalam mulut (Depkes
RI, 1995). Tablet ini biasanya dimaksudkan untuk memberikan efek lokal
pada mulut atau kerongkongan dan umumnya digunakan untuk mengobati
sakit tenggorokan atau untuk mengurangi batuk pada influenza, dan dapat
juga dimaksudkan untuk diabsorpsi secara sistemik setelah ditelan. Jenis
tablet ini dirancang agar tidak hancur di dalam rongga mulut tetapi melarut
atau terkikis secara perlahan-lahan dalam waktu 30 menit atau kurang.
(Lachman, 1994)
Berbeda dengan tablet biasa, pada tablet hisap tidak digunakan
bahan penghancur, dan bahan yang digunakan sebagian besar adalah
bahan-bahan yang larut air. Tablet hisap cenderung menggunakan banyak
pemanis (50% atau lebih dari berat tablet keseluruhan) seperti sukrosa,
laktosa, manitol, sorbitol, dan sebagainya. Selain itu diameter tablet hisap
umumnya lebih besar yaitu >18 mm. Tablet hisap yang baik memiliki
kekerasan sebesar 10-20 kg/cm2 (Gatiningsih, 2008; Lachman, 1994;
2.5.2 Bahan Tambahan
Bahan tambahan atau bahan pembantu tabletasi dapat diartikan
sebagai zat-zat yang memungkinkan suatu obat atau bahan obat yang
memiliki beberapa sifat khusus untuk dibuat menjadi suatu sediaan yang
cocok satu sama lain yang dapat memperbaiki sediaan obat, dengan
mempertimbangkan efek obat, kinerja obat, organoleptis, sifat kimia obat,
dan kemungkinan pengembangan jenis sediaan lain.
Adapun zat-zat tambahan dalam sediaan tablet meliputi :
a. Bahan pengisi
Bahan pengisi diperlukan sebagai pemenuhan kecukupan massa tablet,
dan berfungsi untuk memperbaiki daya kohesi sehingga dapat dikempa
atau untuk memacu aliran. Di samping sifatnya harus netral secara
kimia dan fisiologis, bahan pengisi juga sebaiknya memiliki sifat dapat
dicerna dengan mudah. Adapun contoh bahan pengisi yang umum
digunakan antara lain laktosa, pati, kalsium fosfat dibasa, dan
mikrokristalin selulosa (Depkes, 1995; Voight, 1994)
b. Bahan pengikat
Bahan pengikat adalah bahan tambahan yang diperlukan untuk
memberikan daya adhesi pada massa serbuk sewaktu granulasi dan
memberikan sifat kohesif yang telah ada pada bahan pengisi sehingga
dapat membentuk struktur tablet yang kompak setelah pencetakan dan
meningkatkan daya tahan tablet, oleh karena itu bahan pengikat
menjamin penyatuan beberapa partikel serbuk dalam sebuah butiran
akan dicetak dalam bentuk kering, cairan, atau larutan, tergantung pada
metode pembuatan tablet (Depkes, 1995)
c. Bahan pelincir
Bahan pelincir dapat memenuhi berbagai fungsi yang berbeda,
sehingga banyak dikelompokkan menjadi bahan pengatur aliran
(glidant), bahan pelincir (lubricant) dan bahan pemisah hasil cetakan
(antiadherent). (Voight, 1994)
Bahan pengatur aliran atau glidant berfungsi untuk memperbaiki daya
luncur dan daya gulir bahan yang akan dicetak, karena itu menjamin
terjadinya keteraturan aliran dari corong pengisi ke dalam lubang
cetakan. Glidan juga berfungsi untuk mengurangi penyimpangan
massa, memperkecil gesekan sesama partikel, dan meningkatkan
ketepatan takaran tablet. Contoh zat yang dapat digunakan sebagai
glidan yaitu talk, kalsium/magnesium stearat, asam stearat, PEG, pati,
dan aerosil.
Bahan pelincir atau lubricant berfungsi untuk mengurangi gesekan
logam (stempel di dalam lubang ruang cetak) dan gesekan tablet
dengan logam, serta memudahkan pengeluaran tablet dari mesin
pencetak. Pada umumnya lubrikan bersifat hidrofobik sehingga
cenderung menurunkan kecepatan disintegrasi dan disolusi tablet. Oleh
karena itu kadar lubrikan yang berlebihan harus dihindarkan. Contoh
lubrikan antara lain talk, kalsium atau magnesium stearat, asam stearat,
Bahan pemisah hasil cetakan (antiadherent) adalah bahan yang
berfungsi untuk mencegah lekatnya bahan yang dikempa pada
permukaan stempel atas. Contoh bahan ini adalah talk, amilum maydis,
Cab-O-Sil, natrium lauril sulfat, kalsium/magnesium stearat.
d. Adsorben (Voight, 1994)
Adsorben adalah bahan yang dimaksudkan untuk melindungi zat aktif
atau bahan berkhasiat dari pengaruh kelembaban, membantu
meningkatkan homogenitas campuran, menghindari lembab akibat
reaksi antara bahan dalam sediaan tablet. Yang termasuk bahan ini
misalnya aerosil, avicel, Mg oksida, Mg karbonat, laktosa, bentonit,
dan kaolin
e. Pemanis
Pemanis adalah bahan yang digunakan untuk menutupi atau
memperbaiki rasa tidak enak dari bahan lain dalam sediaan, misalnya
sukrosa, manitol, sorbitol
f. Pengharum
Pengharum adalah bahan yang digunakan untuk menutupi aroma tidak
enak dari bahan lain dalam sediaan dan menutupinya dengan aroma
2.5.3 Monografi Bahan
a. Ekstrak Gambir
Berupa ekstrak etanol gambir (Uncaria gambir Roxb) yang telah
dikeringkan dengan kadar air rata-rata 1,7%. Kandungan utama ekstrak
ini adalah katekin dan tanin.
Katekin Tanin
b. Polyvinylpyrrolidone (PVP)
Sinonim : kollidon, plasdone, povidone, 1-vinyl-2-pyrrolidinone
polymer, polyvidone, poly[1-(2-oxo-1-pyrrolidinyl)ethylene]
Rumus Molekul : (C6H9NO)n
Rumus Bangun :
Bobot molekul : 2500 – 3.000.000
Pemerian : serbuk putih atau krem putih, berbau atau hampir tidak
berbau, bersifat higroskopis, inert
Kelarutan : larut dalam asam, dalam kloroform, dalam etanol, dalam
keton, dalam metanol, dan dalam air. Praktis tidak larut dalam
hidrokarbon dan dalam minyak mineral
Konsentrasi : 0,5 - 5% (Wade, 1994; Lachman, 1994)
c. Sukralosa
Sukralosa memiliki tingkat kemanisan relatif sebesar 600 kali tingkat
kemanisan sukrosa dengan tanpa nilai kalori.
Sinonim : Sukralosa adalah triklorodisakarida yaitu 1,6-Dichloro- 1,6-
dideoxy-D-fructofuranosyl-4-chloro-4-deoxy-α-D-galactopyranoside
atau 4,1,6- trichlorogalactosucrose
Rumus kimia : C12H19Cl3O8
Rumus bangun :
Pemerian : kristal berwarna putih; tidak berbau; mudah larut dalam air,
metanol dan alkohol; sedikit larut dalam etil asetat, serta berasa manis
tanpa purna rasa yang tidak diinginkan.
Sukralosa merupakan bahan tambahan pangan yang aman untuk
dikonsumsi manusia dengan nilai Acceptable Daily Intake (ADI) 10-15
mg/kg berat badan. Codex Alimwntarius Commission (CAC) mengatur
maksimum penggunaan sukralosa pada berbagai produk pangan
berkisar antara 120-5000 mg/kg produk (Anonim, 2007)
d. Dekstrosa
Sinonim : glukosa, d-glukosa, gula jagung, Caridex,
Pemerian : serbuk hablur atau serbuk granul putih, hablur tidak
berwarna, tidak berbau, rasa manis.
Kelarutan : mudah larut dalam air, sangat mudah larut dalam air
mendidih, larut dalam etanol mendidih, sukar larut dalam etanol.
Berat molekul : 198,17
Rumus kimia : C6H12O6.H20
Rumus bangun :
Kegunaan : pengisi, pemanis (Wade, 1994)
e. Laktosa
Pemerian : serbuk hablur, keras, putih atau putih krem, tidak berbau,
rasa agak manis. Stabil di udara, tetapi mudah menyerap bau
Kelarutan : larut dalam 6 bagian air, larut dalam 1 bagian air mendidih,
sukar larut dalam etanol (95%) P, praktis tidak larut dalam kloroform P
dan dalam eter P
Sinonim : o-β-d-galactopyranosyl-(1-4)-α-d-glucopyranose anhydrous
Rumus Molekul : C12H22O11.H2O
Kegunaan : pengisi pada tablet
Konsentrasi : 65-85% (Wade, 1994; Depkes, 1995)
f. Magnesium stearat
Mg stearat merupakan senyawa magnesium dengan campuran
asam-asam organik padat yang diperoleh dari lemak, terutama terdiri dari
magnesium stearat dan magnesium palmitat dalam berbagai
perbandinan. Mengandung setara dengan tidak kurang dari 6,8% dan
tidak lebih dari 8,3% MgO
Sinonim : asam oktadekanoat, garam magnesium
Pemerian : serbuk halus, putih dan voluminus, tidak berasa, bau lemah
khas, mudah melekat di kulit, bebas dari butiran
Kelarutan : tidak larut dalam air, dalam etanol, dan dalam eter
Rumus Kimia : Mg(C18H35O2)2
Kegunaan : pengisi, lubrikan
g. Talkum
Talk adalah magnesium silikat hidrat alam, kadang-kadang
mengandung sedikit alumunium silikat
Sinonim : Magsil Osmanthus, Magsil Star
Pemerian : serbuk hablur, sangat halus dan licin, mudah melekat pada
kulit,bebas dari butiran, berwarna putih atau putih kelabu
Rumus molekul : Mg4(Si2O5)4(OH)4
Kelarutan : tidak larut dalam hampir semua pelarut
Kegunaan : lubrikan, pengisi, diluent
h. Aerosil
Sinonim : colloidal silicon dioxide, fumed silica, light anhydrous
silicic acid, silicic anhydrides, silicon dioxide fumed, Wacker HDK
Rumus kimia : SiO2
Rumus bangun :
Kegunaan : aerosol, adsorben, anticaking agent, disintegran, peningkat
viskositas, glidant (0,1 – 0,5 %) (Wade, 1994).
2.5.4 Metode Pembuatan
Ada beberapa metode dalam pembuatan tablet, namun yang relatif
lebih sering digunakan adalah metode granulasi basah, granulasi kering,
dan metode cetak langsung (Depkes, 1995). Pemilihan metode pembuatan
tablet hisap tergantung dari sifat bahan aktif, oleh karena itu kestabilan
fisikokimia dari bahan aktif menjadi pertimbangan utama dalam tahap
awal formulasi sediaan tablet.
Pada granulasi basah, tujuan utama proses ini adalah untuk
meningkatkan sifat alir, mengurangi porositas bahan, memudahkan
kompresi, menjaga keseragaman pencampuran massa tablet, mengurangi
debu, meningkatkan pembasahan tablet, serta meningkatkan waktu
disolusi (Ansel, 1989)
Granulasi kering dilakukan dengan cara menekan massa serbuk
[image:34.595.113.513.133.549.2]baik, kemudian digiling dan diayak hingga diperoleh granul dengan
ukuran pertikel yang diinginkan. Metode ini digunakan pada keadaan di
mana dosis efektif bahan obat terlalu tinggi untuk cetak langsung dan
bahan obatnya peka terhadap pemanasan dan kelembaban sehingga tidak
dapat diproses secara granulasi basah. Metode ini juga digunakan
khususnya untuk bahan-bahan yang tidak stabil dengan adanya air,
misalnya asetosal (Ansel, 1989).
Metode pembuatan tablet dengan cara cetak langsung adalah
pencetakan bahan obat atau campuran bahan obat-obatan pembantu
berbentuk serbuk tanpa proses pengolahan awal. Oleh karena itu, metode
ini dinilai sangat memuaskan dimana kebutuhan akan kerja relatif lebih
rendah sehingga lebih ekonomis daripada pencetakan dengan metode
granulasi. Selain ekonomis, laju pelepasan bahan aktif dari sediaan tablet
cetak langsung umumnya lebih cepat karena pada saat hancur, bahan aktif
akan langsung dibebaskan dari massa tablet dalam bentuk partikel bebas
karena tidak berada dalam granul (Ansel, 1989)
Keuntungan utama dari proses cetak langsung adalah bahwa bahan
obat yang peka lembab, panas, dan stabilitasnya terganggu akibat operasi
granulasi, akan dapat dibuat menjadi tablet. Meskipun demikian, hanya
sedikit bahan obat yang mampu dikomprimasikan secara langsung tanpa
pengolahan awal dan tanpa penambahan bahan pembantu. Sifat fisik
masing-masing bahan menjadi hal kritis, karena sedikit perubahan dapat
mempengaruhi sifat alir dan kempa sehingga menjadi tidak sesuai lagi
2.5.5 Evaluasi Granul
a. Uji Kadar Air (Voight, 1994)
Evaluasi kadar air digunakan untuk mencegah lembab dari serbuk
yang dapat mempercepat pertumbuhan mikroba dan jamur.
Pengukuran kadar air dilakukan dengan menggunakan alat yang
disebut moisture balance. Syarat kadar air yang baik adalah 2 – 5 %
b. Kompresibilitas (Aulton, 1988; Voight, 1994)
Uji kompresibilitas dilakukan dengan alat yang disebut bulk density.
Persen kompresibilitas dapat dihitung dengan menggunakan rumus :
% kompresibilitas = (BJ mampat – BJ Bulk) x 100%
BJ mampat
Syarat % kompresibilitas yang baik adalah 5 – 15 % menurut tabel
[image:36.595.113.513.139.769.2]berikut :
Tabel 1. Persentase Kompresibilitas Terhadap Sifat Aliran Granul
% Kompresibilitas Sifat Aliran
5-15
12-16
18-21
23-35
35-38
>40
Sangat baik
Baik
Cukup Baik
Buruk
Sangat Buruk
c. Distribusi Ukuran Partikel (Voight, 1994)
Distribusi ukuran partikel sangat penting untuk memperoleh granul
yang kompak dan tidak mudah hancur. Distribusi ukuran partikel
diperoleh dengan metode pengayakan dengan menggunakan alat yang
disebut sieving analyzer (Voight, 1994). Berat yang tertinggal dalam
ayakan ditimbang untuk diketahui persentasenya, agar dapat diketahui
nilai distribusi ukuran partikel pada tiap ukuran ayakan.
Syarat : distribusi ukuran partikel sisa < 10%
d. Sifat Alir (Aulton, 1988; Lachman, 1994)
Untuk menentukan sifat alir berlaku sudut kemiringan aliran, jika suatu
zat berupa serbuk mengalir bebas dari sebuah corong berbentuk
kerucut. adapun untuk mengukur sudut henti adalah dengan mengukur
tinggi dan diameter kerucut yang dihasilkan, sedangkan untuk
mengukur laju alir adalah dengan menghitung waktu yang dibutuhkan
sejumlah granul untuk dapat habis melewati corong (Voight, 1994).
Syarat sudut henti yang baik adalah <25o dan laju alir yang baik adalah
[image:37.595.111.516.161.528.2]> 10 gram/detik menurut tabel berikut :
Tabel 2. Nilai Sudut Henti Terhadap Sifat Alir
Sudut Henti (o) Sifat Aliran
25 – 30
30 – 40
> 40
Baik
Cukup
[image:38.595.115.500.81.529.2]Buruk
Tabel 3. Laju Alir Terhadap Sifat Alir
Laju Alir (gr/detik) Sifat Aliran
> 10
4 – 10
1,6 - 4
< 1,6
Bebas mengalir
Mudah mengalir
Kohesif
Sangat kohesif
2.5.6 Evaluasi Tablet
a. Pemeriksaan Organoleptik (Ansel, 1989)
Pemeriksaan organoleptik meliputi warna, rasa, bau, penampilan
(mengkilap atau kusam), tekstur permukaan (halus atau kasar), derajad
kecacatan seperti serpihan, dan kontaminasi benda asing (rambut, tetesan
minyak, kotoran). Warna yang tidak seragam dan adanya kecacatan pada
tablet selain dapat menurunkan nilai estetikanya juga dapat menimbulkan
persepsi adanya ketidakseragaman kandungan dan kualitas produk yang
buruk.
Pada tablet yang didesain mengandung sejumlah obat di dalam sejumlah
formula, bobot tablet yang dibuat harus diperiksa secara acak untuk
memastikan bahwa setiap tablet mengandung obat dengan jumlah yang
tepat. Syarat keseragaman bobot menurut Farmakope Indonesia Jilid III
adalah bila bobot rata-rata lebih dari 300 mg, jika ditimbang satu per satu
tidak lebih dari 2 buah tablet yang masing-masing bobotnya menyimpang
5% dari bobot rata-ratanya, dan tidak ada satu pun tablet yang bobotnya
menyimpang lebih dari 10% dari bobot rata-ratanya.
c. Keseragaman Ukuran (Ansel, 1989)
Ukuran tablet meliputi diameter dan ketebalan. Ketebalan inilah yang
berhubungan dengan proses pembuatan tablet, karena harus terkontrol
sampai perbedaan 5% dari nilai rata-rata. Pengontrolan ketebalan tablet
diperlukan agar dapat diterima oleh konsumen dan dapat mempermudah
pengemasan.
d. Friabilitas (Lachman, 1994)
Friabilitas dinyatakan sebagai persentase selisih bobot sebelum dan
susudah pengujian, dibagi dengan bobot mula-mula. Tablet yang baik
memiliki keregasan kurang dari 1%.
e. Kekerasan (Parrot, 1971)
Tablet harus memiliki kekuatan atau kekerasan tertentu agar tahan
terhadap berbagai guncangan mekanik pada saat pembuatan, pengepakan,
dan transportasi. Tablet hisap biasanya memiliki kekerasan lebih tinggi
dibandingkan dengan tablet biasa. Syarat kekerasan tablet hisap menurut
[image:39.595.112.514.275.520.2]f. Waktu Hancur (Lachman, 1994)
Waktu hancur adalah waktu yang dibutuhkan oleh sediaan untuk
melarut/terkikis perlahan-lahan di dalam mulut. Untuk tablet hisap, syarat
waktu hancur untuk tablet hisap adalah terkikis perlahan-lahan dalam
jangka waktu 30 menit atau kurang.
2.5. Sistem Imun
Imunitas adalah resistensi terhadap penyakit terutama penyakit
infeksi. Gabungan sel, molekul dan jaringan yang berperan dalam
resistensi terhadap infeksi disebut sistem imun dan reaksi yang
dikoordinasi sel – sel dan molekul – molekul terhadap mikroba dan bahan
lainnya disebut respon imun (Baratawidjaja et al.., 2009). Respon imun
berperan dalam mengenali dan menghancurkan berbagai zat asing yang
masuk ke dalam tubuh. Respon imun dibagi menjadi dua kategori, yaitu
imunitas bawaan (innate immunity) dan imunitas adaptif (adaptive
immunity) (Kaplan Medical, 2002).
a. Imunitas alamiah
Imunitas alamiah adalah imunitas yang diperoleh tanpa
didahului oleh kontak dengan antigen. Imunitas ini bersifat nonspesifik
yang meliputi pertahanan terhadap berbagai macam agen infeksius,
seperti kulit dan membran mukosa, sel natural killer (NK), fagositosis,
inflamasi dan berbagai macam faktor nonspesifik lainnya.
Imunitas adaptif adalah imunitas yang didapat setelah terjadi
paparan terhadap antigen (seperti agen infeksius) bersifat spesifik dan
diperantarai baik oleh antibodi maupun sel limfoid. Imunitas ini dapat
bersifat pasif atau aktif. Imunitas pasif diperankan oleh antibodi atau
limfosit yang telah dibentuk sebelumnya di dalam tubuh penjamu
(host) lain. Keuntungan utama imunisasi pasif dengan antibodi yang
telah dibentuk sebelumya (siap untuk digunakan) adalah tersedianya
antibodi dalam jumlah banyak secara cepat. Kerugiannya adalah
jangka waktu aksi antibodi yang pendek dan reaksi hipersensitivitas
yang dapat terjadi jika diberikan antibodi (imunoglobulin) dari proses
lain. Sedangkan imunitas aktif diinduksi setelah kontak dengan
antigen. Keuntungan imunitas aktif adalah imunitas bersifat jangka
panjang berdasarkan memori kontak dengan antigen pertama kali dan
kemampuan merespon lebih cepat dan lebih banyak ketika terjadi
kontak berikutnya dengan antigen yang sama. Kerugiannya adalah
waktu imunitas lambat dan membutuhkan kontak dengan antigen lebih
lama atau kontak ulangan (Jawetz et al., 2001).
2.5.1 Cluster of Differentiation
Cluster of Differentiation (CD) adalah istilah untuk molekul
permukaan leukosit yang merupakan epitop dan dapat diidentifikasikan
dengan antibody monoclonal. Sel limfosit yang ada dalam berbagai fase
pematangan dapat dibedakan dari ekspresi molekul membran yang dapat
epitop tunggal antigen. Kelas limfosit dengan fungsi tertentu
mengekspresikan protein permukaan tertentu pula. Molekul permukaan
inilah yang disebut dengan Cluster of Differentiation (CD). Ekspresi
molekul membran sel T seperti CD4, CD8, CD28 dan CD45R berperan
sebagai molekul aksesori dalam fungsi sel T atau dalam transduksi sinyal
(Baratawidjaja et al., 2009).
CD4 adalah bagian dari populasi limfosit T yang disebut sebagai
sel T helper. Cara kerja sel ini adalah sebagai penolong, misalnya
melepaskan suatu senyawa yang mengaktifkan sel-sel lain untuk
mematikan atau mengeliminasi antigen (benda asing). Fungsi utama CD4
dalam imun adalah meregulasi sistem imun agar bekerja dengan baik,
dengan merangsang sistem imun nonspesifik berupa fagosit untuk
kemotaksis dan proses fagositosis benda asing. Peran CD4 dalam sistem
imun spesifik humoral adalah merangsang sel B (Limfosit B) untuk
menghasilkan antibodi dan mengatur produksi antibodi, sedangkan dalam
sistem imun seluler berfungsi dalam mengatur CD8 dan NK untuk
membunuh sel sasaran yang terkena infeksi virus.
CD4 adalah sebuah marker atau penanda yang berada di
permukaan sel-sel darah putih manusia, terutama sel-sel limfosit. CD4
pada orang dengan sistem kekebalan yang menurun menjadi sangat
penting, karena berkurangnya nilai CD4 dalam tubuh manusia
menunjukkan berkurangnya sel-sel darah putih atau limfosit yang
seharusnya berperan dalam memerangi infeksi yang masuk ke tubuh
Analisa CD4 dipengaruhi oleh tiga parameter, yaitu % limfosit, %
CD4, dan jumlah mutlak CD4. Jumlah CD4 absolut adalah jumlah sel
CD4 yang ada dalam sistem kekebalan tubuh. Pada orang dengan sistem
kekebalan yang baik, nilai CD4 berkisar antara 1400-1500. Ukuran CD4
persentase memberi sedikit informasi tambahan pada jumlah CD4 mutlak
dalam peramalan risiko jangka pendek pengembangan penyakit, karenanya
jumlah CD4 mutlak merupakan ukuran status kekebalan yang lebih
penting dan pilihan terbaik dibandingkan dengan CD4 persentase,
misalnya untuk mengambil keputusan pengobatan dalam orang dewasa
terinfeksi HIV.
Faktor-faktor yang mempengaruhi jumlah CD4 antara lain meliputi
perbedaan analisis, perbedaan musim, beberapa penyakit bersamaan, dan
penggunaan kortikosteroid. Di samping itu, terdapat pula beberapa faktor
yang dilaporkan memberikan sedikit pengaruh terhadap jumlah nilai CD4,
yaitu gender, usia (pada orang dewasa), faktor risiko, stres psikologis, stres
fisik, dan kehamilan.
Di lingkungan sekitar sangat banyak infeksi yang beredar, baik
berada dalam udara, makanan ataupun minuman. Namun manusia tidak
setiap saat menjadi sakit, karena CD4 masih bisa berfungsi dengan baik
untuk melawan infeksi ini. Jika CD4 berkurang, mikroorganisme yang
patogen akan dengan mudah masuk ke tubuh kita dan menimbulkan
penyakit pada tubuh manusia (Runggu, 2010).
Imunomodulator adalah obat yang dapat mengembalikan dan
memperbaiki sistem imun yang fungsinya terganggu atau untuk menekan
yang fungsinya berlebihan. Obat golongan imunomodulator bekerja
menurut 3 cara, yaitu melalui:
a. Imunorestorasi
Imunorestorasi ialah suatu cara untuk mengembalikan fungsi sistem
imun yang terganggu dengan memberikan berbagai komponen sistem
imun, seperti: immunoglobulin dalam bentuk Immune Serum Globulin
(ISG), Hyperimmune Serum Globulin (HSG), plasma, plasmapheresis,
leukopheresis, transplantasi sumsum tulang, hati dan timus.
b. Imunostimulasi
Imunostimulasi yang disebut juga imunopotensiasi adalah cara
memperbaiki fungsi sistem imun dengan menggunakan bahan yang
merangsang sistem tersebut. Biological Response Modifier (BRM)
adalah bahan-bahan yang dapat merubah respons imun, biasanya
meningkatkan respon imun.
c. Imunosupresi
Imunosupresi merupakan suatu tindakan untuk menekan respons imun.
Kegunaannya terutama pada transplantasi untuk mencegah reaksi
penolakan dan pada berbagai penyakit inflamasi yang menimbulkan
kerusakan atau gejala sistemik, seperti autoimun atau autoinflamasi
Imunorestorasi dan imunostimulasi disebut imunopotensiasi atau
up regulation, sedangkan imunosupresi disebut down regulation.
Untuk mencapai hasil yang diinginkan, suatu imunomodulator
harus memenuhi beberapa syarat. Pertama, zat tersebut harus dapat
memodifikasi respon imun pejamu bukan hanya berefek pada
mikroorganisme saja. Kedua, zat tersebut harus mempunyai efek samping
minimal dan bebas dari efek berbahaya. Imunomodulator yang baik juga
harus bebas dari efek sensitisasi bila zat yang digunakan bersifat alergenik
dan bebas dari efek inhibisi sistem imun pada pemberian jangka panjang
atau berulang (Kresno, 2001).
2.5.3 Kontrol Pembanding
IM® mengandung Echinacea purpurea 250 mg, ekstrak Black
eldelberry 400mg, dan Zinc picolinate 5 mg, dikemas dalam sediaan
kaplet . IM® membantu memperbaiki daya tahan tubuh atau respon imun
tubuh, juga digunakan sebagai terapi pendamping untuk infeksi yang akut
dan kronis, terutama untuk infeksi saluran pernafasan & genitalia seperti
kandidiasis dan vaginitis. Echinacea adalah tumbuhan pertama yang
dibuktikan secara ilmiah khasiat stimulasinya terhadap sistem imun.
(Anonim, 2008; Tjay et al., 2002).
Mekanisme Echinaceae yang bekerja dengan cara menginduksi
sitokin, sedangkan Zn picolinate mengaktivasi membran sel imun pada
merupakan kombinasi yang ideal untuk meningkatkan respon imun
terutama pada keadaan infeksi (Anonim, 2006).
Telah terbukti bahwa Echinacea merupakan imunostimulan non
spesifik, dengan kata lain Echinacea tidak mempunyai hubungan antigenik
dengan patogen-patogen spesifik. Hal ini merupakan hasil dari stimulasi
respon imun seluler seperti fagositosis dan pelepasan sitokin serta
faktor-faktor serum lainnya. Fagositosis (proses ingesti atau menghancurkan
mikroorganisme, sel dan partikel) oleh sel-sel pada sistem
retikuloendotelial, telah digunakan sebagai indikator aktifitas
Evaluasi granul : Kompresibilitas, distribusi ukuran pertikel, laju alir, sudut henti, kadar air
Penyiapan simplisia
Ekstrak kental Uji parameter spesifik
Uji parameter non spesifik
Ekstrak kering
Formula tablet hisap : Ekstrak gambir, PVP, Sukralosa, Laktosa, Mg Stearat, Talk, Aerosil
Mixing
Pencetakan tablet Evaluasi tablet :
friabilitas,uji organoleptik, keseragaman bobot, keseragaman kandungan, waktu hancur
Uji kesukaan Uji CD4
Kruskal wallis test T test
BAB III
KERANGKA KERJA KONSEP
Gambir sebagai obat Katekin gambir diketahui
BAB IV
METODOLOGI PENELITIAN
4.1. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Farmaseutika Program
Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam
Negeri Syarif Hidayatullah Jakarta, Laboratorium Farmasi Angkatan Laut
Jakarta, Laboratorium Makmal Terpadu Fakultas Kedokteran Universitas
Indonesia, dan Laboratorium Sediaan Padat Fakultas Farmasi Universitas
Pancasila. Penelitian ini dilakukan dari bulan Mei sampai bulan Agustus
2010.
4.2 Alat dan Bahan 4.2.1 Alat Penelitian
Alat yang digunakan adalah alat pencetak tablet, desikator,
hardness tester, friabilator, moisture content balance, sieving analyzer,
neraca analitik, jangka sorong, rotary evaporator, erlenmeyer, stop watch,
cawan porselen, corong, statif, krus platina, penggiling (blender), batang
pengaduk, kapas steril, oven, vortex, lemari pendingin, Sysmex Pouch
100i, FACSCalibur, serta peralatan steril yang lazim digunakan di
4.2.2 Bahan Penelitian Simplisia
Simplisia yang digunakan adalah bongkahan gambir yang merupakan
ekstrak air daun dan ranting dari tanaman gambir (Uncaria gambir Roxb)
Bahan Kimia dan Pereaksi
Bahan pelarut untuk ekstraksi adalah etanol 70%.
Bahan untuk penapisan fitokimia adalah ammonia (10%, 25%), kloroform,
HCl (1%, 1:10), pereaksi Dragendorff, pereaksi Mayer, aquadest, lempeng
magnesium, HCl pekat, butanol, larutan besi (III) klorida (FeCl3) 1%,
pereaksi Stiasny, NaOH 1 N, eter, asam asetat anhidrat, H2SO4 pekat,
pereaksi Libermann-Burchard, petroleum eter.
Bahan untuk pembuatan tablet hisap adalah polyvinylpyrrolidone,
sukralosa, dekstrosa, laktosa, talkum, Mg stearat, aerosil, kristal mentol,
pewarna coklat.
Bahan untuk uji CD4 adalah reagen BD Tritest CD4, lysing solution
4.3 Prosedur Penelitian
4.3.1 Penyiapan Bahan yang Digunakan
Sampel yang digunakan adalah Gambir (Uncaria gambir Roxb)
yang diambil dari tanaman gambir, yang terdapat di daerah Padang,
Sumatera Barat. Daun dan ranting dikumpulkan dan dibersihkan dari kotoran yang melekat dengan air bersih mengalir, lalu ditiriskan agar
Simplisia yang sudah kering kemudian digiling dan diayak dengan
ayakan untuk mendapatkan serbuk, lalu simplisia disimpan pada wadah
yang kering dan tertutup rapat, serta dalam ruangan yang terlindung dari
cahaya (Depkes RI, 1986)
4.3.2 Pembuatan Ekstrak Etanol Gambir
Pembuatan ekstrak dilakukan dengan metode maserasi. Sebanyak
500 gram serbuk kering gambir (Uncaria gambir Roxb) dimaserasi
dengan pelarut etanol 70% dan dilakukan pengocokan sesekali. Proses
tersebut dilakukan selama 1-2 minggu dimana sekali dalam 2 hari pelarut
diganti dan disaring. Proses tersebut dilakukan hingga filtrat mendekati
tidak berwarna. Semua filtrat digabung, dan diuapkan atau dipekatkan
dengan rotary evaporator pada suhu 40-50°C hingga diperoleh ekstrak
kental. Ekstrak kental dikeringkan dengan oven pada suhu 30- 40ºC
sampai kering. Dihitung hasil rendemen ekstrak dengan rumus:
Bobot ekstrak yang didapat
% Rendemen = x 100%
Bobot serbuk simplisia yang diekstraksi
4.3.3 Pengujian Parameter Spesifik dan Non Spesifik Simplisia dan Ekstrak (Depkes RI, 2000)
1. Parameter spesifik terdiri dari :
c. Identitas
3) Deskripsi tata nama yaitu nama ekstrak (generik, dagang,
paten), nama latin tumbuhan (sistematika botani), dan bagian
tumbuhan yang digunakan.
4) Ekstrak dapat mempunyai senyawa identitas artinya senyawa
tertentu yang menjadi petunjuk spesifik dengan metode
tertentu.
d. Organoleptik
Parameter ini mendeskripsikan bentuk, warna, bau, dan rasa.
2. Parameter non spesifik terdiri dari:
a. Susut Pengeringan dan Kadar Air
Ekstrak atau simplisia ditimbang dengan seksama sebanyak 1 gram
sampai 2 gram dan dimasukkan ke dalam botol timbang dangkal
bertutup yang sebelumnya telah dipanaskan pada suhu 105oC
selama 30 menit dan telah ditara. Sebelum ditimbang, ekstrak
diratakan dalam botol timbang dengan menggoyang-goyangkan
botol, hingga merupakan lapisan setebal lebih kurang 5 mm sampai
10 mm, kemudian dimasukan ke dalam oven, buka tutupnya.
Pengeringan dilakukan pada suhu penetapan yaitu 105oC hingga
diperoleh bobot tetap lalu ditimbang. Sebelum setiap pengeringan,
botol dibiarkan dalam keadaan tertutup mendingin dalam eksikator
hingga suhu kamar.
b. Kadar Abu
Sebanyak lebih kurang 1-2 gram ekstrak atau simplisia yang telah
atau krus silikat yang telah dipijarkan dan ditara. Ekstrak atau
simplisia diratakan kemudian dipijarkan perlahan-lahan hingga
arang habis, didinginkan, dan ditimbang. Jika arang tidak dapat
hilang, ditambahkan air panas, disaring dengan menggunakan
kertas saring bebas abu. Sisa abu dan kertas saring lalu dipijarkan
dalam krus yang sama. Filtrat dimasukkan ke dalam krus,
diuapkan, dipijarkan hingga bobot tetap, ditimbang. Kadar abu
dihitung terhadap berat ekstrak dan dinyatakan dalam % b/b.
c. Kadar abu tidak larut asam: Abu yang diperoleh pada penetapan
kadar abu, didihkan dengan 25 ml HCl encer selama 5 menit,
dikumpulkan bagian yang tidak larut dalam asam, disaring melalui
krus kaca masir atau kertas saring bebas abu, cuci dengan air panas,
dipijarkan hingga bobot tetap dan ditimbang. Dihitung kadar abu
yang tidak larut dalam asam terhadap bahan yang telah dikeringkan
di udara.
4.3.4 Identifikasi Serbuk Gambir
Identifikasi serbuk daun gambir (Anonim,1989):
a. Pada 2 mg serbuk daun gambir ditambahkan 5 tetes asam sulfat P;
terjadi warna coklat merah
b. Pada 2 mg serbuk daun gambir ditambahkan 5 tetes asam sulfat 10 N;
terjadi warna coklat muda
c. Pada 2 mg serbuk daun gambir ditambahkan 5 tetes larutan natrium
d. Pada 2 mg serbuk daun gambir ditambahkan 5 tetes ammonia (25%) P;
terjadi warna coklat merah
e. Pada 2 mg serbuk daun gambir ditambahkan 5 tetes larutan besi (III)
klorida P 5% b/v; terjadi warna coklat kehitaman
4.3.5 Penapisan Fitokimia (Farnsworth, 1966)
a. Identifikasi Golongan Alkaloid
Sebanyak 2 gram sampel ditambahkan dengan 5 ml ammonia 25%,
digerus dalam mortir, kemudian ditambahkan 10 ml kloroform dan
digerus kembali dengan kuat, campuran tersebut disaring dengan
kertas saring. Filtrat berupa larutan organik diambil (sebagai larutan
A), sebagian dari larutan A (10 ml) diekstraksi dengan 10 ml larutan
HCl 1:10 dengan pengocokan dalam tabung reaksi, diambil larutan
bagian atasnya (larutan B). Larutan A diteteskan beberapa tetes pada
kertas saring dan ditetesi dengan pereaksi Dragendorff. Jika terbentuk
warna merah atau jingga pada kertas saring maka hal itu menunjukkan
adanya senyawa golongan alkaloid dalam sampel.
Larutan B dibagi dalam dua tabung reaksi, ditambahkan
masing-masing pereaksi Dragendorff dan Mayer. Jika terbentuk endapan
merah bata dengan pereaksi Dragendorff dan endapan putih dengan
pereaksi Mayer maka hal itu menunjukkan adanya senyawa golongan
b. Identifikasi Golongan Flavonoid
Sebanyak 1 gram sampel ditambahkan 50 ml air panas, dididihkan
selama 5 menit, disaring dengan kertas saring, diperoleh filtrat yang
akan digunakan sebagai larutan percobaan. Ke dalam 5 ml larutan
percobaan (dalam tabung reaksi) ditambahkan serbuk atau lempeng
magnesium secukupnya dan 1 ml HCl pekat, serta 5 ml butanol,
dikocok dengan kuat lalu dibiarkan hingga memisah. Jika terbentuk
warna pada lapisan butanol (lapisan atas) maka hal itu menunjukkan
adanya senyawa golongan flavonoid.
c. Identifikasi Golongan Saponin
Sebanyak 10 ml larutan percobaan yang diperoleh dari percobaan b
(identifikasi golongan flavonoid), dimasukkan ke dalam tabung reaksi
dan dikocok secara vertikal selama 10 detik, kemudian dibiarkan
selama 10 menit. Jika dalam tabung reaksi terbentuk busa yang stabil
dan jika ditambahkan 1 tetes HCl 1% busa tetap stabil maka hal itu
menunjukkan adanya senyawa golongan saponin.
d. Identifikasi Golongan Tanin
Sejumlah 2 gram sampel ditambahkan 100 ml air, dididihkan selama
15 menit lalu didinginkan dan disaring dengan kertas saring, filtrat
yang diperoleh dibagi menjadi dua bagian. Ke dalam filtrat pertama
ditambahkan 10 ml larutan FeCl3 1%, jika terbentuk warna biru tua
atau hijau kehitaman maka hal itu menunjukkan adanya senyawa
Ke dalam filtrat yang kedua ditambahkan 15 ml pereaksi Stiasny
(formaldehid 30% : HCl pekat = 2 : 1), lalu dipanaskan di atas
penangas air sambil digoyang-goyangkan. Jika terbentuk endapan
warna merah muda menunjukkan adanya tanin katekuat. Selanjutnya
endapan disaring, filtrat dijenuhkan dengan serbuk natrium asetat,
ditambahkan beberapa tetes larutan FeCl3 1%, jika terbentuk warna
biru tinta maka menunjukkan adanya tanin galat.
e. Identifikasi Golongan Kuinon
Diambil 5 ml larutan percobaan dari percobaan b (identifikasi
golongan flavonoid), lalu dimasukkan ke dalam tabung reaksi,
ditambahkan beberapa tetes larutan NaOH 1 N. Jika terbentuk warna
merah maka hal itu menunjukkan adanya senyawa golongan kuinon.
f. Identifikasi Golongan Steroid dan Triterpenoid
Sebanyak 1 gram sampel ditambahkan dengan 20 ml eter, dibiarkan
selama 2 jam dalam wadah dengan penutup rapat lalu disaring dan
diambil filtratnya. 5 ml dari filtrat tersebut diuapkan dalam cawan
penguap hingga diperoleh residua tau sisa. Ke dalam residu
ditambahkan 2 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat
(pereaksi Libermann-Burchard). Jika terbentuk warna hijau atau merah
maka hal itu menunjukkan adanya senyawa golongan steroid dan
triterpenoid dalam simplisia tersebut.
g. Identifikasi Golongan Minyak Atsiri
Sejumlah 2 gram sampel dalam tabung reaksi (volume 20 ml),
diberi lapisan kapas yang telah dibasahi dengan air) pada mulut
tabung, dipanaskan selama 10 menit di atas penangas air dan
didinginkan lalu disaring dengan kertas saring. Filtrat yang diperoleh
diuapkan dalam cawan penguap hingga diperoleh residu. Residu
dilarutkan dengan pelarut alkohol sebanyak 5 ml lalu disaring dengan
kertas saring. Filtratnya diuapkan dalam cawan penguap, jika residu
berbau aromatic at