LAMPIRAN A
DATA PENELITIAN
A.1 DATA HASIL DENSITAS (DENSITY)
Tabel A.1 Data Hasil Analisis Densitas (Density)
Run Massa Kitosan (gram) Konsentrasi Etilen Glikol (v/w) Sampel 1 Sampel 2 Sampel 3 Rata-rata
1 - 0,35 0,723 0,929 0,820 0,824
2 1 0,20 0,888 0,829 0,995 0,909
3 1 0,25 0,921 0,841 0,878 0,880
4 1 0,30 0,793 0,704 1,053 0,823
5 1 0,35 0,851 0,739 0,984 0,738
6 1 0,40 0,892 0,847 0,364 0,612
7 2 0,20 0,838 0,949 1,045 0,944
8 2 0,25 0,847 0,977 0,906 0,910
9 2 0,30 0,852 0,784 1,049 0,895
10 2 0,35 0,839 0,869 0,911 0,863
11 2 0,40 0,692 0,839 0,857 0,796
12 3 0,20 0,899 0,959 1,316 1,058
13 3 0,25 0,958 0,892 1,075 0,975
14 3 0,30 0,873 0,952 0,944 0,923
15 3 0,35 0,934 0,895 0,871 0,900
16 3 0,40 0,853 0,834 0,959 0,882
A.2 DATA HASIL KEKUATAN TARIK (TENSILE STRENGTH)
Tabel A.2 Data Hasil Analisis Kekuatan Tarik (Tensile Strength)
Run Massa Kitosan (gram) Konsentrasi Etilen Glikol (v/w) Sampel 1 Sampel 2 Sampel 3 Rata-rata
1 - 0,35 14,414 14,511 11,965 13,630
2 1 0,20 14,422 15,124 15,097 14,881
3 1 0,25 18,324 18,242 18,127 18,231
4 1 0,30 21,412 19,622 19,659 20,396
5 1 0,35 25,956 26,951 26,281 24,123
6 1 0,40 25,952 25,599 23,818 23,284
7 2 0,20 23,425 21,459 24,968 19,077
8 2 0,25 18,953 19,155 19,123 19,097
9 2 0,35 19,959 19,455 17,877 21,477
10 2 0,35 20,415 21,599 22,417 25,775
11 2 0,40 22,957 24,511 23,434 23,634
12 3 0,20 26,146 25,394 25,779 19,250
13 3 0,25 18,527 19,175 20,048 23,363
14 3 0,30 22,585 23,581 23,923 25,146
A.3 DATA HASIL PEMANJANGAN PADA SAAT PUTUS (ELONGATION
AT BREAK)
Tabel A.3 Data Hasil Analisis Pemanjangan Pada Saat Putus (Elongation at Break)
Run Massa Kitosan (gram) Konsentrasi Etilen Glikol (v/w) Sampel 1 Sampel 2 Sampel 3 Rata-rata
1 - 0,35 0,942 0,984 0,996 0,974
2 1 0,20 1,500 1,601 1,519 1,540
3 1 0,25 1,002 0,998 1,321 1,107
4 1 0,30 1,798 1,766 1,710 1,758
5 1 0,35 1,890 1,992 1,977 1,953
6 1 0,40 1,956 1,950 2,091 1,999
7 2 0,20 1,498 1,579 1,183 1,420
8 2 0,25 0,911 0,914 1,214 1,013
9 2 0,30 1,116 1,156 1,211 1,161
10 2 0,35 1,410 1,506 1,587 1,501
11 2 0,40 1,965 1,998 1,839 1,934
12 3 0,20 1,005 1,137 1,440 1,194
13 3 0,25 1,103 0,987 0,688 0,926
14 3 0,30 0,510 0,549 0,672 0,577
15 3 0,35 1,390 1,300 1,345 1,345
16 3 0,40 1,590 1,567 1,436 1,531
A.4 DATA HASIL MODULUS YOUNG
Tabel A.4 Data Hasil Analisis Modulus Young
Run Massa Kitosan (gram) Konsentrasi Etilen Glikol (v/w) Sampel 1 Sampel 2 Sampel 3 Rata-rata
1 - 0,35 15,301 14,747 12,013 13,993
2 1 0,20 9,615 9,447 9,939 9,663
3 1 0,25 18,287 18,279 13,722 16,469
4 1 0,30 11,909 11,111 11,496 11,602
5 1 0,35 13,733 13,530 13,293 12,352
6 1 0,40 13,268 13,128 11,391 11,648
7 2 0,20 15,638 13,590 21,106 13,435
8 2 0,25 20,805 20,957 15,752 18,852
9 2 0,30 17,884 16,830 14,762 18,499
10 2 0,35 14,479 14,342 14,125 17,172
11 2 0,40 11,683 12,268 12,743 12,220
12 3 0,20 26,016 22,334 17,902 16,122
13 3 0,25 16,797 19,428 29,140 25,230
14 3 0,30 44,284 42,953 35,600 43,581
15 3 0,35 18,380 19,638 18,112 21,019
A.5 DATA HASIL PENYERAPAN AIR (ABSORPTION WATER)
Tabel A.5 Data Hasil Analisis Penyerapan Air (Absorption Water)
Run Massa Kitosan (gram) Konsentrasi Etilen Glikol (v/w) Sampel 1 Sampel 2 Sampel 3 Rata-rata
1 - 0,35 52,14 50,95 54,12 53,476
2 1 0,20 58,55 57,51 55,63 57,230
3 1 0,25 58,99 58,02 59,66 58,890
4 1 0,30 61,43 61,59 61,75 61,590
5 1 0,35 61,89 62,53 61,94 62,120
6 1 0,40 64,95 64,53 65,49 64,990
7 2 0,20 56,28 55,87 56,51 56,220
8 2 0,25 56,94 58,29 58,44 57,890
9 2 0,30 60,41 60,73 59,55 60,230
10 2 0,35 61,42 62,40 59,81 61,210
11 2 0,40 62,78 62,94 62,17 62,630
12 3 0,20 48,22 47,84 50,67 48,910
13 3 0,25 51,48 50,29 52,10 51,290
14 3 0,30 51,04 52,23 52,79 52,020
15 3 0,35 52,32 53,45 53,20 52,990
16 3 0,40 54,92 54,42 52,96 54,100
A.6 DATA HASIL ANALISIS BIOPLASTIK DARI PATI BIJI NANGKA
Tabel A.6 Data Hasil Analisis Bioplastik dari Pati Biji Nangka
Run Massa Kitosan (gram) Konsentrasi Etilen Glikol (v/w) Densitas (gram/cm3 ) Tensile Strengt h (MPa) Elongatio n at Break
(%) Modulu s Young (MPa) Absorption Water (%)
1 - 0,35 0,898 13,630 0,574 13,993 53,476
2 1 0,20 0,909 14,881 1,540 9,663 57,230
3 1 0,25 0,880 18,231 1,107 16,469 58,890
4 1 0,30 0,823 20,396 1,758 11,602 61,590
5 1 0,35 0,738 24,123 1,953 12,352 62,120
6 1 0,40 0,612 23,284 1,999 11,648 64,990
7 2 0,20 0,944 19,077 1,420 13,435 56,220
8 2 0,25 0,910 19,097 1,013 18,852 57,890
9 2 0,30 0,895 21,477 1,161 18,499 60,230
10 2 0,35 0,863 25,775 1,501 17,172 61,210
11 2 0,40 0,796 23,634 1,934 12,220 62,630
12 3 0,20 1,058 19,250 1,194 16,122 48,910
13 3 0,25 0,975 23,363 0,926 25,230 51,290
14 3 0,30 0,923 25,146 0,577 43,581 52,020
15 3 0,35 0,900 28,271 1,345 21,019 52,990
A.7 DATA HASIL ANALISA GUGUS FUNGSI MENGGUNAKAN FTIR
Tabel A.7 Data Hasil Analisa Gugus Fungsi Menggunakan FTIR
Komponen Frekuensi (cm-1) [67]
Bilangan
Gelombang (cm-1) Tipe Vibrasi Ikatan
Pati Biji Nangka
400-3200 3336,85 Alkohol (H-bonded) -H
000-2850 2935,66 Alkana (stretch) -H
900-2800 2819,93 Aldehida -H
270-1940 2063,83 en, Ketena, Isosianat C=Y
680-1630 1639,49 Amida =O
640-1550 1570,06 a dan Amida Primer dan
Sekunder (bend)
-H
375-1300 1342,46 , Sulfonamides, sulfones, =O
300-1000 1246,02
1010,70
Ester
Ester
-O
-O
000-650 929,69 na (out of plane bend) -H
856,39 na (out of plane bend) -H
759,95
705,95
na (out of plane bend)
na (out of plane bend)
-H
-H
785-540 574,79 Klorida -X
Kitosan
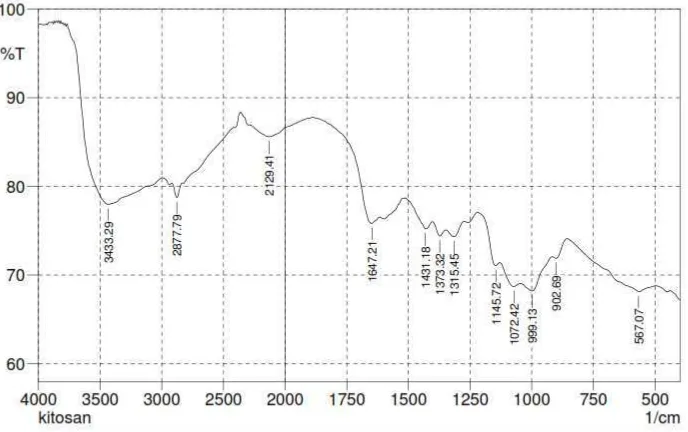
650-3200 3433,29 Ikatan hidrogen -H
000-2850
270-1940
680-1630
2877,79 Alkana (stretch) -H
2129,41 en, Ketena, Isosianat C=Y
1647,21 Amida =O
350-1000 1315,45 Amina -N
300-1000
000-650
1145,72 Eter, Ester -O
1006,84 Eter, Ester -O
999,13
902,69
na (out of plane bend)
na (out of plane bend)
-H
-H
785-540 567,07 Klorida -X
Bioplasik dari pati
Biji Nangka
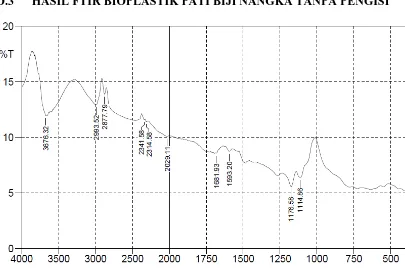
650-3600 3676,32 Alkohol (free) -H
000-2850 2993,52 Alkana (stretch) -H
tanpa Kitosan
270-1940 2029,11 en, Ketena, Isosianat C=Y
680-1630 1681,93 Amida =O
1593,20 Aromatik =C
300-1000 1176,58
1114,86
Ester
Ester
-O
-O
Bioplastik dari Pati
Biji Nangka
dengan Kitosan
650-3600 3649,32 Alkohol (free) -H
000-2850 2993,52 Alkana (stretch) -H
900-2800 2877,79 Aldehida -H
270-1940 2056,12 en, Ketena, Isosianat C=Y
640-1550 1693,20 a dan Amida Primer dan
Sekunder (bend)
-H
475-1600 1597,06 Aromatik =C
300-1000 1172,72
1118,71
Ester
Ester
-O
LAMPIRAN B
CONTOH PERHITUNGAN
Untuk pengujian kekuatan tarik (tensile strength), modulus tarik (tensile modulus),
dan pemanjangan saat putus (elongation at break) telah dihitung oleh Universal
Testing Machine AL-GOTECH 7000 M.
B.1 PERHITUNGAN KADAR AIR PATI BIJI NANGKA
Berikut persamaan untuk menghitung kadar air :
�������� =��������� − �������ℎ��
��������� � 100%
Untuk perhitungan kadar air sampel :
Massa awal pati biji nangka = 3,00 gram
Massa cawan kosong = 35,65 gram
Massa awal pati biji nangka + massa cawan kosong = 38,65 gram
Massa pati biji nangka + cawan setelah pengeringan konstan = 38,23 gram
�������� =��������� − �������ℎ��
��������� � 100% �������� =38,65 ���� −38,23 ����
38,65 ���� � 100%
�������� = 1,086 %
B.2 PERHITUNGAN KADAR ABU PATI BIJI NANGKA
Berikut persamaan untuk menghitung kadar air :
��������= ��������� − �������ℎ��
��������� � 100%
Untuk perhitungan kadar abu sampel :
Massa awal pati biji nangka = 5,00 gram
Massa cawan kosong = 45,34 gram
Massa awal pati biji nangka + massa cawan kosong = 50,34 gram
��������= ��������� − �������ℎ��
��������� � 100%
�������� =50,34 ���� −49,83 ����
50,34 ���� � 100%
�������� = 1,013 %
B.3 PERHITUNGAN ASAM ASETAT 1%
Berikut persamaan untuk menghitung pengenceran :
�1��1 =�2��2
Untuk perhitungan pembuatan asam asetat 1% :
Asam Asetat 1 % = 1.000 ml = 1 liter
Asam Asetat yang digunakan Asam Asetat Glasial dengan kadar 100 %, sehingga :
�1��1 =�2��2 �1� 100 % = 1000 � 1 %
�1 = 10 ��
Jadi, untuk membawa asam asetat 1 % sebanyak 1000 ml dengan cara
mencampurkan 10 ml asam asetat glasial dengan kadar 100 % dan aquadest
sebanyak 990 ml dalam beaker glass 1 L.
B.4 PERHITUNGAN DENSITAS
Berikut persamaan untuk menghitung densitas :
��������= ����� ������
Untuk perhitungan densitas :
Massa bioplastik = 0,70 gram
Panjang bioplastik = 5,00 cm
Lebar bioplastik = 5,00 cm
Tebal bioplastik = 0,20 cm
��������= ����� ������
��������= 0,140 ���� ��3 B.5 PERHITUNGAN PENYERAPAN AIR
Berikut persamaan untuk menghitung penyerapan air :
Penyerapan air=����� ������ ���� −����� ������ ��ℎ��
����� ������ ��ℎ�� � 100%
Untuk perhitungan penyerapan air :
Massa awal bioplastik = 0,119 gram
Massa akhir bioplastik = 0,310 gram
Penyerapan air=����� ������ ���� −����� ������ ��ℎ��
����� ������ ��ℎ�� � 100%
Penyerapan air=0,119 ���� −0,310 ����
0,310 ���� � 100%
Penyerapan air= 61,61 %
Perhitungan diatas dilakukan sebanyak 3 (tiga) kali untuk setiap sampel produk
LAMPIRAN C
DOKUMENTASI PENELITIAN
C.1 PROSES PEMBUATAN LARUTAN KITOSAN
Gambar C.1 Proses Pembuatan Larutan Kitosan
C.2 PROSES PEMBUATAN LARUTAN PATI
C.3 KITOSAN
Gambar C.3 Kitosan
C.4 PATI BIJI NANGKA
C.5 ASAM ASETAT 1 %
Gambar C.5 Asam Asetat 1 %
C.6 ETILEN GLIKOL
C.7 PROSES PEMBUATAN BIOPLASTIK
Gambar C.7 Proses Pembuatan Bioplastik
C.8 PROSES PENCETAKAN BIOPLASTIK
C.9 PRODUK BIOPLASTIK
No Produk Bioplastik Keterangan
1
Bioplastik dengan pengisi kitosan 3 gram volume etilen glikol 0,20
ml/gram
2
Bioplastik dengan pengisi kitosan 3 gram volume etilen glikol 0,25
ml/gram
3
Bioplastik dengan pengisi kitosan 3 gram volume etilen glikol 0,30
ml/gram
4
Bioplastik dengan pengisi kitosan 3 gram volume etilen glikol 0,35
ml/gram
5
Bioplastik dengan pengisi kitosan 3 gram volume etilen glikol 0,40
ml/gram
6
Bioplastik dengan pengisi kitosan 2 gram volume etilen glikol 0,20
7
Bioplastik dengan pengisi kitosan 2 gram volume etilen glikol 0,25
ml/gram
8
Bioplastik dengan pengisi kitosan 2 gram volume etilen glikol 0,30
ml/gram
9
Bioplastik dengan pengisi kitosan 2 gram volume etilen glikol 0,35
ml/gram
10
Bioplastik dengan pengisi kitosan 2 gram volume etilen glikol 0,40
ml/gram
11
Bioplastik dengan pengisi kitosan 1 gram volume etilen glikol 0,20
ml/gram
12
Bioplastik dengan pengisi kitosan 1 gram volume etilen glikol 0,25
ml/gram
13
Bioplastik dengan pengisi kitosan 1 gram volume etilen glikol 0,30
14
Bioplastik dengan pengisi kitosan 1 gram volume etilen glikol 0,35
ml/gram
15
Bioplastik dengan pengisi kitosan 1 gram volume etilen glikol 0,40
ml/gram
16 Bioplastik dengan tanpa pengisi dan
etilen glikol 0,35 ml/gram
Gambar C.9 Produk Bioplastik
C.10 ALAT UJI TARIK (TENSILE STRENGTH)
Gambar C.10 Alat Uji Tarik (Tensile Strength)
Gambar C.11 Alat Uji FTIR (Fourier Transform Infra - Red)
C.12 ALAT UJI SEM (SCANNING ELECTRON MICROSCOPY)
LAMPIRAN D
HASIL PENGUJIAN LAB ANALISIS DAN INSTRUMEN
D.1 HASIL FTIR KITOSAN
Gambar D.1 Hasil FTIR Kitosan
D.2 HASIL FTIR PATI BIJI NANGKA
D.3 HASIL FTIR BIOPLASTIK PATI BIJI NANGKA TANPA PENGISI
Gambar D.3 Hasil FTIR Bioplastik Pati Biji Nangka Tanpa Pengisi
D.4 HASIL FTIR PRODUK BIOPLASTIK DENGAN PENAMBAHAN
KITOSAN DAN PLASTICIZER ETILEN GLIKOL
Gambar D.4 Hasil FTIR Produk Bioplastik dengan Penambahan Kitosan dan
D.5 HASIL UJI PATI, UJI PROTEIN, UJI LEMAK, TEMPERATUR GELATINISASI PATI BIJI NANGKA
DAFTAR PUSTAKA
[1] F.L. Sahwan dkk., “Sistem Pengelolaan Limbah Plastik di Indonesia”, Jurnal
Teknologi Lingkungan, 6(1), (2005) 311 -318.
[2] A. Buzarovska et al., “Eco-challenges of bio-based polymer composites”.
Material, 2, (2009) 911-925.
[3] Sanjaya, I Gede dan Tyas Puspita. “Pengaruh Penambahan Khitosan dan
Plastisizer Gliserol Pada Karakteristik Plastik Biodegradable dari Pati Limbah Kulit Singkong”. Jurusan Teknik Kimia. Institut Teknologi Surabaya, 2011. [4] Selke, Susan E., Handbook of Plastics Technologies: Plastics Recycling An
Biodegradable Plastics. Tersedia di www.digitalengineeringlibrary.com
diunduh 2 Februari 2015.
[5] Anggraini, Fetty, “Aplikasi Plasticizer Gliserol pada Pembuatan Plastik
Biodegradable dari Biji Nangka”, Skripsi, Jurusan Kimia Universitas Negeri
Semarang, 2013.
[6] Badan Pusat Satistik, “Statistik Tanaman Sayuran dan Buah-buahan Semusim Indonesia”, Publikasi, 2088-8392, 2013.
[7] Lu, D. R., C. M. Xiao, S. J. Xu, “Stach-based completely biodegradable polymer materials”, EXPRESS Polymers Letters, Vol.3, No.6, (2009) 366-375.
[8] Saifur Rizal, Sumardi Hadi Sumarlan, Rini Yulianingsih, “Pengaruh Konsentrasi Natrium Bisulfit Dan Suhu Pengeringan Terhadap Sifat Fisik-Kimia Tepung Biji Nangka (Artocarpus heterophyllus)”, Jurnal Bioproses
Komoditas Tropis Vol. 1, No. 2, 2013.
[9] Aguirre, A., Borneo, R., León, A., “Properties of triticale flour protein based films”. LWT – Food Science and Technology 44, 1853–1858, 2011.
[10] Priadi Harahap, Ali, “Pelapisan Melon Menggunakan Film Edibel dari Pati Ubi Kayu dengan Penambahan Sorbitol sebagai Zat Pemlastis”, Skripsi, Fakultas Pertanian Universitas Sumatera Utara, Medan, 2009.
[11] Chrismaya, B., F. Selvy, D. S. Retnowati, “Biofilm dari Pati Nangka dengan Additif Karanginan”, Jurnal Teknologi Kimia dan Industri, Vol. 2, No. 3, (2012) 138-142.
[12] Purbasari dkk., “Bioplastik dari Tepung dan Pati Biji Nangka”, ISBN 978-602-99334-3-7, 2014.
[14] Darni, Yuli dan Herti Utami, “Studi Pembuatan dan Karakteristik Sifat Sorgum dan Hidrofobisitas Bioplastik dari Pati Sorgum”. Jurnal Rekayasa Kimia dan
Lingkungan, Vol.7, No.4, (2010) Hal: 88-93, ISSN 1412-5064.
[15] Pandu Lazuardi, Gilang dan Sari Edi Cahyaningrum, “Pembuatan dan Karakterisasi Bioplastik Berbahan Dasar Kitosan dan Pati Singkong dengan
Plasticizer Gliserol”, UNESA Journal Of Chemistry, Vol. 2, No.3, 2013.
[16] Jones, R. M., Mechanics of Composite Materials. Second Edition. (U.S.A : Taylor & Francis, 1999) hal 49.
[17] Schwartz, M. M., Composite Materials Handbook, (New York : McGraw Hill Book Company, 1984) hal 76.
[18] P Purwanto, Yunasfi., S Purnama, Mashadi, “Karakterisasi Sifat Listrik dan Morfologi Permukaan Bahan Komposit MWCNT-Fe”, Jurnal Ilmiah Daur
Bahan Bakar Nuklir, Vol. 21, No. 1, 2015.
[19] Stevens, E.S., “What Makes Green Plastics Green”, BioCycle, 44(3), 24, 4, 2002.
[20] Koswara, Sutrisno, ”TeknologiPengolahanUmbi-Umbian”. Southeast Asian
Food and Agricultural Science and Technology (SEAFAST) Center, Bogor
Agricultural University, 2013.
[21] Ervan, A, “Sintesis Bioplastik dari Pati Ubi Jalar Menggunakan Penguat Logam ZnO dan Penguat Alami Kitosan, Skripsi, Fakultas Teknik, Universitas Indonesia, 2012.
[22] J.P. Douzals et al., “Microscopic study of starch gelatinization under high hydrostatic pressure”. Agric. Food Chem. . 44, (1996), page:1403–1408.
[23] Menegeristek Bidang Pendayagunaan dan Permasyarakatan Ilmu Pengetahuan dan Teknologi, “ Nangka (Artocarpus heterophyllus Lamk.)”,
[24] Nugraheni, T. C., “Pengaruh Substitusi Tepung Biji Nangka (Artocarpus heterphyllus Lamk.) dengan Penambahan Ekstrak Wortel (Daucus carota L.) terhadap Kualitas Mie Kering Selama Umur impan”, Skripsi, Fakultas Teknobiologi, Universitas Atma Jaya Yogyakarta, Yogyakarta, 2010.
[26] Sari, Kartining Tyas Permana., “Pemanfaatan Tepung Biji Nangka (Artocarpus
Heterophyllus Lamk) Sebagai Substitusi Dalam Pembuatan Kudapan Berbahan
Dasar Tepung Terigu Untuk Pmt Pada Balita (Kajian terhadap Analisis Proksimat serta Sifat Organoleptiknya)”, Skripsi, Jurusan Ilmu Kesehatan Masyarakat Fakultas Ilmu Keolahragaan Universitas Negeri Semarang, 2012.
[27] Yulindo, Yophi., “Migrasi Dioktil Ftalat Dan Etilen Glikol Ke Dalam Struktur Poliuretan Dengan Pemanjang Rantai Diamina Aromatik Dan Pengaruhnya Terhadap Kinerja Material”, Tesis, FMIPA, UI, 2008.
[28] Darni, Yuli, Sri Ismiyati D, Tigor Marbun. “Influence Concentration of Plasticizer and Formulation of Banana Starch – Chitosan to Mechanical Property and Water Uptake of Bioplastic”. International Journal of
Engineering and Science Vol. 1, No.4, 2010.
.
[29] Darni, Yuli, “Penentuan Kondisi Optimum Ukuran Partikel dan Bilangan Reynold pada Sintesis Bioplastik Berbasis Sorgum”, Jurnal Rekayasa Kimia
dan Lingkungan, Vol. 8, No.2, (2011) Hal: 95-103, ISSN 1412-5064.
[30] Widyaningsih, Senny, Dwi Kartika, dan Yuni Tri Nurhayati, ”Pengaruh Penambahan Sorbitol dan Kalsium Karbonat terhadap Karakteristik dan Sifat Beiodegradasi Film dari Pati Kulit Pisang”, Molekul, Vol. 7, No. 1, Hal: 69 – 81, 2012.
[31] ASTM D792-91, Standard Test Method for Density and Specific Gravity (Relative Density) of Plastics by Displacement, The American Society for Testing and Materials, (U.S.A. : Philadelphia 1991).
[32] Ummah, Nathiqoh Al, “Uji Ketahanan Biodegradable Plastic Berbasis Tepung Biji Durian (Durio Zibethinus Murr) Terhadap Air dan Pengukuran Densitasnya”, Skripsi, Jurusan Fisika FMIPA Universitas Negeri Semarang, 2013.
[33] Muthawali, “Kayu Kelapa Sawit”, Universitas Sumatera Utara, 2011.
[34] Surdia, T. dan S. Saito, “Pengetahuan Bahan Teknik”, PT. Pradya Paramita, Jakarta, 1995.
[35] Datsko, J., Material Properties and Manufacturing Processes, (New York : John Wiley and Sons, 1996).
[36] ASTM D 638-00. Standard Test Method for Tensile Properties of Plastics. An American National Standard.
[38] Zhang, V., dan J.H. Han, “Plastikization of Pes Starch Film with Monosaccharide and Polyols”, Jurnal Food ist, Vol. 71, No. 6, Hal: 253-260, 2006.
[39] Ardiansyah, R., “Pemanfaatan Pati Umbi Garut untuk Pembuatan Plastik Biodegradable, Depok: Universitas Indonesia, 2011.
[40] ASTM 570-98. Standard Test Method for Water Absorption of Plastics1. The American Society for Testing and Materials, Philadelphia, U.S.A. 2005.
[41] Thermo, N.C., Introduction to Fourier Transform Infrared Spectrometry, (Madison: Author, 2001).
[42] Fairus dkk., “Pengaruh Konsentrasi HCl dan waktu hidrolisis terhadap Perolehan Glukosa yang Dihasilkan dari Pati Nangka”, Prosiding Seminar
Nasional Teknik Kimia “kejuangan”, 2010.
[43] Standar Nasional Indonesia. Cara Uji Makanan dan Minuman. SNI - 01-2891-1992. Badan Standardisasi Nasional.
[43] Silva, Gervásio Paulo da, Matthias Mack, Jonas Contiero. “Glycerol: A Promising and Abundant Carbon Source for Industrial Microbiology”. Biotechnology advances. Hal 31. 2009, Elsevier.
[44] AOAC. Official Methods of Analisis. “Determination of Moisture Content”. Association of Official Analitycal Chemist. AOAC. Washington DC. USA. 1990.
[45] Jufri, Mahdi dan Rosmala Dewi Akhmad Ridwan Firli, “Studi Kemampuan Pati Biji Durian Sebagai Bahan Pengikat Dalam Tablet Ketoprofen secara Granulasi Basah”, Majalah Ilmu Kefarmasian, vol. III, No.2, Hal: 78-86, ISSN: 1693-9883, 2006.
[46] Rahmawati, Wida, Yovita Asih Kusmawati, Dr, Nita Aryanti. ST, MT., “Karakterisasi Pati Talas (colocasia Esculenta (L.) Schott) Sebagai Alternatif Sumber Pati Industri di Indonesia”. Jurnal Teknologi Kimia dan Industri, Vol. 1 No. 1, (2012) Hal 347-351.
[47] E. Ginting dkk., “Karakteristik Pati Beberapa Varietas Ubi jalar, Didalam : Rahmi Yulianti dan Erliana Ginting, “ Perbedaan Karakteristik Fisik Edible
Film dari Umbi Umbian yang dibuat dengan Penambahan Plasticizer”. Penelitian Pertanian Tanaman Pangan, 31 (2) 2012: hal. 131-136.
[49] E.C.Y. Li-Chan. “Of Protein in Food Systems : an introduction”. The University of British Columbia. Canada. Proteins in Food
Processing.Woodhead Publishing in Food Science and Technology. 2000.
[50] Doutch, James. et al., “Structural Changes During Starch Pasting Using Simultaneous Rapid Visco Analysis ana Small-Angle Neutron Scattering”.
Carbohydrate Polymers 88 (2012) 1061-1071. Elsevier
[51] Kategunya Rengsutthi dan Sanguansri Charoenrein. “Physico-Chemical Properties of Jackfruit Seed Starch (Artocarpus Heterophyllus) and its Application as a Thickener and Stabilizer in Chilli Sauce”. Journal Food
Science and Technology 44 (2011) 1309-1313. Elsevier.
[52] Dimas Damar Adi Krisna. “Pengaruh Regelatinisasi dan Modifikasi Hidrotermal terhadap Sifat Fisik pada Pembuatan Edible Film dari Pati Kacang Merah (Vigna angularis sp)”.Tesis, Program Studi Magister Teknik Kimia Universitas Diponegoro,2011, hal. 17-18.
[53] Didah Nur Faridah, Dedi Fardiaz, Nuri Andarwulan, dan Titi Candra Sunarti, “Karakteristik Sifat Fisikokimia Pati Garut (Maranta arundinaceae)”, Agritech,
Vol.34, No.1, 2014.
[54] Jin-song. Bao, “Accurate Measurement of Pasting Temperature by The Rapid Visco Analyzer: a Case Study Using Rice Flour”. Rice Science. 2008. 15 (1): 69-72. Elsevier
[55] Sondeep Sing et al., “Effect of sowing time on protein quality and starch pasting characteristics in wheat (Triticum aestivum L.) genotypes grown under irrigated and rain-fed conditions”. Food Chemistry 122. 2010. 559–565. Elsevier
[56] Nur Richana dan Titi Chandra Sunarti. “Karakterisasi Sifat Fisikokimia Tepung Umbi dan Tepung Pati dari Umbi Ganyong, Suweg, Ubikelapa dan Gembili”. J.Pascapanen 1(1) (2004): 29-37
[57] Prabowo, Bimo. “Kajian Sifat Fisikokimia Tepung Millet Kuning Dan Tepung Millet Merah”. Skripsi. Program Studi Teknik Hasil Pertanian. Universitas Sebelas Maret. Surakarta 2010.
[58] Fitria Yenda Elpita, Yuli Darni. “Peningkatan Karakteristik Mekanik Dan Fisik Bioplastik Berbahan Dasar Pati Sorgum Dan Serbuk Batang Sorgum’’. Seminar
Nasional Sains & Teknologi VI Lembaga Penelitian dan Pengabdian Universitas Lampung. 2015
[59] Kumar, A.P., Singh, R.P., “Biocomposites of cellulose reinforced starch: improvement of properties by photo-induced crosslinking”, Bioresour.
[60] Khaswar Syamsu, Chilwan Pandji, dan Eva Rosalina Lumbanraja, “Pengaruh Penambahan Polioksietilen-(20)-Sorbitan Monolaurat Pada Karakteristik Bioplastik Poli-Hidroksialkanoat (PHA) Yang Dihasilkan Ralstonia eutropha Pada Substrat Hidrolisat Pati Sagu”, J. Tek. Ind. Pert. Vol. 18(1), (2012) 41-46.
[61] M. Hendra S. Ginting, M. Fauzy Ramadhan Tarigan , Annisa Maharani Singgih. “Effect of Gelatinization Temperature and Chitosan on Mechanical Properties of Bioplastics from Avocado Seed Starch (Persea americana mill) with Plasticizer Glycerol”. The International Journal Of Engineering And Science (IJES). Vol 4. Issue 12. Pages 36-43. 2015. ISSN (e): 2319 – 1813 ISSN (p): 2319 – 1805.
[62] Yao Dou et al., “The Stucture, Tensile Properties and Water Resistance of Hydrolyzed Feather Keratin-Based Bioplastics”, Chinese Journal of Chemical
Engineering. Vol 22. No 7. (2015) Elsevier.
[63] Rinaldi Febrianto Sinaga, Gita Minawarisa Ginting, M. Hendra S Ginting, Rosdanelli Hasibuan. “Pengaruh Penambahan Gliserol Terhadap Sifat Kekuatan Tarik Dan Pemanjangan Saat Putus Bioplastik Dari Pati Umbi Talas’’. Jurnal Teknik Kimia USU, Vol. 3, No. 2. 2014
[64] Ganda Merisiyanto dan Lizda Johar Mawarani. “Pengembangan Plastik
Photobiodegradable Berbahan Dasar Umbi Ubi Jalar”. Jurnal Teknik POMITS
Vol. 2, No. 1, (2013) ISSN: 2337-3539.
[65] Pavia, D.L., Lampman, G.M., and Kriz, G.S., Introduction To Spectroscopy : A
Guide for Students of Organic Chemistry, (Singapore : Brooks/Cole Thomson
BAB III
METODOLOGI PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Kimia Organik, Laboratorium
Operasi Teknik Kimia,Laboratorium Penelitian, dan Laboratorium Proses Industri
Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara,
Medan. Penelitian ini dilakukan selama lebih kurang 6 bulan.
3.2 Bahan dan Peralatan
3.2.1 Bahan
Pada penelitian ini bahan yang digunakan antara lain:
1. Biji buah nangka (Artocarpus Heterophyllus) yang diperoleh dari pasar
Padang Bulan Medan
2. Aquadest yang diperoleh dari toko bahan kimia “Rudang” di Medan
3. Etilen Glikol yang diperoleh dari toko bahan kimia “Rudang” di Medan
4. Asam Asetat (CH3COOH) yang diperoleh dari toko bahan kimia “Rudang”
di Medan
3.2.2 Peralatan
1. Hot plate, thermocouple dan magnetic stirrer
2. Kertas Saring Whatman no. 1
3. Saringan plastik
4. Erlenmeyer
5. Pipet tetes
6. Gelas ukur
7. Corong gelas
8. Beaker glass
9. Magnetic stirrer
10. Desikator
11. Oven listrik
12. Neraca Digital
14. Ayakan 100 mesh
15. Blender
16. Pisau
17. Talenan
18. Cetakan flexiglass 20x20 cm
19.Neraca analitik
3.3 Prosedur Penelitian
Prosedur penelitian dapat dijelaskan sebagai berikut:
3.3.1 Ekstraksi Pati
Pengekstrakan kandungan pati dari biji nangka didasarkan pada metode yang
dilakukan oleh Fairus, dkk (2010) yaitu [42]:
1. Biji nangka sebanyak 100 gram dikupas bagian selubung luar dan kulit
arinya kemudian dibersihkan dengan air bersih.
2. Biji dipotong dengan ukuran lebih kurang 1 cm2 kemudian dihancurkan menggunakan blender dengan bantuan air.
3. Bahan dikeluarkan dari blender dan disaring menggunakan saringan
plastik sampai diperoleh ampas dan cairan filtrat (suspensi pati).
4. Suspensi yang dihasilkan kemudian diendapkan selama 24-48 jam hingga
pati mengendap sempurna.
5. Cairan bagian bawah yang kaya pati kemudian disaring dengan
menggunakan kertas saring Whatman no. 1 hingga didapat pati basah.
6. Endapan yang diperoleh dikeringkan didalam oven dengan suhu 70 oC selama 30 menit.
7. Diperoleh serbuk pati kering, kemudian diayak dengan ayakan 100 mesh
3.3.2 Pembuatan Bioplastik
Pembuatan bioplastik dilakukan berdasarkan metode yang diperoleh dari
Anggarini (2013) dan Dian (2013) yaitu [5][28]:
1. Sejumlah massa pati yang diinginkan ditimbang sebanyak 10 gram.
2. Dibuat larutan pati dengan perbandingan pati : aquades adalah 1 : 20
3. Kemudian dibuat larutan pati dan larutan kitosan sesuai dengan volume
yang telah dihitung pada beaker glass.
4. Beaker glass 500 ml yang berisi larutan pati diletakkan di atas magnetic
stirrer dan diatur temperatur sebesar 88,82 oC selama 25 menit sambil terus diaduk dengan magnetic stirrer berkecepatan 400 rpm
5. Setelah 25 menit ditambahkan etilen glikol dengan variasi 20%, 25%,
30%, 35% dan 40% pada larutan pati, lalu diaduk selama 15 menit.
6. Setelah 15 menit, magnetic stirrer dimatikan.
7. Larutan dituangkan sebanyak 50 ml ke dalam cetakan flexiglass 20x20
cm, kemudian dikeringkan dalam oven pada T = 60 oC selama 24 jam. 8. Setelah dikeringkan, diangkat dan dimasukkan ke dalam desikator selama
24 jam.
9. Kemudian bioplastik dilepas dari cetakannya dan siap dianalisa
3.4. Prosedur Analisa Bioplastik
3.4.1 Analisis Pati
3.4.1.1Kadar Air Dengan Standar AOAC
Adapun prosedur analisis kadar air adalah sebagai berikut [44]:
1. Cawan porselin dikeringkan terlebih dahulu didalam oven pada suhu 105 oC selama 3 jam, lalu didinginkan di dalam desikator selama 30 menit dan ditimbang
sehingga beratnya tetap .
2. Sampel kira – kira ditimbang sebanyak 3 gram dalam cawan .
3. Kemudian dikeringkan dalam oven pada suhu 100 – 105 oC selama 3 jam atau beratnya konstan.
4. Cawan yang berisi sampel dikeringkan dalam desikator lalu ditimbang hingga
beratnya tetap.
��������= ����� ���� −����� ��ℎ��
����� ���� � 100%
3.4.1.2Kadar Abu Dengan Standar AOAC
Adapun prosedur analisis kadar abu adalah sebagai berikut [44]:
2. Cawan yang berisi sampel dipijarkan diatas nyala api pembakar bunsen hingga
tidak berasap lagi .
3. Kemudian dimasukkan kedalam furnace dengan suhu 550 oC selama ± 12 jam. 4. Cawan yang berisi sampel didinginkan dalam desikator lalu ditimbang hingga
beratnya tetap.
�������� =����� ���� −����� ��ℎ��
����� ���� � 100%
3.4.2 Analisis Produk Bioplastik
3.4.2.1Uji Kekuatan Tarik (Tensile Strength) Dengan Standar ASTM D 638
Kekuatan tarik adalah salah satu sifat dasar dari bahan produk bioplastik yang
terpenting dan sering digunakan untuk karakteristik suatu bahan produk bioplastik.
Kekuatan tarik suatu bahan didefenisikan sebagai besarnya beban maksimum (F
maks) yang digunakan untuk memutuskan spesimennya bahan dibagi dengan luas
penampang awal (Ao).
Produk bioplastik dipilih dan dipotong membentuk spesimen untuk pengujian
kekuatan tarik (uji tarik) sesuai dengan standar ASTM D 638. Pengujian kekuatan
tarik dilakukan dengan tensometer terhadap tiap spesimen. Tensometer terlebih
dahulu dikondisikan pada beban 100 kgf dengan kecepatan 500 mm/menit, kemudian
dijepit kuat dengan penjepit yang ada dialat. Mesin dihidupkan dan spesimen akan
tertarik ke atas spesimen diamati sampai putus, dicatat tegangan maksimum dan
regangannya.
3.4.2.2Uji Densitas Dengan Standar ASTM D792-91, 1991
Adapun prosedur analisis densitas adalah sebagai berikut [45]:
1. Film dipotong dengan ukuran 5 cm x 5 cm dan tebal tertentu, kemudian dihitung
volumenya.
2. Kemudian potongan film tersebut ditimbang.
3. Rapat massa (densitas) dari film dapat ditentukan dengan rumus :
�������� = �����
������
3.4.2.3Karakterisasi Fourier Transform Infra-Red (FTIR)
1. Pati biji nangka
2. Kitosan
3. Bioplastik tanpa pengisi kitosan dan plasticizer etilen glikol
4. Bioplastik dengan penambahan pengisi kitosan dan plasticizer etilen glikol
Tujuan dilakukan analisa ini adalah untuk melihat apakah ada atau tidak
terbentuknya gugus baru dalam produk bioplastik dengan pengisi kitosan dan
plasticizer etilen glikol. Analisa Fourier Transform Infra-Red (FTIR) dilakukan di
Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara, Medan.
3.4.2.4Karakterisasi Scanning Electron Microscope (SEM)
Sampel yang akan dianalisa dengan Scanning Electron Microscope (SEM)
yaitu berupa :
1. Pati biji nangka
2. Bioplastik tanpa pengisi kitosan dan plasticizer etilen glikol
3. Bioplastik dengan penambahan pengisi kitosan dan plasticizer etilen glikol
Tujuan dilakukan analisa ini adalah untuk melihat morfologi pati biji nangka,
morfologi penyebaran dengan dan tanpa penambahan pengisi kitosan dan plasticizer
etilen glikol dalam matriks pati biji nangka. Analisa Scanning Electron Microscope
(SEM) dilakukan di Laboratorium Scanning Electron Microscope (SEM), Fakultas
Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara.
3.4.2.5Karakterisasi Temperatur Gelatinisasi
Sampel yang akan dianalisa temperatur gelatinisasinya yaitu berupa :
1. Pati biji nangka
2. Larutan pati biji nangka dengan penambahan asam asetat
3. Larutan pati biji nangka dengan pengisi kitosan tanpa plasticizer etilen glikol
4. Larutan pati biji nangka dengan pengisi kitosan dan plasticizer etilen glikol
Tujuan dilakukan analisa ini adalah untuk melihat temperatur gelatinisasi pati
biji nangka, temperatur gelatinisasi dengan dan tanpa penambahan pengisi kitosan
dan plasticizer etilen glikol dalam matriks pati biji nangka. Analisa Temperatur
Pertanian Universitas Padjajaran. Adapun prosedur karakterisasi temperatur
gelatinisasi sebagai berikut :
1. Isi bak pendingin dengan akuades sampai tanda pada display muncul tanda
bahwa air sudah cukup terisi.
2. Pasang kabel pada stop kontak, nyalakan alat dengan menekan tombol yang
berada di bagian belakang alat, nyalakan juga air pendingin.
3. Atur temperature, time, pump, refrigerate.
4. Jika semua parameter pengaturan sudah sesuai, tekan tombol ON sampai
semua pengaturan posisi on ( perhatikan tanda di display)
5. Pilih menu STD 1 pada menu utama
6. Pasang flashdisk pada alat RVA.
7. Timbang sampel sebanyak 3,5-4 gram (sesuaikan dengan kandungan air
sampel) dan masukan ke canister
8. Tambahkan akuades atau buffer sebanyak 25 gram ( sesuaikan dengan
penimbangan sampel.
9. Simpan canister pada alat dan mulai pengukuran dengan menekan tombol √,
lalu tower sampel pada alat.
10. Alat akan memutar sampel dengan pemanasan pada 50 – 95 0C selama ± 23 menit.
11. Jika sudah selesai, grafik pengukuran bisa di lihat pada display, lalu pilih
option save.
3.4.2.6 Uji Penyerapan Air Dengan Standar ASTM D570-98, 2005
Adapun prosedur analisis penyerapan air adalah sebagai berikut [40]:
1. Dipotong plastik dengan diameter 50,8 mm dan tebal ± 0,18 mm dan ditimbang
berat sampel.
2. Masukkan sampel plastik ke dalam wadah berisi air distilat denngan temperatur
23±1 oC selama 24 jam.
3. Setelah 24 jam, sampel diambil dan dibersihkan dengan menggunakan kain
kering. Penyerapan air dihitung dengan rumus :
Penyerapan air=����� ������ ���� −����� ������ ��ℎ��
����� ������ ��ℎ�� � 100%
3.4.2.6 Uji Densitas Dengan Standar ASTM D792-91, 1991
Adapun prosedur analisis densitas adalah sebagai berikut [31]:
1. Film dipotong dengan ukuran dan tebal tertentu, kemudian dihitung
volume film yang telah dipotong.
2. Kemudian potongan film tersebut ditimbang.
3. Rapat massa (densitas) dari film dapat ditentukan dengan rumus :
3.5 Flowchart Percobaan
[image:33.595.106.514.79.762.2]3.5.1 Flowchart Ekstraksi Pati
Gambar 3.1 Flowchart Ekstraksi Pati
3.5.2 Flowchart Pembuatan Bioplastik
Mulai
Biji nangka dikupas bagian selubung luar dan kulit arinya kemudian dicuci
Biji nangka dipotong dengan ukuran ±1 cm2 dan ditambahkan dengan air kemudian dihancurkan dengan blender
Biji nangka yang telah lumat disaring dan diperas
Mulai
Dibuat larutan pati dengan perbandingan pati : aquades adalah 1 : 20 pada beaker glass 500 ml
Beaker glass 500 ml yang berisi larutan pati diletakkan di atas magnetic stirrer dan diatur temperatur T = 88,82 oC selama 25 menit
Filtrat yang didapat didekantasi selama 24 – 48 jam dan hasil dekantasi lalu disaring dengan kertas Whatman no. 1
Endapan dikeringkan dalam oven pada suhu 50 oC selama ±2 jam
Pati dihaluskan dengan menggunakan ayakan 100 mesh
Selesai
Massa pati ditimbang dengan perbandingan 7;8;dan 9 gram
Gambar 3.2 Flowchart Pembuatan Bioplastik
[image:34.595.177.458.492.716.2]3.5.3 Flowchart Analisa Densitas
Gambar 3.3 Flowchart Analisa Densitas Dimatikan magnetic stirrer setelah 15 menit
Selesai
Dituang kedalam cetakan sebanyak 50 ml
Mulai
Ditimbang film yang sudah dipotong kemudian dihitung dengan rumus analisa densitas Dipotong film dengan ukuran dan tebal tertentu
Dihitung volume film yang telah dipotonng
Selesai
Ditambahkan etilen glikol
kemudian diaduk kembali selama 15 menit
Dikeringkan dalam oven pada T = 60 oC selama 24 jam
Bioplastik dilepas dari cetakannya dan siap dianalisa Diangkat dan dimasukkan dalam desikator selama 24 jam
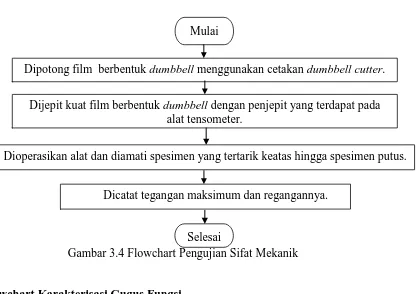
3.5.4 Flowchart Pengujian Sifat Mekanik
Gambar 3.4 Flowchart Pengujian Sifat Mekanik
3.5.5 Flowchart Karakterisasi Gugus Fungsi
Gambar 3.5 Flowchart Karakterisasi Gugus Fungsi Mulai
Dipotong film berbentuk dumbbell menggunakan cetakan dumbbell cutter.
Dijepit kuat film berbentuk dumbbell dengan penjepit yang terdapat pada alat tensometer.
Dioperasikan alat dan diamati spesimen yang tertarik keatas hingga spesimen putus.
Selesai
Mulai
Sampel yang berupa film ditempatkan ke dalam set holder, kemudian dicari spektrum yang sesuai
Hasil yang diperoleh berupa difraktogram hubungan antara bilangan gelombang dengan intensitas
Spektrum FTIR direkam dengan menggunakan spektrometer pada suhu ruang
Selesai
[image:35.595.113.533.108.402.2]3.5.6 Flowchart Analisa Ketahanan Air
Gambar 3.6 Flowchart Uji Ketahanan Air
[image:36.595.123.520.190.704.2]3.5.7 Flowchart Karakterisasi SEM (Scanning Electron Microscope)
Gambar 3.7 Flowchart Karakterisasi Scanning Electron Microscope (SEM) Digunakan timbangan digital, mengukur berat sampel awal (Wo) dengan ukuran
1 x 1 cm
Lalu diisi air aquades kedalam suatu beaker glass sebanyak 5 ml
Mulai
Masukkan sampel bioplastik ke dalam
beaker glass selama 10 detik,
Selesai
Diangkat bioplastik dari mangkok setiap 10 detik dan ditimbang berat sampel (W) dan direndam lagi hingga berat sampel konstan. Lalu dihitung dengan
rumus analisa ketahanan air
Sampel ditempelkan pada set holder dengan perekat ganda
Sampel dilapisi dengan logam emas dalam keadaan vakum Mulai
mpel dimasukkan pada tempatnya di dalam Scanning Electron
Microscope
Selesai
[image:36.595.132.516.438.716.2]BAB IV
HASIL DAN PEMBAHASAN
4.1 HASIL KARAKTERISASI PATI BIJI NANGKA
Berikut ini adalah gambar pati biji nangka (Artocarpus Heterophyllus)
dimana biji nangka yang digunakan dalam penelitian ini diperoleh dari penjual buah
[image:37.595.207.470.261.444.2]pasar Padang Bulan Medan.
Gambar 4.1 Pati Biji Nangka (Artocarpus Heterophyllus)
Berdasarkan 100 gram biji nangka dapat menghasilkan pati biji nangka sebanyak
26,67 gram atau persentase pati sebesar 26,67 %. Gambar 4.1 diatas dapat dilihat
bahwa pati biji nangka yang dihasilkan berwarna putih. Karakterisasi pati dari biji
nangka bertujuan untuk mengetahui persentase komponen yang terkandung di dalam
pati yang dihasilkan, meliputi kadar pati (amilum), kadar amilosa, kadar amilopektin
kadar air, kadar abu, kadar lemak dan kadar protein sehingga diketahui kualitas pati
yang dihasilkan. Karakteristik pati biji nangka dilakukan di Laboratorium Jasa Uji,
Fakultas Teknologi Industri Pertanian, Universitas Padjadjaran, Bandung. Adapun
Tabel 4.1 Hasil Karakterisasi Pati Biji Nangka
Komponen Pati Biji Nangka
Kadar (%) Standar Industri Indonesia (%) [46]
Metode Pengujian
Pati (amilum) 70,22 min 75 SNI 01-2891-1992
- Amilosa 16,39 - -
- Amilopektin 53.83 - -
Air 6,04 maks 14 AOAC
Abu 1,08 maks 1,5 AOAC
Lemak 0,54 - SNI 01-2891-1992
Protein 4,68 - SNI 01-2891-1992
4.1.1Kadar Pati Biji Nangka
Dari hasil penelitian ini, didapat rendemen pati sebesar 26,67 %, dimana dari
100 gram biji nangka dihasilkan pati kering sebanyak 26,67 gram. Karakterisasi
kadar pati menggunakan 5 gram sampel pati biji nangka dan hasil analisa pati biji
nangka diperoleh kadar pati 70,22 %. Kadar pati yang didapat bila dibandingkan
dengan penelitian sebelumnya (Jufri dkk) pada tahun 2006 dengan metode yang
sama lebih tinggi yaitu 68,22 % [45]. Berdasarkan standar mutu pati menurut Standar
Industri Indonesia (SII), kadar pati yang diizinkan adalah minimal 75 % [46]. Jika
dibandingkan dengan kadar pati menurut SII, kadar pati biji nangka sudah mendekati
standar mutu pati menurut SII.
4.1.2Kadar Amilosa dan Amilopektin Pati Biji Nangka
Dari hasil penelitian ini, Karakterisasi kadar amilosa dan amilopektin
menggunakan 100 miligram sampel pati biji nangka dan hasil analisapati biji nangka
diperolehkadar amilosa 16,39% dan kadar amilopektin 53,83 %. Pati terdiri dari dua
fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan
fraksi tidak larut disebut amilopektin. Amilosa memberikan sifat keras sedangkan
amilopektin menyebabkan sifat lengket. Konsentrasi kedua komponen ini nantinya
akan mempengaruhi sifat mekanik dari polimer alami yang terbentuk [21]. Rasio
amilosa dan amilopekti berbeda-beda untuk setiap sumber pati, tetapi umumnya
kandungan amilopektin lebih besar dibandingkan dengan amilosa. Rasio amilosa dan
amilopektin akan berpengaruh pada kemampuan pasta pati dalam membentuk gel,
4.1.3Kadar Air Pati Biji Nangka
Jumlah kadar air dari suatu bahan akan mempengaruhi kualitas daripada bahan
tersebut. Semakin tinggi kadar air dari suatu bahan maka semakin besar pula bahan
tersebut mengalami kerusakan. Hal ini disebabkan oleh pertumbuhan mikroba dan
aktivitas enzim [22]. Kadar air yang diperoleh dari pati biji nangka pada penelitian
ini adalah sebesar 6,04 %. Berdasarkan standar mutu pati menurut SII, kadar air yang
diizinkan adalah maksimal 14 % [47]. Berdasarkan SII, kadar air pati biji nangka
yang diperoleh telah memenuhi standar yang berlaku.
4.1.4Kadar Abu Pati Biji Nangka
Penentuan kadar abu adalah dengan mengoksidasikan semua zat organik pada
suhu yang tinggi, yaitu sekitar 500-600 oC dan kemudian melakukan penimbangan zat yang tertinggal setelah proses pembakaran tersebut [48]. Adapun kadar abu yang
diperoleh dari pati biji nangka adalah sebagai berikut sebesar 1,08 %. Berdasarkan
standar mutu pati menurut SII, kadar abu yang diizinkan adalah maksimal 1,5 %
[46]. Jika dibandingkan dengan kadar abu pati menurut SII, kadar abu pati biji
nangka telah memenuhi.
4.1.5Kadar Protein Pati Biji Nangka
Tujuan dari pengujian kadar protein ialah untuk menentukan persentase
kandungan protein yang dikandung per satuan massa serbuk pati dimana serbuk pati
diperoleh dari hasil ekstraksi biji nangka [49]. Dari hasil penelitian ini, kadar protein
yang diperoleh dari 0,51 gram sampel pati biji nangka dalam 100 gram biji nangka
adalah sebesar 4,68 %.
4.1.6Kadar Lemak Pati Biji Nangka
Tujuan dari pengujian kadar lemak ialah untuk menentukan persentase
kandungan lemak yang terdapat per satuan massa serbuk pati dimana serbuk pati
diperoleh dari hasil ekstraksi biji nangka [49]. Adapun kadar lemak yang diperoleh
dari 2 gram sampel pati biji nangka dalam 100 gram biji nangka adalah sebesar 0,54
4.1.7 Hasil Karakterisasi Profil Gelatinisasi Pati Biji Nangka
Gelatinisasi pati melibatkan granul yang meleleh dalam media larutan dengan
pemanasan. Dalam air, pembengkakan granul meningkat seiring dengan
bertambahnya suhu. Ketika mencapai suhu tertentu butiran larut terganggu oleh
energi yang disediakan, mengakibatkan hilangnya susunan molekuler dan akibatnya
kehilangan kristalinitasnya. Proses ini menyebabkan peningkatan viskositas dan
kelarutan pati yang merupakan hasil dari perubahan irreversibel [22].
Pada penelitian ini metode yang digunakan untuk menetukan perilaku
gelatinisasi pati ditentukan dengan menggunakan Rapid Visco Analyzer (RVA).
RVA adalah metode yang secara luas digunakan untuk menentukan sifat kekentalan
dari pasta pati dan informasi dari sifat kekentalan itu sendiri [50]. Amilografi pati biji
[image:40.595.207.434.335.446.2]nangka yang diukur oleh RVA dapat dilihat pada tabel 4.2 berikut.
Tabel 4.2 Amilografi Pati Biji Nangka
Parameter Pati Biji Nangka
Temperatur Gelatinisasi 88,82 °C
Peak Viscosity 3.276,5 cP
Hold Viscosity 2.453,5 cP
Final Viscosity 5.366 cP
Breakdown 823 cP
Setback 1 2,912,5 cP
Dari Tabel 4.2 diatas dapat dilihat beberapa parameter yang dapat diukur oleh
RVA yaitu temperatur gelatinisasi, peak viscosity, hold viscosity, final viscosity,
breakdown viscosity dan setback viscosity. Temperatur gelatinisasi adalah temperatur
kritis di mana granula pati kehilangan sifat bias ganda (birefringence) dan
kekristalannya selama pemanasan [50]. Nilai temperatur gelatinisasi pati biji nangka
dapat dilihat dari Tabel 4.2 diatas yaitu sebesar 88,82 °C. Temperatur gelatinisasi
yang tinggi dikarenakan kandungan amilosa pati yang tinggi sehingga
pembengkakan granula pati menjadi rendah [51].
Terdapat beberapa tahapan pada proses gelatinisasi. Tahap pertama, pati dalam
air dingin akan menyerap air sampai sekitar 5-30%, proses ini bersifat reversible.
Tahap kedua, akibat pemanasan yang diberikan ikatan hidrogen antara amilosa dan
amilopektin dalam granula pati mulai putus, sehingga air dapat masuk ke dalam
granula pati dan granula mulai mengembang. Proses penyerapan air ke dalam
dimana granula pati membengkak menyebabkan peningkatan yang cepat pada
viskositas akan menghasilkan viskositas maksimum yaitu Peak Viscosity (PV) [53].
Suhu dimana viskositas maksimum tercapai disebut suhu akhir gelatinisasi. Pada
suhu ini granula pati telah kehilangan sifat birefringence-nya dan granula sudah tidak
mempunyai kristal lagi [54]. Makin besar kemampuan mengembang granula pati
maka viskositas pasta makin tinggi [51]. Hasil pengukuran RVA pada penelitian ini,
PV pati biji nangka adalah 3276,5 cP.
Tahap ketiga gelatinisasi terjadi pengembangan granula lebih besar lagi dan
amilosa keluar dari granula pati terdispersi kedalam larutan hingga akhirnya granula
pati pecah [52]. Pecahnya struktur granula pati menyebabkan penurunan viskositas
pasta serta stabilitas viskositas pasta menjadi rendah. setelah sebelumnya mencapai
viskositas puncak terjadi penurunan viskositas menjadi 2453,5 cP. Viskositas ini
disebut hold viscosity (HV). HV merupakan kemampuan granula pati untuk menahan
pemanasan dan tegangan regangan [55]. Selisih nilai antara PV dan HV adalah nilai
viskositas breakdown yaitu sebesar 823 cP. Nilai viskositas breakdown yang rendah
menunjukkan stabilitas granula yang lebih tinggi terhadap pemanasan [55]. Pada
fase pendinginan, viskositas pasta pati kembali meningkat akibat terbentuknya
kembali molekul-molekul amilosa dan amilopektin melalui ikatan hidrogen [53].
Viskositas hasil pengukuran dengan RVA meningkat menjadi 5366 cP. Viskositas ini
disebut viskositas pasta dingin atau Final Viscosity (FV).
Setback yaitu selisih antara HV dengan FV yang menunjukkan kemampuan
pasta pati mengalami retrogradasi yaitu proses pembentukan kembali matriks pati
yang telah mengalami gelatinisasi. Semakin tinggi nilai viskositas balik berarti
semakin tinggi kemampuan pati untuk mengalami retrogradasi [56]. Berdasarkan
hasil RVA maka nilai viskositas balik pati biji nangka adalah 2,912,5 cP. nilai
setback yang tinggi dikarenakan diameter dari pati yang meningkatkan kerapuhan
granula pada saat proses gelatinisasi dan disintegrasi yang memfasilitasi pelepasan
rantai amilosa dan penggabungan kembali amilosa. Pati dengan nilai setback yang
tinggi menunjukkan bahwa banyaknya jumlah amilosa yang berikatan kembali
melalui ikatan hidrogen sehingga struktur pati yang terbentuk menjadi lebih kuat.
4.2 HASIL KARAKTERISASI FTIR PATI BIJI NANGKA, KITOSAN, BIOPLASTIK TANPA / DENGAN PENGISI KITOSAN DAN
PLASTICIZER ETILEN GLIKOL
Karakterisasi FTIR (Fourier Transform Infra Red) pati biji nangka bertujuan
untuk mengetahui gugus fungsi yang terdapat di dalam pati biji nangka, kitosan,
bioplastik dengan kitosan dan bioplastik tanpa kitosan [57]. Karakteristik FTIR dari
bahan pati biji nangka, kitosan, bioplastik dengan kitosan dan bioplastik tanpa
[image:42.595.77.498.245.471.2]kitosan dapat dilihat pada Gambar 4.2 di bawah ini.
Gambar 4.2 Karakterisasi FTIR Kitosan, Pati Biji Nangka, Bioplastik tanpa Kitosan dan
Bioplastik dengan Kitosan
Dari Gambar 4.2 diatas diperoleh informasi beberapa peak yang muncul seperti
yang ditunjukkan Gambar 4.2 tersebut. Gambar 4.2 diatas juga menunjukkan bahwa
untuk bioplastik dengan kitosan dan tanpa kitosan memiliki bentuk spektrum yang
hampir serupa. Dimana hasil FTIR bioplastik dengan kitosan dan tanpa kitosan
sama-sama memiliki gugus O-H dengan daerah serapan ulur yang tidak berbeda jauh
amida yang khas pada daerah 1647,21 cm-1. Selain itu juga terdapat puncak pita serapan gugus hidroksil O-H pada daerah 3433,29 cm-1 [58].
Menurut Darni dan Herti (2010), pada bioplastik yang mengandung gugus fungsi
C=O karbonil dan ester (C-O) mengindikasikan bioplastik tersebut memiliki
kemampuan biodegradabilitas yang mana gugus fungsi tersebut adalah gugus fungsi
yang dimiliki oleh pati dan kitosan. Hal ini disebabkan oleh C=O karbonil dan ester
(C-O) merupakan gugus-gugus yang bersifat hidrofilik. Kemampuan kedua gugus
tersebut dalam mengikat molekul-molekul air yang berasal dari lingkungan
mengakibatkan mikroorganisme yang dapat memasuki matriks plastik juga semakin
banyak seiring dengan semakin tingginya intensitas gugus-gugus yang bersifat
4.3PENGARUH VARIASI PENGISI KITOSAN DAN PLASTICIZER ETILEN GLIKOL TERHADAP DENSITAS BIOPLASTIK
Berikut gambar yang menunjukkan pengaruh variasi pengisi kitosan dan
[image:44.595.126.487.163.348.2]plasticizer etilen glikol terhadap densitas bioplastik
Gambar 4.3 Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen Glikol Terhadap Densitas Bioplastik
Gambar 4.3 menunjukkan hubungan penambahan kitosan dan plasticizer etilen
glikol terhadap densitas bioplastik. Dari gambar di atas dapat dilihat nilai densitas
bioplastik tertinggi yang diperoleh pada penelitian ini adalah 1,058 gram/cm3 pada bioplastik pati biji nangka menggunakan kitosan 3 gram dan etilen glikol 0,20
ml/gram. Densitas bioplastik minimum yang diperoleh pada penelitian ini adalah
0,612 gram/cm3 pada bioplastik pati biji nangka menggunakan kitosan 1 gram dan etilen glikol 0,40 ml/gram.
Dari gambar 4.3 diatas menjelaskan adanya pengaruh penambahan pengisi
kitosan dan plasticizer etilen glikol terhadap densitas bioplastik. Dimana nilai
densitas bioplastik berbanding lurus dengan penambahan jumlah kitosan dan
berbanding terbalik dengan penambahan jumlah etilen glikol. Hal ini disebabkan
oleh kitosan yang berperan sebagai pengisi membuat sruktur bioplastik dengan
kitosan lebih rapat dibanding dengan bioplastik tanpa kitosan. Karena semakin rapat
struktur bioplastik membuat semakin meningkat nilai densitas bioplastik. Sehingga
meningkatnya kandungan dari pengisi berbanding lurus dengan densitas bioplastik
[59]. Dan penambahan etilen glikol berbanding terbalik dengan densitas bioplastik
karena ikatan hidrogen yang terbentuk akibat penambahan plasticizer sehingga
0,
909 0,944 1,
058
0,
880 0,910 0,
975
0,
823 0,895 0,
923
0,
738 0,
863 0,900
0, 612 0, 796 0, 882 0,0 0,2 0,4 0,6 0,8 1,0 1,2
1 2 3
D en si tas ( gr am /c m 3)
Massa Kitosan (Gram)
Etilen Glikol 0,20 ml/gram
Etilen Glikol 0,25 ml/gram
Etilen Glikol 0,30 ml/gram
Etilen Glikol 0,35 ml/gram
struktur rantai polimer semakin berongga. Hal ini menyebabkan kerapatan,
kekakuan, dan rapat massa berkurang sehingga turunnya nilai daripada densitas
bioplastik [60].
4.4PENGARUH VARIASI PENGISI KITOSAN DAN PLASTICIZER ETILEN GLIKOL TERHADAP SIFAT MEKANIK BIOPLASTIK
4.4.1Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen Glikol Terhadap Sifat Kekuatan Tarik Bioplastik
Berikut gambar yang menunjukkan pengaruh variasi kitosan dan plasticizer etilen glikol
[image:45.595.118.481.288.477.2]terhadap sifat kekuatan tarik bioplastik
Gambar 4.4 Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen glikol Terhadap Sifat Kekuatan Tarik Biolastik
Gambar 4.4 menunjukkan hubungan penambahan kitosan dan plasticizer
etilen glikol terhadap kekuatan tarik bioplastik.. Dari gambar di atas dapat dilihat
nilai kekuatan tarik bioplastik tertinggi adalah pada penambahan kitosan 3 gram dan
etilen glikol 0,35 ml/gram yaitu sebesar 28,271 MPa, sedangkan kekuatan tarik
terendah adalah pada penambahan kitosan 1 gram dan etilen glikol 0,20 ml/gram
yaitu sebesar 14,881 MPa.
Dari gambar 4.4 tersebut dapat dilihat adanya pengaruh penambahan pengisi
kitosan dan plasticizer etilen glikol terhadap kekuatan tarik (tensile strength)
bioplastik. Dengan semakin bertambahnya jumlah kitosan dapat menyebabkan nilai
kuat tarik dari bioplastik menjadi meningkat. Hal ini disebabkan oleh penambahan
kitosan sebagai pengisi dapat meningkatkan nilai densitas bioplastik yang
14, 881 19, 077 19, 250 18, 231 19, 097 23, 363 20, 396 21, 477 25, 146 24, 123 25, 775 28, 271 23, 284 23, 634 28, 150 0,0 10,0 20,0 30,0
1 2 3
K ek u a ta n ta ri k (M P a )
Massa Kitosan (Gram)
etilen glikol 0,20 ml/gram
etilen glikol 0,25 ml/gram
etilen glikol 0,30 ml/gram
etilen glikol 0,35 ml/gram
diakibatkan semakin rapatnya struktur bioplastik sehingga kekuatan tarik bioplastik
akan meningkat [59]. Sedangkan penambahan plasticizer berbanding terbalik dengan
penambahan pengisi dimana bertambahnya plasticizer akan menurunkan nilai dari
kekuatan tarik. Hal ini disebabkan oleh penambahan plasticizer yang menurunkan
nilai densitas akibat struktur rantai polimer yang semakin berongga yang
menyebabkan penurunan pada kekuatan tarik [58]. Pada gambar diatas menunjukkan
terjadi penurunan kekuatan tarik pada penambahan 1, 2, dan 3 gram kitosan dengan
etilen glikol 0,35 ml/gram. Menurut Chrismaya (2012), terjadinya penurunan
kekuatan tarik bioplastik disebabkan oleh kondisi keberadaan plasticizer pada dalam
campuran. Hal ini menyebabkan terjadinya keadaan jenuh plasticizer sehingga
terjadi efek plastisasi yang menurunkan nilai dari kekuatan tarik [11].
4.4.2Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen Glikol Terhadap Sifat Pemanjangan Pada Saat Putus Bioplastik
Berikut gambar yang menunjukkan pengaruh variasi kitosan dan plasticizer
[image:46.595.147.504.408.583.2]etilen glikol terhadap sifat pemanjangan pada saat putus bioplastik
Gambar 4.5 Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen Glikol Terhadap Sifat Pemanjangan pada Saat Putus Biolastik
Gambar 4.5 menunjukkan hubungan penambahan kitosan dan plasticizer
etilen glikol terhadap pemanjangan pada saat putus bioplastik pati biji nangka. Dari
gambar di atas dapat dilihat nilai pemanjangan saat putus tertinggi adalah pada
penambahan kitosan 1 gram dengan etilen glikol 0,40 ml/gram yaitu sebesar 1,999
%, sedangkan pemanjangan saat putus terendah adalah pada penambahan kitosan 3
gram dengan etilen glikol 0,30 ml/gram sebesar 0,577 %.
1, 540 1, 420 1, 194 1, 107 1, 013 0, 926 1, 758 1, 161 0, 577 1, 953 1, 501 1, 345 1, 999 1, 934 1, 531 0,0 0,5 1,0 1,5 2,0 2,5
1 2 3
P em a n ja n g a n s a a t P u tu s (%)
Massa Kitosan (Gram)
Etilen Glikol 0,20 ml/gram
Etilen Glikol 0,25 ml/gram
Etilen Glikol 0,30 ml/gram
Etilen Glikol 0,35 ml/gram
Dari gambar 4.5 diatas dapat dilihat adanya pengaruh penambahan pengisi
kitosan dan plasticizer etilen glikol terhadap pemanjangan saat putus (elongation at
break) bioplastik. Menurut Ginting (2015), dengan semakin bertambahnya jumlah
kitosan dapat menyebabkan nilai pemanjangan saat putus dari bioplastik menjadi
menurun. Hal ini dapat disebabkan oleh tingginya kekompakan dari ikatan antar
molekul yang diakibatkan oleh peningkatan ikatan hidrogen saat menambahkan
kitosan sehingga bioplastik yang terbentuk menjadi lebih kuat dan lebih kaku [61].
Berbeda dengan penambahan jumlah etilen glikol, semakin bertambahnya jumlah
etilen glikol yang ditambahkan dapat menyebabkan nilai pemanjangan saat putus
dari bioplastik menjadi meningkat. Hal ini dapat disebabkan penambahan plasticizer
yang membuat bioplastik semakin plastis karena etilen glikol sebagai plasticizer
dapat menambah free volume dalam matriks film dengan mengurangi ikatan
hidrogen antara rantai-rantai polimer [12]. Pada gambar diatas dapat dilihat nilai
pemanjangan saat putus (elongation at break) yang fluktuatif. Nilai pemanjangan
saat putus yang fluktuatif dikarenakan oleh keberadaan plasticizer yang mengalami
tiga keadaan transisi yaitu adsorbsi plasticizer pada ikatan –H dalam pati, kondisi
jenuh plasticizer, dan kondisi lewat jenuh plasticizer. Pada keadaan pertama,
plasticizer dapat mengabsorbsi ikatan –H dalam pati dengan baik sehingga
mengakibatkan bioplastik pada kondisi glassy-nya dimana molekul pati kehilangan
mobilitasnya dan terjadi efek antiplastisasi (tidak elastis) sehingga menyebabkan
bioplastik dalam bersifat keras dan kuat. Sedangkan pada keadaan kedua, plasticizer
dalam kondisi jenuh sehingga terjadi efek plastisasi yang menurunkan nilai dari
kekuatan tarik dan semakin menurun lagi pada tahapan ketiga dimana plasticizer
mengalami kondisi lewat jenuh [11]. Akibat dari ketiga kondisi transisi ini
4.4.3Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen Glikol Terhadap
Modulus Young Bioplastik
Berikut gambar yang menunjukkan pengaruh variasi kitosan dan plasticizer
etilen glikol terhadap Modulus Young bioplastik pati biji nangka berpengisi kitosan
[image:48.595.150.506.187.370.2]dan plasticizer etilen glikol.
Gambar 4.6 Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen Glikol Terhadap Modulus Young Biolastik
Gambar 4.6 menunjukkan hubungan penambahan kitosan dan plasticizer
etilen glikol terhadap Modulus Young bioplastik. Dari grafik pada gambar di atas
dapat dilihat nilai Modulus Young tertinggi adalah pada penambahan kitosan 3 gram
dan etilen glikol 0,30 ml/gram sebesar 43,581 MPa, sedangkan Modulus Young
terendah adalah pada penambahan kitosan 1 gram dan etilen glikol 0,20 ml/gram
sebesar 9,663 MPa.
Dari gambar 4.6 diatas terlihat adanya pengaruh penambahan kitosan dan
plasticizer etilen glikol terhadap Modulus Young bioplastik. Dengan semakin
bertambahnya kitosan maka nilai Modulus Young akan semakin meningkat. Hal ini
dapat disebabkan oleh peningkatan kekompakan dari ikatan antar molekul pada
bioplastik karena ikatan hidrogen yang terjadi akibat penambahan kitosan
menyebakan bentuk dari bioplastik yang menjadi semakin kuat dan kaku [61].
Berbeda halnya dengan penambahan volume etilen glikol dimana semakin banyak
penambahan volume etilen glikol maka nilai Modulus Young akan semakin menurun.
Menurut Fitria dan Yuli (2015), penyebab dari penurunan nilai Modulus Young
akibat penambahan volume plasticizer disebabkan oleh penambahan etilen glikol
9,
663 13,
435 16,122
16,
469 18,852
25, 230 11, 602 18, 499 43, 581 12, 352 17, 172 21, 019 11, 648 12, 220 18, 387 5,0 15,0 25,0 35,0 45,0
1 2 3
M o dul us Y o ung ( M P a )
Massa Kitosan (Gram)
sebagai plasticizer mampu menurunkan gaya intermolekular sepanjang rantai
polimer yang mengakibatkan polimer yang dihasilkan semakin elastis sehingga
semaki kecil derajat kekakuan atau modulus young polimer tersebut [58]. Pada
gambar diatas dapat dilihat nilai modulus young yang fluktuatif. Hal ini dikarenakan
keberadaan plasticizer yang mengalami tiga keadaan transisi yaitu adsorbsi
plasticizer pada ikatan –H dalam pati, kondisi jenuh plasticizer, dan kondisi lewat
jenuh plasticizer. Pada keadaan pertama, plasticizer dapat mengabsorbsi ikatan –H
dalam pati dengan baik sehingga mengakibatkan bioplastik pada kondisi glassy-nya
dimana molekul pati kehilangan mobilitasnya dan terjadi efek antiplastisasi (tidak
elastis) sehingga menyebabkan bioplastik dalam bersifat keras dan kuat. Sedangkan
pada keadaan kedua, plasticizer dalam kondisi jenuh sehingga terjadi efek plastisasi
yang menurunkan nilai dari kekuatan tarik dan semakin menurun lagi pada tahapan
ketiga dimana plasticizer mengalami kondisi lewat jenuh [11]. Jadi dapat
disimpulkan terjadinya nilai modulus young yang fluktuatif dikarenakan plasticizer
mengalami keadaan transisi.
4.5PENGARUH VARIASI PENGISI KITOSAN DAN PLASTICIZER ETILEN GLIKOL TERHADAP PENYERAPAN AIR BIOPLASTIK
Berikut gambar yang menunjukkan pengaruh variasi kitosan dan plasticizer
[image:49.595.124.485.497.672.2]etilen glikol terhadap penyerapan air bioplastik
Gambar 4.7 Pengaruh Variasi Pengisi Kitosan dan Plasticizer Etilen Glikol Terhadap Penyerapan Air Biolastik
Gambar 4.7 menunjukkan hubungan penambahan kitosan dan plasticizer
57, 230 56, 220 48, 910 58, 890 57, 890 51, 290 61, 590 60, 230 52, 020 62, 120 61, 210 52, 990 64, 990 62, 630 54, 100 0,0 20,0 40,0 60,0 80,0
1 2 3
P en y era p a n A ir (%)
Massa Kitosan (Gram)
Etilen Glikol 0,20 ml/gram
Etilen Glikol 0,25 ml/gram
Etilen Glikol 0,30 ml/gram
Etilen Glikol 0,35 ml/gram
gambar di atas dapat dilihat nilai penyerapan air bioplastik tertinggi adalah pada
penambahan kitosan 1 gram dan etilen glikol 0,40 ml/gram yaitu sebesar 64,99 %,
sedangkan penyerapan air terendah adalah pada penambahan kitosan 3 gram dan
etilen glikol 0,20 ml/gram yaitu sebesar 48,91 %.
Dari gambar 4.7 tersebut dapat dilihat adanya pengaruh penambahan pengisi
kitosan dan plasticizer etilen glikol terhadap penyerapan air bioplastik. Dengan
semakin meningkatnya penambahan jumlah etilen glikol dapat menyebabkan nilai
penyerapan air dari bioplastik menjadi bertambah. Kemudian semakin meningkatnya
penambahan jumlah kitosan dapat menyebabkan nilai penyerapan air dari bioplastik
menjadi menurun. Penambahan etilen glikol sebagai plasticizer akan meningkatkan
nilai kelarutan bioplastik terhadap air. Hal ini menyebabkan bioplastik semakin
mudah untuk menyerap air sehingga meningkatkan nilai penyerapan air (62). Dan
kitosan sebagai pengisi memiliki sifat tidak larut dalam air sehingga seiring dengan
penambahan kitosan maka nilai penyerapan air akan semakin kecil [3].
4.6 HASIL KARAKTERISASI MORFOLOGI PERMUKAAN DENGAN
SCANNING ELECTRON MICROSCOPE (SEM)
4.6.1 Hasil Karakterisasi Morfologi Permukaan Pati Biji Nangka dengan
Scanning Electron Microscope (SEM)
Karakterisasi Scanning Electron Microscope (SEM) pati biji nangka
[image:50.595.200.464.517.714.2]ditunjukkan pada Gambar 4.6 dibawah ini.
Gambar 4.8 Karakterisasi SEM Pati Biji Nangka Perbesaran 1000 kali
Gambar 4.8 diatas menunjukkan hasil karakterisasi SEM partikel pati biji
nangka yang berukuran 100 mesh dengan perbesaran 1000 kali. Hasil analisa SEM
menunjukkan bahwa morfologi pati biji nangka memiliki ukuran partikel yang belum
seragam sesuai dengan gambar diatas. Karakterisasi SEM merupakan suatu metode
untuk membentuk bayangan daerah mikroskopis permukaan sampel [63]. Hasil
analisa SEM pati biji nangka yang diperoleh pada penelitian ini memiliki ukuran
granula pati sebesar 7,6 µm.
4.6.2 Hasil Karakterisasi Morfologi Permukaan Bioplastik dengan Scanning
Electron Microscope (SEM)
Karakterisasi SEM (Scanning Electron Microscope) bioplastik tanpa pengisi
kitosan dan plasticizer Etilen Glikol dan bioplastik berpengisi kitosan dan plasticizer
etilen glikol ditunjukkan pada Gambar 4.13 dibawah ini.
[image:51.595.97.506.351.562.2](a) (b)
Gambar 4.9 Karakterisasi SEM Produk Bioplastik
(a) Bioplastik Tanpa Pengisi Kitosan dan Plasticizer Etilen Glikol 0,35 ml/gram dengan Perbesaran 1000 kali
(b) Bioplastik dengan Penambahan Kitosan 3 gram dan Plasticizer Etilen Glikol 0,35 ml/gram dengan Perbesaran 1000 kali
Gambar 4.9 (a) menunjukkan hasil karakterisasi SEM produk bioplastik dan
tanpa penambahan pengisi kitosan dan plasticizer etilen glikol dengan perbesaran
1000 kali. Pada Gambar 4.9 (a) terlihat bahwa bioplastik tanpa pengisi masih telihat
granula pati yang belum tergelatinisasi walaupun beberapa bagian sudah
tergelatinisasi. Gambar 4.9 (a) juga menunjukkan bahwa bioplastik