PE
ENETAPA
S
PRO
U
AN KADA
SECARA
GRAM EK FAK UNIVERSI
AR KALS
A KOMPL
SKRIP
OLEH NURHA NIM 0915
KSTENSI S KULTAS F ITAS SUM MEDA
SIUM PA
LEKSOM
PSI
H: AFNI
24013
SARJANA FARMASI MATERA U
AN
ADA IKAN
METRI
FARMASI
UTARA
N TERI
PE
D
ENETAPA
S
Diajukan un Ge
PRO
U
AN KADA
SECARA
ntuk Meleng elar Sarjana
Univ
GRAM EK FAK UNIVERSI
AR KALS
A KOMPL
SKRIP
gkapi Salah Farmasi Pa versitas Sum
OLEH NURHA NIM 0915
KSTENSI S KULTAS F ITAS SUM MEDA 2011
SIUM PA
LEKSOM
PSI
h Satu Syara ada Fakultas matera Utara
H: AFNI
24013
SARJANA FARMASI MATERA U
AN 1
ADA IKAN
METRI
at untuk Me s Farmasi a
FARMASI
UTARA
N TERI
encapai
LEMBAR PENGESAHAN
PENETAPAN KADAR KALSIUM PADA IKAN TERI SECARA KOMPLEKSOMETRI
NURHAFNI NIM 091524013
Dipertahankann di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Juni 2011
Disetujui Oleh:
Dosen Pembimbing I, Panitia Penguji,
Drs. Syafruddin, M.S., Apt. Drs. Chairul Azhar D., M.Sc., Apt.
NIP 194811111976031003 NIP 194907061980021001
Drs. Syafruddin, M.S., Apt.
Dosen Pembimbing II, NIP 194811111976031003
Prof. Dr. Jansen Silalahi, M.App. Sc., Apt. Drs. Maralaut Batubara, M.Phill., Apt.
NIP 195006071979031001 NIP 195101311976031003
Dra. Tuty Roida Pardede, M.Si., Apt.
NIP 195401101980032001
Dekan,
KATA PENGANTAR
Alhamdulillah, puji dan syukur ke hadirat Allah SWT yang telah
melimpahkan rahmat, karunia dan ridha-Nya, sehingga penulis dapat
menyelesaikan skripsi ini yang berjudul “Penetapan Kadar Kalsium Pada Ikan
Teri Secara Kompleksometri”. Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar Sarjana pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempata ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ayahanda Mahyiddin dan Ibunda Nurhayati serta kakak-adik tercinta, Bang
Adi, Kak Inur, Yus, Lia dan Ima atas semua cinta, kasih sayang, doa yang tulus
serta kesabaran dan pengorbanan baik materi maupun non-materi kepada
penulis.
2. Bapak Drs. Syafruddin, M.S., Apt., dan Bapak Prof. Dr. Jansen Silalahi,
M.App. Sc., Apt., yang telah memberi motivasi dan membimbing dengan
penuh kesabaran, tulus dan ikhlas selam penelitian dan penulisan skripsi ini
berlangsung.
3. Bapak Dekan, staf pengajar dan staf administrasi Fakultas Farmasi yang telah
mendidik penulis selam masa perkuliahan dan membantu kemudahan
administrasi.
4. Bapak Drs. Awaluddin Saragih M.Si., Apt., selaku penasehat akademik yang
5. Ibu Dra. Sudarmi, M.Si., Apt., selaku Kepala Laboratorium Kimia Farmasi
Kuantitatif Fakultas Farmasi USU yang telah memberikan izin dan fasilitas
kepada penulis untuk dapat mengerjakan dan menyelesaikan penelitian.
6. Sahabat-sahabat tersayang Ade, Liana, Sri Kur, Vera serta seluruh
teman-teman Ekstensi Farmasi 2009, rekan-rekan di BPK RSUD Sigli terutama
Instalasi Farmasi dan Apotik Nilam Sigli atas bantuan dan motivasi yang
diberikan selama masa perkuliahan sampai penulisan skripsi ini.
7. Kakak dan abang senior farmasi, adik-adik junior Farmasi, serta seluruh pihak
yang telah banyak ikut membantu hingga selesainya penulisan skripsi ini yang
tidak dapat disebutkan satu persatu.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih jauh dari
kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima
kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, Juni 2011
Penulis,
PENETAPAN KADAR KALSIUM PADA IKAN TERI SECARA KOMPLEKSOMETRI
ABSTRAK
Ikan teri dapat menjadi salah satu sumber kalsium yang baik selain susu, karena ikan teri dikonsumsi utuh bersama tulangnya, berbeda dengan ikan lain yang hanya dikonsumsi dagingnya saja. Tujuan penelitian ini adalah untuk mengetahui kadar kalsium yang terkandung dalam ikan teri.
Dalam penelitian ini dianalisis tiga kelompok ikan teri yang berbeda ukuran yaitu kecil , sedang dan besar yang berasal dari pasar Kembang Tanjong dan Teupen Raya Kabupaten Pidie Nanggroe Aceh Darussalam. Pemeriksaan kalsium dilakukan secara kualitatif dan kuantitatif. Analisis kualitatif dilakukan dengan menggunakan pereaksi asam sulfat encer dan etanol, dan ammonium oksalat. Analisis kuantitatif dilakukan secara titrasi kompleksometri dengan menggunakan dinatrium EDTA sebagai pentiter dan kalkon campur sebagai indikator pada pH 13.
Hasil penelitian menunjukkan bahwa kadar kalsium dalam ikan teri yang berbeda ukuran adalah berbeda. Semakin besar ukuran ikan teri maka kadar kalsium semakin tinggi. Dari analisis diperoleh kadar kalsium yang terkandung dalam ikan teri yang berasal dari pasar Kembang Tanjong adalah 1981,63 ± 14,9547 mg/100 gram untuk ikan teri kecil, pada ikan teri sedang 2196,68 ± 10,1832 mg/100 gram dan pada ikan teri besar adalah 2284,50 ± 15,9736 mg/100 gram. Sedangkan untuk ikan teri yang berasal dari pasar Teupen Raya adalah 1989 ± 14,5360 mg/100 gram untuk ikan teri kecil, pada ikan teri sedang 2207,23 ± 12,1305 mg/100 gram dan pada ikan teri besar adalah 2296,01 ± 11,4356 mg/100 gram.
DETERMINING THE LEVEL OF CALCIUM ON ANCHOVY BY COMPLEXOMETRIC TITRATION
ABSTRACT
Anchovy may be used as a source of calcium in addition to milk, because the anchovy usually consumed with bones, unlike other fish which is consumed meat only. The purpose of study was to determine content of calcium in the anchovy.
This study analyze three groups of anchovy of different sizes those is small, medium and big size originated from Kembang Tanjong market and Teupen Raya market, Aceh Pidie District. analysis of calcium was done by qualitative and quantitative determine. Qualitative analysis was done using dilute sulphuric acid, ethanol and ammonium oxalate. Quantitative analysis was done by complexometric titration with sodium EDTA and using calcon as indicator at pH of 13.
The result of study to showed that content of calcium in the anchovy of different sizes are different. The bigger the size of anchovy then higher the content of calcium. From this study obtained content of calcium in anchovy originated from Kembang Tanjong market was 1981.63 ± 14.9547 mg/100 g for small anchovy, in average anchovy was 2196.68 ± 10.1832 mg/100 g and in big anchovy was
2284.50 ± 15.9736 mg/100 grams. As for the anchovy originating from Teupen Raya market was 1989 ± 14.5360 mg/100 g for small anchovy, the average anchovy was 2207.23 ± 12.1305 mg/100 g and the big anchovy was 2296.01 ± 11.4356 mg/100 grams.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II METODOLOGI PENELITIAN ... 5
2.1 Tempat Dan Waktu Penelitian ... 5
2.2 Bahan-Bahan ... 5
2.3 Alat-Alat ... 5
2.4 Pembuatan Pereaksi ... 6
2.5.1 Pengambilan Sampel ... 7
2.5.2 Pembakuan Larutan Standar Dinatrium EDTA ... 8
2.5.3 Penyiapan Bahan ... 8
2.5.4 Penetapan Kadar Air ... 8
2.5.5 Proses Destruksi Basah ... 8
2.5.6 Analisis Kualitatif ... 10
2.5.7 Analisis Kuantitatif ... 10
2.5.8 Penetapan Kadar Kalsium Karbonat ... 10
2.5.9 Penentuan Uji Perolehan Kembali ... 11
2.5.10 Analisis Data Secara Statistik ... 11
2.5.11 Kadar Kalsium ... 12
BAB III HASIL DAN PEMBAHASAN ... 13
3.1 Analisis Kualitatif ... 13
3.2 Analisis Kuantitatif ... 13
3.2.1 Penetapan Kadar Air Dalam Sampel Ikan Teri ... 13
3.2.2 Analisis Kadar Kalsium Dalam Sampel Ikan Teri ... 14
3.2.3 Uji Perolehan Kembali ... 15
BAB IV KESIMPULAN DAN SARAN ... 16
4.1 Kesimpulan ... 16
4.2 Saran.. ... 16
DAFTAR PUSTAKA ... 17
DAFTAR TABEL
Halaman
Tabel 1. Hasil Analisis Kualitatif Kalsium Dalam Sampel Ikan Teri ... 13
Tabel 2. Hasil Penetapan Kadar Air Pada Sampel Ikan Teri ... 14
DAFTAR GAMBAR
Halaman
Gambar 1. Bagan Alir Proses Destruksi Basah ... 9
Gambar 2. Ikan Teri Besar ... 19
Gambar 3. Ikan Teri Sedang ... 19
Gambar 4. Ikan Teri Kecil ... 19
Gambar 5. Hasil Analisis Kualitatif Dengan Asam Sulfat Encer Dan Etanol 96% ... 20
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Sampel Yang Digunakan ... 32
Lampiran 2. Data Perhitungan Pembakuan Larutan Standar Na2EDTA ... 33
Lampiran 3. Penetapan Kadar Kalsium Karbonat Baku Dengan Metode Titrasi Kompleksometri ... 35
Lampiran 4. Perhitungan Statistik Penetapan Kadar Kalsium Karbonat Baku ... 36
Lampiran 5. Hasil Penetapan Kadar Air Dalam Sampel Ikan Teri ... 37
Lampiran 6. Hasil Analisa Kualitatif ... 39
Lampiran 7. Contoh Perhitungan Kadar Kalsium Dari Sampel Ikan Teri ... 40
Lampiran 8. Hasil Penetapan Kadar Kalsium Dari Sampel Ikan Teri ... 42
Lampiran 9. Penetapan Kadar Kalsium Dalam Sampel Ikan Teri Berat Kering ... 44
Lampiran 10. Hasil Uji Perolehan Kembali Kalsium Setelah Penambahan Larutan Standar Pada Ikan Teri Besar Yang Berasal Dari Teupen Raya ... 45
Lampiran 11. Contoh Perhitungan Analisis Perolehan Kembali Kalsium Dalam Sampel ... 46
Lampiran 12. Perhitungan Koefisien Variasi (% RSD) Ikan Teri Besar Asal Teupen Raya. ... 47
Lampiran 13. Perhitungan Statistik Kadar Kalsium Dari Sampel Yang Dianalisis ... 48
Lampiran 14. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Kecil Asal Kembang Tanjong Dengan Ikan Teri Kecil Asal Teupen Raya ... 55
Lampiran 16. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Besar Asal Kembang Tanjong Dengan Ikan Teri Besar
Asal Teupen Raya ... 59
Lampiran 17. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Kecil Asal Kembang Tanjong Dan Ikan Teri Sedang
Asal Kembang Tanjong ... 61
Lampiran 18. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Sedang Asal Kembang Tanjong Dengan Ikan Teri Besar Asal Kembang Tanjong ... 63
Lampiran 19. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Kecil Asal Teupen Raya Dan Ikan Teri Sedang Asal
Teupen Raya ... 65
Lampiran 20. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan
Teri Sedang Dengan Ikan Teri Besar Asal Teupen Raya ... 67
Lampiran 21. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Kecil Asal Kembang Tanjong Dan Ikan Teri Besar
Asal Kembang Tanjong ... 69
Lampiran 22. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Kecil Asal Kembang Tanjong Dan Ikan Teri Sedang Asal
Teupen Raya ... 71
Lampiran 23. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Kecil Asal Kembang Tanjong Dan Ikan Teri Besar Asal
Teupen Raya ... 73
Lampiran 24. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Sedang Asal Kembang Tanjong Dan Ikan Teri Kecil Asal
Teupen Raya ... 75
Lampiran 25. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Sedang Asal Kembang Tanjong Dan Ikan Teri Besar Asal
Teupen Raya ... 77
Lampiran 26. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Besar Asal Kembang Tanjong Dan Ikan Teri Kecil Asal
Teupen Raya ... 79
Lampiran 27. Pengujian Beda Nilai Rata-Rata Kadar Kalsium Antara Ikan Teri Besar Asal Kembang Tanjong Dan Ikan Teri Sedang Asal
Teupen Raya ... 81
Teri Kecil Asal Teupen Raya Dan Ikan Teri Besar Asal
Teupen Raya ... 83
Lampiran 29. Tabel Nilai Kritis Distribusi t ... 85
PENETAPAN KADAR KALSIUM PADA IKAN TERI SECARA KOMPLEKSOMETRI
ABSTRAK
Ikan teri dapat menjadi salah satu sumber kalsium yang baik selain susu, karena ikan teri dikonsumsi utuh bersama tulangnya, berbeda dengan ikan lain yang hanya dikonsumsi dagingnya saja. Tujuan penelitian ini adalah untuk mengetahui kadar kalsium yang terkandung dalam ikan teri.
Dalam penelitian ini dianalisis tiga kelompok ikan teri yang berbeda ukuran yaitu kecil , sedang dan besar yang berasal dari pasar Kembang Tanjong dan Teupen Raya Kabupaten Pidie Nanggroe Aceh Darussalam. Pemeriksaan kalsium dilakukan secara kualitatif dan kuantitatif. Analisis kualitatif dilakukan dengan menggunakan pereaksi asam sulfat encer dan etanol, dan ammonium oksalat. Analisis kuantitatif dilakukan secara titrasi kompleksometri dengan menggunakan dinatrium EDTA sebagai pentiter dan kalkon campur sebagai indikator pada pH 13.
Hasil penelitian menunjukkan bahwa kadar kalsium dalam ikan teri yang berbeda ukuran adalah berbeda. Semakin besar ukuran ikan teri maka kadar kalsium semakin tinggi. Dari analisis diperoleh kadar kalsium yang terkandung dalam ikan teri yang berasal dari pasar Kembang Tanjong adalah 1981,63 ± 14,9547 mg/100 gram untuk ikan teri kecil, pada ikan teri sedang 2196,68 ± 10,1832 mg/100 gram dan pada ikan teri besar adalah 2284,50 ± 15,9736 mg/100 gram. Sedangkan untuk ikan teri yang berasal dari pasar Teupen Raya adalah 1989 ± 14,5360 mg/100 gram untuk ikan teri kecil, pada ikan teri sedang 2207,23 ± 12,1305 mg/100 gram dan pada ikan teri besar adalah 2296,01 ± 11,4356 mg/100 gram.
DETERMINING THE LEVEL OF CALCIUM ON ANCHOVY BY COMPLEXOMETRIC TITRATION
ABSTRACT
Anchovy may be used as a source of calcium in addition to milk, because the anchovy usually consumed with bones, unlike other fish which is consumed meat only. The purpose of study was to determine content of calcium in the anchovy.
This study analyze three groups of anchovy of different sizes those is small, medium and big size originated from Kembang Tanjong market and Teupen Raya market, Aceh Pidie District. analysis of calcium was done by qualitative and quantitative determine. Qualitative analysis was done using dilute sulphuric acid, ethanol and ammonium oxalate. Quantitative analysis was done by complexometric titration with sodium EDTA and using calcon as indicator at pH of 13.
The result of study to showed that content of calcium in the anchovy of different sizes are different. The bigger the size of anchovy then higher the content of calcium. From this study obtained content of calcium in anchovy originated from Kembang Tanjong market was 1981.63 ± 14.9547 mg/100 g for small anchovy, in average anchovy was 2196.68 ± 10.1832 mg/100 g and in big anchovy was
2284.50 ± 15.9736 mg/100 grams. As for the anchovy originating from Teupen Raya market was 1989 ± 14.5360 mg/100 g for small anchovy, the average anchovy was 2207.23 ± 12.1305 mg/100 g and the big anchovy was 2296.01 ± 11.4356 mg/100 grams.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Mineral memegang peranan penting dalam pemeliharaan fungsi tubuh.
Keseimbangan mineral dalam cairan tubuh sangat penting dalam pengaturan kerja
enzim, pemeliharaan keseimbangan asam-basa, membantu transfer ikatan-ikatan
penting melalui membran sel dan pemeliharaan kepekaan otot dan saraf terhadap
rangsangan (Almatsier, 2004).
Kalsium merupakan mineral yang banyak terdapat dalam tubuh. Sebagian
besar berada dalam jaringan keras yaitu tulang dan gigi terutama dalam bentuk
hidroksiapatit [(3Ca3(PO4)2.Ca(OH)2]. Kepadatan tulang dan deposisi kalsium
bervariasi menurut umur. Pada bagian pertama pertumbuhan kepadatan tulang
mengalami peningkatan dan menurun secara berangsur setelah dewasa. Selain itu
kalsium berada dalam intra dan ekstraseluler dan memegang peranan penting
dalam mengatur fungsi sel dan impuls syaraf (Linder, 1992).
Susu dan produk olahan susu seperti keju merupakan sumber kalsium
yang utama. Selain itu ikan yang dimakan dengan tulangnya termasuk ikan kering
merupakan sumber kalsium yang baik. Serelia, kacang-kacangan dan hasil
olahannya seperti tahu dan tempe, dan sayuran hijau merupakan sumber kalsium
yang baik juga. Tetapi bahan ini mengandung banyak zat-zat yang menghambat
penyerapan kalsium seperti serat, fitat dan oksalat (Almatsier, 2004).
Ikan teri merupakan salah satu sumber kalsium yang terjangkau oleh
Nutry Survey Indonesia, kandungan kalsium dalam ikan teri lebih tinggi daripada
susu. Kalsium dari ikan teri akan bermanfaat jika dikonsumsi secara langsung. Di
dalam tubuh kalsium bekerja sama dengan laktosa dan vitamin D dalam
pembentukan massa tulang, serta dengan kalium untuk menurunkan tekanan darah
tinggi (Ahira, 2010).
Menurut Direktorat Gizi Departemen Kesehatan RI (1996), kandungan
kalsium dalam ikan teri jauh lebih tinggi dibandingkan dengan kandungan
kalsium pada ikan lain. Hal ini karena ikan teri dikonsumsi utuh dengan
tulangnya, sedangkan ikan lain hanya dikonsumsi dagingnya saja.
Berdasarkan uraian di atas, maka penulis tertarik untuk meneliti
kandungan kalsium yang terkandung pada ikan teri. Pemilihan ini didasarkan
karena masyarakat cenderung menganggap bahwa sumber kalsium yang baik
adalah susu beserta produk olahan susu, dan sering mengesampingkan sumber
kalsium yang lain. Ikan teri yang digunakan dalam penelitian ini adalah ikan teri
tawar kering yang berasal dari pasar Kembang Tanjong dan pasar Teupen Raya
Kabupaten Pidie Nanggroe Aceh Darussalam, dengan pertimbangan perairan laut
Aceh khususnya Kabupaten Pidie masih bebas dari pencemaran.
Penetapan kadar kalsium dapat dilakukan dengan metode gravimetri,
spektrofotometri serapan atom dan titrasi kompleksometri. Metode gravimetri
dapat dilakukan terhadap sampel yang mengandung kalsium tinggi, namun
metode ini memerlukan proses yang panjang dan waktu yang lama. Penetapan
kadar kalsium secara spektrofotometri serapan atom sangat sensitif sehingga dapat
singkat. Metode kompleksometri dapat digunakan untuk kadar kalsium yang
tinggi, waktu yang dibutuhkn juga singkat.
Karena kadar kalsium pada ikan teri cukup tinggi (2%), maka peneliti
menggunakan titrasi kompleksometri. Titrasi kompleksometri yaitu titrasi
berdasarkan pembentukan kompleks antara kation dengan zat pembentuk
kompleks. Sebagai zat pembentuk kompleks yang banyak digunakan adalah
garam dinatrium etilen diamin tetra asetat (dinatrium EDTA) (Ditjen POM, 1979).
1.2 Perumusan Masalah
1. Dapatkah kadar kalsium dalam ikan teri ditetapkan secara
kompleksometri?
2. Berapa kadar kalsium yang terkandung dalam ikan teri?
3. Apakah ada perbedaan kadar kalsium yang terkandung dalam beberapa
jenis ukuran ikan teri?
1.3 Hipotesis
1. Kadar kalsium dalam ikan teri dapat ditentukan secara kompleksometri
2. Kadar kalsium yang terkandung dalam ikan teri sangat tinggi
3. Tidak ada perbedaan kadar kalsium pada beberapa jenis ukuran ikan teri.
1.4 Tujuan
1. Untuk mengetahui apakah kadar kadar kalsium dalam ikan teri dapat
ditetapkan secara kompleksometri
3. Untuk melihat adanya kesamaan kadar kalsium yang terkandung dalam
beberapa jenis ukuran ukuran ikan teri
1.5 Manfaat
Dengan adanya hasil dari penelitian ini, diharapkan dapat memberikan
informasi kepada masyarakat tentang kandungan kalsium pada ikan teri.
BAB II
TINJAUAN PUSTAKA
2.1 Mineral
Banyak unsur logam dan mineral yang ditemukan dalam sel makhluk
hidup, namun hanya 22 unsur yang diketahui sebagai mineral esensial. Mineral
esensial berperan penting dalam aktivitas fungsi organ yang sangat penting untuk
kehidupan, yaitu untuk pertumbuhan atau daya reproduksi. Bila salah satu unsur
mineral hilang, maka dapat menyebabkan gejala-gejala defisiensi dan bila unsur
mineral tersebut diberikan dapat menormalkan pertumbuhan dan kesehatan orang
tersebut. Mineral esensial dibagi menjadi dua bagian yaitu makroelemen yang
ditemukan cukup tinggi dalam jaringan dan mikroelemen yang terkandung dalam
jumlah yang sangat rendah dalam jaringan. Yang termasuk ke dalam
makroelemen yang esensial adalah kalsium, fosfor, kalium, sulfur, natrium, klor
dan magnesium. Sedangkan yang termasuk ke dalam mikroelemen adalah besi,
iodium, tembaga, seng, mangan dan kobal (Darmono, 1995).
2.2 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat dalam tubuh,
yaitu 1,5 - 2% dari berat badan orang dewasa atau sekitar 1 kg. 99% dari jumlah
ini berada dalam jaringan keras yaitu tulang dan gigi terutama dalam bentuk
hidroksiapatit [(3Ca3(PO4)2.Ca(OH)2]. Dalam keadaan seimbang, kalsium tulang
dan kalsium plasma berada dalam konsentrasi 2,25 - 2,60 mmol/liter (9 - 10,4
peningkatan dan menurun secara berangsur setelah dewasa. Selain itu kalsium
juga tersebar luas dalam tubuh. Dalam cairan ekstraseluler dan intraseluler,
kalsium berperan dalam mengatur fungsi sel seperti untuk transmisi saraf,
kontraksi otot, penggumpalan darah dan menjaga permeabilitas membran sel.
Kalsium juga mengatur kerja hormon dan faktor pertumbuhan (Almatsier, 2004).
2.3 Fungsi Kalsium
Selain pada pembentukan tulang dan gigi, kalsium juga berperan pada
proses fisiologik dan biokimia tubuh seperti proses pembekuan darah, eksitabilitas
syaraf otot, kerekatan seluler, transmisi impul-impul saraf, memelihara dan
meningkatkan fungsi membran sel, mengaktifkan enzim dan sekresi hormon.
Kerangka tulang yang merupakan cadangan besar kalsium kompleks yang tidak
larut, berada dalam keseimbangan dinamik dengan kalsium bentuk larut dalam
sirkulasi (Suhardjo, 2000).
Dilihat dari senyawa kimia, bentuk tulang tidak stabil. Kalsium dan fosfor
dari tulang dapat dibebaskan dan diresorpsi dalam tubuh jika terjadi kekuarangan,
terutama pada masa hamil dan menyusui. Resorpsi ini diatur oleh hormon
paratinoid. Jika asupan kalsium rendah, glandula paratinoid akan terangsang
untuk memproduksi hormon yang bekerjauntuk meresorpsi kalsium dari tulang
dan untuk menjaga kekurangan kalsium tersebut. Fosfor yang terikat dengan
kalsium akan ikut terbebaskan dari tulang dan diekskresikan. Absorpsi kalsium
dari usus juga diatur oleh hormon paratinoid dengan memproduksi
1,25-dihidroksikolekalsiferol yang merupakan derivat dari vitamin D yang sangat
2.4 Hal Yang Mempengaruhi Absorpsi Kalsium
Penyerapan kalsium dipengaruhi umur dan kondisi tubuh. Pada usia
kanak-kanak atau masa pertumbuhan, sekitar 50-70% kalsium yang dicerna
diserap. Tetapi pada usia dewasa, hanya sekitar 10-40% yang mampu diserap
tubuh. Penyerapan kalsium terjadi pada usus kecil bagian atas, tepat setelah
lambung. Penyerapan kalsium dapat dihambat apabila ada zat organik yang dapat
bergabung dengan kalsium dan membentuk garam yang tidak larut. Contoh
senyawa organik tersebut adalah asam oksalat dan asam fitat. Kalsium dan asam
okasalat akan membentuk garam kalsium oksalat yang tidak larut. Asam oksalat
banyak ditemukan dalam bit yang masih hijau, bayam rhubarb dan coklat. Asam
fitat banyak terkandung dalam bekatul gandum merah (Winarno, 2004).
Serat dapat menurunkan absorpsi kalsium, karena serat menurunkan waktu
transit makanan dalam saluran cerna, sehingga menurunkan kesempatan untuk
absorpsi. Keadaan stres mental juga dapat menurunkan absorpsi dan
meningkatkan ekskresi kalsium. Dalam suasana basa dengan fosfor, kalsium
membentuk kalsium fosfat yang tidak larut air yang dapat menyebabkan absorpsi
kalsium (Winarno, 2004).
2.5 Akibat Kekurangan Dan Kelebihan Kalsium
Pada masa pertumbuhan, kekurangan kalsium dapat mengganggu
pertumbuhan. Tulang kurang kuat, mudah bengkok dan rapuh. Setelah dewasa,
terutama setelah usia 50 tahun, terjadi kehilangan kalsium dari tulang yang
menyebabkan tulang menjadi rapuh dan mudah patah. Keadaan ini dikenal
itu, kekurangan kalsium juga dapat mnyebabkan osteomalasia yang biasanya
terjadi karena kekurangan vitamin D dan ketidakseimbangan konsumsi kalsium
terhadap fosfor. Terganggunya mineralisasi matriks tulang yang menyebabkan
menurunnya kandungan kalsium dalam tulang. Rendahnya kadar kalsium dalam
darah dapat menyebabkan tetani atau kejang. Kelebihan kalsium dapat
menyebabkan batu ginjal atau gangguan ginjal. Selain itu dapat juga
menyebabkan konstipasi. Karena itu, sebaiknya konsumsi kalsium tidak melebihi
2500 mg sehari (Almatsier, 2004).
2.6 Sumber Kalsium
Susu dan produk olahan susu seperti keju dan es krim merupakan sumber
kalsium yang utama. Sayuran tertentu seperti brokoli, kacang-kacangan dan
buah-buahan juga merupakan sumber kalsium (Suhardjo, 2000).
Selain itu ikan yang dimakan dengan tulangnya termasuk ikan kering
merupakan sumber kalsium yang baik. Serelia, kacang-kacangan dan hasil
olahannya seperti tahu dan tempe, dan sayuran hijau merupakan sumber kalsium
yang baik juga. Tetapi bahan ini mengandung banyak zat-zat yang menghambat
penyerapan kalsium seperti serat, fitat dan oksalat (Almatsier, 2004).
Ikan teri merupakan salah satu sumber kalsium yang terjangkau oleh
seluruh kalangan karena harganya yang murah dan mudah didapat. Berdasarkan
Nutry Survey Indonesia, kandungan kalsium dalam ikan teri lebih tinggi daripada
susu, dan akan bermanfaat jika dikonsumsi langsung. Dalam tubuh kalsium
bekerja sama dengan laktosa dan vitamin D dalam pembentukan massa tulang,
2.7 Ikan Teri
Ikan teri (teri) masuk dalam famili Engraulidae dengan nama ilmiah
Stolephorus sp. Deskripsinya adalah sebagai berikut: a. badan seperti cerutu,
sedikit silindris; b. bagian perut membulat; c. kepala pendek; d. moncong nampak
jelas dan meruncing; e. anal sirip dubur sedikit kebelakang; f. duri-duri lemah
sirip punggung; g. warna pucat bila sisik terlepas (La Anas, 2008).
Ikan teri hampir dapat dijumpai di seluruh lautan kecuali daerah Kutub,
mulai dari Samudera Atlantik, Samudera Hindia dan Samudera Pasifik, dan lebih
senang berada di perairan yang beriklim sedang. Pada umumnya, teri dapat
beradaptasi dengan berbagai suhu dan salinitas air. Bentuk tubuhnya memanjang
dan terlihat sangat ramping, berkisar 2 – 40 cm, warna tubuhnya seperti perak
mengkilat. Sebagai ikan pelagis yang berukuran kecil, ikan teri hidup
bergerombol. Biasanya gerombolan Teri dapat dijumpai di daerah perairan yang
dangkal, air payau yang berdasar lumpur, seperti daerah muara dan teluk. Proses
bertelur (pemijahan) ikan teri terjadi antara bulan Oktober dan Maret, setidaknya
62 mil dari pantai dan dekat dari permukaan air. Ikan teri akan memijah di air
yang agak hangat atau paling tidak suhu air > 12°C (Anonim, 2010).
Di perairan laut Indonesia ditemukan sembilan jenis Stolephorus. Teri
merupakan satu diantara ikan yang terkenal. Teri ditangkap dalam jumlah banyak
dan dijual dalam keadaan segar atau setelah dijadikan ikan asin (Utami, 2001).
2.8 Komposisi Ikan
Hewan mempunyai peranan yang sangat kecil dalam makanan kita.
1% jumlah kalori yang kita makan. Dari keseluruhan protein yang kita makan,
hanya 3% dari daging, 7% dari ikan dan kurang dari 1% berasal dari
masing-masing susu dan telur. Ikan merupakan salah satu makanan yang memenuhi
kriteria gizi berimbang. Daging ikan merupakan bahan biologis yang tersusun dari
protein, karbohidrat, lemak, vitamin, enzim dan sebagainya. Unsur-unsur
anorganik terbanyak pada ikan adalah kalsium, fosfor dan sulfur. Seperlima (20%)
daging ikan tersusun dari protein, lemak 5%, mineral 5%, vitamin, serat dan air
70% (Saparinto, 2006).
Ikan teri merupakan salah satu sumber kalsium terbaik untuk mencegah
pengeroposan tulang. Ikan teri merupakan sumber kalsium yang tahan dan tidak
mudah larut dalam air. Kandungan gizi dalam 100 gram teri segar meliputi energi
77 kkal; protein l6gr; lemak 1.0 gr; kalsium 500 mg; phosfor 500 mg; besi 1.0 mg;
Vit A RE 47; dan Vit B 0.1 mg (Isnandi, 2008).
Ikan merupakan sumber protein dan lemak, namun komposisinya sangat
bervariasi antara ikan yang satu dengan ikan lainnya. Perbedaan komposisi baik
jumlah maupun komponen penyusunnya disebabkan oleh berbagai faktor, dapat
berasal dari dalam maupun dari luar tubuh ikan sendiri (Saparinto, 2006).
Faktor intrinsik adalah jenis dan golongan ikan, umur ikan, jenis kelamin
dan sifat turunan. Faktor yang paling berpengaruh adalah jenis golongan ikan.
Pengaruh umur dalam variasi komposisi kimia terlihat pada kandungan lemak
daging ikan. Semakin tua ikan, maka kandungan lemaknya akan cenderung makin
banyak. Ikan yang memakan jenis ikan lainnya, komposisi dagingnya berbeda
dengan ikan yang hanya memakan tumbuhan. Faktor ekstrinsik antara lain daerah
2.9 Penetapan Kadar Kalsium
Penetapan kadar kalsium dapat dilakukan dengan metode gravimetri,
spektrofotometri serapan atom dan titrasi kompleksometri. Pada metode
gravimetri, kalsium diendapkan sebagai kalsium oksalat dengan mengolah suatu
larutan dalam asam klorida panas dengan amonium oksalat dan perlahan-lahan
menetralkan dengan larutan air-amonia. Endapan dicuci dengan larutan amonium
oksalat encer dan kemudian ditimbang sebagai kalsium karbonat dengan
memanaskan pada suhu 475-525oC dalam tanur listrik (Basset, 1994).
Pada spektrofotometri serapan atom, pengukuran kadar kalsium
berdasarkan radiasi yang diserap oleh atom yang tidak tereksitasi dalam bentuk
uap. Pada suhu nyala udara etilen (± 2300oC) atom kalsium berada dalam keadaan
dasar. Jika seberkas energi radiasi yang terdiri dari spektrum untuk kalsium
dilewatkan melalui nyala ini, sdejumlah atom dalam keadaan dasar akan
menyerap energi dari panjang gelombangyang khas dan mencapai keadaan energi
yang lebih tinggi. Jumlah energi radiasi yang diserap berbanding lurus dengan
konsentrasi unsur dalam suatu larutan sampel (Basset,1994).
Titrasi kompleksometri yaitu titrasi berdasarkan pembentukan kompleks
antara kation dengan zat pembentuk kompleks. Sebagai zat pembentuk kompleks
yang banyak digunakan adalah garam dinatrium etilen diamin tetra asetat
(dinatrium EDTA). Untuk setiap ml larutan dinatrium EDTA setara dengan 2,004
2.10 Titra Tit menentuka etilen diam dapat mem EDTA de membentu alkali tana (Rohman, Re
dapat d ilih
Un Penambah dengan sej akan mem Indikator eriokrom jingga pir hidroksi n asi Komple trasi kompl
an kadar g
min tetra a
mbentuk ko engan loga uk komplek ah dilakuka 2007). eaksi pembe hat dibawah ntuk menen han indikato jumlah keci mecah komp yang digu (Eriochrom
rokatekol; j
naftol (Rohm
eksometri
leksometri m
garam-garam
setat (EDT
ompleks yan
am alkali
ks yang tid
an pada pH
entukan kom
h ini:
ntukan titik
or sebelum t
il logam. Pa
pleks logam
unakan unt
m Black T, M
jingga xilen
man, 2007).
merupakan
m logam. T
TA). Kecual
ng stabil de
tanah sep
dak stabil.
10 dengan
mpleks kals
k akhir tit
titrasi akan
ada saat titi
m-indikator d tuk titrasi Mordant Bl nol; asam metode ya Titran yang
li dengan n
engan semu perti kalsiu Karenanya n mengguna sium denga trasi diguna membentuk
k akhir titra
dan mengha
komplekso
lack II, Sol
kalkon kar
ang sering d
g sering di
natrium dan
ua logam. P
um dan m
titrasi untu
akan larutan
an etilen dia
akan indika
k kompleks
asi, sedikit k
asilkan warn
ometri anta
ochrome B
rbonat; kalm
digunakan u
igunakan a
n kalium, E
Pada pH re
magnesium
uk logam-l
n bufer amm
amin terta a
kator zat w
s antara indi
kelebihan E
na yang ber
ara lain: H
2.11 Macam-Macam Titrasi Kompleksometri
1. Titrasi Langsung
Larutan yang mengandung ion logam dibuferkan sampai pH yang
dikehendaki, dan dititrasi langsung dengan larutan EDTA standar. Untuk
mencegah terjadinya pengendapan hidroksida logam, ditambahkan sedikit zat
pengkompleks pembantu seperti tartrat, sitrat atau trietanolamin. Pengurangan
kadar logam pada titik ekivalen ditetatpkan dari perubahan warna suatu indikator
logam yang berespon terhadap perubahan-perubahan pM. Titik akhir titrasi juga
dapat ditetapkan dengan metode-metode amperometri, konduktometri, atau dalam
beberapa keadaan dapat dengan metode potensiometri (Basset, 1994).
2. Titrasi Kembali
Metode ini digunakan bila reaksi antara kation dan EDTA lambat atau
tidak tersedia indikator yang cocok. EDTA ditambahkan berlebih dan
kelebihannya dititrasi dengan suatu larutan standar magnesium dengan
menggunakan kalmagit sebagai indikator. Kompleks magnesium EDTA yang
kestabilan nya lebih rendah dan kation yang akan ditetapkan, tidak terseger oleh
magnesium. Metode ini dapat digunakan untuk menetapkan logam dalam
endapan-endapan, seperti timbel dalam timbel sulfat dan kalsium dalam kalsium
oksalat (Underwood, 1986).
3. Titrasi Substitusi
Apabila ion logam tidak memberikan hasil yang jelas bila dititrasi secara
langsung atau dengan titrasi kembali, maka dapat ditetapkan dengan
menggunakan metode ini. Atau jika ion logam tersebut membentuk kompleks
kalsium. Kalsium, timbal dan raksa dapat ditentukan dengan metode ini dengan
menggunakan indikator hitam eriokrom dengan hasil yang memuaskan (Rohman,
2007).
4. Titrasi Alkalimetri
Bila suatu larutan dinatrium etilendiamintetraasetat, Na2H2Y, ditambahkan
kepada suatu larutan yang mengandung logam dan terbentuk kompleks yang
disertai pembebasan dua ekivalen ion hidrogen. Ion hidrogen yang dibebaskan
dapat dititrasi dengan larutan natrium hidroksida standar dengan menggunakan
indikator asam-basa, atau secara potensiometri. Larutan logam yang akan
ditetapkan harus dinetralkan dengan tepat sebelum titrasi. Hal ini sangat sukar
dilakukan karena hidrolisis banyak garam dan merupakan kelemahan titrasi
alkalimetri (Basset, 1994).
2.12 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunakannya.
Beberapa parameter analisis yang harus dipertimbangkan adalah sebagai berikut:
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedeakatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan hasil
Metode simulasi
Metode simulasi dilalukan dengan menambahkan sejumlah analit murni
kedalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran
tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang
ditambahkan (kadar yang sebenarnya) (Harmita, 2004).
Metode penambahan baku
Metode ini dilakukan dengan cara menambahkan sejumlah analit dengan
konsentrasi tertentu pada sampel yang diperiksa, lalu di analisis dengan metode
yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa
penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan kedalam sampel dapat
ditemukan kembali. Rentang persen perolehan kembali yang diizinkan pada setiap
konsentrasi analit pada matriks dapat dilihat pada Tabel 1.
Tabel 1. Rentang persen perolehan kembali yang diizinkan Jumalah analit pada matriks sampel
(%)
Persen perolehan kembali yang diizinkan (%)
100 98 – 102
>10 98 – 102
>1 97 – 103
>0,1 95 – 105
0,01 90 – 107
0,001 90– 107
(Harmita, 2004)
b.Keseksamaan
Kesekamaan (presisi) diukur sebagai simpangan baku relatif atau koefisien
variasi. Keseksamaan merupakan ukuran yanmg menunjukkan derajat kesesuaian
antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk
c. Selektivitas
Selektivitas (spesifisitas) metode yang mengacu pada sejauh mana ia dapat
menentukan analit tertentu (s) dalam campuran yang kompleks tanpa gangguan
dari komponen lain dalam campuran (APVMA, 2004).
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon
baik secara langsung maupun dengan bantuan transformasi matematika,
menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit
dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang
dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima
(Harmita, 2004).
e. Batas deteksi dan batas kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam smapel yang masih dapat memenuhi
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini merupakan penelitian deskriptif, yang mendeskripsikan
kadar kalsium dalam ikan teri. Penelitian dilakukan di Laboratorium Kimia
Farmasi Kuantitatif Fakultas Farmasi USU pada bulan Februari – April 2011.
3.2 Bahan-Bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah ikan teri tawar kering
yang berasal dari pasar Kembang Tanjong dan pasar Teupen Raya Kabupaten
Pidie NAD (Gambar dapat dilihat pada Lampiran 1, Halaman 32).
3.2.2 Pereaksi
Bahan-bahan yang digunakan dalam penelitian ini adalah berkualitas pro
analisis dari E.Merck jika tidak dinyatakan lain yaitu: asam nitrat, hidrogen
peroksida, natrium hidroksida, hidroksilamin HCl, kalium sianida, dinatium etilen
diamin tetra asetat, kalkon, natrium sulfat anhidrat, zink sulfat, amonium klorida,
eriokrom black T, natrium klorida, kalsium karbonat, asam klorida, asam sulfat,
etanol, amonium oksalat, dan akuades (laboratorium Kimia Farmasi Kuantitatif).
3.3 Alat-Alat
Neraca analitik (Boeco Germany), blender, hot plate, pH indikator
3.4 Prosedur Penelitian
3.4.1 PengambilanSampel
Pengambilan sampel dilakukan dengan cara membeli dari pedagang di
pasar Kembang Tanjong dan pasar Teupen Raya. Pengambilan sampel dilakukan
secara sampling purposive yang dikenal juga sebagai sampling pertimbangan
dimana pengambilan sampel dilakukan berdasarkan pertimbangan bahwa semua
ikan teri homogen kandungan kalsiumnya.
3.4.2 Pembuatan Pereaksi
3.4.2.1 Larutan NaOH 30% b/v
Pembuatan larutan NaOH 30% b/v sesuai dengan prosedur yang tercantum
pada Farmakope Indonesia Edisi III tahun 1979. Dilarutkan 30 gram NaOH
dengan sejumlah akuades, diencerkan dengan akuades sampai 100 ml.
3.4.2.2 Larutan Hidroksilamin HCl 10% b/v
Pembuatan larutan hidroksilamin HCl 10% b/v sesuai dengan prosedur
yang tercantum pada Farmakope Indonesia Edisi III tahun 1979. Dilarutkan 10
gram hidroksilamin HCl dengan sedikit akuades, dan diencerkan dengan akuades
sampai 100 ml.
3.4.2.3 Larutan Na2EDTA 0,05 M
Pembuatan larutan Na2EDTA 0,05 M sesuai dengan prosedur yang
tercantum pada Farmakope Indonesia Edisi III tahun 1979. Sebanyak 18,61 gram
Na2EDTA dilarutkan dalam sejumlah akuades. Diencerkan dengan akuades
3.4.2.4 Indikator Kalkon Campur 1% b/b
Pembuatan indikator kalkon campur 1% b/b sesuai dengan prosedur yang
tercantum pada Farmakope Indonesia Edisi III tahun 1979. Kalkon ditimbang
sebanyak 100 mg, dicampur dengan 10 gram natrium sulfat anhidrat.
3.4.2.5 Larutan Dapar Amonium Klorida pH 10
Pembuatan larutan dapar amonium klorida pH 10 sesuai dengan prosedur
yang tercantum pada Farmakope Indonesia Edisi III tahun 1979. Dilarutkan 7
gram amonium klorida p dalam 57 ml amonia p, diencerkan dengan akuades
secukupnya hingga 100 ml.
3.4.2.6 Indikator Eriokrom Black T 1% b/b
Pembuatan indikator eriokrom black T 1% b/b sesuai dengan prosedur
yang tercantum pada Farmakope Indonesia Edisi III tahun 1979. Dicampur 10 mg
EBT dan 1 gram natrium klorida, digerus sampai homogen.
3.4.2.7 Larutan Asam Klorida 7,4% b/v
Pembuatan larutan asam klorida 7,4% b/v sesuai dengan prosedur yang
tercantum pada Farmakope Indonesia Edisi III tahun 1979. Dilarutkan 20 ml asam
klorida 37% dalam 100 ml akuades.
3.4.2.8 Larutan Natrium Hidroksida 4,0% b/v
Pembuatan larutan natrium hidroksida 4,0% b/v sesuai dengan prosedur
yang tercantum pada Farmakope Indonesia Edisi III tahun 1979. Dilarutkan 4
gram natrium hidroksida dengan sejumlah akuades bebas CO2 dan diencerkan
3.4.2.9 Larutan Amonium Oksalat 2,5% b/v
Pembuatan larutan amonium oksalat 2,5% b/v sesuai dengan prosedur
yang tercantum pada Farmakope Indonesia Edisi III tahun 1979. Dilarutkan 2,5
gram amonium oksalat dengan sejumlah akuades, diencerkan dengan akuades
sampai 100 ml.
3.4.2.10 Asam Sulfat Encer
Tambahkan secara hati-hati 57 ml asam sulfat P ke dalam lebih kurang
100 ml air, didinginkan hingga suhu kamar dan diencerkan dengan akuades
hingga 1000 ml.
3.4.2.11 Pembuatan Larutan Baku Kalsium
Pembuatan larutan baku kalsium sesuai dengan prosedur yang tercantum
pada Farmakope Indonesia Edisi III tahun 1979. Sebanyak 1 gram kalsium
karbonat dimasukkan kedalam labu tentukur 100 ml, ditambahkan 20 ml akuades.
Digoyangkan hingga terbentuk bubur, ditutup mulut labu. Ditambahkan 10 ml
asam klorida 7,4% b/v dengan pipet disisipkan diantara mulut labu dengan tutup
labu, digoyang untuk melarutkan kalsium karbonat. Dibilas mulut labu, tutup labu
dan permukaan pipet bagian luar dengan akuades. Diencerkan dengan akuades
sampai garis tanda.
3.4.3 Pembakuan Dinatrium EDTA
Ditimbang seksama ± 220 mg ZnSO4.7H2O, dilarutkan dalam 25 ml air,
ditambahkan 5 ml dapar ammonium klorida pH 10 kemudian ditambahkan 50 mg
indikator Hitam Eriokrom T campur, dititrasi dengan Na2EDTA sampai terjadi
warna biru yang stabil (Ditjen POM, 1979). Normalitas Na2EDTA dihitung
Normalitas Na2EDTA =
O H . ZnSO BE Vb Vt
W
2 47 )
(
Keterangan:
W = Berat ZnSO4.7H2O (mg)
Vt = Volume larutan Na2EDTA titrasi ZnSO4
Vb = Volume larutan Na2EDTA titrasi blanko
Data dan contoh perhitungan normalitas Na2EDTA dapat dilihat pada Lampiran
2 Halaman 33.
3.4.4 Penetapan Kadar Kalsium Karbonat
Ditimbang saksama 100 mg kalsium karbonat. Dimasukkan ke dalam
erlenmeyer 250 ml, ditambahkan 10 ml air dan digoyangkan sampai menjadi
bubur. Ditutup dengan gelas arloji, ditambahkan 2 ml asam klorida 7,4% b/v
dengan menyisipkan pipet di antara gelas arloji dan mulut erlenmeyer.
Digoyangkan sampai kalsium karbonat larut. Dibilas gelas arloji, bagian luar pipet
dan bagian pinggir erlenmeyer dengan menggunakan akuades. Ditambahkan
akuades sampai volume 50 ml. Ditambahkan 15 ml larutan dinatrium edetat
0,0485 N dari buret 50 ml sambil diaduk. Ditambahkan 15 ml natrium hidroksida
4% b/v. Dititrasi dengan larutan dinatrium edetat menggunakan 300 mg indikator
kalkon campur hingga terbentuk warna biru (Depkes RI, 1979). Kadar kalsium
karbonat baku dihitung dengan menggunakan rumus:
% Kalsium = ( ) x100%
W
N x Ca atom berat x Vb
Vt
Keterangan:
Vt = volume larutan Na2EDTA titrasi CaCO3 (ml)
N = normalitas Na2EDTA (N)
W = berat kalsium karbonat (mg)
Data dan contoh perhitungan kadar kalsium dalam kalsium karbonat dapat dilihat
pada Lampiran 3 Halaman 35.
3.4.5 Penetapan Kadar Air
Ikan teri ditimbang ±100 gram, dan dihaluskan dengan menggunakan
blender. Ditimbang seksama 5 gram ikan teri yang telah dihaluskan, lalu
dimasukkan kedalam krus porselen yang telah dikeringkan selama 30 menit pada
suhu 105oC dan ditimbang. Diratakan dengan menggoyangkan secara perlahan.
Dimasukkan kedalam oven dengan suhu 105oC selama 3 jam. Didinginkan dan
ditimbang. Dilanjutkan pengeringan dengan jarak waktu penimbangan selama 1
jam (Ditjen POM, 1995). Kadar air dihitung dengan menggunakan rumus di
bawah ini:
% 100 n
dikeringka sebelum
Berat
n dikeringka setelah
Berat -n dikeringka sebelum
Berat air
Kadar
% x
Data dan contoh perhitungan kadar air pada sampel yang dianalisis dapat dilihat
pada Lampiran 5 Halaman 37.
3.4.6 Proses Destruksi Basah
Daging ikan yang telah dihaluskan ditimbang seksama masing-masing 10
gram, dimasukkan ke dalam erlenmeyer, kemudian ditambahkan 20 ml HNO3
65% b/v dan 6 ml H2O2 50% b/v (Brix,1983). Lalu didiamkan selama 24 jam
dengan tujuan agar dapat mempercepat proses destruksi yang akan dilakukan.
Setelah itu dipanaskan pada suhu ± 100oC dengan menggunakan hot plate selama
3 jam hingga sampel berwarna kuning muda jernih. Dipindahkan kedalam labu
Kemudian disaring dengan menggunakan kertas saring dengan membuang 10 ml
larutan pertama hasil penyaringan. Larutan hasil destruksi ini digunakan untuk uji
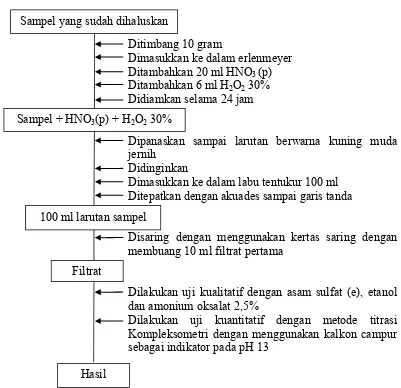
kualitatif dan uji kuantitatif (Haswell, 1991). Bagan alir proses destruksi basah
dapat dilihat pada Gambar 1 di bawah ini.
Ditimbang 10 gram
Dimasukkan ke dalam erlenmeyer Ditambahkan 20 ml HNO3 (p) Ditambahkan 6 ml H2O2 30% Didiamkan selama 24 jam
Dipanaskan sampai larutan berwarna kuning muda jernih
Didinginkan
Dimasukkan ke dalam labu tentukur 100 ml Ditepatkan dengan akuades sampai garis tanda
Disaring dengan menggunakan kertas saring dengan membuang 10 ml filtrat pertama
Dilakukan uji kualitatif dengan asam sulfat (e), etanol dan amonium oksalat 2,5%
[image:39.595.113.514.186.574.2]Dilakukan uji kuantitatif dengan metode titrasi Kompleksometri dengan menggunakan kalkon campur sebagai indikator pada pH 13
Gambar 1. Bagan Alir Proses Destruksi Basah
2.4.7 Analisis Kualitatif
Hasil destruksi dilarutkan dalam beberapa ml air, dimasukkan ke dalam
labu tentukur 100 ml dan ditambahkan akuades sampai garis tanda, dan disaring.
Filtrat digunakan uji kualitatif dengan menggunakan pereaksi: Sampel yang sudah dihaluskan
Sampel + HNO3(p) + H2O2 30%
100 ml larutan sampel
1. Cairan jernih diambil ± 2 ml dan dimasukkan kedalam tabung reaksi, lalu
ditambahkan ± 1 ml larutan ammonium oksalat 2,5% b/v, dikocok dan
didiamkan. Terbentuk endapan putih (Svehla, 1990).
2. Diambil ± 2 ml larutan jernih dan dimasukkan ke dalam tabung reaksi, lalu
ditambahkan 1 ml H2SO4(e) dan 1 ml etanol, dikocok dan didiamkan.
Terbentuk endapan putih berupa kristal jarum (Svehla,1990).
2.4.8 Analisis Kuantitatif
Hasil destruksi dilarutkan dalam beberapa ml air, dimasukkan ke dalam
labu tentukur 100 ml kemudian ditambahkan air sampai garis tanda, kemudian
disaring. Diambil 25 ml, diencerkan dengan air suling hingga 100 ml,
ditambahkan 8 ml NaOH 30% b/v, 5 ml larutan hidroksilamin HCl 10% b/v dan
30 mg KCN. Kemudian dititrasi dengan Na2EDTA 0,0485 N, dan pada lebih
kurang 2 ml sebelum titik akhir titrasi, ditambahkan 100 mg indikator kalkon
campur. Titrasi dilanjutkan hingga warna larutan berubah dari merah ungu
menjadi hijau. Perlakuan diulangi sebanyak 6 kali (Basset, 1994).
2.5.9 Penentuan Uji Perolehan Kembali
10 gram ikan teri yang telah dihaluskan, dimasukkan kedalam erlenmeyer
250 ml, ditambahkan 10 ml larutan baku kalsium. Dilakukan proses yang sama
seperti prosedur 3.5.3 dan 3.5.5 Persen recovery dihitung dengan rumus:
% 100 n
ditambahka yang
standar larutan
kadar
sampel kadar
-standar) (sampel
l kadar tota Recovery
% x
2.5.10 Analisis Data Secara Statistik
Hasil yang diperoleh dari satu seri penetapan kadar terhadap satu macam
dengan yang lain sehingga timbul kecenderungan untuk menolak hasil yang
sangat menyimpang (Rohman, 2007).
Untuk memastikan hasil yang sangat menyimpang ditolak atau diterima,
perlu dilakukan analisis data secara statistikam pada taraf kepercayaan 95% (α =
0,05), hasil analisis ditolak jika Qhitung > Qtabel (Rohman, 2007).
Untuk menghitung nilai Q digunakan rumus:
terendah yang
nilai tertinggi nilai
terdekat yang
nilai -dicurigai yang
nilai Qhitung
Selanjutnya nilai Qhitung ini dibandingkan dengan nilai Qtabel. Jika nilai
Qhitung ini lebih kecil dari Qkritis, maka hipotesis diterima (Rohman, 2007).
2.5.11 Kadar Kalsium
Kadar yang diperoleh dari hasil pengukuran larutan sampel, ditentukan
rata-ratanya secara statistik dengan taraf kepercayaaan 95% (Wibisono, 2005)
dengan rumus sebagai berikut:
µ = X± t(1/2,df) s/ √ n
keterangan :
µ = interval kepercayaan kadar sampel
X = kadar rata-rata sampel
t(1/2,df) = nilai tkritis dengan df (derajat bebas) = n-1 dan α = 0,05
s = standar deviasi
n = jumlah perlakuan
data diterima jika tidak berbeda secara bermakna pada interval
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
mengetahui ada tidaknya kalsium dalam sampel. Pereaksi yang digunakan untuk
analisis kualitatif adalah asam sulfat encer dan etanol dan amonium oksalat 2,5%
b/v. Hasil analisis kualitatif logam kalsium dalam sampel dapat dilihat pada Tabel
[image:42.595.119.507.309.391.2]1 dan Lampiran 6 Halaman 39.
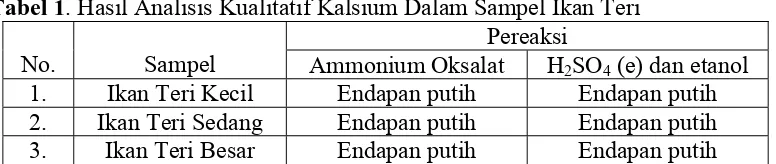
Tabel 1. Hasil Analisis Kualitatif Kalsium Dalam Sampel Ikan Teri
No. Sampel
Pereaksi
Ammonium Oksalat H2SO4 (e) dan etanol
1. Ikan Teri Kecil Endapan putih Endapan putih
2. Ikan Teri Sedang Endapan putih Endapan putih
3. Ikan Teri Besar Endapan putih Endapan putih
Tabel di atas menunjukkan bahwa ketiga sampel mengandung logam
kalsium. Sampel dikatakan positif mengandung kalsium jika terbentuk endapan
putih dengan penambahan ammonium okasalat. Dan dengan penambahan asam
sulfat encer dan etanol akan membentuk endapan putih berupa kristal jarum yang
dapat dilihat di bawah mikroskop (Svehla, 1990).
4.2 Analisis Kuantitatif
4.2.1 Penetapan Kadar Air Dalam Sampel Ikan Teri
Hasil penetapan kadar air pada sampel dapat dilihat pada Tabel 2.
Tabel 2. Hasil Penetapan Kadar Air Pada Sampel Ikan Teri
No. Asal Sampel Kadar Air (%)
1. Pasar Kembang Tanjong Ikan Teri Kecil 17,27
Ikan Teri Sedang 17,29
Ikan Teri Besar 17,32
2. Pasar Teupen Raya Ikan Teri Kecil 17,20
Ikan Teri Sedang 17,19
Dari Tabel dapat dilihat bahwa kadar air dalam ikan teri tersebut tidak jauh
berbeda. Ini menunjukkan bahwa kadar air ini tidak terlalu berpengaruh pada
perbedaan kadar kalsium pada ikan teri.
4.2.2 Analisis Kadar Kalsium Dalam Sampel Ikan Teri
Penetapan kadar kalsium dilakukan secara titrasi kompleksometri. Data
dan contoh perhitungan dapat dilihat pada Lampiran 7 Halaman 40 dan
Lampiran 8 Halaman 42. Penetapan kadar kalsium juga dilakukan dihitung
terhadap berat kering ikan teri. Data dan contoh perhitungan dapat dilihat pada
Lampiran 9 Halaman 44.
Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat
dilihat pada Lampiran 13 Halaman 48). Hasil analisis kuantitatif kalsium pada
[image:43.595.114.506.422.547.2]sampel dapat dilihat pada Tabel 3.
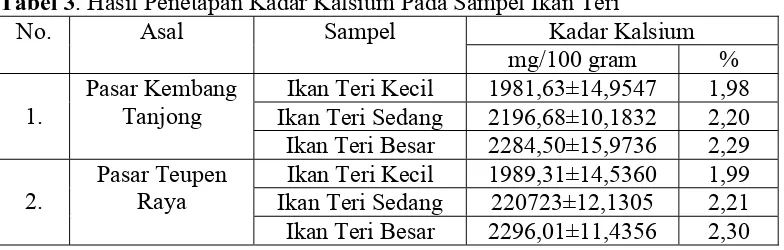
Tabel 3. Hasil Penetapan Kadar Kalsium Pada Sampel Ikan Teri
No. Asal Sampel Kadar Kalsium
mg/100 gram %
1.
Pasar Kembang Tanjong
Ikan Teri Kecil 1981,63±14,9547 1,98 Ikan Teri Sedang 2196,68±10,1832 2,20 Ikan Teri Besar 2284,50±15,9736 2,29
2.
Pasar Teupen Raya
Ikan Teri Kecil 1989,31±14,5360 1,99 Ikan Teri Sedang 220723±12,1305 2,21 Ikan Teri Besar 2296,01±11,4356 2,30
Dari tabel di atas dapat dilihat bahwa ada perbedaan kadar kalsium pada
ikan teri kecil dengan ikan teri sedang, antara ikan teri sedang dan ikan teri besar
baik yang berasal dari pasa Kembang Tanjong maupun yang berasal dari pasar
Teupen Raya. Perbedaan ini dapat dikarenakan perbedaan bentuk tulang dari ikan
teri. Tulang ikan teri kecil lebih lunak dan halus dibandingkan dengan tulang ikan
Menurut Direktorat Gizi Depkes RI (1996), kadar kalsium pada ikan teri
nasi kering adalah 1000 mg/100 gram sampel. Sedangkan untuk ikan teri kering
adalah 1200 mg/100 gram sampel, dan 2381 mg/100 gram sampel untuk ikan teri
kering sekali. Dari hasil pengujian didapat bahwa kadar kalsium lebih tinggi pada
ikan teri besar dari pada ikan teri kecil.
Dilakukan uji beda rata-rata secara statistik dengan distribusi t pada taraf
kepercayaan 95% (perhitungan dapat dilihat pada Lampiran 14 sampai 28,
Halaman 55 sampai 83). Dari perhitungan diperoleh bahwa Hipotesa (Ho)
diterima untuk perbandingan kadar kalsium dari ikan teri dari dua pasar, yaitu
tidak terdapat perbedaan kadar kalsium dari ikan teri yang berasal dari pasar
Kembang Tanjong dengan pasar Teupen Raya untuk jenis ikan teri yang sama.
Sedangkan untuk perbandingan kadar kalsium pada beberapa jenis ikan teri,
Hipotesa (Ho) ditolak. Yaitu terdapat perbedaan kadar kalsium pada jenis ikan teri
yang berbeda.
4.2.3 Uji Perolehan Kembali
Hasil uji perolehan Kembali dapat dilihat bahwa perolehan Kembali
kalsium yang ditambahkan sebesar 98,42% dan persen RSD rata-rata adalah
0,0979%. Data, hasil perhitungan dan contoh perhitungan uji perolehan kembali
dapat dilihat pada Lampiran 10 Halaman 45 dan Lampiran 11 Halaman 46.
Perhitungan koefisien variasi (%RSD) dapat dilihat pada Lampiran 12 Halaman
47. Kisaran rata-rata hasil uji perolehan kembali yang diizinkan untuk >1% adalah
97-103%, sedangkan persen RSD yang diizinkan adalah tidak lebih dari 2%
(Harmita, 2004). Dari hasil yang diperoleh tersebut dapat disimpulkan bahwa
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil pengujian dapat disimpulkan bahwa kadar kalsium pada ikan
teri dapat ditetapkan dengan metode titrasi kompleksometri. Hasil pengujian
diperoleh kadar kalsium dalam ikan teri yang berasal dari pasar Kembang
Tanjong adalah: ikan teri kecil 1981,63 ± 14,9547 mg/100 gram, ikan teri sedang
2196,68 ± 10,1832 mg/100 gram dan ikan teri besar 2284,50 ± 15,9736 mg/100
gram. Sedangkan untuk ikan teri yang berasal dari pasar Teupen Raya adalah:
ikan teri kecil, 1989 ± 14,5360 mg/100 gram, ikan teri sedang 2207,23 ± 12,1305
mg/100 gram dan ikan teri besar 2296,01 ± 11,4356 mg/100 gram.
Terdapat perbedaan yang signifikan kadar kalsium antara ikan teri kecil,
dengan ikan teri sedang dan besar yang berasal dari pasar Kembang Tanjong.
Pada ikan teri yang berasal dari pasar Teupen Raya, juga terdapat perbedaan yang
signifikan kadar kalsium antara ikan teri kecil, ikan teri sedang dan ikan teri besar.
Hasil penelitian ini menunjukkan bahwa kadar kalsium dalam ikan teri
cukup tinggi, sehingga dapat menjadi salah satu sumber kalsium yang baik selain
susu dan produk olahan susu. Dengan mengkonsumsi ikan teri 50 g, sudah
mencukupi kebutuhan kalsium harian menurut angka kecukupan gizi.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk memeriksa kadar mineral
DAFTAR PUSTAKA
Ahira, A. (2010). Mengenal Manfaat Ikan Teri.
http://www.anneahira.com/ikan/ikan-teri.htm. Tanggal akses 30 Oktober 2010.
Almatsier, S. (2001). Prinsip Dasar Ilmu Gizi. Jakarta : Gramedia Pustaka Utama. Jakarta : Hal : 228, 235, 242.
Anonim. (2010). Si Kecil Yang Kaya Nutrisi.
http://ikanlautindonesia.blogspot.com/2010/02/si-kecil-yang-kaya nutrisi.html. Tanggal akses 16 Maret 2011.
Australian Pesticides & Veterinary Medicines Authority. (2004). Guidelines For The Validation Of Analytical Methods For Active Constituent, Agricultural
And Veterinary Chemical Products. Australia: APVMA. Hal: 3-6.
Basset, J, dkk. (1994). Vogel Kimia Analisis Kuantitatif Anorganik. Jakarta. Penerbit Buku Kedokteran. Hal: 373.
Brix, H., dkk. (1983). The Reproducibility In The Determination Of Heavy Metals
In Marine Plant Material. Amsterdam: Elsevier Scientific Publishing
Company. Hal: 73.
Darmono. (1995). Logam Dalam Sistem Biologi Makhluk Hidup. Jakarta. UI-Press. Hal: 49-50, 124.
Direktorat Gizi Departemen Kesehatan RI. (1996). Daftar Komposisi Bahan
Makanan. Jakarta: Penerbit Bhratara. Hal: 27-28.
Ditjen POM, (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan Republik Indonesia. Jakarta. Hal: 53, 644, 649, 653, 665, 683, 693, 712, 745.
Ditjen POM, (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan Republik Indonesia. Jakarta. Hal: 1036.
Harmita. (2004). Petunjuk Pelaksaan Validasi Metode Dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. Vol.1 No.3. Hal: 117-119, 122, 123, 127, 128, 130-132.
Hasswell, S. J. (1991). Atomic Absorption Spectrometry. Amsterdam: Elsevier Scientific Publishing Company. Hal: 198.
Isnandi. (2008). Ikan Teri
La Anas. (2008). Ikan Teri.
http://mykalambe.multiply.com/photos/album/10/Ikan_Teri%20http://ww w.pipp.kp.go.id/pipp2/species.html?idkat=2&idsp=39%20http://www.pan
daisikek.net/sosial-budaya/ikan-teri%20http://research.kahaku.go.jp/zoology/Fishes_of_Libong/data/p008_ 01b.html. Tanggal akses 30 Oktober 2010.
Linder, M. C. (1992). Biokimia Nutrisi Dan Metabolisme. Jakarta. Universitas Indonesia Press. Hal: 248.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal: 298.
Saparinto, S. (2006). Gizi Dan Aneka Masakan Dari Bahan Ikan. Semarang. Dahara Prize. Ha: 9, 10, 17 dan 18.
Svehla, G. (1990), Vogel Buku Teks Analisa Kuantitatif Anorganik. Edisi V. Jakarta: Kalman Media Pustaka. Hal: 300-303.
Underwood, A. L. & Day, R.A. (1986). Analisis kimia kuantitatif. Jakarta: Erlangga. Hal: 219.
Utami, E, M, & Sujono, K,. (2001). Usaha Perikanan Indonesia. Jakarta. Mutiara Sumber Widya. Hal: 60.
Wibisono,Y. (2005). Metode Statistik. Cetakan I. Yogyakarta: Gadjah Mada University Press. Hal: 22, 385.
Lampiran
Gambar 2
[image:48.595.113.323.116.649.2]Gambar 3
Gambar 4
n 1. Sampel
. Ikan Teri B
. Ikan Teri
. Ikan Teri K
l yang Digu
Besar
Sedang
Kecil
Lampiran 2. Data Perhitungan Pembakuan Larutan Standar Na2EDTA
No. Berat ZnSO4.7H2O (mg)
Volume Na2EDTA (ml)
Volume Titrasi Blanko (ml)
1. 225,4 16,75 0,5
2. 219,8 16,30 0,5
3. 229,5 16,95 0,5
Normalitas Na2EDTA =
O H . ZnSO BE Vb Vt W 2 47 ) ( Keterangan:
W = Berat ZnSO4.7H2O (mg)
Vt = Volume larutan Na2EDTA titrasi ZnSO4
Vb = Volume larutan Na2EDTA titrasi blanko
BE ZnSO4.7H2O = 287,43
N1 = 43 , 287 ) 5 , 0 75 , 16 ( 4 , 225 x
= 0,0483 N
N2 = 43 , 287 ) 5 , 0 30 , 16 ( 8 , 219 x
= 0,0484 N
N3 = 43 , 287 ) 5 , 0 95 , 16 ( 5 , 229 x
= 0,0485 N
Harga Rata-rata dan Deviasi:
Nr1 = 2 2 1 N N = 2 0484 , 0 0483 , 0
= 0,0484 N
Nr2 = 2 3 1 N N = 2 0485 , 0 0483 , 0
= 0,0484 N
Nr3 = 2 3 2 N N = 2 0485 , 0 0484 , 0
= 0,0485 N
d1 = 100%
1 1 1 x Nr Nr N
= 100%
0484 , 0 0484 , 0 0483 , 0 x
d2 = 100% 2
2 3
x Nr
Nr N
= 100%
0484 , 0
0484 , 0 0485 , 0
x
= 0,21%
d3 = 100%
3 3 3
x Nr
Nr N
= 100%
0485 , 0
0485 , 0 0485 , 0
x
= 0%
Normalitas Na2EDTA adalah normalitas rata-rata dengan deviasi terkecil,
Lampiran 3. Penetapan Kadar Kalsium Karbonat Baku Dengan Metode Titrasi
Kompleksometri
Data Penetapan Kadar Kalsium Karbonat Baku Dengan Metode Kompleksometri
No. Berat CaCO2 Baku (mg)
Volume Titran (ml)
% Kadar % Kadar
Rata-Rata
1. 102,4 21,25 39,39
2. 102,2 21,05 39,13
3. 100,4 20,65 39,01 39,20
4. 102,9 21,30 39,29
5. 103,8 21,50 39,33
6. 104,0 21,40 39,07
Normalitas Na2EDTA yang digunakan adalah 0,0485 N
% Kalsium = x100%
W
N x Ca atom berat x Vb Vt
Keterangan:
Vt = volume larutan Na2EDTA titrasi CaCO3 (ml)
Vb = volume larutan Na2EDTA titrasi blanko (ml)
N = normalitas Na2EDTA (N)
W = berat kalsium karbonat (mg)
Perhitungan:
% Kalsium = 100%
4 , 102
0485 , 0 08 , 40 ) 5 , 0 25 , 21 (
x x
x
= 39,39%
Dihitung % kadar setiap berat kalsium, kemudian diambil rata-ratanya sebagai %
Lampiran 4. Perhitungan Statistik Penetapan Kadar Kalsium Karbonat Baku
No. Xi (%) (Xi –
X
) (Xi –X
)21. 39,39 0,17 0,0289
2. 39,07 -0,13 0,0169
3. 39,03 -0,17 0,0289
4. 39,33 0,13 0,0169
5. 39,37 0,17 0,0289
6. 39,05 -0,15 0,0225
∑ Xi = 235,22
X
= 39,20∑ (Xi –
X
)2 = 0,1430SD =
1 )
( 2
n X Xi
=
1 6
1430 , 0
= ± 0,1691
Dari 6 data yang diperoleh, data ke-3 adalah data yang paling menyimpang maka
dilakukan uji Q.
Q =
03 , 39 77 , 39
05 , 39 03 , 39
= 74 , 0
02 , 0
= -0,0270
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
Rata-rata kadar kalsium baku pada taraf kepercayaan 95% adalah:
μ =
X
± t1/2α,dkn
SD
= 39,2 ± 2,5706.
6 1691 ,
0
Lampiran 5. Hasil Penetapan Kadar Air Dari Sampel Ikan Teri
A.Contoh Perhitungan Penetapan Kadar Air
% 100 n dikeringka sebelum Berat n dikeringka setelah Berat -n dikeringka sebelum Berat air Kadar
% x
Berat sebelum dikeringkan = 5,0567 gram
Berat setelah dikeringkan = 4,1583 gram
Kadar air (%) = 100%
0567 , 5 1583 , 4 0567 , 5 x = 17,29%
B. Data Hasil Penetapan Kadar Air Dari Sampel Ikan Teri
1. Hasil Penetapan Kadar Air Dari Ikan Teri Kecil Asal Kembang Tanjong
No. Berat Awal (g) Berat Akhir (g) Kadar Air (%) 1. 2. 3. 4. 5. 6. 5,0567 5,0278 5,0991 5,0875 5,0580 5,0116 4,1826 4,1583 4,2188 4,2097 4,1856 4,1458 17,29 17,29 17,26 17,25 17,25 17,28
X
= 17,272. Hasil Penetapan Kadar Air Dari Ikan Teri Sedang Asal Kembang Tanjong
No. Berat Awal (g) Berat Akhir (g) Kadar Air (%) 1. 2. 3. 4. 5. 6. 5,0721 5,0139 5,0398 5,0162 5,0122 5,0713 4,1928 4,1487 4,1670 4,1467 4,1483 4,1960 17,33 17,26 17,32 17,33 17,24 17,26
3. Hasil Penetapan Kadar Air Dari Ikan Teri Besar Asal Kembang Tanjong
No. Berat Awal (g) Berat Akhir (g) Kadar Air (%) 1. 2. 3. 4. 5. 6. 5,0481 5,0650 5,0477 5,0173 5,0388 5,0190 4,1768 4,1918 4,1699 4,1458 4,1691 4,1462 17,26 17,24 17,39 17,37 17,26 17,39
X
= 17,324. Hasil Penetapan Kadar Air Dari Ikan Teri Kecil Asal Teupen Raya
No. Berat Awal (g) Berat Akhir (g) Kadar Air (%) 1. 2. 3. 4. 5. 6. 5,0756 5,0864 5,0514 5,0375 5,0556 5,0532 4,2097 4,2151 4,1866 4,1650 4,1820 4,1785 17,06 17,13 17,12 17,32 17,28 17,31
X
= 17,205. Hasil Penetapan Kadar Air Dari Ikan Teri Sedang Asal Teupen Raya
No. Berat Awal (g) Berat Akhir (g) Kadar Air (%) 1. 2. 3. 4. 5. 6. 5,0225 5,0318 5,0509 5,0616 5,0197 5,0416 4,1531 4,1603 4,1882 4,1981 4,1523 4,1800 17,31 17,32 17,08 17,06 17,28 17,09
X
= 17,196. Hasil Penetapan Kadar Air Dari Ikan Teri Besar Asal Teupen Raya
No. Berat Awal (g) Berat Akhir (g) Kadar Air (%) 1. 2. 3. 4. 5. 6. 5,0384 5,0365 5,0250 5,0344 5,0401 5,0189 4,1587 4,1672 4,1597 4,1559 4,1717 4,1441 17,46 17,26 17,22 17,45 17,23 17,43
Lampiran
Gambar 5
Gambar 6 Laruta
n 6. Hasil A
. Hasil Ana
. Hasil Ana an Sampel
Analisis Kua
alisis Kualita
alisis Kualita L A
alitatif
atif dengan
atif dengan Larutan Sam Amonium Ok
H2SO4 (e) d
larutan amo mpel +
ksalat
dan etanol
[image:55.595.114.384.387.672.2]Lampiran 7. Contoh Perhitungan Kadar Kalsium Dari Sampel Ikan Teri
Kadar kalsium (mg/g sampel) =
) / (
) (
Vl Va Bsx
xBAxN Vb
Vt
Keterangan:
Vt = volume larutan Na2EDTA titrasi sampel (ml)
Vb = volume larutan Na2EDTA titrasi blanko (ml)
BA = berat atom kalsium
N = normalitas larutan Na2EDTA
Bs = berat sampel (g)
Va = volume aliquot yang diambil
Vl = volume larutan sampel
Contoh penetapan kadar kalsium pada ikan teri kecil asal Kembang Tanjong:
Volume larutan Na2EDTA titrasi sampel = 26,20 ml
Volume larutan Na2EDTA titrasi blanko = 0,5 ml
Berat atom kalsium = 40,08
Normalitas larutan Na2EDTA = 0,0485 N
Berat sampel = 10,0150 g
Volume aliquot = 25 ml
Volume larutan = 100 ml
Kadar Kalsium (mg/g bahan) =
) 100 / 25 ( 0150 , 10
0485 , 0 08 , 40 ) 5 , 0 20 , 26 (
x x x
= 19,9532 mg/g
= 1995,32 mg kalsium/100 g sampel
Kadar Kalsium (%) = 100%
100
) 100 / (
x g
g mg
= 100% 100
32 , 1995
x g
mg
= 100%
100 99532 , 1
x g
g
Lampiran 8. Hasil Penetapan Kadar Kalsium Dari Sampel Ikan Teri
1. Hasil Penetapan Kadar Kalsium Dari Ikan Teri Kecil Asal Kembang Tanjong
No. Berat Sampel
(g) Volume Titran (ml) Kadar (mg/100 g) Kadar (%) 1. 2. 3. 4. 5. 6. 10,0150 10,0110 10,0097 10,0008 10,0110 10,0062 26,20 26,20 25,85 25,80 26,15 25,85 1995,32 1996,11 1969,18 1967,05 1992,23 1969,87
X
=1981 2,00 2,00 1,97 1,97 1,99 1,97X
=1,982. Hasil Penetapan Kadar Kalsium Dari Ikan Teri Sedang Asal Kembang Tanjong
No. Berat Sampel
(g) Volume Titran (ml) Kadar