PENETAPAN KADAR KALSIUM
SECARA SPEKTROFOTOMETRI SERAPAN ATOM DAN
FOSFOR SECARA SPEKTROFOTOMETRI SINAR TAMPAK
PADA IKAN TERI (Stolephorus spp.)
SKRIPSI
OLEH:
MAULIDA SARA REGAR
NIM 101501011
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR KALSIUM
SECARA SPEKTROFOTOMETRI SERAPAN ATOM DAN
FOSFOR SECARA SPEKTROFOTOMETRI SINAR TAMPAK
PADA IKAN TERI (Stolephorus spp.)
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
MAULIDA SARA REGAR
NIM 101501011
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALSIUM SECARA
SPEKTROFOTOMETRI SERAPAN ATOM DAN FOSFOR
SECARA SPEKTROFOTOMETRI SINAR TAMPAK PADA
IKAN TERI (Stolephorus spp.)
OLEH:
MAULIDA SARA REGAR
NIM 101501011
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 05 Februari 2015 Pembimbing I
Drs. Maralaut Batubara, M.Phill., Apt. NIP 195101311976031003
Pembimbing II
Prof. Dr. Muchlisyam, M.Si., Apt. NIP 195006221980021001
Panitia Penguji,
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Drs. Maralaut Batubara, M.Phill., Apt. NIP 195101311976031003
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
Dra. Siti Nurbaya, M.Si., Apt. NIP 195008261974122001
Medan, Februari 2015 Fakultas Farmasi
Universitas Sumatera Utara a.n Dekan,
Wakil Dekan I,
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
berkat, rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian
dan penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul
Penetapan Kadar Kalsium Secara Spektrofotometri Serapan Atom dan Fosfor
Secara Spektrofotometri Sinar Tampak pada Ikan Teri (Stolephorus spp.).
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara
Medan, yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan
pendidikan. Bapak Drs. Maralaut Batubara, M.Phill., Apt., dan Bapak Prof. Dr.
Muchlisyam, M.Si., Apt., yang telah membimbing dan memberikan petunjuk
serta saran - saran selama penelitian hingga selesainya skripsi ini. Bapak Drs.
Fathur Rahman Harun, M.Si., Apt., Ibu Dra. Sudarmi, M.Si., Apt., dan Ibu Dra.
Siti Nurbaya, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik,
saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan Ibu
staf pengajar Fakultas Farmasi USU Medan yang telah mendidik selama
perkuliahan dan Bapak Prof., Dr., Jansen Silalahi, M.App. Sc., Apt., selaku
kepada penulis selama masa perkuliahan. Bapak Prof. Dr. rer. nat. Effendy De
Lux Putra, S.U., Apt., selaku kepala Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan izin dan fasilitas untuk
penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada
terhingga kepada Ayahanda Marwan Siregar dan Ibunda Maryam Lubis, yang
telah memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun,
pengorbanan baik materi maupun motivasi beserta doa yang tulus yang tidak
pernah berhenti. Abang dan kakak tercinta Rahmad Gandhi Siregar dan
Fatihayana Regar serta seluruh keluarga yang selalu mendoakan dan memberikan
semangat. Sahabat-sahabat terbaikku serta semua pihak yang tidak dapat
disebutkan satu persatu yang telah banyak membantu hingga selesainya penulisan
skripsi ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis
berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Januari 2015 Penulis,
PENETAPAN KADAR KALSIUM SECARA SPEKTROFOTOMETRI SERAPAN ATOM DAN FOSFOR SECARA SPEKTROFOTOMETRI
SINAR TAMPAK PADA IKAN TERI (Stolephorus spp.)
ABSTRAK
Ikan teri merupakan salah satu sumber kalsium dan fosfor yang baik selain susu, karena dikonsumsi bersama dengan tulangnya. Berbeda dengan ikan lain yang hanya dikonsumsi dagingnya saja. Tujuan dari penelitian ini adalah untuk mengetahui kadar kalsium dan fosfor serta perbedaan kadar kalsium dan fosfor yang terdapat pada beberapa kelompok ikan teri.
Dalam penelitian ini dianalisis tiga kelompok ikan teri yaitu ikan teri tawar, teri nasi dan teri toge. Penetapan kadar kalsium dilakukan secara spektrofotometri serapan atom menggunakan nyala asetilen-udara pada panjang gelombang 422,7 nm dan untuk fosfor dilakukan secara spektrofotometri sinar tampak pada panjang gelombang 710 nm.
Hasil penetapan kadar kalsium untuk ikan teri tawar, teri nasi dan teri toge adalah (2556,6971 + 14,4363) mg/100g; (575,9832 + 5,6563) mg/100g; dan (551,6137 + 3,8413) mg/100g. Hasil penetapan kadar fosfor untuk ikan teri tawar, teri nasi dan teri toge adalah (1314,0248 + 12,3870) mg/100g; (371,6593 + 5,2116) mg/100g; dan (564,6504 + 8,1462) mg/100g.
Dari hasil analisis dapat dilihat perbedaan yang signifikan antara kadar kalsium dan fosfor pada beberapa kelompok ikan teri. Berdasarkan hasil penelitian tersebut dapat disimpulkan bahwa kadar kalsium dan fosfor pada ikan teri tawar lebih tinggi daripada ikan teri nasi dan teri toge.
DETERMINATION OF CALCIUM CONTENT BY ATOMIC ABSORPTION SPECTROPHOTOMETRY AND PHOSPHORUS BY VISIBLE SPECTROPHOTOMETRY IN ANCHOVY (Stolephorus spp.)
ABSTRACT
Anchovy is one good source of calcium and phosphorus beside milk, because consumed with bones, unlike other fish which is consumed meat only. The purpose of this study was to determine the levels of calcium and phosphorus as well as differences in the levels of calcium and phosphorus are found in some groups of anchovy.
This study analyze three groups of anchovy is teri tawar, teri nasi and teri toge. Determination of calcium performed by atomic absorption spectrophotometry using acetylene-air at wavelength of 422,7 nm and visible spectrophotometry at a wavelength of 710 nm for phosphorus.
The results of the determination of calcium for teri tawar, teri nasi and teri toge is (2556.6971 + 14.4363) mg/100g; (575.9832 + 5.6563) mg/100g; and (551.6137 + 3.8413) mg/100g . The results of the determination of phosphorus levels for teri tawar, teri nasi and teri toge is (1314.0248 + 12.3870) mg/100g; (371.6593 + 5.2116) mg/100g; and (564.6504 + 8.1462) mg/100g .
From the results of the analysis can be a significant difference between the levels of calcium and phosphorus in some groups of anchovy. Based on these results it can be concluded that the levels of calcium and phosphorus in teri tawar is higher than teri nasi and teri toge.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 ... Latar Belakang ... 1
1.2 ... Perumusan Masalah ... 3
1.3 ... Hipotesis ... 3
1.4 ... Tujuan Penelitian ... 3
1.5 ... Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1.1 Klasifikasi ikan teri ... 5
2.1.2 Kandungan gizi ... 5
2.2 Mineral ... 6
2.2.1 Kalsium ... 6
2.2.2 Fosfor ... 7
2.3 Spektrofotometri Serapan Atom ... 8
2.3.1 Instrumen spektrofotometri serapan atom ... 10
2.3.2 Gangguan-gangguan pada spektrofotometri serapan atom ... 12
2.4 Spektrofotometri Sinar Tampak dan Ultraviolet ... 13
2.5 Validasi Metode Analisis ... 15
BAB III METODE PENELITIAN ... 17
3.1 Tempat dan Waktu Penelitian ... 17
3.2 Bahan-bahan ... 17
3.3.1 Sampel ... 17
3.3.2 Pereaksi ... 17
3.3 Alat-alat ... 17
3.4 Identifikasi Sampel ... 17
3.5 Pembuatan Pereaksi ... 18
3.5.1 Larutan asam nitrat (1:1) v/v ... 18
3.5.2 Larutan H2SO4 5N ... 18
3.5.3 Larutan ammonium molibdat 4% b/v ... 18
3.5.4 Larutan asam askorbat 0,1N ... 18
3.5.7 Larutan Pengembang warna fosfor ... 19
3.6 Prosedur Penelitian ... 19
3.6.1 Pengambilan Sampel ... 19
3.6.2 Penyiapan Sampel ... 19
3.6.3 Proses destruksi kering ... 19
3.6.4 Pembuatan larutan sampel ... 20
3.7 Analisis Kualitatif ... 20
3.7.1 Kalsium ... 20
3.7.1.1 Uji kristal kalsium dengan larutan asam sulfat 1N ... 20
3.7.2 Fosfor ... 20
3.7.2.1 Analisis dengan pereaksi ammonium molibdat ... 20
3.8 Analisis Kuantitatif ... 21
3.8.1 Kalsium ... 21
3.8.1.1 Pembuatan kurva kalibrasi kalsium ... 21
3.8.1.2 Penetapan kadar kalsium dalam sampel teri tawar ... 21
3.8.1.3 Penetapan kadar kalsium dalam sampel teri nasi ... 21
3.8.1.4 Penetapan kadar kalsium dalam sampel teri medan ... 22
3.8.2 Fosfor ... 22
3.8.2.1 Pembuatan Larutan Induk Baku KH2PO4 (LIB I) ... 22
3.8.2.4 Pembuatan kurva kalibrasi fosfor ... 23
3.8.2.5 Penetapan kadar fosfor dalam sampel teri tawar ... 23
3.8.2.6 Penetapan kadar fosfor dalam sampel teri nasi ... 24
3.8.2.7 Penetapan kadar fosfor dalam sampel teri medan ... 24
3.9 Analisis Data Secara Statistik ... 24
3.9.1 Penolakan hasil pengamatan ... 24
3.10 Uji Validasi Metode ... 25
3.10.1 Penentuan batas deteksi dan batas kuantitasi .... 25
3.10.2 Uji perolehan kembali (recovery) ... 26
3.10.3 Simpangan baku relatif ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Identifikasi Sampel ... 28
4.2 Analisis Kualitatif ... 28
4.3 Analisis Kuantitatif ... 29
4.3.1 Penentuan panjang gelombang maksimum senyawa kompleks molibdenum ... 29
4.3.2 Penentuan waktu kerja kompleks molibdenum pada panjang gelombang maksimum 710 nm .... 29
4.3.3 Kurva kalibrasi kalsium secara spektrofotometri serapan atom ... 30
4.3.4 Kurva kalibrasi fosfor secara spektrofotometri sinar tampak ... 30
4.3.5 Analisis kadar kalsium secara spektrofotometri serapan atom ... 31
4.3.7 Batas deteksi dan batas kuantitasi ... 33
4.4 Uji Validasi Metode ... 34
4.4.1 Uji perolehan kembali (recovery) ... 34
4.4.2 Simpangan baku relatif ... 35
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Halaman
Tabel 4.1 Hasil analisis kualitatif pada sampel ikan teri tawar, teri nasi dan teri toge yang telah di destruksi ... 28
Tabel 4.2 Hasil analisis kadar kalsium pada sampel ... 32
Tabel 4.3 Hasil analisis kadar fosfor pada sampel ... 33
Tabel 4.4 Batas deteksi dan batas kuantitasi mineral kalsium dan fosfor ... 34
Tabel 4.5 Persen uji perolehan kembali (recovery) kadar kalsium . . 34
Tabel 4.6 Persen uji perolehan kembali (recovery) kadar fosfor ... 34
Tabel 4.7 Nilai simpangan baku dan simpangan baku relatif kalsium ... 35
DAFTAR GAMBAR
Halaman
Gambar 4.1 Kurva serapan senyawa kompleks molibdenum dengan konsentrasi 5,0 µg/ml ... 29
Gambar 4.2 Kurva kalibrasi kalsium ... 30
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil identifikasi sampel ... 40
Lampiran 2. Gambar sampel ... 41
Lampiran 3. Hasil analisis kualitatif mineral kalsium ... 42
Lampiran 4. Hasil analisis kualitatif mineral fosfor ... 43
Lampiran 5. Gambar alat spektrofotometer serapan atom, spektrofotometer uv-visible dan tanur ... 44
Lampiran 6. Bagan alir proses destruksi kering ... 46
Lampiran 7. Bagan alir proses pembuatan larutan sampel ... 47
Lampiran 8. Perhitungan Konsentrasi Larutan Induk Baku KH2PO4 ... 48
Lampiran 9. Data Penentuan Kerja pada Panjang Gelombang 710 nm ... 49
Lampiran 10. Data kalibrasi kalsium dengan spektrofotometer serapan atom, perhitungan persamaan garis regresi dan koefisien korelasi (r) ... 51
Lampiran 11. Data kalibrasi fosfor dengan spektrofotometer sinar tampak, perhitungan persamaan garis regresi dan koefisien korelasi (r) ... 52
Lampiran 12. Hasil analisis kadar kalsium pada sampel ... 53
Lampiran 13. Hasil analisis kadar fosfor pada sampel ... 54
Lampiran 15. Perhitungan statistik kadar kalsium pada sampel ... 57
Lampiran 16. Perhitungan statistik kadar fosfor pada sampel ... 63
Lampiran 17. Perhitungan batas deteksi dan batas kuantitasi kalsium dan fosfor ... 70
Lampiran 18. Hasil analisis kadar kalsium setelah penambahan larutan baku pada masing-masing sampel ... 72
Lampiran 19. Contoh perhitungan uji perolehan kembali kadar kalsium ... 73
Lampiran 20. Hasil analisis kadar fosfor setelah penambahan larutan baku pada masing-masing sampel ... 76
Lampiran 21. Contoh perhitungan uji perolehan kembali kadar fosfor ... 77
Lampiran 22. Perhitungan simpangan baku relatif (RSD) kadar kalsium ... 80
Lampiran 23. Perhitungan simpangan baku relatif (RSD) kadar fosfor ... 83
PENETAPAN KADAR KALSIUM SECARA SPEKTROFOTOMETRI SERAPAN ATOM DAN FOSFOR SECARA SPEKTROFOTOMETRI
SINAR TAMPAK PADA IKAN TERI (Stolephorus spp.)
ABSTRAK
Ikan teri merupakan salah satu sumber kalsium dan fosfor yang baik selain susu, karena dikonsumsi bersama dengan tulangnya. Berbeda dengan ikan lain yang hanya dikonsumsi dagingnya saja. Tujuan dari penelitian ini adalah untuk mengetahui kadar kalsium dan fosfor serta perbedaan kadar kalsium dan fosfor yang terdapat pada beberapa kelompok ikan teri.
Dalam penelitian ini dianalisis tiga kelompok ikan teri yaitu ikan teri tawar, teri nasi dan teri toge. Penetapan kadar kalsium dilakukan secara spektrofotometri serapan atom menggunakan nyala asetilen-udara pada panjang gelombang 422,7 nm dan untuk fosfor dilakukan secara spektrofotometri sinar tampak pada panjang gelombang 710 nm.
Hasil penetapan kadar kalsium untuk ikan teri tawar, teri nasi dan teri toge adalah (2556,6971 + 14,4363) mg/100g; (575,9832 + 5,6563) mg/100g; dan (551,6137 + 3,8413) mg/100g. Hasil penetapan kadar fosfor untuk ikan teri tawar, teri nasi dan teri toge adalah (1314,0248 + 12,3870) mg/100g; (371,6593 + 5,2116) mg/100g; dan (564,6504 + 8,1462) mg/100g.
Dari hasil analisis dapat dilihat perbedaan yang signifikan antara kadar kalsium dan fosfor pada beberapa kelompok ikan teri. Berdasarkan hasil penelitian tersebut dapat disimpulkan bahwa kadar kalsium dan fosfor pada ikan teri tawar lebih tinggi daripada ikan teri nasi dan teri toge.
DETERMINATION OF CALCIUM CONTENT BY ATOMIC ABSORPTION SPECTROPHOTOMETRY AND PHOSPHORUS BY VISIBLE SPECTROPHOTOMETRY IN ANCHOVY (Stolephorus spp.)
ABSTRACT
Anchovy is one good source of calcium and phosphorus beside milk, because consumed with bones, unlike other fish which is consumed meat only. The purpose of this study was to determine the levels of calcium and phosphorus as well as differences in the levels of calcium and phosphorus are found in some groups of anchovy.
This study analyze three groups of anchovy is teri tawar, teri nasi and teri toge. Determination of calcium performed by atomic absorption spectrophotometry using acetylene-air at wavelength of 422,7 nm and visible spectrophotometry at a wavelength of 710 nm for phosphorus.
The results of the determination of calcium for teri tawar, teri nasi and teri toge is (2556.6971 + 14.4363) mg/100g; (575.9832 + 5.6563) mg/100g; and (551.6137 + 3.8413) mg/100g . The results of the determination of phosphorus levels for teri tawar, teri nasi and teri toge is (1314.0248 + 12.3870) mg/100g; (371.6593 + 5.2116) mg/100g; and (564.6504 + 8.1462) mg/100g .
From the results of the analysis can be a significant difference between the levels of calcium and phosphorus in some groups of anchovy. Based on these results it can be concluded that the levels of calcium and phosphorus in teri tawar is higher than teri nasi and teri toge.
BAB I
PENDAHULUAN
1.1Latar Belakang
Ikan teri atau ikan bilis adalah sekelompok ikan laut kecil anggota
keluarga Engraulidae. Nama ini mencakup berbagai ikan dengan warna tubuh
perak kehijauan atau kebiruan. Walaupun anggota Engraulidae ada yang memiliki
panjang maksimum 23 cm, nama ikan teri biasanya diberikan bagi ikan dengan
panjang maksimum 5 cm. Moncongnya tumpul dengan gigi yang kecil dan tajam
pada kedua-dua rahangnya (Anonimc, 2014).
Ikan teri (Stolephorus spp.) mempunyai ciri-ciri umum yaitu badan seperti
cerutu, sedikit silindris, bagian perut membulat, tubuhnya ramping, panjang
kurang dari 12 cm, kepala pendek, moncong nampak jelas dan meruncing, anal
sirip dubur sedikit ke belakang, duri-duri lemah sirip punggung, warna pucat bila
sisik terlepas, jenis pelagis pantai (Anonima, 2014).
Berdasarkan Nutry Survey Indonesia, kandungan kalsium dalam ikan teri
lebih tinggi daripada susu. Kalsium dari ikan teri akan bermanfaat jika dikonsumsi
secara langsung. Di dalam tubuh kalsium bekerja sama dengan laktosa dan
vitamin D dalam pembentukan massa tulang, serta dengan kalium untuk
menurunkan tekanan darah tinggi (Anonimb, 2014). Ikan teri yang dikonsumsi
sekalian dengan tulangnya juga banyak mengandung fosfor yang berguna untuk
kesehatan gigi dan tulang. Menurut Almatsier (2004), kadar kalsium dan fosfor
pada 100 gram ikan teri kering adalah 1200 mg dan 1500 mg.
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh,
jumlah ini, 99% berada di dalam jaringan keras, yaitu tulang dan gigi terutama
dalam bentuk hidroksiapatit [(3Ca3(PO4)2.Ca(OH)2]. Di dalam cairan ekstraselular
dan intraselular kalsium memegang peranan penting dalam mengatur fungsi sel,
seperti untuk transmisi saraf, kontraksi otot, penggumpalan darah dan menjaga
permeabilitas membran sel (Almatsier, 2004).
Fosfor merupakan mineral kedua terbanyak di dalam tubuh, yaitu 1% dari
berat badan. Kurang lebih 85% fosfor di dalam tubuh terdapat sebagai kalsium
fosfat, yaitu bagian dari kristal hidroksiapatit di dalam tulang dan gigi yang tidak
dapat larut. Hidroksiapatit memberi kekuatan dan kekakuan pada tulang. Fosfor di
dalam tulang berada dalam perbandingan 1:2 dengan kalsium. Fosfor selebihnya
terdapat di dalam semua sel tubuh, separuhnya di dalam otot dan di dalam cairan
ekstraselular (Almatsier, 2004).
Sampel yang digunakan dalam penelitian ini adalah ikan teri kering
(Stolephorus spp.) yang terbagi dalam tiga kelompok yaitu teri tawar, teri nasi dan
teri toge. Teri tawar berwarna kuning dan memiliki ukuran tubuh yang lebih besar
dibandingkan teri nasi dan teri toge. Teri toge merupakan jenis teri yang berwarna
putih, ukurannya lebih besar daripada teri nasi. Sedangkan teri nasi hampir mirip
dengan teri toge namun berukuran lebih kecil.
Metode penetapan kadar kalsium di dalam literatur antara lain
kompleksometri (Rivai, 1995), gravimetri, permanganometri, dan
spektrofotometri serapan atom (Gandjar dan Rohman, 2007). Penetapan kadar
fosfor dapat dilakukan secara spektrofotometri sinar tampak (Lim, 1991).
Adapun alasan untuk meneliti kalsium pada ikan teri dengan metode
mengukur kadar logam dalam jumlah kecil dan spesifik untuk setiap logam tanpa
dilakukan pemisahan (Khopkar, 1990). Sedangkan untuk meneliti fosfor pada ikan
teri digunakan metode spektrofotometri sinar tampak karena metode ini lebih
sederhana dan lebih sensitif (Lim, 1991).
Berdasarkan uraian di atas, maka peneliti ingin mengetahui kadar kalsium
secara spektrofotometri serapan atom dan fosfor secara spektrofotometri sinar
tampak pada ikan teri (Stolephorus spp.).
1.2Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut:
1. Berapakah kadar kalsium dan fosfor yang terdapat pada ikan teri tawar, teri
nasi, dan teri toge?
2. Apakah terdapat perbedaan kadar kalsium dan fosfor antara ikan teri tawar, teri
nasi, dan teri toge?
1.3 Hipotesis
Hipotesis dalam penelitian ini adalah:
1. Ikan teri tawar, teri nasi dan teri toge memiliki kandungan kalsium dan fosfor
pada kadar tertentu.
2. Terdapat perbedaan kadar kalsium dan fosfor antara ikan teri tawar, teri nasi
dan teri toge.
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Untuk mengetahui kadar kalsium dan fosfor yang terdapat pada ikan teri tawar,
2. Untuk mengetahui perbedaan kadar kalsium dan kadar fosfor antara ikan teri
tawar, teri nasi dan teri toge.
1.5 Manfaat Penelitian
Untuk mengetahui kadar kalsium dan fosfor pada ikan teri (Stolephorus
spp.) agar dapat dimanfaatkan sebagai salah satu bahan makanan yang dapat
BAB II
TINJAUAN PUSTAKA
2.1 Ikan Teri
2.1.1 Klasifikasi ikan teri
Menurut Anonimc (2014), klasifikasi ikan teri adalah sebagai berikut:
Filum : Chordata
Sub-Filum : Vertebrae
Class : Actinopterygii
Ordo : Clupeiformes
Famili : Engraulidae
Genus : Stolephorus
Species : Stolephorus spp.
2.1.2 Kandungan gizi
Ikan teri yang selama ini banyak dikonsumsi oleh masyarakat ternyata
merupakan sumber kalsium yang sangat baik untuk mencegah osteoporosis.
Kalsium pada ikan teri berasal dari bagian tulang yang ikut termakan
bersama-sama bagian daging. Seperti halnya pada manusia, kalsium pada ikan juga
terakumulasi pada bagian tulang. Karena tulang pada ikan teri relatif kecil dan
lunak dibandingkan jenis ikan lainnya maka memungkinkan untuk ikut
dikonsumsi (Wirakusumah, 2007).
Ikan teri (Stolephorus spp.) merupakan sumber kalsium yang tahan dan
tidak mudah larut dalam air. Ikan teri (Stolephorus spp.) juga sebagai bahan
pangan yang mempunyai nilai gizi tinggi dengan kandungan mineral, vitamin,
dibutuhkan untuk pertumbuhan tubuh dan kecerdasan manusia. Ikan teri
merupakan salah satu sumber kalsium terbaik untuk mencegah pengeroposan
tulang. Kandungan gizi dalam 100 gram teri segar meliputi energy 77 kkal;
protein l6 gr; lemak 1.0 gr; kalsium 500 mg; phosfor 500 mg; besi 1.0 mg; Vit A
RE 47; dan Vit B 0.1 mg (Anonima, 2014).
2.2 Mineral
Mineral merupakan bagian dari tubuh dan memegang peranan penting
dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun
fungsi tubuh secara keseluruhan. Keseimbangan ion-ion mineral di dalam cairan
tubuh diperlukan untuk pengaturan pekerjaan enzim-enzim, pemeliharaan
keseimbangan asam-basa, membantu transfer ikatan-ikatan penting melalui
membran sel dan pemeliharaan kepekaan otot dan saraf terhadap rangsangan
(Almatsier, 2004).
2.2.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh,
yaitu 1,5-2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Dari
jumlah ini, 99% berada dalam jaringan keras, yaitu tulang dan gigi terutama
dalam bentuk hidroksiapatit [(3Ca3(PO4)2.Ca(OH)2]. Kalsium tulang berada dalam
keadaan seimbang dengan kalsium plasma konsentrasi kurang lebih 2,25-2,60
mmol/l (9-10,4 mg/100 ml). Densitas berbeda menurut umur, meningkat pada
bagian pertama kehidupan dan menurun berangsur setelah dewasa. Selebihnya
kalsium tersebar luas di dalam tubuh. Di dalam cairan ekstraselular dan
seperti untuk transmisi saraf, kontraksi otot, penggumpalan darah dan menjaga
permeabilitas membran sel (Almatsier, 2004).
Kalsium mempunyai berbagai fungsi dalam tubuh antara lain untuk
pembentukan tulang dan gigi, mengatur pembekuan darah, sebagai katalisator
reaksi-reaksi biologik dan berperan dalam kontraksi otot. Kalsium di dalam tulang
mempunyai dua fungsi: (a) sebagai bagian dari struktur tulang; (b) sebagai tempat
menyimpan kalsium. Beberapa fungsi kalsium lain adalah meningkatkan fungsi
transpor membran sel, kemungkinan dengan bertindak sebagai stabilisator
membran, dan transmisi ion melalui membran organel sel (Almatsier, 2004).
Angka kecukupan rata-rata sehari untuk kalsium bagi orang Indonesia
ditetapkan oleh Widyakarya dan Gizi LIPI (1998) sebagai berikut, untuk bayi
sebesar 300-400 mg, anak-anak 500 mg, remaja 600-700 mg, dewasa 500-800 mg,
ibu hamil dan menyusui > 400 mg. Sumber kalsium utama adalah susu dan hasil
susu, seperti keju. Ikan dimakan dengan tulang, termasuk ikan kering merupakan
sumber kalsium yang baik. Serelia, kacang-kacangan dan hasil kacang-kacangan,
tahu dan tempe, dan sayuran hijau merupakan sumber kalsium yang baik juga,
tetapi bahan makanan ini mengandung banyak zat yang menghambat penyerapan
kalsium seperti serat, fitat dan oksalat (Almatsier, 2004).
2.2.2 Fosfor
Fosfor merupakan mineral kedua terbanyak di dalam tubuh, yaitu 1% dari
berat badan. Kurang lebih 85% fosfor di dalam tubuh terdapat sebagai kalsium
fosfat, yaitu bagian dari kristal hidroksiapatit di dalam tulang dan gigi yang tidak
dapat larut. Hidroksiapatit memberi kekuatan dan kekakuan pada tulang. Fosfor di
terdapat di dalam semua sel tubuh, separuhnya di dalam otot dan di dalam cairan
ekstraselular (Almatsier, 2004).
Selain untuk pertumbuhan tulang dan gigi, fosfor mempunyai peranan
dalam metabolisme karbohidrat, lemak dan protein, sebagai fosfolipid, fosfor
merupakan komponen esensial bagi banyak sel dan merupakan alat transport asam
lemak. Fosfor berperan pula dalam mempertahankan keseimbangan asam-basa
(Pudjiadi, 2000).
Pada umumnya bahan makanan yang mengandung banyak kalsium
merupakan juga sumber fosfor, seperti susu, keju, daging, ikan, telur, dan saleria.
Biasanya kira-kira 70% dari fosfor yang berada dalam makanan dapat diserap oleh
tubuh. Penyerapan akan lebih baik bila fosfor dan kalsium dimakan dalam jumlah
yang sama (Pudjiadi, 2000).
Kecukupan fosfor rata-rata sehari untuk Indonesia ditetapkan sebagai
berikut (Widyakarya Pangan dan Gizi LIPI 1993), untuk bayi sebesar 200-250
mg, anak-anak 250-400 mg, remaja dan dewasa 400-500 mg, ibu hamil dan
menyusui >200->300 mg (Almatsier, 2004).
Kelebihan fosfor karena makanan jarang terjadi. Bila kadar fosfor darah
terlalu tinggi, ion fosfat akan mengikat kalsium sehingga dapat menimbulkan
kejang. Kekurangan fosfor karena makan juga jarang terjadi. Kekurangan fosfor
bisa terjadi bila menggunakan obat antasida untuk menetralkan asam lambung
seperti aluminium hidroksida. Aluminium hidroksida mengikat fosfor sehingga
tidak dapat diabsorpsi. Kekurangan fosfor juga dapat terjadi pada penderita yang
kehilangan banyak cairan melalui urin. Kekurangan fosfor menyebabkan rasa
2.3 Spektrofotometri Serapan Atom
Pemanfaatan prinsip serapan atom pada bidang analisis adalah seorang
Australia bernama Alan Walsh di tahun 1955 (Khopkar, 1990). Spektrofotometri
serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral, dan
sinar yang diserap biasanya sinar tampak atau sinar ultraviolet (Gandjar dan
Rohman, 2007).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur -
unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara
analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak
bergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini
cocok untuk analisis kelumit logam karena mempunyai kepekaan yang tinggi
(batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan
interferensinya sedikit (Gandjar dan Rohman, 2007).
Metode spektrofotometri serapan atom mendasarkan pada prinsip absorbsi
cahaya oleh atom. Atom - atom akan menyerap cahaya pada panjang gelombang
tertentu, tergantung pada sifat unsurnya. Misalkan natrium menyerap pada 589
nm, uranium pada 358,5 nm, sedang kalium pada 766,5 nm. Cahaya pada panjang
gelombang ini mempunyai cukup energi untuk mengubah tingkat elektronik suatu
atom yang mana pada transisi elektronik suatu atom bersifat spesifik. Dengan
absorpsi energi, berarti memperoleh lebih banyak energi, suatu atom pada
keadaan dasar dapat ditingkatkan ke tingkat eksitasi. Tingkat-tingkat eksitasinya
pun bermacam - macam. Misalkan, suatu unsur Na dengan nomor atom 11
mempunyai konfigurasi elektron 1s2, 2s2, 2p6 dan 3s1, tingkat dasar untuk elektron
tingkat 4p dengan energi 3,6 eV, masing - masing sesuai dengan panjang
gelombang 589 nm dan 330 nm (Khopkar, 1990).
2.3.1 Instrumen Spektrofotometer Serapan Atom
Bagian instrumentasi spektrofotometer serapan atom adalah sebagai
berikut:
a. Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri dari tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Tabung logam ini diisi dengan gas mulia (neon atau
argon) dengan tekanan rendah. Bila antara anoda dan katoda diberi suatu selisih
tegangan yang tinggi (600 volt), maka katoda akan memancarkan berkas - berkas
elektron yang bergerak menuju anoda yang mana kecepatan dan energinya sangat
tinggi. Elektron - elektron dengan energi tinggi ini dalam perjalanannya menuju
anoda akan bertabrakan dengan gas - gas mulia yang diisikan tadi (Gandjar dan
Rohman, 2007).
Akibat dari tabrakan-tabrakan ini membuat unsur-unsur gas mulia akan
kehilangan elektron dan menjadi ion bermuatan positif. Ion-ion gas mulia yang
bermuatan positif ini selanjutnya akan bergerak ke katoda dengan kecepatan dan
energi yang tinggi pula. Sebagaimana disebutkan di atas, pada katoda terdapat
unsur-unsur yang akan dianalisis. Unsur-unsur ini akan ditabrak oleh ion-ion
positif gas mulia. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar dari
permukaan katoda. Atom-atom unsur dari katoda ini kemudian akan mengalami
spektrum pancaran dari unsur yang sama dengan unsur yang akan dianalisis
(Gandjar dan Rohman, 2007).
b. Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom - atom netral yang masih dalam keadaan
asas. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu
sampel menjadi uap atom - atom yaitu: dengan nyala (flame) dan dengan tanpa
nyala (flameless) (Gandjar dan Rohman, 2007).
- Nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi
bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh
nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen - udara
suhunya sebesar 2200ºC dan gas asetilen - dinitrogen oksida (N2O) sebesar
3000ºC. Sumber nyala yang paling banyak digunakan adalah campuran asetilen
sebagai bahan pembakar dan udara sebagai bahan pengoksidasi (Gandjar dan
Rohman, 2007).
- Tanpa nyala (Flame)
Pengatoman dilakukan dalam tungku dari grafit seperti tungku yang
dikembangkan oleh Masmann. Sejumlah sampel diambil sedikit, lalu diletakkan
dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris
dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat
yang akan dianalisis berubah menjadi atom - atom netral dan pada fraksi atom ini
dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga
c. Monokromator
Pada spektrofotometri serapan atom, monokromator dimaksudkan untuk
memisahkan dan memilih panjang gelombang yang digunakan dalam analisis dari
sekian banyak panjang gelombang yang dihasilkan lampu katoda berongga
(Gandjar dan Rohman, 2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Gandjar dan Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang
menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2007).
2.3.2 Gangguan-gangguan pada spektrofotometri serapan atom
Gangguan - gangguan (interference) pada spektrofotometri serapan atom
adalah peristiwa - peristiwa yang menyebabkan pembacaan absorbansi unsur yang
dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan
konsentrasinya dalam sampel (Gandjar dan Rohman, 2007). Secara luas dapat
dikategorikan menjadi dua kelompok, yakni interferensi spektral dan interferensi
kimia (Khopkar, 1990).
Menurut Gandjar dan Rohman, (2007), gangguan - gangguan yang terjadi
pada spektrofotometri serapan atom adalah:
1. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom
yang terjadi di dalam nyala.
3. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang
dianalisis, yakni absorbansi oleh molekul - molekul yang tidak terdisosiasi di
dalam nyala. Adanya gangguan - gangguan di atas dapat diatasi dengan
menggunakan cara - cara sebagai berikut:
a.Penggunaan nyala/suhu atomisasi yang lebih tinggi
b.Penambahan senyawa penyangga
c.Pengekstraksian unsur yang akan dianalisis
d.Pengekstraksian ion atau gugus pengganggu
4. Gangguan oleh penyerapan non-atomik. Gangguan jenis ini berarti terjadinya
penyerapan cahaya dari sumber sinar yang bukan berasal dari atom - atom
yang akan dianalisis.
2.4 Spektrofotometri Sinar Tampak dan Sinar Ultraviolet
Spektrofotometer Ultraviolet dan Visibel adalah pengukuran panjang
gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi
oleh sampel. Sinar ultraviolet dan cahaya tampak memiliki energi yang cukup
untuk mempromosikan elektron pada kulit terluar ke tingkat energi yang lebih
tinggi. Spektrofotometer Ultraviolet dan Visibel biasanya digunakan untuk
molekul dan ion organik atau kompleks di dalam larutan. Spektrum Ultraviolet
dan Visibel sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari
analit di dalam larutan bisa ditentukan dengan mengukur absorbansi pada panjang
gelombang tertentu dengan menggunakan hukum Lambert-Beer. Sinar ultraviolet
Panjang gelombang cahaya UV atau cahaya tampak bergantung pada
mudahnya promosi elektron. Molekul-molekul yang memerlukan lebih banyak
energi untuk promosi elektron, akan menyerap pada panjang gelombang yang
lebih pendek. Molekul yang memerlukan energi yang lebih sedikit akan menyerap
pada panjang gelombang yang lebih panjang. Senyawa yang menyerap cahaya
dalam daerah tampak mempunyai elektron yang lebih mudah dipromosikan
daripada senyawa yang menyerap pada panjang gelombang UV yang lebih pendek
(Gandjar dan Rohman, 2007).
Metode spektrofotometri langsung seperti analisis ultraviolet banyak
digunakan di dalam analisis tetapi biasannya kurang selektif. Selektivitas atau
kekhasan dapat ditingkatkan melalui pemisahan atau dengan mereaksikan gugus
fungsional yang sesuai. Misalnya dengan menambahkan reagensia tertentu
sehingga dihasilkan warna yang kemudian diukur pada daerah visibel (Gandjar
dan Rohman, 2007).
Warna sinar tampak dapat dihubungkan dengan panjang gelombangnya.
Sinar putih mengandung radiasi pada semua panjang gelombang di daerah sinar
tampak. Sinar pada panjang gelombang tunggal (radiasi monokromatik) dapat
dipilih dari sinar putih. Spektrofotometer yang sesuai untuk pengukuran di daerah
spektrum ultraviolet dan sinar tampak terdiri atas suatu sistem optik dengan
kemampuan menghasilkan sinar monokromatis dalam jangkauan panjang
gelombang 200-800 nm (Gandjar dan Rohman, 2007).
Alat spektrofotometri pada dasarnya terdiri atas sumber sinar,
alat ukur atau pencatat. Spektrofotometer dapat bekerja secara otomatik ataupun
tidak, dan dapat mempunyai sistem sinar tunggal dan ganda (Ditjen POM, 1979).
Sebagai sumber cahaya biasanya digunakan lampu hidrogen atau
deuterium untuk pengukuran UV dan lampu tungsten untuk pengukuran pada
cahaya tampak. Panjang gelombang dari sumber cahaya akan dibagi oleh
pemisahan atau monokromator (Dachriyanus, 2004).
2.5 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita,
2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi
metode analisis adalah sebagai berikut:
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan
ditentukan dengan dua cara, yaitu: metode simulasi (Spiked-placebo recovery) dan
metode penambahan baku (standart addition method) (Harmita,2004).
Metode simulasi (Spiked-placebo recovery) merupakan metode yang
dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu
bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang
Metode penambahan baku (standart addition method) merupakan metode
yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan
divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa
penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan ke dalam sampel dapat
ditemukan kembali (Harmita, 2004).
b. Keseksamaan (presisi)
Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Keseksamaan atau presisi diukur sebagai
simpangan baku atau simpangan baku relatif (koefisien variasi) (Harmita, 2004).
c. Batas deteksi (Limit of detection) dan batas kuantitasi (Limit of
quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara Medan pada bulan September 2014- November 2014.
3.2 Bahan - Bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah ikan teri tawar, ikan
teri nasi, dan ikan teri toge yang diperoleh secara purposif di Pusat Pasar, Medan.
3.2.2 Pereaksi
Bahan - bahan yang digunakan dalam penelitian ini berkualitas pro analisis
keluaran E. Merck yaitu asam nitrat 65% b/v, asam sulfat 96% b/v, etanol 96%
v/v, larutan baku kalsium 1000 µg/ml, ammonium molibdat, asam askorbat,
kalium dihidrogen fosfat, kalium antimonil tatrat, akuabides (PT. Ikapharmindo
Putramas).
3.3 Alat- alat
Alat yang digunakan adalah alat - alat gelas (Pyrex dan Oberoi), blender,
botol kaca, hot plate, oven, kertas saring Whatman No. 42, krus porselen, neraca
analitik (AND GF-200), spatula, spektrofotometer serapan atom Hitachi Z-2000
lengkap dengan lampu katoda kalsium dengan nyala udara-asetilen,
spektrofotometer UV-Visible (Hitachi U-1800), dan tanur (Stuart).
3.4 Identifikasi Sampel
Identifikasi sampel dilakukan oleh Dinas Kelautan dan Perikanan
3.5 Pembuatan Pereaksi
3.5.1 Larutan asam nitrat (1:1) v/v
Sebanyak 500 ml larutan asam nitrat 65% diencerkan dengan 500 ml
akuabides (Isacc, 1990).
3.5.2 Larutan H2SO4 5 N
Dipipet 70,0 ml H2SO4 96% v/v, dimasukkan perlahan-lahan melalui
dinding ke dalam labu tentukur 500 ml yang telah berisi air suling setengahnya.
Dicukupkan volumenya dengan air hingga garis tanda (Lancashire, 2011).
3.5.3 Larutan ammonium molibdat 4%b/v
Ditimbang seksama 20,0 g ammonium molibdat. Kemudian dimasukkan
ke dalam labu tentukur 500 ml, ditambah dengan air suling dan dicukupkan
volumenya dengan air suling hingga garis tanda (Lancashire, 2011).
3.5.4 Larutan asam askorbat 0,1 N
Ditimbang seksama 8,8 g asam askorbat dan dilarutkan dalam labu
tentukur 500 ml dengan air suling dan dicukupkan volumenya dengan air suling
hingga garis tanda (Lancashire, 2011).
3.5.5 Larutan kalium antimonil tatrat 0,274% b/v
Ditimbang seksama 0,274 g kalium antimonil tartat, dimasukkan ke dalam
labu tentukur 100 ml ditambah dengan air suling hingga garis tanda (Lancashire,
2011).
3.5.6 Larutan H2SO4 1 N
Sebanyak 3 ml larutan asam sulfat 96% diencerkan dengan akuabides
3.5.7 Larutan pengembang warna fosfor
Dicampur 500 ml asam sulfat 5 N, 150 ml ammonium molibdat 4% b/v,
300 ml asam askorbat 0,1 N dan 50 ml kalium antimonil tatrat 0,274% b/v
(Lancashire, 2011).
3.6 Prosedur Penelitian
3.6.1 Pengambilan sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposive
yang dikenal juga sebagai sampling pertimbangan dimana sampel ditentukan atas
dasar pertimbangan bahwa sampel yang diambil dapat mewakili populasi
(Budiarto, 2004).
3.6.2 Penyiapan sampel
Sebanyak 250 g masing-masing ikan teri toge, teri nasi, dan teri tawar
dicuci bersih dengan air mengalir dan ditiriskan sampai air cuciannya kering.
Sampel kemudian dihaluskan dengan blender. Dikeringkan dalam oven sampai
kering seperti semula.
3.6.3 Proses destruksi kering
Sampel yang telah dihaluskan dan dikeringkan dalam oven ditimbang
seksama sebanyak 5 g dalam krus porselen, diarangkan di atas hot plate, lalu
diabukan dalam tanur dengan temperatur awal 100 dan perlahan - lahan
temperatur dinaikkan hingga suhu 500 dengan interval 25 setiap 5 menit.
Setelah dilakukan pengabuan selama 60 jam, suhu tanur diturunkan, pada
krus porselen dikeluarkan dan dibiarkan hingga dingin pada desikator. Abu
ditambahkan 5 ml asam nitrat(1:1), kemudian diuapkan pada hot plate sampai
awal 100 dan perlahan - lahan temperatur dinaikkan hingga suhu 500 dengan
interval 25 setiap 5 menit. Pengabuan dilakukan selama 1 jam dan dibiarkan
hingga dingin pada desikator (Isacc, 1990).
3.6.4 Pembuatan larutan sampel
Sampel hasil destruksi dilarutkan dalam 5 ml asam nitrat (1:1), lalu
dipindahkan ke dalam labu tentukur 100 ml, dibilas krus porselen dengan 10 ml
akuabides sebanyak tiga kali dan dicukupkan dengan akuabides hingga garis
tanda. Kemudian disaring dengan kertas saring Whatman No. 42 dimana 5 ml
filtrat pertama dibuang untuk menjenuhkan kertas saring kemudian filtrat
selanjutnya ditampung ke dalam botol (Isacc, 1990).
3.7 Analisis Kualitatif
3.7.1 Kalsium
3.7.1.1 Uji kristal kalsium dengan larutan asam sulfat 1N
Larutan sampel hasil destruksi sebanyak 1 - 2 tetes diteteskan pada object
glass kemudian ditetesi dengan larutan asam sulfat 1N dan etanol 96% v/v akan
terbentuk endapan putih lalu diamati di bawah mikroskop. Jika terdapat kalsium
akan terlihat kristal berbentuk jarum (Svehla, 1990).
3.7.2 Fosfor
3.7.2.1 Analisis dengan pereaksi ammonium molibdat
Kedalam tabung reaksi dimasukan 5,0 ml sampel, ditambah pereaksi
ammonium molibdat 4% b/v ± 2 ml, dikocok lalu diamkan, maka akan terbentuk
3.8 Analisis Kuantitatif
3.8.1 Kalsium
3.8.1.1 Pembuatan kurva kalibrasi kalsium
Larutan baku kalsium (1000 µg/ml) sebanyak 0,5 ml dimasukkan kedalam
labu tentukur 50 ml lalu diencerkan dengan akuabides hingga garis tanda. Dari
larutan tersebut (10 µg/ml) dipipet masing-masing 0,5 ml; 1,0 ml; 1,5 ml; 2,0 ml
dan 2,5 ml dimasukkan ke dalam labu tentukur 25 ml dan diencerkan dengan
akuabides hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 0,2
µg/ml; 0,4 µg/ml; 0,6 µg/ml; 0,8 µg/ml dan 1,0 µg/ml, lalu dilakukan pengukuran
pada panjang gelombang 422,7 nm dengan tipe nyala udara-asetilen.
3.8.1.2 Penetapan kadar kalsium dalam sampel teri tawar
Larutan sampel hasil destruksi dipipet sebanyak 1 ml dimasukkan ke
dalam labu tentukur 100 ml dan dicukupkan dengan akuabides hingga garis tanda.
Lalu dipipet 1 ml dimasukkan ke dalam labu tentukur 50 ml (Faktor pengenceran
= 5000 kali). Lalu diukur absorbansinya dengan menggunakan spektrofotometer
serapan atom pada panjang gelombang 422,7 nm dengan tipe nyala udara-asetilen.
Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi
larutan baku kalsium. Konsentrasi kalsium dalam sampel dihitung berdasarkan
persamaan garis regresi dari kurva kalibrasi.
3.8.1.3 Penetapan kadar kalsium dalam sampel teri nasi
Larutan sampel hasil destruksi dipipet sebanyak 0,2 ml dimasukkan ke
dalam labu tentukur 100 ml dan dicukupkan dengan akuabides hingga garis tanda
(Faktor pengenceran = 500 kali). Lalu diukur absorbansinya dengan menggunakan
nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang
kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel dihitung
berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.8.1.4 Penetapan kadar kalsium dalam sampel teri toge
Larutan sampel hasil destruksi dipipet sebanyak 0,2 ml dimasukkan ke
dalam labu tentukur 100 ml dan dicukupkan dengan akuabides hingga garis tanda
(Faktor pengenceran = 500 kali). Lalu diukur absorbansinya dengan menggunakan
spektrofotometer serapan atom pada panjang gelombang 422,7 nm dengan tipe
nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang
kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel dihitung
berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.8.2 Fosfor
3.8.2.1 Pembuatan Larutan Induk Baku KH2PO4 (LIB I)
Ditimbang 0,44 g KH2PO4 yang telah dikeringkan di dalam oven dengan
suhu 1050C selama 1 jam, kemudian dimasukan ke dalam labu tentukur 100 ml,
ditambahkan 5,0 ml HNO3 5 N, dikocok hingga larut, dicukupkan volumenya
dengan akuabides hingga garis tanda. Diperoleh konsentrasi fosfor pada larutan
induk baku (LIB I) adalah 1000 µg/ml.
3.8.2.2 Pembuatan kurva serapan larutan KH2PO4
Dipipet 0,5 ml dari LIB I, dimasukan kedalam labu tentukur 100 ml,
ditambahkan akuabidest sampai garis tanda (5 µg/ml). Di pipet 1 ml dari larutan
(5 µg/ml) di masukan ke dalam erlenmeyer, ditambahkan 5 ml akuabides dan
ditambahkan 1 ml larutan pengembang fosfor, kocok. Diukur serapan pada
3.8.2.3 Penentuan waktu kerja
Dipipet 0,5 ml dari LIB I, dimasukan kedalam labu tentukur 100 ml,
dicukupkan volumenya dengan akuabides hingga garis tanda (5 µg/ml). Dipipet 1
ml dari larutan tersebut, ditambahkan 5,0 ml akuabides dan 1,0 ml larutan
pengembang warna fosfor, dikocok, dan kemudian didiamkan. Diukur serapan
pada panjang gelombang maksimum 710 nm mulai menit ke-10 hingga menit ke
60 dengan interval 1 menit.
3.8.2.4 Pembuatan kurva kalibrasi fosfor
Dipipet 0,1 ml; 0,2 ml; 0,3 ml; 0,4 ml; 0,5 ml dari LIB I, dimasukan
kedalam labu tentukur 100 ml, kemudian dicukupkan volumenya sampai garis
tanda. Dipipet 1 ml larutan tersebut, ditambahkan 5,0 ml akuabides dan 1 ml
larutan pengembang warna fosfor, dikocok dan diamkan selama 49 menit. Dengan
konsentrasi larutan 0,1429 µg/ml; 0,2857 µg/ml; 0,4286 µg/ml; 0,5714 µg/ml;
0,7143 µg/ml. Kemudian diukur serapan pada panjang gelombang 710 nm pada
menit ke-49 menit dengan spektrofotometri sinar tampak.
3.8.2.5 Penetapan kadar fosfor dalam sampel teri tawar
Dipipet 0,2 ml larutan sampel, dimasukan kedalam labu tentukur 100 ml,
dicukupkan volume dengan akuabides hingga garis tanda. Dipipet 1,0 ml larutan
tersebut, dimasukan ke dalam erlenmeyer, ditambahkan 5,0 ml akuabides dan 1
ml larutan pengembang warna fosfor, dikocok (Faktor Pengenceran = 3500 kali).
Diamkan selama 49 menit. Diukur serapan pada panjang gelombang maksimum
710 nm. Pengukuran harus dilakukan dalam rentang waktu kerja yang telah di
3.8.2.6 Penetapan kadar fosfor dalam sampel teri nasi
Dipipet 0,8 ml larutan sampel, dimasukan kedalam labu tentukur 100 ml,
dicukupkan volume dengan akuabides hingga garis tanda. Dipipet 1,0 ml larutan
tersebut, dimasukan ke dalam erlenmeyer, ditambahkan 5,0 ml akuabides dan 1
ml larutan pengembang warna fosfor, dikocok (Faktor Pengenceran = 875 kali).
Diamkan selama 49 menit. Diukur serapan pada panjang gelombang maksimum
710 nm. Pengukuran harus dilakukan dalam rentang waktu kerja yang telah di
peroleh.
3.8.2.7 Penetapan kadar fosfor dalam sampel teri toge
Dipipet 0,4 ml larutan sampel, dimasukan kedalam labu tentukur 100 ml,
dicukupkan volume dengan akuabides hingga garis tanda. Dipipet 1,0 ml larutan
tersebut, dimasukan ke dalam erlenmeyer, ditambahkan 5,0 ml akuabides dan 1
ml larutan pengembang warna fosfor, dikocok (Faktor Pengenceran = 1750 kali).
Diamkan selama 49 menit. Diukur serapan pada panjang gelombang maksimum
710 nm. Pengukuran harus dilakukan dalam rentang waktu kerja yang telah di
peroleh.
Menurut Gandjar dan Rohman, (2007), kadar mineral dalam sampel dapat
dihitung dengan cara sebagai berikut:
(g) Sampel Berat
n pengencera Faktor
x (ml) Volume x
(µg/ml) i
Konsentras (µg/g)
Logam
Kadar
3.9 Analisis Data Secara Statistik
3.9.1 Penolakan hasil pengamatan
Kadar kalsium, dan fosfor yang diperoleh dari hasil pengukuran
masing-masing larutan sampel dianalisis dengan metode standar deviasi. Menurut
SD =
1 -nX
-Xi 2
Keterangan: Xi = Kadar sampel
X = Kadar rata-rata sampel
n = Jumlah perlakuan
Untuk mencari t hitung digunakan rumus:
t hitung =
n SD
X Xi
/
dan untuk menentukan kadar mineral di dalam sampel dengan interval
kepercayaan 99%, α = 0,01, dk = n-1, dapat digunakan rumus:
Kadar mineral : µ =
X
± (t(α/2, dk) x SD / √n )Keterangan:
X = Kadar rata-rata sampel
SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1)
α = Interval kepercayaan
n = Jumlah perlakuan
Dari hasil pengujian dapat dilihat dengan jelas perbedaan kadar kalsium
dan fosfor yang signifikan antar sampel. Oleh karena itu tidak dilakukan uji
statistik lebih lanjut.
3.10 Uji Validasi Metode Analisis
3.10.1 Penentuan batas deteksi dan batas kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama.
Menurut Harmita (2004), batas deteksi dan batas kuantitasi dapat dihitung
dengan rumus sebagai berikut:
Simpangan Baku ( X
SY ) =
2
2
n Yi Y
Batas deteksi (LOD) =
slope X SY x 3
Batas kuantitasi (LOQ) =
slope X SY x 10
3.10.2 Uji perolehan kembali (recovery)
Menurut Harmita, (2004), uji perolehan kembali atau recovery dapat
dilakukan dengan metode penambahan larutan standar (standard addition
method). Larutan baku yang ditambahkan untuk kalsium yaitu 13 ml larutan baku
kalsium (konsentrasi 1000 µg/ml) untuk teri tawar, 3 ml larutan baku kalsium
(konsentrasi 1000 µg/ml) untuk teri nasi dan teri toge. Larutan baku yang
ditambahkan untuk fosfor yaitu 7 ml larutan baku fosfor (konsentrasi 1000 µg/ml)
untuk teri tawar, 2 ml larutan baku fosfor (konsentrasi 1000 µg/ml) untuk teri
nasi, dan 3 ml larutan baku fosfor (konsentrasi 1000 µg/ml) untuk teri toge.
Sampel ikan teri yang telah dihaluskan ditimbang secara seksama
sebanyak 5 g di dalam krus porselen, lalu ditambahkan 13 ml larutan baku
kalsium (konsentrasi 1000 µg/ml) untuk teri tawar, 3 ml larutan baku kalsium
(konsentrasi 1000 µg/ml) untuk teri nasi dan teri toge. Dan untuk fosfor
ml untuk teri nasi dan 3 ml untuk teri toge. Kemudian dilanjutkan dengan
prosedur destruksi kering seperti yang telah dilakukan sebelumnya.
Menurut Harmita, (2004), persen perolehan kembali dapat dihitung dengan
rumus di bawah ini:
% Perolehan Kembali= CF- CA x 100%
Keterangan :
CA = Kadar logam dalam sampel sebelum penambahan baku (mg/100g)
CF = Kadar logam dalam sampel setelah penambahan baku (mg/100g)
C*A = Kadar larutan baku yang ditambahkan (mg/100g)
3.10.3 Simpangan baku relatif
Menurut Harmita, (2004), keseksamaan atau presisi diukur sebagai
simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi
merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji
individual ketika suatu metode dilakukan secara berulang untuk sampel yang
homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan
adanya keseksamaan metode yang dilakukan. Adapun rumus untuk menghitung
simpangan baku relatif adalah:
RSD = 100% X
SD
Keterangan :
X = Kadar rata-rata sampel
SD = Standar Deviasi
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Sampel
Hasil identifikasi sampel yang dilakukan oleh Dinas Kelautan dan
Perikanan Kabupaten Aceh Selatan terhadap ikan teri adalah jenis Stolephorus
spp. suku Engraulidae. Hasil identifikasi sampel dapat dilihat pada Lampiran 1,
halaman 40.
4.2 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
mengetahui ada atau tidaknya ion - ion kalsium, dan fosfor dalam sampel. Data
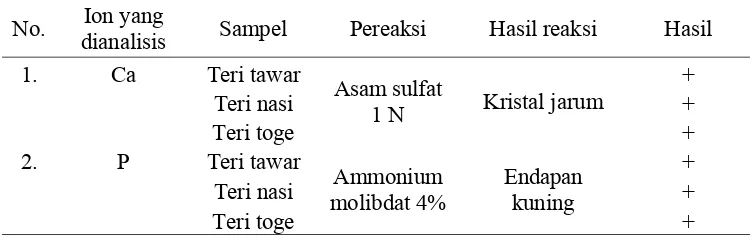
[image:47.612.131.508.405.524.2]dapat dilihat pada Tabel 4.1 dan Lampiran 3 dan 4 halaman 42 dan 43.
Tabel 4.1 Hasil analisis kualitatif pada sampel ikan teri tawar, teri nasi dan teri toge yang telah didestruksi
No. Ion yang
dianalisis Sampel Pereaksi Hasil reaksi Hasil
1. Ca Teri tawar
Asam sulfat
1 N Kristal jarum
+
Teri nasi +
Teri toge +
2. P Teri tawar
Ammonium molibdat 4%
Endapan kuning
+
Teri nasi +
Teri toge +
Keterangan : + : Mengandung ion
Hasil pada Tabel 4.1 menunjukkan bahwa pengujian kualitatif ion kalsium
dan fosfor terhadap sampel yang mengandung ion kalsium menghasilkan endapan
putih kalsium sulfat berbentuk kristal jarum dengan penambahan larutan asam
sulfat 1 N. Juga ion fosfor menghasilkan endapan kuning dengan penambahan
reaksi kristal dari masing - masing kedua ion tersebut membuktikan larutan
sampel mengandung ion kalsium, dan fosfor.
4.3 Analisis Kuantitatif
4.3.1 Penentuan panjang gelombang maksimum senyawa kompleks molibdenum
Penentuan panjang gelombang maksimum senyawa kompleks fosfor
molibdat dilakukan dengan mengukur serapan dari larutan baku dengan
konsentrasi 5 µg/ml pada rentang panjang gelombang maksimum 400-800 nm
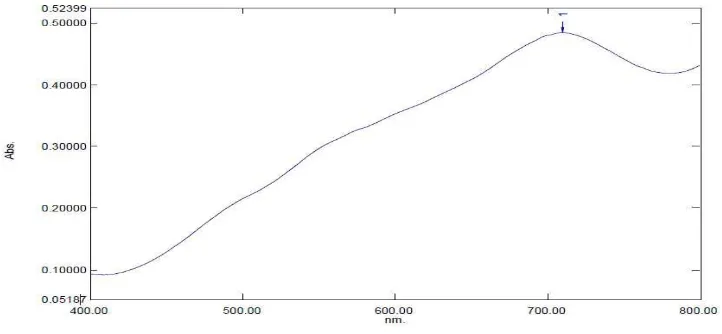
[image:48.612.139.500.306.473.2]dengan menggunakan spektrofotometer sinar tampak.
Gambar 4.1 Kurva Serapan Senyawa Kompleks Molibdenum dengan Konsentrasi 5,0 µg/ml
Dari gambar 4.1 dapat dilihat hasil pengukuran serapan maksimum pada
panjang gelombang 710 nm. Panjang gelombang yang diperoleh ini sesuai dengan
literatur, yaitu pada rentang 610-750 nm yang merupakan rentang panjang
gelombang untuk warna komplementer biru-hijau (Day dan Underwood, 1986).
4.3.2 Penentuan Waktu Kerja Kompleks Molibdenum pada Panjang Gelombang Maksimum 710 nm
kerja dilakukan dengan mengukur serapan dari larutan baku dengan konsentrasi
5,0 µg/ml selama 60 menit pada panjang gelomabang 710 nm. Dari hasil
penelitian diperoleh serapan bahwa serapan senyawa kompleks tersebut stabil
pada menit ke-49 hingga menit ke-51. Data penentuan waktu kerja dapat dilihat
pada Lampiran 9, halaman 49.
4.3.3 Kurva kalibrasi kalsium secara spektrofotometri serapan atom
Kurva kalibrasi kalsium diperoleh dengan cara mengukur absorbansi dari
larutan baku kalsium pada panjang gelombang 422,7 nm. Kurva kalibrasi larutan
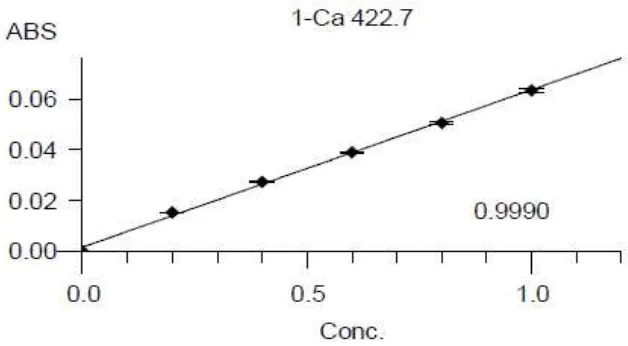
[image:49.612.152.466.325.498.2]baku kalsium dapat dilihat pada Gambar 4.2.
Gambar 4.2 Kurva kalibrasi kalsium
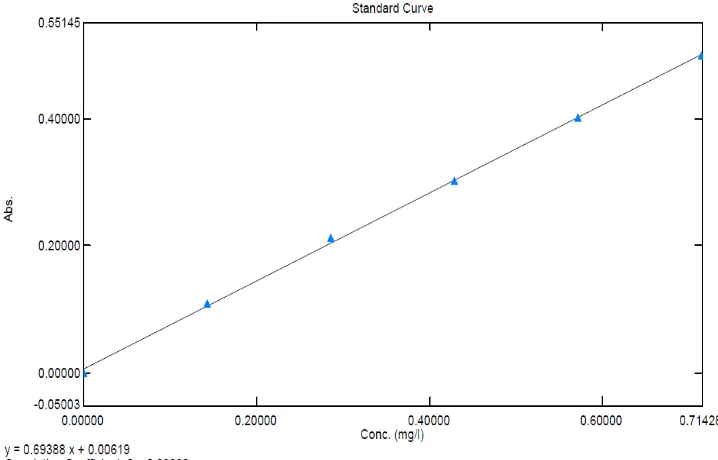
4.3.4 Kurva kalibrasi fosfor secara spektrofotometri sinar tampak
Kurva kalibrasi fosfor diperoleh dengan cara mengukur absorbansi dari
larutan baku pada panjang gelombang 710 nm. Kurva kalibrasi larutan baku fosfor
Gambar 4.3 Kurva kalibrasi fosfor
Hasil pengukuran kurva kalibrasi diperoleh persamaan garis regresi yaitu
Y = 0,0622X + 0,0015 untuk kalsium dan Y = 0,6939X + 0,0062 untuk fosfor.
Berdasarkan gambar di atas diperoleh hubungan yang linear antara
konsentrasi dengan absorbansi, dengan koefisien korelasi (r) kalsium sebesar
0,9990; dan fosfor sebesar 0,9997. Nilai r ≥ 0,95 menunjukkan adanya korelasi
linier yang menyatakan adanya hubungan antara X (Konsentrasi) dan Y
(Absorbansi) (Shargel dan Andrew, 1999). Data hasil pengukuran absorbansi
larutan baku kalsium, dan fosfor dan perhitungan persamaan garis regresi dapat
dilihat pada Lampiran 10 dan 11, halaman 51 dan 52.
4.3.5 Penetapan kadar kalsium secara spektrofotometri serapan atom
Penentuan kadar kalsium dilakukan secara spektrofotometri serapan atom.
Konsentrasi mineral kalsium dalam sampel ditentukan berdasarkan persamaan
kalsium dalam sampel berada pada rentang kurva kalibrasi maka masing-masing
sampel diencerkan terlebih dahulu dengan faktor pengenceran yang berbeda -
beda. Faktor pengenceran untuk penentuan kadar kalsium pada teri tawar adalah
sebesar 5000 kali, pada teri nasi dan teri toge adalah sebesar 500 kali. Data dan
perhitungan dapat dilihat pada Lampiran 12 dan 14, halaman 53 dan 55.
Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat
dilihat pada Lampiran). Hasil analisis kuantitatif mineral kalsium dapat dilihat
[image:51.612.132.501.313.377.2]pada Tabel 4.2 berikut ini.
Tabel 4.2 Hasil analisis kadar kalsium pada sampel
No Sampel Kadar kalsium (mg/100g)
1. Teri tawar 2556,6971 + 14,4363
2. Teri nasi 575,9832 + 5,6563
3. Teri toge 551,6137 + 3,8413
Hasil pada Tabel 4.2 menunjukkan bahwa ikan teri tawar, teri nasi, dan teri
toge memiliki kandungan mineral kalsium yang berbeda. Kadar kalsium dalam
ikan teri tawar lebih tinggi dibandingkan kadar kalsium teri nasi dan teri toge.
Akibat kekurangan kalsium pada masa pertumbuhan dapat menyebabkan
gangguan pertumbuhan. Tulang kurang kuat, mudah bengkok dan rapuh. Semua
orang dewasa, terutama sesudah usia 50 tahun, kehilangan kalsium dari tulangnya.
Tulang menjadi rapuh dan mudah patah yang dinamakan osteoporosis (Almatsier,
2004).
Spektrofotometri Serapan Atom dapat digunakan sampai 61 logam, non
logam yang dapat dianalisis adalah fosfor dan boron. Sumber nyala yang dipakai
adalah udara-asetilen dengan tempratur nyala 2200°C yang dapat mengatomisasi
ditentukan dengan metode emisi secara fotometri nyala, dengan sumber nyala
propana-udara (1700°C), serta Kalsium membutuhkan suhu yang lebih tinggi
dalam proses atomisasi. Untuk menguraikan senyawa yang bersifat refraktori
secara sempurna menggunakan sumber nyala N2O-asetilen (3000°C), atau dengan
penambahan senyawa penyangga seperti Sr dan La yang dapat mengikat gugus
penggangu (Gandjar dan Rohman, 2007). Tetapi dalam hal ini diperhitungkan
keterbatasan alat serta bahan yang ada.
4.3.6 Penetapan kadar fosfor secara spektrofotometri sinar tampak
Penetapan kadar fosfor dilakukan dengan menggunakan metode asam
askorbat secara spektrofotometri sinar tampak. Sampel yang telah didestruksi
kering berupa PO43- bereaksi dengan ammonium molibdat dan kalium antimonil
tartrat dalam suasana asam membentuk kompleks fosfomolibdat lalu direduksi
dengan asam askorbat membentuk kompleks molibdenum yang bewarna biru dan
stabil selama 2 menit, diukur pada menit ke-49 pada panjang gelombang 710 nm.
Data dan perhitungan dapat dilihat pada Lampiran 13 dan 14, halaman 54 dan 55.
Analisis kemudian dilanjutkan dengan perhitungan statistik dengan
distribusi t pada tingkat kepercayaan 99% (α = 0,01). Berdasarkan hasil
perhitungan statistik tersebut diperoleh kesimpulan bahwa rata-rata kadar fosfor
[image:52.612.130.504.599.664.2]pada sampel dapat dilihat pada Tabel 4.3 di bawah ini.
Tabel 4.3 Hasil analisis kadar fosfor pada sampel
No Sampel Kadar fosfor (mg/100g)
1. Teri tawar 1314,0248 + 12,3870
2. Teri nasi 371,6593 + 5,2116
Menurut Almatsier (2004), kadar kalsium dan fosfor pada ikan teri kering
adalah 1200 mg/100 gram dan 1500 mg/100 gram. Dari hasil pengujian didapat
bahwa kadar kalsium pada teri tawar adalah sebesar (2556,6971 + 14,4363) mg/
100 gram, teri nasi (575,9832 + 5,6563) mg/ 100 gram, dan pada teri toge
(551,6137 + 3,8413) mg/ 100 gram. Sedangkan kadar fosfor pada teri tawar
adalah sebesar (1314,7563 + 12,3870 mg/100 gram, teri nasi (371,6593 + 5,2116)
mg/100 gram, dan pada teri toge (564,6504 + 8,1462) mg/100 gram. Perbedaan
kadar ini dapat dikarenakan perbedaan bentuk tulang dari ikan teri. Tulang ikan
teri kecil lebih lunak dan halus dibandingkan dengan tulang ikan teri besar,
sehingga mempengaruhi komposisi kalsium dan fosfor dari ikan teri.
4.3.7 Batas deteksi dan batas kuantitasi
Berdasarkan data kurva kalibrasi kalsium dan fosfor diperoleh batas
deteksi dan batas kuantitasi untuk kedua mineral tersebut. Batas deteksi dan batas
[image:53.612.132.506.470.517.2]kuantitasi kalsium dan fosfor dapat dilihat pada Tabel 4.4.
Tabel 4.4 Batas deteksi dan batas kuantitasi mineral kalsium dan fosfor
No Mineral Batas Deteksi (µg/ml) Batas Kuantitasi (µg/ml)
1. Kalsium 0,0565 0,1885
2. Fosfor 0,0222 0,0741
Dari hasil perhitungan diperoleh batas deteksi untuk pengukuran kalsium
dan fosfor masing-masing sebesar 0,0565 µg/ml dan 0,0222 µg/ml sedangkan
batas kuantitasinya sebesar 0,1885 µg/ml dan 0,0741 µg/ml.
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh
pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi.
Perhitungan batas deteksi dan batas kuantitasi dapat dilihat pada Lampiran 17,
4.4 Uji Validasi Metode Analisis
4.4.1 Uji perolehan kembali (Recovery)
Hasil uji perolehan kembali (recovery) kadar kalsium dan fosfor setelah
penambahan masing - masing larutan baku dalam sampel dapat dilihat pada Tabel
[image:54.612.131.497.237.309.2]4.5 dan 4.6 berikut ini.
Tabel 4.5 Persen uji perolehan kembali (recovery) kadar kalsium
No. Sampel Recovery (%) Syarat rentang persen recovery (%)
1. Teri tawar 98,49 80-120
2. Teri nasi 93,47 80-120
3. Teri toge 93,40 80-120
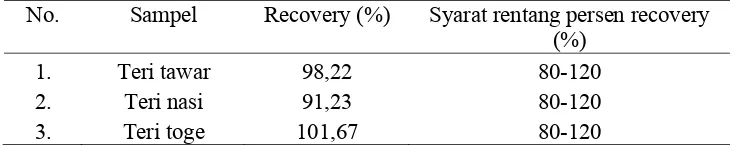
Tabel 4.6 Persen uji perolehan kembali (recovery) kadar fosfor
No. Sampel Recovery (%) Syarat rentang persen recovery (%)
1. Teri tawar 98,22 80-120
2. Teri nasi 91,23 80-120
3. Teri toge 101,67 80-120
Berdasarkan Tabel 4.5 dan 4.6 di atas, dapat dilihat bahwa rata - rata hasil
uji perolehan kembali (recovery) berturut - turut untuk mineral kalsium teri tawar
98,49%, teri nasi 93,47%, dan teri toge 93,40%. Sedangkan hasil uji perolehan
kembali (recovery) berturut-turut untuk mineral fosfor teri tawar 98,22%, teri nasi
91,23%, dan teri toge 101,67%. Persen recovery tersebut menunjukkan
kecermatan kerja yang memuaskan pada saat pemeriksaan kadar kalsium dan
fosfor dalam sampel. Hasil uji perolehan kembali (recovery) ini memenuhi syarat
akurasi yang telah ditetapkan, jika rata - rata hasil perolehan kembali (recovery)
berada pada rentang 80 - 120% (Harmita, 2004). Hasil uji perolehan kembali
[image:54.612.130.498.347.420.2]baku dan contoh perhitungan dapat dilihat pada Lampiran 18 dan 20, halaman 72
dan 76.
4.4.2 Simpangan baku relatif
Nilai simpangan baku dan simpangan baku relatif untuk kalsium dan
fosfor pada sampel ikan teri dapat dilihat pada Tabel 4.7 dan 4.8, sedangkan
[image:55.612.130.509.261.324.2]perhitungannya dapat dilihat pada Lampiran 22 dan 23, halaman 80 dan 83.
Tabel 4.7 Nilai simpangan baku dan simpangan baku relatif kalsium
No Sampel Simpangan Baku Simpangan Baku Relatif
1. Teri tawar 0,83 0,84%
2. Teri nasi 1,54 1,65%
3. Teri toge 1,37 1,47%
Tabel 4.8 Nilai simpangan baku dan simpangan baku relatif fosfor
No Sampel Simpangan Baku Simpangan Baku Relatif
1. Teri tawar 1,13 1,15%
2. Teri nasi 0,61 0,69%
3. Teri toge 1,62 1,59%
Berdasarkan Tabel 4.7 dan 4.8 di atas, dapat dilihat nilai simpangan baku
(SD) untuk mineral kalsium pada teri tawar 0,83; teri nasi 1,54 dan teri toge 1,37
sedangkan untuk nilai simpangan baku relatif pada teri tawar 0,84%, teri nasi
1,65% dan teri toge 1,47%. Dan nilai simpangan baku (SD) untuk mineral fosfor
pada teri tawar 1,13; teri nasi 0,61 dan teri toge 1,62 sedangkan untuk nilai
simpangan baku relatif pada teri tawar 1,15%, teri nasi 0,69% dan teri toge 1,59%.
Menurut Harmita, (2004), nilai simpangan baku relatif (RSD) untuk analit dengan
kadar part per million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan
kadar part per billion (ppb) adalah tidak lebih dari 32%. Dari hasil yang
[image:55.612.132.507.362.424.2]BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian, maka dapat diperoleh kesimpulan sebagai
berikut:
1. Berdasarkan hasil analisis mineral kalsium secara spektrofotometri serapan
atom menunjukkan bahwa kadar kalsium pada ikan teri tawar, teri nasi, dan teri
toge adalah (2556,6971 ± 14,4363) mg/100g, (575,9832 ± 5,6563) mg/100g,
(551,6137 ± 3,8413) mg/100g. Sedangkan hasil analisis mineral fosfor secara
spektrofotometri sinar tampak menunjukkan bahwa kadar fosfor pada ikan teri
tawar, teri nasi, dan teri toge adalah (1314,0248 ± 12,3870) mg/100g,
(371,6593 ± 5,2116) mg/100g, (564,6504 ± 8,1462) mg/100g.
2. Dari hasil pengujian menunjukkan bahwa terdapat perbedaan yang signifikan
antara kadar kalsium dan fosfor antar sampel.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk meneliti mineral lain seperti
DAFTAR PUSTAKA
Anonima. (2014). Diversifikasi