PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
DALAM UMBI LOBAK (
Raphanus sativus
L.) DENGAN
METODE SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
FALDA SEPTIANA
NIM 131524024
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
DALAM UMBI LOBAK (
Raphanus sativus
L.) DENGAN
METODE SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
FALDA SEPTIANA
NIM 131524024
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
DALAM UMBI LOBAK (
Raphanus sativus
L.) DENGAN
METODE SPEKTROFOTOMETRI SERAPAN ATOM
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 28 Agustus 2015
OLEH: FALDA SEPTIANA
NIM 131524024
Medan, September 2015 Fakultas Farmasi
Universitas Sumatera Utara Pejabat Dekan
Dr. Masfria, M.S., Apt. NIP 195707231986012001
Panitia Penguji,
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt. NIP195006071979031001
Pembimbing II,
Prof. Dr. rer. nat. E. De Lux Putra. S.U., Apt. NIP 195306191983031001
Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195401101980032001
Sri Yuliasmi, S. Farm., M. Si., Apt. NIP 198207032008122002
Drs. Fathur Rahman Harun, M.Si.,Apt. NIP 195201041980031002
Pembimbing I,
Drs. Fathur Rahman Harun, M.Si.,Apt. NIP 195201041980031002
iv
KATA PENGANTAR
Bismillaahirrahmaanirrahiim,
Puji dan syukur penulis ucapkan kehadirat Allah SWT, Tuhan semesta
alam, yang telah melimpahkan rahmat dan keberkahan-Nya, sehingga penulis
dapat menyelesaikan penelitian dan penyusunan skripsi ini, serta shalawat dan
salam bagi Rasulullah Muhammad SAW sebagai suri tauladan dalam hidup dan
kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul
“Penetapan Kadar Kalium, Kalsium dan Natrium dalam Umbi Lobak (Raphanus sativus L.)Dengan Metode Spektrofotometri Serapan Atom”.
Penulis mengucapkan terima kasih kepada Ibu Dr. Masfria, M.S., Apt
selaku Pejabat Dekan Fakultas Farmasi Universitas Sumatera Utarayang telah
memberikan fasilitas selama masa pendidikan dan penelitian. Penulis juga
mengucapkan terima kasih kepada Bapak Drs. Fathur Rahman Harun, M.Si., Apt.,
dan Bapak Prof. Dr.rer. nat. Effendy De Lux Putra, S.U., Apt., selaku dosen
pembimbing yang telah memberikan banyak waktu, bimbingan dan nasihat
selama penelitian hingga selesainya penyusunan skripsi ini. Selain itu, penulis
juga mengucapkan terima kasih kepada Bapak Prof. Dr. Jansen Silalahi,
M.App.Sc., Apt, Ibu Dra. Tuty Roida Pardede, M.Si., Apt. Dan Ibu Sri Yuliasmi,
S. Farm., M. Si., Apt. Selaku dosen penguji yang telah memberikan evaluasi dan
masukan kepada penulis dalam penyusunan skripsi ini serta demi kesempurnaan
v
Ismail M.Si., Apt. Selaku dosen pembimbing akademik yang telah memberikan
banyak waktu, nasihat dan bimbingan selama masa pendidikan.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Ayahanda
N. Suharno dan Ibunda Sumirah tercinta yang telah memberikan pengorbanan
tidak ternilai, baik moril maupun materil, juga kepada kedua adik penulis, Naomi
Dwi Aprina dan Widya Tri Monica atas do’a dan dukungannya selama proses
pendidikan hingga penyelesaian skripsi ini.
Penulis juga mengucapkan terima kasih kepada para sahabat penulis,
teman-teman seperjuangan dari Palembang, teman–teman seperjuangan
dilaboratorium penelitian dan teman-teman S-1 Ekstensi tahun 2013 dan Reguler
Farmasi USU, terima kasih atas dukungannya dalam penyelesaian skripsi ini. Dan
kepada semua pihak yang terlibat, semoga berlapis-lapis keberkahan dilimpahkan
di tiap keadaan.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan,
sehingga penulis mengharapkan kritik dan saran yang bersifat membangun.Akhir
kata, semoga tulisan ini dapat bermanfaat bagi pembaca dan menjadi sumbangan
yang berarti bagi ilmu pengetahuan khususnya dalam bidang ilmu farmasi.
Medan, Agustus 2015 Penulis,
vi
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM DALAM UMBI LOBAK (Raphanus sativus L.) DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Lobak (Raphanus sativus L.) adalah anggota keluarga kubis-kubisan yang ditanam diberbagai daerah, yang mana seluruh bagian tanaman lobak dapat dimanfaatkan untuk berbagai keperluan dalam kehidupan manusia.Umbi lobak dapat dimakan mentah sebagai lalapan, dibuat acar atau asinan, direbus dan disayur.Daunnya yang masih muda dapat dijadikan lalapan mentah ataupun dimasak. Selain itu umbi lobak juga memiliki banyak khasiat sebagai obat tradisional, mengandung berbagai nutrisi yang bermanfaat bagi tubuh berupa mineral yaitu kalsium, fosfor, besi, natrium dan kalium. tujuan dari penelitian ini adalah untuk mengetahui penurunan kadar mineral kalium, kalsium dan natrium pada umbi lobak segar dan umbi lobak rebus.
Sampel diambil dari perkebunan warga Kota Berastagi Kabupaten Karo Medan. Sebelum dilakukan analisis mineral ini diubah terlebih dahulu dari bentuk organik menjadi mineral anorganik dengan menggunakan proses dekstruksi kering. Penetapan kadar ketiga mineral dilakukan menggunakan spektrofotometer serapan atom dengan nyala udara asetilen pada panjang gelombang 766,5 nm untuk kalium, panjang gelombang 422,7 nm untuk kalsium dan panjang gelombang 589,0 nm untuk natrium.
Hasil penelitian menunjukkan kadar kalium dalam umbi lobak segar dan umbi lobak rebus adalah 246,5599 ± 31,8540 mg/100 g dan 146,1934 ± 14,8109 mg/100 g. Kadar kalsium dalam umbi lobak segar dan umbi lobak rebus adalah 28,9644 ± 0,2965 mg/100 g dan 25,1493 ± 0,9462 mg/100 g. Kadar natrium pada umbi lobak segar dan umbi lobak rebus adalah 16,7984 ± 0,6970 mg/100 g dan 10,3169 ± 1,1941mg/100 g. Persentase penurunan kadar mineral pada umbi lobak setelah dilakukan perebusan adalah sebesar 40,71 % untuk kalium, 12,36 % untuk kalsium dan 38,58 % untuk natrium.
Secara statistik, uji beda rata-rata kandungan kalium, kalsium dan natrium untuk umbi lobak segar dan umbi lobak rebus dengan menggunakan uji t, menyimpulkan bahwa kandungan kalium, kalsium dan natrium pada umbi lobak segar lebih tinggi secara signifikan dari umbi lobak rebus.
vii
DETERMINATION OF POTASSIUM, CALCIUM AND SODIUM LEVELS IN RADISH TUBER (Raphanus sativus L.) WITH ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Radish (Raphanus sativus L.) is a member of the cabbage family are planted in various areas, in which all parts of the plant radish can be used for various purposes in human life. Radish tubers can be eaten raw as fresh vegetables, made pickles or pickled, boiled and be cooked. The young leaves can be used raw or cooked vegetables. Besides tuber radish also has many benefits as a traditional medicine, contains a variety of nutrients that are beneficial to the body in the form of minerals that calcium, phosphorus, iron, sodium and potassium. The purpose of this study was to determine the reduced levels of minerals potassium, calcium and sodium in fresh tuber radish and boiled tuber radish.
Sample were taken from the plantation residents ini berastagi city, Karo Regency medan. Before to the analysis this minerals are first converted from organic forms into inorganic mineral by using the dry destruction process. The three minerals assay was performed using atomic absorption spectrophotometer with Acetylene air flame at a wavelength of 766.5 nm for potassium, the wavelength of 42.7 nm for calcium and wavelength 589.0 nm for sodium.
The results showed that levels of potassium in the fresh radish tuber and boiled radish tubers is 246.5599 ± 31.8540 mg/100 g and 146.1934 ± 14.8109 mg/100 g. Calcium levels in in the fresh radish tuber and boiled radish tubers are 28.9644 ± 0.2965 mg/100g and 25.1493 ± 0.9462 mg/100 g. Sodium levels in in the fresh radish tuber and boiled radish tubers are 16.7984 ± 0.6970 mg/100 g and 10.3169 ± 1.1941 mg/100 g. The percentage of decrease in the mineral levels in content in the fresh radish tuber and boiled radish tubers were 40.71% for potassium, 12.36% for calcium and 38.58 % for sodium
Statistically, the average difference test potassium, calcium and sodium for in the fresh radish tuber and boiled radish tubers using the t test, concluded that the content of potassium, calcium and sodium in fresh radish tuber is significantly higher than boiled radish tuber.
viii DAFTAR ISI
Halaman
JUDUL ... ….. i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRAC ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB IPENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Lobak ... 5
2.1.1 Taksonomi Tanaman Lobak ... 6
2.1.2 Morfologi Tanaman Lobak ... 7
2.2 Mineral ... 8
ix
2.2.2 Kalsium ... 10
2.2.3 Natrium ... 11
2.3 Spektrofotometri Serapan Atom ... 12
2.3.1 Prinsip Dasar Spektrofotometri Serapan Atom ... 12
2.3.2 Instrumensasi Spektrofotometri Serapan Atom ... 13
2.3.3 Gangguan-gangguan Pada Spektrofotometri Serapan Atom ... 15
2.4 Metode Validasi ... 16
BAB III METODE PENELITIAN ... 20
3.1 Tempat dan Waktu Penelitian ... 20
3.2Bahan- bahan ... 20
3.2..1 Sampel ... 20
3.2.2 Pereaksi ... 20
3.3Alat - alat... 21
3.4 Pembuatan Pereaksi larutan HNO3 (1:1) ... 21
3.5 Prosedur Penelitian ... 21
3.5.1 Pengambilan Sampel ... 21
3.5.2 Penyiapan Sampel ... 21
3.5.3 Proses Destruksi ... 22
3.5.4 Pembuatan Larutan Sampel ... 22
3.5.5 Pemeriksaan Kuantitatif ... 23
3.5.5.1 Pembuatan Kurva Kalibrasi Kalium ... 23
3.5.5.2 Pembuatan Kurva Kalibrasi Kalsium ... 23
x
3.5.6 Penetapan Kadar Kalium, Kalsium dan Natrium
dalam Sampel ... 24
3.5.6.1 Penetapan Kadar Kalium Dalam Umbi Lobak Segar Dan Umbi Lobak Rebus ... 24
3.5.6.2 Penetapan Kadar Kalsium Dalam Umbi Lobak Segar Dan Umbi Lobak Rebus ... 25
3.5.6.5 Penetapan kadar Natrium Dalam Umbi Lobak Segar dan Umbi Lobak Rebus ... 25
3.5.7Analisa Data Secara Statistik ... 26
3.5.7.1 Penolakan Hasil Pengamatan ... 26
3.5.7.2 Pengujian Beda NIlai Rata-Rata Antar Sampel ... 27
3.5.8 Uji akurasi (Recovery) ... 28
3.5.9 Uji Presisi (Simpangan baku Relatif) ... 29
3.5.10 Penentuan Batas Deteksi (Limit Of Detection) dan Batas Kuantitasi (Limit Of Quantitation) ... 29
BAB IV HASIL DAN PEMBAHASAN ... 31
4.1 Kurva Kalibrasi Kalium, Kalsium dan natrium ... 31
4.2 Analisis Kadar Kalium, Kalsium dan Natrium Dalam Umbi Lobak Segar dan Umbi Lobak Rebus ... 33
4.3. Uji akurasi (Recovery) ... 34
4.4 Uji Presisi (Simpangan Baku Relatif) ... 37
4.5 Batas Deteksi dan Batas Kuantitasi ... 37
BAB V KESIMPULAN DAN SARAN ... 39
5.1 Kesimpulan ... 39
xi
DAFTAR PUSTAKA ... 40
xii
DAFTAR TABEL
Tabel Halaman
4.1 Hasil analisis kadar kalium, kalsium dan natrium dalam
sampel... 33
4.2 Hasil penurunan kadar kalium, kalsium dan natrium pada
umbi lobak segar dan umbi lobak rebus ... 34
4.3 Hasil uji beda rata-rata kadar kalium, kalsium dan natrium antar sampel... 35
4.4 Persen uji perolehan kembali (recovery) kadar kalium,
kalsium dan natrium ... 36
4.5 Batas deteksi dan batas kuantitasi kalium, kalsium dan
xiii
DAFTAR GAMBAR
Gambar Halaman
2.1 Sistem Peralatan Spektrofotometri Serapan Atom ... 13
4.1 Kurva Kalibrasi Larutan Baku Kalium ... 31
4.2 Kurva Kalibrasi Larutan Baku Kalsium ... 32
xiv
DAFTAR LAMPIRAN
Lampiran Halaman
1. Gambar Umbi Lobak... 42
2. Hasil Identifikasi Tanaman ... 43
3. Bagan Alir Proses Destruksi Kering (Umbi Lobak Segar) 44
4. Bagan Alir Proses Destruksi Kering (Umbi Lobak Rebus) 45
5. Bagan Alir Pembuatan Larutan Sampel ... 46
6. Data Kalibrasi Kalium Dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis regresi dan Koefisien Korelasi ... 47
7. Data Kalibrasi Kalsium Dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis regresi dan Koefisien Korelasi ... 49
8. Data Kalibrasi Natrium Dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis regresi dan Koefisien Korelasi ... 51
9. Hasil Analisis Kadar Kalium, Kalsium dan Natrium
Dalam Umbi Lobak Segar (LS) ... 53
10. Hasil Analisis Kadar Kalium, Kalsium dan Natrium
Dalam Umbi Lobak Rebus (LR) ... 54
11. Contoh Perhitungan Kadar Kalium, Kalsium dan
Natrium dalam Umbi Lobak Segar (LS) ... 55
12. Perhitungan Statistik kadar kalium, Kalsium dan
Natrium dalam Sampel umbi Lobak Segar (LS) ... 57
13. Perhitungan Statistik kadar kalium, Kalsium dan
Natrium dalam Sampel umbi Lobak Rebus (LR) ... 64
14. Persentase Penurunan Kadar Kalium, Kalsium dan
xv
15. Pengujian Nilai Beda Rata-Rata Kadar Kalium,
Kalsium dan Natrium pada Umbi Lobak Segar dan Umbi Lobak Rebus ... 71
16. Hasil analisis Kadar Kalium, kalsium dan Natrium
Sebelum dan Sesudah penambahan masing-masing
larutan baku Pada umbi Lobak ... 77
17. Perhitungan Uji Perolehan Kembali Kadar Kalium,
kalsium dan natrium Dalam Umbi Lobak ... 80
18. Perhitungan Simpangan Baku Relatif (RSD) Dalam
sampel Umbi Lobak ... 98
19. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi
(LOQ) ... 101
20. Gambar Alat Spektrofotometer Serapan Atom dan Alat
Tanur ... 104
21. Tabel Distribusi t ... 104
vi
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM DALAM UMBI LOBAK (Raphanus sativus L.) DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Lobak (Raphanus sativus L.) adalah anggota keluarga kubis-kubisan yang ditanam diberbagai daerah, yang mana seluruh bagian tanaman lobak dapat dimanfaatkan untuk berbagai keperluan dalam kehidupan manusia.Umbi lobak dapat dimakan mentah sebagai lalapan, dibuat acar atau asinan, direbus dan disayur.Daunnya yang masih muda dapat dijadikan lalapan mentah ataupun dimasak. Selain itu umbi lobak juga memiliki banyak khasiat sebagai obat tradisional, mengandung berbagai nutrisi yang bermanfaat bagi tubuh berupa mineral yaitu kalsium, fosfor, besi, natrium dan kalium. tujuan dari penelitian ini adalah untuk mengetahui penurunan kadar mineral kalium, kalsium dan natrium pada umbi lobak segar dan umbi lobak rebus.
Sampel diambil dari perkebunan warga Kota Berastagi Kabupaten Karo Medan. Sebelum dilakukan analisis mineral ini diubah terlebih dahulu dari bentuk organik menjadi mineral anorganik dengan menggunakan proses dekstruksi kering. Penetapan kadar ketiga mineral dilakukan menggunakan spektrofotometer serapan atom dengan nyala udara asetilen pada panjang gelombang 766,5 nm untuk kalium, panjang gelombang 422,7 nm untuk kalsium dan panjang gelombang 589,0 nm untuk natrium.
Hasil penelitian menunjukkan kadar kalium dalam umbi lobak segar dan umbi lobak rebus adalah 246,5599 ± 31,8540 mg/100 g dan 146,1934 ± 14,8109 mg/100 g. Kadar kalsium dalam umbi lobak segar dan umbi lobak rebus adalah 28,9644 ± 0,2965 mg/100 g dan 25,1493 ± 0,9462 mg/100 g. Kadar natrium pada umbi lobak segar dan umbi lobak rebus adalah 16,7984 ± 0,6970 mg/100 g dan 10,3169 ± 1,1941mg/100 g. Persentase penurunan kadar mineral pada umbi lobak setelah dilakukan perebusan adalah sebesar 40,71 % untuk kalium, 12,36 % untuk kalsium dan 38,58 % untuk natrium.
Secara statistik, uji beda rata-rata kandungan kalium, kalsium dan natrium untuk umbi lobak segar dan umbi lobak rebus dengan menggunakan uji t, menyimpulkan bahwa kandungan kalium, kalsium dan natrium pada umbi lobak segar lebih tinggi secara signifikan dari umbi lobak rebus.
vii
DETERMINATION OF POTASSIUM, CALCIUM AND SODIUM LEVELS IN RADISH TUBER (Raphanus sativus L.) WITH ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Radish (Raphanus sativus L.) is a member of the cabbage family are planted in various areas, in which all parts of the plant radish can be used for various purposes in human life. Radish tubers can be eaten raw as fresh vegetables, made pickles or pickled, boiled and be cooked. The young leaves can be used raw or cooked vegetables. Besides tuber radish also has many benefits as a traditional medicine, contains a variety of nutrients that are beneficial to the body in the form of minerals that calcium, phosphorus, iron, sodium and potassium. The purpose of this study was to determine the reduced levels of minerals potassium, calcium and sodium in fresh tuber radish and boiled tuber radish.
Sample were taken from the plantation residents ini berastagi city, Karo Regency medan. Before to the analysis this minerals are first converted from organic forms into inorganic mineral by using the dry destruction process. The three minerals assay was performed using atomic absorption spectrophotometer with Acetylene air flame at a wavelength of 766.5 nm for potassium, the wavelength of 42.7 nm for calcium and wavelength 589.0 nm for sodium.
The results showed that levels of potassium in the fresh radish tuber and boiled radish tubers is 246.5599 ± 31.8540 mg/100 g and 146.1934 ± 14.8109 mg/100 g. Calcium levels in in the fresh radish tuber and boiled radish tubers are 28.9644 ± 0.2965 mg/100g and 25.1493 ± 0.9462 mg/100 g. Sodium levels in in the fresh radish tuber and boiled radish tubers are 16.7984 ± 0.6970 mg/100 g and 10.3169 ± 1.1941 mg/100 g. The percentage of decrease in the mineral levels in content in the fresh radish tuber and boiled radish tubers were 40.71% for potassium, 12.36% for calcium and 38.58 % for sodium
Statistically, the average difference test potassium, calcium and sodium for in the fresh radish tuber and boiled radish tubers using the t test, concluded that the content of potassium, calcium and sodium in fresh radish tuber is significantly higher than boiled radish tuber.
1 BAB I
PENDAHULUAN
1.1Latar Belakang
Lobak (Raphanus Sativus L.) adalah anggota keluarga kubis-kubisan yang ditanam diberbagai daerah di dunia. Ada dua tipe lobak yakni lobak tipe dua
tahunan yang berasal dari iklim non-tropis dan iklim tropis (Suprakarn, dkk.,
2005). Hampir seluruh bagian tanaman lobak dapat dimanfaatkan untuk berbagai
keperluan dalam kehidupan manusia.Umbi lobak dapat dimakan mentah sebagai
lalapan, dibuat acar atau asinan, direbus dan disayur.Daunnya yang masih muda
dapat dijadikan lalapan mentah ataupun dimasak.Dalam berbagai literatur
ditemukan bahwa tanaman lobak berkhasiat sebagai obat tradisional (Rukmana,
1995).
Lobak merupakan diuretik yang cukup kuat. Pembuangan asam urat melalui
urin akan terbantu dengan minum jus lobak. Fungsi lainnya adalah sebagai
perangsang napsu makan dan memperbaiki kerja pencernaan.Lobak juga memiliki
enzim diastase dalam jumlah banyak yang berfungsi mempermudah dan
memperlancar pencernaan zat pati dalam usus.Lobak dapat dipakai untuk
menghalangi penumpukan lemak dalam jaringan tubuh.Jus lobak dan jeruk sangat
baik untuk system saraf sehingga mengurangi ketegangan (stress), karena
kandungan vitamin B-nya tinggi.Minyak yang terdapat dalam lobak baik untuk
membersihkan empedu dan ginjal sehingga mencegah timbulnya batu ginjal (Adi,
2006).
Berbagai nutrisi yang bermanfaat bagi tubuh yang terdapat pada umbi
2
gr, karbohidrat 5,30 g, serat 0,60 g, abu 0,50 g, vitamin B1 0,03 mg, vitamin B2
0,03 mg, vitamin C 25,00 mg dan niasin 0,3 mg. sedangkan mineral yang
dikandungnya adalah kalsium 32,00 mg, fosfor 21,00 mg, zat besi 0,60 mg,
natrium 10,0 mg, kalium 218,0 mg (Rukmana, 1995).
Kalium merupakan cairan intra seluler utama, dan memainkan peranan
penting pada proses metabolisme sel. Kalium hanya terdapat sedikit pada cairan
ekstra seluler (Horne dan Swearingen, 1995). Peningkatan asupan kalium dalam
diet telah dihubungkan dengan penurunan tekanan darah, karena kalium dapat
memicu natriuresis (kehilangan natrium melalui urin) dan bermanfaat bagi
kesehatan jantung (Barasi, 2007).Namun, bila kelebihan kalium menyebabkan
hiperkalemia yang dapat menyebabkan aritmia jantung, konsentrasi yang lebih
tinggi lagi dapat menyebabkan henti jantung atau fibrilasi jantung (Yasmir dan
Ferawati, 2012).
Kalsium ada dalam tubuh dalam bentuk garam kalsium dan sebagai
ionisasi (Tambayong, 1999).Kalsium dan mineral lain memberi kekuatan dan
bentuk pada tulang dan gigi (Almatshier, 2004). Kalsium dapat mengatur tekanan
darah, pada penderita tekanan darah tinggi kalsium yang masuk kedalam darah
akan menurunkan tekanan darah. Sedangkan pada keadaan normal kalsium akan
membantu mempertahankan tekanan darah. Tekanan darah yang stabil mampu
mencegah stres dan menimbulkan perasaan rileks (Astawan dan Leomitro, 2009).
Natrium adalah kation utama dalam darah dan cairan ekstraseluler yang
mencakup 95% dari seluruh kation.Oleh karena itu, mineral ini sangat berperan
dalam pengaturan cairan tubuh, termasuk tekanan darah dan keseimbangan asam
3
perbedaan potensial (listrik) yang perlu bagi kontraksi otot dan penerusan impuls
disaraf (Tan dan Rahardja, 2007).Dalam keadaan normal, natrium yang
dikeluarkan melalui urine sejajar dengan jumlah natrium yang dikonsumsi.Jumlah
natrium dalam urin tinggi bila konsumsi tinggi dan rendah jika konsumsi rendah
(Almatshier, 2004).
Berdasarkan uraian diatas, peneliti tertarik untuk meniliti kandungan
kalium, kalsium, dan natrium yang terdapat dalam umbi lobak (Raphanus sativus
L.). Metode yang dipilih untuk mengetahui kadar kalium, kalsium dan natrium
pada sampel dengan menggunakan metode spektrofotometri serapan atom, karena
cara analisis ini dapat memberikan kadar total unsur logam dalam suatu sampel
dan tidak bergantung pada bentuk molekul dari logam dalam sampel tersebut.
Metode ini sangat cocok digunakan untuk analisis sekelumit logam karena
kepekaannya yang tinggi (batas deteksi kurang dari 1ppm), pelaksanaannya
relatif sederhana, dan interferensinya sedikit ( Gandjar dan Rohman, 2009).
1.2Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini
dapat dirumuskan sebagai berikut:
a. Berapakah kadar mineral kalium, kalsium dan natrium dalam umbi lobak
segar dan umbi lobak rebus ?
b. Apakah terdapat penurunan kadar kalium, kalsium dan natrium pada umbi
4 1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis dalam
penelitian ini dapat dirumuskan sebagai berikut:
a. Umbi lobak segar dan umbi lobak rebus memiliki kandungan mineral
kalium, kalsium dan natrium dalam jumlah tertentu.
b. Terdapat penurunan kadar kalium, kalsium dan natrium pada umbi lobak
segar dan umbi lobak rebus.
1.4Tujuan
Berdasarkan hipotesis di atas, maka tujuan dari penelitian ini dapat
dirumuskan sebagai berikut:
a. Untuk mengetahui kadar kalium, kalsium dan natrium dalam umbi lobak
segar dan umbi lobak rebus.
b. Untuk mengetahui penurunan kadar kalium, kalsium dan natrium dalam
umbi lobak segar dan umbi lobak rebus.
1.5Manfaat
Untuk memberikan informasi kepada masyarakat perbedaan kandungan
kalium,natrium dan kalsium padaumbi lobak segar dan umbi lobak rebus.
sehingga masyarakat dapat memilih cara mengkonsumsi umbi lobak yang baik
dalam bentuk segar atau dengan perebusan yang baik tanpa mengurangi nilai
5 BAB II
TINJAUAN PUSTAKA
2.1 Lobak
Lobak (Raphanus sativus L.) adalah anggota keluarga kubis dan ditanam diberbagai lokasi didunia.Umbi lobak yang rasanya agak pedas memiliki bentuk,
dan ukuran yang bervariasi.Tipe yang pertama adalah tipe dua tahunan yang
berasal dari iklim non-tropis dan memerlukan periode dingin untuk
berbunga.Lobak jepang, amerika, dan eropa termasuk dalam jenis ini. Tipe yang
kedua berasal dari daerah tropis yang tidak memerlukan periode dingin untuk
berbunga (Suprakarn, dkk., 2005).
Hampir seluruh bagian tanaman lobak dapat dimanfaatkan untuk berbagai
keperluan dalam kehidupan manusia.Umbi lobak dapat dimakan mentah sebagai
lalapan, dibuat acar atau asinan, direbus dan disayur.Daunnya yang masih muda
dapat dijadikan lalapan mentah ataupun dimasak.Dalam berbagai literatur
ditemukan bahwa tanaman lobak berkhasiat sebagai obat tradisional (Rukmana,
1995).
Lobak merupakan diuretik yang cukup kuat. Pembuangan asam urat
melalui urin akan terbantu dengan minum jus lobak. Fungsi lainnya adalah
sebagai perangsang napsu makan dan memperbaiki kerja pencernaan.Lobak juga
memiliki enzim diastase dalam jumlah banyak yang berfungsi mempermudah dan
memperlancar pencernaan zat pati dalam usus.Lobak dapat dipakai untuk
menghalangi penumpukan lemak dalam jaringan tubuh.Jus lobak dan jeruk sangat
6
kandungan vitamin B-nya tinggi.Minyak yang terdapat dalam lobak baik untuk
membersihkan empedu dan ginjal sehingga mencegah timbulnya batu ginjal (Adi,
2006).
Dalam kapasitasnya sebagai bahan sayur-mayur yang banyak digemari
masyarakat luas, ternyata lobak memiliki gizi yang cukup tinggi dan lengkap
komposisinya, beberapa kandungan gizi pada tanaman lobak tiap 100 g bahan
adalah kalori 21,0 kkal, protein 0,6 g, lemak 0,10 g, karbohidrat 5,30 g, serat 0,60
g, abu 0,50 g, vitamin B1 0,03 mg, vitamin B2 0,03 mg, vitamin C 25,00 mg dan
niasin 0,3 mg. sedangkan mineral yang dikandungnya adalah kalsium 32,00 mg,
fosfor 21,00 mg, zat besi 0,60 mg, natrium 10,0 mg, kalium 218,0 mg (Rukmana,
1995).
2.1.1 Taksonomi Tanaman Lobak
Kedudukan tanaman lobak dalam sistematika tumbuhan (taksonomi)
menurut Rukmana (1995), dikelompokkan sebagai berikut :
Kingdom : Plantae (tumbuh-tumbuhan).
Divisi : Spermatophyta (tumbuhan berbiji)
Sub-divisi : Angiospermae (berbiji tertutup)
Kelas : Dicotyledonae (biji berkeping dua)
Famili : Brassicaceae (Cruciferae)
Genus : Raphanus
Spesies : Raphanus sativus L.
Kerabat dekat tanaman lobak yang termasuk suku kubis-kubisan
7
sativus L. yang umum dibudidayakan adalah Rades (R. sativus L. var. radicula
Pres. A. DC.). Tanaman ini berasal dari Rusia dan Asia tropis yang bentuk
umbinya bulat sampai semi bundar mirip dengan umbi rades (Rukmana, 1995).
2.1.2 Morfologi Tanaman Lobak
Lobak merupakan tanaman semusim atau setahun (annual) yang berbentuk perdu.Susunan tubuh tanaman lobak pada dasarnya terdiri atas akar, batang, daun,
bunga, buah dan biji.Perakaran tanaman lobak dibedakan atas tiga macam yaitu
akar tunggang, akar lembaga dan akar cabang atau akar serabut.Akar tembaga
(Radicula) terbentuk pada stadium biji berkecambah, kemudian berkembang membesar dan memanjang menjadi akar tunggang (radix primaria). Lambat laun akar tunggang ini akan berubah bentuk dan fungsinya sebagai tempat
penyimpanan makanan cadangan atau disebut “umbi” yang sekaligus tempat
menempelnya akar-akar rambut (fibrilia) (Rukmana, 1995).
Bentuk umbi lobak umumnya bulat panjang, warna kulit dan daging umbi
putih bersih, namun setelah ditemukan ragam varietas lobak hibrida (Daikon) banyak mengalami perubahan-perubahan.Ukuran umbi lobak hibrida umumnya
besar-besar dengan bentuk umbi sangat bervariasi antar bulat-panjang, semibulat
sampai bundar.Demikian pula warna kulit dan daging umbi lobak hibrida sangat
beragam, diantaranya ada yang berwarna putih-bersih dan putih kehijau-hijauan
(Rukmana, 1995).
Batang umbi lobak sangat pendek seolah-olah hampir tidak jelas
penampilan batangnya.Struktur batang ini berbuku-buku dan sedikit berkayu
tempat melekatnya tangkai daun.Daun lobak bentuknya panjang lonjong,
8
halus.Struktur daun lobak cultivura lokal umumnya tumbuh tunggal, namun pada
lobak hibrida tiap tangkai daun terdapat beberapa helai daun yang letaknya
berpasangan seolah-olah menjari (Rukmana, 1995).
Tanaman lobak yang umurnya cukup dewasa untuk memasuki fase
reproduktif akan menghasilkan rangkaian bunga. Rangkaian bunga tumbuh dari
ujung tanaman, bercabang banyak dan tiap cabang rangkaian bunga terdapat
banyak kuntum bunga yang berwarna putih dengan variasi warna ungu dibagian
ujungnya.Bunga lobak dapat menghasilkan buah yang bentuknya mirip “polong”,
tiap buah (polong) berisi biji antara 1-6 butir.Bentuk biji lobak bulat kecil,
sewaktu masih muda berwarna hijau, sedangkan setelah tua menjadi warna hitam
atau kecoklatan.Biji-biji inilah yang banyak dipergunakan sebagai bahan
perbanyakan tanaman secara generatif (Rukmana, 1995).
2.2 Mineral
Mineral adalah bagian dari tubuh yang memegang peranan penting dalam
pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun fungsi
tubuh secara keseluruhan. Disamping itu, mineral berperan dalam berbagai tahap
metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim (Almatsier,
2004).
Tubuh tidak mampu mensintesa mineral sehingga unsur-unsur ini harus
didapatkan melalui makanan.Mineral merupakan unsur essensial bagi fungsi
normal dengan enzim dan sangat penting dalam pengendalian komposisi dalam
9
proses metabolism berlangsung. Mineral merupakan konstituen essensial pada
jaringan, lemak, cairan dan otot (Budiyanto, 2004).
Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral
makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg
sehari, sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari. Jumlah
mineral mikro dalam tubuh kurang dari 15 mg. Yang termasuk mineral makro
adalah natrium, kalium, kalsium, fosfor, magnesium dan sulfur. Adapun yang
termasuk mineral mikro adalah besi, seng, mangan dan tembaga (Almatsier,
2004).
2.2.1 Kalium
Tubuh manusia mengandung sekitar 2,6 mg K perkilogram berat badan
tanpa atau bebas lemak, terutama bagian yang banyak mengandung unsur kalium
yaitu sel-sel saraf dan otot, dalam jumlah kecil dijumpai dalam cairan ekstra
selluler. Di dalam cairan ekstraselluler unsur kalium sama halnya dengan natrium,
yang merupakan kation penting yang berperan dalam keseimbangan pH dan
osmolaritas ( Kartasapoetra dan Marsetyo, 2008).
Kalium terdapat di dalam semua makanan berasal dari tumbuh-tumbuhan
dan hewan. Sumber utama adalah makanan mentah/segar, terutama buah, sayuran
dan kacang-kacangan. Kebutuhan minimum akan kalium ditaksir sebanyak 2000
mg sehari (Almatsier, 2004).
Beberapa fungsi kalium dalam tubuh menurut Almatsier (2004) adalah :
a. Bersama dengan natrium memelihara keseimbangan cairan dan elektrolit
10
b. Bersama kalsium kalium berperan dalam transmisi saraf dan relaksasi otot
c. Didalam sel, kalium berfungsi dalam metabolism energy, sintesis glikogen
dan protein
d. Perbandingan kalium dan natrium dalam darah dapat mengatur atau
mempertahankan tekanan darah normal.
2.2.2 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh,
yaitu 1,5-2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Dari
jumlah ini, sebanyak 99% berada di dalam jaringan keras, yaitu tulang dan gigi,
selebihnya tersebar luas di dalam tubuh. Di dalam cairan ekstraselular dan
intraselular, kalsium memegang peranan penting dalam mengatur fungsi sel,
seperti untuk transmisi impuls di saraf, kontraksi otot, penggumpalan darah dan
menjaga permeabilitas membran sel (Almatsier, 2004).
Kalsium diekskresikan lewat urin serta feses dan untuk mencegah
kehilangan ini diperlukan kalsium melalui makanan. Kalsium tambahan
diperlukan dalam keadaan tertentu seperti pada masa pertumbuhan mulai dari
anak-anak hingga usia remaja dan pada saat hamil untuk memenuhi kebutuhan
janin (Budiyanto, 2004).
Angka kecukupan rata-rata sehari untuk kalsium bagi orang Indonesia
yang ditetapkan adalah 300mg–400mg pada bayi, 500mg pada anak-anak,
600mg–700mg pada remaja, 500mg–800mg pada orang dewasa, serta lebih besar
11
pertumbuhan dapat menyebabkan gangguan pertumbuhan seperti tulang kurang
kuat, mudah bengkok dan rapuh (Almatsier, 2004).
Sumber kalsium utama adalah susu dan hasil olahan susu seperti keju. Ikan
yang dimakan dengan tulang, termasuk ikan kering merupakan sumber kalsium
yang baik. Sereal, kacang-kacangan dan hasil kacang-kacangan, tahu, tempe, serta
sayuran hijau merupakan sumber kalsium yang baik (Almatsier, 2004).
Menurut Kartasapoetra dan Marsetyo (2008) kekurangan kalsium didalam
tubuh dapat menimbulkan :
a. Karies dentis atau kerusakan pada gigi
b. Pertumbuhan tulang menjadi tidak sempurna dan dapat menimbulkan
rakhitis
c. Apabila terdapat bagian tubuh yang terluka darah akan sukar membeku
d. Terjadinya kekejangan pada otot.
2.2.3 Natrium
Natrium adalah kation utama dalam cairan ekstraselluler.Terdapat 35-40%
natrium di dalam tubuh pada cairan saluran cerna, cairan empedu dan pankreas
mengandung banyak natrium.Sumber utama natrium adalah garam dapur atau
NaCl (Almatsier, 2004).
Sumber natrium diantaranya adalah: keju, ikan asin, udang, sayur-sayuran,
bayam, seledri, sereal, buah-buahan, susu, telur dan daging. Natrium harus berada
dalam jumlah yang cukup pada makanan agar kecukupan Na dapat terjamin.
Tubuh sendiri dapat mengatur kadar Na dalam tubuh dan mengeluarkannya
12
jumlah yang berlebih pada keadaan ini asupan Na perlu dibatasi (Budiyanto,
2004).
Beberapa fungsi natrium bagi tubuh menurut Almatsier (2004) adalah:
a. Mengatur tekanan osmosis pada sel
b. Menjaga keseimbangan asam basa didalam tubuh
c. Berperan dalam transmisi saraf dan kontraksi otot
d. Berperan dalam absorbs glukosa dan sebagai alat angkut zat-zat lain
melalui membran.
2.3 Spektrofotometri Serapan Atom
2.3.1 Prinsip Dasar Spektrofotometri Serapan Atom
Spektroskopi serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak
tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok
untuk analisis logam karena mempunyai kepekaan yang tinggi (batas deteksi
kurang dari 1 ppm), pelaksanaannya relatif sederhana dan interferensinya sedikit
(Gandjar dan Rohman, 2009).
Spektroskopi serapan atom didasarkan pada absorbsi cahaya oleh atom.
Atom-atom akan menyerap cahaya pada panjang gelombang tertentu tergantung
pada sifat unsurnya. Sebagai contoh kalium menyerap cahaya pada panjang
gelombang 766,5 nm; kalsium menyerap cahaya pada panjang gelombang 422,7
nm dan Natrium menyerap cahaya pada panjang gelombang 589,0 nm. Cahaya
13
elektronik suatu atom. Dengan menyerap suatu energi, maka atom akan
memperoleh energi sehingga suatu atom pada keadaan dasar dapat dinaikkan
tingkat energinya ke tingkat eksitasi (Khopkar, 1990; Gandjar dan Rohman,
2009).
Interaksi materi dengan berbagai energi seperti energi panas, energi
radiasi, energi kimia dan energi listrik selalu memberikan sifat-sifat yang spesifik
untuk setiap unsur. Besarnya perubahan yang terjadi biasanya sebanding dengan
jumlah unsur atau persenyawaan yang terdapat di dalamnya. Proses interaksi ini
mendasari analisis spektrofotometri atom yang dapat berupa emisi dan absorbsi
(Gandjar dan Rohman, 2009).
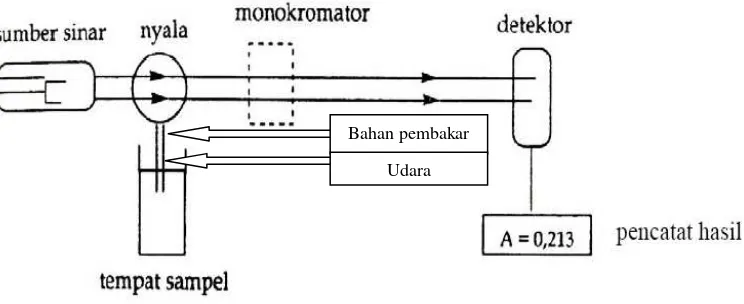
2.3.2 Instrumentasi Spektrofotometri Serapan Atom
Menurut Gandjar dan Rohman(2009), sistem peralatan spektrofotometer
[image:30.595.128.500.457.609.2]serapan atom dapat dilihat pada Gambar 2.1.
Gambar 2.1 Sistem Peralatan Spektrofotometri Serapan Atom (Gandjar dan Rohman, 2009).
a. Sumber sinar
Sumber sinar yang umum dipakai adalah lampu katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
Bahan pembakar
14
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari
unsur atau dilapisi unsur yang sama dengan unsur yang akan dianalisis. Tabung
logam ini diisi dengan gas mulia dengan tekanan rendah yang jika diberikan
tegangan pada arus tertentu, katoda akan memancarkan elektron-elektron yang
bergerak menuju anoda dengan kecepatan dan energi yang tinggi. Elektron dengan
energi tinggi ini akan bertabrakan dengan gas mulia sehingga gas mulia
kehilangan elektron dan menjadi ion bermuatan positif. Ion gas mulia bermuatan
positif akan bergerak menuju katoda dengan kecepatan dan energi yang tinggi
sehingga menabrak unsur-unsur yang terdapat pada katoda. Akibat tabrakan ini,
unsur-unsur akan terlempar ke luar permukaan katoda dan mengalami eksitasi ke
tingkat energi elektron yang lebih tinggi (Gandjar dan Rohman, 2009).
b. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral. Ada berbagai macam alat
yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom
yaitu dengan nyala (flame) dan tanpa nyala (flameless) (Gandjar dan Rohman, 2009).
Teknik atomisasi dengan nyala bergantung pada suhu yang dapat dicapai
oleh gas-gas yang digunakan. Untuk gas batubara-udara suhunya kira-kira sebesar
1800ºC, gas alam-udara 1700ºC, gas udara 2200ºC dan gas
asetilen-dinitrogen oksida sebesar 3000ºC. Sumber nyala yang paling banyak digunakan
adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi
15
Teknik atomisasi tanpa nyala dapat dilakukan dengan meletakkan
sejumlah sampel di dalam tungku dari grafit kemudian dipanaskan dengan sistem
elektris dengan cara melewatkan arus listrik pada tabung grafit. Akibat pemanasan
ini, zat yang akan dianalisis akan berubah menjadi atom-atom netral dan
dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadi
proses penyerapan energi (Gandjar dan Rohman, 2009).
c. Monokromator
Pada spektrofotometri serapan atom, monokromator berfungsi untuk
memisahkan dan memilih panjang gelombang yang digunakan untuk analisis. Di
dalam monokromator, terdapat suatu alat yang digunakan untuk memisahkan
panjang gelombang yang disebut dengan chopper (Gandjar dan Rohman, 2009). d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman. Biasanya, detektor yang digunakan adalah tabung
penggandaan foton (photomultiplier tube) (Gandjar dan Rohman, 2009).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai sistem pencatatan hasil. Pencatatan hasil dilakukan dengan suatu alat yang telah
terkalibrasi untuk pembacaan suatu transmisi atau absorbsi. Hasil pembacaan
dapat berupa angka atau kurva dari suatu alat perekam yang menggambarkan
absorbansi atau intensitas emisi (Gandjar dan Rohman, 2009).
2.3.3 Gangguan-gangguan pada Spektrofotometri Serapan Atom
16
dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan
konsentrasinya dalam sampel (Gandjar dan Rohman, 2009).
Menurut Gandjar dan Rohman(2009), gangguan-gangguan yang terjadi
pada spektrofotometri serapan atom adalah:
1. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi
banyaknya sampel yang mencapai nyala.
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom
yang terjadi di dalam nyala.
3. Gangguan oleh absorbansi yang disebabkan bukan absorbansi atom yang
dianalisis, yakni absorbansi oleh molekul-molekul yang terdisosiasi di dalam
nyala.
4. Gangguan oleh penyerapan non-atomik.
2.4 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Tindakan
ini dilakukan untuk menjamin bahwa metode analisis akurat, spesifik,
reprodusibel dan tahan akan kisaran analit yang akan dianalisis (Gandjar dan
Rohman, 2009; Harmita, 2004).
Menurut Harmita (2004) beberapa parameter analisis yang harus
dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
17 1. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Untuk mencapai kecermatan yang tinggi, dapat dilakukan dengan berbagai cara seperti
menggunakan peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut
yang baik, pengontrolan suhu dan pelaksanaannya yang cermat, taat asas sesuai
prosedur. Kecermatan ditentukan dengan dua cara yaitu:
i. Metode simulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke
dalam campuran bahan pembawa sediaan farmasi lalu campuran tersebut
dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan
(kadar yang sebenarnya) (Harmita, 2004).
ii. Metode penambahan baku (standard additionmethod)
Dalam metode penambahan baku, sampel dianalisis lalu sejumlah tertentu
analit yang diperiksa ditambahkan ke dalam sampel, dicampur dan dianalisis lagi.
Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang
diharapkan) (Harmita, 2004).
Dalam kedua metode tersebut, persen perolehan kembali dinyatakan
sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Metode
adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut.
Persen perolehan kembali ditentukan dengan menentukan berapa persen analit
18 2. Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara
hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika
prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari
campuran yang homogen. Presisi merupakan ukuran keterulangan metode analisis
dan biasanya dinyatakan sebagai simpangan baku relatif dari sejumlah sampel
yang berbeda signifikan secara statistik (Harmita, 2004).
3. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuan suatu
metode mengukur zat tertentu saja secara cermat dan seksama dengan adanya
komponen lain yang mungkin ada dalam matriks sampel. Selektivitas biasanya
dinyatakan sebagai derajat penyimpangan metode yang dilakukan terhadap
sampel yang mengandung bahan yang ditambahkan berupa cemaran, hasil urai,
senyawa sejenis, dan senyawa lain yang dibandingkan terhadap hasil analisis
sampel yang tidak mengandung bahan lain yang ditambahkan (Harmita, 2004).
4. Linearitas dan Rentang
Liniearitas merupakan kemampuan suatu metode untuk memperoleh hasil-hasil
uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran yang
diberikan. Linearitas suatu metode merupakan ukuran seberpa baik kurva kalibrasi
yang menghubungkan antara absorbansi (y) dengan konsentrasi (x). Liniearitas
dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang
berbeda-beda. Rentang metode adalah pernyataan batas terendah dan tertinggi
analit yang sudah ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan
19 5. Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah jumlah analit terkecil dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan dibandingkan dengan blanko.
Batas kuantitasi merupakan parameter pada analisis dan diartikan sebagai
kuantitas analit terkecil dalam sampel yang masih dapat memenuhi kriteria cermat
dan seksama (Harmita, 2004).
6. Ketangguhan Metode (Ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang diperoleh
dari analisis sampel yang sama dalam berbagai kondisi uji normal, seperti
laboratorium, analisis, instrumen, bahan pereaksi, suhu dan hari yang berbeda.
Ketangguhan metode dinyatakan sebagai tidak adanya pengaruh perbedaan
operasi atau lingkungan kerja terhadap hasil uji (Harmita, 2004).
7. Kekuatan (Robustness)
Kekuatan merupakan kemampuan metode untuk tetap tidak terpengaruh
oleh adanya variasi parameter metode yang kecil. Kekuatan suatu metode adalah
dengan membuat variasi parameter-parameter penting dalam suatu metode secara
sistematis lalu mengukur pengaruhnya pada pemisahan (Gandjar dan Rohman,
20 BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara Medan pada bulanFebruari 2015- Mei 2015. Metode
penelitian dilakukan secara deskriptif yakni suatu metode dimana peneliti
menggambarkan atau menganalisis suatu hasil yang ada dimasyarakat tanpa
memberikan kontrol atau perlakuan terhadap sampel.
3.2 Bahan – Bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah Umbi Lobak segar
yang diambil darikebun warga yang berada di jalan Udara Berastagi , Kabupaten
Kaban Jahe, Kota Medan, Sumatera Utara.
3.2.2 Pereaksi
Semua bahan yang digunakan dalam penelitian ini berkualitas pro analisa
keluaran E. Merck kecuali disebutkan lain yaitu akua demineralisata
(Laboratorium Penelitian Fakultas Farmasi USU), asam nitrat (HNO3) 65% b/v,
larutan baku kalium 1000 µg/mL, larutan baku kalsium 1000 µg/mL, dan larutan
21 3.3Alat – Alat
Spektrofotometer Serapan Atom Hitachi Z-2000 lengkap dengan lampu
katoda kalium, kalsium dan natrium, neraca analitik (AND GF-200), hot plate
(FISONS), oven (Dynamica), neraca analitik (BOECO), botol kaca, alumunium
foil alat tanur (Nabertherm), blender (cosmos), kertas saring Whatman No.42, krus porselen dan alat – alat gelas (Pyrex dan Oberol), Udara Asetilen.
3.4 Pembuatan Pereaksi Larutan HNO3 (1:1)
Sebanyak 500 mL larutan HNO3 65% b/v diencerkan dengan 500 mL akua
demineralisata (Isaac, 2000).
3.5 Prosedur Penelitian
3.5.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan carasampling purposif
yang dikenal juga sebagai sampling pertimbangan, dimana sampel ditentukan atas
dasar pertimbangan bahwa sampel yang diambil dapat mewakili populasi
(Budiarto, 2004).
3.5.2 Penyiapan Sampel
Sebanyak 1000 g umbi lobak segar (yang tidak ditentukan kadar airnya)
dibersihkan dari pengotoran, dicuci bersih dengan akua demineralisata, ditiriskan
dan dipotong. Selanjutnya dikeringkan di udara terbuka selama 15 menit,
kemudian dibagi menjadi dua bagian masing-masing ditimbang 500 g untuk yang
segar dan 500 g untuk yang direbus, proses perebusan dilakukan selama 10 menit
22
Kemudiandihaluskan dengan blender.Perlakuan yang sama juga dilakukan untuk
umbi lobak yang direbus (yang tidak ditentukan kadar airnya).
3.5.3 Proses Destruksi
Sampel yang telah dihaluskan ditimbang seksama sebanyak 25 g didalam
krus porselen, diarangkan di atas hot plate, lalu diabukan dalam tanur dengan temperatur awal 100 dan perlahan–lahan temperatur dinaikkan hingga suhu 500
dengan interval 25 setiap 5 menit. Pengabuan dilakukan selama 72 jam
(dihitung saat suhu sudah 500℃), lalu setelah suhu tanur ±27℃, krus porselen
dikeluarkan dan dibiarkan hingga dingin. Abu ditambahkan 5 mL HNO3 (1:1),
kemudian diuapkan pada hot plate sampai kering. Krus porselen dimasukkan kembali ke dalam tanur dengan temperatur awal 100 dan perlahan–lahan
temperatur dinaikkan hingga suhu 500 dengan interval 25 setiap 5 menit.
Pengabuan dilakukan selama 1 jam dan dibiarkan hingga dingin di dalam tanur
(suhu tanur ±27℃) (Isaac, 2000).
3.5.4 Pembuatan Larutan Sampel
Sampel hasil destruksi dilarutkan dalam 5 mL HNO3 (1:1), lalu
dipindahkan ke dalam labu tentukur 50 mL, dibilas krus porselen dengan 10 mL
akua demineralisata sebanyak tiga kali dan dicukupkan dengan akua
demineralisata hingga garis tanda. Kemudian disaring dengan menggunakan
kertas saring Whatman No. 42dimana5 mL filtrat pertama dibuang untuk
menjenuhkan kertas saring kemudian filtrat selanjutnya ditampung ke dalam botol
23 3.5.5 Pemeriksaan Kuantitatif
3.5.5.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (konsentrasi 1000 µg/mL) dipipet sebanyak 1 mL,
dimasukkan ke dalam labu tentukur 100 mL dan dicukupkan hingga garis tanda
dengan akua demineralisata (konsentrasi 10µg/mL).
Larutan yang digunakan untuk membuat kurva kalibrasi kalium dibuat
dengan cara memipet (2,5; 4,0; 5,5; 7,0 dan 8,5) mL larutanbaku kalium 10
µg/mL, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan
hingga garis tanda dengan menggunakan akua demineralisata (larutan ini
mengandung konsentrasi kalium (0,5; 0,8; 1,1; 1,4 dan 1,7) µg/ml dan kemudian
diukur absorbansi pada panjang gelombang 766,50 nm dengan nyala
udara-asetilen.
3.5.5.2 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (konsentrasi 1000 µg/ml) dipipet sebanyak 1 ml,
dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda
dengan akua demineralisata (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi kalsium dibuat dengan memipet (6,0; 7,0;
8,0; 9,0 dan 10,0) ml larutanbaku 10 µg/ml, masing-masing dimasukkan ke dalam
labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akua
demineralisata (larutan ini mengandung (1,2; 1,4; 1,6; 1,8 dan 2,0) µg/ml dan
diukur absorbansi pada panjang gelombang 422,7 nm dengan nyala
24 3.5.5.3 Pembuatan Kurva Kalibrasi Natrium
Larutan baku Natrium (konsentrasi 1000 µg/ml) dipipet sebanyak 1 ml,
dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda
dengan akua demineralisata (konsentrasi 10µg/ml).
Larutan untuk kurva kalibrasi Natrium dibuat dengan (2,5; 5,0; 10,0; 15,0
dan 20,0) ml larutanbaku 10 µg/ml, masing-masing dimasukkan ke dalam labu
tentukur 50 ml dan dicukupkan hingga garis tanda dengan akua demineralisata
(larutan ini mengandung (0,5, 1,0, 2,0 ,3,0 dan 4,0) µg/ml dan diukur absorbansi
pada panjang gelombang 589,0 nm dengan nyala udara-asetilen.
3.5.6 Penetapan Kadar Kalium, Kalsium dan Natrium dalam Sampel
Sebelum dilakukan penetapan kadar kalium, kalsium dan natrium dalam
sampel, terlebih dahulu alat spektrofotometer serapan atom dikondisikan dan
diatur metodenya sesuai dengan mineral yang akan diperiksa agar tidak terjadi
kesalahan pada saat pengukuran.
3.5.6.1 Penetapan Kadar Kalium Dalam Umbi Lobak Segar dan Umbi Lobak Rebus
Larutan sampel hasil destruksi dipipet sebanyak 0,1 ml dimasukkan ke
dalam labu tentukur 100 ml dan dicukupkan dengan akua demineralisata sampai
garis tanda, (Faktor pengenceran = 100/0,1= 1000 kali ). Lalu diukur
absorbansinya dengan menggunakan spektrofotometer serapan atom yang telah
dikondisikan dan diatur metodenya dimana penetapan kadar untuk kalium
dilakukan pada panjang gelombang 766,50 nm dengan nyala udara-asetilen. Nilai
25
baku kalium. Konsentrasi kalsium dalam sampel ditentukan berdasarkan
persamaan garis regresi dari kurva kalibrasi.
3.5.6.2 Penetapan Kadar Kalsium Dalam Umbi Lobak Segar dan Umbi Lobak Rebus
Larutan sampel hasil destruksi dipipet sebanyak 0,5 ml dimasukkan ke
dalam labu tentukur 50 ml dan dicukupkan dengan akua demineralisata sampai
garis tanda (Faktor pengenceran = 50 ml/0,5 ml = 100 kali). Lalu diukur
absorbansinya dengan menggunakan spektrofotometer serapan atom yang telah
dikondisikan dan diatur metodenya dimana penetapan kadar kalsium dilakukan
pada panjang gelombang 422,7 nm dengan nyala udara-asetilen. Nilai absorbansi
yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium.
Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis
regresi dari kurva kalibrasi.
3.5.6.3 Penetapan Kadar Natrium Dalam Umbi Lobak Segar dan Umbi Lobak Rebus
Larutan sampel hasil destruksi dipipet sebanyak 1 ml dimasukkan ke
dalam labu tentukur 50 ml dan dicukupkan dengan akua demineralisata hingga
garis tanda (Faktor pengenceran= 50 ml/1 ml= 50 kali). Lalu diukur
absorbansinya dengan menggunakan spektrofotometer serapan atom yang telah
dikondisikan, pada panjang gelombang 589,0 nm dengan nyala udara-asetilen.
Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi
larutan bakunatrium. Konsentrasi natrium dalam sampel ditentukan berdasarkan
persamaan garis regresi dari kurva kalibrasi.
Kadar mineral kalium, kalsium dan natrium dalam sampel dapat dihitung
26 n pengencera Faktor x (g) Sampel Berat (ml) Volume x (µg/ml) i Konsentras (µg/g) Logam Kadar =
Konsentrasi (µg/ml) didapatkan dari persamaan regresi kurva kalibrasi:
Y = aX + b
Y= Absorbansi
X= Konsentrasi
3.5.7 Analisis Data Secara Statistik
3.5.7.1 Penolakan Hasil Pengamatan
Menurut Sudjana (2005) kadar kalsium dan kalium yang diperoleh dari
hasil pengukuran masing-masing larutan sampel dianalisis dengan metode standar
deviasi menggunakan rumus sebagai berikut:
SD =
(
)
1 -n X -Xi 2
∑
Keterangan : Xi = Kadar sampel
−
X = Kadar rata-rata sampel n = jumlah perlakuan
Untuk mencari t hitung digunakan rumus:
t hitung =
n SD X Xi / −
dan untuk menentukan kadar mineral di dalam sampel dengan interval
kepercayaan 99%, α = 0.01, dk = n-1, dapat digunakan rumus:
27 Keterangan :
−
X = Kadar rata-rata sampel
SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1)
α = interval kepercayaan
n = jumlah perlakuan
3.5.7.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Menurut Sudjana ( 2005) sampel yang dibandingkan adalah independen
dan jumlah pengamatan masing-masing lebih kecil dari 30 dan variansi (σ) tidak
diketahui sehingga dilakukan uji F untuk mengetahui apakah variansi kedua
populasi sama (σ1 = σ2)atau berbeda (σ1 ≠ σ2) dengan menggunakan rumus di
bawah ini:
Fo = 2
2 2 1
S S
Keterangan : Fo = Beda nilai yang dihitung
S1 = Standar deviasi terbesar
S2 = Standar deviasi terkecil
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka
dilanjutkan uji dengan distribusi t dengan rumus:
(X1 – X2)
to =
Sp √1/n1 + 1/n2
Keterangan : X1 = kadar rata-rata sampel 1 n 1 = Jumlah perlakuan sampel 1
X2 = kadar rata-rata sampel 2 n 2 = Jumlah perlakuan sampel 2
28
Jika Fo melewati nilai kritis F, dilanjutkan uji dengan distribusi t dengan rumus :
(X1 – X2)
to =
√S12/n1 + S22/n2
Keterangan : X1 = kadar rata-rata sampel 1 S1 = Standar deviasi sampel 1
X2 = kadar rata-rata sampel 2 S2 = Standar deviasi sampel 2
n 1 = Jumlah perlakuan sampel 1 n 2 = Jumlah perlakuan sampel 2
Ketiga sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai
kritis t, dan sebaliknya.
3.5.8 Uji Akurasi(Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode
penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan
penentuan kadar mineral dalam sampel setelah penambahan larutan standar
dengan konsentrasi tertentu (Ermerdan McB. Miller, 2005). Umbi lobak yang
telah dihaluskan ditimbang secara seksama sebanyak 25 gram di dalam krus
porselen, lalu ditambahkan 6 ml larutan baku kalium (konsentrasi 1000 µg/ml);
1,5 ml larutan baku kalsium (konsentrasi 1000 µg/ml) dan 2 ml larutan baku
natrium (konsentrasi 1000 µg/ml), kemudian dilanjutkan dengan prosedur
destruksi kering seperti yang telah dilakukan sebelumnya. Hasil dekstruksi
dilakukan pengerjaan sama dengan pembuatan larutan sampel pada penetapan
29
Menurut Harmita (2004) persen perolehan kembali dapat dihitung dengan
rumus di bawah ini:
100% d baku larutan Kadar awal sampel dalam logam rata) -Kadar(rata sampel dalam logam total Kadar × − alamsampel
3.5.9 Uji Presisi (Simpangan Baku Relatif)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang
memenuhi persyaratan menunjukkan adanya keseksamaan metode yang
dilakukan.
Menurut Harmita (2004) rumus untuk menghitung simpangan baku relatif
adalah sebagai berikut:
RSD = ×100%
X SD
Keterangan :
−
X = Kadar rata-rata sampel
SD = Standar Deviasi
RSD = Relative Standard Deviati
3.5.10 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan.Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
30
Menurut Harmita (2004) batas deteksi dan batas kuantitasi ini dapat
dihitung dengan rumus sebagai berikut
Simpangan Baku (
X
SY ) =
(
)
2
2
− −
∑
nYi Y
Batas deteksi (LOD) =
slope X SY x
3
Batas kuantitasi (LOQ) =
slope X SY x
31 BAB IV
HASIL DAN PEMBAHASAN
4.1 Kurva Kalibrasi Kalium, Kalsium dan Natrium
Kurva kalibrasi kalium, kalsium dan natrium diperoleh dengan cara
mengukur absorbansi dari larutan baku kalium, kalsium dan natrium pada panjang
gelombang masing-masing yaitu 766,5 nm, 422,7 nm dan 589,0 nm. Berdasarkan
hasil pengukuran kurva kalibrasi untuk logam kalium diukur dengan rentang
konsentrasi 0,5 µg/ml sampai 1,7 µg/ml diperoleh persamaan garis regresi yaitu:
Y = 0,0274 X + 0,0004, untuk logam kalsium diukur dengan rentang konsentrasi
1,2 µg/ml sampai 2,0 µg/ml diperoleh persamaan regresi Y = 0,0258 X + 0,0012
dan untuk logam natrium diukur dengan rentang konsentrasi 0,5 µg/ml sampai 4,0
µg/ml diperoleh persamaan regresi Y = 0,1676 X + 0,0131.
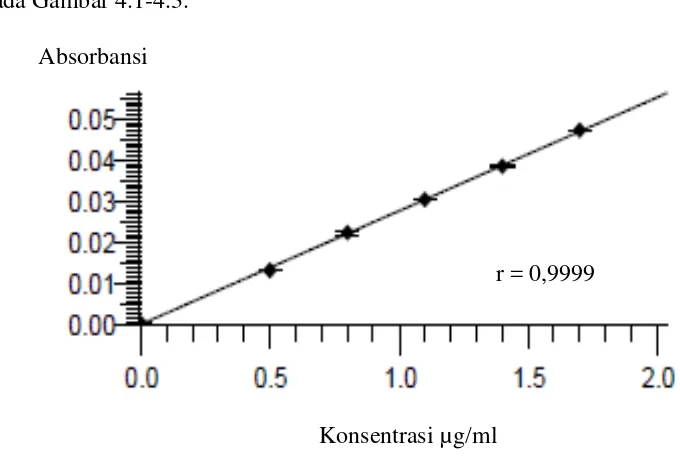
Kurva kalibrasi larutan baku kalium, kalsium dan natrium dapat dilihat
[image:48.595.123.463.478.710.2]pada Gambar 4.1-4.3.
Gambar 4.1. Kurva Kalibrasi Larutan Baku Kalium r = 0,9999
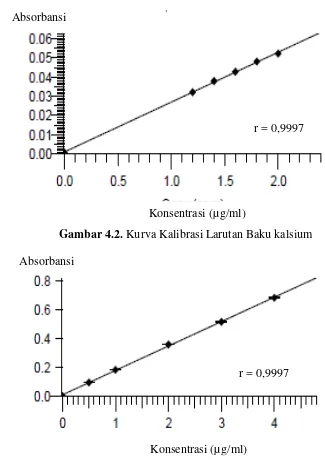
32 µg/ml
[image:49.595.126.451.51.516.2]Gambar 4.2. Kurva Kalibrasi Larutan Baku kalsium
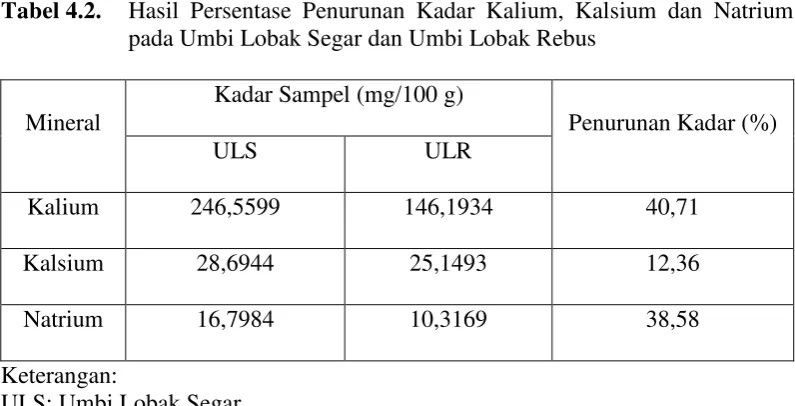
Gambar 3.2. Kurva Kalibrasi Larutan Baku Natrium
K
Gambar 4.3. Kurva Kalibrasi Larutan Baku Natrium
Keterangan:
X = Konsentrasi (µg/ml)
Y = Absorbansi
Berdasarkan kurva di atas diperoleh hubungan yang linear antara
konsentrasi dengan absorbansi, dengan koefisien korelasi (r) kalium sebesar
0,9999; kalsium sebesar 0,9997 dan natrium sebesar 0,9997. Nilai r ≥ 0,97
menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X r = 0,9997
r = 0,9997 Konsentrasi (µg/ml)
Konsentrasi (µg/ml) Absorbansi
[image:49.595.139.446.277.513.2]33
(konsentrasi) dan Y (absorbansi) (Ermer dan McB. Miller, 2005). Data hasil
pengukuran absorbansi larutan baku kalium, kalsium dan natrium, serta
perhitungan persamaan garis regresi dapat dilihat pada Lampiran 6, Lampiran 7
dan Lampiran 8, halaman 47-52.
4.2 Analisis Kadar Kalium, Kalsium dan Natrium dalam Umbi Lobak Segar dan Umbi Lobak Rebus
Penentuan kadarkalium, kalsium dan natrium pada umbi lobak dilakukan
dengan metode spektrofotometri serapan atom. Data dan contoh perhitungan hasil
analisis kuantitatif mineral kalium, kalsium dan natrium dapat dilihat pada
Lampiran 9, Lampiran 10 dan Lampiran 11, halaman 53-55. Analisis dilanjutkan
dengan perhitungan statistik (perhitungan dapat dilihat pada Lampiran 12 dan
Lampiran 13,halaman 57 dan 64. Hasil analisis kuantitatif mineral kalium,
kalsium dan natrium pada umbi lobak dapat dilihat pada Tabel 4.1.
Tabel 4.1. Hasil Analisis Kadar Kalium, Kalsium dan Natrium dalam Umbi lobak Segar dan umbi lobak rebus
No. Sampel Kadar Kalium
(mg/100 g)
Kadar Kalsium (mg/100 g)
Kadar Natrium (mg/100 g)
1. ULS 246,5599 ± 31,8540 28,9644 ± 0,2965 16,7984 ± 0,6970
2. ULR 146,1934 ± 14,8109 25,1493 ± 0,9462 10,3169 ± 1,1941
Keterangan:
ULS: Umbi Lobak Segar ULR: Umbi Lobak Rebus
Hasil penelitian menunjukkan bahwa kadar kalium dan natrium lebih besar
dibandingkan dengan yang disebutkan oleh Rukmana (2005) yakni 10,0 mg/100g
untuk natrium dan 218,0 mg/100g untuk kalium. Sedangkan untuk kalsium
34
Perbedaan kadar pada tiap mineral ini dipengaruhi berbagai faktor
diantaranya keadaan tanah, letak geografis, tempat tumbuh dan keadaan musim.
Selain itu Fitriani, dkk (2012) menyatakan bahwa kesuburan tanah adalah mutu tanah
untuk bercocok tanam, ditentukan oleh interaksi sejumlah sifat fisika, kimia dan biologi
bagian tubuh tanah yang menjadi habitat akar-akar aktif tanaman. Kesuburan dapat dilihat
dari kemampuan tanah menghasilkan buah tanaman yang dipanen, kandungan mineral
pada buah tersebut dan dari sejumlah unsur hara essensial, yang paling banyak diserap
oleh tanaman diantaranya adalah unsur hara kalium (K), kalsium (Ca) dan natrium (Na).
Oleh karena itu terdapat perbedaan kadar mineral pada tiap lokasi pengambilan sampel
yang berbeda.
Data yang didapat kemudian dihitung besar persentase penurunan kadar
dari masing-masing mineral pada umbi lobak segar dan umbi lobak rebus yang
dapat dilihat pada tabel 4.2 (perhitungan dapat dilihat pada Lampiran 14pada
[image:51.595.113.511.457.660.2]halaman 70).
Tabel 4.2. Hasil Persentase Penurunan Kadar Kalium, Kalsium dan Natrium pada Umbi Lobak Segar dan Umbi Lobak Rebus
Mineral
Kadar Sampel (mg/100 g)
Penurunan Kadar (%)
ULS ULR
Kalium 246,5599 146,1934 40,71
Kalsium 28,6944 25,1493 12,36
Natrium 16,7984 10,3169 38,58
Keterangan:
35
Hasil uji beda nilai rata-rata mineral kalium, kalsiun dan natrium dapat
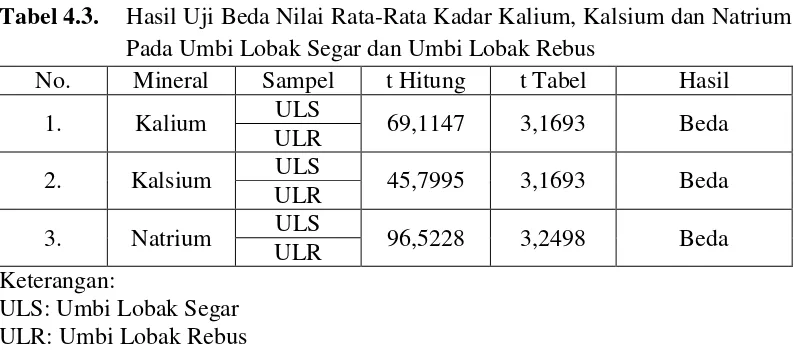
[image:52.595.114.511.139.314.2]dilihat pada tabel 4.3.
Tabel 4.3. Hasil Uji Beda Nilai Rata-Rata Kadar Kalium, Kalsium dan Natrium Pada Umbi Lobak Segar dan Umbi Lobak Rebus
No. Mineral Sampel t Hitung t Tabel Hasil
1. Kalium ULS 69,1147 3,1693 Beda
ULR
2. Kalsium ULS 45,7995 3,1693 Beda
ULR
3. Natrium ULS 96,5228 3,2498 Beda
ULR Keterangan:
ULS: Umbi Lobak Segar ULR: Umbi Lobak Rebus
Berdasarkan Tabel 4.2 di atas dapat diketahui bahwa terdapat penurunan
kadar kalium, kalsium dan Natrium pada umbi lobak segar dan umbi lobak rebus
yang diperoleh dari hasil analisis.
Berdasarkan Tabel 4.3 di atas. Dapat diketahui bahwa terdapat perbedaan
kadar kalsium, kalium, dan natrium pada umbi lobak segar dan direbus. Perreta
dan Breg (2003), menyatakan bahwa proses memasak dengan mudah dapat
merusak vitamin dan menurunkan kadar mineral. Tingkat kerusakan vitamin dan
penurunan kadar mineral dapat bergantung pada lamanya proses memasak dan
tingginya temperatur.
Selain itu dapat diketahui bahwa, kadar kalium dan natrium di dalam umbi
lobak segar jauh lebih besar dibandingkan dengan kadar kalium pada umbi lobak
rebus. Hal ini dapat terjadi karena kalium dan natrium pada umbi lobak rebus
banyak terlarut pada pada proses perebusan karena sebagian besar mineral
tersebut pada umbi lobak terikat dalam bentuk kompleks yang larut dalam air,
bersifat dinamis sehingga mudah tercuci dengan air dan penurunan pH (Novizan,
36
Kadar kalsium dalam umbi lobak segar mengalami penurunan yang tidak
terlalu jauh dengan umbi lobak rebus dikarenakan sifat kalsium didalam tanaman
berupa oksalat, karbonat dan fosfat yang sukar larut, bersifat mengendap dalam
air, namun kadar tetap berkurang karena terjadinya pelepasan kalsium selama
proses pemanasan (Sumarsih dan Widodo, 2007).
4.3 Uji Akurasi (Recovery)
Hasil uji perolehan kembali (recovery) kadar kalium, kalsium dan natrium setelah penambahan masing-masing larutan baku kalium, kalsium dan natrium
dalam sampel dapat dilihat pada Lampiran 16,halaman 77. Perhitungan persen
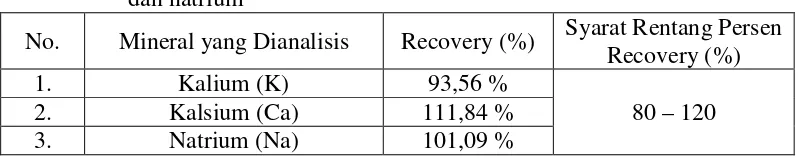
[image:53.595.113.512.465.544.2]recovery kalium, kalsium dan natrium dalam sampel dapat dilihat pada Lampiran 17,halaman 80-97.Persen recovery kalium, kalsium dan natrium dalam sampel dapat dilihat pada Tabel 4.4.
Tabel 4.4. Persen Uji Perolehan Kembali ( %recovery) Kadar Kalium, Kalsium dan natrium
No. Mineral yang Dianalisis Recovery (%) Syarat Rentang Persen
Recovery (%)
1. Kalium (K) 93,56 %
80 – 120
2. Kalsium (Ca) 111,84 %
3. Natrium (Na) 101,09 %
Berdasarkan tabel di atas, dapat dilihat bahwa rata-rata hasil uji perolehan
kembali (recovery) untuk kandungan kalium adalah 93,56%; untuk kandungan kalsium adalah 111,84% dan untuk kandungan natrium adalah 101,09%. Persen
recovery tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar kalium, kalsium dan natrium dalam sampel. Hasil uji
37
jika rata-rata hasil perolehan kembali (recovery) berada pada rentang 80%–120% (Harmita, 2004).
4.4 Uji Presisi (Simpangan Baku Relatif)
Dari perhitungan yang dilakukan terhadap data hasil pengukuran kadar
mineral kalium, kalsium dan natrium pada umbi lobak, diperoleh nilai simpangan
baku (SD) sebesar 4,5091% untuk mineral kalium; 2,0997% untuk mineral
kalsium; 0,7168% untuk mineral natrium dan nilai simpangan baku relatif (RSD)
sebesar 4,82% untuk mineral kalium; 1,87 %untuk mineral kalsium; 0,70%untuk
mineral natrium. Menurut Harmita (2004), nilai simpangan baku relatif (RSD)
untuk analit dengan kadar part per million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per billion (ppb) RSDnya adalah tidak lebih dari 32%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan
memiliki presisi yang baik pada Lampiran 18, halaman 98.
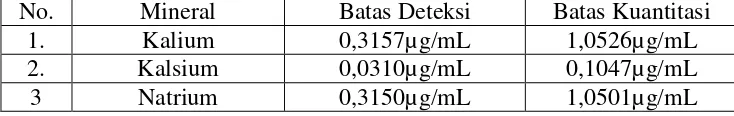
4.5 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalium, kalsium dan natriumi diperoleh
batas deteksi dan batas kuantitasi untuk ketiga mineral tersebut.Dari hasil
perhitungan diperoleh untuk pengukuran batas deteksi kalium, kalsium dan
[image:54.595.127.494.666.724.2]natrium.
Tabel 4.5 Batas Deteksi Dan B