PENETAPAN KADAR MINERAL KALSIUM, KALIUM DAN
NATRIUM PADA DAUN KARI (Murraya koenigii (L.) Spreng)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
MIFTAHURRAHMAH
NIM 121524088
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR MINERAL KALSIUM, KALIUM DAN
NATRIUM PADA DAUN KARI (Murraya koenigii (L.) Spreng)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan Sebagai Salah Satu Syarat Untuk Meraih Gelar Sarjana Farmasi Pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
MIFTAHURRAHMAH
NIM 121524088
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR MINERAL KALSIUM, KALIUM DAN
NATRIUM PADA DAUN KARI (Murraya koenigii (L.) Spreng)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
MIFTAHURRAHMAH
NIM 121524088
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 30 Mei 2015
Disetujui Oleh: Pembimbing I,
Prof. Dr. UripHarahap, Apt Prof. SumadioHadisahputra, Apt. NIP 195301011983031004 NIP 1 11281983031002
Medan, Juni 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
Prof. Dr. Julia Reveny, M.Si., Apt. NIP 195807101986012001
Pembimbing I,
Dr. Masfria, M.S., Apt. NIP 195707231986012001
Panitia Penguji,
Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt. NIP 195306191983031001
Pembimbing II,
Sri Yuliasmi, S.Farm., M.Si., Apt. NIP 198207032008122002
Dra. Siti Nurbaya, M.Si., Apt. NIP 195008261974122001
Dra. Masria Lasma Tambunan, M.Si., Apt. NIP 195005081977022001
iv
KATA PENGANTAR
Bismillahirrahmanirrahim,
Puji syukur penulis ucapkan kehadirat Allah SWT atas segala limpahan
rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah Muhammad
SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul
Penetapan Kadar Mineral Kalsium, Kalium dan Natrium pada Daun Kari (Murraya
koenigii (L.) Spreng) secara Spektrofotometri Serapan Atom.
Pada kesempatan kali ini dengan segala kerendahan hati penulis
mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Prof. Dr. Julia Reveny,
M.Si., Apt. selaku Wakil Dekan I Fakultas Farmasi USU Medan, yang telah
memberikan pengarahan dan bimbingan dalam menyelesaikan skripsi ini. Ibu Dr.
Masfria, M.S., Apt., dan Ibu Sri Yuliasmi, S.Farm., M.Si., Apt. yang telah
membimbing dan memberikan petunjuk serta saran-saran selama penelitian hingga
selesainya skripsi ini. Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., Ibu
Dra. Siti Nurbaya, M.Si., Apt., dan Ibu Dra. Masria Lasma Tambunan, M.Si., Apt.,
selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis
dalam menyelesaikan skripsi ini. Bapak Prof. Dr. rer. nat. Effendy De Lux Putra,
S.U., Apt., selaku Kepala Laboratorium Penelitian USU yang telah memberikan izin
dan fasilitas untuk penulis sehingga dapat mengerjakan serta menyelesaikan
v
Puridawati yang telah memberikan cinta dan kasih sayang yang tidak ternilai dengan
apapun, motivasi beserta doa yang tulus dan tak pernah henti. Adik-adik tercinta,
Putri Nahrisah, S.Pd., Muhammad Bustanul Arifin, Abyzar dan seluruh keluarga
besar yang selalu setia memberikan do’a dan dukungan penuh kepada penulis.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh
dari kesempurnaan. Oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis
berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Juni 2015 Penulis
vi
PENETAPAN KADAR MINERAL KALSIUM, KALIUM DAN NATRIUM
PADA DAUN KARI (Murraya koenigii (L.) Spreng) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Mineral merupakan kebutuhan tubuh manusia yang mempunyai peranan penting dalam pemeliharaan fungsi tubuh. Mineral banyak ditemukan dalam berbagai jenis buah dan sayuran. Daun kari merupakan salah satu tanaman yang dapat memberi asupan mineral dari luar tubuh dalam jumlah tertentu. Kandungan mineral daun kari adalah natrium 79,8 mg/100 g, kalium 811 mg/100 g, kalsium 166 mg/100 g, fosfor 600 mg/100 g dan besi 3,1 mg/100 g. Secara umum masyarakat khususnya daerah Sumatera seperti Aceh dan Medan mengkonsumsi daun kari sebagai bumbu dalam masakan. Daun kari merupakan sayuran yang dapat dimakan mentah, rebus atau dibuat kari. Penelitian ini bertujuan untuk mengetahui perbedaan kadar mineral kalsium, kalium dan natrium serta persentase penurunan kadar mineral-mineral tersebut pada daun kari setelah proses perebusan.
Analisis kuantitatif dilakukan dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm untuk kalsium, 766,5 nm untuk kalium dan 589,0 nm untuk natrium. Sampel daun kari diambil secara sampling purposif pada pekarangan rumah di kawasan jalan pembangunan dr. Mansyur USU Medan. Sampel tersebut terdiri dari daun kari segar dan daun kari rebus. Perlakuan sampel dilakukan dengan proses destruksi kering.
Hasil penelitian menunjukkan dalam keadaan segar kadar kalsium (193,5287 ± 0,9231) mg/100 g, kalium (1139,6203 ± 4,3952) mg/100 g dan natrium (43,0720 ± 0,3970) mg/100 g, sedangkan dalam keadaan rebus kadar kalsium (182,4140 ± 0,3628) mg/100 g, kalium (1042,4144 ± 3,3526) mg/100 g dan natrium (37,8909 ± 1,4803) mg/100 g. Persentase penurunan kadar mineral kalsium sebesar 5,7432 %, kalium sebesar 8,5297 % dan natrium sebesar 12,0289 %.
Secara statistik uji beda rata-rata kadar mineral kalsium, kalium dan natrium antara daun kari segar dan daun kari rebus dengan menggunakan distribusi F menyimpulkan bahwa kadar mineral kalsium, kalium dan natrium pada daun kari segar lebih tinggi secara signifikan dari daun kari rebus.
vii
ANALYSIS MINERAL CONTENT OF CALCIUM, POTASSIUM, AND
SODIUM IN CURRY LEAVE (Murraya koenigii (L.) Spreng)
BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Mineral is a necessity of the human body with an important role in the maintenance of body functions. Minerals are found in a wide variety of fruits and vegetables. Curry leaves is one of the plants that can give mineral intake from outside the body in a certain amount. The main mineral content of curry leaves is potassium 79.8 mg/100 g, sodium 811 mg/100 g, calcium 166 mg/100 g, phosphorus 600 mg/100 g and iron 3.1 mg/100 g. In general, the particular regions such as Aceh and Medan Sumatra consuming curry leaves as a spice in cooking. Curry leaves are vegetables that can be eaten raw, boiled or made curry. This study aims to determine the differences in the levels of the minerals calcium, potassium and sodium as well as the percentage decrease in the levels of these minerals in curry leaves after boiling process.
Quantitative analysis was performed using atomic absorption spectrophotometer at a wavelength of 422.7 nm for calcium, 766.5 nm to 589.0 nm for potassium and sodium. Samples taken purposively curry leaves in the yard in the area of pembangunan street dr. Mansyur USU Medan. The sample consisted of fresh curry leaves and curry leaves boiled. The treatments were conducted with dry destruction process.
The results showed in the fresh state levels of calcium (193.5287 ± 0.9231) mg/100 g, potassium (1139.6203 ± 4.3952) mg/100 g and sodium (43.0720 ± 0.3970) mg/100 g, while in a state boiled calcium levels (182.4140 ± 0.3628) mg/100 g, potassium (1042.4144 ± 3.3526) mg/100 g and sodium (37.8909 ± 1.4803) mg/100 g. The percentage decrease in calcium mineral content of 5.7432%, 8.5297% of potassium and sodium of 12.0289%.
Statistically different test average mineral content of calcium, potassium and sodium of fresh curry leaves and curry leaves boiled with using the F distribution concluded that the mineral content of calcium, potassium and sodium in fresh curry leaves significantly higher than curry leaves boiled.
viii
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 3
1.3Hipotesis ... 4
1.4Tujuan Penelitian ... 4
1.5Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1Daun Kari (Murraya koenigii (L.) Spreng) ... 5
2.1.1Sistematika Tanaman Kari ... 5
2.1.2Kandungan Gizi dan Manfaat Daun Kari ... 6
2.2Mineral ... 7
2.2.1Kalsium ... 7
ix
2.2.3Natrium ... 9
2.3Spektrofotometri Serapan Atom ... 9
2.3.1 Prinsip Dasar Spektrofotometri Serapan Atom ... 9
2.3.2 Instrumentasi Spektrofotometer Serapan Atom ... 10
2.3.3 Gangguan-gangguan pada Spektrofotometri Serapan Atom ... 12
2.4Validasi Metoda Analisis ... 13
BAB III METODE PENELITIAN ... 16
3.1Tempat dan Waktu Penelitian ... 16
3.2Bahan-bahan ... 16
3.2.1Sampel ... 16
3.2.2Pereaksi ... 16
3.3Alat-Alat ... 16
3.4Pembuatan Pereaksi ... 17
3.4.1Larutan HNO3 (1:1) ... 17
3.4.2Larutan Asam Pikrat 1% b/v ... 17
3.4.3Larutan H2SO4 1 N ... 17
3.5Prosedur Penelitian ... 17
3.5.1Pengambilan Sampel ... 17
3.5.2Penyiapan Sampel ... 17
3.5.3Proses Destruksi Kering ... 18
3.5.4Pembuatan Larutan Sampel ... 18
3.5.5Analisis Secara Kualitatif ... 19
x
3.5.5.2Kalium ... 19
3.5.5.3Natrium ... 20
3.5.6Analisis Secara Kuantitatif ... 20
3.5.6.1Pembuatan Kurva Kalibrasi Kalsium ... 20
3.5.6.2Pembuatan Kurva Kalibrasi Kalium ... 21
3.5.6.3Pembuatan Kurva Kalibrasi Natrium ... 21
3.5.6.4Penetapan Kadar Kalsium ... 22
3.5.6.5Penetapan Kadar Kalium ... 22
3.5.6.6Penetapan Kadar Natrium ... 23
3.5.6.7Perhitungan Kadar Kalsium, Kalium dan Natrium dalam Sampel ... 23
3.5.7Analisis Data Secara Statistik ... 23
3.5.8Validasi Metoda Analisis ... 24
3.5.8.1Uji Kecermatan (Accuracy) ... 24
3.5.8.2Uji Keseksamaan (Presisi) ... 26
3.5.8.3Penentuan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) ... 26
3.5.8.4Pengujian Beda Nilai Rata-Rata Antar Sampel ... 27
BAB IV HASIL DAN PEMBAHASAN ... 29
4.1Identifikasi Tumbuhan ... 29
4.2Analisis Kualitatif ... 29
4.3Analisis Kuantitatif ... 30
xi
4.3.2 Penetapan Kadar Mineral Kalsium, Kalium dan
Natrium pada Sampel ... 32
4.3.3 Uji Kecermatan (Accuracy) ... ... 35
4.3.4 Uji Keseksamaan (Presisi) ... 36
4.3.5 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) 36 4.3.6 Pengujian Beda Nilai Rata-rata Kadar Kalsium, Kalium dan Natrium pada Sampel Daun Kari Segar dan Daun Kari Rebus ... 37
BAB V KESIMPULAN DAN SARAN ... 39
5.1 Kesimpulan ... 39
5.2 Saran ... 39
DAFTAR PUSTAKA ... 40
xii
DAFTAR TABEL
Halaman
Tabel 2.1 Kandungan Gizi pada Daun Kari ... 6
Tabel 4.1 Hasil Analisis Kualitatif pada Daun Kari ... 29
Tabel 4.2 Hasil Penetapan Kadar Mineral Kalsium, Kalium dan Natrium pada Daun Kari Segar (DKS) dan Daun Kari Rebus (DKR) ... 33
Tabel 4.3 Persen Perolehan Kembali (Recovery) Mineral Kalsium, Kalium dan Natrium pada Sampel ... 35
Tabel 4.4 Nilai Simpangan Baku dan Simpangan Baku Relatif Mineral Kalsium, Kalium dan Natrium ... 36
Tabel 4.5 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Mineral Kalsium, Kalium dan Natrium ... 37
xiii
DAFTAR GAMBAR
Halaman
Gambar 2.1 Sistem Peralatan Spektrofotometer Serapan Atom ... 10
Gambar 4.1 Kurva Kalibrasi Secara Spektrofotometri Serapan Atom . 31
Gambar 4.2 Diagram Kadar Mineral Kalsium, Kalium dan Natrium pada Sampel Daun Kari Segar (DKS) dan Daun Kari
xiv
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil Identifikasi Tumbuhan ... 42
Lampiran 2. Gambar Sampel Daun Kari ... 43
Lampiran 3. Gambar Alat Laboratorium Penelitian ... 44
Lampiran 4. Gambar Hasil Analisis Kualitatif ... 46
Lampiran 5. Bagan Alir Proses Destruksi Kering ... 47
Lampiran 6. Bagan Alir Pembuatan Larutan Sampel ... 49
Lampiran 7. Data Hasil Pengukuran Absorbansi Larutan Standar Kalsium, Kalium, dan Natrium ... 50
Lampiran 8. Perhitungan Persamaan Garis Regresi ... 51
Lampiran 9. Hasil Penetapan Kadar Mineral Kalsium, Kalium dan Natrium dalam Sampel ... 55
Lampiran 10. Contoh Perhitungan Kadar Mineral Kalsium, Kalium, dan Natrium Pada Sampel ... 57
Lampiran 11. Perhitungan Persentase Penurunan Kadar Mineral Kalsium, Kalium dan Natrium pada Sampel ... 61
Lampiran 12. Perhitungan Statistik Kadar Mineral Kalsium pada Sampel ... 62
Lampiran 13. Perhitungan Statistik Kadar Mineral Kalium pada Sampel ... 66
Lampiran 14. Perhitungan Statistik Kadar Mineral Natrium pada Sampel ... 70
Lampiran 15. Rekapitulasi Data Kadar Mineral Kalsium, Kalium dan Natrium pada Daun Kari (Murraya koenigii (L.) Spreng) Sebelum Uji-t . ... 74
xv
Lampiran 17. Pengujian Beda Nilai Rata-Rata Kadar Mineral Kalsium pada Daun Kari ... 78
Lampiran 18. Pengujian Beda Nilai Rata-Rata Kadar Mineral Kalium pada Daun Kari ... 80
Lampiran 19. Pengujian Beda Nilai Rata-Rata Kadar Mineral Natrium pada Daun Kari ... 82
Lampiran 20. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Kalsium, Kalium dan Natrium ... 84
Lampiran 21. Hasil Persen Perolehan Kembali (Recovery) Kadar Mineral Kalsium, Kalium dan Natrium Setelah Penambahan Larutan Baku ... 87
Lampiran 22. Perhitungan Persen Perolehan Kembali (Recovery) Kadar Mineral Kalsium, Kalium dan Natrium pada Sampel ... 88
Lampiran 23. Perhitungan Simpangan Baku Relatif (RSD) Kalsium, Kalium dan Natrium pada Sampel ... 91
vi
PENETAPAN KADAR MINERAL KALSIUM, KALIUM DAN NATRIUM
PADA DAUN KARI (Murraya koenigii (L.) Spreng) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Mineral merupakan kebutuhan tubuh manusia yang mempunyai peranan penting dalam pemeliharaan fungsi tubuh. Mineral banyak ditemukan dalam berbagai jenis buah dan sayuran. Daun kari merupakan salah satu tanaman yang dapat memberi asupan mineral dari luar tubuh dalam jumlah tertentu. Kandungan mineral daun kari adalah natrium 79,8 mg/100 g, kalium 811 mg/100 g, kalsium 166 mg/100 g, fosfor 600 mg/100 g dan besi 3,1 mg/100 g. Secara umum masyarakat khususnya daerah Sumatera seperti Aceh dan Medan mengkonsumsi daun kari sebagai bumbu dalam masakan. Daun kari merupakan sayuran yang dapat dimakan mentah, rebus atau dibuat kari. Penelitian ini bertujuan untuk mengetahui perbedaan kadar mineral kalsium, kalium dan natrium serta persentase penurunan kadar mineral-mineral tersebut pada daun kari setelah proses perebusan.
Analisis kuantitatif dilakukan dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm untuk kalsium, 766,5 nm untuk kalium dan 589,0 nm untuk natrium. Sampel daun kari diambil secara sampling purposif pada pekarangan rumah di kawasan jalan pembangunan dr. Mansyur USU Medan. Sampel tersebut terdiri dari daun kari segar dan daun kari rebus. Perlakuan sampel dilakukan dengan proses destruksi kering.
Hasil penelitian menunjukkan dalam keadaan segar kadar kalsium (193,5287 ± 0,9231) mg/100 g, kalium (1139,6203 ± 4,3952) mg/100 g dan natrium (43,0720 ± 0,3970) mg/100 g, sedangkan dalam keadaan rebus kadar kalsium (182,4140 ± 0,3628) mg/100 g, kalium (1042,4144 ± 3,3526) mg/100 g dan natrium (37,8909 ± 1,4803) mg/100 g. Persentase penurunan kadar mineral kalsium sebesar 5,7432 %, kalium sebesar 8,5297 % dan natrium sebesar 12,0289 %.
Secara statistik uji beda rata-rata kadar mineral kalsium, kalium dan natrium antara daun kari segar dan daun kari rebus dengan menggunakan distribusi F menyimpulkan bahwa kadar mineral kalsium, kalium dan natrium pada daun kari segar lebih tinggi secara signifikan dari daun kari rebus.
vii
ANALYSIS MINERAL CONTENT OF CALCIUM, POTASSIUM, AND
SODIUM IN CURRY LEAVE (Murraya koenigii (L.) Spreng)
BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Mineral is a necessity of the human body with an important role in the maintenance of body functions. Minerals are found in a wide variety of fruits and vegetables. Curry leaves is one of the plants that can give mineral intake from outside the body in a certain amount. The main mineral content of curry leaves is potassium 79.8 mg/100 g, sodium 811 mg/100 g, calcium 166 mg/100 g, phosphorus 600 mg/100 g and iron 3.1 mg/100 g. In general, the particular regions such as Aceh and Medan Sumatra consuming curry leaves as a spice in cooking. Curry leaves are vegetables that can be eaten raw, boiled or made curry. This study aims to determine the differences in the levels of the minerals calcium, potassium and sodium as well as the percentage decrease in the levels of these minerals in curry leaves after boiling process.
Quantitative analysis was performed using atomic absorption spectrophotometer at a wavelength of 422.7 nm for calcium, 766.5 nm to 589.0 nm for potassium and sodium. Samples taken purposively curry leaves in the yard in the area of pembangunan street dr. Mansyur USU Medan. The sample consisted of fresh curry leaves and curry leaves boiled. The treatments were conducted with dry destruction process.
The results showed in the fresh state levels of calcium (193.5287 ± 0.9231) mg/100 g, potassium (1139.6203 ± 4.3952) mg/100 g and sodium (43.0720 ± 0.3970) mg/100 g, while in a state boiled calcium levels (182.4140 ± 0.3628) mg/100 g, potassium (1042.4144 ± 3.3526) mg/100 g and sodium (37.8909 ± 1.4803) mg/100 g. The percentage decrease in calcium mineral content of 5.7432%, 8.5297% of potassium and sodium of 12.0289%.
Statistically different test average mineral content of calcium, potassium and sodium of fresh curry leaves and curry leaves boiled with using the F distribution concluded that the mineral content of calcium, potassium and sodium in fresh curry leaves significantly higher than curry leaves boiled.
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Mineral merupakan kebutuhan tubuh manusia yang mempunyai peranan
penting dalam pemeliharaan fungsi tubuh seperti pengaturan kerja enzim-enzim,
pemeliharaan keseimbangan asam-basa, membantu pembentukan ikatan yang
memerlukan mineral seperti pembentukan hemoglobin (Almatsier, 2004). Mineral
banyak ditemukan dalam berbagai jenis tanaman yang digunakan sebagai obat salah
satunya adalah daun kari.
Tanaman kari (Murraya koenigii (L.) Spreng) merupakan salah satu tanaman
yang tergolong famili Rutaceae yang diperkenalkan oleh seorang ahli botani asal
Swedia dan German, yaitu Johann Andreas Murray dan Gerhard Koenig (Seidemann,
2005). Tanaman kari umumnya lebih dikenal sebagai daun kari (curry-leaf tree) yang
merupakan tanaman yang banyak tumbuh di India, Nepal, Sri Lanka dan beberapa
negara Asia Selatan serta paling banyak ditemui hampir di seluruh wilayah India
(Singh, dkk., 2014).
Di Indonesia daun kari banyak terdapat pada beberapa daerah di Sumatera
seperti Aceh dan Medan. Daun ini biasanya digunakan sebagai bumbu dalam
masakan. Selain itu, daun kari mempunyai khasiat sebagai obat herbal untuk
menyembuhkan beberapa jenis penyakit diantaranya hipertensi (Vinuthan, dkk.,
2004), reumatik dan diabetes (Tembhurne dan Sakarkar, 2009). Daun kari memiliki
kandungan kimia diantaranya air (63,4%), protein (5,9%), lemak (0,9%), karbohidrat
2
natrium 79,8 mg/100 g (Subramanian, dkk., 2012), kalium 811 mg/100 g, kalsium
166 mg/100 g, fosfor 600 mg/100 g dan besi 3,1 mg/100 g (Sakhale, dkk., 2007).
Sumber mineral selain dihasilkan oleh tubuh, juga harus diperoleh dari luar
tubuh. Pada umumnya masyarakat dapat memperoleh asupan mineral kalsium dan
kalium dari buah-buahan seperti jeruk, semangka, pisang, tomat serta sayur-sayuran
atau tanaman obat yang berwarna hijau seperti daun singkong, daun kari, daun
pepaya, kangkung, bayam dan brokoli. Sumber asupan mineral natrium mudah
ditemukan dalam makanan sehari-hari seperti garam dapur dan makanan laut
(Rosmarkam dan Yuwono, 2002).
Kalsium, kalium dan natrium merupakan mineral yang mempengaruhi
tekanan darah (Barasi, 2007). Peningkatan asupan mineral kalsium menghasilkan
penurunan 1,4 mmHg pada tekanan darah sistolik dan 0,8 mmHg pada tekanan darah
diastolik. Peningkatan asupan mineral kalium dapat menurunkan tekanan darah
sistolik sekitar 4 mmHg dan tekanan darah diastolik sekitar 2,5 mmHg. Peningkatan
asupan mineral kalsium dan kalium serta penurunan asupan mineral natrium
memiliki efek yang sangat baik untuk menurunkan tekanan darah. Pada penderita
hipertensi, mineral natrium dapat menurunkan tekanan darah sistolik sekitar 5 mmHg
dan tekanan darah diastolik sekitar 3 mmHg (Almatsier, 2004).
Apabila kadar mineral kalium dalam darah berlebih akan mengalami
hiperkalemia, sedangkan kekurangan mineral kalium akan mengalami hipokalemia.
Keseimbangan jumlah mineral kalium dalam tubuh tergantung dari jumlah mineral
natrium dalam darah sehingga dapat mempengaruhi tekanan darah. Dalam hal ini
3
natrium merupakan mineral yang sangat berperan dalam pengaturan cairan tubuh,
termasuk tekanan darah dan keseimbangan asam-basa (Barasi, 2007).
Keseimbangan mineral-mineral tersebut dalam tubuh sangatlah penting. Oleh
karena itu peneliti melakukan penelitian untuk mengetahui kadar mineral kalsium,
kalium, dan natrium yang terdapat pada daun kari serta berperan untuk menambah
asupan mineral dalam tubuh. Sampel yang diuji dalam penelitian ini adalah daun kari
segar (DKS) dan daun kari rebus (DKR).
Berbagai metode dapat diterapkan dalam pemeriksaan kandungan kalsium,
kalium dan natrium. Kalsium dapat diperiksa dengan metode kompleksometri,
permanganometri, gravimetri dan spektrofotometri serapan atom. Kalium dan
natrium dapat diperiksa dengan metode gravimetri, titrimetri dan spektrofotometri
serapan atom (Khopkar, 1984). Pemeriksaaan kalsium, kalium dan natrium pada
penelitian ini dilakukan dengan menggunakan metode Spektrofotometri Serapan
Atom karena metode ini adalah salah satu metode yang mudah, analisisnya cepat,
dan ketelitiannya sampai tingkat kecil serta tidak memerlukan pemisahan
pendahuluan (Khopkar, 1984) sehingga dipilih untuk pemeriksaan kalsium, kalium,
dan natrium pada daun kari segar (DKS) dan daun kari rebus (DKR).
1.2Perumusan Masalah
Berdasarkan latar belakang diatas, maka permasalahan dalam penelitian ini
dapat dirumuskan sebagai berikut:
a. Apakah terdapat perbedaan kadar mineral kalsium, kalium dan natrium pada
4
b. Berapakah persentase penurunan kadar mineral kalsium, kalium dan natrium
pada daun kari setelah proses perebusan?
1.3 Hipotesis
Berdasarkan masalah yang dirumuskan diatas, maka hipotesis dalam
penelitian ini adalah sebagai berikut:
a. Terdapat perbedaan kadar mineral kalsium, kalium dan natrium pada daun
kari segar dan daun kari rebus.
b. Kadar mineral kalsium, kalium dan natrium pada daun kari mengalami
penurunan dengan proses perebusan dalam jumlah tertentu.
1.4 Tujuan Penelitian
Penelitian ini bertujuan untuk:
a. Mengetahui perbedaan kadar mineral kalsium, kalium dan natrium pada daun
kari segar dan daun kari rebus secara signifikan.
b. Mengetahui persentase penurunan kadar mineral kalsium, kalium dan natrium
pada daun kari segar dan daun kari rebus.
1.5 Manfaat Penelitian
Memberikan informasi kepada masyarakat bahwa adanya perbedaan kadar
mineral kalsium, kalium dan natrium antara daun kari segar dan daun kari rebus
sehingga masyarakat dapat memilih cara yang tepat untuk mengkonsumsi daun kari,
baik yang segar maupun yang direbus agar dapat menjaga keseimbangan cairan
5
BAB II
TINJAUAN PUSTAKA
2.1Daun Kari (Murraya koenigii (L.) Spreng)
Daun kari (Murraya koenigii (L.) Spreng) merupakan daun majemuk dan
bentuk daunnya menyirip. Bentuk daun kari hampir sama dengan daun salam, hanya
ukurannya lebih kecil dan baunya lebih tajam dibandingkan dengan daun salam.
Secara morfologi pohon kari bisa tumbuh mencapai 4-6 meter, memiliki tangkai
panjang dan setiap tangkai berjumlah ganjil yaitu terdiri dari 11-21 helai daun,
memiliki bunga yang kecil dan berwarna putih, serta memiliki buah yang berwarna
coklat kehitaman. Batang daun kari berwarna hijau gelap kecoklatan, daun yang
masih muda berwarna hijau muda dan daun yang sudah tua berwarna hijau tua
(Singh, dkk., 2014).
2.1.1Sistematika Tanaman Kari
Menurut Singh, dkk., (2014) dan Herbarium Bogoriense LIPI (2015),
taksonomi tanaman kari termasuk dalam tatanama tumbuhan sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub-divisi :
Kelas :
Angiospermae
Ordo : Sapindales
Famili : Rutaceae
Genus :
Binomial : Murraya
Murrayakoenigii (L.) Spreng
6
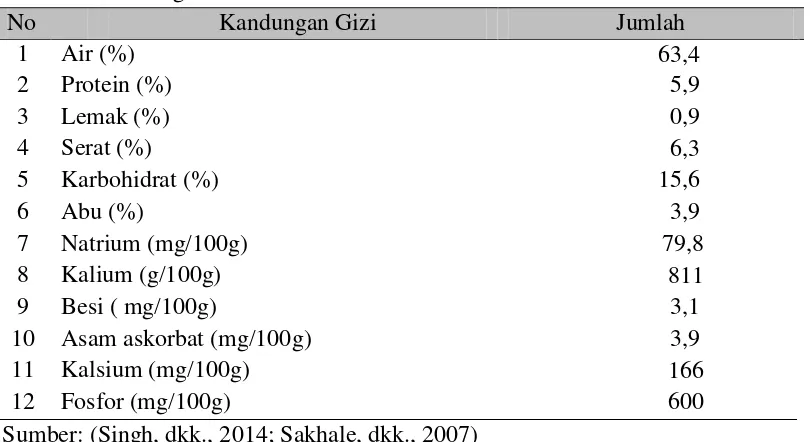
2.1.2Kandungan Gizi dan Manfaat Daun Kari
Daun kari memiliki banyak manfaat dan kandungan gizi yang baik. Adapun
kandungan gizi pada daun kari diantaranya:
Tabel 2.1 Kandungan Gizi Pada Daun Kari
No Kandungan Gizi Jumlah
1 Air (%) 63,4
2 Protein (%) 5,9
3 Lemak (%) 0,9
4 Serat (%) 6,3
5 Karbohidrat (%) 15,6
6 Abu (%) 3,9
7 Natrium (mg/100g) 79,8
8 Kalium (g/100g) 811
9 Besi ( mg/100g) 3,1
10 Asam askorbat (mg/100g) 3,9
11 Kalsium (mg/100g) 166
12 Fosfor (mg/100g) 600
Sumber: (Singh, dkk., 2014; Sakhale, dkk., 2007)
Daun kari merupakan sumber vitamin A, vitamin B, vitamin C, vitamin B2,
kalsium dan besi dalam jumlah banyak. Daun kari segar berwarna hijau jika dimakan
mentah dapat menyembuhkan disentri. Daun kari juga bermanfaat bagi wanita yang
menderita kekurangan kalsium seperti osteoporosis serta dapat mengatasi mual dan
muntah akibat gangguan pencernaan (Singh, dkk., 2014).
Daun kari sangat efektif untuk mengobati tekanan darah tinggi, diabetes,
kolesterol, luka bakar, erupsi kulit dan katarak. Selain daripada daunnya, akar
tanaman kari dapat digunakan untuk mengobati penyakit ginjal. Kegunaan daun kari
yang cukup penting adalah dapat melarutkan penumpukan kalsium dalam tubuh yang
menyebabkan jaringan sendi dan arteri menjadi keras dan tidak dapat diserap oleh
7
2.2Mineral
Mineral adalah unsur-unsur yang berada dalam bentuk sederhana. Dalam
ilmu gizi biasanya disebut nutrisi/zat gizi anorganik dan sangat dibutuhkan tubuh
terutama untuk proses metabolisme (Almatsier, 2004). Mineral dibagi ke dalam dua
kelompok yaitu mineral makro dan mineral mikro. Mineral makro merupakan
mineral yang dibutuhkan oleh tubuh dalam jumlah lebih dari 100 mg per hari
sedangkan mineral mikro merupakan mineral yang dibutuhkan tubuh dalam jumlah
kurang dari 100 mg per hari. Unsur-unsur yang termasuk ke dalam mineral makro
adalah kalsium, fosfor, magnesium, natrium, kalium dan klor, sedangkan yang
termasuk ke dalam mineral mikro adalah besi, seng, iodium, mangan, selenium dan
kromium (Devi, 2010).
Berdasarkan kegunaan dalam aktivitas kehidupan, mineral dibagi menjadi
dua kelompok yaitu mineral esensial dan mineral non esensial. Mineral esensial
adalah mineral yang diperlukan dalam proses fisiologi makhluk hidup untuk
menghindari penyakit defisiensi mineral. Mineral non esensial adalah mineral yang
belum diketahui dengan pasti kegunaannya, sehingga jika jumlahnya melebihi
jumlah normal didalam tubuh akan menyebabkan keracunan bahkan berbahaya bagi
makhluk hidup (Almatsier, 2004).
2.2.1Kalsium
Kalsium merupakan mineral yang paling banyak terdapat didalam tubuh,
yaitu 1,5–2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Dari
jumlah ini, sebanyak 99% berada di dalam jaringan keras, yaitu tulang dan gigi,
8
kalsium berperan penting dalam mengatur fungsi sel, seperti kontraksi otot dan
penggumpalan darah (Almatsier, 2004).
Kalsium dieksresikan lewat urin serta feses dan untuk mencegah kehilangan
ini diperlukan asupan kalsium melalui makanan. Asupan kalsium tambahan
diperlukan dalam keadaan tertentu seperti pada masa pertumbuhan mulai dari
anak-anak, hingga usia remaja dan pada saat hamil untuk memenuhi kebutuhan janin
(Almatsier, 2004).
Angka kecukupan rata-rata dalam sehari asupan kalsium bagi orang Indonesia
yang ditetapkan adalah 300 mg – 400 mg pada bayi, 500 mg pada anak-anak, 600 mg
– 700 mg pada remaja, 500 mg – 800 mg pada orang dewasa, serta lebih besar dari
400 mg pada ibu hamil dan menyusui. Kekurangan asupan mineral kalsium pada
masa pertumbuhan dapat menyebabkan gangguan pertumbuhan seperti tulang kurang
kuat, mudah bengkok dan rapuh (Almatsier, 2004).
2.2.2Kalium
Kalium terutama terdapat didalam sel dan sebanyak 95% kalium berada di
dalam cairan intraseluler. Kalium memegang peranan dalam pemeliharaan
keseimbangan cairan elektrolit dan asam basa (Almatsier, 2004; Winarno, 1992).
Selain itu kalium berfungsi dalam menghantar pesan ke syaraf otot, menurunkan
tekanan darah dan mengirim oksigen ke otak (Almatsier, 2004).
Kekurangan kalium dapat terjadi akibat banyaknya kehilangan kalium
melalui saluran cerna dan ginjal. Kekurangan kalium menyebabkan lemah, lesu,
kehilangan nafsu makan dan konstipasi. Kelebihan kalium akut dapat terjadi bila
konsumsi kalium tanpa diimbangi oleh kenaikan eksresi. Hiperkalemia akut dapat
9
Kalium terdapat didalam semua makanan yang berasal dari
tumbuh-tumbuhan dan hewan. Sumber utama adalah makanan mentah/segar, terutama buah,
sayuran dan kacang-kacangan. Kebutuhan minimum akan kalium ditaksir sebanyak
2000 mg sehari (Almatsier, 2004).
2.2.3Natrium
Natrium adalah kation utama dalam darah dan cairan ekstraseluler yang
mencakup 95% dari seluruh kation. Oleh karena itu, mineral ini sangat berperan
dalam pengaturan cairan tubuh, termasuk tekanan darah dan keseimbangan asam
basa (Barasi, 2007).
Natrium sebagian besar mengatur tekanan osmosis dan menjaga cairan agar
tidak keluar dari darah dan masuk ke dalam sel. Bila jumlah natrium didalam sel
meningkat secara berlebihan, air akan masuk ke dalam sel, akibatnya sel akan
membengkak. Keseimbangan cairan juga akan terganggu bila seseorang kehilangan
natrium. Air akan memasuki sel untuk mengencerkan natrium dalam sel. Cairan
ekstraseluler akan menurun. Perubahan ini dapat menurunkan tekanan darah
(Almatsier, 2004). Defisiensi natrium dapat mengakibatkan kurang sempurnanya
pencernaan karbohidrat, sedangkan kelebihan natrium dapat menyebabkan darah
tinggi serta hilangnya mineral kalium (Almatsier, 2004).
2.3Spektrofotometri Serapan Atom
2.3.1 Prinsip Dasar Spektrofotometri Serapan Atom
Spektrofotometri serapan atom digunakan untuk analisi kuantitatif
10
analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak
tergantung pada bentuk molekul dari logam dalam sampel tersebut.
Interaksi materi dengan berbagai energi seperti energi panas, energi radiasi,
energi kimia, dan energi listrik selalu memberikan sifat-sifat yang spesifik untuk
setiap unsur. Besarnya perubahan yang terjadi biasanya sebanding dengan jumlah
unsur atau persenyawaan yang terdapat didalamnya. Proses interaksi ini mendasari
analisis spektrofotometri atom yang dapat berupa emisi dan absorpsi (Gandjar dan
Rohman, 2007).
2.3.2 Instrumentasi Spektrofotometer Serapan Atom
Sistem peralatan spektrofotometer serapan atom dapat dilihat pada gambar
berikut ini:
Gambar 2.1 Sistem Peralatan Spektrofotometer Serapan Atom (Harris, 2007).
a. Sumber Sinar
Sumber sinar yang umum dipakai adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu
11
dilapisi unsur yang sama dengan unsur yang akan dianalisis. Tabung logam ini diisi
dengan gas mulia dengan tekanan rendah yang jika diberikan tegangan pada arus
tertentu, katoda akan memancarkan elektron-elektron yang bergerak menuju anoda
dengan kecepatan dan energi yang tinggi. Elektron dengan energi tinggi ini akan
bertabrakan dengan gas mulia sehingga gas mulia kehilangan elektron dan menjadi
ion bermuatan positif. Ion gas mulia bermuatan positif akan bergerak menuju katoda
dengan kecepatan dan energi yang tinggi sehingga menabrak unsur-unsur yang
terdapat pada katoda. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar
permukaan katoda dan mengalami eksitasi ke tingkat energi elektron yang lebih
tinggi (Gandjar dan Rohman, 2007).
b. Tempat Sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral. Ada berbagai macam alat yang
dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan
nyala (flame) dan tanpa nyala (flameless) (Gandjar dan Rohman, 2007).
Teknik atomisasi dengan nyala bergantung pada suhu yang dapat dicapai oleh
gas-gas yang digunakan. Untuk gas batubara-udara suhunya kira-kira sebesar
1800°C, gas alam-udara 1700°C, gas udara 2200°C, dan gas
asetilen-dinitrogen oksida sebesar 3000°C. Sumber nyala yang paling banyak digunakan
adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi
(Gandjar dan Rohman, 2007).
c. Monokromator
Pada spektrofotometer serapan atom, monokromator berfungsi untuk
12
dalam monokromator, terdapat suatu alat yang digunakan untuk memisahkan
panjang gelombang yang disebut dengan chopper (Gandjar dan Rohman, 2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat
pengatoman. Biasanya detektor yang digunakan adalah tabung penggandaan foton
(photomutliplier tube) (Gandjar dan Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
sistem pencatatan hasil. Pencatatan hasil dilakukan dengan suatu alat yang telah
terkalibrasi untuk pembacaan suatu transmisi atau absorbsi. Hasil pembacaan dapat
berupa angka atau kurva dari suatu alat perekam yang menggambarkan absorbansi
atau intensitas emisi (Gandjar dan Rohman, 2007).
2.3.3 Gangguan-gangguan Pada Spektrofotometri Serapan Atom
Gangguan-gangguan (interference) pada Spektrofotometri Serapan Atom
adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang
dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan
konsentrasinya dalam sampel (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), gangguan-gangguan yang terjadi pada
spektrofotometri serapan atom adalah:
1. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi
banyaknya sampel yang mencapai nyala.
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang
13
3. Gangguan oleh absorbansi yang disebabkan bukan absorbansi atom yang
dianalisis, yakni absorbansi oleh molekul-molekul yang terdisosiasi di dalam
nyala.
4. Gangguan oleh penyerapan non-atomik.
Cara mengatasi gangguan-gangguan tersebut adalah dengan bekerja pada
panjang gelombang yang lebih besar atau pada suhu yang lebih tinggi. Jika kedua
cara ini masih belum bisa membantu menghilangkan gangguan-gangguan tersebut,
maka satu-satunya cara adalah dengan mengukur besarnya penyerapan non-atomik
menggunakan sumber sinar yang memberikan spektrum kontinyu (Gandjar dan
Rohman, 2007).
2.4 Validasi Metoda Analisis
Validasi metoda analisis adalah suatu tindakan penilaian terhadap parameter
tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter
tersebut memenuhi persyaratan untuk penggunaannya. Tindakan ini dilakukan untuk
menjamin bahwa metode analisis akurat dan spesifik (Gandjar dan Rohman, 2007;
Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi
metode analisis adalah sebagai berikut:
1. Kecermatan (accuracy)
Kecermatan (akurasi) adalah ukuran yang menunjukkan derajat kedekatan
hasil analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Untuk mencapai
14
peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik,
pengontrolan suhu, dan pelaksanaannya yang cermat, taat asas sesuai prosedur.
Kecermatan ditentukan dengan dua cara yaitu:
− Metode Simulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke dalam
campuran bahan pembawa sediaan farmasi lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang
sebenarnya) (Harmita, 2004).
− Metode Penambahan Baku (standard addition method)
Dalam metode penambahan baku, sampel dianalisis lalu sejumlah tertentu analit
yang diperiksa ditambahkan ke dalam sampel, dicampur dan dianalisis lagi.
Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang
diharapkan) (Harmita, 2004).
Dalam kedua metode tersebut, persen perolehan kembali dinyatakan sebagai
rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Metode adisi dapat
dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada
sampel yang diperiksa, lalu dianalisis dengan metode tersebut. Persen perolehan
kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan tadi
dapat ditemukan (Harmita, 2004).
2. Keseksamaan (precision)
Keseksamaan (presisi) adalah ukuran yang menunjukkan derajat kesesuaian
antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata
jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari
15
dan biasanya dinyatakan sebagai simpangan baku relatif dari sejumlah sampel yang
berbeda signifikan secara statistik (Harmita, 2004).
3. Batas Deteksi dan Batas Kuantitasi
Batas deteksi (limit of detection, LOD) adalah jumlah analit terkecil dalam
sampel yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan
dengan blangko. Batas kuantitasi (limit of quantitation, LOQ) merupakan parameter
pada analisis dan diartikan sebagai kuantitas analit terkecil dalam sampel yang masih
16
BAB III
METODE PENELITIAN
3.1Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi USU pada
bulan September – Nopember 2014.
3.2 Bahan-bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah daun kari yang diambil
pada pekarangan rumah di kawasan jalan pembangunan dr. Mansyur USU Medan.
Sampel tersebut terdiri dari daun kari segar dan daun kari rebus.
3.2.2 Pereaksi
Semua bahan yang digunakan dalam penelitian ini berkualitas pro analisis
keluaran E. Merck kecuali disebutkan lain yaitu asam nitrat 65% v/v, H2SO4 96%
v/v, etanol 96% v/v, larutan standar (kalsium, kalium dan natrium) dan akua
demineralisata (Laboratorium Penelitian Fakultas Farmasi USU).
3.3Alat-alat
Spektrofotometer Serapan Atom (Hitachi Z-2000) dengan tipe nyala
udara-asetilen lengkap dengan lampu katoda Ca, K dan Na, neraca analitik (ANDGF 200),
tanur (Stuart), blender, hot plate, kertas saring Whatman no. 42, krus porselen,
17
3.4Pembuatan Pereaksi
3.4.1Larutan HNO3 (1:1)
Diencerkan sebanyak 50 mL larutan HNO3 65% dengan 50 mL air suling
(Ditjen BPOM, 1979).
3.4.2Larutan Asam Pikrat 1% b/v
Dilarutkan 1 g asam pikrat dengan air suling hingga 100 mL (Ditjen POM,
1979).
3.4.3Larutan H2SO4 1 N
Dipipet 3 mLH2SO4 96%dan dimasukkan perlahan-lahan melalui dindinglabu
tentukur 100 mL yang telah berisi air suling setengahnya. Dicukupkan volumenya
dengan air suling hingga garis tanda.
3.5Prosedur Penelitian
3.5.1Pengambilan Sampel
Pengambilan sampel dilakukan secara sampling purposif yaitu ditentukan
atas dasar pertimbangan bahwa sampel yang diambil mempunyai karakteristik yang
sama dengan sampel yang ada dan dianggap sebagai sampel representatif (Sudjana,
2002).
3.5.2Penyiapan Sampel
a. Daun Kari Segar
Sebanyak 1 kg daun kari segar dibersihkan dari pengotoran, dicuci bersih dengan
air mengalir, kemudian dicuci kembali dengan akua demineralisata dan ditiriskan
beberapa saat. Kemudian dikeringkan dengan cara diangin-anginkan, lalu
18 b. Daun Kari Rebus
Sebanyak 1 kg daun kari segar dibersihkan dari pengotoran, dicuci bersih dengan
air mengalir, kemudian dicuci kembali dengan akua demineralisata. Kemudian
direbus dalam panci yang berisi air mendidih sebanyak 2000 mL. Selama proses
perebusan, panci ditutup dan sesekali dilakukan pengadukan agar sampel terebus
secara merata. Selanjutnya sampel diangkat dan ditiriskan beberapa saat.
Kemudian dikeringkan dengan cara diangin-anginkan, lalu dipotong-potong
kira-kira ± 1 cm dan dihaluskan dengan blender.
3.5.3Proses Destruksi Kering
Sampel yang telah dihaluskan masing-masing ditimbang sebanyak 10 g,
dimasukkan ke dalam krus porselen, lalu diarangkan di atas hot plate selama 10 jam,
kemudian diabukan dengan tanur pada temperatur awal 100°C dan dinaikkan
perlahan-lahan hingga 500°C dengan interval 25°C setiap 5 menit. Pengabuan
dilakukan selama 45 jam dan dibiarkan hingga dingin dalam desikator. Abu
ditambahkan 5 mL larutan HNO3 (1:1), kemudian diuapkan pada hote plate sampai
kering. Krus porselen dimasukkan kembali ke tanur dengan temperatur awal 100°C
dan dinaikkan perlahan-lahan hingga suhu 500°C dengan interval 25°C setiap 5
menit. Pengabuan dilakukan selama 1 jam dan dibiarkan hingga dingin dalam
desikator (Isaac, 1990).
3.5.4Pembuatan Larutan Sampel
Dilarutkan sampel hasil destruksi dengan 5 mL HNO3 dan dimasukkan ke
dalam labu tentukur 50 mL, dibilas krus porselen hingga tiga kali, kemudian larutan
dicukupkan dengan akua demineralisata hingga garis tanda (Horwitz, 2000).
19
pertama untuk menjenuhkan kertas saring, kemudian ditampung filtrat selanjutnya
dalam botol. Filtrat ini digunakan sebagai larutan sampel untuk dianalisis secara
kualitatif dan kuantitatif.
3.5.5Analisis Secara Kualitatif
3.5.5.1Kalsium
a. Uji Nyala Ni/Cr
Dibersihkan kawat Ni/Cr dengan HCl pekat, lalu dipijar pada api
bunsen sampai tidak memberikan warna khusus pada nyala bunsen.
Kemudian dicelupkan kawat pada sampel daun kari segar dan daun kari
rebus, lalu dipijar pada api bunsen, diamati warna yang terjadi pada nyala
bunsen. Jika terdapat kalsium akan terbentuk warna merah bata pada nyala
bunsen (Vogel, 1990).
b. Uji Kristal Kalsium dengan Asam Sulfat 1 N
Diteteskan larutan sampel sebanyak 1-2 tetes pada object glass,
kemudian ditetesi dengan larutan asam sulfat dan etanol 96% akan terbentuk
endapan putih, lalu diamati di bawah mikroskop. Jika terdapat ion kalsium
akan terlihat kristal berbentuk jarum (Vogel, 1990).
3.5.5.2Kalium
a. Uji Nyala Ni/Cr
Dibersihkan kawat Ni/Cr dengan HCl pekat, lalu dipijar pada api
bunsen sampai tidak memberikan warna khusus pada nyala bunsen.
Kemudian dicelupkan kawat pada sampel daun kari segar dan daun kari
20
bunsen. Jika terdapat kalium akan terbentuk warna ungu pada nyala bunsen
(Vogel, 1990).
b. Uji Kristal Kalium dengan Asam Pikrat
Diteteskan larutan sampel sebanyak 1-2 tetes pada object glass,
kemudian ditetesi dengan larutan asam pikrat, dibiarkan ± 5 menit, lalu
diamati dibawah mikroskop. Jika terdapat ion kalium akan terlihat kristal
berbentuk jarum besar (Vogel, 1990).
3.5.5.3Natrium
a. Uji Nyala Ni/Cr
Dibersihkan kawat Ni/Cr dengan HCl pekat, lalu dipijar pada api
bunsen sampai tidak memberikan warna khusus pada nyala bunsen.
Kemudian dicelupkan kawat pada sampel daun kari segar dan daun kari
rebus, lalu dipijar pada api bunsen, diamati warna yang terjadi pada nyala
bunsen. Jika terdapat natrium akan terbentuk warna kuning keemasan pada
nyala bunsen (Vogel, 1990).
b. Uji Kristal Natrium dengan Asam Pikrat
Diteteskan 1-2 tetes larutan sampel pada object glass, kemudian
ditetesi dengan larutan asam pikrat, dibiarkan ± 5 menit, lalu diamati di
bawah mikroskop. Jika terdapat ion natrium, akan terlihat kristal berbentuk
jarum halus (Vogel, 1990).
3.5.6Analisis Secara Kuantitatif
3.5.6.1Pembuatan Kurva Kalibrasi Kalsium
Dipipet larutan baku kalsium (1000 µg/mL) sebagai LIB I sebanyak 1 mL,
21
demineralisata hingga garis tanda (konsentrasi 10 µg/mL) digunakan sebagai LIB II.
Dari larutan LIB II tersebut (10 µg/mL) dipipet masing-masing 5,0 mL; 10 mL; 15
mL; 20 mL dan 25 mL, kemudian dimasukkan ke dalam labu tentukur 25 mL dan
dicukupkan dengan akua demineralisata hingga garis tanda sehingga diperoleh
konsentrasi berturut-turut 2,0 µg/mL; 4,0 µg/mL; 6,0 µg/mL; 8,0 µg/mL dan 10,0
µg/mL. Kemudian diukur kurva kalibrasi kalsium pada panjang gelombang 422,7 nm
dengan tipe nyala udara-asetilen.
3.5.6.2Pembuatan Kurva Kalibrasi Kalium
Dipipet larutan baku kalium (1000 µg/mL) sebagai LIB I sebanyak 1 mL,
dimasukkan ke dalam labu tentukur 100 mL dan dicukupkan dengan akua
demineralisata hingga garis tanda (konsentrasi 10 µg/mL) digunakan sebagai LIB II.
Dari larutan LIB II tersebut (10 µg/mL) dipipet masing-masing 5,0 mL; 10 mL; 15
mL; 20 mL dan 25 mL, kemudian dimasukkan ke dalam labu tentukur 25 mL dan
dicukupkan dengan akua demineralisata hingga garis tanda sehingga diperoleh
konsentrasi berturut-turut 2,0 µg/mL; 4,0 µg/mL; 6,0 µg/mL; 8,0 µg/mL dan 10,0
µg/mL. Kemudian diukur kurva kalibrasi kalium pada panjang gelombang 766,5 nm
dengan tipe nyala udara-asetilen.
3.5.6.3Pembuatan Kurva Kalibrasi Natrium
Dipipet larutan baku natrium (1000 µg/mL) sebagai LIB I sebanyak 1 mL,
dimasukkan ke dalam labu tentukur 100 mL dan dicukupkan dengan akua
demineralisata hingga garis tanda (konsentrasi 10 µg/mL) digunakan sebagai LIB II.
Dari larutan LIB II tersebut (10 µg/mL) dipipet masing-masing 1,0 mL; 2,0 mL; 3,0
mL; 4,0 mL dan 5,0 mL, kemudian dimasukkan ke dalam labu tentukur 50 mL dan
22
konsentrasi berturut-turut 0,2 µg/mL; 0,4 µg/mL; 0,6 µg/mL; 0,8 µg/mL dan 1,0
µg/mL. Kemudian diukur kurva kalibrasi natrium pada panjang gelombang 589,0 nm
dengan tipe nyala udara-asetilen.
3.5.6.4Penetapan Kadar Kalsium
Dipipet masing-masing larutan sampel (daun kari segar dan daun kari rebus)
sebanyak 0,5 mL, dimasukkan ke dalam labu tentukur 50 mL (faktor pengenceran =
100 kali) dan dicukupkan dengan akua demineralisata hingga garis tanda. Lalu
diukur absorbansinya dengan menggunakan spektrofotometer serapan atom yang
telah dikondisikan dan diatur metodenya, dimana penetapan kadar kalsium dilakukan
pada panjang gelombang 422,7 nm. Nilai absorbansi yang diperoleh harus berada
dalam rentang kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam
sampel ditentukan berdasarkan persamaan garis regresi pada kurva kalibrasi.
3.5.6.5Penetapan Kadar Kalium
Dipipet masing-masing larutan sampel (daun kari segar dan daun kari rebus)
sebanyak 0,1 mL, dimasukkan ke dalam labu tentukur 50 mL (faktor pengenceran =
500 kali) dan dicukupkan dengan akua demineralisata hingga garis tanda. Lalu
diukur absorbansinya dengan menggunakan spektrofotometer serapan atom yang
telah dikondisikan dan diatur metodenya, dimana penetapan kadar kalium dilakukan
pada panjang gelombang 766,5 nm. Nilai absorbansi yang diperoleh harus berada
dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel
23
3.5.6.6Penetapan Kadar Natrium
Dipipet masing-masing larutan sampel (daun kari segar dan daun kari rebus)
sebanyak 0,2 mL, dimasukkan ke dalam labu tentukur 50 mL (faktor pengenceran =
250 kali) dan dicukupkan dengan akua demineralisata hingga garis tanda. Lalu
diukur absorbansinya dengan menggunakan spektrofotometer serapan atom yang
telah dikondisikan dan diatur metodenya, dimana penetapan kadar natrium dilakukan
pada panjang gelombang 589,0 nm. Nilai absorbansi yang diperoleh harus berada
dalam rentang kurva kalibrasi larutan baku natrium. Konsentrasi natrium dalam
sampel ditentukan berdasarkan persamaan garis regresi pada kurva kalibrasi.
3.5.6.7Perhitungan Kadar Kalsium, Kalium dan Natrium dalam Sampel
Kadar kalsium, kalium dan natrium dalam sampel dapat dihitung dengan cara
sebagai berikut:
Kadar (µg/g) =C × V × Fp W
Keterangan: C = konsentrasi logam dalam larutan sampel (µg/mL) V = volume larutan sampel (mL)
Fp = faktor pengenceran W = berat sampel (g)
3.5.7 Analisis Data Secara Statistik
Menurut Gandjar dan Rohman (2007), kadar kalsium, kalium dan natrium
yang diperoleh dari hasil pengukuran masing-masing larutan sampel diuji secara
statistik dengan cara menghitung standar deviasi menggunakan rumus sebagai
berikut:
��= �∑(Xi−X�)
2
24 Keterangan: Xi = kadar sampel
�� = kadar rata-rata sampel N = jumlah pengulangan
Kadar yang diperoleh dari hasil pengukuran masing-masing ke enam larutan
sampel diuji secara statistik dengan uji
t
.Dengan adanya uji
t
maka dapat diketahui data ditolak atau diterima dandapat dihitung dengan menggunakan rumus sebagai berikut:
t
hitung =�
(��−��)
�� √� �
�
Hasil pengujian atau nilai thitung yang diperoleh ditinjau terhadap tabel distribusi t,
apabila thitung > ttabel maka data tersebut ditolak.
Menurut Sudjana (2002), untuk mengetahui kadar kalsium, kalium dan
natrium di dalam sampel dengan interval kepercayaan 99%, α = 0,05, dk = n-1,
dapat digunakan rumus sebagai berikut:
μ
=
�
�
±
�
(12�, ��)
x SD
⁄
√
n
Keterangan: µ = kadar mineral
�� = kadar rata-rata sampel
t = harga t tabel sesuai (dk =
n
-1) α = tingkat kepercayaanSD = standar deviasi n = jumlah perlakuan
3.5.8Validasi Metoda Analisis
3.5.8.1Uji Kecermatan (Accuracy)
Menurut Harmita (2004), kecermatan dinyatakan sebagai persen perolehan
kembali (recovery) larutan baku yang ditambahkan. Uji kecermatan (accuracy)
25
dilakukan dengan menambahkan sejumlah larutan baku dengan konsentrasi tertentu
pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut. Persen perolehan
kembali ditentukan dengan menentukan berapa persen larutan baku yang
ditambahkan tadi dapat ditemukan.
Dalam metode ini, penambahan larutan bakunya adalah 10% dan konsentrasi
semua larutan baku yang digunakan adalah 1000 µg/mL. Larutan baku yang
ditambahkan yaitu kalsium 1,8 mL (1,8 mg), kalium 10,4 mL (10,4 mg) dan natrium
0,4 mL (0,4 mg). Sampel yang telah dihaluskan ditimbang secara seksama sebanyak
10 g dalam krus porselen, dilanjutkan dengan proses destruksi kering. Kemudian
dibuat larutan sampel dan dianalisis secara kuantitatif yaitu diukur absorbansinya
dengan menggunakan spektrofotometer serapan atom dan konsentrasinya
berdasarkan persamaan regresi pada kurva kalibrasi.
Kadar analit dalam metode penambahan baku dapat dihitung dengan rumus
sebagai berikut:
�
�
+
�
=
�
1�
2Keterangan:
C = kadar analit dalam sampel
S = kadar analit yang ditambahkan pada sampel
R1= respon yang diberikan sampel
R2 = respon yang diberikan campuran sampel dengan tambahan analit
Perhitungan perolehan kembali dapat juga ditetapkan dengan rumus sebagai berikut:
% Perolehan Kembali = (CF −CA) C∗A
× 100%
26
CA = konsentrasi sampel sebelum penambahan baku
CF = konsentrasi sampel setelah penambahan baku
C∗A = konsentrasi analit yang ditambahkan
3.5.8.2Uji Keseksamaan (Presisi)
Menurut Harmita (2004), Keseksamaan diukur sebagai simpangan baku
atau simpangan baku relatif (koefisien variasi). Adapun rumus untuk menghitung
simpangan baku relatif adalah:
��� =��
�� × 100%
Keterangan : �� = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation (koefisien variasi)
3.5.8.3Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit
of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Batas deteksi merupakan
parameter uji batas. Penentuan batas deteksi ini ditentukan dengan mendeteksi analit
dalam sampel (Harmita, 2004).
Batas kuantitasi merupakan parameter pada analisis renik dan diartikan
sebagai kuantitasi terkecil analit dalam sampel yang masih dapat memenuhi kriteria
cermat dan seksama (Harmita, 2004).
Batas deteksi (LOQ) dan batas kuantitasi (LOD) dapat dihitung dengan
rumus sebagai berikut:
Simpangan Baku
=
�
∑(Y−Yi )2
n−2
Batas Deteksi (LOD)
=
3�� �����27
3.5.8.4Pengujian Beda Nilai Rata-Rata Antar Sampel
Dalam penelitian biasanya menggunakan dua sampel atau lebih sebagai objek
penelitiannya. Sampel-sampel tersebut dibandingkan untuk melihat ada atau tidaknya
perbedaan setelah sampel-sampel tersebut diberi perlakuan berbeda. Oleh karena itu
dilakukan uji perbedaan nilai rata-rata antar sampel.
Menurut Sudjana (2002), prinsip pengujian beda nilai rata-rata adalah melihat
ada atau tidaknya perbedaan variasi kedua kelompok data dengan menggunakan
rumus:
�
�=
�
12
�
21Keterangan:
Fo = beda nilai yang dihitung
�2 = standar deviasi sampel 1 (mg/100 g)
�2 = standar deviasi sampel 2 (mg/100 g)
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F, maka dilanjutkan uji
dengan distribusi t dengan rumus:
t� = (X�1−X�2) Sp�1 n⁄ 1+ 1 n⁄ 2
S� =�(n1−1)S1
2+ (n
2− 1)S22
n1+ n2 − 2
Keterangan:
��1 = kadar rata-rata sampel 1
��2 = kadar rata-rata sampel 2
Sp = simpangan baku
�1 = jumlah perlakuan sampel 1
�2 = jumlah perlakuan sampel 2
Jika Fo melewati nilai kritis F maka dilanjutkan uji dengan distribusi t dengan rumus:
t� = (X�1−X�2) Sp X �S12
n1
� + S22
n2
28 Keterangan:
��1 = kadar rata-rata sampel 1
��2 = kadar rata-rata sampel 2
S1 = standar deviasi sampel 1
S2 = standar deviasi sampel 2
�1 = jumlah perlakuan sampel 1
�2 = jumlah perlakuan sampel 2
29
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh bagian Herbarium Bogoriense Bidang
Botani Pusat Penelitian Biologi LIPI Bogor. Hasil identifikasi menunjukkan bahwa
tumbuhan yang digunakan adalah daun kari dengan jenis Murraya koenigii (L.)
Spreng dari suku Rutaceae. Data hasil identifikasi tumbuhan dapat dilihat pada
Lampiran 1, halaman 42.
4.2 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
mengidentifikasi mineral kalsium, kalium dan natrium. Data hasil analisis kualitatif
[image:46.595.100.499.490.713.2]dapat dilihat pada Tabel 4.1 dan pada Lampiran 4, halaman 46.
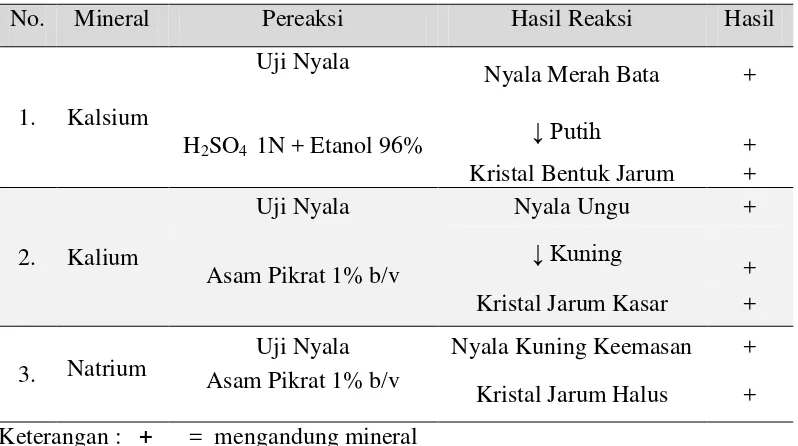
Tabel 4.1 Hasil Analisis Kualitatif pada Daun Kari
No. Mineral Pereaksi Hasil Reaksi Hasil
1. Kalsium
Uji Nyala
Nyala Merah Bata +
H2SO4 1N + Etanol 96%
↓ Putih
+ Kristal Bentuk Jarum +
2. Kalium
Uji Nyala Nyala Ungu +
Asam Pikrat 1% b/v
↓ Kuning
+
Kristal Jarum Kasar +
3. Natrium
Uji Nyala Nyala Kuning Keemasan + Asam Pikrat 1% b/v
Kristal Jarum Halus +
30
Pada Tabel 4.1 menunjukkan bahwa sampel daun kari mengandung mineral
kalsium, kalium dan natrium. Sampel dinyatakan positif mengandung mineral
kalsium karena menghasilkan endapan putih dengan penambahan asam sulfat 1 N
dan etanol 96%, kemudian diamati secara mikroskopis berupa kristal bentuk jarum
serta memberikan nyala warna merah bata setelah dilakukan uji nyala dengan
menggunakan kawat Ni/Cr. Sampel dinyatakan positif mengandung mineral kalium
karena menghasilkan endapan kuning dengan penambahan asam pikrat 1% b/v,
kemudian diamati secara mikroskopis berupa kristal bentuk jarum kasar serta
memberikan nyala warna ungu setelah dilakukan uji nyala dengan menggunakan
kawat Ni/Cr. Sampel dinyatakan positif mengandung mineral natrium karena dengan
penambahan asam pikrat 1% b/v dan diamati secara mikroskopis berupa kristal
bentuk jarum halus serta memberikan nyala warna kuning keemasan setelah
dilakukan uji nyala dengan menggunakan kawat Ni/Cr (Vogel, 1990).
4.3 Analisis Kuantitatif
4.3.1 Kurva Kalibrasi Kalsium, Kalium dan Natrium
Kurva kalibrasi kalsium, kalium dan natrium diperoleh dengan cara mengukur
absorbansi dari larutan baku kalsium; kalium dan natrium pada panjang gelombang
422,7 nm; 766,5 nm dan 589,0 nm. Dari pengukuran kurva kalibrasi masing-masing
diperoleh persamaan regresi diantaranya adalah Y= 0,038547 X + 0,004881 pada
kalsium; Y= 0,04501 X - 0,01113 pada kalium dan Y= 0,140129 X – 0,000886 pada
natrium. Kurva kalibrasi larutan baku kalsium, kalium dan natrium dapat dilihat pada
31 a.
b.
[image:48.595.100.518.99.646.2]c.
Gambar 4.1 Kurva Kalibrasi Secara Spektrofotometri Serapan Atom
32
Berdasarkan kurva kalibrasi pada Gambar 4.1, maka diperoleh hubungan yang
linear antara absorbansi (y) dengan konsentrasi (x). Dimana nilai koefisien korelasi
(r) masing-masing dari kurva kalibrasi yaitu kalsium sebesar 0,9996; kalium sebesar
0,9992 dan natrium sebesar 0,9998. Semua kurva kalibrasi logam nilai r ≥ 0,997
menunjukkan adanya kolerasi linear antara absorbansi dengan konsentrasi (Ermer
dan McB. Miller, 2005).
4.3.2 Penetapan Kadar Mineral Kalsium, Kalium dan Natrium pada Sampel
Sampel yang digunakan pada pengujian kadar mineral kalsium, kalium dan
natrium adalah daun kari yang terdiri dari daun kari segar dan daun kari rebus.
Sampel daun kari dapat dilihat pada Lampiran 2, halaman 43.
Penetapan kadar mineral kalsium, kalium dan natrium dilakukan dengan
metode spektrofotometri serapan atom. Sumber nyala yang digunakan adalah
Udara-Asetilen (UA) dengan suhu nyala 2200°C yang dapat mengatomisasi hampir semua
elemen. Kalsium yang membutuhkan suhu yang tinggi dalam proses atomisasi hanya
dapat teratomisasi sempurna menggunakan sumber nyala ini dengan penambahan
unsur-unsur penyangga seperti Sr dan La (Gandjar dan Rohman, 2011). Namun
kekurangan unsur-unsur penyangga tersebut adalah bernilai mahal. Kalium dan
natrium pada dasarnya merupakan logam alkali yang dapat teratomisasi sempurna
dengan sumber nyala Udara-Propana (UP) ataupun dapat menggunakan grafit
furnace, akan tetapi dalam hal ini keterbatasan alat dan bahan sangat diperhitungkan.
Konsentrasi mineral kalsium, kalium dan natrium pada sampel ditentukan
berdasarkan persamaan garis regresi pada kurva kalibrasi masing-masing mineral
tersebut. Data hasil penetapan kadar mineral kalsium, kalium dan natrium pada
sampel secara kuantitatif ini dapat dilihat pada Lampiran 9, halaman 55 dan contoh
33
Analisis dilanjutkan dengan perhitungan statistik. Data perhitungan statistik
kadar mineral dapat dilihat pada Lampiran 12, halaman 62; Lampiran 13, halaman
66; dan Lampiran 14, halaman 70. Data hasil penetapan kadar mineral kalsium,
kalium dan natrium pada sampel dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil Penetapan Kadar Mineral Kalsium, Kalium dan Natrium pada
Sampel Daun Kari Segar (DKS) dan Daun Kari Rebus (DKR).
Mineral
Kadar Mineral (mg/100 g)
Penurunan Kadar Mineral
(%)
DKS DKR
Kalsium 193,5287 ± 0,9231 182,4140 ± 0,3628 5,7432 Kalium 1139,6203 ± 4,3952 1042,4144 ± 3,3526 8,5297 Natrium 43,0720 ± 0,3970 37,8909 ± 1,4803 12,0289 Keterangan :
DKS = Daun Kari Segar DKR = Daun Kari Rebus
Berdasarkan hasil penetapan kadar mineral kalsium, kalium dan natrium yang
tercantum pada Tabel 4.2, daun kari segar mengandung mineral kalsium, kalium dan
natrium lebih tinggi dibandingkan dengan daun kari rebus. Mineral kalsium dalam
keadaan segar sebesar (193,5287 ± 0,9231) mg/100 g dan rebus sebesar (182,4140 ±
0,3628) mg/100 g. Mineral kalium dalam keadaan segar sebesar (1139,6203 ±
4,3952) mg/100 g, rebus sebesar (1042,4144 ± 3,3526) mg/100 g. Mineral natrium
dalam keadaan segar sebesar (43,0720 ± 0,3970) mg/100 g, rebus sebesar (37,8909 ±
1,4803) mg/100 g. Penurunan kadar mineral diantaranya kalsium sebanyak 5,7432%,
34
Gambar 4.2 Diagram Kadar Mineral Kalsium, Kalium dan Natrium pada Sampel
Daun Kari Segar (DKS) dan Daun Kari Rebus (DKR).
Berdasarkan diagram pada Gambar 4.2, menunjukkan bahwa kadar mineral
daun kari mengalami penurunan kadar secara signifikan dalam jumlah tertentu
setelah proses perebusan. Hal ini diduga karena proses perebusan memberikan
peningkatan terhadap kelarutan mineral yang terkandung di dalam sampel sehingga
dapat mengakibatkan terjadinya pemutusan interaksi mineral dengan komponen
lainnya pada sampel tersebut seperti protein, karbohidrat, lemak, vitamin, serat dan
komponen-komponen kimia lainnya (Santoso, dkk., 2006).
Berbeda dari literatur yang menyatakan bahwa kadar mineral kalsium 166
mg/100 g (Sakhale, dkk., 2007), kalium 811 mg/100 g dan natrium 79,8 mg/100 g
(Subramanian, dkk., 2012), penelitian ini justru menghasilkan kadar kalsium lebih
rendah serta kadar kalium dan natrium lebih tinggi dibandingkan dengan kadar
kalsium, kalium dan natrium pada literatur. Hal ini dapat dipengaruhi oleh beberapa
faktor seperti tempat tumbuh tanaman, kesuburan tanaman, perlakuan terhadap
tanaman dan iklim (Rosmarkam dan Yuwono, 2002).
0 200 400 600 800 1000 1200 1400
Kadar Mineral
Mineral
Kadar Mineral Kalsium, Kalium dan Natrium pada Sampel
[image:51.595.110.499.86.294.2]35
4.3.3 Uji Kecermatan (Accuracy)
Uji kecermatan (accuracy) dinyatakan pada hasil persen perolehan kembali
(recovery) kadar mineral kalsium, kalium dan natrium setelah penambahan larutan
baku kalsium, kalium dan natrium dapat dilihat pada Lampiran 21, halaman 87.
Contoh perhitungan persen perolehan kembali (recovery) dapat dilihat pada
Lampiran 22, halaman 88. Data hasil persen perolehan kembali (recovery) dapat
[image:52.595.101.507.308.410.2]dilihat pada Tabel 4.3.
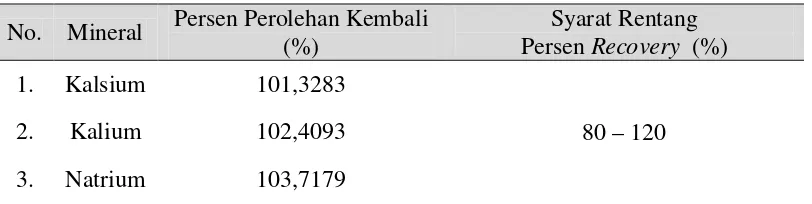
Tabel 4.3 Persen Perolehan Kembali (Recovery) Mineral Kalsium, Kalium dan
Natrium pada Sampel
No. Mineral Persen Perolehan Kembali (%)
Syarat Rentang Persen Recovery (%)
1. Kalsium 101,3283
80 – 120 2. Kalium 102,4093
3. Natrium 103,7179
Berdasarkan Tabel 4.3 di atas, dapat dilihat bahwa rata-rata hasil uji
perolehan kembali (recovery) kalsium adalah 101,3283 %, untuk kalium adalah
102,4093 % dan untuk natrium adalah 103,7179 %. Persen perolehan kembali
(recovery) tersebut menunjukkan kecermatan kerja yang memuaskan pada saat
pemeriksaan kadar kalsium, kalium dan natrium dalam sampel. Hasil yang diperoleh
dari persen perolehan kembali memberikan ketepatan pada pemeriksaan kandungan
mineral dalam sampel. Hasil yang diperoleh dari uji kecermatan (accuracy) ini
memenuhi syarat akurasi yang telah ditetapkan yaitu rata-rata hasil perolehan
36
4.3.4 Uji Keseksamaan (Presisi)
Keseksamaan diukur sebagai simpangan baku atau simpangan baku relatif
(koefisien variasi). Nilai simpangan baku dan simpangan baku relatif untuk mineral
kalsium, kalium dan natrium dapat dilihat pada Tabel 4.4. Perhitungan simpangan
[image:53.595.102.505.254.340.2]baku relatif (RSD) dapat dilihat pada Lampiran 23, halaman 91.
Tabel 4.4 Nilai Simpangan Baku dan Simpangan Baku Relatif Mineral Kalsium,
Kalium dan Natrium
No. Mineral Simpangan Baku Simpangan Baku Relatif
1. Kalsium 1,3852 1,3670%
2. Kalium 2,7002 2,6367%
3. Natrium 4,8310 4,6578%
Berdasarkan Tabel 4.4, dapat dilihat nilai simpangan baku (SD) mineral
kalsium adalah sebesar 1,3852, kalium adalah sebesar 2,7002, dan natrium adalah
sebesar 4,8310. Nilai simpangan baku relatif (RSD) mineral kalsium sebesar
1,3670%, kalium sebesar 2,6367% dan natrium sebesar 4,6578%.
Menurut Harmita (2004), nilai simpangan baku relatif (RSD) untuk analit
dengan kadar part per million (ppm) adalah tidak lebih dari 16%. Dari hasil yang
diperoleh menunjukkan bahwa metode yang dilakukan memiliki presisi yang baik.
4.3.5 Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of
Quantitation)
Berdasarkan data kurva kalibrasi kalsium, kalium dan natrium diperoleh batas
deteksi (LOD) dan batas kuantitasi (LOQ) pada ketiga mineral tersebut. Batas
deteksi dan batas kuantitasi kalsium, kalium dan natrium dapat dilihat pula pada
37
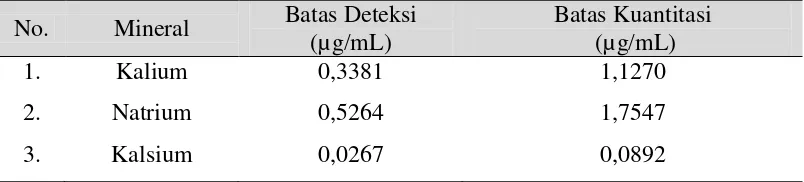
Tabel 4.5 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Mineral Kalsium, Kalium dan Natrium pada Sampel
Berdasarkan Tabel 4.5, dari hasil perhitungan dapat dilihat bahwa semua hasil
yang diperoleh pada pengukuran sampel berada diatas batas deteksi dan batas
kuantitasi. Perhitungan batas deteksi dan batas kuantitasi dapat dilihat pada Lampiran
20, halaman 84.
4.3.6 Pengujian Beda Nilai Rata-rata Kadar Kalsium, Kalium dan Natrium pada Sampel Daun Kari Segar dan Daun Kari Rebus
Pengujian beda nilai rata-rata kadar kalsium, kalium dan natrium pada sampel
bertujuan untuk melihat apakah ada perbedaan yang signifikan pada rata-rata kadar
kalsium, kalium dan natrium antara sampel daun kari segar dengan daun kari rebus.
Uji statistik yang digunakan yaitu uji beda nilai rata-rata kadar kalsium, kalium dan
<