PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
PADA DAUN KUCAI (Allium schoenoprasum, L.)
SEGAR DAN DIREBUS SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
IKSEN
NIM 111501043
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
PADA DAUN KUCAI (Allium schoenoprasum, L.)
SEGAR DAN DIREBUS SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
IKSEN
NIM 111501043
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
PADA DAUN KUCAI (Allium schoenoprasum, L.) SEGAR DAN
DIREBUS SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
OLEH:
IKSEN
NIM 111501043
Dipertahankan di Hadapan Pantia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal 23 Mei 2015
Medan, 23Mei 2015
Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
Prof. Dr. Julia Reveny, M.Si., Apt. NIP 195807101986012001
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Prof. Dr. Ginda Haro, M.Sc., Apt. Prof. Dr. rer. nat. E. De Lux Putra, S.U., Apt.
NIP 195108161980031002 NIP 195306191983031001
Prof. Dr. Ginda Haro, M.Sc., Apt. Pembimbing II, NIP 195108161980031002
Dr. Masfria, M.S., Apt. Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195707231986012001 NIP 195201041980031002
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Tuhan yang Maha Esa atas segala
limpahan berkat, rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan
penelitian dan penyusunan skripsi ini. Skripsi ini disusun untuk melengkapi salah
satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara, dengan judul Penetapan Kadar Kalium, Kalsium, dan
Natrium Pada Daun Kucai (Allium schoenoprasum, L.) Segar dan Direbus Secara
Spektrofotometri Serapan Atom.
Pada kesempatan ini dengan kerendahan hati dan hormat, penulis
mengucapkan terimakasih kepada Bapak Prof. Dr. Ginda Haro, M.Sc., Apt. Dan
Ibu Dr. Masfria, M.S., Apt. yang telah membimbing, memberikan petunjuk,
saran-saran serta motivasi selama penelitian hingga selesainya skripsi ini. Bapak
Prof. Dr. Sumadio Hadisahputra, Apt. Selaku Dekan Fakultas Farmasi USU
Medan, yang telah memberikan bimbingan dan penyediaan fasilitas sehingga
penulis dapat menyelesaikan pendidikan. Bapak Prof. Dr. rer. nat. Effendy De
Lux Putra, S.U., Apt., Bapak Drs. Fathur Rahman, M.Si., Apt., dan Bapak Drs.
Nahitma Ginting, M.Si., Apt. selaku dosen penguji yang telah memberikan kritik,
saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan Ibu
staf pengajar Fakultas Farmasi USU Medan yang telah mendidik perkuliahan dan
Ibu Dra. Aswita Hanif Lubis, M.Si., Apt., selaku penasehat akademik yang selalu
memberikan bimbingan kepada penulis selama masa perkuliahan.
Penulis juga mengucapkan terima kasih dan penghargaan tiada terhingga
kepada Ayahanda Harun Wijaya, dan Ibunda Ernawaty Suherman yang telah
pengorbanan baik materi maupun non-materi. Serta saudaraku Suryaty, Suryany
dan Andios atas segala doa, kasih sayang dan memberikan semangat.
Sahabat-sahabatku Jessica Novia, Lusiana Juwita, David, Sheilla, Virginia, Wanda, dan
Feby terima kasih untuk perhatian, semangat, doa, dan kebersamaan selama ini,
serta teman-teman Farmasi USU 2011 yang telah ikut membantu penulis yang
tidak dapat disebutkan satu persatu.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi
kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini
bermanfaat bagi kita semua.
Medan, 23 Mei 2015 Penulis
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
PADA DAUN KUCAI (Allium schoenoprasum L.)
SEGAR DAN DIREBUS SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
Abstrak
Kucai (Allium schoenoprasum, L.) adalah tanaman yang berumur panjang
yang sangat mudah tumbuh. Tanaman ini dikenal sebagai sayuran dari keluarga
Liliaceae. Seluruh bagian dari tanaman kucai dapat dimakan. Kucai juga dapat digunakan secara segar maupun direbus sebagai bagian dari bumbu masakan. Secara tradisional, kucai digunakan sebagai obat anti hipertensi. Penelitian ini bertujuan untuk mengetahui perbedaan kandungan kalium, kalsium, dan natrium pada kucai yang segar dan direbus.
Sampel kucai didestruksi kering, kemudian analisis kuantitatif kalium, kalsium, dan natrium dilakukan dengan menggunakan spektrofotometer serapan atom (SSA) yaitu kalium pada panjang gelombang 766,50 nm, kalsium pada panjang gelombang 422,7 nm, dan natrium pada panjang gelombang 589,0 nm. Keuntungan dari metode ini adalah dapat menentukan kadar logam dalam jumlah kecil serta tanpa dipengaruhi oleh keberadaan logam yang lain.
Hasil peneltian ini menunjukkan kadar kalium pada daun kucai segar sebesar (321,1147 ± 0,9891) mg/100 g dan pada daun kucai rebus sebesar (169,2157 ± 1,9352) mg/100 g. Kadar kalsium pada daun kucai segar sebesar
(47,4054 ± 0,7960) mg/100 g dan pada daun kucai rebus sebesar (43,8424 ± 0,1995) mg/100 g. Kadar natrium pada daun kucai segar sebesar
(10,0729 ± 0,0619) mg/100 g sedangkan pada daun kucai rebus sebesar (4,2025 ± 0,0564) mg/100 g. Sedangkan persentase penurunan kadar mineral
setelah direbus untuk kalium adalah 47,30%, untuk kalsium sebesar 7,52%, dan untuk natrium sebesar 58,28 %. Secara statistik uji beda rata-rata kandungan kalium, kalsium, dan natrium antara daun kucai segar dan rebus dengan menggunakan distribusi F, menyimpulkan bahwa kandungan kalium, kalsium, dan natrium pada daun kucai segar lebih tinggi secara signifikan dari daun kucai rebus.
DETERMINATION OF POTASSIUM, CALCIUM, AND
SODIUM LEVEL IN CHIVE (Allium schoenoprasum L.)
FRESH AND BOILED IN
ATOMIC ABSORPTION SPECTROPHOTOMETRY
Abstract
Chives ( Allium schoenoprasum L. ) is a long-lived plants which are very easy to grow . This plant is known as the vegetable of the Liliaceae family . All parts of the chives edible . Chives can also be used fresh or boiled as part of spice in cooking . Traditionally , chives are used as anti hypertension drugs . This study aims to determine the differences in potassium , calcium , and sodium in fresh chives and boiled
Samples were dried destruction, and quantitative analysis of potassium, calcium, and sodium were calculated using atomic absorption specrophotometry (AAS). Potassium was at a wavelenght of 766.50 nm, calcium at 422.7 nm and sodium at 589.0 nm. The advangtage of this method is to determine the metal content in small quantities and without being affected by the presence of others metals.
The results showed the level of potassium in chives is (321.1147 ± 0.9891) mg/100 g and the boiled chives for (169.2157 ± 1.9352) mg/100 g. Levels of calcium in fresh chives (47.4054 ± 0.7960) mg/100 g and boiled chives for
(43.8424 ± 0.1995) mg/100 g. Levels of sodium in fresh chives (10.0729 ± 0.0619) mg/100 g and boiled chives for (4.2025 ± 0.0564) mg/100 g.
Decreasing percentage in chives after boiled for potassium is 47.30%, 7.52 % for calcium, and 58.28% for sodium. Statistically defferent test average content of potassium, calcium and sodium between fresh chives and boiled using the F distibution, concluded that the content of potassium, calcium, and sodium in fresh chive significantly higher than boiled chives.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iv
ABSTRAK ... v
ABSTRACT ... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Sampel ... 5
2.1.1 Taksonomi Kucai ... 5
2.1.2 Deskripsi Tanaman Kucai ... 5
2.1.3 Nama Daerah ... 6
2.1.4 Khasiat Kucai ... 7
2.2.1 Kalsium ... 8
2.2.2 Kalium ... 8
2.2.3 Natrium ... 9
2.3 Spektrofotometri Serapan Atom ... 9
2.4 Validasi Metode Analisis ... 12
BAB III METODOLOGI PERCOBAAN ... 15
3.1 Tempat dan Waktu Penelitian ... 15
3.2 Alat ... 15
3.3 Bahan ... 15
3.4 Pembuatan Pereaksi ... 16
3.4.1 Larutan HNO3 (1:1) ... 16
3.4.2 Larutan H2SO4 1 N ... 16
3.4.3 Asam Pikrat 1% ... 16
3.5 Prosedur Penelitian ... 16
3.5.1 Pengambilan Sampel ... 16
3.5.2 Penyiapan Bahan ... 16
3.5.3 Prosedur Dekstruksi Kering ... 17
3.5.4 Pembuatan Larutan Sampel ... 17
3.5.5 Analisa Kualitatif ... 18
3.5.5.1 Kalium ... 18
3.5.5.2 Kalsium ... 18
3.5.5.3 Natrium ... 19
3.5.6 Analisa Kuantitatif ... 19
3.5.6.2 Pembuatan Kurva Kalibrasi Kalsium ... 20
3.5.6.3 Pembuatan Kurva Kalibrasi Natrium ... 20
3.5.7 Penetapan Kadar Mineral Dalam Sampel ... 20
3.5.7.1 Penetapan Kadar Kalium ... 20
3.5.7.2 Penetapan Kadar Kalsium ... 21
3.5.7.3 Penetapan Kadar Natrium ... 21
3.5.8 Perhitungan Kadar Kalium, Kalsium, dan Natrium dalam Sampel ... 22
3.5.9 Analisa Data Secara Statistik ... 22
3.5.9.1 Penolakan Hasil Pengamatan ... 22
3.5.9.2 Pengujian Beda Nilai Rata – rata Antar Sampel ... 23
3.5.10 Uji Perolehan Kembali ( Recovery) ... 24
3.5.11 Simpangan Baku Relatif ... 25
3.5.12 Penentuan Batas Deteksi dan Batas Kuantisasi ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Pemeriksaan Kualitatif ... 27
4.2 Pemeriksaan Kuantitatif ... 28
4.2.1 Kurva Kalibrasi Kalium, Kalsium dan Natrium ... 28
4.2.2 Analisis Kandungan Kalium, Kalsium, dan Natrium Dalam Daun Kucai Segar dan Daun Kucai Rebus .. 30
4.2.3 Uji Perolehan Kembali ( Recovery) ... 34
4.2.4 Simpangan Baku Relatif ... 35
4.2.5 Batas Deteksi dan Batas Kuantisasi ... 35
BAB V KESIMPULAN DAN SARAN ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Halaman
Tabel 4.1 Analisa Kandungan Kalium, Kalsium, dan Natrium Dalam
Sampel Yang Dianalisa ... 27
Tabel 4.2 Uji Nyala ... 27
Tabel 4.3 Hasil Analisis Perhitungan Q-test ... 31
Tabel 4.4 Hasil Analisa Kuantitatif Kadar Kalium, Kalsium, dan Natrium pada Daun Kucai Segar dan Daun Kucai Rebus .. 31
Tabel 4.5 Hasil Penurunan Kadar Kalium, Kalsium, dan Natrium pada Daun Kucai Segar dan Daun Kucai Rebus ... 32
Tabel 4.6 Hasil Uji Beda Rata-rata Kad ar Kalium, Kalsium, dan Natrium Antar Sampel ... 33
Tabel 4.7 Uji Perolehan Kembali (Recovery) ... 34
Tabel 4.8 Hasil Perhitungan Simpangan Baku Relatif (RSD) ... 35
DAFTAR GAMBAR
Halaman
Gambar 2.1 Komponen Spektrofotometri Serapan Atom ... 12
Gambar 4.1 Kurva Kalibrasi Larutan Induk Baku Kalium ... 28
Gambar 4.2 Kurva Kalibrasi Larutan Induk Baku Kalsium... 29
Gambar 4.3 Kurva Kalibrasi Larutan Induk Baku Natrium... 29
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Gambar Kucai dan Abu Hasil Destruksi Dari Kucai ... 40
Lampiran 2 Bagan Alir Proses Destruksi Kering ... 41
Lampiran 3 Bagan Alir Pembuatan Samapel ... 42
Lampiran 4 Data Kalibrasi Kalium dengan Spektrofotometri Serapan Atom ... 43
Lampiran 5 Data Kalibrasi Kalsium dengan Spektrofotometri Serapan Atom ... 45
Lampiran 6 Data Kalibrasi Kalsium dengan Spektrofotometri Serapan Atom ... 47
Lampiran 7 Perhitungan Batas Deteksi dan Batas Kuantisasi ... 49
Lampiran 8 Hasil Analisis Kadar Kalium, Kalsium, dan Natrium dalam Daun Kucai Segar ... 52
Lampiran 9 Hasil Analisis Kadar Kalium, Kalsium, dan Natrium dalam Daun Kucai Rebus ... 53
Lampiran 10 Contoh Perhitungan Kadar Kalium, Kalsium, dan Natrium dalam Daun Kucai Segar ... 54
Lampiran 11 Contoh Perhitungan Kadar Kalium, Kalsium, dan Natrium dalam Daun Kucai Rebus ... 56
Lampiran 12 Perhitungan Persentase Pengurangan Kadar Kalium, Kalsium dan Natrium dalam Daun Kucai Rebus ... 58
Lampiran 13 Perhitungan Statistik Kadar Kalium dalam Sampel ... 59
Lampiran 14 Perhitungan Statistik Kadar Kalsium dalam Sampel ... 63
Lampiran 15 Perhitungan Statistik Kadar Natrium dalam Sampel ... 67
Lampiran 17 Pengujian Beda Rata - rata Kadar Kalsium Antara Daun
Kucai Segar dan Daun Kucai Rebus ... 73
Lampiran 18 Pengujian Beda Rata - rata Kadar Natrium Antara Daun
Kucai Segar dan Daun Kucai Rebus ... 75
Lampiran 19 Hasil Uji Recovery Kalium, Kalsium, dan Natrium dalam
Daun Kucai Segar ... 77
Lampiran 20 Contoh Hasil Uji Recovery Kalium, Kalsium, dan Natrium
dalam Daun Kucai Segar ... 78
Lampiran 21 Perhitungan Simpangan Baku Relatif ( RSD ) Kadar
Kalium, Kalsium, dan Natrium dalam Daun Kucai Segar . 81
Lampiran 22 Gambar Alat Spektrofotometer Serapan Atom dan Tanur . 84
Lampiran 23 Uji Kualitatif Kalium, Kalsium, dan Natrium ... 85
Lampiran 24 Tabel Distribusi t ... 86
Lampiran 25 Tabel Nilai Kritis Distribusi F ... 87
Lampiran 26 Tabel Nilai Qkritis pada Tarif Kepercayaan 95% pada Uji
Dua Sisi ... 88
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM
PADA DAUN KUCAI (Allium schoenoprasum L.)
SEGAR DAN DIREBUS SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
Abstrak
Kucai (Allium schoenoprasum, L.) adalah tanaman yang berumur panjang
yang sangat mudah tumbuh. Tanaman ini dikenal sebagai sayuran dari keluarga
Liliaceae. Seluruh bagian dari tanaman kucai dapat dimakan. Kucai juga dapat digunakan secara segar maupun direbus sebagai bagian dari bumbu masakan. Secara tradisional, kucai digunakan sebagai obat anti hipertensi. Penelitian ini bertujuan untuk mengetahui perbedaan kandungan kalium, kalsium, dan natrium pada kucai yang segar dan direbus.
Sampel kucai didestruksi kering, kemudian analisis kuantitatif kalium, kalsium, dan natrium dilakukan dengan menggunakan spektrofotometer serapan atom (SSA) yaitu kalium pada panjang gelombang 766,50 nm, kalsium pada panjang gelombang 422,7 nm, dan natrium pada panjang gelombang 589,0 nm. Keuntungan dari metode ini adalah dapat menentukan kadar logam dalam jumlah kecil serta tanpa dipengaruhi oleh keberadaan logam yang lain.
Hasil peneltian ini menunjukkan kadar kalium pada daun kucai segar sebesar (321,1147 ± 0,9891) mg/100 g dan pada daun kucai rebus sebesar (169,2157 ± 1,9352) mg/100 g. Kadar kalsium pada daun kucai segar sebesar
(47,4054 ± 0,7960) mg/100 g dan pada daun kucai rebus sebesar (43,8424 ± 0,1995) mg/100 g. Kadar natrium pada daun kucai segar sebesar
(10,0729 ± 0,0619) mg/100 g sedangkan pada daun kucai rebus sebesar (4,2025 ± 0,0564) mg/100 g. Sedangkan persentase penurunan kadar mineral
setelah direbus untuk kalium adalah 47,30%, untuk kalsium sebesar 7,52%, dan untuk natrium sebesar 58,28 %. Secara statistik uji beda rata-rata kandungan kalium, kalsium, dan natrium antara daun kucai segar dan rebus dengan menggunakan distribusi F, menyimpulkan bahwa kandungan kalium, kalsium, dan natrium pada daun kucai segar lebih tinggi secara signifikan dari daun kucai rebus.
DETERMINATION OF POTASSIUM, CALCIUM, AND
SODIUM LEVEL IN CHIVE (Allium schoenoprasum L.)
FRESH AND BOILED IN
ATOMIC ABSORPTION SPECTROPHOTOMETRY
Abstract
Chives ( Allium schoenoprasum L. ) is a long-lived plants which are very easy to grow . This plant is known as the vegetable of the Liliaceae family . All parts of the chives edible . Chives can also be used fresh or boiled as part of spice in cooking . Traditionally , chives are used as anti hypertension drugs . This study aims to determine the differences in potassium , calcium , and sodium in fresh chives and boiled
Samples were dried destruction, and quantitative analysis of potassium, calcium, and sodium were calculated using atomic absorption specrophotometry (AAS). Potassium was at a wavelenght of 766.50 nm, calcium at 422.7 nm and sodium at 589.0 nm. The advangtage of this method is to determine the metal content in small quantities and without being affected by the presence of others metals.
The results showed the level of potassium in chives is (321.1147 ± 0.9891) mg/100 g and the boiled chives for (169.2157 ± 1.9352) mg/100 g. Levels of calcium in fresh chives (47.4054 ± 0.7960) mg/100 g and boiled chives for
(43.8424 ± 0.1995) mg/100 g. Levels of sodium in fresh chives (10.0729 ± 0.0619) mg/100 g and boiled chives for (4.2025 ± 0.0564) mg/100 g.
Decreasing percentage in chives after boiled for potassium is 47.30%, 7.52 % for calcium, and 58.28% for sodium. Statistically defferent test average content of potassium, calcium and sodium between fresh chives and boiled using the F distibution, concluded that the content of potassium, calcium, and sodium in fresh chive significantly higher than boiled chives.
BAB I
PENDAHULUAN
1.1 Latar BelakangKucai (Allium schoenoprasum, L.) diketahui berasal dari sebagian wilayah
Amerika Utara dan Eropa Utara. Tanaman ini dikenal sebagai sayuran daun dari
keluarga Liliaceae (tanaman berumbi) dan biasa disajikan dalam irisan kecil-kecil.
Selain sebagai tanaman sayur, kucai juga sering ditanam sebagai tanaman hias.
Kucai dapat tumbuh pada berbagai jenis tanah. Pertumbuhan akan sangat baik jika
ditanam pada tanah yang agak dalam dan dipenuhi dengan kompos. Kucai adalah
tanaman yang berumur panjang (perrenial) (Pinzon, dkk., 2013) dimana dapat
terus hidup hingga beberapa tahun jika keadaan tanahnya terus dijaga, yaitu tanah
yang subur (Andarwulan dan Faradilla, 2012).
Masyarakat Indonesia telah lama memanfaatkan kucai untuk pengobatan,
diantaranya untuk mengatasi keputihan, sembelit serta infeksi kuman bakteri
dalam usus. Selain itu kucai juga berkhasiat melancarkan aliran darah, sekaligus
mencegah pembekuan darah (Andarwulan dan Faradilla, 2012). Belakangan ini
kucai secara tradisional digunakan sebagai obat penurun tekanan darah tinggi.
Efek hipotensi ekstrak etanol dan ekstrak n-heksan simplisia segar kucai sudah
diteliti (Fidrianny, dkk., 2003).
Seluruh bagian dari tanaman kucai dapat dimakan (dari pucuk sampai
umbinya). Daun kucai beraroma khas namun berbeda dengan aroma daun prei
(Allium porrum) maupun daun bawang (Allium cepa). Aroma kucai lebih dekat ke
bawang putih sehingga lebih sering disebut sebagai garlic-chives. Bunga kucai
kucai sebagai salah satu bumbu masakan favorit (Andarwulan dan Faradilla,
2012).
Berdasarkan penjelasan di atas penulis tertarik untuk meneliti kandungan
kalium, kalsium dan natrium yang terdapat pada daun kucai. Natrium berperan
menjaga keseimbangan cairan ekstraseluler agar cairan tidak keluar ke darah dan
masuk ke dalam sel-sel, sedangkan di dalam sel kalium yang menjaga agar cairan
tidak keluar dari sel. Konsumsi kalium yang banyak akan meningkatkan
konsentrasinya di dalam cairan intraseluler, sehingga cenderung menarik cairan
dari bagian ekstraseluler dan menyebabkan polyuri. Kalium dapat bersifat
sebagai diuresis dimana dapat menurunkan tekanan darah. Kalium dan kalsium
berperan dalam transmisi saraf dan relaksasi otot. Kalsium juga penting dalam
pembentukan tulang dan gigi (Almatsier, 2013).
Metode kompleksometri, spektrofotometri serapan atom dan gravimetri
banyak digunakan untuk penetapan kadar kalium, kalsium dan natrium tetapi,
pada penelitian ini dilakukan dengan menggunakan spektrofotometer serapan
atom karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm)
dan pelaksanaannya relatif cepat dan sederhana, dan interferensinya sedikit
(Gandjar dan Rohman, 2007).
Berdasarkan uraian di atas, penulis tertarik untuk meneliti kandungan
kalium, kalsium, dan natrium yang terdapat pada daun kucai segar dan daun kucai
rebus. Dengan demikian, metode yang dipilih untuk penetapan kadar kalium,
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut :
a. Berapakah kadar kalium, kalsium, dan natrium yang terkandung dalam daun
kucai segar dan direbus ?
b. Apakah terdapat perbedaan kadar mineral kalium, kalsium, dan natirum pada
daun kucai segar dan direbus ?
1.3 Hipotesis
Hipotesis dalam penelitian ini adalah :
a. Daun kucai segar dan direbus memiliki kadar kalium, kalsium, dan natrium
dalam jumlah berbeda.
b. Terdapat perbedaan kadar mineral kalium, kalsium, dan natrium pada daun
kucai segar dan direbus
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah :
a. Untuk menentukan perbedaan kadar mineral kalium, kalsium, dan natrium
pada daun kucai segar dan direbus.
b. Untuk menentukan adanya perbedaan kadar mineral kalium, kalsium, dan
1.5 Manfaat Penelitian
Manfaat dari penelitian ini adalah dapat memberikan informasi kepada
masyarakat tentang kandungan mineral kalium, kalsium, dan natrium pada daun
kucai (Allium schoenoprasum, L.) segar dan direbus sehingga dapat digunakan
sebagai salah satu makanan untuk memenuhi asupan nutrisi bagi tubuh dan
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sampel.2.1.1 Taksonomi Kucai.
Menurut United States Department of Agriculture (2015), klasifikasi
lengkap dari tanaman kucai adalah sebagai berikut:
Kingdom : Plantae
Subkingdom : Tracheobionta
Super Divisio : Spermatophyta
Divisi : Magnoliophyta
Kelas : Magnoliopsida (Berkeping satu / monokotil)
Sub kelas : Liliidae
Ordo : Liliales
Family : Liliaceae
Genus : Allium
Species : Allium schoenoprasum L.
2.1.2 Deskripsi Tanaman Kucai ( Allium schoenoprasum L.)
Umum : Tinggi sekitar 15-50 cm, membentuk rumpun, dan berumbi.
Daun : Bearoma khas, berwarna hijau, ramping, pipih dan memanjang.
Bunga : Berwarna putih atau ungu (Andarwulan dan Faradilla, 2012).
Allium schoenoprasum umumnya memiliki tinggi 15-30 cm. Bercabang
pada dasarnya. Helaian daun tipis dengan umbi berbentuk lonjong. Kulit umbi
sangat tipis, putih. Batang bulat, biasanya bertekstur halus. Umbinya kecil, bulat
panjang yang hampir sama. Kucai tumbuh di daerah pada ketinggian ± 1700 m
dpl. Kucai menyukai kondisi tanah yang basah dan bersuhu dingin.
Penyebarannya meliputi Eropa Selatan, Iran, India dan Cina, Amerika Utara (New
York sampai Colorado Selatan) dan Jepang (Badan POM RI, 2008).
Kucai (Allium schoenoprasum, L.) diketahui berasal dari sebagian wilayah
Amerika Utara dan Eropa Utara. Tanaman ini dikenal sebagai sayuran daun dari
keluarga Liliaceae (tanaman berumbi) dan biasa disajikan dalam irisan kecil-kecil.
Selain sebagai tanaman sayur, kucai juga sering ditanam sebagai tanaman hias.
Kucai dapat tumbuh pada berbagai jenis tanah. Pertumbuhan akan sangat baik jika
ditanam pada tanah yang agak dalam dan dipenuhi dengan kompos
Kucai dapat tumbuh di bawah panas matahari ataupun di tempat yang
teduh. Musim kemarau tidak terlalu mempengaruhi perkembangan kucai karena
masih memiliki umbi sebagai cadangan air. Sama seperti bawang, kucai
mempunyai akar berbawang dan daun. Selain itu, kucai dapat ditanam dari bijinya
(Andarwulan dan Faradilla, 2012). Kucai adalah tanaman yang berumur panjang
(perrenial) (Pinzon, dkk., 2013) dimana dapat terus hidup hingga beberapa tahun
jika keadaan tanahnya terus dijaga, yaitu tanah yang subur (Andarwulan dan
Faradilla, 2012).
2.1.3 Nama Daerah
Nama Daerah :
Sumatera: Lokio (Melayu); ganda isi (Palembang). Jawa: Langkio, kucai (Sunda,
Jawa).
Chivet, cive garlic, chive (Inggris), patzia (Cekoslovakia), ciboullete (Perancis),
schnittlauch (Jerman), cipoletta (Italia), cebollino (Spanyol), purlog (Denmark),
bislook (Belanda) (Badan POM RI, 2008).
2.1.4 Khasiat Kucai
Berbagai manfaat kucai untuk pengobatan, diantaranya untuk mengatasi
keputihan, sembelit serta infeksi kuman bakteri dalam usus, melancarkan aliran
darah, sekaligus mencegah pembekuan darah (Andarwulan dan Faradilla, 2012).
Selain itu, kucai juga berfungsi untuk menghambat tumor dan berperan sebagai
antioksidan (Lalage, 2013). Belakangan ini kucai secara tradisional digunakan di
Indonesia sebagai obat herbal penurun tekanan darah tinggi (Amalia, dkk., 2008).
Efek hipotensi ekstrak etanol dan ekstrak n-heksan simplisia segar kucai sudah
diteliti (Fidrianny, dkk., 2003).
2.2 Mineral
Mineral merupakan salah satu unsur yang memegang peranan penting
dalam pemeliharaan fungsi tubuh yang baik pada tingkat sel, jaringan, organ,
maupun fungsi tubuh secara keseluruhan. Mineral digolongkan ke dalam mineral
makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh
dalam jumlah lebih dari 100 mg/hari (natrium, klorida, kalium, fosfor, dan
magnesium), sedangkan mineral mikro adalah mineral yang dibutuhkan tubuh
2.2.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh,
yaitu 1,5 – 2% dari berat orang dewasa atau kurang lebih sebanyak 1 kg.
Peningkatan kebutuhan akan kalsium terjadi pada masa pertumbuhan, kehamilan,
dan meyusui (Almatsier, 2013).
Mineral kalsium mempunyai berbagai fungsi dalam tubuh antara lain
untuk pembentukan tulang dan gigi, mengatur pembekuan darah, katalisator
reaksi-reaksi biologik, serta kontraksi otot. Jumlah yang dianjurkan per hari untuk
anak-anak sebesar 500 mg, remaja 600-700 mg, dan dewasa sebesar 500-800 mg
(Almatsier, 2013).
Konsumsi kalsium hendaknya tidak melebihi 2500 mg sehari. Kelebihan
kalsium dapat menimbulkan batu ginjal atau gangguan ginjal. Kekurangan
kalsium pada masa pertumbuhan dapat menyebabkan gangguan pertumbuhan
sehingga tulang menjadi kurang kuat, mudah bengkok dan rapuh (Almatsier,
2013).
2.2.2 Kalium
Kalium merupakan salah satu mineral makro yang berperan dalam
pengaturan keseimbangan tubuh. Sebanyak 95% kalium berada di dalam cairan
intraseluler. Bersama dengan natrium, kalium memegang peranan dalam
pemeliharaan keseimbangan cairan tubuh. Bersama dengan kalsium, kalium
berperan dalam transmisi saraf dan relaksasi otot (Almatsier, 2013).
Kekurangan kalium karena makanan jarang terjadi, sepanjang seseorang
cukup makan sayuran dan buah segar. Kebutuhan minimun akan kalium ditaksir
2.2.3 Natrium
Natrium adalah kation utama dalam darah dan cairan ekstraseluler. Fungsi
natrium di dalam tubuh bersama-sama dengan kalium menjaga kesimbangan
cairan di dalam tubuh dan sebagai penghantar implus dalam serabut saraf.
Kebutuhan natrium diperkirakan sebesar 500 mg/hari. Kelebihan natrium dapat
menimbulkan edema dan hipertensi sedangkan kekurangan natrium dapat
menyebabkan kejang, apatis, serta kehilangan nafsu makan (Almatsier, 2013).
2.3 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom berprinsip pada absorpsi cahaya oleh atom.
Atom-atom menyerap cahaya pada panjang gelombang tertentu, tergantung pada
sifat unsurnya. Cahaya pada panjang gelombang ini mempunyai cukup energi
untuk mengubah tingkat elektronik suatu atom. Dengan absorpsi energi, berarti
memperoleh lebih banyak energi, suatu atom pada keadaan dasar dinaikkan
tingkat energinya ke tingkat eksitasi ( Khopkar, 1985).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif
unsur-unsur mineral dalam jumlah kecil (trace) dan sangat kecil (ultratrace). Cara ini
memberikan kadar total unsur mineral dalam suatu sampel dan tidak tergantung
pada bentuk molekul mineral dalam sampel tersebut (Gandjar dan Rohman,
2007). Keuntungan dari metode spektrofotometri serapan atom adalah analisis
yang cepat (10-15 detik per sampel per elemen), presisi yang sangat baik,
interferensi sedikit, pelaksanaan yang sederhana, biaya yang murah serta lampu
yang spesifik untuk masing-masing logam (Koplik, 2014).
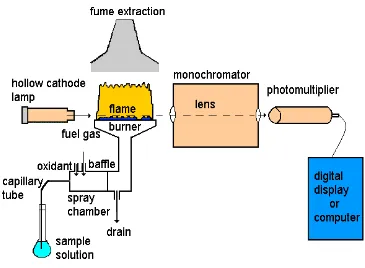
Adapun instrumentasi spektrofotometri serapan atom adalah sebagai
a. Sumber Radiasi
Sumber radiasi yang digunakan adalah lampu katoda berongga
(haloow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang
mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga
yang dilapisi dengan logam tertentu (Gandjar dan Rohman, 2007).
b. Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang
akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam
keadaan dasar. Ada berbagai macam alat yang digunakan untuk mengubah
sampel menjadi uap atom-atomnya, yaitu:
1. Dengan nyala ( Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan
menjadi uap atomnya dan untuk proses atomisasi. Suhu yang dapat
dicapai oleh nyala tergantung pada gas yang digunakan, misalnya
untuk gas asetilen-udara suhunya sebesar 2200oC. Sumber nyala
asetilen-udara ini merupakan sumber yang paling banyak digunakan.
Pada sumber nyala ini asetilen sebagai bahan pengoksidasi (Gandjar
dan Rohman, 2007).
2. Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku grafit. Sejumlah sampel
diambil sedikit (hanya beberapa µL), lalu diletakkan dalam tabung
grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris
dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini,
pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu
katoda berongga sehingga terjadilah proses penyerapan energi yang
memenuhi kaidah analisis kuantitatif(Gandjar dan Rohman, 2007).
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih
spektrum sesuai dengan panjang gelombang yang digunakan dalam
analisis dari sekian banyak spektrum yang dihasilkan lampu katoda
berongga (Gandjar dan Rohman, 2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang
melalui tempat pengatoman (Gandjar dan Rohman, 2007).
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang
diterima dari detektor sehingga dapat dibaca alat pencatat hasil ( Redout)
(Gandjar dan Rohman, 2007).
f. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan
sebagai pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa
kurva yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan
Gambar 2.1. Sistem Peralatan Spektrofotometer Serapan Atom (Anonim, 2014).
Menurut Gandjar dan Rohman (2007), gangguan-gangguan yang terjadi
pada Spektrofotometri Serapan Atom adalah:
1. Gangguan yang berasal dari matriks sampel yang mana dapat
mempengaruhi banyaknya sampel yang mencapai nyala.
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya
atom yang terjadi di dalam nyala.
3. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi
atom yang dianalisiss, yakni absorbansi oleh molekul-molekul yang
tidak terdisosiasi di dalam nyala.
4. Gangguan oleh penyerapan non-atomik.
Adapun gangguan-gangguan di atas dapat diatasi dengan menggunakan
cara-cara sebagai berikut:
b. Penambahan senyawa penyangga
c. Pengekstraksian unsur yang akan dianalisis
d. Pengekstraksian ion atau gugus pengganggu.
2.4 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita,
2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi
metode analisis sebagai berikut:
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan
hasil analisis dengan kadar analit sebenarnya. Kecermatan dinyatakan
sebagai persen perolehan kembali (recovery) analit yang ditambahkan
(Harmita, 2004). Kecermatan ditentukan dengan dua cara, yaitu:
1. Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode
yang dilakukan dengan cara menambahkan sediaan farmasi plasebo,
lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan
kadar analit yang ditambahkan (kadar yang sebenarnya) (Harmita,
2004).
2. Metode penambahan baku
Metode penambahan baku (Standard addition method) merupakan
dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis
dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan
sampel yang dianalisis tanpa penambahan sejumlah analit. Persen
perolehan kembali ditentukan dengan menentukan berapa persen analit
yang ditambahkan ke dalam sampel dapat ditemukan kembali
(Harmita, 2004).
b. Keseksamaan (presisi)
Keseksamaan atau presisi diukur sebagai simpangan baku atau
simpangan baku relatif (koefisien variasi). Keseksamaan atau presisi
merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji
individual ketika suatu metode dilakukan secara berulang untuk sampel
yang homogen (Harmita, 2004).
c. Batas deteksi (Limit of detection) dan batas kuantisasi (Limit of
quantitation).
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang
dapat dideteksi yang masih memberikan respon signifikan, sedangkan
batas kuantisasi merupakan kuantitas terkecil analit dalam sampel yang
BAB III
METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Kimia Farmasi Kualitatif dan
Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan
September 2014 – Desember 2014
3.2 Alat
Alat-alat yang digunakan adalah spektrofotometer serapan atom (Hitachi
Zeeman-2000) dengan nyala udara-asetilen lengkap dengan lampu katoda K, Ca,
dan Na, Purelah UHQ ( ELGA), neraca analisis (BOECO), tanur (Stuart), hot
plate (BOECO), kertas saring Whatman no. 42, krus porselen, dan alat-alat gelas
(Pyrex).
3.3 Bahan
Bahan-bahan kimia yang digunakan dalam penelitian ini yaitu
akuademineralisata, asam nitrat ( HNO3) 65% b/v, larutan baku kalium nitrat
1000 µg/mL, larutan baku kalsium nitrat 1000 µg/mL dan larutan baku natrium
nitrat 1000 µg/mL. Sampel yang digunakan dalam penelitian ini adalah daun
3.4 Pembuatan Pereaksi 3.4.1 Larutan HNO3 (1:1)
Larutan HNO3 65% b/v sebanyak 500 mL diencerkan dengan 500 mL
akuademineralisata (Isaac, 1998).
3.4.2. Larutan H2SO4 1N
Larutan H2SO4 96% v/v sebanyak 3 mL diencerkan dengan
akuademineralisata hingga 100 mL.
3.4.3. Asam Pikrat 1% b/v
Asam pikrat sebanyak 1 gram dilarutkan dalam akuademineralisata hingga
100 mL.
3.5 Prosedur Penelitan 3.5.1 Pengambilan Sampel
Pengambilan sampel dilakukan dengan cara sampling purposif yaitu
anggota sampel ditentukan berdasarkan ciri tertentu yang dianggap mempunyai
hubungan yang erat dengan ciri populasi tanpa membandingkan dengan daerah
lain ( Arikunto, 2013). Bagian tanaman yang diambil sebagai sampel adalah daun
hingga tangkai daun kucai
3.5.2 Penyiapan Bahan
Daun kucai ditimbang sebanyak 1 kg, dicuci bersih, dikeringkan dengan
cara diangin-anginkan, dibagi menjadi 2 bagian, masing-masing ± 500 g, bagian
pertama ditiris kecil-kecil dan bagian kedua direbus terlebih dahulu dengan 2000
mL akuademineralisata yang telah didihkan selama 5 menit lalu ditiriskan
3.5.3 Proses Dekstruksi Kering
Sampel yang telah dihaluskan masing-masing ditimbang sebanyak 25 g,
dimasukkan ke dalam krus porselen, diarangkan di atas hot plate lalu diabukan di
tanur dengan temperatur awal 100oC dan perlahan-lahan dinaikkan menjadi 500oC
dengan interval 25oC setiap 5 menit. Pengabuan dilakukan selama 14 jam dan
dibiarkan dingin lalu dipindahkan ke desikator. Abu dibasahi dengan 10 tetes
akuademineralisata dan ditambahkan 3-4 mL HNO3 (1:1) secara hati-hati.
3.5.4 Pembuatan Larutan Sampel
Abu hasil dekstruksi yang telah dingin dilarutkan dengan 5 mL HNO3
(1:1) hingga diperoleh larutan bening lalu dituangkan ke dalam labu tentukur 100
mL, sisa pada krus porselen dibilas 3 kali dengan akuademineralisata, dituangkan
ke dalam labu tentukur, kemudian larutan dicukupkan volumenya dengan
akuademineralisata hingga 100 mL dan disaring dengan kertas saring Whatman
No. 42, filtrat pertama dibuang sebanyak 5 mL untuk menjenuhkan kertas saring
kemudian filtrat selanjutnya ditampung dalam botol. Filtrat ini digunakan sebagai
larutan sampel untuk analisa kualitatif dan kuantitatif kalium, kalsium dan
3.5.5 Analisa Kualitatif 3.5.5.1 Kalium
3.5.5.1.1 Dengan Uji Nyala
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen
sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan
sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen.
Jika terdapat kalium akan terbentuk warna ungu pada nyala bunsen (Vogel, 1979).
3.5.5.1.2 Uji Kristal Kalium dengan Asam Pikrat
Larutan zat diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop. Jika
terdapat kalium, akan terlihat kristal berbentuk jarum besar (Vogel, 1979).
3.5.5.2 Kalsium
3.5.5.2.1 Dengan Uji Nyala
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen
sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan
sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen.
Jika terdapat kalsium akan terbentuk warna merah bata pada nyala bunsen (Vogel,
1979).
3.5.5.2.2 Uji Kristal Kalsium dengan Asam Sulfat 1 N
Larutan zat diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan asam sulfat 1 N dan etanol 96% v/v akan terbentuk endapan putih lalu
diamati di bawah mikroskop. Jika terdapat kalsium, akan terlihat kristal berbentuk
3.5.5.3 Natrium
3.5.5.3.1 Dengan Uji Nyala
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen
sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan
sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen.
Jika terdapat natrium akan terbentuk warna kuning keemasan pada nyala bunsen
(Vogel, 1979).
3.5.5.3.2 Uji Kristal Natrium dengan Asam Pikrat
Larutan zat diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan asam pikrat, dibiarkan ± 5 menit lalu diamatai di bawah mikroskop. Jika
terdapat natrium, akan terlihat kristal berbentuk jarum kecil (Vogel, 1979).
3.5.6 Analisa Kuantitatif
3.5.6.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/mL) dipipet sebanyak 5 mL, dimasukkan
ke dalam labu tentukur 100 mL dan dicukupkan hingga garis tanda dengan
akuademineralisata (konsentrasi 50 µg/mL).
Larutan untuk kurva kalibrasi kalium dibuat dengan memipet (2; 4; 6; 8;
dan 10) mL larutan baku 50 µg/mL, masing-masing dimasukkan ke dalam labu
tentukur 50 mL dan dicukupkan hingga garis tanda dengan akuademineralisata
(larutan ini mengandung (2,0; 4,0; 6,0; 8,0; dan 10,0) µg/mL) dan diukur pada
panjang gelombang 766,5 nm.
Larutan baku kalsium (1000 µg/mL) dipipet sebanyak 5 mL, dimasukkan
ke dalam labu tentukur 100 mL dan dicukupkan hingga garis tanda dengan
akuademineralisata (konsentrasi 50 µg/mL).
Larutan untuk kurva kalibrasi kalsium dibuat dengan memipet (2; 4; 6; 8;
dan 10) mL larutan baku 50 µg/mL, masing-masing dimasukkan ke dalam labu
tentukur 50 mL dan dicukupkan hingga garis tanda dengan akuademineralisata
(larutan ini mengandung (2,0; 4,0; 6,0; 8,0; dan 10,0) µg/mL) dan diukur pada
panjang gelombang 422,7 nm.
3.5.6.3 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (1000 µg/mL) dipipet sebanyak 1 mL, dimasukkan
ke dalam labu tentukur 100 mL dan dicukupkan hingga garis tanda dengan
akuademineralisata (konsentrasi 10 µg/mL).
Larutan untuk kurva kalibrasi natrium dibuat dengan memipet (1,0; 2,0;
3,0; 4,0; dan 5,0) mL larutan baku 10 µg/mL, masing-masing dimasukkan ke
dalam labu tentukur 50 mL dan dicukupkan hingga garis tanda dengan
akuademineralisata (larutan ini mengandung (0,2; 0,4; 0,6; 0,8; dan 1,0) µg/mL)
dan diukur absorbansinya pada panjang gelombang 589,0 nm.
3.5.7 Penetapan Kadar Mineral Dalam Sampel 3.5.7.1 Penetapan Kadar Kalium
Larutan sampel daun kucai segar dan direbus hasil dekstruksi sebanyak 0,1
mL dimasukkan ke dalam labu tentukur 50 mL dan dicukupkan dengan
akuademineralisata hingga garis tanda.
Diukur absorbansinya dengan menggunakan spektrofotometer serapan
absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan
baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan
persamaan garis regresi dari kurva kalibrasi.
3.5.7.2 Penetapan Kadar Kalsium
Larutan sampel daun kucai segar dan direbus hasil dekstruksi sebanyak 1
mL dimasukkan ke dalam labu tentukur 50 mL dan dicukupkan dengan
akuademineralisata hingga garis tanda.
Diukur absorbansinya dengan menggunakan spektrofotometer serapan
atom pada panjang gelombang 422,7 nm dengan nyala udara-asetilen. Nilai
absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan
baku kalsium. Konsentrasi kalsium dalam sampel ditentukan berdasarkan
persamaan garis regresi dari kurva kalibrasi.
3.5.7.3 Penetapan Kadar Natrium
Larutan sampel daun kucai segar dan direbus hasil dekstruksi sebanyak 1
mL dimasukkan ke dalam labu tentukur 100 mL dan dicukupkan dengan
akuademineralisata hingga garis tanda.
Diukur absorbansinya dengan menggunakan spektrofotometer serapan
atom pada panjang gelombang 589,0 nm dengan nyala udara-asetilen. Nilai
absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan
baku natrium. Konsentrasi natrium dalam sampel ditentukan berdasarkan
persamaan garis regresi dari kurva kalibrasi.
3.5.8 Perhitungan Kadar Kalium, Kalsium dan Natrium dalam Sampel
Kadar (µg/mL) =
Keterangan:
C = Konsentrasi logam dalam larutan sampel (µg/mL) V = Volume larutan sampel (mL)
Fp = Faktor pengenceran
W = Berat sampel (gram)
3.5.9 Analisa Data Secara Statistik 3.5.9.1 Penolakan Hasil Pengamatan
Menurut Gandjar dan Rohman (2007), cara untuk melakukan pencilan atau
hasil yang sangat menyimpang adalah dengan Q-test yang juga dikenal dengan
Dixon’s Q-test yang dirumuskan sebagai berikut :
Q hitung=
Selanjutnya nilai Qhitung ini dibandingkan dengan nilai Qkritis (Qtabel atau nilai yang
diperoleh dari tabel statistik ). Jika nilai Qhitung lebih kecil dari nilai Qkritis, maka
hipotesis nul (null hypothesis ) diterima berarti tidak ada perbedaan antara nilai
yang dicurigai dengan nilai-nilai lain. Sebaliknya, jika nilai Qhitung lebih besar dari
nilai Qkritis, maka hipotesis null ditolak berarti ada perbedaan yang bermakna
antara nilai yang dicurigai dengan nilai-nilai lain.
Menurut Sudjana (2005), untuk menghitung kadar sebenarnya secara
statistik digunakan rumus sebagai berikut:
µ = X ± t( , dk ) x SD/
SD =
Keterangan:
SD = standar deviasi
µ = interval kepercayaan
X = kadar rata-rata sampel
t = harga t tabel sesuai dengan dk= n - 1
Xi = kadar sampel
n = jumLah pengulangan
= tingkat kepercayaan
dk = derajat kebebasan (dk= n-1)
3.5.9.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Menurut Sudjana (2013), sampel yang dibandingkan adalah independen
dan jumlah pengamatan masing-masing lebih kecil dari 30 dan variansi ( ) tidak
diketahui sehingga dilakukan uji F untuk mengetahui apakah variansi kedua
populasi sama ( 1 = 2) atau berbeda ( 1 = 2) dengan menggunakan rumus:
Fo = S12 / S22
Keterangan:
Fo = Beda nilai yang dihitung
S1 = Standar deviasi sampel 1
S2 = Standar deviasi sampel 2
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F, maka
dilanjutkan uji dengan distribusi T dengan rumus:
t
o =Keterangan:
X1 = kadar rata-rata sampel 1
Sp = simpangan baku
n1 = jumlah perlakuan sampel 1
n2 = jumlah perlakuan sampel 2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai
kritis t dan sebaliknya jika Fo melewati nilai kritis F, maka dilanjutkan uji dengan
distribusi t dengan rumus :
t
o =Keterangan:
X1 = kadar rata-rata sampel 1
X2 = Kadar rata-rata sampel 2
S1 = Standar deviasi sampel 1
S2 = Standar deviasi sampel 2
n1 = Jumlah perlakuan sampel 1
n2 = Jumlah perlakuan sampel 2
3.5.10 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode
penambahan larutan standar (Standard addition method). Dalam metode ini, kadar
mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan
penentuan kadar mineral dalam sampel setelah penambahan larutan standar
dengan konsentrasi tertentu (Harmita, 2004). Larutan baku yang ditambahkan
yaitu, 6 mL larutan baku kalium (konsentrasi 1000 µg/mL), 1,5 mL larutan baku
kalsium (konsentrasi 1000 µg/mL) dan 1 mL larutan baku natrium (konsentrasi
1000 µg/mL)
Sampel yang telah dihaluskan ditimbang secara seksama sebanyak 25
gram di dalam krus porselen, lalu ditambahkan 6 mL larutan baku kalium
µg/mL) dan 1 mL larutan baku natrium (konsentrasi 1000 µg/mL), kemudian
dilanjutkan dengan prosedur dekstruksi kering seperti yang telah dilakukan
sebelumnya.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan
rumus berikut:
% Perolehan Kembali = (CF-CA) / C*A x 100%
Keterangan:
CA = kadar logam dalam sampel sebelum penambahan baku
CF = kadar logam dalam sampel setelah penambahan baku
C*A = kadar larutan baku yang ditambahkan
3.5.11 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang
memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan
(Harmita, 2004).
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah sebagai berikut:
RSD
=
Keterangan:
= Kadar rata-rata sampel
SD = Standar Deviasi
3.5.12 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Batas deteksi adalah jumLah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan dibandingkan dengan blanko.
Batas deteksi merupakan parameter uji batas. Batas kuantitasi merupakan
parameter pada analisa renik dan diartikan sebagai kuantitas terkecil analit dalam
sampel yang masih dapat memenuhi kriteris cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut :
Simpangan Baku Residual (Sy/ x) =
Batas Deteksi (LOD) =
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pemeriksaan Kualitatif
Analisa kualitatif dilakukan sebagai analisa pendahuluan untuk
mengetahui adanya kalsium, kalium dan natrium dalam larutan sampel yang akan
dianalisa secara kuantitatif dengan Spektrofotometer Serapan Atom. Hasil analisa
kualitatif kalsium, kalium dan natrium dapat dilihat pada Tabel 4.1 dan 4.2
Tabel 4.1. Analisa kualitatif kalsium, kalium dan natrium dalam sampel yang dianalisis
No Ion yang Dianalisis Pereaksi Hasil Reaksi Keterangan
1 Kalsium Asam sulfat 1 N Kristal jarum +
2 Kalium Asam Pikrat Kristal jarum
besar
+
3 Natrium Asam Pikrat Kristal jarum
kecil
+
Keterangan + : mengandung ion
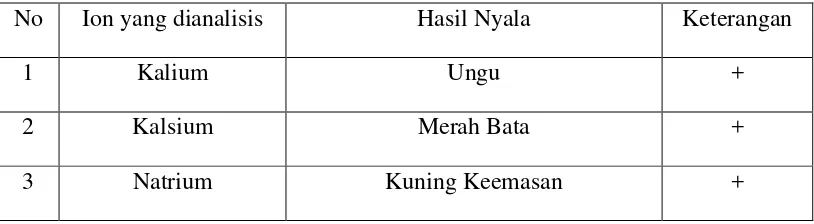
Tabel 4.2. Uji nyala kalium, kalsium, dan natrium dalam larutan sampel yang dianalisis
No Ion yang dianalisis Hasil Nyala Keterangan
1 Kalium Ungu +
2 Kalsium Merah Bata +
3 Natrium Kuning Keemasan +
[image:44.595.108.516.387.529.2] [image:44.595.109.516.620.732.2]Tabel diatas menunjukkan bahwa larutan sampel mengandung kalsium, kalium,
dan natrium (Lampiran 23 Halaman 85)
4.2 Pemeriksaan Kuantitatif
4.2.1 Kurva Kalibrasi Kalium, Kalsium, dan Natrium
Kurva kalibrasi dalam Spektrofotometri Serapan Atom dibuat dengan
memasukkan sejumlah tertentu konsentrasi larutan dalam sistem dilanjutkan
dengan pengukuran absorbansinya. Dalam praktek disarankan untuk membuat
paling tidak empat konsentrasi baku yang berbeda dan satu blanko untuk
membuat kurva baku yang linear yang menyatakan hubungan antara absorbansi
(A) dengan konsentrasi analit untuk melakukan analisis (Gandjar dan Rohman,
2007).
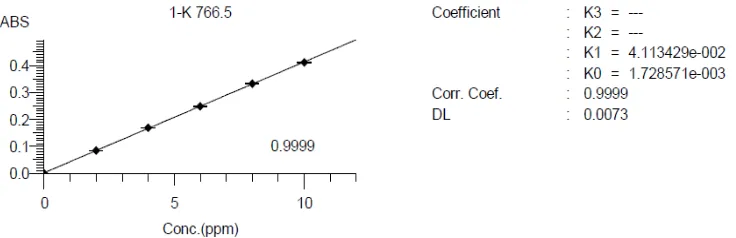
Dari pengukuran kurva kalibrasi diperoleh persamaan regresi yaitu Y =
0,04113X + 0,00175 untuk kalium, Y = 0,03517X + 0,004717 untuk kalsium, dan
Y = 0,1036X - 0,00015 untuk natrium.
Kurva Kalibrasi larutan baku kalium, kalsium, dan natrium dapat dilhat
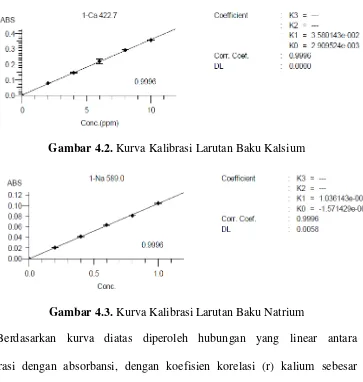
[image:45.595.153.521.551.670.2]pada Gambar 4.1 – 4.3 .
Gambar 4.2. Kurva Kalibrasi Larutan Baku Kalsium
Gambar 4.3. Kurva Kalibrasi Larutan Baku Natrium
Berdasarkan kurva diatas diperoleh hubungan yang linear antara
konsentrasi dengan absorbansi, dengan koefisien korelasi (r) kalium sebesar
0,9999, kalsium sebesar 0,9995, dan natrium sebesar 0,9996. Nilai r ≥ 0,99
menunjukkan adanya korelasi linear yang menyatakan hubungan antara X
(Konsentrasi) dan Y (Absorbansi) (Rohman, dkk., 2012). Data hasil pengukuran
absorbansi larutan baku kalium, kalsium, dan natrium dan perhitungan persamaan
4.2.2 Analisis Kandungan Kalium, Kalsium, dan Natrium dalam Daun Kucai Segar dan Daun Kucai Rebus
Penentuan kadar kalium, kalsium dan natrium dilakukan secara
spektrofotometri serapan atom. Konsentrasi mineral kalium, kalsium, dan natrium
dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi
larutan baku masing-masing mineral. Agar konsentrasi mineral kalium, kalsium,
dan natrium dalam sampel berada pada rentang kurva kalibrasi maka
masing-masing sampel diencerkan terlebih dahulu dengan faktor pengencean yang
berbeda-beda.
Disarankan absorbansi sampel tidak melebihi dari absorbansi baku
tertinggi dan tidak kurang dari absorbansi baku terendah. Dengan kata lain,
absorbansi sampel harus terletak pada kisaran absorbansi kurva baku. Jika
absorbansi sampel terletak di luar kisaran absorbansi kurva baku, maka diperlukan
pengenceran atau pemekatan. Pembacaan absorbansi sampel di luar kisaran
absorbansi baku tidak direkomendasikan karena kurangnya linearitas(Gandjar dan
Rohman, 2007).
Faktor pengenceran untuk penentuan kadar kalium pada daun kucai segar
dan daun kucai rebus adalah sebesar (50/0,1) kali, faktor pengenceran untuk
penentuan kadar kalsium pada daun kucai segar dan daun kucai rebus adalah
sebesar (50/1) kali, dan faktor pengenceran untuk penentuan kadar natrium pada
daun segar dan daun kucai rebus adalah sebesar (100/1) kali. Data dan contoh
perhitungan dapat dilihat pada Lampiran 8 - 11 halaman 52 – 57.
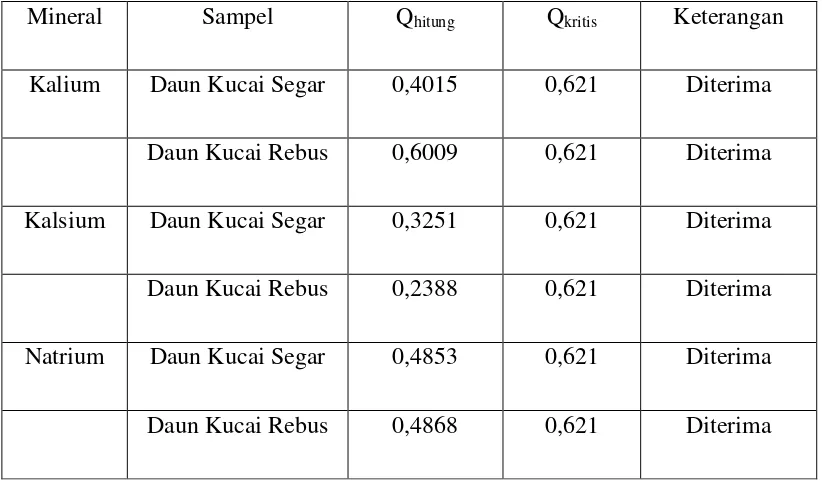
Analisis dilanjutkan dengan perhitungan statistik Q-test untuk memastikan
untuk ditolak atau diterima. Hasil statistik menunjukkan data dapat diterima
semua karena nilai Qhitung ≤ Qkritis. Hasil analisis perhitungan statistik Q-test dapat
[image:48.595.107.518.197.439.2]dilihat pada Tabel4.3.
Tabel 4.3 Hasil Analisis Pehitungan Statistik Q-test
Mineral Sampel Qhitung Qkritis Keterangan
Kalium Daun Kucai Segar 0,4015 0,621 Diterima
Daun Kucai Rebus 0,6009 0,621 Diterima
Kalsium Daun Kucai Segar 0,3251 0,621 Diterima
Daun Kucai Rebus 0,2388 0,621 Diterima
Natrium Daun Kucai Segar 0,4853 0,621 Diterima
Daun Kucai Rebus 0,4868 0,621 Diterima
Hasil perhitungan dapat dilihat pada Lampiran 13 - 15 halaman 59 sampai
dengan halaman 70.
Hasil analisis kuantitatif mineral kalium, kalsium, dan natrium pada
Tabel 4.4 Hasil Analisis Kuantitatif Kadar Kalium, Kalsium, dan Natrium dalam Sampel
No Sampel Kadar Kalium
(mg/100g)
Kadar Kalsium
(mg/100g)
Kadar Natrium
(mg/100g)
1 DKS 321,1147±0,9891 47,4054±0,7960 10,0729±0,0619
2 DKR 169,2157±1,9352 43,8423±0,1995 4,2025±0,0564
Keterangan :
DKS : Daun Kucai Segar
DKR : Daun Kucai Rebus
Data yang didapat kemudian dihitung berapa besar penurunan kadar dari
masing - masing mineral pada sampel yaitu penurunan kadar kalium, kalsium,
dan natrium pada daun kucai segar. (Perhitungan dapat dilihat pada Lampiran 12
Halaman 58 )
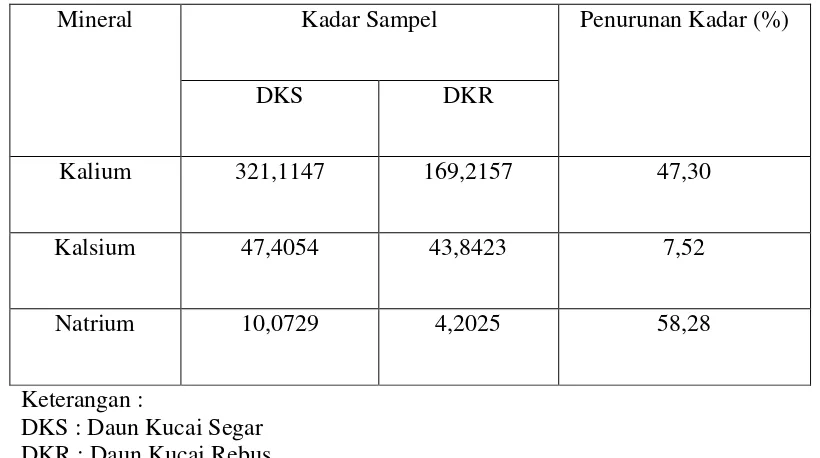
Tabel 4.5 Hasil Penurunan Kadar Kalium, Kalsium, dan Natrium pada Daun Kucai Segar dan Daun Kucai Rebus
Mineral Kadar Sampel Penurunan Kadar (%)
DKS DKR
Kalium 321,1147 169,2157 47,30
Kalsium 47,4054 43,8423 7,52
Natrium 10,0729 4,2025 58,28
Keterangan :
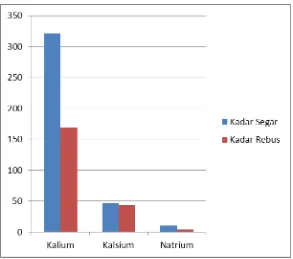
[image:49.595.103.513.469.698.2]Gambar 4.4 Grafik Penurunan Kadar Kalium, Kalsium dan Natrium
Tabel 4.6 Hasil Uji Beda Rata-rata Kadar Kalium, Kalsium, dan Natrium antar Sampel.
No Kadar Sampel t hitung t tabel Hasil
1 Kalium DKS
179,6618 2,2281 Beda
DKR
2 Kalsium DKS
11,1614 2,2281 Beda
DKR
3 Natrium DKS
180,0736 2,2281 Beda
DKR
Keterangan :
DKS : Daun Kucai Segar DKR : Daun Kucai Rebus
Berdasarkan Tabel 4.5 di atas dapat diketahui terdapat penurunan kadar
kalium, kalsium, dan natrium pada daun kucai segar dan rebus yang diperoleh
[image:50.595.109.517.415.614.2]Berdasarkan Tabel 3.5 di atas dapat diketahui bahwa kadar kalsium pada
daun kucai segar tidak jauh berbeda daripada kadar kalsium pada daun kucai yang
direbus dengan penurunan sebesar 7,52 %. Kadar kalsium dalam daun kucai segar
mengalami penurunan yang tidak terlalu jauh dengan daun kucai rebus karena
sifat kalsum oksalat yang merupakan bentuk kalsium yang terdapat pada daun
yang sukar larut dalam air, namun kadar tetap berkurang karena terjadinya
pelepasan kalsium karena proses pemanasan. Selanjutnya, kadar kalium dan
narium pada daun kucai segar jauh lebih besar dari kadar kalium dan natrium pada
daun kucai rebus karena sebagian besar kalium dan natrium pada daun terikat
dalam bentuk kalium oksalat dan natrium oksalat yang mudah larut dalam air (
Hoffmann, 2003.). Jadi, saat direbus maka kadar mineral kalium dan natrium yang
terdapat di dalamnya berkurang.
Pada tabel 4.6 dapat diketahui bahwa terdapat perbedaan yang signifikan
antara daun kucai segar dan daun kucai rebus. Hal ini disebabkan karena nilai t –
hitung jauh lebih besar dibandingkan nilai t – tabel.
4.2.3 Uji Perolehan Kembali ( Recovery)
Hasil uji perlolehan kembali (Recovery) kadar kalium, kalsium, dan
natrium setelah penambahan masing – masing larutan baku kalium, kalsium, dan
natrium dalam sampel dapat dilihat pada lampiran 19, Halaman 77 . Perhitungan
persen recovery kalium, kalsium, dan natrium dalam sampel dapat dilihat pada
Tabel 4.7 Persen Uji Recovery Kadar Kalium, Kalsium, dan Natrium.
No Mineral yang dianalisis Recovery (%) Syarat rentang recovery
(%)
1 Kalium 109,09
80-120
2 Kalsium 89,31
3 Natrium 92,23
Berdasarkan tabel di atas dapat dilihat bahwa rata-rata hasil uji perolhan
kembali (reovery) untuk kandungan kalium adalah 109,09%, untuk kalisum
adalah 89,31 % , dan untuk natrium adalah 92,23 %. Persen recovery tersebut
menunjukkan kcermatan kerja yang memuaskan pada saat pemeriksaan kadar
kalium, kadar kalsium, dan kadar natrium dalam sampel. Hasil uji perolehan
kembali (recovery) ini memenuhi persayaratan akurasi yang telah ditetapkan, jika
rata-rata hasil perolehan kembali (recovery) berada ada rentang 80-120% (Ermer
dan McB. Miller, 2005).
4.2.4 Simpangan Baku Relatif
Dari perhitungan yang dilakukan terhadap hasil pengukuran kadar mineral
kalium, kalsium, dan natrium pada daun kucai diperoleh nilai simpangan baku
Tabel 4.8 Hasil Perhitungan Simpangan Baku Relatif (RSD)
No Mineral Sampel Simpangan Baku Relatif (RSD)
1 Kalium 7,48 %
2 Kalsium 6,86 %
3 Natrium 0,76 %
Menurut Harmita (2004), nilai simpangan baku relatif (RSD) untuk analit
dengan kadar part per million (ppm) RSDnya adalah 16%. Dari hasil yang
diperoleh dapat dilihat bahwa metode yang telah dilakukan memiliki presisi yang
baik. Hasil perhitungan dapat dilihat pada Lampiran 21 Halaman 81 sampai
Halaman 83.
4.2.5 Batas Dekteksi dan Batas Kuantisasi
Berdasarkan data kurva kalibrasi kalium, kalsium, dan natrium diperoleh
batas deteksi dan batas kuantisasi untuk ketiga mineral dapat dilihat pada Tabel
[image:53.595.108.516.586.758.2]4.9
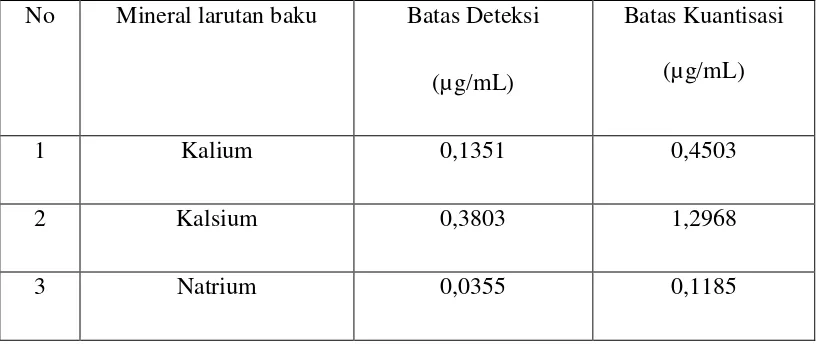
Tabel 4.9 Hasil Perhitungan Batas Dekteksi dan Batas Kuantisasi
No Mineral larutan baku Batas Deteksi
(µg/mL)
Batas Kuantisasi
(µg/mL)
1 Kalium 0,1351 0,4503
2 Kalsium 0,3803 1,2968
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh
pada pengukuran sampel berada di atas batas deteksi dan batas kuantisasi .
Perhitungan batas deteksi dan kuantisasi dapat dilihat pada Lampiran 7 Halaman
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan1. Hasil penetapan kadar kalium, kalsium, natrium secara spektrofotometri
serapan atom menunjukkan adanya perbedaan kadar kalium, kalsium, dan
natrium pada daun kucai segar dan daun kucai rebus. Hasil penelitian
menunjukkan kadar kalium pada daun kucai segar sebesar (321,1147 ±
0,9891) mg/100 g dan pada daun kucai rebus sebesar (169,2157 ± 1,9352)
mg/100 g. Kadar kalsium pada daun kucai segar sebesar (47,4054 ±
0,7960) mg/100 g dan pada daun kucai rebus sebesar (43,8424 ± 0,1995)
mg/100 g. Kadar natrium pada daun kucai segar sebesar (10,0729 ±
0,0619) mg/100 g sedangkan pada daun kucai rebus sebesar (4,2025 ±
0,0564) mg/100 g.
2. Hasil uji statistik yaitu uji beda rata-rata kadar mineral antara daun kucai
segar dan rebus, menyimpulkan bahwa terdapat perbedaan yang signifikan
kadar kalium, kalsium, dan natrium antara daun kucai segar dan rebus
dengan tingkat kepercayaan 95%.
5.2 Saran
1. Disarankan kepada peneliti selanjutnya untuk meneliti mineral fosfor, besi,
mangan, seng, dan magnesium yang terdapat dalam daun kucai.
2. Disarankan kepada masyarakat apabila tidak begitu menyukai aroma daun
DAFTAR PUSTAKA
Almatsier, S. (2013). Prinsip Dasar Ilmu Gizi. Cetakan Kesembilan.Jakarta: PT.
Gramedia Pustaka Utama. Hal. 230, 233, 236.
Amalia, L., Sukandar, E.Y., Roesli, R.M.A., dan Sigit, J.I. (2008). The Effect of
Ethanol Extract of Kucai (Allium schoenoprasum L.) Bulbs on Serum
Nitric Oxide Level in Male Wistar Rats. Internasional Journal of
Pharmacology. 4(6): 487.
Andarwulan, N., dan Faradilla, R.H.F. (2012). Sayuran Fenolik Pada Beberapa
Sayuran Indigenous Dari Indonesia. Bogor: SEAFAST Center, IPB. Hal. 57-60.
Anonim. (2014).Flame Atomic Absorption Spectroscopy. Diakses tanggal 27
Mei 2015. http://www.fisica.unam.mx/liquids/atomic_absorption.php
Arikunto, S. (2013). Prosedur Penelitian : Suatu Pendekatan Praktek. Jakarta :
Rineka Cipta. Hal. 113-114.
Badan POM RI. (2008). Acuan Sediaan Herbal. Volume keempat. Edisi pertama.
Jakarta: Badan Pengawas Obat dan Makanan Republik Indonesia. Hal. 42-43.
Ermer, J. dan McB. Miller, J. H. (2005). Method Validation in Pharmaceutical
Analysis. A Guide to Best Practice. Weinheim: Wiley–Vch Verlag Gmbh & Co. KGaA. Hal. 171.
Fidrianny, I., Kosasih, P., Soediro, S., dan Elin, Y. (2003). Efek Antihipertensi dan hipotensi Beberapa Fraksi dari Ekstrak Etanol Umbi Lapis Kucai
(Allium schoenoprasum L., Liliaceae). Jurnal Matematika dan Sains.
8(4): 147-150.
Gandjar, I. G. dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Pertama.
Yogyakarta: Pustaka Pelajar. Hal. 18, 22-23, 298-322.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara
Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3):
117-135.
Helrich, K. (1990). Official Methods of the Association of Official Analytical
Chemist. Edisi kelimabelas. Virginia: AOAC International. Hal. 42.
Hoffmann, D. (2003). Medicail Herbalism: The Science and Practice of Herbal
Isaac, R.A. (1988). Metal in Plants: Atomic Absorption Spectrophotometric Method. Disunting Oleh: Helrich, K. (1990). Official Method of Analysis of the association of official of chemist. Edisi Kelima belas. Virginia: AOAC Internasional. Hal. 42.
Khopkar, S.M. (1985). Basic Concepts of Analitytical Chemistry. Penerjemah: A. Saptorahajo (1990). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Hal. 275.
Koplik, R. (2014). Atomic Spectrometry. Diunduh dari
Lalage, Z. (2013). Khasiat Selangit 101 Buah & Sayur. Klaten: Galmas Publisher.
Hal. 43.
Pinzon, A. M., Castilo, B., dan Londono, M.T., (2013). Characterization of The
Mechanical Properties of Chives ( Allium schoenoprasum L.).Agronomia
Colombiana. 31(1): 83-88.
Rohman, A., Harsojo, Raharjo, T.J., Sismindari, Triyana, K., dan Astuti, P.
(2012). Analisis Makanan Dan Lingkungan Secara Fisika-Kimia. Cetakan
I. Yogyakarta: Pustaka Pelajar. Hal. 26.
Sudjana. (2013). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Hal.
168-254.
United States Department of Agriculture. (2015). Chive. Diunduh dari
2015.
Vogel, A.I. (1979). Textbook of Macro and Semimacro Qualitative Inorganic
Lampiran 1. Gambar Kucai
Lampiran 2. Bagan Alir Proses Destruksi Kering
Kucai
Dicuci bersih
Ditiriskan dan dipotong kecil-kecil
Sampel yang telah dipotong
Ditimbang seksama sebanyak 25 g di atas
kurs
Diarangkan di atas hot plate selama 2 jam
Diabukan di dalam tanur dengan
temperatur awal 100OC dan perlahan –
lahan temperatur dinaikkan hingga suhu
500oC dengan interval 25oC setiap 5 menit
Lampiran 3. Bagan Alir Pembuatan Larutan Sampel
Sampel yang telah
did k i
Dilarutkan dalam 5 mL HNO3 (1:1)
Dipindahkan ke dalam labu tentukur 100 mL
Dibilas kurs porselen sebanyak tiga kali dengan
akuademineralisata dan dicukupkan dengan akua
demineralisata hingga garis tanda
Filtrat
Dimasukkan ke dalam botol
Larutan Sampel
Dilakukan analisis kualitatif dan kuantitatif dengan
Spektrofotometer Serapan Atom pada λ 766,5 nm untu
kadar kalium, pada λ 422,7 nm untuk kadar kalsium, dan
pada λ 589,0 nm untuk kadar natrium
Lampiran 4. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No Konsentrasi (µg/mL)
(X)
Absorbansi (Y)
1 0,0000 -0,0001
2 2,0000 0,0845
3 4,0000 0,1684
4 6,0000 0,2482
5 8,0000 0,3322
6 10,0000 0,4112
No X Y XY X2 Y2
1 0,0000 -0,0001 0,0000 0,0000 0,0000
2 2,0000 0,0845 0,1690 4,0000 0,0071
3 4,0000 0,1684 0,6736 16,0000 0,0284
4 6,0000 0,2482 1,4892 25,0000 0,0616
5 8,0000 0,3322 2,6576 64,0000 0,1104
6 10,0000 0,4112 4,1120 100,0000 0,1691
∑ 30,0000
=5,0000
1,2444 =0,2704
9,1014 220,0000 0,3766
a =
=
= 0,04113
= a + b
b = - a
= 0,2074 - (0,04113)(5)
Maka persamaan garis regresinya adalah Y = 0,04113 X + 0,00175
r =
=
=
Lampiran 5. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No Konsentrasi (µg/mL)
(X)
Absorbansi (Y)
1 0,0000 -0,0002
2 2,0000 0,0812
3 4,0000 0,1472
4 6,0000 0,2121
5 8,0000 0,2879
6 10,0000 0,3552
No X Y XY X2 Y2
1 0,0000 -0,0002 0,0000 0,0000 0,0000
2 2,0000 0,0812 0,1624 4,0000 0,0066
3 4,0000 0,1472 0,5888 16,0000 0,0217
4 6,0000 0,2121 1,2726 25,0000 0,0450
5 8,0000 0,2879 2,3032 64,0000 0,0829
6 10,0000 0,3552 3,552 100,0000 0,1692
∑ 30,0000
=5,0000
1,0834 =0,1806
7,8790 220,0000 0,2824
a =
=
= 0,03517
= a + b
b = - a
= 0,1806 - (0,03517)(5,0000)
Maka persamaan garis regresinya adalah Y = 0,03517 X + 0,004717
r =
=
=
Lampiran 6. Data Kalibrasi Natrium dengan Spektrofotometer Serapan Atom Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No Konsentrasi (µg/mL)
(X)
Absorbansi (Y)
1 0,0000 -0,0005
2 0,2000 0,0206
3 0,4000 0,0416
4 0,6000 0,0633
5 0,8000 0,0808
6 1,0000 0,1041
No X Y XY X2 Y2
1 0,0000 -0,0005 0,0000 0,0000 0,0000
2 0,2000 0,0206 0,00412 0,0400 0,0004
3 0,4000 0,0416 0,01664 0,1600 0,0017
4 0,6000 0,0633 0,03798 0,2500 0,0040