PEMURNIAN ALKALI DAN KRISTALISASI SUHU RENDAH
DARI MINYAK IKAN HASIL SAMPING PENGALENGAN
MACKEREL (Scomber japonicus)
IKLIL FUADI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis yang berjudul “Pemurnian Alkali dan Kristalisasi Suhu Rendah dari Minyak Ikan Hasil Samping Pengalengan Mackerel (Scomber japonicus)” adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau kutipan dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Februari 2015
Iklil Fuadi
Hasil Samping Pengalengan Mackerel (Scomber japonicus). Dibimbing oleh SUGENG HERI SUSENO dan BUSTAMI IBRAHIM.
Minyak ikan hasil samping pengalengan mackerel merupakan sumber omega-3 yang potensial namun belum banyak dimanfaatkan. Minyak yang dihasilkan berkualitas rendah untuk pakan karena penggunaan suhu tinggi pada proses pre-cooking sehingga perlu ditingkatkan mutunya agar mempunyai nilai tambah dan mengurangi ketergantungan terhadap impor minyak ikan. Pemurnian perlu dilakukan untuk mendapatkan minyak ikan dengan kualitas yang lebih baik sehingga layak untuk dikonsumsi. Tujuan dari penelitian ini adalah mengkarakterisasi dan meningkatkan mutu minyak ikan hasil samping pengalengan mackerel dengan pemurnian alkali menggunakan NaOH kemudian diuji stabilitasnya dengan dan tanpa penambahan antioksidan selama penyimpanan dan pembuatan konsentrat omega-3 dengan metode kristalisasi suhu rendah.
Hasil pengukuran proksimat menunjukkan bahwa ikan mackerel termasuk ikan berlemak tinggi dengan kadar lemak 9,93±0,77%. Minyak mackerel memiliki kadar EPA dan DHA masing-masing 7,31% dan 19,22% dengan nilai asam lemak bebas (FFA) 4%, bilangan asam (AV) 7,95 mgKOH/g, bilangan peroksida (PV) 6,27 meq/kg, bilangan anisidin (AnV) 11,12 meq/kg, nilai total oksidasi (totoks) 23,65 meq/kg dan bilangan iod 197,96. Pengujian logam berat daging mackerel, minyak kasar dan minyak hasil refining diperoleh hasil dibawah batas standar IFOS ≤ 0,1 ppm.
Perlakuan pemurnian alkali terpilih adalah berdasarkan 16 oBe dengan nilai FFA 0,38%, AV 0,75 mgKOH/g, PV 4,93 meq/kg, AnV 10,39 meq/kg dan nilai total oksidasi 20,26 meq/kg. Penambahan antioksidan BHT 200 ppm pada minyak hasil refining mampu menghambat laju oksidasi hingga 3 minggu pada suhu ruang. Pemurnian alkali dapat meningkatkan persentase kandungan total asam lemak masing-masing 5,55% hingga 9,2% dan penyimpanan minyak 6,22% hingga 10,01%.
Kristalisasi suhu rendah menggunakan aseton mempunyai nilai iod tertinggi yaitu 305,83 dan kandungan omega-3 EPA 10,63 dan DHA 27,14 serta nilai total oksidasi terendah dibanding pelarut lain. Kristalisasi suhu rendah menggunakan aseton dapat meningkatkan pengayaan kandungan omega-3 hingga 1,27 kali dibanding minyak kasar (awal) menjadi 39,28%. .
Mackerel (Scomber japonicus) Oil Canning Byproduct. Supervised by SUGENG HERI SUSENO and BUSTAMI IBRAHIM.
Fish oil from mackerel canning byproduct is a potential source of omega-3 but has not been fully utilized. Oil quality parameter showed a crude oil with feed quality due to the use of high temperatures on pre-cooking process. The crude oil need to be upgrade, to get higher value compared to imported oil. Purification required to increase the oil quality so it can be used as human food. The purpose of this study was to characterize and improve the quality of mackerel oil using alkali refining with NaOH for stability test with antioxidant addition during storage and omega-3 concentrate production using low-temperature crystallization.
Mackerel are categorized as a high fat fish with a fat content 9.93%. Mackerel crude oil had high levels of EPA and DHA, 7.31% and 19.22%, respectively. The value of free fatty acids (FFA) were 4%, acid value (AV) 7.95 mg KOH/g, peroxide value (PV) 6.27 meq/kg, anisidine value (AnV) 11.12 meq/kg total oxidation value (totox) 23.65 meq/kg and iodine value 197.96. The heavy metals content of meat, crude oil and refining mackerel oil obtained were safe as regulate by IFOS standard ≤ 0.1 ppm.
The purification treatment selected by alkali refining with NaOH was according to 16 oBe with FFA 0.38%, AV 0.75 mgKOH/g, PV 4.93 meq/kg, AnV 10.39 meq/kg and totox 20.26 meq/kg. The refining oil that added BHT 200 ppm was able to inhibit oxidation rate for 3 weeks than refining oil without BHT and crude oil, during storage. Alkali refining showed an increase total fatty acid 5.55% to 9.2%than crude oiland storaging 6.22% to 10.01%.
Low-temperature crystallization with acetone had the highest iodine value 305.83 and omega-3 content (EPA 10.63 and DHA 27.14 respectively)and lowest oxidation parameter than n-hexane and isopropyl alcohol. Low-temperature crystallization with acetone could enrich omega-3 content to 1.27 times than crude oil (39.28%).
©
Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
MACKEREL (Scomber japonicus)
IKLIL FUADI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Teknologi Hasil Perairan
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
NIM : Program Studi :
Disetujui oleh
Komisi Pembimbing
Diketahui oleh
Tanggal Ujian: 25 November 2014 Tanggal Lulus: C351124021
Teknologi Hasil Perairan
Dr Sugeng Heri Suseno, SPi MSi Ketua
Dr Ir Bustami Ibrahim, MSc Anggota
Ketua Program Studi Teknologi Hasil Perairan
Dr Ir Wini Trilaksani, MSc
Dekan Sekolah Pascasarjana
rahmat dan karunia-Nya sehingga tesis dengan judul Pemurnian Alkali dan Kristalisasi Suhu Rendah dari Minyak Ikan Hasil Samping Pengalengan Mackerel (Scomber japonicus)ini dapat diselesaikan.
Keberhasilan penulis mengikuti pendidikan di Sekolah Pascasarjana IPB tidak lepas dari dukungan berbagai pihak. Penulis menyampaikan banyak terimakasih yang setulusnya kepada:
1 Dr Sugeng Heri Suseno, SPi MSi. Selaku ketua komisi pembimbing dan Dr Ir Bustami Ibrahim, MSc sebagai anggota komisi pembimbing atas kesediaan waktu untuk membimbing, memberikan arahan dan masukan selama penulisan dan penyusunan tesis ini.
2 Manajemen PT Maya Food Industries atas bantuan bahan baku penelitian minyak ikan mackerel.
3 Keluarga besar penulis, bapak H M. Rofiq, ibu Hj Sri Handayani, istri Nur Isnaini Trisnawati dan ananda tercinta Hafshoh Hafidhotul Hasna’ atas motivasi, doa, semangat dan dukungan baik moril maupun materiil selama penulis menempuh studi.
4 Teman-teman tim minyak ikan Titot Bagus Arifianto, Boyke Raymond Toisutta, Patricia Lavrina PK, Yosephina MJ Batafor, Jeny Ernawati Tambunan, I Wayan Kukuh, La Ode Huli dan Septina Mugi Rahayu.
5 Teman-teman Pasca THP 2011, 2012 dan 2013 atas kerjasama yang baik selama studi.
6 Teman-teman dan semua pihak yang telah membantu tersusunnya tesis ini
Penulis menyadari bahwa tesis ini masih ada kekurangan. Semoga karya ilmiah ini membawa manfaat bagi seluruh civitas IPB khususnya dan masyarakat Indonesia umumnya.
Bogor, Februari 2015
DAFTAR GAMBAR
2 KARAKTERISASI MINYAK IKAN HASIL SAMPING PENGALENGAN MACKEREL (Scomber japonicus) Pendahuluan
Bahan dan Metode Hasil dan Pembahasan Simpulan
3 PEMURNIAN ALKALI MINYAK IKAN HASIL SAMPING PENGALENGAN MACKEREL (Scomber japonicus)
Pendahuluan Bahan dan Metode Analisis Data
Hasil dan Pembahasan Simpulan
4 STABILITAS MINYAK MACKEREL DENGAN ATAU TANPA ANTIOKSIDAN BHT SELAMA PENYIMPANAN SUHU
RUANG
13
13 15
16
26 27 28
39 52
53 1 Persentase kandungan gizi daging mackerel
2 Kandungan logam berat daging dan minyak hasil samping pengalengan mackerel
3 Profil asam lemak minyak ikan hasil samping pengalengan mackerel 4 Hasil pengamatan asam lemak bebas dan parameter oksidasi minyak
hasil samping pengalengan mackerel
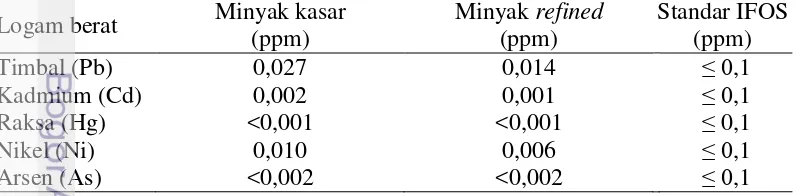
5 Kandungan logam berat minyak kasar dan minyak refined hasil samping pengalengan mackerel
6 Profil asam lemak minyak kasar dan refined
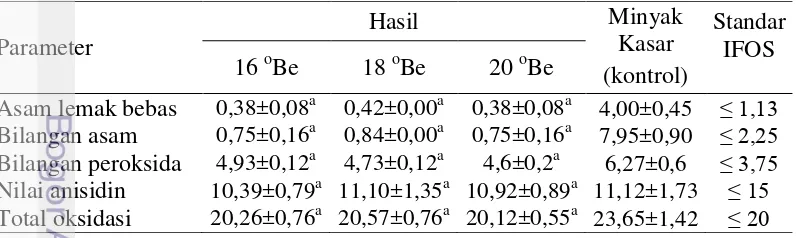
7 Hasil pengamatan parameter oksidasi minyak ikan mackerel 8 Profil asam lemak minyak ikan hasil pemurnian dan penyimpanan
selama 4 minggu (% w/w)
9 Profil asam lemak minyak ikan dan konsentrat omega-3 (% w/w) 10 Hasil pengamatan FFA, parameter oksidasi (PV, AnV, Totoks) dan
4 1 Road map penelitian
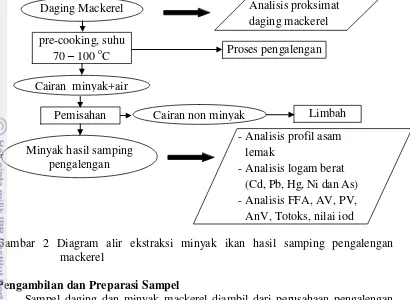
2 Diagram alir ekstraksi minyak ikan hasil samping pengalengan mackerel
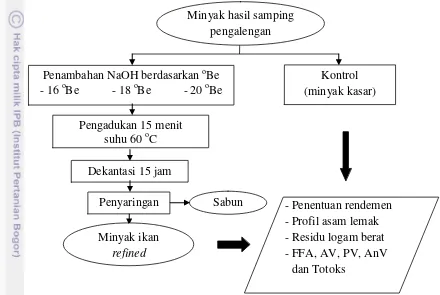
3 Diagram alir pemurnian alkali minyak ikan hasil samping pengalengan mackerel (modifikasi metode Irianto (1992))
4 Histogram rendemen minyak hasil pemurnian alkali 5 Reaksi penyabunan (Ketaren 1986)
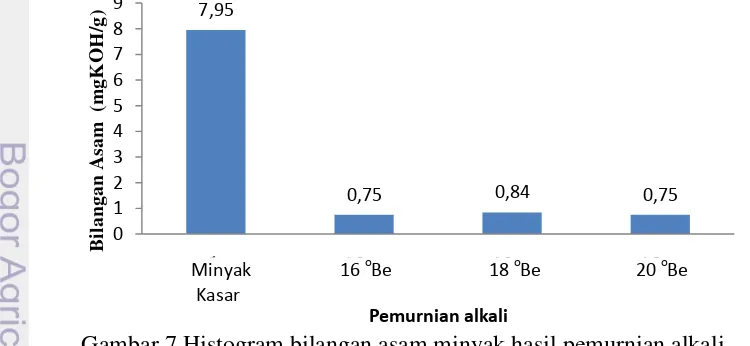
6 Histogram nilai asam lemak bebas minyak hasil pemurnian alkali 7 Histogram bilangan asam minyak hasil pemurnian alkali
8 Histogram bilangan peroksida minyak hasil pemurnian alkali 9 Histogram nilai anisidin minyak hasil pemurnian alkali 10 Histogram nilai total oksidasi minyak hasil pemurnian alkali 11 Digram alir pengujian stabilitas minyak ikan selama penyimpanan
(modifikasi metode Ansorena dan Astiasaran (2004)) 12 Grafik nilai asam lemak bebas minyak selama penyimpanan 13 Grafik bilangan asam minyak selama penyimpanan
14 Grafik nilai peroksida minyak selama penyimpanan 15 Grafik nilai anisidin minyak selama penyimpanan 16 Grafik nilai total oksidasi minyak selama penyimpanan
17 Diagram alir pembuatan konsentrat omega-3 metode kristalisasi pelarut suhu rendah (modifikasi metode Wanasundara (1996)) 18 Histogram nilai asam lemak bebas minyak dan konsentrat omega-3 19 Histogram bilangan asam minyak dan konsentrat omega-3
1 Perhitungan hasil analisi logam berat minyak mackerel kasar (crude) dan minyak mackerel refined
2 Kromatogram dari hasil Gas Chromatography minyak hasil samping pengalengan mackerel kasar (awal)
3 Kromatogram dari hasil Gas Chromatography minyak hasil refining
tanpa BHT (awal)
4 Kromatogram dari hasil Gas Chromatography minyak hasil refining
dengan BHT (awal)
5 Kromatogram dari hasil Gas Chromatography minyak hasil samping pengalengan mackerel kasar (penyimpanan 4 minggu)
6 Kromatogram dari hasil Gas Chromatography minyak hasil refining
tanpa BHT (penyimpanan 4 minggu)
7 Kromatogram dari hasil Gas Chromatography minyak hasil refining
dengan BHT (penyimpanan 4 minggu)
8 Kromatogram dari hasil Gas Chromatography konsentrat minyak mackerel dengan pelarut Iso Propil Alkohol
9 Kromatogram dari hasil Gas Chromatography konsentrat minyak mackerel dengan pelarut n-Heksan
10 Kromatogram dari hasil Gas Chromatography konsentrat minyak mackerel dengan pelarut Aseton
11 Konsentrasi NaOH dengan berbagai derajat Baumé (Hodgson 1995) 12 Analysis of Variance (ANOVA) konsentrasi NaOH berdasarkan
derajat baume (oBe) terhadap nilai free fatty acid (FFA) 13 Uji lanjut Duncanfree fatty acid (FFA)
14 Analysis of Variance (ANOVA) konsentrasi NaOH berdasarkan derajat baume (oBe) terhadap acid value (AV)
15 Uji lanjut Duncanacid value (AV)
16 Analysis of Variance (ANOVA) konsentrasi NaOH berdasarkan derajat baume (oBe) terhadap peroxide value (PV)
17 Uji lanjut Duncanperoxide value (PV)
18 Analysis of Variance (ANOVA) konsentrasi NaOH berdasarkan derajat baume (oBe) terhadap anisidine value (AnV)
19 Uji lanjut Duncananisidine value (AnV)
20 Analysis of Variance (ANOVA) konsentrasi NaOH berdasarkan derajat baume (oBe) terhadap nilai total oksidasi (totox)
21 lanjut Duncan nilai total oksidasi (totox)
22 Analysis of Variance (ANOVA) konsentrasi NaOH berdasarkan derajat baume (oBe) terhadap rendemen
23 Uji lanjut Duncan nilai rendemen
24 Analysis of Variance (ANOVA) penggunaan antioksidan dan waktu penyimpanan terhadap nilai free fatty acid (FFA)
25 Uji lanjut Duncan nilai FFA penggunaan antioksidan 26 Uji lanjut Duncan nilai FFA waktu penyimpanan
27 Analysis of Variance (ANOVA) penggunaan antioksidan dan waktu penyimpanan terhadap acid value
28 Uji lanjut Duncanacid value penggunaan antioksidan
29 Uji lanjut waktu penyimpanan
30 Analysis of Variance (ANOVA) penggunaan antioksidan dan waktu penyimpanan terhadap peroxide value (PV)
31 Uji lanjut Duncanperoxide value penggunaan antioksidan 32 Uji lanjut Duncanperoxide value waktu penyimpanan
33 Analysis of Variance (ANOVA) penggunaan antioksidan dan waktu penyimpanan terhadap anisidine value (AnV)
34 Uji lanjut Duncananisidine value penggunaan antioksidan 35 Uji lanjut Duncananisidine value waktu penyimpanan
36 Analysis of Variance (ANOVA) penggunaan antioksidan dan waktu penyimpanan terhadap nilai total oksidasi (totox)
37 Uji lanjut Duncan nilai total oksidasi penggunaan antioksidan 38 Uji lanjut Duncan nilai total oksidasi waktu penyimpanan
39 Analysis of Variance (ANOVA) jenis pelarut terhadap nilai free fatty acid (FFA)
40 Uji lanjut Duncanfree fatty acid (FFA)
41 Analysis of Variance (ANOVA) jenis pelarut terhadap acid value
(AV)
42 Uji lanjut Duncanacid value (AV)
43 Analysis of Variance (ANOVA) jenis pelarut terhadap peroxide value
(PV)
44 Uji lanjut Duncanperoxide value (PV)
45 Analysis of Variance (ANOVA) jenis pelarut terhadap anisidine value
(AnV)
46 Uji lanjut Duncananisidine value (AnV)
47 Analysis of Variance (ANOVA) jenis pelarut terhadap nilai total oksidasi (totox)
48 Uji lanjut Duncan nilai total oksidasi (totox)
1 PENDAHULAN
Latar Belakang
Pengalengan ikan merupakan salah satu industri modern sektor kelautan dan perikanan dengan volume terbesar kedua setelah pembekuan. Bahan baku industri pengalengan ikan di Indonesia didominasi ikan-ikan pelagis kecil seperti mackerel dan sardin dengan volume produksi bulan Januari-Agustus 2012 sebesar 272.177.060 kg (Ditjen P2HP 2012). Berdasarkan data KKP (2012), impor komoditi mackerel mengalami kenaikan selama tahun 2007-2011 yaitu 25.872.116 - 93.789.155 kg. Proses pengalengan selain menghasilkan hasil samping padatan juga cairan minyak dalam jumlah besar. Pada tahap pre-cooking, daging akan mengeluarkan cairan minyak bercampur air. Cairan tersebut ditiriskan dan ditampung dalam bak untuk dipisahkan antara minyak dengan air. Minyak yang dihasilkan dilabel minyak sardin, meskipun volume produksi lebih besar ikan mackerel yaitu rata-rata hingga 20 ton daging/hari di PT MFI Pekalongan. Berdasarkan jumlah tersebut dapat menghasilkan minyak hasil samping pengalengan mackerel sebesar 100 kg (0,5% b/b).
Kajian tentang minyak dari ikan mackerel belum banyak dilakukan. Hal ini dikarenakan proses pengalengan mackerel berdampingan dengan pengalengan sardin sehingga pengolahan hasil sampingnya berada dalam satu unit. Minyak yang dihasilkan masih berupa minyak kasar kualitas pakan karena penggunaan suhu tinggi pada proses pre-cooking. Suseno et al. (2011), menjelaskan bahwa kualitas minyak hasil samping masih rendah untuk pakan belum layak untuk konsumsi manusia. Pemurnian perlu dilakukan untuk mendapatkan minyak ikan dengan kualitas yang lebih baik sehingga layak untuk dikonsumsi. Menurut Estiasih dan Ahmadi (2004), minyak hasil samping pengalengan masih mengandung bahan non minyak sehingga perlu dimurnikan. Pemurnian alkali dapat menghilangkan kotoran dengan mekanisme fraksi tersabunkan mengabsorpsi alkali dan terkoagulasi oleh proses hidrasi.
Kualitas minyak ikan dipengaruhi tingkat oksidasi yang terjadi. Minyak ikan mudah mengalami oksidasi selama penyimpanan, sehingga perlu ditambah antioksidan. Antioksidan Butylated Hydroxytoluene (BHT) dikenal sebagai antioksidan untuk lemak dan minyak karena memiliki kemampuan antioksidan yang baik dan ekonomis. Antioksidan BHT biasa digunakan sebagai food additive
untuk mencegah ketengikan (Iqbal dan Bhanger 2005). Antioksidan BHT lebih efektif dan murah dibanding antioksidan alami (Suja et al. 2004). Batas maksimum BHT untuk produk lemak dan minyak yang diperbolehkan di Indonesia yaitu 200 ppm (BPOM 2013).
Pemanfaatan minyak ikan hasil samping pengalengan mackerel berpotensi digunakan sebagai sumber omega-3. Minyak ikan dari famili Scombroidae, Clupeidae dan Salmonidae mengandung Eicosapentaenoic Acid (EPA) dan
omega-3 mampu mencegah penyakit kardiovaskuler serta membantu perkembangan otak dan retina mata pada bayi.
Konsumsi dalam bentuk konsentrat lebih baik dibandingkan minyak asli karena menjaga asupan lemak total tetap rendah. Konsentrat omega-3 yang dihasilkan mempunyai bentuk yang berbeda tergantung teknik yang digunakan. Teknik kristalisasi suhu rendah dipilih karena konsentrat asam lemak omega-3 yang didapat berbentuk trigliserida. Menurut Nettleton (1995), bentuk trigliserida lebih stabil dibanding bentuk asam lemak bebas dan lebih mudah diserap tubuh dibandingkan bentuk metil ester asam lemak. Shahidi dan Wanasundara (1998) menjelaskan, kristalisasi suhu rendah digunakan untuk memisahkan bentuk trigliserida, asam lemak, ester dan lemak lainnya yang mempunyai kelarutan tinggi pada pelarut organik pada suhu dibawah 0 oC. Kelarutan asam lemak dan ester dalam pelarut mempunyai ketetapan yaitu lemak jenuh kurang larut dibanding lemak monoenoic dan dienoic pada panjang rantai yang sama, isomer
trans kurang larut dibanding isomer cis dan lemak rantai lurus kurang larut dibanding rantai bercabang.
Pada penelitian ini akan dibahas potensi minyak ikan hasil samping pengalengan mackerel sebagai sumber asam lemak omega-3. Minyak ikan dikarakterisasi dan dimurnikan dengan alkali selanjutnya dilakukan pengkonsentrasian sehingga diharapkan menghasilkan konsentrat omega-3 yang memenuhi standar dan layak dikonsumsi sebagai suplemen atau bahan tambahan pangan untuk mengurangi ketergantungan terhadap impor minyak ikan.
Permasalahan
Tujuan Tujuan dari penelitian ini adalah:
1 Menentukan karakteristik minyak ikan hasil samping pengalengan mackerel. 2 Memilih konsentrasi larutan NaOH berdasarkan oBe yang terbaik terhadap
rendemen dan kualitas minyak hasil refining.
3 Menentukan kualitas dan stabilitas minyak ikan hasil refining dengan atau tanpa penambahan antioksidan selama penyimpanan.
4 Memilih pelarut terbaik pada pembuatan konsentrat omega-3 minyak ikan hasil
refining metode kristalisasi suhu rendah.
Manfaat Penelitian Manfaat dari penelitian ini antara lain mengetahui:
1 Kandungan gizi, residu logam berat, kualitas dan profil asam lemak dari minyak hasil samping pengalengan ikan mackerel.
2 Jumlah dan konsentrasi NaOH yang dibutuhkan untuk pemurnian alkali minyak hasil samping pengalengan ikan mackerel.
3 Profil asam lemak, nilai asam lemak bebas, peroksida, anisidin serta total oksidasi minyak hasil refining selama penyimpanan.
4 Pelarut terbaik pada produksi omega-3 dengan metode kristalisasi suhu rendah.
Ruang Lingkup Penelitian
1 Mengkarakterisasi minyak hasil samping pengalengan ikan mackerel yang terdiri dari analisis proksimat bahan baku daging mackerel, analisis asam lemak bebas, analisis parameter oksidasi, kandungan logam berat dan analisis profil asam lemak.
2 Melakukan pemurnian alkali dengan NaOH berdasarkan nilai asam lemak bebas minyak ikan.
3 Melakukan penyimpanan minyak dalam bentuk kasar dan refined (tanpa BHT atau dengan BHT) dan lama penyimpanan (0, 1, 2, 3 dan 4 minggu).
4 Melakukan produksi konsentrat omega-3 metode kristalisasi suhu rendah dengan pelarut yang berbeda (Aseton, n-Heksan dan Iso Propil Alkohol).
Hipotesis
Hipotesis yang akan diajukan dalam penelitian ini adalah sebagai berikut: 1 Penggunaan konsentrasi NaOH yang berbeda pada pemurnian alkali memberikan
pengaruh terhadap kualitas minyak ikan.
2 Penggunaan antioksidan dan waktu penyimpanan memberikan pengaruh terhadap kualitas dan stabilitas minyak ikan.
Road map mengenai kajian literatur penelitian minyak ikan yang telah ada dan perkembangan penelitian yang telah dilakukan dapat dilihat pada Gambar 1.
2 KARAKTERISASI MINYAK IKAN HASIL SAMPING
PENGALENGAN MACKEREL (Scomber japonicus)
Pendahuluan Latar belakang
Ikan mackerel (Scomber japonicus Houttuyn, 1782) merupakan ikan pelagis yang habitatnya berada di perairan tropis dan subtropis meliputi Samudra Atlantik, Hindia, Pasifik dan perairan sekitarnya. Ikan mackerel termasuk salah satu ikan berlemak yang hidup pada kedalaman antara 0 sampai 300 m, ikan ini kaya asam lemak tidak jenuh omega-3 seperti Eicosapentaenoic Acid (EPA, 20:5n-3) dan DocosahexaenoicAcid (DHA, 22:6n-3) (Bae dan Lim 2013). Negara di Asia yang menangkap mackerel terbesar yaitu China dan Jepang yaitu masing-masing 0,52 juta ton dan 0,47 juta ton (FAO 2012).
Pengalengan ikan, khususnya mackerel sangat diminati masyarakat, sehingga setiap tahun produksinya meningkat. Peningkatan produksi ini juga meningkatkan hasil samping yang berpotensi menghasilkan nilai tambah jika dikelola dengan baik. Pada tahapan pre-cooking proses pengalengan akan menghasilkan cairan minyak ikan yang bercampur dengan air dalam jumlah sedikit yang berasal dari daging yang dipanaskan. Cairan tersebut ditiriskan sebelum daging diisi saus. Cairan hasil penirisan ditampung dalam bak dan dipisahkan minyaknya dengan cara mengalirkan cairan pada lapisan atas yang berupa minyak ke bak lainnya. Minyak yang dihasilkan berkualitas rendah karena penggunaan suhu tinggi pada proses pre-cooking.
Minyak ikan yang diperoleh dari hasil samping industri umumnya melibatkan pemasakan bahan baku menggunakan panas, sehingga kualitasnya rendah. Produksi minyak ikan sangat potensial dan sudah banyak dilakukan, namun hanya sebagai produk samping sehingga kualitasnya sering diabaikan. Beberapa penelitian minyak ikan dari hasil samping yaitu Zuta et al. (2003) melakukan ekstraksi minyak ikan dari isi perut, daging dan kulit ikan mackerel menghasilkan rendemen minyak masing-masing 9,18%, 9,2% dan 38,1%. Chantachum etal. (2000) melakukan produksi minyak ikan dari kepala tuna pre-cooked dan non pre-cooked dengan rendemen 2,8% dan 4,8%. Aidos etal. (2002) menggunakan limbah ikan herring menghasilkan rendemen minyak 9,3%.
Berdasarkan karakteristik minyak sebagai hasil samping, maka minyak ikan hasil samping pengalengan mackerel mempunyai potensi untuk dikembangkan. Karakterisasi awal minyak ikan hasil samping pengalengan menjadi hal yang perlu dikaji untuk meningkatkan nilai tambah minyak hasil samping sebagai bahan pangan atau suplemen sumber omega-3.
Tujuan
Penelitian ini bertujuan untuk mengetahui karakteristik dari minyak ikan hasil samping pengalengan mackerel melalui analisis:
1 Proksimat dari bahan baku daging ikan mackerel.
4 Asam lemak bebas, bilangan asam, nilai peroksida, nilai anisidin total oksidasi (totoks) dan bilangan iod minyak ikan hasil samping pengalengan mackerel.
Bahan dan Metode Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Februari sampai Maret 2014. Tempat pelaksanaan penelitian karakterisasi minyak hasil samping pengalengan mackerel yaitu Laboratorium Pusat Rekayasa Pangan untuk pengujian proksimat; Laboratorium Peternakan untuk pengujian logam berat; Laboratorium Bahan Baku Hasil Perairan, Departemen Teknologi Hasil Perairan untuk preparasi sampel, pengujian asam lemak bebas, bilangan asam, bilangan peroksida dan total oksidasi; Laboratorium Terpadu Fakultas Peternakan untuk penggunaan spektrofotometer pada pengujian nilai anisidin; dan Laboratorium Terpadu Institut Pertanian Bogor untuk pengujian profil asam lemak.
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah daging ikan mackerel dan minyak hasil samping pengalengan mackerel dari PT Maya Food Industries Pekalongan. Bahan untuk pengujian parameter oksidasi minyak seperti kloroform, asam asetat glasial, ethanol, trimethylpentane, natrium thiosulfate 0,01 N, KOH 0,1 N, aquades, p-anisidine, phenolphtalein indicator, kalium iodide
(KI), kanji, pereaksi wijs, bahan-bahan untuk pengujian proksimat, logam berat dan standar pengujian profil asam lemak.
Alat-alat yang digunakan adalah jerigen, gelas ukur, beaker glass, erlenmeyer, labu takar, tabung reaksi, pipet, timbangan analitik, thermometer, penangas, panci, stopwatch, perangkat titrasi dan spektrofotometer merk Agilent 8453 untuk pengujian kualitas minyak ikan. Alat-alat yang digunakan untuk analisis proksimat antara lain oven, perangkat kjeldahl, soxlet, alat titrasi, cawan porselen, gegep, tanur, destilator. Alat-alat yang digunakan untuk analisa logam berat antara lain alat destruksi, labu destruksi, perangkat Atomic Absorption Spectrofotometer (AAS) dan perangkat kromatografi gas (gas chromatography) merek Shimadzu GC 2010 Plus untuk pengujian profil asam lemak.
Metode Penelitian
Gambar 2 Diagram alir ekstraksi minyak ikan hasil samping pengalengan mackerel
Pengambilan dan Preparasi Sampel
Sampel daging dan minyak mackerel diambil dari perusahaan pengalengan ikan di Pekalongan, Jawa Tengah, Indonesia. Sampel mackerel dicuci dengan air bersih kemudian dilakukan penyiangan untuk memisahkan antara kepala, daging dan isiperut, daging dihomogenisasi untuk analisis proksimat. Sampel minyak diambil dari hasil penirisan ikan kaleng setelah proses pre-cooking yang telah mengalami dekantasi sehingga terpisah dari sebagian pengotor dan komponen non minyak. Sampel minyak diambil dan dibawa menggunakan wadah kedap udara dan cahaya (jerigen).
Analisis Proksimat
Analisis proksimat merupakan suatu analisis yang dilakukan untuk mengetahui komposisi kimia suatu bahan, diantaranya:
Analisis kadar air (AOAC 2005)
Cawan porselen dikeringkan dalam oven pada suhu 105 oC selama 1 jam, selanjutnya cawan dimasukkan ke dalam desikator (kurang lebih 15 menit) dan dibiarkan sampai dingin kemudian ditimbang. Sebanyak 5 g contoh dimasukkan ke dalam cawan tersebut, kemudian dikeringkan dengan oven pada suhu 105 oC selama 5 jam atau hingga beratnya konstan, kemudian cawan tersebut dimasukkan ke dalam desikator dan dibiarkan sampai dingin dan ditimbang.
Perhitungan kadar air :
B - C B - A
Keterangan : A = Berat cawan kosong (g)
B = Berat cawan yang diisi dengan sampel (g)
C = Berat cawan dengan sampel yang sudah dikeringkan (g) Kadar air (%) = x 100%
Cairan minyak+air
Minyak hasil samping pengalengan pre-cooking, suhu
70 – 100 oC
- Analisis profil asam lemak
- Analisis logam berat (Cd, Pb, Hg, Ni dan As) - Analisis FFA, AV, PV, AnV, Totoks, nilai iod -
Analisis proksimat daging mackerel Daging Mackerel
Pemisahan Cairan non minyak
Proses pengalengan
Analisis kadar abu (AOAC 2005)
Cawan pengabuan dikeringkan di dalam oven pada suhu 105 oC selama 1 jam, didinginkan selama 15 menit di dalam desikator dan ditimbang hingga didapatkan berat yang konstan. Sampel sebanyak 5 g dimasukkan ke dalam cawan pengabuan dan dipijarkan di atas nyala api bunsen hingga tidak berasap, kemudian dimasukkan ke dalam tanur pengabuan dengan suhu 600 oC selama 1 jam, kemudian ditimbang hingga didapatkan berat yang konstan.
Kadar abu ditentukan dengan rumus: C - A B - A
Keterangan : A = Berat cawan porselen kosong (g) B = Berat cawan dengan sampel (g)
C = Berat cawan dengan sampel setelah dikeringkan (g)
Analisis kadar protein (AOAC 2005)
Pengukuran kadar protein dilakukan dengan metode mikro Kjeldahl. Sampel ditimbang sebanyak 0,25 g, kemudian dimasukkan ke dalam labu Kjeldahl 100 mL, lalu ditambahkan 0,25 g selenium dan 3 mL H2SO4 pekat. Contoh didestruksi pada suhu 410 oC selama kurang lebih 1 jam sampai larutan jernih lalu didinginkan. Setelah dingin, ke dalam labu Kjeldahl ditambahkan 50 mL akuades dan 20 mL NaOH 40%, kemudian dilakukan proses destilasi dengan suhu destilator 100 oC. Hasil destilasi ditampung dalam labu erlenmeyer 125 mL yang berisi campuran 10 mL asam borat (H3BO3) 2% dan 2 tetes indikator
bromcresol green-methyl red yang berwarna merah muda. Setelah volume destilat mencapai 40 mL dan berwarna hijau kebiruan, maka proses destilasi dihentikan. Lalu destilat dititrasi dengan HCl 0,1 N sampai terjadi perubahan warna merah muda. Volume titran dibaca dan dicatat. Larutan blanko dianalisis seperti contoh. Kadar protein dihitung dengan rumus sebagai berikut :
Kadar protein (%) = % N x faktor konversi
(mL HCl – mL blanko) x N HCl x 14,007 Mg contoh x faktor koreksi alat
Keterangan : Faktor konversi = 6,25 Faktor koreksi alat = 2,5%
Analisis kadar lemak (AOAC 2005)
Bobot sampel Keterangan : W1 = Berat sampel (g)
W2 = Berat labu lemak kosong (g) W3 = Berat labu lemak dengan lemak (g)
Analisis kadar karbohidrat (AOAC 2005)
Analisis karbohidrat dilakukan by difference, yaitu hasil pengurangan dari 100% dengan kadar air, kadar abu, kadar protein dan kadar lemak, sehingga kadar karbohidrat tergantung pada faktor pengurangannya. Hal ini karena karbohidrat sangat berpengaruh terhadap zat gizi lainnya.
Analisis kadar karbohidrat dapat dihitung dengan persamaan berikut:
Karbohidrat (%) = 100% - (kadar air + kadar abu + kadar lemak + kadar protein)
Analisis logam berat Cd, Pb, Hg, Ni dan As (AOAC 2005)
Analisis logam berat dilakukan dengan menimbang 1 g contoh ke dalam erlenmeyer, kemudian ditambahkan 5 mL HNO3 pekat dan 1 mL HClO4, didiamkan 24 jam. Sampel dipanaskan pada suhu 100 oC selama 1 jam 30 menit, kemudian ditingkatkan menjadi 130 oC selama 1 jam, kemudian suhu ditingkatkan lagi menjadi 150 oC selama 2 jam 30 menit (sampai uap kuning habis, bila masih ada uap kuning, waktu pemanasan ditambah lagi). Setelah uap kuning habis, suhu ditingkatkan menjadi 170 oC selama 1 jam, kemudian suhu ditingkatkan lagi menjadi 200 oC selama 1 jam (terbentuk uap putih). Destruksi selesai dengan terbentuknya endapan putih. Ekstrak didinginkan kemudian diencerkan dengan air bebas ion menjadi 10 mL, lalu dikocok.
Larutan baku kalibrasi persediaan As, Cd, Pb, Ni dan Hg disiapkan dengan konsentrasi masing-masing 1000 μg/mL. Larutan baku kalibrasi As dibuat dengan konsentrasi 5, 10, 20, 30 dan 50 μg/L dalam larutan asam nitrat 0,5 % v/v. Larutan baku kalibrasi Cd dibuat dengan konsentrasi 0,5; 1; 2; 3 dan 5 μg/L dalam larutan asam nitrat 0,5 % v/v. Larutan baku kalibrasi Pb dibuat dengan konsentrasi 5; 10; 20; 30 dan 50 μg/L dalam larutan asam nitrat 0,5% v/v. Larutan baku kalibrasi Ni dibuat dengan konsentrasi 5; 10; 20; 30 dan 50 μg/L dalam larutan asam nitrat 0,5% v/v. Larutan baku kalibrasi Hg dibuat dengan konsentrasi 0,5; 1; 2; 3 dan 5 μg/L dalam larutan asam klorida 3% v/v.
Larutan uji dibuat dengan metode digesti kering/pengabuan, yaitu dengan menimbang 2,5 g contoh, kemudian dimasukkan ke dalam cawan porselen dan ditambahkan 3 mL larutan MgNO3 50%. Larutan dikeringkan di atas penangas air, residu diabukan terlebih dahulu dalam mantel pemanas sampai tidak terdapat asap, kemudian dipanaskan dalam tanur pada suhu 500 oC selama 3 jam. Larutan didinginkan dan ditambahkan 25 mL larutan HCl 6 M, disaring ke dalam labu ukur 50 mL dan diencerkan dengan air sampai tanda. Pereaksi blanko dibuat seperti penyiapan larutan uji tetapi tanpa penambahan contoh.
Kurva kalibrasi didapatkan dengan cara disuntikkan larutan baku kalibrasi dan larutan modifier ke dalam alat AAS (rasio injeksi larutan baku dan modifier = 20 μL : 5 μL). Buat kurva antara respon (serapan atau tinggi puncak) dengan kadar dari masing-masing larutan baku. Hitung kadar As, Cd, Pb, Ni, Hg (μg/g) dalam contoh dengan persamaan garis regresi kurva kalibrasi, menggunakan rumus:
Konsentrasi logam dari kurva kalibrasi
Analisis profil asam lemak (AOAC 2005)
Metode analisis yang digunakan yaitu menggunakan prinsip mengubah asam lemak menjadi turunannya, yaitu metil ester sehingga dapat terdeteksi oleh alat kromatografi. Hasil analisis akan terekam dalam suatu lembaran yang terhubung dengan rekorder dan ditunjukkan melalui beberapa puncak pada waktu retensi tertentu sesuai dengan karakter masing-masing asam lemak dan dibandingkan dengan standar. Sebelum melakukan injeksi metil ester, dilakukan metilasi sehingga terbentuk metil ester dari masing-masing asam lemak.
Model alat kromatografi gas yang digunakan adalah Shimadzu GC 2010 Plus, gas yang digunakan sebagai fase bergerak adalah gas nitrogen dengan laju alir 30 mL/menit dan sebagai gas pembakar adalah hidrogen dan oksigen, kolom yang digunakan adalah capilary column merk Quadrex dengan diameter dalam 0,25 mm. Perangkat kromatografi gas (gas chromatography) yang digunakan dalam penelitian ini untuk analisis identifikasi asam lemak adalah Shimadzu GC 2010 Plus.
Sebanyak 20-40 mg contoh lemak atau minyak dimasukkan dalam tabung bertutup teflon dengan 1 mL NaOH dalam metanol dan dipanaskan dalam penangas air selama 20 menit, selanjutnya ditambahkan 2 mL BF3 20% dan 5 mg/mL standar internal ke dalam campuran, campuran dipanaskan lagi selama 20 menit, kemudian didinginkan. 2 mL NaCl jenuh dan 1 mL isooktan ditambahkan, lalu dikocok. Lapisan isooktan yang terbentuk dipindahkan dengan bantuan pipet tetes ke dalam tabung berisi 0,1 g Na2SO4 anhidrat, kemudian dibiarkan 15 menit. Fraksi cair yang terbentuk dipisahkan, sedangkan fraksi minyak yang terbentuk diinjeksikan ke dalam instrumen Gas Cromatography sebanyak 1 μL, setelah
sebelumnya dilakukan penginjeksian 1 μL campuran standar FAME (Supelco 37 component FAME mix). Waktu retensi dan puncak masing-masing komponen diukur lalu dibandingkan dengan waktu retensi standar untuk mendapatkan informasi mengenai jenis dan komponen-komponen dalam contoh.
Kondisi alat GC pada saat analisis:
a) Kolom = Cyanopropil methylsil (capilary column)
b) Dimensi kolom = P = 60 m, Ø dalam = 0,25 mm, 0,25 μm film tickness c) Laju alir N2 = 30 mL/menit
d) Laju alir H2 = 40 mL/menit e) Laju alir udara = 400 mL/menit f) Suhu injektor = 220 °C
g) Suhu detektor = 240 °C h) Suhu terprogram = 125-225 °C i) Inject volume = 1 μL
Cara perhitungan kandungan komponen dalam contoh adalah sebagai berikut:
Ax/As x Cstandar x Vcontoh/100 x100%
Gram contoh
Analisis asam lemak bebas/free fatty acid (AOCS 1998)
Sebanyak 2 gram minyak ditambahkan 25 mL alkohol 95% netral (erlenmeyer 200 mL), panaskan di dalam penangas air selama 10 menit, kemudian campuran tersebut ditetesi indikator PP sebanyak 2 tetes, kemudian dikocok dan dititrasi dengan KOH 0,1 N hingga timbul warna pink yang tidak hilang dalam 10 detik. Jumlah KOH yang dibutuhkan dicatat untuk menentukan % FFA.
Persentase FFA dihitung berdasarkan persamaan berikut:
V x N x 282,5 10 G
Keterangan : V = Jumlah titrasi KOH (mL) N = Normalitas KOH (0,1 N)
282,5 = Berat molekul asam lemak oleat G = Berat sampel (g)
Analisis bilangan asam/acid value (AV) (AOCS 1998)
Penentuan bilangan asam dilakukan dengan cara titrasi KOH terhadap sampel yang menggunakan prinsip jumlah KOH yang diperlukan (mg) untuk menetralkan 1 g lemak. Berikut persamaan untuk mendapatkan bilangan asam (mg KOH/g lipid):
V x N x 56,1 /
Keterangan :
Analisis bilangan peroksida/peroxide value (PV) (AOCS 1998)
Sebanyak 5 g sampel dimasukkan ke dalam labu erlenmeyer ukuran 250 mL, kemudian ditambahkan 30 mL larutan asam asetat dan kloroform (3:2), kemudian ditambahkan 0,5 mL larutan kalium iodide (KI) jenuh sambil diaduk, selanjutnya ditambahkan 30 mL aquades. Titrasi dilakukan dengan menggunakan 0,01 N natrium thiosulfate (Na2S2O3) hingga larutan berubah warna menjadi kuning, setelah itu ditambahkan 0,5 mL larutan indikator kanji 1% yang akan merubah warna larutan menjadi biru. Titrasi dilanjutkan dengan terus mengocok larutan hingga berubah warna menjadi biru muda yang menandakan pelepasan
iodine dari lapisan kloroform, lanjutkan titrasi dengan hati-hati hingga warna biru pada larutan hilang. Perhitungan nilai peroksida dilakukan dengan persamaan berikut:
V x N x 1000 0 G
Keterangan : V = Jumlah titrasi natrium thiosulfate (mL) N = Normalitas natrium thiosulfate (0,01 N) G = Berat sampel (g)
Analisis nilai anisidin/anisidine value (AnV) (AOCS 1998)
Larutan uji 1 dibuat dengan cara melarutkan 2 g sampel ke dalam 25 mL
anisidine (2,5 g/L) ke dalam 5 mL larutan uji 1, kemudian dikocok dan dihindarkan dari cahaya. Larutan referensi dibuat dengan cara menambahkan 1 mL larutan p-anisidine (2,5 g/L) ke dalam 5 mL larutan trimethylpentane, kemudian dikocok dan dihindarkan dari cahaya. Larutan uji 1 diukur nilai absorbansinya pada 350 nm dengan menggunakan pelarut trimethylpentane
sebagai larutan kompensasi. Larutan uji 2 diukur nilai absorbansi pada 350 nm tepat 10 menit setelah larutan disiapkan dengan menggunakan larutan referensi sebagai kompensasi. Nilai anisidin ditetapkan dengan persamaan berikut:
25 x (1,2 A2– A1) G
Keterangan : A1 = Absorbansi larutan uji 1 A2 = Absorbansi larutan uji 2
G = Berat sampel yang digunakan pada larutan uji 1 (g)
Analisis nilai total oksidasi (AOCS 1998)
Penentuan nilai total oksidasi dilakukan dengan persamaan berikut :
Total oksidasi (meq/kg) = (2PV + AnV)
Keterangan :
Analisis bilangan iod/iodine value (IV) dengan metode Wijs (AOAC 2005) Analisis bilangan iod dilakukan dengan mengambil sampel sebanyak 0,1 gr dalam erlenmeyer bertutup, kemudian ditambahkan 20 mL kloroform dan 25 mL pereaksi Wijs, didiamkan selama 30 menit di ruang gelap sambil dikocok-kocok. Selanjutnya ditambahkan 10 mL kalium iodide (KI) 15 % dan erlenmeyer dibilas dengan 100 mL aquades. Titrasi dilakukan dengan natrium thiosulfate 0,1 N sampai warna berubah menjadi kuning muda, kemudian ditambahkan indikator kanji 1 % dan titrasi lagi hingga warna biru tepat hilang. Analisis terhadap blanko dilakukan dengan cara yang sama, sampel diganti dengan akuades sebagai blanko. Perhitungan bilangan iod sebagai berikut :
V titran (blangko-contoh) x N x 12,69 G
Keterangan : V = Jumlah titrasi natrium thiosulfate (mL) N = Normalitas natrium thiosulfate (0,01 N) 12,69 = Berat molekul iod
G = Berat sampel (g)
Hasil dan Pembahasan Kandungan Proksimat Daging Mackerel
Analisis proksimat dilakukan untuk mengetahui kandungan gizi dan komposisi kimia suatu bahan, meliputi kandungan air, lemak, protein, abu dan karbohidrat dari sampel. Hasil pengukuran proksimat menunjukkan bahwa daging ikan mackerel memiliki kadar air yang cukup tinggi, yaitu 67,32±1,02%, kadar
= Bilangan iod (%)
abu sebesar 1,69±0,16% dan kadar lemak 9,93±0,77%. Berdasarkan data kadar lemak, menurut kategori Ackman (1989), ikan mackerel termasuk kategori ikan berlemak tinggi yaitu dengan kadar lemak >8%. Hasil ini sesuai dengan penelitian Lim (2012) yang mengukur kadar air mackerel (S. japonicus) sebesar 67,71 %, kadar abu sebesar 1,77 % dan kadar lemak 9,04%. Hasil penentuan kandungan zat gizi daging ikan mackerel (Scomber japonicus) disajikan dalam Tabel 1.
Tabel 1 Persentase kandungan gizi daging mackerel
Komposisi (%)
Berdasarkan Tabel 1 kadar protein daging mackerel sebesar 20,59±1,20%. Menurut Bae dan Lim (2012) kadar protein daging mackerel yaitu antara 20,61 – 22,16%. Hasil perhitungan kadar karbohidrat dengan metode by difference
menunjukkan bahwa daging ikan mackerel memiliki kadar karbohidrat sebesar 0,47±0,29%. Hasil perhitungan karbohidrat dengan metode by difference ini merupakan metode penentuan kadar karbohidrat dalam pangan secara kasar, dimana serat kasar juga terhitung sebagai karbohidrat. Kadar proksimat daging mackerel sangat dipengaruhi oleh lingkungan dan habitat tempat tinggal dari ikan tersebut (Bae et al. 2011; Lim 2012; Bae dan Lim 2012; Bae dan Lim 2013). Faktor umur, ukuran serta jenis kelamin dari spesies juga ikut berpengaruh terhadap kadar proksimat ikan. Boran dan Karacam (2011) menambahkan bahwa spesifik spesies dan perbedaan lokasi penangkapan juga mempengaruhi kandungan proksimat daging mackerel.
Kandungan Logam Berat
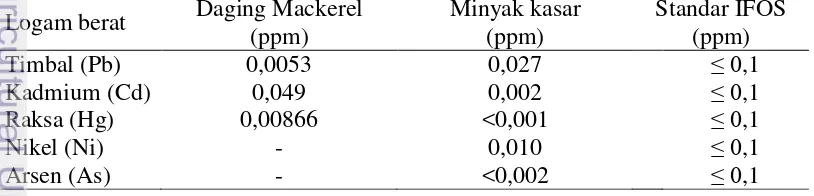
Hasil penentuan residu logam berat menunjukkan kandungan logam berat yang terdapat dalam daging ikan mackerel yang digunakan dan minyak hasil samping pengalengan masih dalam ambang batas yang ditetapkan IFOS (2011). Namun terjadi peningkatan konsentrasi timbal (Pb) dibanding bahan baku awal, peningkatan kandungan Pb pada minyak mackerel, diduga disebabkan oleh kontaminasi selama proses pengalengan dimana uap dari boiler dan air yang digunakan dapat menyebabkan peningkatan kandungan Pb pada minyak yang dihasilkan. Kandungan logam berat daging dan minyak mackerel disajikan pada Tabel 2.
Tabel 2 Kandungan logam berat daging dan minyak hasil samping pengalengan mackerel
Hasil penelitian menunjukkan kadar logam berat kadmium (Cd), raksa (Hg) dan Arsen (As) masih berada dibawah ambang batas yang ditetapkan oleh IFOS. Cd dapat terakumulasi dalam tubuh manusia dan memicu gangguan jantung, kerusakan tulang dan gangguan reproduksi. Raksa dapat mempengaruhi perubahan perkembangan otak bayi secara normal dan dalam jumlah yang tinggi dapat mengganggu perkembangan syaraf orang dewasa (CEC 2001). Arsen dapat meningkatkan timbulnya kanker melalui makanan yang dikonsumsi. Variasi logam berat produk hasil perairan juga dipengaruhi oleh habitat, tempat penangkapan dan musim (Bae et al. 2011; Bae dan Lim 2013). Karakteristik bahan baku mackerel yang digunakan juga dapat mempengaruhi tingginya kandungan logam berat tergantung daerah penangkapan, musim, pakan, suhu dan salinitas perairan (Bae et al. 2011).
Profil Asam Lemak
Pengujian profil asam lemak dimaksudkan untuk mengetahui komposisi asam lemak dari minyak hasil samping pengalengan mackerel. Berdasarkan hasil analisis profil asam lemak (Tabel 3) terlihat bahwa minyak ikan hasil samping pengalengan mackerel mengandung asam lemak jenuh (SFA) sebesar 27,15% lebih tinggi dibandingkan asam lemak tak jenuh tunggal (MUFA) yaitu 15,54%, sedangkan PUFA sebesar 30,99% yang didominasi Docosahexaenoic Acid, C22:6n3 (DHA) sebesar 19,22%. Hasil ini sesuai penelitian Bae dan Lim (2012); Lim (2012) bahwa daging mackerel (Scomber japonicus) mempunyai asam lemak tak jenuh dominan yaitu DHA dengan nilai antara 13,61 – 27,58%. Menurut Kazufumi et al. (2003), kadar DHA mackerel dipengaruhi variasi musim. Bae dan Lim (2012; 2013); Lim (2012) menambahkan bahwa selain musim, lokasi penangkapan juga berpengaruh terhadap kandungan asam lemak ikan mackerel.
Ikan mackerel yang digunakan pada penelitian ini merupakan ikan yang habitatnya di perairan tropis dan subtropis. Pada ikan yang habitatnya pada suhu yang lebih rendah, pembentukan ikatan PUFA meningkat (Lahdes et al. 2000). Variasi kandungan asam lemak omega-3 pada ikan juga disebabkan oleh faktor makanan. Menurut Ackman (1989), kandungan asam lemak omega-3 pada ikan bukan merupakan hasil sintesa alami dari tubuh ikan, melainkan hasil pembentukan dari sumber makanan yang berupa phytoplankton, zooplankton, algae, copepoda, dan kerang-kerangan.
Asam lemak tak jenuh dalam minyak ikan merupakan komponen terbesar dalam minyak ikan. Komponen asam lemak yang terkandung dalam minyak dapat diketahui melalui analisis Gas Chromatography (GC). Jumlah asam lemak tidak jenuh di dalam minyak ikan yang tinggi, yaitu sebesar 46,51% dari seluruh total komponen. Asam lemak tidak jenuh dengan banyak ikatan rangkap (PUFA), yaitu meliputi asam lemak omega-3 sebesar 27,44% dengan kadar Eicosapentaenoic Acid, C20:5n3 (EPA) sebesar 7,31% dan DHA 19,22%; asam lemak omega-6 yaitu 3,19%; dan asam lemak omega-9 sebesar 10,19%.
Tabel 3 Profil asam lemak minyak ikan hasil samping pengalengan mackerel
Asam Lemak/Fatty Acid % (w/w)
Asam laurat C12:0 0,07
Asam tridekanoat C13:0 0,08
Asam miristat C14:0 3,44
Asam pentadekanoat C15:0 0,94
Asam palmitat C16:0 16,34
Asam heptadekanoat C17:0 0,93
Asam stearat C18:0 4,24
Asam arakidat C20:0 0,6
Asam heneikosanoat C21:0 0,11
Asam behenat C22:0 0,23
Asam lignoserat C24:0 0,17
Total SFA 27,15
Asam miristoleat C14:1 0,02
Asam palmitoleat C16:1 3,49
Asam elaidat C18:1n9t 0,12
Asam oleat C18:1n9c 10,19
Asam cis-11-eicosenoat C20:1 1
Asam erukat C22:1n9 0,33
Asam nervonat C24:1 0,39
Total MUFA 15,54
Asam linoleat C18:2n6c 1,18
Asam linolelaidat C18:2n9t 0,06
Asam linolenat C18:3n3 0,91
Asam ϒ-linolenat C18:3n6 0,13
Asam cis-11,14-eicosedienoat C20:2 0,25
Asam cis-8,11,14-eicosetrienoat C20:3n6 0,11
Asam arachidonat C20:4n6 1,77
Asam cis-5,8,11,14,17-eicosapentaenoat C20:5n3 7,31
Asam cis-13,16-docosadienoat C22:2 0,03
Asam cis-4,7,10,13,16,19-docosaheksaenoat C22:6n3 19,22
Total PUFA 30,97
Total asam lemak teridentifikasi 73,66 Asam Lemak Bebas/Free Fatty Acid (FFA)
Pengujian asam lemak bebas dan parameter oksidasi minyak hasil samping pengalengan mackerel menunjukkan nilai diatas ambang batas IFOS (International Fish Oil Standard) kecuali nilai anisidin, sedangkan menurut IFOMA (International Fishmeal and Oil Manufacturers Association) oleh Bimbo (1998), semua parameter pengujian minyak hasil samping pengalengan mackerel masih dibawah ambang batas.
meningkat pada penyimpanan yang semakin lama, hal ini karena terjadi hidrolisis trigliserida pada minyak dan juga karena perpecahan serta oksidasi ikatan rangkap asam lemak (Crexi et al. 2010). Hasil pengamatan asam lemak bebas dan parameter oksidasi minyak hasil samping pengalengan mackerel disajikan pada Tabel 4.
Tabel 4 Hasil pengamatan asam lemak bebas dan parameter oksidasi minyak hasil samping pengalengan mackerel
Parameter Hasil Standar
IFOS IFOMA Bilangan asam didapat menggunakan prinsip jumlah KOH yang diperlukan (mg) untuk menetralkan 1 g lemak atau bisa juga didapatkan dengan perkalian konstanta 1,99 dengan nilai FFA. Bilangan asam yang didapatkan dari penelitian ini sebesar 7,95±0,61 mg KOH/g. Hasil ini lebih tinggi dari standar IFOS yang menyatakan minyak layak konsumsi harus memiliki bilangan asam dibawah 2,25 mg KOH/g.
Tingginya bilangan asam pada minyak disebabkan proses ekstraksi yang dilakukan, penggunaan panas selama ekstraksi minyak hasil samping pengalengan sangat berpengaruh terhadap tingginya bilangan asam. Menurut Mohanarangan (2012), bilangan asam sangat bergantung kepada komposisi minyak, metode ekstraksi dan kesegaran bahan mentah. Bilangan asam sangat berhubungan dengan nilai asam lemak bebas, sehingga sering digunakan untuk menentukan keberadaan nilai FFA.
Bilangan Peroksida/PeroxideValue (PV)
Analisis bilangan peroksida dilakukan untuk mengetahui tingkat kerusakan minyak. Bilangan peroksida menunjukkan tingkat oksidasi yang baru terjadi sebagai produk oksidasi primer. Bilangan peroksida minyak ikan mackerel pada penelitian ini adalah 6,27±1,73 meq/kg. Nilai bilangan peroksida minyak ikan mackerel tersebut memenuhi standar minyak berdasarkan IFOMA, yaitu sebesar 3-20 meq/kg, namun melebihi standar IFOS yaitu ≤ 3,75. Nilai oksidasi sangat penting sebagai indikator mutu minyak, semakin rendah nilai oksidasi primer dan sekunder, maka kualitas minyak yang dihasilkan akan semakin baik. Indikasi oksidasi primer adalah nilai peroksida yang penting untuk mengetahui kualitas minyak karena tahap pertama oksidasi adalah terbentuknya hidroperoksida.
bilangan peroksida. Aidos et al. (2002), menjelaskan bahwa nilai peroksida sangat tergantung pada suhu saat ekstraksi.
Nilai Anisidin/Anisidine Value (AnV)
Nilai anisidin merupakan parameter oksidasi lemak yang mengukur produk oksidasi sekunder lemak yang dikarakterisasi oleh degradasi lemak yang diinisiasi oleh hidroperoksida, sehingga menghasilkan produk sampingan karbonil yang yang bersifat non-volatile (Aidos et al. 2003). Berdasarkan hasil penelitan, nilai anisidin untuk minyak hasil samping pengalengan mackerel adalah 11,12±0,90 meq/kg. Hasil tersebut sesuai kualitas minyak ikan berdasarkan standar IFOMA yaitu 4-60 maupun IFOS ≤ 15 meq/kg. Menurut Hamilton et al. (1988) minyak yang berkualitas bagus harus memiliki nilai anisidin dibawah 20 meq/Kg.
Pengujian nilai anisidin metode AOCS didasarkan pengukuran ekspresi warna menggunakan spektrofotometer. Menurut O’Brien (2009) aldehid yang merupakan produk oksidasi sekunder di dalam minyak dan reagen p-anisidine
yang digunkan pada pengujian anisidin bereaksi dalam kondisi asam dan ekspresi warna pada minyak sangat tergantung kepada jumlah aldehid dan strukturnya. Nilai anisidin pada minyak hasil samping pengalengan menunjukkan nilai dibawah standar IFOS, hal ini dikarenakan minyak yang digunakan masih baru dan belum mengalami penyimpanan lama, sehingga belum terbentuk oksidasi sekunder yang ditandai dengan terbentuknya aldehid.
Nilai Total Oksidasi (Totoks)
Nilai totoks adalah jumlah total oksidasi primer dan sekunder yang didapatkan dengan menjumlahkan dua kali nilai peroksida dengan nilai anisidin (Perrin 1996). Nilai totoks minyak ikan hasil samping pengalengan mackerel pada penelitian ini yaitu 23,65±1,42 meq/kg, masih masuk standar minyak ikan berdasarkan IFOMA yaitu 10-60, sementara IFOS menyatakan minyak layak konsumsi harus memiliki nilai totoks dibawah 20 meq/Kg.
Nilai totoks yang melebihi batas IFOS berhubungan dengan tingginya nilai peroksida minyak, hal ini dikarenakan nilai totoks tergantung dari hasil pengujian bilangan peroksida, semakin tinggi bilangan peroksida, maka semakin tinggi nilai total oksidasi (totoks). Tingginya bilangan peroksida berhubungan dengan suhu saat ekstraksi minyak ikan. Pengujian parameter oksidasi yang meliputi bilangan peroksida, anisidin dan totoks merupakan pengujian kualitas minyak ikan yang sangat penting untuk dilakukan, karena dapat digunakan untuk mengukur sejauh mana reaksi oksidasi yang terjadi pada minyak.
Bilangan Iod/Iodine Value (IV)
Penentuan bilangan iod sangat penting untuk menunjukkan derajat ketidakjenuhan dan rata-rata berat molekul suatu asam lemak. Endo et al. (2005), menjelaskan bahwa semakin tinggi angka iod, maka ketidakjenuhan minyak semakin tinggi. Minyak ikan termasuk minyak dengan ketidakjenuhan tinggi yang didominasi asam lemak omega-3. Penentuan bilangan iod dapat digunakan untuk memprediksi kandungan omega-3 yang terdapat pada minyak ikan, meskipun tidak dapat ditentukan dengan tepat.
dikarenakan asam lemak pada minyak mackerel didominasi asam lemak tidak jenuh. Ikatan rangkap yang terdapat pada asam lemak yang tidak jenuh akan bereaksi dengan iod, sehingga bilangan iod menjadi ukuran ketidakjenuhan pada lemak atau minyak. Gliserida dengan tingkat ketidakjenuhan yang tinggi, akan mengikat iod dalam jumlah yang lebih besar (Crexi et al. 2009).
Simpulan
3 PEMURNIAN ALKALI MINYAK IKAN HASIL SAMPING PENGALENGAN MACKEREL (Scomber japonicus)
Pendahuluan Latar Belakang
Hasil pengujian minyak mackerel pada tahap karakterisasi menunjukkan bahwa kualitas minyak hasil samping pengalengan mackerel masih rendah. Namun, hasil pengujian profil asam lemak menunjukkan bahwa minyak mackerel memiliki kadar EPA dan DHA yang cukup tinggi yaitu masing-masing 7,31% dan 19,22%, sehingga merupakan sumber omega-3 yang sangat potensial. Hal ini merupakan tantangan tersendiri dalam upaya meningkatkan kualitas minyak ikan, seperti diketahui bahwa PUFA terutama omega-3 sangat rentan mengalami oksidasi yang dapat menurunkan kualitas minyak.
Kualitas minyak ikan menjadi perhatian tersendiri dalam proses produksi minyak ikan. Minyak ikan hasil samping pengalengan mempunyai kualitas rendah karena penggunaan suhu tinggi saat ekstraksi, meskipun bahan baku yang digunakan berupa daging produk yang akan dikalengkan, namun hasil pengujian parameter oksidasi dan kandungan asam lemak bebas diawal menunjukkan bahwa minyak hasil samping pengalengan mempunyai nilai diatas ambang standar IFOS, sehingga perlu perlakuan lanjutan untuk meningkatkan kualitas minyak ikan.
Salah satu perlakuan untuk meningkatkan kualitas minyak ikan yaitu pemurnian dengan menggunakan alkali (alkali refining). Garam alkali yang biasa digunakan yaitu KOH dan NaOH. Pada penelitian ini akan digunakan NaOH karena merupakan jenis alkali yang sering digunakan pada proses pemurnian alkali dengan harga yang relatif murah, NaOH juga lebih efisien jika digunakan dalam proses pemurnian alkali. Pemurnian dengan alkali berperan menghilangkan kotoran dengan mekanisme fraksi tersabunkan mengabsorpsi alkali dan terkoagulasi oleh proses hidrasi, kemudian bahan tidak larut terperangkap pada bahan yang terkoagulasi. Alkali dengan asam lemak bebas membentuk senyawa tidak larut air dan sebagian besar pigmen terabsorpsi oleh fraksi tersabunkan. Menurut Estiasih dan Ahmadi (2004), minyak ikan hasil samping pengalengan masih mengandung bahan-bahan non minyak sehingga perlu dimurnikan untuk menghilangkan komponen non minyak tersebut.
Tujuan
Penelitian ini bertujuan untuk melakukan pemurnian alkali dengan NaOH berdasarkan derajat baume (oBe) yang berbeda pada minyak ikan dari hasil samping pengalengan mackerel melalui analisis:
1 Rendemen minyak hasil pemurnian alkali 2 Profil asam lemak
3 Asam lemak bebas, bilangan asam, bilangan peroksida, nilai anisidin dan nilai total oksidasi (totoks)
Bahan dan Metode Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Maret 2014. Tempat pelaksanaan penelitian pemurnian alkali minyak hasil samping pengalengan mackerel yaitu Laboratorium Bahan Baku Hasil Perairan, Departemen Teknologi Hasil Perairan untuk pengujian asam lemak bebas, bilangan asam, bilangan peroksida dan nilai total oksidasi (totoks); Laboratorium Terpadu Fakultas Peternakan untuk penggunaan spektrofotometer pada pengujian nilai anisidin; Laboratorium Peternakan untuk pengujian logam berat dan Laboratorium Terpadu Institut Pertanian Bogor.
Bahan dan Alat Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah minyak hasil samping pengalengan mackerel. Bahan untuk pengujian parameter oksidasi minyak seperti kloroform, asam asetat glasial, ethanol, trimethylpentane, natrium thiosulfate 0,01 N, KOH 0,1 N, aquades, p-anisidine, phenolphtalein indicator,
kalium iodide (KI), kanji, bahan-bahan untuk pengujian logam berat dan standar pengujian profil asam lemak.
Alat-alat yang digunakan adalah gelas ukur, beaker glass, erlenmeyer, labu takar, tabung reaksi, pipet, timbangan analitik, thermometer, penangas, panci, stopwatch, perangkat titrasi dan spektrofotometer merk Agilent 8453 untuk pengujian kualitas minyak ikan. Alat-alat yang digunakan untuk analisa logam berat antara lain alat destruksi, labu destruksi, perangkat Atomic Absorption Spectrofotometer (AAS) dan perangkat kromatografi gas (gas chromatography) merek Shimadzu GC 2010 Plus untuk pengujian profil asam lemak.
Metode Penelitian
Penelitian tahap ini yaitu perlakuan pemurnian alkali menggunakan NaOH berdasarkan derajat Baume (oBe) hasil analisis asam lemak bebas (FFA) pada tahap karakterisasi. Konsentrasi NaOH dilihat berdasarkan ketetapan pada Lampiran 11. Kebutuhan jumlah larutan NaOH dihitung dengan rumus berikut :
Karakterisasi awal minyak ikan hasil samping pengalengan mackerel menunjukkan bahwa nilai FFA 4%. Berdasarkan nilai FFA awal pada tahap karakterisasi tersebut, maka pada penelitian ini akan menggunakan oBe 16, 18 dan
20. Minyak hasil pemurnian alkali dianalisis kualitasnya dan dibandingkan dengan minyak kasar (awal). Parameter yang diamati antara lain rendemen minyak ikan hasil pemurnian, analisis nilai asam lemak bebas (FFA), bilangan asam (AV), nilai peroksida (PV), nilai anisidin (AnV), nilai total oksidasi (totoks) dan analisis profil asam lemak perlakuan terpilih. Setiap perlakuan diuji tiga kali ulangan. Diagram alir penelitian pemurnian alkali minyak hasil samping pengalengan mackerel (Scomber japonicus) disajikan pada Gambar 3.
Gambar 3 Diagram alir pemurnian alkali minyak ikan hasil samping pengalengan mackerel (modifikasi metode Irianto 1992)
Analisis logam berat Cd, Pb, Hg, Ni dan As (AOAC 2005)
Analisis logam berat dilakukan dengan menimbang 1 gram contoh ke dalam erlenmeyer, kemudian ditambahkan 5 mL HNO3 pekat dan 1 mL HClO4, didiamkan 24 jam. Sampel dipanaskan pada suhu 100 oC selama 1 jam 30 menit, kemudian ditingkatkan menjadi 130 oC selama 1 jam, kemudian suhu ditingkatkan lagi menjadi 150 oC selama 2 jam 30 menit (sampai uap kuning habis, bila masih ada uap kuning, waktu pemanasan ditambah lagi). Setelah uap kuning habis, suhu ditingkatkan menjadi 170 oC selama 1 jam, kemudian suhu ditingkatkan lagi menjadi 200 oC selama 1 jam (terbentuk uap putih). Destruksi selesai dengan terbentuknya endapan putih. Ekstrak didinginkan kemudian diencerkan dengan air bebas ion menjadi 10 mL, lalu dikocok.
Larutan baku kalibrasi persediaan As, Cd, Pb, Ni dan Hg disiapkan dengan konsentrasi masing-masing 1000 μg/mL. Larutan baku kalibrasi As dibuat dengan konsentrasi 5, 10, 20, 30 dan 50 μg/L dalam larutan asam nitrat 0,5 % v/v. Larutan baku kalibrasi Cd dibuat dengan konsentrasi 0,5; 1; 2; 3 dan 5 μg/L dalam larutan asam nitrat 0,5 % v/v. Larutan baku kalibrasi Pb dibuat dengan konsentrasi
Kontrol (minyak kasar) Penambahan NaOH berdasarkan oBe
- 16 oBe - 18 oBe - 20 oBe
Pengadukan 15 menit suhu 60 oC
Dekantasi 15 jam
Minyak ikan
refined
Minyak hasil samping pengalengan
Penyaringan - Penentuan rendemen
- Profil asam lemak - Residu logam berat - FFA, AV, PV, AnV
Bobot sampel
5; 10; 20; 30 dan 50 μg/L dalam larutan asam nitrat 0,5% v/v. Larutan baku kalibrasi Ni dibuat dengan konsentrasi 5; 10; 20; 30 dan 50 μg/L dalam larutan asam nitrat 0,5% v/v. Larutan baku kalibrasi Hg dibuat dengan konsentrasi 0,5; 1; 2; 3 dan 5 μg/L dalam larutan asam klorida 3% v/v.
Larutan uji dibuat dengan metode digesti kering/pengabuan, yaitu dengan menimbang 2,5 g contoh, kemudian dimasukkan ke dalam cawan porselen dan ditambahkan 3 mL larutan MgNO3 50%. Larutan dikeringkan di atas penangas air, residu diabukan terlebih dahulu dalam mantel pemanas sampai tidak terdapat asap, kemudian dipanaskan dalam tanur pada suhu 500 oC selama 3 jam. Larutan didinginkan dan ditambahkan 25 mL larutan HCl 6 M, disaring ke dalam labu ukur 50 mL dan diencerkan dengan air sampai tanda. Pereaksi blanko dibuat seperti penyiapan larutan uji tetapi tanpa penambahan contoh.
Kurva kalibrasi didapatkan dengan cara disuntikkan larutan baku kalibrasi dan larutan modifier ke dalam alat AAS (rasio injeksi larutan baku dan modifier = 20 μL : 5 μL). Buat kurva antara respon (serapan atau tinggi puncak) dengan kadar dari masing-masing larutan baku. Hitung kadar As, Cd, Pb, Ni, Hg (μg/g) dalam contoh dengan persamaan garis regresi kurva kalibrasi, menggunakan rumus:
Konsentrasi logam dari kurva kalibrasi
Analisis profil asam lemak (AOAC 2005)
Metode analisis yang digunakan yaitu menggunakan prinsip mengubah asam lemak menjadi turunannya, yaitu metil ester sehingga dapat terdeteksi oleh alat kromatografi. Hasil analisis akan terekam dalam suatu lembaran yang terhubung dengan rekorder dan ditunjukkan melalui beberapa puncak pada waktu retensi tertentu sesuai dengan karakter masing-masing asam lemak dan dibandingkan dengan standar. Sebelum melakukan injeksi metil ester, dilakukan metilasi sehingga terbentuk metil ester dari masing-masing asam lemak.
Model alat kromatografi gas yang digunakan adalah Shimadzu GC 2010 Plus, gas yang digunakan sebagai fase bergerak adalah gas nitrogen dengan laju alir 30 mL/menit dan sebagai gas pembakar adalah hidrogen dan oksigen, kolom yang digunakan adalah capilary column merk Quadrex dengan diameter dalam 0,25 mm. Perangkat kromatografi gas yang digunakan dalam penelitian ini untuk analisis identifikasi asam lemak adalah Shimadzu GC 2010 Plus.
Sebanyak 20-40 mg contoh lemak atau minyak dimasukkan dalam tabung bertutup teflon dengan 1 mL NaOH dalam metanol dan dipanaskan dalam penangas air selama 20 menit, selanjutnya ditambahkan 2 mL BF3 20% dan 5 mg/mL standar internal ke dalam campuran, campuran dipanaskan lagi selama 20 menit, kemudian didinginkan. 2 mL NaCl jenuh dan 1 mL isooktan ditambahkan, lalu dikocok. Lapisan isooktan yang terbentuk dipindahkan dengan bantuan pipet tetes ke dalam tabung berisi 0,1 gram Na2SO4 anhidrat, kemudian dibiarkan 15 menit. Fraksi cair yang terbentuk dipisahkan, sedangkan fraksi minyak yang terbentuk diinjeksikan ke dalam instrumen Gas Cromatography sebanyak 1 μL,
setelah sebelumnya dilakukan penginjeksian 1 μL campuran standar FAME (Supelco 37 component FAME mix). Waktu retensi dan puncak masing-masing komponen diukur lalu dibandingkan dengan waktu retensi standar untuk mendapatkan informasi mengenai jenis dan komponen-komponen dalam contoh.
Kondisi alat GC pada saat analisis:
a) Kolom = Cyanopropil methylsil (capilary column)
b) Dimensi kolom = P = 60 m, Ø dalam = 0,25 mm, 0,25 μm film tickness c) Laju alir N2 = 30 mL/menit
d) Laju alir H2 = 40 mL/menit e) Laju alir udara = 400 mL/menit f) Suhu injektor = 220 °C
g) Suhu detektor = 240 °C h) Suhu terprogram = 125-225 °C i) Inject volume = 1 μL
Cara perhitungan kandungan komponen dalam contoh adalah sebagai berikut: Ax/As x Cstandar x Vcontoh/100 x100%
Gram contoh
Keterangan : Ax = Area sampel Cstandar = Konsentrasi standar As = Area standar Vcontoh = Volume contoh
Analisis asam lemak bebas/free fatty acid (AOCS 1998)
Sebanyak 2 gram minyak ditambahkan 25 mL alkohol 95% netral (erlenmeyer 200 mL), panaskan di dalam penangas air selama 10 menit, kemudian campuran tersebut ditetesi indikator PP sebanyak 2 tetes, kemudian dikocok dan dititrasi dengan KOH 0,1 N hingga timbul warna pink yang tidak hilang dalam 10 detik. Jumlah KOH yang dibutuhkan dicatat untuk menentukan % FFA.
Persentase FFA dihitung berdasarkan persamaan berikut:
V x N x 282,5 10 G
Keterangan : V = Jumlah titrasi KOH (mL) N = Normalitas KOH (0,1 N)
282,5 = Berat molekul asam lemak oleat G = Berat sampel (g)
Analisis bilangan asam/acid value (AV) (AOCS 1998)
Penentuan bilangan asam dilakukan dengan cara titrasi KOH terhadap sampel yang menggunakan prinsip jumlah KOH yang diperlukan (mg) untuk menetralkan 1 g lemak. Berikut persamaan untuk mendapatkan bilangan asam (mg KOH/g lipid):
V x N x 56,1 /
Keterangan :
Analisis bilangan peroksida/peroxide value (PV) (AOCS 1998)
Sebanyak 5 g sampel dimasukkan ke dalam labu erlenmeyer ukuran 250 mL, kemudian ditambahkan 30 mL larutan asam asetat dan kloroform (3:2),
FFA (%) =
G Bilangan asam (mg KOH/g) =
kemudian ditambahkan 0,5 mL larutan kalium iodide (KI) jenuh sambil diaduk, selanjutnya ditambahkan 30 mL aquades. Titrasi dilakukan dengan menggunakan 0,01 N natrium thiosulfate (Na2S2O3) hingga larutan berubah warna menjadi kuning, setelah itu ditambahkan 0,5 mL larutan indikator kanji 1% yang akan merubah warna larutan menjadi biru. Titrasi dilanjutkan dengan terus mengocok larutan hingga berubah warna menjadi biru muda yang menandakan pelepasan
iodine dari lapisan kloroform, lanjutkan titrasi dengan hati-hati hingga warna biru pada larutan hilang. Perhitungan nilai peroksida dilakukan dengan persamaan berikut:
V x N x 1000 0 G
Keterangan : V = Jumlah titrasi natrium thiosulfate (mL) N = Normalitas natrium thiosulfate (0,01 N) G = Berat sampel (g)
Analisis nilai anisidin/anisidine value (AnV) (AOCS 1998)
Larutan uji 1 dibuat dengan cara melarutkan 2 g sampel ke dalam 25 mL
trimethylpentane. Larutan uji 2 dibuat dengan cara menambahkan 1 mL larutan p
-anisidine (2,5 g/L) ke dalam 5 mL larutan uji 1, kemudian dikocok dan dihindarkan dari cahaya. Larutan referensi dibuat dengan cara menambahkan 1 mL larutan p-anisidine (2,5 g/L) ke dalam 5 mL larutan trimethylpentane, kemudian dikocok dan dihindarkan dari cahaya. Larutan uji 1 diukur nilai absorbansinya pada 350 nm dengan menggunakan pelarut trimethylpentane
sebagai larutan kompensasi. Larutan uji 2 diukur nilai absorbansi pada 350 nm tepat 10 menit setelah larutan disiapkan dengan menggunakan larutan referensi sebagai kompensasi. Nilai anisidin ditetapkan dengan persamaan berikut:
25 x (1,2 A2– A1) G Keterangan : A1 = Absorbansi larutan uji 1
A2 = Absorbansi larutan uji 2
G = Berat sampel yang digunakan pada larutan uji 1 (g)
Analisis nilai total oksidasi (AOCS 1998)
Penentuan nilai total oksidasi dilakukan dengan persamaan berikut :
Total oksidasi (meq/kg) = (2PV + AnV)
Keterangan :
Analisis Data
Data yang diperoleh pada perlakuan pemurnian alkali dianalisis dengan menggunakan Rancangan Acak Lengkap (RAL) dengan percobaan satu faktor yaitu konsentrasi NaOH berdasarkan derajat baume (oBe). Perlakuan ini dianalisis menggunakan Analysis of Variance (ANOVA) dengan kaidah pengambilan keputusan sebagai berikut (Steel and Torrie 1993):
Nilai peroksida (meq/kg) =