EKSPRESI VASCULAR ENDOTHELIAL GROWTH
FACTOR (VEGF) PADA KARSINOMA HIDUNG DAN
SINUS PARANASAL
Tesis
Diajukan untuk Melengkapi Tugas dan Memenuhi Salah satu
Syarat untuk Mencapai Spesialis dalam Bidang
Ilmu Kesehatan Telinga Hidung Tenggorok
Bedah Kepala Leher
Oleh :
MARWAN MOEHARMAN
PROGRAM PENDIDIKAN DOKTER SPESIALIS BIDANG
ILMU KESEHATAN TELINGA HIDUNG TENGGOROK
BEDAH KEPALA LEHER
FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA
Lembar Pengesahan
Tanggal 10 Juni 2010
Disetujui untuk diajukan ke sidang ujian oleh:
Pembimbing 1
Dr. Hafni, Sp.THT-KL(K) NIP: 195609111984032001
Pembimbing 2
Prof. Ramsi Lutan, dr. Sp. THT-KL(K) NIP: 130 318 044
Pembimbing 3
Dr. dr. Delfitri Munir, Sp. THT-KL(K) NIP: 195401261984031001
Diketahui oleh
Ketua Program Studi Ilmu Kesehatan Telinga Hidung Tenggorok Bedah Kepala Leher Fakultas Kedokteran Universitas Sumatera Utara
Prof. Askaroellah Aboet, dr, SpTHT-KL(K) NIP: 194603051975031001
Tesis dengan judul
EKSPRESI VASCULAR ENDOTHELIAL GROWTH
FACTOR (VEGF) PADA KARSINOMA HIDUNG DAN
SINUS PARANASAL
Diketahui Oleh :
Ketua Departemen Ketua Program Studi
Prof. Abdul Rachman Saragih,dr.Sp.THT-KL(K) Prof. Askaroellah Aboet dr.Sp.THT-KL(K)
Telah disetujui dan diterima baik oleh pembimbing
Ketua
dr. Hafni, Sp.THT-KL(K)
Anggota
KATA PENGANTAR
Dengan mengucapkan Bismillahirahmanirrahim, saya sampaikan rasa
syukur kehadirat Allah SWT karena dengan rahmat dan karuniaNya saya
dapat menyelesaikan tesis ini sebagai salah satu syarat dalam
menyelesaikan pendidikan untuk memperoleh Spesialis dalam bidang Ilmu
Kesehatan Telinga Hidung Tenggorok dan Bedah kepala leher di Fakultas
Kedokteran Universitas Sumatera Utara Medan. Saya menyadari penulisan
tesis ini masih jauh dari sempurna, baik isi maupun bahasannya. Walaupun
demikian, mudah-mudahan tulisan ini dapat menambah perbendaharaan
penelitian tentang Ekspresi Vascular Endothelial Growth Factor (VEGF)
pada Karsinoma Hidung dan Sinus Paranasal.
Dengan telah selesainya tulisan ini, pada kesempatan ini dengan tulus
hati saya mengucapkan terima kasih yang tak terhingga dan penghargaan
setinggi-tingginya kepada yang terhormat :
Dr. Hafni, Sp.THT-KL(K) atas kesediaannya sebagai ketua pembimbing
penelitian ini, begitu juga kepada Prof. Ramsi Lutan, dr. Sp.THT-KL(K),
Dr. dr. Delfitri Munir, Sp.THT-KL(K) sebagai anggota pembimbing dan Prof.
H.M. Nadjib Dahlan Lubis, dr. Sp. PA(K) dan dr. Arlinda Sari Wahyuni, MKes
sebagai konsultan ahli. Ditengah kesibukan beliau , dengan penuh perhatian
dan kesabaran, telah banyak memberi bantuan, bimbingan, saran dan
pengarahan yang sangat bermanfaat kepada saya dalam menyelesaikan
Dengan telah berakhirnya masa pendidikan saya, pada kesempatan
yang berbahagia ini perkenankanlah saya menyampaikan penghargaan dan
terima kasih yang sebesar-besarnya kepada :
Yang terhormat Rektor Universitas Sumatera Utara, Bapak Prof.
Syahril Pasaribu, dr. SpA(K) DTM&H dan mantan Rektor Universitas
Sumatera Utara, Prof. Chairuddin Panusunan Lubis, dr. SpA(K) DTM&H yang
telah memberikan kesempatan kepada penulis untuk mengikuti Program
Pendidikan Dokter Spesialis di Departemen THT-KL Fakultas Kedokteran
Universitas Sumatera Utara.
Yang terhormat Dekan Fakultas Kedokteran Universitas Sumatera
Utara Prof. Gontar Alamsyah Siregar, dr. Sp.PD(KGEH) dan mantan Dekan
Fakultas Kedokteran USU Prof. Sutomo Kasiman, dr. Sp.JP(K) dan Prof T.
Bahri Anwar, dr. SpJP(K) atas kesempatan yang diberikan kepada saya
untuk mengikuti program pendidikan dokter di Fakultas Kedokteran USU.
Yang terhormat Bapak Direktur RSUP H. Adam Malik Medan, Direktur
RS Tembakau Deli Medan, Direktur RSUD Lubuk Pakam dan Direktur Rumkit
TK I Medan dan Direktur RSUD F.L. Tobing Sibolga yang telah mengizinkan
dan telah memberikan kesempatan pada saya untuk menjalani masa
pendidikan di rumah sakit yang beliau pimpin.
Yang terhormat Ketua Departemen / Staf Radiologi FK.USU / RSUP.
H.Adam Malik Medan, Ketua Departemen / Staf Anestesi FK.USU RSUP.
H.Adam Malik Medan, Ketua Departemen / Staf Patologi Anatomi FK.USU
stase asisten di bagian tersebut dan kami ucapkan terima kasih
sebanyak-banyaknya.
Yang terhormat Ketua Departemen Ilmu Kesehatan Telinga Hidung
Tenggorok dan Bedah Kepala Leher Fakultas Kedokteran USU Prof. Abdul
Rachman Saragih, dr. Sp.THT-KL(K) dan Ketua Program Studi Ilmu
Kesehatan THT-KL Fakultas Kedokteran USU, Prof. Askaroellah Aboet, dr.
Sp.THT-KL(K) yang telah memberikan izin, kesempatan dan ilmu kepada
saya dalam mengikuti pendidikan spesialisasi sampai selesai.
Yang terhormat supervisor di jajaran Departemen THT-KL Fakultas
Kedokteran USU/RSUP. H.Adam Malik Medan, dr. Asroel Aboet, Sp.THT-KL,
Prof. Ramsi Lutan, dr. Sp.THT-KL(K), dr. Yuritna Haryono, Sp.THT-KL (K),
Prof. Askaroellah Aboet, dr. Sp.THT-KL(K), Prof. Abdul Rachman Saragih,
dr. Sp.THT-KL(K), dr. Muzakkir Zamzam, SpTHT-KL(K), dr. Mangain
Hasibuan, SpTHT-KL, dr.T.Sofia Hanum, Sp.THT-KL (K), Dr. Dr. Delfitri
Munir, SpTHT-KL(K), dr.Linda I Adenin,Sp.THT-KL, dr.Hafni,Sp.THT-KL (K),
dr. Ida Sjailandrawati Hrp, SpTHT-KL, dr.Adlin Adnan,Sp.THT-KL, dr. Rizalina
A. Asnir, Sp.THT-KL, (Almh) dr. Ainul Mardhiah, Sp.THT-KL, dr. Siti Nursiah,
Sp.THT-KL, dr. Andrina Y.M. Rambe, Sp.THT-KL, dr.Harry Agustaf Asroel,
Sp.THT-KL, dr. Farhat, Sp.THT-KL, dr. T. Siti Hajar Haryuna, Sp.THT-KL, dr.
Aliandri, Sp.THT-KL, dr. Asri Yudhistira, Sp.THT-KL, dr. Devira Zahara,
SpTHT-KL, dr. H.R. Yusa Herwanto, SpTHT-KL dan dr. M. Pahala Hanafi
Harahap, SpTHT-KL. Terima kasih atas segala ilmu, keterampilan dan
Yang tercinta teman-teman sejawat PPDS Ilmu Kesehatan THT-KL
Fakultas Kedokteran USU, atas bantuan, nasehat, saran maupun
kerjasamanya selama masa pendidikan.
Yang terhormat perawat/paramedis dan seluruh karyawan/karyawati
RSUP H. Adam Malik Medan , khususnya Departemen/SMF THT-KL yang
selalu membantu dan bekerjasama dengan baik dalam menjalani tugas
pendidikan dan pelayanan kesehatan selama ini.
Yang mulia dan tercinta Ayahanda dr. H. Moeharman Idham, SpPD
KPTI (Alm) dan Ibunda Hj. Sulastri, ananda sampaikan rasa hormat dan
terima kasih yang tak terhingga serta penghargaan yang setinggi-tingginya
atas kasih sayang yang telah diberikan dan dilimpahkan kepada ananda
sejak dalam kandungan, dilahirkan, dibesarkan dan diberi pendidikan yang
baik serta diberikan suri tauladan yang baik hingga menjadi landasan yang
kokoh dalam menghadapi kehidupan ini, dengan memanjatkan doa kehadirat
Allah SWT, Ya Allah ampuni dosa kami dan dosa kedua orang tua kami,
serta kasihilah mereka sebagaimana mereka mengasihi kami sejak kecil.
Yang tercinta Bapak mertua Zulfikri Tala, S.H. dan Ibu mertua Nirwisna
Martias, S.H. yang selama ini telah memberikan dorongan dan restu untuk
selalu menuntut ilmu setinggi-tingginya.
Kepada istriku tercinta dr. Sri Mella Tala, serta buah hati kami
tersayang Muhammad Zaki Moeharman, tiada kata yang lebih indah yang
dapat saya ucapkan selain ucapan terima kasih yang setulus-tulusnya atas
tiada henti-hentinya kepada ayahanda sehingga dengan ridho Allah SWT
akhirnya kita sampai pada saat yang berbahagia ini.
Kepada Kakak dan Abang ipar penulis mengucapkan terima kasih atas
limpahan kasih sayang dan tak henti-hentinya memberikan dorongan serta
doa kepada penulis.
Kepada seluruh kerabat dan handai taulan yang tidak dapat kami
sebutkan satu persatu, yang telah memberikan bantuan kami ucapkan terima
kasih yang sebesar-besarnya.
Akhirnya izinkanlah saya mohon maaf yang setulus-tulusnya atas
segala kesalahan dan kekurangan kami selama mengikuti pendidikan ini,
semoga segala bantuan, dorongan, petunjuk yang diberikan kepada kami
selama mengikuti pendidikan kiranya mendapat balasan yang berlipat ganda
dari Allah SWT, Yang maha pemurah, maha pengasih dan maha penyayang.
Amin.
Medan, Juli 2010 Penulis
Ekspresi Vascular Endothelial Growth Factor pada Karsinoma Hidung dan Sinus Paranasal
Abstrak
Latar Belakang : Karsinoma hidung dan sinus paranasal adalah tumor ganas yang cenderung didiagnosis pada stadium lanjut, sehingga angka
survival rendah dan prognosis penderita jelek. Salah satu faktor yang diduga
berperan dalam progresivitas tumor dan metastase tumor adalah
overekspresi vascular endothelial growth factor (VEGF) yang berperan
penting dalam proses angiogenesis tumor. Penelitian ini dilakukan untuk
melihat ekspresi VEGF pada karsinoma hidung dan sinus paranasal, serta
melihat hubungan ekspresi VEGF dengan stadium dan jenis histopatologi
karsinoma hidung dan sinus paranasal.
Metode Penelitian : Penelitian dilakukan dengan studi potong lintang (cross
sectional study) di Departemen THT-KL FK USU / RSUP H. Adam Malik
Medan, secara non probability consecutive sampling mulai Mei 2009.
Terhadap penderita karsinoma hidung dan sinus paranasal dilakukan
pemeriksaan histopatologi dan imunohistokimia dari jaringan hidung dan
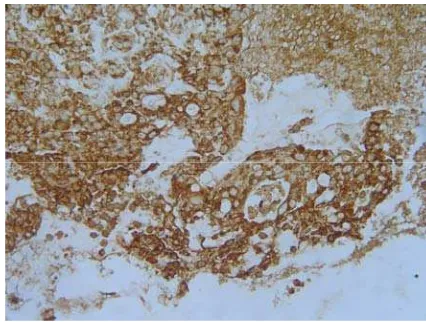
sinus paranasal yang diperoleh dari biopsi. Ekspresi VEGF dinilai pada
sitoplasma yang terwarnai merah kecoklatan. Data dianalisa dengan uji
korelasi Spearman dan uji chi square dengan tingkat kemaknaan 5%.
dijumpai pada 23 dari 25 kasus karsinoma hidung dan sinus paranasal
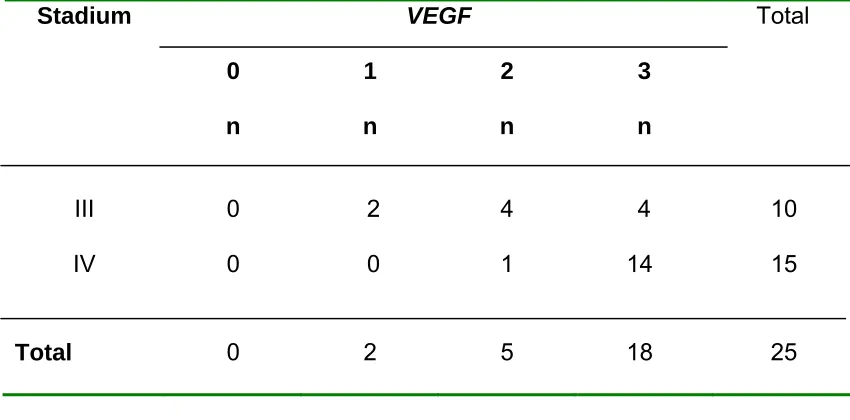
(92,0%). Dijumpai korelasi yang bermakna antara stadium lanjut tumor
dengan ekspresi VEGF pada karsinoma hidung dan sinus paranasal
(p < 0,05). Tidak dijumpai hubungan yang bermakna antara jenis
histopatologi dengan ekspresi VEGF pada karsinoma hidung dan sinus
paranasal (p > 0,05).
Kesimpulan : Ekspresi VEGF cukup tinggi pada penderita karsinoma hidung dan sinus paranasal. Kemungkinan VEGF berperan dalam proses
angiogenesis pada karsinoma hidung dan sinus paranasal.
Abstract
Background : Sinonasal carcinoma is a malignancy that tend to diagnosed at advanced stage with low survival and prognosis rate. One of the factor that
may play a role in progresivity and metastasis of tumour is overexpression of
vascular endothelial growth factor (VEGF) which is a key role in tumour
angiogenesis. The aim of this study is to learn the expression of VEGF in
sinonasal carcinoma, and to learn the association of VEGF expression with
tumour stage and histopathologic type of sinonasal carcinoma.
Study design and methods : This is a cross sectional study performed in ENT-HNS Department of Medical School of University of North Sumatera / H.
Adam Malik Hospital. Sample was collected by non probability consecutive
sampling, starting from Mei 2009. Sinonasal carcinoma patients underwent
histophatologic examination and immunohistochemical analysis from
sinonasal biopsy. VEGF expression analysed by red-brown stained
cytoplasm. Data was analysed by Spearman’s correlation test and chi square
test.
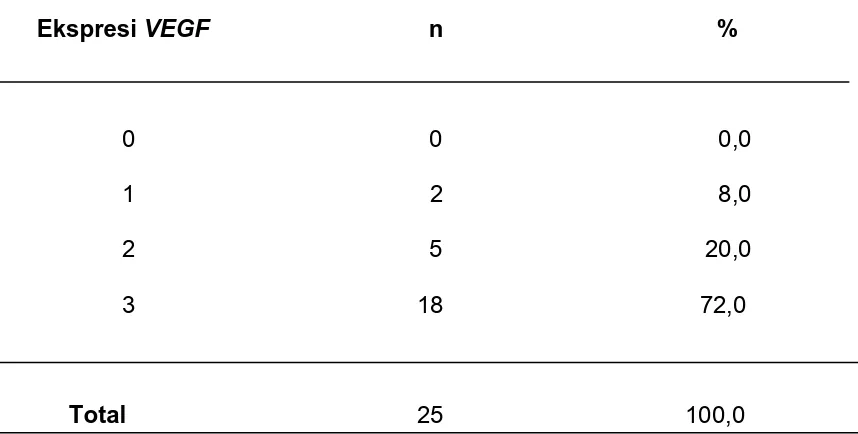
Results : VEGF positive expression was found in 25 of 25 (100.0%) sinonasal carcinoma cases. VEGF over expression was found in 23 of 25
(92.0%) sinonasal carcinoma cases. Significance correlation was found
between tumour stage and VEGF expression (p > 0.05). No significance
association was found between histophatologic type and VEGF expression
Conclusions : VEGF expression is relatively high in sinonasal carcinoma patient. VEGF may play a role in the angiogenesis of sinonasal carcinoma.
DAFTAR ISI
2.1.2 Anatomi dan Fungsi Sinus Paranasal ………… 13
2.1.3 Epidemiologi ……….. 18
2.1.4 Etiologi ………. 19
2.1.5 Patologi ……… 20
2.1.6 Gejala Klinis ……… 21
2.1.7 Diagnosis ……… 23
2.1.8 Klasifikasi Klinis ………. 23
2.1.9 Stadium Tumor ……….. 24
2.1.10 Penatalaksanaan ………. 27
2.2 Vascular Endothelial Growth Factor …... 29
2.2.1 Angiogenesis ……….. 29
2.2.2 Angiogenesis yang Diinduksi Tumor ………….. 30
2.2.3 Famili VEGF ……… 33
2.2.5 Peran VEGF pada Angiogenesis ……….... 37
2.2.6 Regulasi VEGF ……….. 41
2.2.7 Ekspresi VEGF ……….. 45
2.2.8 Anti VEGF ……….. 46
BAB 3 : KERANGKA KONSEPTUAL ……… 48
BAB 4 : METODE PENELITIAN ………. 49
4.1 Rancangan Penelitian ……… 49
4.2 Lokasi dan Waktu Penelitian ……… 49
4.3 Populasi, Sampel, Besar Sampel, Teknik Pengambilan Sampel ………... 49
4.3.1 Populasi ……… 49
4.3.2 Sampel Penelitian ……….. 50
4.3.3 Besar Sampel ………... 51
4.3.4 Teknik Pengambilan Sampel ... 51
4.4 Variabel Penelitian ……….. 52
4.4.1 Klasifikasi Variabel Penelitian ……….. 52
4.4.2 Definisi Operasional Variabel ……….. 52
4.5 Bahan Penelitian ……… 54
4.6 Instrumen Penelitian …...……….. 54
4.7 Kerangka Kerja ………... 57
4.8 Pelaksanaan Penelitian ………. 57
4.9 Cara Analisis Data ……….. 58
BAB 5 ANALISIS HASIL PENELITIAN... 59
BAB 7 KESIMPULAN DAN SARAN ……….. 72
7.1 Kesimpulan ………. 72
7.2 Saran ……… 72
KEPUSTAKAAN ……… 73
LAMPIRAN ……….. 77
Lampiran 1. Data Sampel Penelitian ……….. 77
Lampiran 2. Status Penelitian ……….. 79
Lampiran 3. Lembar Penjelasan Mengenai Penelitian ……… 83
Lampiran 4. Naskah Penjelasan ………. 86
Lampiran 5. Lembar Persetujuan Setelah Penjelasan ……… 88
Lampiran 6. Persetujuan Komite Etik Penelitian ……….. 89
Ekspresi Vascular Endothelial Growth Factor pada Karsinoma Hidung dan Sinus Paranasal
Abstrak
Latar Belakang : Karsinoma hidung dan sinus paranasal adalah tumor ganas yang cenderung didiagnosis pada stadium lanjut, sehingga angka
survival rendah dan prognosis penderita jelek. Salah satu faktor yang diduga
berperan dalam progresivitas tumor dan metastase tumor adalah
overekspresi vascular endothelial growth factor (VEGF) yang berperan
penting dalam proses angiogenesis tumor. Penelitian ini dilakukan untuk
melihat ekspresi VEGF pada karsinoma hidung dan sinus paranasal, serta
melihat hubungan ekspresi VEGF dengan stadium dan jenis histopatologi
karsinoma hidung dan sinus paranasal.
Metode Penelitian : Penelitian dilakukan dengan studi potong lintang (cross
sectional study) di Departemen THT-KL FK USU / RSUP H. Adam Malik
Medan, secara non probability consecutive sampling mulai Mei 2009.
Terhadap penderita karsinoma hidung dan sinus paranasal dilakukan
pemeriksaan histopatologi dan imunohistokimia dari jaringan hidung dan
sinus paranasal yang diperoleh dari biopsi. Ekspresi VEGF dinilai pada
sitoplasma yang terwarnai merah kecoklatan. Data dianalisa dengan uji
korelasi Spearman dan uji chi square dengan tingkat kemaknaan 5%.
dijumpai pada 23 dari 25 kasus karsinoma hidung dan sinus paranasal
(92,0%). Dijumpai korelasi yang bermakna antara stadium lanjut tumor
dengan ekspresi VEGF pada karsinoma hidung dan sinus paranasal
(p < 0,05). Tidak dijumpai hubungan yang bermakna antara jenis
histopatologi dengan ekspresi VEGF pada karsinoma hidung dan sinus
paranasal (p > 0,05).
Kesimpulan : Ekspresi VEGF cukup tinggi pada penderita karsinoma hidung dan sinus paranasal. Kemungkinan VEGF berperan dalam proses
angiogenesis pada karsinoma hidung dan sinus paranasal.
Abstract
Background : Sinonasal carcinoma is a malignancy that tend to diagnosed at advanced stage with low survival and prognosis rate. One of the factor that
may play a role in progresivity and metastasis of tumour is overexpression of
vascular endothelial growth factor (VEGF) which is a key role in tumour
angiogenesis. The aim of this study is to learn the expression of VEGF in
sinonasal carcinoma, and to learn the association of VEGF expression with
tumour stage and histopathologic type of sinonasal carcinoma.
Study design and methods : This is a cross sectional study performed in ENT-HNS Department of Medical School of University of North Sumatera / H.
Adam Malik Hospital. Sample was collected by non probability consecutive
sampling, starting from Mei 2009. Sinonasal carcinoma patients underwent
histophatologic examination and immunohistochemical analysis from
sinonasal biopsy. VEGF expression analysed by red-brown stained
cytoplasm. Data was analysed by Spearman’s correlation test and chi square
test.
Results : VEGF positive expression was found in 25 of 25 (100.0%) sinonasal carcinoma cases. VEGF over expression was found in 23 of 25
(92.0%) sinonasal carcinoma cases. Significance correlation was found
between tumour stage and VEGF expression (p > 0.05). No significance
association was found between histophatologic type and VEGF expression
Conclusions : VEGF expression is relatively high in sinonasal carcinoma patient. VEGF may play a role in the angiogenesis of sinonasal carcinoma.
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Tumor ganas hidung dan sinus paranasal meliputi kurang dari 1% dari
seluruh keganasan dan sekitar 3% pada saluran pernapasan atas (Thomson,
2006). Karena tumor tumbuh dalam tulang, sulit mengetahuinya secara dini.
Asal tumor juga sulit ditentukan, apakah dari hidung atau sinus karena
biasanya pasien berobat dalam keadaan penyakit telah lanjut dan tumor telah
memenuhi rongga hidung dan sinus (Roezin, Mangunkusumo, Soetjipto,
2004). Insiden tertinggi tumor ganas hidung dan sinus paranasal ditemukan
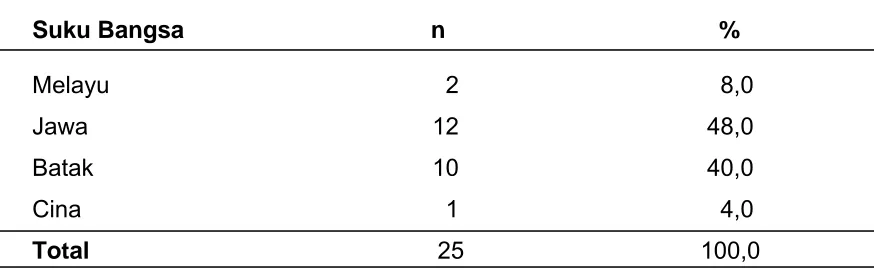
di Jepang yaitu 2 per 100.000 penduduk pertahun. Di bagian THT FK UI RS
Cipto Mangunkusumo, keganasan ini ditemukan pada 10,1% dari seluruh
tumor ganas THT (Roezin, Mangunkusumo, Soetjipto, 2004). Rifqi
mengemukakan data yang dikumpulkannya dari rumah sakit umum di
sepuluh kota besar di Indonesia bahwa frekuensi tumor hidung dan sinus
adalah 9,3 – 25,3% dari keganasan THT dan berada pada peringkat kedua
sesudah tumor ganas nasofaring (Tjahyadewi dan Wiratno, 1999). Di RSUP
H. Adam Malik Medan selama Januari 2002 sampai dengan Desember 2008
pasien yang dirawat dengan diagnosis karsinoma hidung dan sinus paranasal
adalah sebanyak 52 kasus.
Etiologi dari tumor ganas hidung dan sinus paranasal belum diketahui,
nikel, debu kayu, kulit, formaldehid, kromium, minyak isopropil dan lain-lain.
(Zimmer dan Carrau, 2006). Pekerja dibidang ini mendapat kemungkinan
terjadi keganasan hidung dan sinus jauh lebih besar. Alkohol, makanan yang
diasin atau diasap diduga meningkatkan kemungkinan terjadi keganasan,
sebaliknya buah-buahan dan sayuran mengurangi kemungkinan terjadinya
keganasan (Roezin, Mangunkusumo, Soetjipto, 2004).
Tumor ganas hidung dan sinus paranasal adalah tumor yang sangat
sulit untuk diterapi karena berhubungan dengan prognosis yang buruk. Salah
satu alasan buruknya prognosis adalah dekatnya anatomi kavum nasi dan
sinus paranasal ke struktur-struktur vital seperti dasar tengkorak, otak, mata,
dan arteri karotis. Lokasi yang kompleks ini membuat reseksi bedah tumor
hidung dan sinus paranasal merupakan suatu tantangan dan kadang-kadang
tidak mungkin untuk dilakukan (Wong dan Kraus, 2001).
Operasi dengan radioterapi pasca operasi adalah terapi standar untuk
tumor ganas hidung dan sinus paranasal. Penatalaksanaan yang optimal
untuk tumor ganas hidung dan sinus paranasal masih kontroversial. Hal ini
dipengaruhi oleh banyaknya tipe histologi dan daerah yang ikut terlibat. Untuk
meningkatkan angka harapan hidup, kemoterapi diberikan sebagai terapi
adjuvan dalam berbagai metode yang luas (Wong dan Kraus, 2001), dan dari
beberapa penelitian telah disimpulkan kombinasi anti VEGF (Vascular
Endothelial Growth Factor) dengan kemoterapi atau radioterapi menghasilkan
efek antitumor yang lebih baik daripada pemberian kemoterapi atau
Overekspresi VEGF telah dihubungkan dengan progresivitas tumor
dan prognosis yang buruk dalam berbagai macam tumor, termasuk tumor
sinus maksila, tumor lidah, gingiva, dan mandibula, tumor kolorektal,
lambung, pankreas, payudara, paru dan melanoma, acute myeloid leukemia,
hepar dan ovarium (Rosen, 2002; Hicklin dan Ellis, 2005; Strauss et al,
2005). VEGF merupakan faktor proangiogenik yang berperan dalam
angiogenesis untuk pertumbuhan tumor, invasi dan metastasis tumor
(Agulnik dan Siu, 2005).
Angiogenesis adalah pembentukan pembuluh darah baru yang berasal
dari pembuluh darah yang telah ada (Josko et al, 2000; Rosen, 2002).
Angiogenesis sangat dibutuhkan dalam pembentukan organ baru serta untuk
diferensiasi saat embriogenesis, penyembuhan luka dan fungsi reproduksi
wanita (Josko et al, 2000; Rosen, 2002). Dalam kondisi patologi,
angiogenesis dibutuhkan pada proses pertumbuhan tumor solid dan pada
proses metastasis (Rosen, 2002; Medinger dan Drevs, 2005; Hicklin dan
Ellis, 2005). Tumor membutuhkan angiogenesis untuk tumbuh di atas ukuran
1-2 mm3 (Rosen, 2002). Angiogenesis diperlukan untuk suplai oksigen,
nutrisi, faktor pertumbuhan dan hormon, enzim proteolitik, dan
mempengaruhi faktor hemostatik yang mengontrol koagulasi dan sistem
fibrinolitik, serta penyebaran sel-sel tumor ke tempat jauh (Hicklin dan Ellis,
2005).
Angiogenesis merupakan proses yang sangat kompleks, yang
faktor-faktor anti angiogenik (Rosen, 2002; Hicklin dan Ellis, 2005). Ekspresi VEGF
dalam sel-sel tumor distimulasi oleh hipoksia, onkogen dan inaktivasi gen
supresor tumor (p53) dan oleh berbagai sitokin (Rosen, 2002). Aktivasi aksis
VEGF / VEGF reseptor (VEGFR) memicu jaringan sinyal multipel yang
menghasilkan survival sel endotel, mitogenesis, migrasi, diferensiasi dan
permeabilitas vaskular serta mobilisasi sel-sel progenitor endotel dari
sumsum tulang ke sirkulasi perifer (Hicklin dan Ellis, 2005).
Karena peran sentralnya dalam angiogenesis tumor, jalur VEGF /
VEGFR telah menjadi fokus utama riset dasar dan pengembangan
obat-obatan di bidang onkologi (Hicklin dan Ellis, 2005).
Berdasarkan latar belakang yang telah diuraikan di atas, peneliti
tertarik untuk mengetahui ekspresi VEGF pada karsinoma hidung dan sinus
paranasal, dimana overekspresi VEGF telah dihubungkan dengan
progresivitas tumor dan prognosis yang buruk.
1.2 Perumusan Masalah
Berdasarkan latar belakang diatas, penderita karsinoma hidung dan
sinus paranasal stadium lanjut memiliki prognosis yang buruk. Peneliti
tertarik untuk mengetahui ekspresi VEGF pada karsinoma hidung dan sinus
paranasal, bagaimana overekspresi VEGF dihubungkan dengan progresivitas
1.3 Tujuan Penelitian 1.3.1. Tujuan Umum
Mengetahui ekspresi Vascular Endothelial Growth Factor pada
karsinoma hidung dan sinus paranasal.
1.3.2. Tujuan Khusus
a. Mengetahui ekspresi VEGF pada penderita karsinoma
hidung dan sinus paranasal.
b. Mengetahui ekspresi VEGF pada berbagai stadium
karsinoma hidung dan sinus paranasal.
c. Mengetahui ekspresi VEGF pada berbagai jenis
histopatologi karsinoma hidung dan sinus paranasal
1.4 Manfaat Penelitian
a. Dapat memahami peran VEGF pada karsinoma hidung dan
sinus paranasal dalam progresifitas dan prognosis penyakit.
b. Sebagai dasar penelitian selanjutnya dalam pemberian anti
VEGF terhadap karsinoma hidung dan sinus paranasal untuk
meningkatkan efek terapi dasar karsinoma hidung dan sinus
BAB 2
TINJAUAN KEPUSTAKAAN
2.1 Tumor Ganas Hidung dan Sinus Paranasal 2.1.1 Anatomi Dan Fisiologi Hidung
Hidung merupakan organ penting yang seharusnya mendapat
perhatian lebih dari biasanya dan hidung merupakan salah satu organ
pelindung tubuh terhadap lingkungan yang tidak menguntungkan. Hidung
terdiri atas hidung luar dan hidung dalam. Hidung luar menonjol pada garis
tengah diantara pipi dengan bibir atas, struktur hidung luar dapat dibedakan
atas tiga bagian yaitu: paling atas kubah tulang yang tak dapat digerakkan,
dibawahnya terdapat kubah kartilago yang sedikit dapat digerakkan dan yang
paling bawah adalah lobolus hidung yang mudah digerakkan
(Ballenger,1994; Hilger, 1997; Levine, 2005).
Bagian puncak hidung biasanya disebut apeks. Agak keatas dan
belakang dari apeks disebut batang hidung (dorsum nasi), yang berlanjut
sampai kepangkal hidung dan menyatu dengan dahi. Yang disebut kolumela
membranosa mulai dari apeks, yaitu diposterior bagian tengah pinggir dan
terletak sebelah distal dari kartilago septum. Titik pertemuan kolumela
dengan bibir atas dikenal sebagai dasar hidung. Disini bagian bibir atas
membentuk cekungan dangkal memanjang dari atas kebawah yang disebut
(lubang hidung) kanan dan kiri, sebelah latero-superior dibatasi oleh ala nasi
dan sebelah inferior oleh dasar hidung (Ballenger, 1994 ; Hilger, 1997).
Hidung luar dibentuk oleh kerangka tulang dan tulang rawan yang
dilapisi oleh kulit, jaringan ikat dan beberapa otot kecil yang berfungsi untuk
melebarkan atau menyempitkan lubang hidung. Bahagian hidung dalam
terdiri atas struktur yang membentang dari os internum disebelah anterior
hingga koana di posterior, yang memisahkan rongga hidung dari nasofaring.
Rongga hidung atau kavum nasi berbentuk terowongan dari depan
kebelakang, dipisahkan oleh septum nasi dibagian tengahnya menjadi kavum
nasi kanan dan kiri. Pintu atau lubang masuk kavum nasi bagian depan
disebut nares anterior dan lubang belakang disebut nares posterior (koana)
yang menghubungkan kavum nasi dengan nasofaring (Ballenger, 1994 ;
Hilger, 1997).
Bagian dari kavum nasi yang letaknya sesuai ala nasi, tepat
dibelakang nares anterior, disebut dengan vestibulum. Vestibulum ini dilapisi
oleh kulit yang banyak mengandung kelenjar sebasea dan rambut-rambut
panjang yang disebut dengan vibrise (Ballenger,1994).
Tiap kavum nasi mempunyai 4 buah dinding yaitu dinding medial,
lateral, inferior dan superior. Dinding medial hidung ialah septum nasi.
Septum nasi ini dibentuk oleh tulang dan tulang rawan, dinding lateral
terdapat konka superior, konka media dan konka inferior. Yang terbesar dan
letaknya paling bawah ialah konka inferior, kemudian yang lebih kecil adalah
ialah konka suprema dan konka suprema biasanya rudimenter. Konka inferior
merupakan tulang tersendiri yang melekat pada os maksila dan labirin
etmoid, sedangkan konka media, superior dan suprema merupakan bagian
dari labirin etmoid. Celah antara konka inferior dengan dasar hidung
dinamakan meatus inferior, berikutnya celah antara konkha media dan
inferior disebut meatus media dan sebelah atas konkha media disebut
meatus superior ( Ballenger, 1994 ; Hilger, 1997)
Meatus medius merupakan salah satu celah yang penting dan
merupakan celah yang lebih luas dibandingkan dengan meatus superior.
Disini terdapat muara dari sinus maksila, sinus frontal dan bagian anterior
sinus etmoid. Dibalik bagian anterior konka media yang letaknya
menggantung, pada dinding lateral terdapat celah yang berbentuk bulat sabit
yang dikenal sebagai infundibulum. Ada suatu muara atau fisura yang
berbentuk bulan sabit menghubungkan meatus medius dengan infundibulum
yang dinamakan hiatus semilunaris. Dinding inferior dan medial infundibulum
membentuk tonjolan yang berbentuk seperti laci dan dikenal sebagai
prosesus unsinatus (Ballenger, 1994).
Di bagian atap dan lateral dari rongga hidung terdapat sinus yang
terdiri atas sinus maksila, etmoid, frontalis dan sphenoid. Dan sinus maksila
merupakan sinus paranasal terbesar diantara lainnya, yang berbentuk
piramid iregular dengan dasarnya menghadap ke fossa nasalis dan
puncaknya kearah apek prosesus zigomatikus os maksilla ( Ballenger, 1994 ;
Perdarahan hidung
Secara garis besar perdarahan hidung berasal dari 3 sumber utama
yaitu
1. Arteri etmoidalis anterior
2. Arteri etmoidalis posterior cabang dari arteri oftalmika
3. Arteri sfenopalatina, cabang terminal arteri maksilaris interna yang
berasal dari arteri karotis eksterna (Ballenger, 1994).
Bagian bawah rongga hidung mendapat pendarahan dari cabang arteri
maksilaris interna, diantaranya ialah ujung arteri palatina mayor dan arteri
sfenopalatina yang keluar dari foramen sfenopalatina bersama nervus
sfenopalatina dan memasuki rongga hidung dibelakang ujung posterior konka
media. Bagian depan hidung mendapat pendarahan dari cabang-cabang
arteri fasialis (Ballenger, 1994; Hilger, 1997).
Pada bagian depan septum terdapat anastomosis dari cabang-cabang
arteri sfenopalatina, arteri etmoid anterior, arteri labialis superior dan arteri
palatina mayor, yang disebut pleksus Kieesselbach (little’s area). Pleksus
Kiesselbach letaknya superfisial dan mudah cedera oleh trauma, sehingga
sering menjadi sumber epistaksis (Ballenger,1994; Hilger,1997).
Vena-vena hidung mempunyai nama yang sama dan berjalan
berdampingan dengan arterinya. Vena di vestibulum dan struktur luar hidung
bermuara ke vena oftalmika yang berhubungan dengan sinus kavernosus
Persarafan hidung
Bagian depan dan atas rongga hidung mendapat persarafan sensoris
dari nervus etmoidalis anterior, yang merupakan cabang dari nervus
nasosiliaris, yang berasal dari nervus oftalmikus. Saraf sensoris untuk hidung
terutama berasal dari cabang oftalmikus dan cabang maksilaris nervus
trigeminus. Cabang pertama nervus trigeminus yaitu nervus oftalmikus
memberikan cabang nervus nasosiliaris yang kemudian bercabang lagi
menjadi nervus etmoidalis anterior dan etmoidalis posterior dan nervus
infratroklearis. Nervus etmoidalis anterior berjalan melewati lamina kribrosa
bagian anterior dan memasuki hidung bersama arteri etmoidalis anterior
melalui foramen etmoidalis anterior, dan disini terbagi lagi menjadi cabang
nasalis internus medial dan lateral. Rongga hidung lainnya, sebagian besar
mendapat persarafan sensoris dari nervus maksila melalui ganglion
sfenopalatina (Ballenger,1994; Hilger,1997). Ganglion sfenopalatina, selain
memberi persarafan sensoris, juga memberikan persarafan vasomotor atau
otonom untuk mukosa hidung. Ganglion ini menerima serabut serabut
sensoris dari nervus maksila. Serabut parasimpatis dari nervus petrosus
profundus. Ganglion sfenopalatina terletak dibelakang dan sedikit di atas
ujung posterior konka media (Ballenger,1994).
Nervus Olfaktorius turun melalui lamina kribrosa dari permukaan
penghidu pada mukosa olfaktorius di daerah sepertiga atas hidung
(Ballenger, 1994; Hilger, 1997).
Fisiologi hidung
Hidung berfungsi sebagai indra penghidu, menyiapkan udara inhalasi
agar dapat digunakan paru serta fungsi filtrasi. Sebagai fungsi penghidu,
hidung memiliki epitel olfaktorius berlapis semu yang berwarna kecoklatan
yang mempunyai tiga macam sel-sel syaraf yaitu sel penunjang, sel basal
dan sel olfaktorius. Fungsi filtrasi, memanaskan dan melembabkan udara
inspirasi akan melindungi saluran napas dibawahnya dari kerusakan. Partikel
yang besarnya 5-6 mikrometer atau lebih, 85% - 90% disaring didalam
hidung dengan bantuan transpor mukosiliar (Ballenger, 1994 ; Hilger, 1997 ;
McCaffrey, 2000).
Fungsi hidung terbagi atas beberapa fungsi utama yaitu (1) Sebagai
jalan nafas, (2) Alat pengatur kondisi udara, (3) Penyaring udara, (4) Sebagai
indra penghidu, (5) Untuk resonansi suara, (6) Turut membantu proses
bicara, (7) Reflek nasal (Ballenger,1994).
2.1.2 Anatomi dan fungsi sinus paranasal
Sinus paranasal merupakan salah satu organ tubuh manusia yang
sangat bervariasi pada setiap individu. Ada empat pasang sinus paranasal
mulai dari yang terbesar adalah sinus maksilla, sinus frontalis, sinus etmoid
tulang-tulang kepala hingga terbentuk rongga didalam tulang-tulang. Semua sinus
mempunyai muara kedalam hidung (Lang,1989).
Sinus maksila
Sinus maksila merupakan sinus paranasal terbesar. Bentuknya
segitiga, dengan dinding anterior sinus adalah permukaan fasial os maksila
yang disebut fossa kanina, dinding posteriornya adalah permukaan
infratemporal maksila, dinding medialnya ialah dinding lateral rongga hidung,
dinding superiornya adalah dasar orbita dan dinding inferiornya ialah
prosesus alveolaris dan palatum. Ostium sinus maksila berada disebelah
superior dinding medial sinus dan bermuara ke hiatus semilunaris berjalan
melalui infundibulum etmoid (Ballenger,1994 ; Weir, 1997).
Sinus frontal
Sinus frontal yang terletak di os frontal mulai terbentuk sejak bulan
keempat fetus, berasal dari sel-sel resesus frontal atau dari sel-sel
infundibulum etmoid. Sesudah lahir, sinus frontal mulai berkembang pada
usia 8-10 tahun dan akan mencapai ukuran maksimal sebelum usia 20 tahun
(Hilger,1997).
Sinus frontal kanan dan kiri biasanya tidak simetris, satu lebih besar
dari pada lainnya dan dipisahkan oleh sekat yang terletak digaris tengah.
Kurang lebih 15 % orang dewasa hanya mempunyai satu sinus frontal dan
adalah 2,8 cm tingginya, lebarnya 2,4 cm dan dalamnya 2cm (Hilger, 1994).
Sinus frontal dipisahkan oleh tulang yang relatif tipis dari orbita dan fossa
serebri anterior, sehingga infeksi dari sinus frontal mudah menjalar kedaerah
ini. Sinus frontal ini berdrainase melalui ostiumnya dan bermuara ke meatus
media (Ballenger,1994).
Sinus etmoid
Dari semua sinus paranasal, sinus etmoid yang paling bervariasi dan
akhir-akhir ini dianggap paling penting, karena dapat merupakan sumber
infeksi bagi sinus-sinus lainnya. Sinus etmoid, mula-mula terbentuk pada
janin berusia 4 bulan dan berkembang sesuai dengan bertambahnya usia
hingga dewasa. Pada orang dewasa bentuk sinus etmoid seperti piramid
dengan dasarnya dibagian posterior. Ukurannya dari anterior ke posterior 4-5
cm, tinggi 2,4 cm dan lebarnya 0,5 cm dibagian anterior dan 1,5 cm dibagian
posterior (Ballenger,1994)
Sinus etmoid berongga-rongga, terdiri dari sel-sel yang menyerupai
sarang tawon. Jumlah sel-selnya sangat bervariasi antara 4-17 sel (rata-rata
9 sel). Ada dua kelompok sel-sel tersebut. Kelompok anterior yang bermuara
kemeatus medius dan kelompok posterior yang bermuara ke meatus
superior. Sel anterior dan posterior dipisahkan oleh lempeng tulang
transversal yang tipis. Tempat perlekatan konka media pada dinding lateral
dan posterior. Kelompok sel anterior terdapat didepan dan bawahnya sedang
kelompok posterior ada di atas dan belakangnya (Ballenger,1994).
Atap sinus etmoid yang disebut fovea etmoidalis berbatasan dengan
lamina kribrosa. Dinding lateral sinus adalah lamina papirasea yang sangat
tipis dan membatasi sinus etmoid dari rongga orbita. Dibagian belakang sinus
etmoid posterior berbatasan dengan sinus sfenoid (Ballenger,1994).
Sinus sfenoid
Sebelum anak berusia 3 tahun sinus sfenoid masih kecil, namun telah
berkembang sempurna pada usia 12 sampai 15 tahun. Letaknya didalam os
sfenoid dan ukuran serta bentuknya sangat bervariasi. Sepasang sinus ini
dipisahkan satu sama lain oleh septum tulang yang tipis, letaknya jarang di
tengah, sehingga salah satu sinus akan lebih besar dari pada sisi lainnya
(Ballenger,1994)
Masing-masing sinus sfenoid berhubungan dengan meatus superior
melalui celah kecil menuju ke resesus sfeno-etmoidalis. Ukuran ostium sinus
sfenoid berkisar antara 0,5 sampai 4 mm dan letaknya kira 10 sampai 20 mm
di atas dasar sinus. Ukuran sinus ini kira-kira : usia 1 tahun 2,5 x 2,5 x 1,5
mm dan pada usia 9 tahun 15 x 12 x 10,5 mm. Isi rata-rata sekitar 7,5 ml
(0,05 sampai 30 ml). Batas-batasnya ialah sebelah superior terdapat fossa
serebri media dan kelenjar hipofisa, sebelah inferiornya atap nasofaring,
interna dan disebelah posteriornya berbatasan dengan fossa serebri posterior
didaerah pons (Ballenger,1994).
Fungsi sinus paranasal
Beberapa teori yang dikemukakan sebagai fungsi sinus paranasal antara lain
a. Sebagai pengatur kondisi udara (air conditioning)
Sinus berfungsi sebagai ruang tambahan untuk memanaskan dan
mengatur kelembaban udara inspirasi. Volume pertukaran udara dalam
ventilasi sinus kurang lebih 1/1000 volume sinus pada tiap kali bernafas
sehingga diperlukan beberapa jam untuk pertukaran udara total dalam sinus
(Soetjipto dan Mangunkusumo, 2004).
b. Sebagai penahan suhu (thermal insulators)
Sinus paranasal berfungsi sebagai penahan (buffer) panas, melindungi
orbita dan fossa serebri dari suhu rongga hidung yang berubah-ubah
(Soetjipto dan Mangunkusumo, 2004).
c. Membantu keseimbangan kepala
Sinus membantu keseimbangan kepala karena mengurangi berat
tulang muka. Akan tetapi bila udara dalam sinus diganti dengan tulang, hanya
sehingga teori ini dianggap tidak bermakna (Soetjipto dan Mangunkusumo,
2004).
d. Membantu resonansi suara
Sinus mungkin berfungsi sebagai rongga untuk resonansi suara dan
mempengaruhi kualitas suara. Akan tetapi ada yang berpendapat, posisi
sinus dan ostiumnya tidak memungkinkan sinus berfungsi sebagai resonator
yang efektif (Soetjipto dan Mangunkusumo, 2004).
e. Sebagai peredam perubahan tekanan udara
Fungsi ini berjalan bila ada perubahan tekanan yang besar dan
mendadak, misalnya pada waktu bersin atau membuang ingus (Soetjipto dan
Mangunkusumo, 2004).
f. Membantu produksi mukus
Mukus yang dihasilkan oleh sinus paranasal memang jumlahnya kecil
dibandingkan dengan mukus dari rongga hidung, namun efektif untuk
membersihkan partikel yang turut masuk dengan udara inspirasi karena
mukus ini keluar dari meatus medius (Soetjipto dan Mangunkusumo, 2004).
2.1.3 Epidemiologi
Tumor ganas di daerah hidung dan sinus paranasal relatif jarang
hanya sekitar tiga persen dari malignansi di daerah kepala dan leher (Tufano
et al, 1999; Michael et al, 2005). Diperkirakan 55% tumor ganas hidung dan
sinus paranasal berasal dari sinus maksila, 35% dari kavum nasi, sembilan
persen dari sinus etmoid dan sisanya dari sinus frontal dan sinus sfenoid
(Fasunla dan Lasisi, 2007).
Insiden tertinggi tumor ganas hidung dan sinus paranasal ditemukan di
Jepang yaitu dua per 100.000 penduduk pertahun. Di bagian THT FK UI RS
Cipto Mangunkusumo, keganasan ini ditemukan pada 10,1% dari seluruh
tumor ganas THT. Laki-laki ditemukan lebih banyak dengan rasio laki-laki
banding wanita sebesar 2:1 (Roezin, Mangunkusumo, Soetjipto, 2004). Rifqi
mengemukakan data yang dikumpulkannya dari rumah sakit umum di
sepuluh kota besar di Indonesia bahwa frekuensi tumor hidung dan sinus
adalah 9,3 – 25,3% dari keganasan THT dan berada pada peringkat kedua
sesudah tumor ganas nasofaring (Tjahyadewi dan Wiratno, 1999). Di RSUP
H. Adam Malik Medan selama Januari 2002 sampai dengan Desember 2008
pasien yang dirawat dengan diagnosa tumor ganas hidung dan sinus
paranasal adalah sebanyak 52 kasus.
Insidensi di India sekitar 0,44% dari seluruh keganasan di India
dengan perbandingan antara pria dan wanita adalah 0,57% banding 0,44%.
Insiden pada tahun 2000 adalah 0,3 per 100.000 penduduk. Kebanyakan
melibatkan sinus maksila diikuti dengan sinus etmoid, frontal dan sfenoid.
2.1.4 Etiologi
Etiologi tumor ganas hidung dan sinus paranasal masih belum
diketahui dengan pasti, tetapi diduga terpapar beberapa zat hasil industri.
Pekerja-pekerja pada industri logam berat yang terpapar dengan nikel,
chromium dan radium menunjukkan peningkatan insiden tumor ganas hidung
dan sinus paranasal. Selain itu terdapat beberapa zat yang diduga sebagai
penyebab yaitu gas mustard, larutan isopropil dan senyawa hidrokarbon.
Rokok, alkohol, makanan yang diasinkan atau diasap diduga meningkatkan
kemungkinan terjadi keganasan, sebaliknya buah-buahan dan sayuran
mengurangi kemungkinan terjadi keganasan (Bhattacharyya, 2002; Lund,
2003; Roezin, Mangunkusumo, Soetjipto, 2004; Zimmer dan Carau, 2006).
2.1.5 Patologi
Tumor ganas di daerah hidung dan sinus paranasal menurut
histopatologinya dibagi atas:
a. Epitel: - Karsinoma sel skuamus
- Karsinoma sel transisional
- Adenokarsinoma
- Adenoid kistik karsinoma
- Melanoma
- Neuroblastoma olfaktorius
b. Non epitel - Sarkoma jaringan lunak
- Rhabdomyosarkoma
- Leiomyosarkoma
- Fibrosarkoma
- Liposarkoma
- Angiosarkoma
- Miksosarkoma
- Hemangioperisitoma
- Sarkoma jaringan penghubung
- Kondrosarkoma
- Osteosarkoma
c. Tumor limforetikular: - limfoma
- Plasmasitoma
- Tumor giant sel
Sebagian besar keganasan pada hidung dan sinus paranasal berasal
dari epitel (Zimmer dan Carrau, 2006).
2.1.6 Gejala Klinis
Gejala tergantung dari asal primer tumor serta arah dan perluasannya.
Biasanya tumor didalam sinus maksila tidak memberikan gejala sampai
terjadi perluasan ke organ lain, dan sering ditemukan secara kebetulan pada
menyerupai gejala sinusitis seperti obstruksi hidung unilateral dan rinorea,
sekretnya sering bercampur darah atau terjadi epistaksis (Wong dan Krause,
2001; Roezin, Mangunkusumo, Soetjipto, 2004; Dhingra, 2007).
Pada stadium lanjut dapat terjadi penyebaran ke organ lain sehingga
sukar ditentukan asal tumor primernya. Perluasan tumor dapat menimbulkan
keluhan sebagai berikut:
a. Perluasan ke medial akan menyebabkan gejala hidung tersumbat,
rinore kronik satu sisi disertai epistaksis. Tumor dapat juga terlihat di
kavum nasi.
b. Perluasan keatas melalui dasar orbita menyebabkan diplopia dan
pendorongan bola mata.
c. Perluasan kearah anterior menyebabkan pembesaran pipi satu sisi,
sehingga muka menjadi asimetris. Kadang-kadang terjadi infiltrasi dan
ulserasi. Bila mengenai nervus infra orbitalis, dapat menyebabkan
parestesi kulit pipi.
d. Tumor yang berasal dari dasar antrum dan meluas kearah bawah
menimbulkan keluhan-keluhan gigi. Dapat juga timbul bengkak dan
ulserasi pada palatum, prosesus alveolaris atau sulkus gingivobukal.
e. Perluasan kearah belakang, dapat ke fossa pterigomaksila dan lamina
pterigoid, dan penyebarannya juga dapat ke nasofaring, sinus sfenoid
dan dasar tengkorak.
f. Penyebaran intrakranial dapat terjadi melalui etmoid, fossa kribiformis
g. Penyebaran limfatik jarang terjadi, hanya pada stadium lanjut. Paling
sering adalah pembengkakan kelenjar getah bening di daerah sub
mandibula.
h. Metastasis jauh jarang terjadi, paling sering terjadi di paru dan
kadang-kadang pada tulang (Dhingra, 2007)
2.1.7 Diagnosis
Diagnosis dapat ditegakkan berdasarkan anamnesis, pemeriksaan
fisik, radiologi dan biopsi. Diagnosis pasti ditegakkan berdasarkan
pemeriksaan histopatologi (Wong dan Krause, 2001; Roezin,
Mangunkusumo, Soetjipto, 2004; Dhingra, 2007).
2.1.8 Klasifikasi Klinis a. Klasifikasi Ohngren
Bidang imajiner yang melalui kantus medius dan angulus mandibula.
Bidang ini membagi rahang atas menjadi struktur superior posterior
(suprastruktur) dan struktur inferior anterior (infrastruktur). Adapun
yang termasuk suprastruktur adalah dinding tulang sinus maksila
bagian posterior dan separuh bagian posterior dinding atas. Tumor di
dibandingkan tumor di daerah suprastruktur (Wong dan Kraus, 2001;
Dhingra, 2007).
b. Klasifikasi Lederman’s
Membuat dua garis horizontal melalui dasar orbita dan melalui dasar
antrum. Garis tersebut membagi daerah:
1) Suprastruktur: sinus etmoid, sinus sfenoid, sinus frontal serta
daerah olfaktorius dari hidung.
2) Mesostruktur: sinus maksilaris dan daerah respiratori hidung.
3) Infrastruktur: meliputi prosesus alveolaris.
Klasifikasi tersebut selanjutnya menggunakan garis vertikal sejajar
dinding medial orbita dan membagi sinus etmoid dan fossa nasalis dari
sinus maksila (Dhingra, 2007)
2.1.9 Stadium Tumor
Cara penentuan stadium tumor ganas hidung dan sinus paranasal
yang terbaru adalah menurut American Joint Committee on Cancer (AJCC)
2006 yaitu (Grene et al, 2006; Scurry et al, 2007):
Tumor primer (T) Sinus maksila
TX Tumor primer tidak bisa ditentukan
T0 Tidak tampak tumor primer
Tis Kasinoma insitu
Tulang
T2 Tumor menyebabkan erosi dan destruksi tulang hingga palatum dan
atau meatus media tanpa melibatkan dinding posterior sinus maksila
dan fossa pterigoid
T3 Tumor menginvasi dinding posterior tulang sinus maksila, jaringan
subkutan, dinding dasar dan medial orbita, fossa pterigoid, sinus
etmoid.
T4a Tumor menginvasi bagian anterior orbita, kulit pipi, fossa pterigoid,
fossa infratemporal, fossa kribriformis, sinus sfenoid atau frontal
T4b Tumor menginvasi salah satu dari apek orbita, dura, otak, fossa kranial
medial, nervus kranialis selain dari divisi maksilaris nervus V,
nasofaring atau klivus
Kavum nasi dan sinus etmoid
TX Tumor primer tidak bisa ditentukan
T0 Tidak tampak tumor
Tis Karsinoma insitu
T1 Tumor terbatas pada salah satu bagian dengan atau tanpa invasi
tulang
T2 Tumor berada di dua bagian dalam satu regio atau tumor meluas dan
melibatkan daerah nasoetmoidal kompleks dengan atau tanpa invasi
T3 tumor menginvasi dinding medial atau dasar orbita, sinus maksila,
palatum atau fossa kribriformis.
T4a Tumor menginvasi salah satu dari bagian anterior orbita, kulit hidung
dan pipi, ekstensi minimal ke fossa kranialis anterior, fossa pterigoid,
sinus sfenoid atau frontal.
T4b Tumor menginvasi salah satu dari apeks orbita, dura, otak, fossa
kranial medial, nervus kranialis selain nervus V, nasofaring atau klivus
Kelenjar getah bening regional (N)
NX Tidak dapat ditentukan pembesaran kelenjar
N0 Tidak ada pembesarah kelenjar
N1 Pembesaran satu kelenjar ipsilateral < 3 cm
N2 Pembesaran satu kelenjar ipsilateral 3-6 cm, atau multipel kelenjar
ipsilateral < 6 cm atau metastasis bilateral atau kontralateral < 6 cm
N2a Metastasis satu kelenjar ipsilateral 3-6 cm
N2b Metastasis multipel kelanjar ipsilateral, tidak lebih dari 6 cm.
N2c Metastasis kelenjar bilateral atau kontralateral, tidak lebih dari 6 cm.
N3 Metastasis kelenjar limfe lebih dari 6 cm
Metastasis jauh (M)
MX Metastasis jauh tidak bisa ditentukan
M0 Tidak ada metastasis jauh
M1 Terdapat metastasis jauh
I T1 N0 M0
II T2 N0 M0
III T3 N0 M0
T1 N1 M0
T2 N1 M0
T3 N1 M0
IVA T4a N0 M0
T4a N1 M0
T1 N2 M0
T2 N2 M0
T3 N2 M0
T4a N2 M0
IVB T4b semua N M0
semua T N3 M0
IVC semua T semua N M1
2.1.10 Penatalaksanaan
Sampai sekarang belum ada parameter pengobatan untuk tumor
ganas hidung dan sinus paranasal. Para ahli berpendapat bahwa satu cara
pengobatan saja hasilnya adalah buruk, sehingga mereka menganjurkan
cara terapi kombinasi antara operasi, radioterapi dan kemoterapi (Roezin,
Mangunkusumo, Soetjipto, 2004; Dhingra, 2007).
Operasi merupakan modal utama dalam mengatasi keganasan hidung
dan sinus paranasal. Oleh karena sebagian besar keganasan hidung dan
sinus paranasal berasal dari sinus maksila sehingga operasi maksilektomi
menjadi pilihan utama baik parsial maupun total maksilektomi tergantung
perluasan dan keganasan tumor (Roezin, Mangunkusumo, Soetjipto, 2004).
b. Radioterapi
Radioterapi dapat digunakan sebagai modalitas tunggal, sebagai
tambahan pada operasi, atau sebagai terapi paliatif. Penelitian terbaru
menyebutkan bahwa radioterapi pasca operasi dapat meningkatkan kontrol
lokal tetapi tidak menyebabkan angka bertahan hidup yang absolut. Para ahli
lebih menyukai radioterapi pasca operasi karena volume tumor yang lebih
kecil dapat dimusnahkan, dan batas tumor yang tidak teradiasi menjadi lebih
jelas saat dilakukan operasi dan juga penyembuhan luka pasca operasi lebih
dapat diprediksi (Zimmer dan Carrau, 2006)
c. Kemoterapi
Penggunaan kemoterapi pada keganasan hidung dan sinus paranasal
adalah sebagai terapi paliatif untuk mengurangi rasa sakit. Samant dkk
(2004) melaporkan penggunaan Cisplatin intra arteri dosis tinggi dengan
radioterapi konkomitan pada pasien dengan karsinoma sinus paranasal.
Angka bertahan hidup selama lima tahun adalah 53%. Pasien-pasien yang
mempunyai resiko operasi yang buruk dan menolak untuk dilakukan operasi
dapat dilakukan kombinasi terapi antara radioterapi dan kemoterapi (Zimmer
2.2 Vascular Endothelial Growth Factor
2.2.1 Angiogenesis
Angiogenesis adalah pembentukan pembuluh darah baru yang berasal
dari pembuluh darah yang telah ada (Josko et al, 2000; Rosen, 2002).
Angiogenesis sangat dibutuhkan dalam pembentukan organ baru serta untuk
diferensiasi saat embriogenesis, penyembuhan luka dan fungsi reproduksi
wanita (Josko et al, 2000; Rosen, 2002). Angiogenesis dapat dipicu oleh
berbagai kondisi patologis, seperti reumatoid artritis, retinopati diabetik,
degenerasi makular, psoriasis dan pertumbuhan serta metastasis tumor.
(Rosen, 2002; Plank dan Sleeman, 2003).
Tumor membutuhkan angiogenesis untuk tumbuh di atas ukuran 1-2
mm3 (Rosen, 2002). Angiogenesis diperlukan untuk suplai oksigen, nutrien,
faktor pertumbuhan dan hormon, enzim proteolitik, mempengaruhi faktor
hemostatik yang mengontrol koagulasi dan sistem fibrinolitik, dan penyebaran
sel-sel tumor ke tempat jauh. (Hicklin dan Ellis, 2005).
Angiogenesis merupakan proses yang sangat kompleks, yang
diregulasi secara ketat oleh faktor-faktor proangiogenik (VEGF) dan
faktor-faktor anti angiogenik (Rosen, 2002; Hicklin dan Ellis, 2005). Suatu tumor
avaskular bergantung pada difusi pasif untuk suplai oksigen dan makanan
serta untuk pembuangan produk sisa. Hal ini membatasi ukuran tumor
sampai sekitar 2 mm, yang disebut keadaan dorman. Sel-sel tumor yang
hipoksik akan memproduksi faktor-faktor pertumbuhan, termasuk VEGF.
Mulanya inhibitor melebihi faktor pertumbuhan dan sel endotel tetap diam.
Akan tetapi, saat tumor mampu memproduksi cukup faktor pertumbuhan
dan/atau menekan ekspresi inhibitor, akan terjadi ‘angiogenic switch’ menuju
proses angiogenesis (Plank dan Sleeman, 2003). ‘Angiogenic switch’
merupakan pertanda proses malignansi (Hicklin dan Ellis, 2005).
2.2.2 Angiogenesis yang Diinduksi Tumor
Model terkini proses angiogenesis tumor menyarankan bahwa proses
ini melibatkan tumbuhnya tunas pembuluh dari pembuluh darah yang ada
dan menyatunya progenitor endotel menjadi pembuluh vaskular baru. Proses
ini meliputi berbagai kejadian yaitu proliferasi, migrasi dan invasi sel-sel
endotel, organisasi sel-sel endotel menjadi struktur tubular yang fungsional,
maturasi pembuluh, dan regresi pembuluh (Detmar, 2000; Hicklin dan Ellis,
2005). Pada jaringan normal, kestabilan vaskular dipertahankan oleh
pengaruh yang dominan dari inhibitor angiogenesis endogen terhadap
stimulus angiogenik, sebaliknya angiogenesis tumor diinduksi oleh
peningkatan sekresi faktor angiogenik dan/atau penurunan regulasi inhibitor
angiogenesis (Detmar, 2000).
Permulaan Angiogenesis
Pada permulaan angiogenesis, stimulus angiogenik yang diterima
menyebabkan sel endotel kapiler sekitar tumor teraktivasi, kontak yang erat
(protease) yang mempunyai efek mendegradasi jaringan ekstraseluler. Ada
banyak jenis enzim proteolitik tersebut, tetapi secara garis besar dibagi
menjadi matrix metalloproteases (MMPs) dan plasminogen activator
(PA)/sistem plasmin. Target awal protease adalah membran dasar. Setelah
terdegradasi, sel endotel akan dapat bergerak melalui gap yang ada pada
membran dasar menuju matriks ekstraseluler. Sel-sel endotel sekitar akan
bergerak mengisi gap pada membran dasar dan mengikuti sel-sel endotel
sebelumnya menuju matriks ekstraseluler. Karena itu, fungsi pertama faktor
pertumbuhan angiogenik adalah menstimulasi produksi protease oleh sel-sel
endotel. Hal ini merupakan faktor kunci pada rangkaian angiogenesis, sebab
tanpa adanya aktivitas proteolitik, sel-sel endotel akan dihambat oleh
membran dasar hingga tidak dapat keluar dari kapiler (pembuluh) induk
(Plank dan Sleeman, 2003).
Migrasi Sel Endotel, Proliferasi dan Pembentukan Pembuluh
Setelah ekstravasasi, sel endotel terus mensekresi enzim proteolitik,
yang akan mendegradasi matriks ekstraseluler. Sel endotel terus bergerak
menjauhi pembuluh induk menuju tumor, membentuk tunas kecil. Sel endotel
akan bertambah dari pembuluh induk hingga tunas memanjang. Awalnya
tunas-tunas ini bergerak paralel satu sama lain, akan tetapi pada jarak
tertentu dari pembuluh induk, mulai condong menuju tunas lainnya. Hal ini
akan membentuk loop tertutup (anastomose), yang akan memungkinkan
penting dalam pembentukan jaringan vaskular fungsional, akan tetapi
stimulus yang pasti terhadap perubahan arah tunas dan anastomosis masih
belum diketahui (Plank dan Sleeman, 2003).
Fase Vaskular
Dalam fase vaskular, pada angiogenesis fisiologis, ketika jaringan
target telah tervaskularisasi, ekspresi faktor pertumbuhan angiogenik akan
berkurang. Migrasi, proliferasi dan proteolisis sel-sel endotel akan berhenti
dan pembuluh darah yang baru terbentuk mengalami proses maturasi. Ikatan
yang kuat antar sel distabilkan di endotel dan sel endotel mensekresi protein
(laminin, kolagen) untuk membentuk membran dasar. Akhirnya sel-sel
penyokong periendotel (perisit) direkrut dan pembuluh darah baru menjadi
bagian sistem vaskular yang stabil. Proses maturasi biasanya tidak terjadi
pada angiogenesis tumor, karena masih tetap terdapat daerah hipoksik di
dalam tumor yang tetap memproduksi faktor angiogenik. Selain itu, ketika
daerah vaskularisasi yang baru pada tumor terus bertambah, akan melebihi
suplai darahnya sendiri sehingga menimbulkan daerah hipoksik sendiri.
Angiogenesis akan terus berlangsung dan kapiler-kapiler baru terus tumbuh,
meningkatkan suplai darah ke tumor yang sekarang tumbuh pesat dan
heterogen (Plank dan Sleeman, 2003).
Akan tetapi, berlanjutnya angiogenesis akan meningkatkan
yang sangat ganas, kebutuhan akan pembuluh darah baru biasanya tidak
pernah terpenuhi (Plank dan Sleeman, 2003).
Kapiler tumor biasanya tidak matang dan tidak stabil karena tidak
terbentuknya membran dasar, disebabkan faktor angiogenik terus diproduksi.
Pembuluh baru akan berbentuk ireguler, rapuh dan berliku-liku (Plank dan
Sleeman, 2003).
2.2.3 Famili VEGF
Famili VEGF yang secara genetik berhubungan sebagai faktor
pertumbuhan angiogenik dan limfangiogenik terdiri dari 6 glikoprotein yaitu
VEGF-A (biasa disebut VEGF), VEGF-B, VEGF-C, VEGF-D, VEGF-E, dan
placenta growth factor (PlGF) (Hicklin dan Ellis, 2005).
In vivo, ekspresi VEGF-A telah menunjukkan peran kuncinya dalam
vaskulogenesis fisiologik dan angiogenesis. Pada tikus, delesi homozigot dan
heterozigot pada gen VEGF secara embrionik letal, menimbulkan defek pada
vaskulogenesis dan abnormalitas kardiovaskular. VEGF-A juga berperan
penting dalam proses angiogenik postnatal, termasuk penyembuhan luka,
ovulasi, menstruasi, mempertahankan tekanan darah serta kehamilan.
VEGF-A juga telah dihubungkan dengan berbagai kondisi patologis yang
berkaitan dengan peningkatan angiogenesis, seperti artritis, psoriasis,
degenerasi makular dan retinopati diabetik (Hicklin dan Ellis, 2005).
Pada tikus, ketiadaan VEGF-B dan PlGF menunjukkan tidak ada defek
yang menyarankan bahwa peran VEGF-B dan PlGF mungkin berlebihan.
Akan tetapi tidak adanya PlGF akan mengganggu angiogenesis, ekstravasasi
plasma, dan pertumbuhan kolateral saat iskemia, peradangan, penyembuhan
luka dan pertumbuhan tumor yang menyarankan bahwa peran PlGF pada
keadaan patologis yang terjadi pada orang dewasa (Hicklin dan Ellis, 2005).
Homolog VEGF yaitu VEGF-C dan VEGF-D memegang peran kunci
pada limfangiogenesis saat embrionik dan postnatal. Delesi homozigot gen
VEGF-C pada tikus bersifat letal embrionik dan delesi heterozigot akan
menyebabkan defek postnatal yang berhubungan dengan defek
perkembangan limfatik. VEGF-C dan VEGF-D mungkin juga berperan dalam
pertumbuhan pembuluh darah baru, terutama pada keadaan patologik seperti
pertumbuhan tumor. Akan tetapi perannya pada angiogenesis tumor masih
belum jelas. VEGF-E bukan homolog VEGF mamalia, tetapi protein viral yang
dikode virus Orf parapoxvirus (Hicklin dan Ellis, 2005; Guang, 2007).
2.2.4 Reseptor VEGF
Ligan VEGF menengahi efek angiogeniknya melalui reseptor yang
berbeda. Dua reseptor diidentifikasi pada sel endotel dikenal sebagai
reseptor tirosin kinase spesifik VEGFR-1 (fms-like tyrosine kinase1/Flt-1) dan
VEGFR-2 (KDR/Flk-1). Saat ini VEGFR-3 (fms-like tyrosine kinase 4/Flt-4)
telah diidentifikasi dan dihubungkan dengan proses limfangiogenesis
VEGFR-1 merupakan reseptor untuk VEGF-A dan mempunyai
kemampuan untuk mengikat VEGF-B dan PlGF. VEGFR-1 sangat penting
untuk angiogenesis fisiologik dan angiogenesis pertumbuhan. Beberapa studi
juga mengindikasikan bahwa VEGFR-1 mempunyai peran fungsional positif
pada beberapa tipe sel, yang berpartisipasi pada migrasi monosit, rekrutmen
progenitor sel endotel, meningkatkan sifat adesif sel-sel natural killer, dan
menginduksi faktor pertumbuhan dari sel-sel sinusoidal hati (Hicklin dan Ellis,
2005; Shibuya, 2006).
Studi oleh Autiero dkk. menunjukkan aktivasi VEGFR-1 oleh PlGF
menyebabkan transfosforilasi VEGFR-2 pada sel endotel sehingga terjadi
koekspresi terhadap reseptor tersebut. Studi lain menunjukkan bahwa pada
kondisi patologik seperti tumorigenesis, VEGFR-1 merupakan regulator
angiogenesis yang positif dan poten. Bukti terakhir menyarankan fungsi
VEGFR-1 berbeda sesuai tahap perkembangan, berbagai kondisi patologik
dan fisiologik, dan tipe sel dimana dia diekspresikan (Hicklin dan Ellis, 2005;
Shibuya, 2006).
VEGFR-2 menengahi mayoritas efek akhir VEGF-A pada
angiogenesis, termasuk permeabilitas mikrovaskular, proliferasi, invasi,
migrasi dan survival sel endotel. Aktivasi spesifik VEGFR-2 dengan VEGF-E
telah menunjukkan aktivitas sel endotel yang poten in vitro dan in vivo,
dengan kuat menyokong gagasan bahwa aktivasi VEGFR-2 sendiri dapat
secara efisien menstimulasi angiogenesis. Seperti telah dijelaskan
dipengaruhi ko-ekspresi dan aktivasi VEGFR-1 (Hicklin dan Ellis, 2005;
Shibuya, 2006; Tabernero, 2007).
VEGFR-3 adalah reseptor tirosin kinase yang berasal dari klon lapisan
sel leukemia dan plasenta manusia. VEGFR-3 condong berikatan dengan
VEGF-C dan VEGF-D. VEGFR-3 diekspresikan melalui vaskulatur embrionik,
tapi saat perkembangan dan ketika dewasa, ekspresinya terbatas pada
sel-sel endotel limfatik. Pada manusia dewasa, VEGFR-3 dipercaya mempunyai
berbagai peran : membantu perkembangan kardiovaskular dan pembentukan
jaringan vaskular primer saat embriogenesis, dan memfasilitasi
limfangiogenesis ketika dewasa. Aktivasi dan peningkatan regulasi ligan
VEGFR-3 telah diobservasi pada beberapa neoplasma, seperti kanker
payudara dan melanoma, dengan peningkatan level VEGF-C dan VEGF-D
yang berhubungan dengan metastase kelenjar limfe pada pasien. Inhibisi
sinyal VEGFR-3 dengan menggunakan VEGFR-3 solubel menunjukkan
pengurangan limfangiogenesis dan metastase kelenjar limfe tumor (Hicklin
dan Ellis, 2005; Shibuya, 2006).
2.2.5 Peran VEGF Pada Angiogenesis
Vascular Endothelial Growth Factor merupakan golongan faktor
angiogenik terbaik. Telah jelas ditemukan bahwa VEGF adalah kekuatan
utama dibalik angiogenesis tumor dan pembentukan seluruh pembuluh
darah. Tiga aktivitas pokok sel endotel dalam angiogenesis yaitu sekresi
tersebut dan bekerja secara spesifik pada sel endotel (VEGFR secara
eksklusif terekspresi pada sel endotel). VEGF juga bertindak sebagai faktor
survival sel endotel dengan menghambat apoptosis. (Rosen, 2002; Plank dan
Sleeman, 2003). Fungsi VEGF pada sel endotel yaitu meningkatkan
permeabilitas vaskular 50.000 kali lebih poten dari histamin. VEGF
mengaktivasi sel endotel dengan efek perubahan morfologi sel endotel,
perubahan cytoskeleton, dan menstimulasi migrasi dan pertumbuhan sel
endotel. VEGF bersifat mitogen terhadap sel endotel yang menyebabkan
proliferasi sel. VEGF juga menginduksi berbagai enzim dan protein yang
penting untuk proses degradasi membran dasar, yang berguna bagi sel
endotel untuk migrasi dan invasi yang merupakan tahap penting pada
angiogenesis (Hicklin dan Ellis, 2005).
Permeabilitas
VEGF sebenarnya ditemukan karena kemampuannya membuat vena
dan vena kecil hiperpermeabel terhadap molekul makro dalam sirkulasi,
sehingga pertama kali disebut sebagai vascular permeability factor (VPF).
Faktanya VEGF salah satu penginduksi permeabilitas vaskular yang paling
poten, 50.000 kali lebih poten dari histamin. Kemampuannya untuk
meningkatkan permeabilitas mikrovaskular merupakan salah satu peran yang
paling penting untuk VEGF, terutama dengan mempertimbangkan
hipermeabilitas pembuluh tumor yang diperkirakan berperan besar untuk
Mekanisme pasti bagaimana VEGF meningkatkan permeabilitas
mikrovaskular belum sepenuhnya jelas. Studi terakhir menyarankan bahwa
VEGF menginduksi permeabilitas mungkin dimediasi via jalur calcium
dependent yang melibatkan produksi oksida nitrat dan aktivasi jalur Akt dan
peningkatan cGMP, dengan aktivasi jalur Erk1/2 dengan cara stimulasi
prostaglandin PGI2 (Hicklin dan Ellis, 2005).
Aktivasi Sel Endotel
VEGF menghasilkan berbagai efek yang berbeda pada sel-sel endotel
dan endotel vaskular. Efek-efek tersebut termasuk perubahan dalam
morfologi sel endotel, perubahan cytoskeleton, dan stimulasi pertumbuhan
dan migrasi sel endotel. VEGF menyebabkan peningkatan ekspresi berbagai
gen-gen sel endotel yang berbeda, termasuk faktor jaringan prokoagulan;
protein jalur fibrinolitik, termasuk urokinase, aktivator plasminogen tipe
jaringan, inhibitor aktivator plasminogen tipe 1, dan urokinase inhibitor; matrix
metalloprotease; GLUT-1 transporter glukosa; sintase oksida nitrat; integrin;
dan berbagai mitogen (Hicklin dan Ellis, 2005).
Survival
VEGF pertama kali tampak bekerja sebagai faktor survival pada sel-sel
endotel retina, dan sekarang telah menunjukkan kerjanya dalam menyokong
survival beberapa macam sel-sel endotel baik in vitro dan in vivo. In vitro,
mengaktivasi jalur PI3K-Akt yang juga meningkatkan regulasi protein
antiapoptotik seperti bcl-2 dan A1; hal ini akan menhambat aktivasi caspase,
dan meningkatkan regulasi anggota famili penghambat apoptosis termasuk
survivin dan XIAP. VEGF juga mengaktivasi focal adhesion kinase (FAK) dan
protein yang berhubungan yang telah menunjukkan kerjanya
mempertahankan sinyal survival sel-sel endotel (Hicklin dan Ellis, 2005).
In vivo, injeksi VEGF eksogen dapat mempertahankan pembuluh
retina yang belum matang dari kerusakan, dan ketergantungan terhadap
VEGF telah didapati pada sel-sel endotel pembuluh tumor yang baru
terbentuk, tetapi tidak didapati pada pembuluh tumor yang telah stabil (Hicklin
dan Ellis, 2005).
Proliferasi
VEGF adalah suatu mitogen bagi sel-sel endotel. Proliferasi sel
endotel ini tampaknya melibatkan aktivasi Erk1/2 kinase yang dimediasi
VEGFR-2. Aktivitas mitogenik VEGF mungkin juga melibatkan jalur protein
kinase C, yang sebagian diregulasi oleh oksida nitrat. Walau peran mitogen
VEGF penting bagi sel endotel, penting dicatat bahwa faktor angiogenik lain
peran mitogennya bagi sel endotel lebih baik. Akan tetapi faktor angiogenik
lain aktivitas pluripotennya kurang dibandingkan VEGF untuk proses-proses
Invasi dan Migrasi
Degradasi membran dasar dibutuhkan untuk migrasi dan invasi sel
endotel dan merupakan langkah awal yang penting dalam memulai
angiogenesis. VEGF menginduksi berbagai macam enzim dan protein yang
penting untuk proses degradasi, termasuk matrix degrading
metalloproteinases, metalloproteinase interstitial collagenase, dan serin
protease seperti urokinase-type plasminogen activator (uPA) dan tissue-type
plasminogen activator (TTPA). Aktivasi bahan-bahan tersebut mengarah ke
lingkungan yang prodegradasi yang memfasilitasi migrasi dan pertunasan sel
endotel (Hicklin dan Ellis, 2005).
Mekanisme intraselular dimana VEGF menyebabkan peningkatan
migrasi sel endotel belum sepenuhnya dimengerti, tetapi tampaknya
melibatkan sinyal yang berhubungan dengan FAK yang menyebabkan
pergantian adhesi fokal dan organisasi filamen actin serta reorganisasi actin
yang diinduksi MAPK p38. Sebagai tambahan, telah diusulkan bahwa oksida
nitrat juga berperan penting dalam migrasi sel endotel yang diinduksi VEGF.
Oksida nitrat telah diimplikasikan dalam proses podokinesis sel endotel dan
aktivasi sintase oksida nitrat endotel yang tergantung pada Akt yang
dibutuhkan pada proses migrasi sel yang diinduksi VEGF (Hicklin dan Ellis,
2005).