KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA ISOLASI SENYAWA STEROID/TRITERPENOID
DARI EKSTRAK
n
-HEKSAN RUMPUT LAUT
Turbinaria
ornata
(Turner) J. Agardh.
SKRIPSI
OLEH:
DINDA ADELIA AZHARI
NIM 121524114
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA ISOLASI SENYAWA STEROI/TRITERPENOID
DARI EKSTRAK n-HEKSAN RUMPUT LAUT
Turbinaria ornata
(Turner) J. Agardh
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DINDA ADELIA AZHARI
NIM 121524114
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA ISOLASI SENYAWA STEROID/TRITERPENOID DARI EKSTRAK
n-HEKSAN RUMPUT LAUT Turbinaria ornata (Turner) J. Agardh
OLEH:
DINDA ADELIA AZHARI NIM 121524114
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 6 Februari 2015
Disetujui oleh:
Pembimbing I, Panitia Penguji,
Dra. Aswita Hafni Lubis, M.Si., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 195304031983032001 NIP 195709091985112001
Dra. Aswita Hafni Lubis, M.Si., Apt. Pembimbing II, NIP 195304031983032001
Dra. Suwarti Aris, M.Si., Apt. Dra. Herawaty Ginting, M.Si., Apt NIP 195107231982032001 NIP 195112231980032002
Dra. Erly Sitompul, M.Si., Apt. NIP 195006121980032001
Medan, April 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah memberikan karunia
yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang
berjudul “Karakterisasi Simplisia dan Skrining Fitokimia serta Isolasi Senyawa
Steroid/Triterpenoid dari Ekstrak n-Heksan Rumput Laut Turbinaria ornata
(Turner) J. Agardh”. Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera
Utara.
Penulis menyampaikan terima kasih yang sebesar-besarnya kepada Ibu
Dra. Aswita Hafni Lubis, M.Si., Apt., dan Ibu Dra. Suwarti Aris, M.Si., Apt.,
yang telah meluangkan waktu dan tenaga dalam membimbing penulis dengan
penuh kesabaran dan tanggung jawab, memberikan petunjuk dan saran-saran
selama penelitian hingga selesainya skripsi ini. Kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan Fakultas Farmasi yang telah menyediakan
fasilitas kepada penulis selama perkuliahan di Fakultas Farmasi. Penulis juga
mengucapkan terima kasih kepada Ibu Dr. Marline Nainggolan, M.S., Apt., selaku
ketua penguji, Ibu Dra.
Sitompul, M.Si., Apt selaku anggota penguji yang telah memberikan saran untuk
menyempurnakan skripsi ini serta Bapak dan Ibu staf pengajar Fakultas Farmasi
USU yang telah banyak membimbing penulis selama masa perkuliahan hingga
selesai.
Penulis juga mempersembahkan rasa terima kasih yang tak terhingga
Yuniati, Yunaida dan Yunita atas limpahan kasih sayang, semangat dan doa yang
tak ternilai dengan apa pun.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum
sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang
membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, 6 Februari 2015 Penulis,
Karakterisasi Simplisia dan Skrining Fitokimia serta Isolasi Senyawa Steroid/Triterpenoid dari Ekstrak n-heksan Rumput Laut
Turbinaria ornata (Turner) J. Agardh
ABSTRAK
Turbinaria ornata (Turner) J. Agardh merupakan salah satu jenis sumber
daya alam Indonesia yang berpotensi sebagai bahan obat. Turbinaria ornata
(Turner) J. Agardh termasuk dalam suku Sargassaceae yang juga menunjukkan adanya aktivitas antibakteri, antitumor dan antiimflamasi. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, skrining fitokimia serta untuk isolasi senyawa steroid/triterpenoid yang diidentifikasi dengan spektrofotometri Ultraviolet dan spektrofotometri Inframerah.
Pemeriksaan meliputi karakteristik simplisia dan skrining fitokimia terhadap serbuk simplisia. Ekstraksi dilakukan secara perkolasi dengan pelarut
n-heksan, penentuan fase gerak dengan kromatografi lapis tipis, isolasi dengan menggunakan kromatografi kolom dan dikromatografi lapis tipis. Kemurnian isolat ditentukan dengan kromatografi lapis tipis dua arah dan isolat yang diperoleh diidentifikasi secara spektrofotometri sinar ultraviolet dan spektrofotometri sinar inframerah.
Hasil pemeriksaan karakteristik simplisia diperoleh kadar air 9,94%, kadar sari yang larut dalam air 11,28%, kadar sari yang larut dalam etanol 2,34%, kadar abu total 16,45% dan kadar abu yang tidak larut asam 0,68%. Hasil skrining fitokimia memberikan hasil positif terhadap steroid/triterpenoid, saponin dan glikosida. Hasil analisis isolat secara spektrofotometri sinar Ultraviolet memberikan absorbansi maksimum pada panjang gelombang 206,80 nm menunjukkan adanya gugus kromofor dan hasil spektrofotometri sinar Inframerah menunjukkan adanya gugus C-O,-CH3, -CH2, C=C, C-H alifatis dan -OH.
Kata kunci: isolasi, kromatografi kolom, steroid/triterpenoid, Turbinaria
Simplex Characterization and Phytochemical Screening and Isolation of Steroid/Triterpenoid Compounds From n-Hexane Fraction of Seaweed
Turbinaria ornata (Turner) J. Agardh
ABSTRACT
Turbinaria ornata (Turner) J. Agardh is one type of Indonesia’s natural
resources potensial as medicine. Turbinaria ornata (Turner) J. Agardh is a one of the Sargassaceae showed antibacterial, antitumor and antiinflammatory activity. The purpose of this study was to determine the simplex characteristics, the phytochemical screening and the isolation of steroid/triterpenoid compounds. The isolates were characterized by ultraviolet and infrared spectrophotometries.
Simplex characterization and phytochemical screening of simplex powder. Extraction was accomplished by percolation using n-hexane as solvent, determination of mobile phase ratio with Thin Layer Chromatography then the
n-hexane extract was isolated with Coloumn Chromatography and Thin Layer Chromatography. The purity of isolate were confirmed by two-dimensional Thin Layer Cromatography and the pure isolate was characterized using ultraviolet and infrared spectrophotometric methods.
The result obtained from simplex characterization were water content 11.28%, ethanol-soluble extract content 2.34%, total ash content 16.45%, acid-insoluble ash content 0.68%. The result of phytochemical screening of seaweed
Turbinaria ornata (Turner) J. Agardh showed the presence of steroid/triterpenoid,
saponin and glycosides. The result of isolate was then characterized by Ultraviolet spectrophotometry that gave maximum wavelength 206,80 nm indicating the presence of chromophore and the result of IR spectrophotometry indicated the presence of C-O, -CH3, CH2, C=C, aliphatic C-H and –OH functional groups.
Key words: isolation, coloumn chromatography, steroid/triterpenoid, Turbinaria
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Habitat ... 5
2.1.2 Morfologi tumbuhan ... 5
2.1.5 Perkembangbiakan tumbuhan ... 6
2.1.6 Kandungan kimia tumbuhan ... 7
2.2 Uraian Kandungan Kimia Tumbuhan ... 7
2.2.1 Alginat ... 7
2.2.2 Glikosida ... 8
2.2.3 Saponin ... 9
2.2.4 Steroid/triterpenoid ... 9
2.3 Ekstraksi ... 11
2.4 Kromatografi ... 13
2.4.1 Kromatografi lapis tipis ... 13
2.4.2 Kromatografi kolom... 15
2.4.3 Kromatografi lapis tipis dua arah ... 15
2.5 Spektrofotometri ... 16
2.5.1 Spektrofotometri sinar ultraviolet ... 16
2.5.2 Spektrofotometri sinar inframerah ... 17
BAB III METODE PENELITIAN ... 19
3.1 Alat ... 19
3.2 Bahan ... 19
3.3 Pembuatan Pereaksi ... 20
3.3.1 Pereaksi Bouchardat ... 20
3.3.2 Pereaksi Dragendorff ... 20
3.3.3 PereaksiMeyer ... 20
3.3.4 Pereaksi Molish ... 20
3.3.6 Pereaksi timbal (II) asetat 0,4 M ... 21
3.3.7 Pereaksi asam klorida 2 N ... 21
3.3.8 Pereaksi asam sulfat 2 N ... 21
3.3.9 Pereaksi kloralhidrat ... 21
3.3.10 Pereaksi Penyemprot Liebermann-Burchard ... 21
3.4 Pengambilan dan Pengolahan Bahan Tumbuhan ... 21
3.4.1 Pengambilan bahan tumbuhan ... 21
3.4.2 Identifikasi bahan tumbuhan ... 22
3.4.3 Pengolahan tumbuhan ... 22
3.5 Pemeriksaan Karakteristik ... 22
3.5.1 Pemeriksaan makroskopik ... 22
3.5.2 Pemeriksaan mikroskopik ... 22
3.5.3 Penetapan kadar air ... 22
3.5.4 Penetapan kadar sari yang larut dalam air ... 23
3.5.5 Penetapan kadar sari yang larut dalam etanol ... 24
3.5.6 Penetapan kadar abu total ... 24
3.5.7 Penetapan kadar abu yang tidak larut dalam asam ... 24
3.6 Skrining Fitokimia ... 25
3.6.1 Pemeriksaan alkaloid ... 25
3.6.2 Pemeriksaan flavonoid ... 25
3.6.3 Pemeriksaan glikosida ... 25
3.6.4 Pemeriksaan saponin ... 26
3.7 Pembuatan Ekstrak ... 27
3.8 Analisis Ekstrak n-heksan Secara KLT ... 27
3.9 Isolasi Ekstrak n-heksan dengan Kromatografi Kolom ... 28
3.10 Pencuciaan Kristal ... 29
3.11 Uji Kemurnian Isolat ... 29
3.12 Identifikasi Isolat ... 30
3.12.1 Identifikasi isolat secara spektrofotometri UV ... 30
3.12.2 Identifikasi isolat secara spektrofotometri IR ... 30
BAB IV HASIL DAN PEMBAHASAN ... 31
4.1 Hasil Identifikasi Tumbuhan ... 31
4.2 Hasil Karakterisasi ... 31
4.2.1 Hasil pemeriksaan makroskopik ... 31
4.2.2 Hasil pemeriksaan mikroskopik ... 31
4.2.3 Hasil pemeriksaan karakteristik ... 32
4.3 Hasil Skrining Fitokimia ... 33
4.4 Hasil Isolasi Senyawa steroid/triterpenoid ... 34
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Tabel Halaman
4.1 Tabel hasil pemeriksaan karakteristik simplisia rumput laut ... 32
4.2 Tabel hasil skrining fitokimia simplisia rumput laut ... 33
DAFTAR GAMBAR
Gambar Halaman
2.1 Gambar struktur ikatan karbon-oksigen antara gula dan cincin
aromatik ... 8
2.2 Gambar struktur ikatan karbon-karbon antara gula dan cincin aromatik ... 8
2.3 Gambar struktur nikleosidin ... 8
2.4 Gambar struktur sinigrin ... 9
2.5 Gambar struktur dasar steroid dan sistem penomorannya ... 10
2.6 Gambar struktur kolesterol ... 10
2.7 Gambar struktur stigmasterol ... 10
2.8 Gambar struktur ergosterol ... 11
2.9 Gambar struktur spongesterol ... 11
DAFTAR LAMPIRAN
Lampiran Halaman
1 Identifikasi tumbuhan ... 41
2 Bagan kerja penelitian ... 42
3 Gambar makroskopik rumput laut ... 43
4 Gambar mikroskopik rumput laut ... 45
5 Bagan skrining fitokimia dan karakteristik serbuk simplisia .. 46
6 Bagan pembuatan ekstrak n-heksan rumput laut Turbinaria ornata (Turner) J. Agardh ... 47
7 Bagan kromtografi kolom ... 48
8 Kromatogram dan harga Rf dari fraksi n-heksan rumput laut Turbinaria ornata (Turner) J. Agardh ... 49
9 Kromatogram KLT hasil fraksinasi kolom ... 51
10 Kromatogram hasil KLT dua arah isolat murni ... 55
11 Spektrum UV isolat rumput laut Turbinaria ornata (Turner) J. Agardh ... 56
12 Spektrum IR isolat rumput laut Turbinaria ornata (Turner) J. Agardh ... 57
Karakterisasi Simplisia dan Skrining Fitokimia serta Isolasi Senyawa Steroid/Triterpenoid dari Ekstrak n-heksan Rumput Laut
Turbinaria ornata (Turner) J. Agardh
ABSTRAK
Turbinaria ornata (Turner) J. Agardh merupakan salah satu jenis sumber
daya alam Indonesia yang berpotensi sebagai bahan obat. Turbinaria ornata
(Turner) J. Agardh termasuk dalam suku Sargassaceae yang juga menunjukkan adanya aktivitas antibakteri, antitumor dan antiimflamasi. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, skrining fitokimia serta untuk isolasi senyawa steroid/triterpenoid yang diidentifikasi dengan spektrofotometri Ultraviolet dan spektrofotometri Inframerah.
Pemeriksaan meliputi karakteristik simplisia dan skrining fitokimia terhadap serbuk simplisia. Ekstraksi dilakukan secara perkolasi dengan pelarut
n-heksan, penentuan fase gerak dengan kromatografi lapis tipis, isolasi dengan menggunakan kromatografi kolom dan dikromatografi lapis tipis. Kemurnian isolat ditentukan dengan kromatografi lapis tipis dua arah dan isolat yang diperoleh diidentifikasi secara spektrofotometri sinar ultraviolet dan spektrofotometri sinar inframerah.
Hasil pemeriksaan karakteristik simplisia diperoleh kadar air 9,94%, kadar sari yang larut dalam air 11,28%, kadar sari yang larut dalam etanol 2,34%, kadar abu total 16,45% dan kadar abu yang tidak larut asam 0,68%. Hasil skrining fitokimia memberikan hasil positif terhadap steroid/triterpenoid, saponin dan glikosida. Hasil analisis isolat secara spektrofotometri sinar Ultraviolet memberikan absorbansi maksimum pada panjang gelombang 206,80 nm menunjukkan adanya gugus kromofor dan hasil spektrofotometri sinar Inframerah menunjukkan adanya gugus C-O,-CH3, -CH2, C=C, C-H alifatis dan -OH.
Kata kunci: isolasi, kromatografi kolom, steroid/triterpenoid, Turbinaria
Simplex Characterization and Phytochemical Screening and Isolation of Steroid/Triterpenoid Compounds From n-Hexane Fraction of Seaweed
Turbinaria ornata (Turner) J. Agardh
ABSTRACT
Turbinaria ornata (Turner) J. Agardh is one type of Indonesia’s natural
resources potensial as medicine. Turbinaria ornata (Turner) J. Agardh is a one of the Sargassaceae showed antibacterial, antitumor and antiinflammatory activity. The purpose of this study was to determine the simplex characteristics, the phytochemical screening and the isolation of steroid/triterpenoid compounds. The isolates were characterized by ultraviolet and infrared spectrophotometries.
Simplex characterization and phytochemical screening of simplex powder. Extraction was accomplished by percolation using n-hexane as solvent, determination of mobile phase ratio with Thin Layer Chromatography then the
n-hexane extract was isolated with Coloumn Chromatography and Thin Layer Chromatography. The purity of isolate were confirmed by two-dimensional Thin Layer Cromatography and the pure isolate was characterized using ultraviolet and infrared spectrophotometric methods.
The result obtained from simplex characterization were water content 11.28%, ethanol-soluble extract content 2.34%, total ash content 16.45%, acid-insoluble ash content 0.68%. The result of phytochemical screening of seaweed
Turbinaria ornata (Turner) J. Agardh showed the presence of steroid/triterpenoid,
saponin and glycosides. The result of isolate was then characterized by Ultraviolet spectrophotometry that gave maximum wavelength 206,80 nm indicating the presence of chromophore and the result of IR spectrophotometry indicated the presence of C-O, -CH3, CH2, C=C, aliphatic C-H and –OH functional groups.
Key words: isolation, coloumn chromatography, steroid/triterpenoid, Turbinaria
BAB I
PENDAHULUAN
1.1 Latar Belakang
Indonesia adalah salah satu negara yang mempunyai daerah perairan yang
cukup luas, 2/3 dari luas wilayahnya terdiri dari lautan yang di dalamnya
terkandung sumber daya alam yang sangat besar dan potensial sebagai bahan
makanan atau sebagai obat-obatan, seperti rumput laut (Winarno, 1990).
Rumput laut memiliki kandungan metabolit primer dan metabolit
sekunder. Kandungan metabolit primer rumput laut seperti alginat, serat, protein
dan vitamin (Limantara dan Heriyanto, 2010) banyak dimanfaatkan sebagai bahan
industri dan bahan kosmetik untuk pemeliharaan kulit. Selain kandungan
metabolit primer rumput laut yang bernilai ekonomis, kandungan metabolit
sekunder dari rumput laut juga memiliki aktivitas sebagai antibakteri dan
antijamur (Reskika, 2011). Jenis rumput laut yang bernilai ekonomis dan telah
diperdagangkan sejak dahulu, yaitu dari golongan rumput laut merah
(Rhodophyta), rumput laut hijau (Chlorophyta) dan rumput laut coklat
(Phaeophyta) (Anggadiredja, dkk., 2011).
Rumput laut coklat (Phaeophyceae) potensial digunakan sebagai sumber
penghasil alginat. Rumput laut coklat yang juga sebagai penghasil alginat
diantaranya adalah dari jenis Turbinaria sp., Padina sp., dan Sargassum sp.
Alginat adalah salah satu kelompok polisakarida yang terbentuk dalam dinding sel
alga coklat, dengan kadar mencapai 40% dari total berat kering dan memegang
peranan penting dalam mempertahankan struktur jaringan alga (Rasyid, 2003).
industri antara lain sebagai pengental, pensuspensi dalam sirup dan penstabil
(Anggadiredja, dkk., 2011).
Turbinaria ornata (Turner) J. Agardh adalah jenis rumput laut coklat yang
banyak ditemukan di pantai Lampuuk, Propinsi Nanggroe Aceh Darussalam,
namun belum banyak dibudidayakan ataupun dikembangkan secara optimal oleh
masyarakat setempat. Beberapa penelitian yang telah dilakukan menunjukkan
bahwa Turbinaria sp. berpotensi sebagai antibakteri (Vijayabakar and Shiyamala,
2011), sebagai antitumor (Fajarningsih, dkk., 2008) serta sebagai antiinflamasi
(Ananthi, dkk., 2011).
Senyawa steroid terdapat pada hewan, tanaman tingkat tinggi bahkan
terdapat pula pada beberapa tanaman tingkat rendah seperti pada jamur (fungi),
fungsi steroid antara lain untuk meningkatkan laju perpanjangan sel tumbuhan
serta untuk merangsang pertumbuhan pucuk tumbuhan. Steroid banyak terdapat di
alam tetapi dalam jumlah yang terbatas dan juga mempunyai aktivitas biologis
(Robinson,1995).
Golongan senyawa steroid/triterpenoid merupakan komponen aktif dari
tumbuhan yang telah digunakan untuk mengobati beberapa penyakit dan
digunakan dalam bidang farmasi seperti untuk pembuatan obat-obat kontrasepsi
dan antiinflamasi (Robinson, 1995).
Berdasarkan hal diatas maka peneliti tertarik untuk melakukan penelitian
terhadap spesies rumput laut Turbinaria ornata (Turner) J. Agardh yang meliputi
pemeriksaan terhadap karakterisasi simplisia, skrining fitokimia dan isolasi
senyawa steroid/triterpenoid dari ekstrak n-heksan rumput laut Turbinaria ornata
lengkap mengenai karakterisasi simplisia, skrining fitokimia dan isolasi golongan
senyawa kimia dari rumput laut Turbinaria ornata (Turner) J. Agardh.
1.2 Perumusan Masalah
a. Apakah hasil karakterisasi simplisia rumput laut Turbinaria ornata
(Turner) J. Agardh dapat dijadikan sebagai acuan pada penelitian
selanjutnya?
b. Apakah golongan senyawa kimia yang terkandung dalam simplisia rumput
laut Turbinaria ornata (Turner) J. Agardh?
c. Apakah senyawa steroid/triterpenoid hasil isolasi dapat diidentifikasi
secara Spektofotometri UV dan Spektrofotometri IR?
1.3Hipotesis
a. Turbinaria ornata (Turner) J. Agardh belum tercantum dalam MMI
(Materia Medika Indonesia) sehingga karakteristik simplisia rumput laut
yang diperoleh dapat dijadikan sebagai informasi dan acuan pada
penelitian selanjutnya.
b. Golongan senyawa kimia yang terkandung didalam simplisia rumput laut
Turbinaria ornata (Turner) J. Agardh adalah glikosida, saponin dan
steroid/triterpenoid.
c. Hasil isolasi senyawa steroid/triterpenoid dapat diidentifikasi secara
Spektrofotometri UV dan Spektrofotometri IR.
1.4Tujuan Penelitian
a. Untuk mengetahui karakteristik simplisia rumput laut Turbinaria ornata
b. Untuk mengetahui golongan senyawa kimia yang terkandung dalam
simplisia rumput laut Turbinaria ornata (Turner) J. Agardh.
c. Untuk mengetahui apakah isolat dapat diidentifikasi secara
Spektrofotometri UV dan Spektrofotometri IR.
1.5 Manfaat Penelitian
Manfaat dari penelitian ini adalah sebagai informasi mengenai
karakteristik dan kandungan senyawa kimia dari simplisia rumput laut Turbinaria
ornata (Turner) J. Agardh serta untuk pengembangan obat tradisional khususnya
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi habitat dan sebaran tumbuhan, morfologi
tumbuhan, sistematika tumbuhan, nama daerah, perkembangbiakan tumbuhan dan
kandungan kimia tumbuhan.
2.1.1 Habitat
Daerah sebaran beberapa jenis rumput laut di Indonesia sangat luas, baik
yang tumbuh secara alami maupun yang dibudidayakan. Wilayah sebaran rumput
laut yang tumbuh terdapat hampir diseluruh perairan dangkal laut Indonesia
(Anggadiredja, dkk., 2011).
Habitat dan sebaran Turbinaria ornata (Turner) J. Agardh di Indonesia
umumnya tumbuh di perairan dangkal dengan daerah karang berlubang yang
memiliki arus kuat dan juga tumbuh di atas batu koral dengan arus lemah (Aslan,
1998). Pengaruh alam yang banyak menentukan sebaran rumput laut adalah
cahaya matahari, jenis substrat, kadar garam, ombak dan pasang surut. Rumput
laut tidak dapat tumbuh pada kedalaman yang tidak terjangkau cahaya matahari
dan substrat dasar tempat melekat biasanya berupa karang, batu, lumpur, pasir,
kerang atau pada kayu (Atmadja, dkk., 1996). 2.1.2 Morfologi tumbuhan
Rumput laut tidak memperlihatkan adanya perbedaan antara akar, batang
dan daun, bentuk tersebut sebenarnya hanya talus saja (Aslan, 1998). Turbinaria
ornata (Turner) J. Agardh berupa talus berwarna coklat gelap, mempunyai batang
menyerupai terompet dengan panjang 1,5 cm pada daerah ujung daun mempunyai
pinggir yang tajam runcing. Akar bercabang tidak teratur (Atmadja, dkk., 1996).
2.1.3 Sistematika tumbuhan
Menurut hasil identifikasi di Lembaga Ilmu Pengetahuan Indonesia Pusat
Penelitian Oseanografi Jakarta, taksonomi rumput laut coklat diklasifikasikan
sebagai berikut:
Divisi : Phaeophyta
Kelas : Phaeophyceae
Ordo : Fucales
Suku : Sargassaceae
Genus : Turbinaria
Spesies : Turbinaria ornata (Turner) J. Agardh
2.1.4 Nama daerah
Nama daerah Turbinaria ornata (Turner) J. Agardh adalah agar-agar
makina (Ambon), sarip geremes (Garut).
2.1.5 Perkembangbiakan tumbuhan
Perkembangbiakan rumput laut coklat dapat melalui dua cara, yaitu secara
vegetatif dengan talus dan secara generatif dengan spora. Perkembangbiakan
secara vegetatif dikembangkan dengan cara fragmentasi, yaitu potongan talus
yang kemudian tumbuh menjadi tanaman baru. Perkembangbiakan secara
generatif dikembangkan melalui spora. Pertemuan dua gamet membentuk zigot
yang selanjutnya berkembang menjadi sporofit. Individu ini yang mengeluarkan
Faktor biologi utama yang menjadi pembatas produktivitas rumput laut
yaitu faktor persaingan dan pemangsa dari hewan herbivora. Produktivitas dapat
juga dihambat oleh faktor morbiditas dan mortalitas rumput laut itu sendiri.
Morbiditas dapat disebabkan oleh penyakit dari infeksi mikroorganisme, tekanan
lingkungan perairan (fisika dan kimia perairan) yang buruk serta tumbuhnya
tanaman penempel (parasit). Mortalitas dapat disebabkan oleh pemangsaan
hewan-hewan herbivora (Aslan, 1998).
2.1.6 Kandungan kimia tumbuhan
Turbinaria ornata (Turner) J. Agardh merupakan jenis rumput laut coklat
yang menghasilkan metabolit primer berupa senyawa hidrokoloid yang disebut
alginat (Limantara dan Heriyanto, 2010). Jenis rumput laut yang termasuk kelas
Phaeophyceae (alga coklat) memiliki kandungan protein, sedikit lemak, beta
karoten, violasantin dan fukosantin serta mineral, seperti kalium, kalsium, fosfor,
natrium, zat besi, dan iodium. Fukosantin merupakan pigmen yang dominan
menutupi pigmen lainnya dan menyebabkan warna coklat pada rumput laut coklat
serta mempunyai persediaan makanan (hasil fotosintesis) berupa laminaran
(Yulianto, 2007).
2.2 Uraian Kandungan Kimia Tumbuhan 2.2.1 Alginat
Alginat merupakan hidrokoloid yang diekstraksi dari Phaeophyceae (alga
coklat), dikenal dalam dunia industri karena banyak manfaatnya (Aslan, 1998).
Alginat menjadi sangat penting karena penggunaanya yang cukup luas dalam
industri, antara lain sebagai bahan pengental dan pensuspensi dalam sirup
Indonesia yang memiliki potensi untuk diolah menjadi alginat adalah Sargassum
sp., Turbinaria sp. dan Padina sp. (Atmadja, dkk., 1996).
2.2.2 Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai
menjadi gula (glikon) dan senyawa lain (aglikon). Umumnya glikosida mudah
terhidrolisis oleh asam mineral atau enzim (Sirait, 2007).
Berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan menjadi
(Sirait, 2007):
a. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui
jembatan O.
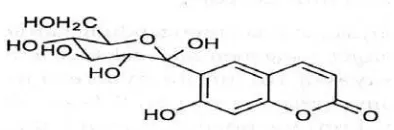
Gambar 2.1 Ikatan karbon-oksigen antara gula dan cincin aromatik
b. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui
jembatan C.
Gambar 2.2 Ikatan karbon-karbon antara gula dan cincin aromatik
c. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui
jembatan N. Contoh: nikleosidin.
d. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan
S. Contoh: sinigrin.
Gambar 2.4 Sinigrin 2.2.3 Saponin
Saponin adalah senyawa aktif permukaan yang kuat yang menimbulkan
busa jika dikocok dalam air dan pada konsentrasi yang rendah sering
menyebabkan hemolisis sel darah merah. Saponin tersebar luas diantara tanaman
tingkat tinggi. Saponin merupakan senyawa berasa pahit, menusuk, menyebabkan
bersin dan mengakibatkan iritasi terhadap selaput lendir (Robinson, 1995).
Molekul saponin terdiri dari dua bagian yaitu, aglikon dan glikon. Bagian
aglikon dari molekul saponin disebut genin atau sapogenin. Berdasarkan
aglikonnya, Hostettman dan Marston (1995) membagi saponin menjadi 3 kelas
utama yaitu:
1. Saponin triterpenoid
2. Saponin steroid
3. Saponin steroid alkaloid.
2.2.4 Steroid/triterpenoid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam
satuan isoprena dan secara biosintesis masuk jalur asam mevalonat diturunkan
dari hidrokarbon C30 asiklik, yaitu skualena. Triterpenoid berupa senyawa tanpa
warna, berbentuk kristal, sering kali bertitik leleh tinggi (Harborne, 1987).
ialah reaksi Liebermann-Burchard yang biasanya menghasilkan warna hijau-biru
(Harborne, 1987). Triterpenoid juga menunjukkan aktivitas antibakteri, antifungi
(Robinson, 1995) dan antikanker (Atenza, dkk., 2009).
Triterpenoid dapat dibagi menjadi empat golongan senyawa, yaitu
triterpen, steroid, saponin dan glikosida jantung (Harborne, 1987).
Steroid adalah senyawa triterpenoid yang kerangka dasarnya sistem cincin
siklopentana perhidrofenantren. Senyawa ini tersebar luas di alam dan mempunyai
fungsi biologis yang sangat penting misalnya untuk kontrasepsi dan antiinflamasi
(Harborne, 1987). Kerangka dasar dan sistem penomoran steroid (Robinson,
1995) dapat dilihat pada gambar berikut ini:
Gambar 2.5 Struktur dasar steroid dan sistem penomorannya Menurut sumbernya, steroid dibagi atas (Manitto, 1981):
a. Zoosterol yaitu steroid yang berasal dari hewan, misalnya kolesterol.
Gambar 2.6 Kolesterol
b. Fitosterol yaitu steroid yang berasal dari tumbuhan, misalnya stigmasterol.
c. Mycosterol yaitu steroid yang berasal dari fungi, misalnya ergosterol.
Gambar 2.8 Ergosterol
d. Marinesterol yaitu steroid yang berasal dari organisme laut, misalnya
spongesterol.
Gambar 2.9 Spongesterol
2.3 Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari
jaringan tumbuhan maupun hewan dengan pelarut yang sesuai. Sebelum ekstraksi
dilakukan biasanya bahan dikeringkan terlebih dahulu kemudian dihaluskan pada
derajat kehalusan tertentu (Harborne, 1987).
Menurut Depkes (2000), ada beberapa metode ekstraksi yang sering
digunakan antara lain yaitu:
a. Cara dingin 1. Maserasi
Maserasi adalah penyarian simplisia dengan cara perendaman
menggunakan pelarut disertai sesekali pengadukan pada temperatur kamar.
Maserasi yang dilakukan pengadukan secara terus menerus disebut maserasi
kinetik sedangkan yang dilakukan panambahan ulang pelarut setelah dilakukan
2. Perkolasi
Adalah proses penyarian simplisia menggunakan alat perkolator dengan
pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya
dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap
pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya
(penetesan/penampungan ekstrak) terus menerus sampai diperoleh perkolat.
b. Cara panas 1. Refluks
Adalah proses penyarian simplisia pada temperatur titik didihnya
menggunakan alat dengan pendingin balik dalam waktu tertentu dimana pelarut
akan terkondensasi menuju pendingin dan kembali ke labu.
2. Digesti
Adalah proses penyarian dengan pengadukan kontinu pada temperatur
lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada temperatur
40-50°C.
3. Sokletasi
Adalah proses penyarian menggunakan pelarut yang selalu baru, dilakukan
dengan menggunakan alat khusus (soklet) dimana pelarut akan terkondensasi.
4. Infundasi
Adalah proses penyarian dengan menggunakan pelarut air pada temperatur
90°C selama 15 menit.
5. Dekoktasi
Adalah proses penyarian dengan menggunakan pelarut air pada temperatur
2.4 Kromatografi
Kromatografi adalah suatu metode yang digunakan untuk pemisahan
komponen cuplikan yang komponen-komponennya terdistribusi antara dua fase,
salah satunya diam dan yang lainnya bergerak (Rohman, 2009).
Pada dasarnya semua cara kromatografi menggunakan dua fase yaitu fase
diam (stationary phase) dan fase gerak (mobile phase). Cara-cara kromatografi
dapat digolongkan sesuai dengan sifat-sifat dari fase diam, yang dapat berupa zat
padat atau zat cair (Sastrohamidjojo, 1985).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis termasuk kromatografi absobsi, sebagai fase diam
digunakan zat padat yang disebut adsorben (penyerap) dan fase gerak adalah zat
cair yang disebut larutan pengembang. Kromatografi lapis tipis merupakan
metode pemisahan campuran analit dengan mengelusi analit melalui suatu
lempeng kromatografi lalu melihat komponen/analit yang terpisah dengan
penyemprotan atau pewarnaan (Adnan, 1997).
Lapisan pemisah dari kromatografi lapis tipis terdiri atas bahan
berbutir-butir (fase diam), di tempatkan pada penyangga berupa plat gelas, logam atau
lapisan yang cocok. Campuran yang akan dipisah berupa larutan yang ditotolkan
baik berupa bercak ataupun pita. Setelah plat atau lapisan di masukkan ke dalam
bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak),
pemisahan terjadi selama perambatan kapiler (pengembangan) (Stahl, 1985).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara.
Senyawa yang tidak berwarna dilakukan pengamatan dengan sinar ultraviolet.
ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm), jika
dengan cara itu senyawa tidak dapat dideteksi maka harus disemprot dengan
pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan
kemudian bila perlu dengan pemanasan (Gritter, dkk., 1991).
a. Fase diam
Fase diam berupa lapisan tipis yang terdiri atas bahan padat yang
dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca,
plastik atau logam (Gritter, dkk., 1991).
Partikel fase diam dengan butiran yang kasar tidak akan memberikan hasil
yang memuaskan. Salah satu cara untuk memperbaiki hasil pemisahan adalah
dengan menggunakan fase diam yang butirannya halus. Penyerap yang banyak
dipakai untuk kromatografi lapis tipis adalah silika gel, alumunium oksida,
selulosa dan poliamida (Sastrohamidjojo, 1985).
b. Fase gerak
Fase gerak ialah medium angkut dan terdiri atas satu atau beberapa
pelarut. Pemilihan sistem pelarut yang dipakai didasarkan atas prinsip like
dissolves like yaitu untuk memisahkan sampel yang bersifa non polar digunakan
sistem pelarut yang bersifat non polar dan untuk memisahkan sampel yang
bersifat polar digunakan sistem pelarut yang bersifat polar (Stahl, 1985).
c. Harga Rf
Mengidentifikasi noda-noda dalam kromatografi lapis tipis sangat lazim
menggunakan harga Rf (Retardation Factor) yang didefinisikan sebagai:
Faktor-faktor yang mempengaruhi harga Rf antara lain:
1. Struktur kimia dari senyawa yang sedang dipisahkan
2. Sifat penyerap
3. Tebal dan kerataan lapisan penyerap
4. Pelarut dan derajat kemurniannya
5. Derajat kejenuhan uap pengembang dalam bejana
6. Jumlah cuplikan
7. Suhu (Sastrohamidjojo, 1985).
2.4.2 Kromatografi kolom
Kromatografi kolom biasanya digunakan untuk memisahkan suatu
campuran, berupa pipa gelas yang dilengkapi dengan kran, penyerap dan gelas
penyaring didalamnya. Ukuran kolom tergantung pada banyaknya zat yang akan
dipisahkan dan penyerap yang digunakan gelas wool atau kapas (Sastrohamidjojo,
1985).
Kromatografi kolom memerlukan waktu yang lama dan bahan yang cukup
banyak, sehingga perlu dipastikan campuran pelarut yang terbaik untuk
pemisahan. Masalah ini dapat dipecahkan melalui penerapan data KLT dan
pemakaian elusi landaian. Fraksi kolom yang mengandung senyawa yang sama
diperiksa dengan KLT kemudian digabungkan, diuapkan dengan tekanan rendah,
namun masih mungkin diperlukan rekristalisasi untuk memperoleh senyawa
murni (Gritter, dkk.,1991).
2.4.3 Kromatografi lapis tipis dua arah (two-dimensional TLC)
KLT dua arah atau KLT dua dimensi ini bertujuan untuk meningkatkan
hampir sama, karena nilai Rf juga hampir sama. Dua sistem fase gerak yang
sangat berbeda dapat digunakan secara berurutan pada suatu campuran tertentu,
sehingga memungkinkan untuk melakukan pemisahan analit yang mempunyai
tingkat polaritas yang hampir sama (Rohman, 2009).
KLT dua arah dilakukan dengan melakukan penotolan sampel disalah satu
sudut lapisan lempeng tipis dan mengembangkannya sebagaimana biasa dengan
fase gerak pertama. Lempeng kromatografi selanjutnya dipindahkan dari chamber
pengembang dan eluen dibiarkan menguap dari lempeng. Lempeng dimasukkan
ke dalam chamber yang menggunakan eluen kedua sehingga pengembangan dapat
terjadi pada arah kedua yang tegak lurus dengan arah pengembangan yang
pertama (Rohman, 2009).
2.5 Spektrofotometri
2.5.1 Spektrofotometri sinar ultraviolet
Menurut Dachriyanus (2004), spektrofotometri UV-visibel adalah pengukuran
panjang gelombang dan intensitas sinar ultraviolet dan sinar tampak yang
diabsorbsi oleh sampel. Spektrum ultraviolet adalah suatu gambaran yang
menyatakan hubungan antara panjang gelombang atau frekuensi sinar UV
terhadap intensitas serapan (adsorbansi). Sinar ultraviolet mempunyai panjang
gelombang antara 200 - 400 nm (Sastrohamidjojo, 1985).
Ketika suatu atom atau molekul menyerap cahaya maka energi tersebut
akan menyebabkan tereksitasinya elektron pada kulit terluar ketingkat energi yang
lebih tinggi. Tipe eksitasi tergantung panjang gelombang cahaya yang diserap.
Gugus yang dapat mengabsorpsi cahaya disebut dengan gugus kromofor
2.5.2 Spektrofotometri sinar inframerah
Sinar inframerah dilewatkan melalui cuplikan senyawa organik, maka
sejumlah frekuensi diserap sedang frekuensi yang lain diteruskan atau
ditransmisikan tanpa diserap. Pengukuran pada spketrum inframerah dilakukan
pada daerah bilangan gelombang 2000-4000cm-1. Beberapa kegunaan penggunaan
spektrofotometri inframerah (Dachriyanus, 2004), antara lain:
a. Menentukan gugus fungsi suatu senyawa organik
b. Mengetahui informasi struktur suatu senyawa organik dengan membandingkan
daerah sidik jarinya.
Cara menganalisa spektrum inframerah dari senyawa yang tidak diketahui. adalah
pertama harus ditentukan ada atau tidaknya beberapa gugus fungsional utama,
seperti C=O , O-H , C-O, C=C, C≡N, C≡C dan NO
2. Menurut pavia (1988),
langkah-langkah umum untuk memeriksa pita-pita serapan yang penting yang
umum untuk memeriksa gugus yang penting pada spektrum inframerah sebagai
berikut :
1. Apakah terdapat gugus karbonil?
Gugus C=O memberikan puncak pada daerah 1660-1820 cm-1. Puncak ini
biasanya merupakan yang terkuat dengan lebar medium pada spektrum.
2. Jika gugus C=O ada, periksalah gugus-gugus berikut dan jika C=O tidak ada
langsung ke nomor 3.
a. Asam: yaitu pada serapan melebar 2500-3000 cm -1 (biasanya tumpang
tindih dengan C-H).
b. Amida: yaitu pada serapan medium di dekat 3500 cm-1, kadang-kadang
c. Ester : yaitu pada serapan dengan intensitas medium di daerah 1000–1300
cm-1.
d. Anhidrida : mempunyai dua serapan C=O di daerah 1810 dan 1760 cm-1.
e. Aldehida : yaitu dua serapan lemah di dekat 2850-2750 cm-1 disebelah
kanan serapan C-H
f. Keton : jika kelima kemungkinan diatas tidak ada.
3. Jika gugus C=O tidak ada
a. Alkohol/fenol : periksalah gugus OH, yaitu serapan melebar di daerah
3300-3600 cm-1 yang diperkuat adanya serapan C-O di daerah 1000-1300 cm-1.
b. Amina : periksalah gugus N-H , yaitu serapan medium di daerah 3500 cm-1.
c. Eter : periksalah gugus C-O (dan tidak adanya –OH), yaitu serapan medium
di daerah 1000–1300 cm-1.
4. Ikatan rangkap dua atau cincin aromatik yaitu adanya :
a. C=C yang mempunyai serapan lemah di daerah 1650 cm-1.
b. Serapan medium sampai kuat pada daerah 1450-1650 cm-1 sering
menunjukkan adanya cincin aromatik.
5. Ikatan rangkap tiga yaitu adanya;
a. C=N yang mempunyai serapan medium dan tajam di daerah 2250 cm-1
b. C=C mempunyai serapan lemah tapi tajam di daerah 2150 cm-1 periksa juga
CH asetilenik di dekat 3300 cm-1.
6. Hidrokarbon
a. Apakah kelima kemungkinan diatas tidak ada.
b. Serapan utama di daerah CH dekat 3000 cm-1.
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksperimental. Penelitian meliputi
pengumpulan dan pengolahan bahan tumbuhan, identifikasi bahan tumbuhan,
karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak n-heksan, analisis
ekstrak n-heksan dengan Kromatografi Lapis Tipis, Kromatografi Kolom, uji
kemurnian dengan KLT dua arah dan identifikasi isolat secara Spektrofotometri
UV dan Spektrofotometri IR. Penelitian dilakukan di Laboratorium Fitokimia dan
Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat
Alat-alat yang digunakan pada penelitian ini terdiri dari alat-alat gelas
laboratorium, blender (Phillips), desikator, krus porselin, lemari pengering,
mikroskop (Olympus), neraca analitik (Vibra Aj), oven (Fisher Scientific),
seperangkat alat perkolasi, seperangkat alat kromatografi kolom, hair dryer
(Maspion), botol penyemprot, seperangkat alat penetapan kadar air,
spektrofotometer UV (Shimadzu), spektrofotometri IR (IR-Prestige 21).
3.2 Bahan
Bahan yang digunakan adalah talus rumput laut Turbinaria ornata
(Turner) J. Agardh. Bahan-bahan kimia berkualitas pro analisis (E-Merck) yaitu:
amil alkohol, asam asetat anhidrida, asam klorida pekat, asam nitrat pekat, asam
sulfat pekat, benzen, besi (III) klorida, bismuth (III) nitrat, isopropanol,
kloroform, metanol, n-heksan, natrium hidroksida, raksa (II) klorida, serbuk
α-naftol, plat lapis silika gel GF254, silika gel 60 H. Bahan kimia berkualitas
teknis: etanol 96% dan air suling.
3.3 Pembuatan Pereaksi
Prosedur pembuatan pereaksi berdasarkan referensi dari Materia Medika
Indonesia Jilid VI (1995).
3.3.1 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida ditimbang, dilarutkan dalam air suling
secukupnya, lalu ditambahkan 2 g iodium kemudian ditambahkan air suling
hingga diperoleh larutan 100 ml.
3.3.2 Pereaksi Dragendorff
Larutan bismut nitrat P 40% b/v dalam asam nitrat P sebanyak 20 ml
dicampur dengan 50 ml kalium iodida P 54,4% b/v, didiamkan sampai memisah
sempurna, lalu diambil lapisan jernih dan diencerkan dengan air secukupnya
hingga 100 ml.
3.3.3 Pereaksi Mayer
Larutan raksa (II) klorida P 2,266% b/v sebanyak 60 ml dicampur dengan
10 ml larutan kalium iodida P 50% b/v, kemudian ditambahkan air secukupnya
hingga 100 ml.
3.3.4 Pereaksi Molish
Sebanyak 3 g α-naftol ditimbang, dilarutkan dalam asam nitrat 0,5 N
hingga diperoleh larutan 100 ml.
3.3.5 Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air
3.3.6 Pereaksi timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat ditimbang, kemudian dilarutkan dalam
air suling bebas karbon dioksida sebanyak 100 ml.
3.3.7 Pereaksi asam klorida 2 N
Sebanyak 17 ml larutan asam klorida pekat ditambahkan air suling hingga
diperoleh larutan 100 ml.
3.3.8 Pereaksi asam sulfat 2 N
Sebanyak 9,8 ml larutan asam sulfat pekat ditambahkan air suling sampai
100 ml.
3.3.9 Pereaksi kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20 ml
air suling.
3.3.10 Pereaksi penyemprot Liebermann-Burchard
Sebanyak 5 ml asam sulfat pekat dicampurkan dengan 50 ml etanol 96%,
kemudian ditambahkan dengan hati-hati 5 ml asam asetat anhidrida ke dalam
campuran tersebut dan dinginkan.
3.4Pengambilan dan Pengolahan Bahan Tumbuhan 3.4.1 Pengambilan bahan tumbuhan
Pengambilan bahan tumbuhan dilakukan secara purposif yaitu tanpa
membandingkan dengan bahan tumbuhan yang sama dari daerah lain. Bahan
tumbuhan yang digunakan dalam penelitian ini adalah rumput laut Turbinaria
ornata (Turner) J. Agardh yang diperoleh dari pantai Lampuuk, Propinsi
3.4.2 Identifikasi bahan tumbuhan
Identifikasi tumbuhan dilakukan di Identifikasi bahan tumbuhan dilakukan
di Lembaga Ilmu Pengetahuan Indonesia Pusat Penelitian Oseanografi, Jakarta.
3.4.3 Pengolahan bahan tumbuhan
Bahan tumbuhan yang digunakan adalah talus rumput laut Turbinaria
ornata (Turner) J. Agardh. Rumput laut dibersihkan dari kotoran-kotoran yang
melekat seperti pasir dan sisa-sisa karang, dicuci dengan air mengalir, ditiriskan
kemudian ditimbang sebagai berat basah, selanjutnya dikeringkan dalam lemari
pengering pada temperatur ± 40°C sampai kering (ditandai bila diremas rapuh),
kemudian ditimbang sebagai berat kering. Simplisia yang telah kering dihaluskan
dengan menggunakan blender sampai menjadi serbuk lalu disimpan pada suhu
kamar.
3.5 Pemeriksaan Karakteristik 3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, tekstur
dan ukuran serta pemeriksaan organoleptik dengan mengamati warna, rasa dan
bau dari talus rumput laut Turbinaria ornata (Turner) J. Agardh.
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia rumput laut
Turbinaria ornata (Turner) J. Agardh. Serbuk ditaburkan di atas kaca objek yang
telah ditetesi kloralhidrat, ditutup dengan kaca penutup kemudian diamati di
bawah mikroskop.
a. Penjenuhan toluen
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu
alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2
jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume
air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
b. Penetapan kadar air simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama dimasukkan
ke dalam labu berisi toluen yang telah dijenuhkan, kemudian labu dipanaskan
hati-hati selama 15 menit, setelah toluen mendidih, kecepatan tetesan diatur 2
tetes per detik sampai sebagian besar air terdestilasi. Kecepatan destilasi
dinaikkan sampai 4 tetes tiap detik, setelah semua air terdestilasi, bagian dalam
pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian
tabung penerima dibiarkan mendingin pada suhu kamar, setelah air dan toluen
memisah sempurna, lalu volume air dibaca dengan ketelitian 0,05 ml. Selisih
kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam
bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1998).
3.5.4 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dengan 100 ml
air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu
bersumbat, dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18
jam, kemudian disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai kering
dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa
dipanaskan pada suhu 105ºC sampai bobot tetap. Kadar dalam persen sari yang
3.5.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 ml
etanol 96% di dalam labu bersumbat sambil dikocok sesekali selama 6 jam
pertama, kemudian dibiarkan selama 18 jam, setelah itu disaring cepat untuk
menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan dalam cawan
penguap yang berdasar rata yang telah dipanaskan dan ditara sampai kering. Sisa
yang diperoleh dipanaskan pada suhu 105ºC sampai bobot tetap. Kadar dalam
persen sari yang larut dalam etanol 96% dihitung terhadap bahan yang telah
dikeringkan (Depkes, 1995).
3.5.6 Penetapan kadar abu total
Sebanyak 2 gserbuk simplisia yang telah digerus dan ditimbang seksama
dimasukkan kedalam krus porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus dipijar perlahan-lahan sampai arang habis, pijaran dilakukan pada
suhu 600ºC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh
bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Depkes,
1995).
3.5.7 Penetapan kadar abu yang tidak larut dalam asam
Abu yang diperoleh pada penetapan kadar abu total dididihkan dalam
asam klorida encer sebanyak 25 ml selama 5 menit, bagian yang tidak larut dalam
asam dikumpulkan, disaring melalui kertas saring bebas abu, dicuci dengan air
panas, lalu dipijar sampai bobot tetap, kemudian didinginkan dan ditimbang.
Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah
3.6 Skrining Fitokimia 3.6.1 Pemeriksaan alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml
asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2
menit, didinginkan lalu disaring. Filtrat dipakai untuk tes alkaloid. Diambil 3
tabung reaksi, lalu ke dalam masing-masing tabung reaksi dimasukkan 0,5 ml
filtrat.
Pada tabung I : ditambahkan 2 tetes pereaksi Mayer, terbentuk endapan
menggumpal berwarna putih atau kuning.
Pada tabung II : ditambahkan 2 tetes pereaksi Dragendorff, terbentuk endapan
berwarna coklat atau jingga kecoklatan.
Pada tabung III : ditambahkan 2 tetes pereaksi Bourchardat, terbentuk endapan
berwarna coklat sampai kehitaman.
Alkaloid disebut positif jika terjadi endapan atau kekeruhan pada dua atau
tiga dari percobaan di atas (Depkes, 1995).
3.6.2 Pemeriksaan flavonoid
Serbuk simplisia ditimbang sebanyak 10 g, ditambahkan 10 ml air panas,
dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml
filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml
amil alkohol, dikocok dan dibiarkan memisah. Flavonoid positif jika terjadi warna
merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g, lalu disari dengan 30 ml
asam klorida 2 N, kemudian direfluks selama 10 menit, didinginkan, lalu disaring.
Diambil 20 ml filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4
M dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran
isopropanol dan kloroform (2:3), perlakuan ini diulangi sebanyak 3 kali. Sari
organik dikumpulkan dan ditambahkan Na2SO4 anhidrat, disaring, kemudian
diuapkan pada temperatur tidak lebih dari 50ºC, sisanya dilarutkan dalam 2 ml
metanol. Sari air digunakan untuk percobaan berikut, 0,1 larutan percobaan
dimasukkan dalam tabung reaksi, kemudian diuapkan di atas penangas air. Pada
sisa ditambahkan 2 ml air dan 5 tetes larutan pereaksi Molish, lalu ditambahkan
dengan perlahan-lahan 2 ml asam sulfat pekat melalui dinding tabung, terbentuk
cincin ungu pada batas kedua cairan, menunjukkan adanya ikatan gula (glikon)
atau glikosida (Depkes, 1995).
3.6.4 Pemeriksaan saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukkan ke dalam
tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan kemudian dikocok
kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1 sampai 10 cm yang
stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes
asam klorida 2 N menunjukkan adanya saponin (Depkes, 1995).
3.6.5 Pemeriksaan tanin
Serbuk simplisia ditimbang sebanyak 0,5 g, disari dengan 10 ml air suling
lalu disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan
diambil sebanyak 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%.
Warna biru atau hijau kehitaman yang terjadi pada larutan menunjukkan adanya
3.6.6 Pemeriksaan steroid/triterpenoid
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml n-heksan selama 2
jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan
beberapa tetes pereaksi Liebermann-Burchard. Warna biru atau biru kehijauan
yang terjadi menunjukkan adanya steroid, sedangkan warna merah, merah muda
atau ungu menunjukkan adanya triterpenoid (Harborne, 1987).
3.7 Pembuatan Ekstrak
Pembuatan ekstrak n-heksan rumput laut Turbinaria ornata (Turner) J.
Agardh dilakukan dengan cara perkolasi. Prosedur pembuatan ekstrak secara
perkolasi, yaitu sebanyak 500 g serbuk simplisia dibasahi dengan n-heksan dan
dibiarkan selama 3 jam kemudian dimasukkan ke dalam alat perkolator, lalu
dituang cairan penyari n-heksan sampai semua simplisia terendam dan terdapat
selapis cairan penyari diatasnya, mulut tabung perkolator ditutup dengan
alumunium foil dan dibiarkan selama 24 jam, kemudian kran dibuka dan
dibiarkan tetesan ekstrak mengalir dengan kecepatan 1 ml per menit, perkolat
ditampung. Cairan penyari ditambahkan berulang-ulang secukupnya sehingga
selalu terdapat cairan penyari di atas simplisia. Perkolasi dihentikan setelah
tetesan perkolat terakhir tidak bereaksi lagi dengan pereaksi
Liebermann-Bouchard. Ekstrak lalu dipekatkan dengan alat penguap vakum putar hingga
diperoleh ekstrak kental (Depkes, 1979).
3.8 Analisis Ekstrak n-heksan secara Kromatografi Lapis Tipis (KLT)
Ekstrak n-heksan dianalisis secara KLT menggunkan fase diam silika gel
(90:10), (80:20), (70:30), (60:40) dan (50:50). Sebagai penampak bercak
digunakan pereaksi Liebermann-Bouchard.
Cara kerja:
Ekstrak dilarutkan dengan n-heksan lalu ditotolkan pada plat lapis tipis
silika gel GF254, kemudian dimasukkan kedalam chamber yang telah jenuh
dengan uap fase gerak. Fase gerak dibiarkan naik sampai batas pengembang. Plat
dikeluarkan dan dikeringkan, lalu disemprot dengan penampak bercak
Liebermann-Bouchard, kemudian dipanaskan dalam oven pada suhu 110○C
selama 10 menit lalu diamati warna yang terbentuk dan dihitung harga Rf.
Kromatogram hasil KLT dapat dilihat pada Lampiran 8, halaman 49.
3.9 Isolasi Ekstrak n-heksan dengan Kromatografi Kolom
Ekstrak n-heksan di kromatografi kolom menggunakan pelarut landaian
yaitu n-heksan:etil asetat dengan perbandingan 100:0, 90:10, 80:20, 70:30, 60:40,
50:50, 40:60, 30:70, 20:80, 10:90, 0:100 dan diakhiri dengan metanol.
Cara kerja:
Seperangkat alat kromatografi kolom dipasang kemudian ke dalam dasar
kolom dimasukkan kapas yang telah bebas lemak, kemudian dimasukkan larutan
fase gerak. Silika gel 60 H dibuat bubur dengan larutan fase gerak n-heksan
diaduk sampai homogen dan bebas dari gelembung udara, kran dibuka kemudian
bubur silika dimasukkan kedalam kolom secara perlahan-lahan sambil dinding
kolom diketuk-ketuk untuk menghilangkan gelembung udara dan fase gerak tetap
dialiri sampai semua silika gel turun, lalu didiamkan sampai kolom kompak,
n-heksan ditambahkan dengan sedikit fase diam dan diaduk rata lalu dimasukkan
kedalam kolom secara perlahan-lahan. Setelah sampel turun tepat setinggi fase
diam melalui dinding kolom secara perlahan-lahan dialiri dengan fase gerak
sambil kran kolom dibuka. Hasil elusi masing-masing ditampung sebanyak 5 ml
dalam vial yang telah diberi nomor. Untuk pola kromatogram yang sama
digabung menjadi satu fraksi. Kromatogram analisis KLT hasil kromatografi
kolom dapat dilihat pada Lampiran 9, halaman 51.
3.10 Pencucian Kristal
Kristal hasil isolasi Kromatografi Kolom dicuci berulang kali dengan
metanol dingin tetes demi tetes sampai diperoleh kristal amorf berwarna putih.
3.11 Uji Kemurnian Isolat
Isolat hasil isolasi dilakukan KLT dua arah menggunakan fase gerak I
yaitu n-heksan:etilasetat (70:30) dan fase gerak II toluen:etilasetat (80:20) dengan
fase diam plat lapis tipis silika gel GF254 dan penampak bercak pereaksi
Liebermann-Burchard.
Cara kerja:
Isolat ditotolkan pada plat lapis silika gel GF254 ukuran 10x10 lalu dielusi
memakai fase gerak I yaitu n-heksan:etilasetat (70:30) hingga mencapai batas
pengembang, kemudian plat dikeluarkan dari dalam bejana dan dikeringkan.
Setelah plat kering dielusi kembali dengan arah yang berbeda 90° memakai fase
gerak II yaitu toluen:etilasetat (80:20), disemprot dengan memakai penampak
bercak Liebermann-Burchard, setelah itu plat dipanaskan pada suhu 105℃ selama
10 menit lalu diamati warna yang terbentuk. Hasil uji kemurnian isolat dapat
3.12 Identifikasi Isolat
Identifikasi isolat dilakukan secara spektrofotometri ultraviolet dan
spektrofotometri inframerah yang dilakukan di Laboratorium Penelitian Fakultas
Farmasi USU Medan.
3.12.1 Identifikasi isolat secara Spektofotometri UV Cara kerja:
Identifikasi isolat secara spektrofotometri UV dilakukan dengan cara isolat
dilarutkan dalam pelarut metanol, kemudian dimasukkan kedalam kuvet yang
telah dibilas dengan larutan sampel. Absorbansi larutan sampel diukur pada
panjang gelombang 200-400 nm. Hasil identifikasi isolat secara Spektrofotometri
UV dapat dilihat pada Lampiran 11, halaman 56.
3.12.2 Identifikasi isolat secara Spektrofotometri IR Cara kerja:
Identifikasi isolat secara spektrofotometri IR dilakukan dengan cara
mencampurkan 1 mg isolat dengan 150 mg kalium bromida menggunakan alat
mixture vibrator, kemudian dicetak menjadi pelet pada tekanan 11,5 ton dan
dimasukkan ke dalam spektrofotometer inframerah serta diukur absorbansinya
pada frekuensi 400-4000 cm-1. Hasil Identifikasi isolat secara Spektrofotometri IR
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Lembaga Ilmu Penelitian
Indonesia Pusat Penelitian Oseanografi, Jakarta adalah rumput laut jenis
Turbinaria ornata (Turner) J. Agardh, famili Sargassaceae. Hasil identifikasi
tumbuhan dapat dilihat pada Lampiran 1, halaman 41.
4.1Hasil Karakterisasi
4.2.1 Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik terhadap tanaman segar rumput laut
Turbinaria ornata (Turner) J. Agardh diperoleh berupa talus utama silindris, tegak
dan kasar, tinggi mencapai 17 cm, bentuk daun yang menyerupai terompet dengan
pinggir tajam dengan organoleptik warna coklat tua dan memiliki rasa dan bau
yang khas dan hasil pemeriksaan makroskopik terhadap simplisia rumput laut
Turbinaria ornata (Turner) J. Agardh diperoleh simplisia berupa talus yang
mengecil dengan panjang 5-9 cm dan daun yang menciut dengan organoleptik
warna coklat tua dan memiliki rasa dan bau yang khas. Gambar rumput laut segar
simplisia dapat dilihat pada Lampiran 3, halaman 43.
Hasil pemeriksaan makroskopik terhadap serbuk simplisia rumput laut
diperoleh serbuk kasar, organoleptik warna coklat serta memiliki rasa dan bau
yang khas. Gambar serbuk simplisia dapat dilihat pada Lampiran 3, halaman 44.
4.2.2 Hasil pemeriksaan mikroskopik
Hasil mikroskopik dari serbuk simplisia diperoleh adanya sel parenkim
merupakan sel-sel yang berperan dalam perkembangbiakan (Stewart, 2006).
Gambar hasil mikroskopik serbuk simplisia dapat dilihat pada Lampiran 5,
halaman 45.
4.2.3 Hasil pemeriksaan karakteristik
Hasil pemeriksaan karakteristik dari serbuk simplisia rumput laut
Turbinaria ornata (Turner) J. Agardh dapat diliat pada Tabel 4.1 berikut:
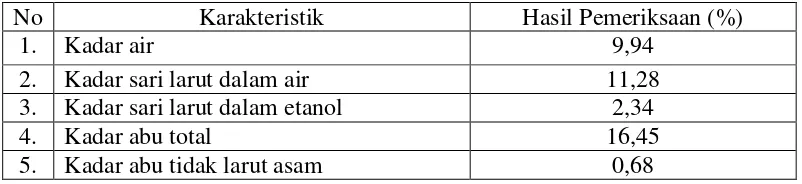
Tabel 4.1 Hasil pemeriksaan karakteristik simplisia rumput laut
No Karakteristik Hasil Pemeriksaan (%)
1. Kadar air 9,94
2. Kadar sari larut dalam air 11,28 3. Kadar sari larut dalam etanol 2,34
4. Kadar abu total 16,45
5. Kadar abu tidak larut asam 0,68
Monografi simplisia rumput laut Turbinaria ornata (Turner) J. Agardh
belum tercantum dalam Materia Medika Indonesia (MMI), sehingga tidak ada
acuan dalam menentukan parameternya. Tabel 4.1 menunjukkan kadar air pada
simplisia rumput laut sebesar 9,94%, kadar tersebut memenuhi persyaratan umum
yaitu lebih kecil dari 10%. Kadar air yang lebih besar dari 10% dapat menjadi
media pertumbuhan kapang dan jasad renik lainnya (Depkes, 2000).
Penetapan kadar sari yang larut dalam air menyatakan jumlah zat yang
tersari dalam pelarut air seperti glikosida, gula, protein, enzim dan zat warna,
sedangkan penetapan kadar sari yang larut dalam etanol menyatakan jumlah zat
yang tersari dalam pelarut etanol seperti glikosida, steroid, flavonoid, saponin,
tanin (Depkes, 1995).
Penetapan kadar abu total dan kadar abu tidak larut asam bertujuan untuk
melebihi nilai yang ditetapkan karena dapat berbahaya (toksik) bagi kesehatan.
Penetapan kadar abu total menyatakan jumlah kandungan senyawa anorganik
dalam simplisia misalnya Mg, Ca, Na, Zn dan K. Kadar abu tidak larut dalam
asam untuk mengetahui kadar senyawa anorganik yang tidak larut dalam asam
misalnya silikat. Perhitungan pemeriksaan karakteristik serbuk simplisia rumput
laut Turbinaria ornata (Turner) J. Agardh dapat dilihat pada Lampiran 13,
halaman 58-62.
4.3 Hasil Skrining Fitokimia
Hasil skrining fitokimia terhadap rumput laut Turbinaria ornata (Turner) J.
Agardh diketahui bahwa talus rumput laut mengandung senyawa-senyawa kimia
seperti terlihat pada tabel 4.2 dibawah ini:
Tabel 4.2 Hasil skrining fitokimia simplisia rumput laut
No Pemeriksaan Hasil
1. Alkaloid -
2. Flavonoid -
3. Glikosida +
4. Saponin +
5. Steroid/Triterpenoid +
6. Tanin -
Keterangan: (+) Positif : mengandung golongan senyawa (−) Negatif : tidak mengandung golongan senyawa
Hasil skrining fitokimia terhadap serbuk simplisia diperoleh simplisia
tidak mengandung alkaloid, penambahan pereaksi Mayer, Bourchardat maupun
Dragendroff tidak terbentuk endapan; mengandung glikosida, penambahan
pereaksi Molish dan asam sulfat pekat membentuk cincin ungu; mengandung
saponin, terbentuknya busa lebih besar dari 1 cm yang stabil dengan pengocokkan
mengandung triterpenoid, penambahan pereaksi Liebermann-Burchad membentuk
warna merah ungu (Robinson, 1995).
4.4 Hasil Isolasi Senyawa Steroid/Triterpenoid
Ekstraksi dilakukan dengan cara perkolasi menggunakan pelarut n-heksan,
dari hasil perkolasi 500 g serbuk simplisia diperoleh ekstrak sebanyak 1,6 g.
Analisis KLT dari ekstrak n-heksan menunjukkan bahwa fase gerak yang dipilih
adalah n-heksan:etilasetat (70:30) karena menghasilkan pemisahan noda steroid/
triterpenoid yang paling baik.
Ekstrak n-heksan diisolasi secara kromatografi kolom dengan pelarut landaian n
-heksan:etilasetat dengan perbandingan 100:0, 90:10, 80:20, 70:30,60:40, 50:50,
40:60, 30:70, 20:80, 10:90, 0:100, dan metanol sehingga diperoleh eluat sebanyak
74 vial. Masing-masing eluat dikromatografi lapis tipis dengan fase gerak n
-heksan:etilasetat (70:30) dengan penampak bercak Lieberman-Burchard. Eluat
yang mempunyai pola kromatogram yang sama di gabung menjadi satu fraksi,
sehingga diperoleh 13 eluat yaitu E1 (vial 1-13), E2 (vial 14-16), E3 (vial 17-20),
E4 (vial 21-22), E5 (vial 23-25), E6 (vial 26-29), E7 (vial 30-34), E8 (vial 35-43),
E9(vial 44-49), E10 (vial 50-56), E11 (vial 57-59), E12 (vial 60-68) dan E13
(69-74). Noda berwarna merah ungu dengan pemisahan yang baik terdapat pada E6
(vial 26-29), pada E6 ditemukan kristal yaitu pada V26, V27, V28, V29 kemudian
dilakukan penggabungan pada keempat vial tersebut, karena masih terdapat
pengotoran maka kristal dicuci dengan metanol dingin sampai diperoleh kristal
yang baik dan murni. Terhadap isolat dilakukan KLT dua arah dengan fase gerak I
n-heksan:etilasetat (70:30) dan fase gerak II toluen-etilasetat (80:20). Isolat
Isolat diidentifikasi secara spektrofotometri ultraviolet (UV) dan
spektrofotometri inframerah (IR). Hasil pengukuran secara spektrofotometri UV
dapat dilihat pada gambar berikut ini:
Pada hasil pengukuran secara spektrofotometri UV memberikan panjang
gelombang maksimum sebesar 206,80 nm, hal ini menunjukan adanya gugus
kromofor (Dachriyanus, 2004).
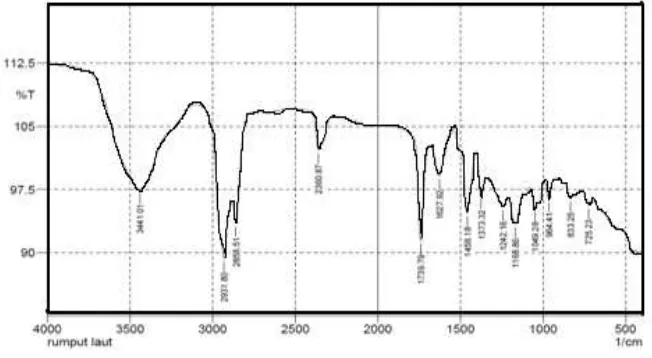
Hasil spektrofotometri inframerah (IR) menunjukkan pada bilangan
gelombang 3441,01cm-1 terdapat gugus -OH (3200-3500 cm-1). Gugus -OH
tersebut diperkuat oleh adanya serapan pada daerah bilangan gelombang
1029,28cm-1 yang menunjukkan adanya gugus C-O (990-1060 cm-1). Adanya pita
yang tajam dan kuat pada bilangan gelombang 2931,80 cm-1 menunjukkan adanya
gugus C-H alifatis yang diperkuat oleh puncak pada bilangan gelombang 1458,18
cm-1 menunjukkan adanya gugus metilen (CH2) (1450-1470 cm-1). Puncak pada
bilangan gelombang 1373,32cm-1 menunjukkan adanya gugus metil (CH3)
(1350-A
bs
or
ba
ns
i
1380 cm-1). Pita serapan pada bilangan gelombang 1627,92 cm-1 menunjukkan
adanya gugus C=C non konjugasi (1500-1900 cm-1) (Supratman, 2010).
Pengukuran dengan spektrofotometri inframerah dilakukan untuk
mengetahui gugus fungsi dari suatu senyawa. Menyinari sebuah molekul dengan
sinar infra merah yang berbeda-beda frekuensi atau bilangan gelombangnya maka
gugus-gugus fungsi dari tingkatan energi yang sesuai akan bergetar (Supratman,
2010). Gugus fungsi tersebut akan menyerap sinar inframerah dengan bilangan
gelombang yang akan direkam dalam puncak sebuah spektrum.
Berikut ini adalah gambar spektrum inframerah dari isolat
Gambar 4.1 Spektrum inframerah isolat
Tabel 4.3 Data bilangan gelombang isolat hasil isolasi dengan spektrofotometri inframerah
No. Bilangan Gelombang (Cm-1) Gugus Fungsi
1. 1029,28 C-O
2. 1373,32 -CH3
3. 1458,18 -CH2
4. 1627,92 C=C
5. 2931,80 C-H Alifatis
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat diambil
kesimpulan bahwa:
a. Hasil karakterisasi simplisia rumput laut Turbinaria ornata (Turner) J.
Agardh diperoleh kadar air 9,94%, kadar sari yang larut dalam air 11,28%,
kadar sari yang larut dalam etanol 2,34%, kadar abu total 16,45% dan
kadar abu yang tidak larut asam 0,68%.
b. Hasil skrining fitokimia simplisia rumput laut Turbinaria ornata (Turner)
J. Agardh mengandung senyawa kimia glikosida, saponin dan
steroid/triterpenoid.
c. Hasil analisis isolat secara spektrofotometri UV memberikan panjang
gelombang maksimum 206,8 nm dan hasil pengukuran dengan
spektrofotometri inframerah menunjukkan adanya gugus C-O, -CH3, -CH2,
C=C, C-H alifatis dan –OH.
5.2 Saran
Peneliti selanjutnya disarankan untuk elusidasi struktur kimia dari
senyawa steroid/triterpenoid yang terdapat dalam ekstrak n-heksan rumput laut