EVALUASI PENGARUH GELLING AGENT TERHADAP STABILITAS FISIK dan PROFIL DIFUSI SEDIAAN GEL
MINYAK BIJI JINTEN HITAM (Nigella sativa Linn)
Skripsi
Oleh:
ARDIAN S. NURHAKIM NIM: 106102003366
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN UNIVERSITAS ISLAM NEGERI (UIN) SYARIF HIDAYATULLAH
MINYAK BIJI JINTEN HITAM (Nigella sativa Linn)
Skripsi
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Far)
Oleh:
ARDIAN S. NURHAKIM NIM: 106102003366
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN UNIVERSITAS ISLAM NEGERI (UIN) SYARIF HIDAYATULLAH
ii
LEMBAR PERSETUJUAN SKRIPSI
NAMA : ARDIAN S. NURHAKIM NIM : 106102003366
JUDUL : EVALUASI PENGARUH GELLING AGENT TERHADAP STABILITAS FISIK dan PROFIL DIFUSI SEDIAN GEL MINYAK BIJI JINTEN HITAM (Nigella sativa Linn)
Disetujui oleh :
Pembimbing I Pembimbing II
Farida Sulistiawati, M.Si, Apt Yuni Anggraeni, S.Si, Apt NIP. 196701052006042001 NIP. 198310282009012008
Mengetahui,
Ketua Program Studi Farmasi UIN Syarif Hidayatullah Jakarta
iii
EVALUASI PENGARUH GELLING AGENT TERHADAP STABILITAS FISIK dan PROFIL DIFUSI SEDIAAN GEL
MINYAK BIJI JINTEN HITAM (Nigella sativa Linn)
Telah disetujui, diperiksa dan dipertahankan dihadapan tim penguji oleh Ardian S. Nurhakim
NIM: 106102003366
Menyetujui, Pembimbing:
1. Pembimbing I Farida Sulistiawati, M.Si, Apt. ... 2. Pembimbing II Yuni Anggraeni, S.Si, Apt. ...
Penguji:
1. Ketua Penguji Drs. M. Yanis Musdja, M.Sc, Apt. ... 2. Anggota Penguji I Drs. M. Yanis Musdja, M.Sc, Apt. ... 3. Anggota Penguji II Zilhadia, M.Si, Apt. ... 4. Anggota Penguji III Ahmad Musir, M.Sc, Apt. ...
Mengetahui,
Dekan Fakultas Kedokteran Dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta
Prof. DR. (hc). dr. M.K. Tadjudin, Sp. And
iv
LEMBAR PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI BENAR-BENAR HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA MANAPUN.
BOGOR, 27 SEPTEMBER 2010 18 SYAWAL 1431
v
Teruntuk Ayah Bundaku yang selalu Ananda cintai dalam relung hati yang terdalam
Ibarat sinar mentari begitulah kasihmu sepanjang zaman yang teruntai begitu indahnya
Ananda haturkan terima kasih atas segala kasih sayang yang sedari kecil telah diberikan dengan tulus
Setiap doa yang terlantun untuk Ananda menjadi pelipur hati dalam setiap langkah.
Tanpa cintamu bagai taman tak berbunga dan bagaikan malam tak berbintang
Pengorbananmu tak akan pernah tergantikan dengan apapun yang Ananda miliki
Duhai Rabbi sejahterakanlah Ayah Bundaku dengan nikmat-Mu yang tak pudar ditelan masa
Teruntuk Saudaraku yang kusayangi karena Allah
Tanamlah cinta dalam hati
Biarkan Ia tumbuh berkembang hanya karena Allah
Ukirlah dalam setiap langkah agar Ia senantiasa terlukis indah di dasar jiwa
Ingatlah bahwa kita semua ada dalam kekuasaan Allah dan cinta kasih-Nya
vi ABSTRAK
Judul : Evaluasi Pengaruh Gelling Agent Terhadap Stabilitas Fisik dan Profil Difusi Sediaan Gel Minyak Biji Jinten Hitam (Nigella sativa Linn)
Minyak biji jinten hitam (Nigella sativa Linn) diketahui berkhasiat untuk menyembuhkan berbagai penyakit dan masalah pada kulit, salah satunya sebagai antioksidan. Oleh karena itu minyak biji jinten hitam dibuat sediaan gel dengan variasi gelling agent. Komposisi basis gel dibuat dengan menggunakan tiga gelling agent, yaitu Natrium Karboksi Metil Selulosa (Na CMC) dengan konsentrasi 4%, 5%; Hidroksi Propil Metil Selulosa (HPMC) dengan konsentrasi 3%, 4%; dan Karbopol 940 dengan konsentrasi 0,5%, 1%. Berdasarkan hasil evaluasi pemeriksaan fisik dan pelepasan zat aktif, gel menunjukan stabilitas fisik yang baik dan formula VI (basis karbopol 1%) menunjukan pelepasan zat aktif paling tinggi.
vii
Title : Evaluation of Gelling Agent Effect On the Physical Stability and Diffusion Profile of Gel Black Cumin Seed Oil (Nigella sativa Linn)
Black cumin seed oil (Nigella sativa Linn) is known efficacious to cure various diseases and skin problems, such as antioxidant. Therefore, black cumin seed oil gel was formulated with a variety of gelling agent. The composition of the gel base was made by using the three gelling agents, namely Sodium Carboxy Methyl Cellulose (Na CMC) with a concentration of 4%, 5%; Hydroxy Propyl Methyl Cellulose (HPMC) with a concentration of 3%, 4%, and Carbopol 940 with a concentration of 0,5 %, 1%. Based on the evaluation of physical stability and release of active substances, gel showed good physical stability and the formula VI (Carbopol base 1%) showed the highest release of active substances.
viii
KATA PENGANTAR
Segala puji bagi Allah Tuhan semesta alam, yang telah memberi pertolongan serta kemampuan kepada kami, karena hanya dari-Nya lah segala kekuatan sehingga kami dapat menyelesaikan skripsi dengan judul “Evaluasi Pengaruh Gelling Agent Terhadap Stabilitas Fisik dan Profil Difusi Sediaan Gel Minyak Biji Jinten Hitam (Nigella sativa Linn)”. Semoga shalawat dan salam senantiasa tercurah kepada junjungan kita, Nabi Muhammad SAW, penyandang gelar al-amin teladan yang mulia, keluarga dan para sahabatnya, serta orang-orang yang mengikuti jejak mereka hingga hari pembalasan nanti.
Tulisan ini tidak akan terwujud, hingga orang-orang baik hati membantu dan mendukung kami dalam menyelesaikannya. Ketulusan hati kami untuk menuturkan terima kasih kepada orang-orang dermawan yang telah banyak membantu, baik berupa materi, teori, ilmu, waktu dan segalanya yang begitu berharga.
Kepada Ibu Farida Sulistiawati M.Si, Apt., selaku pembimbing I, dan Ibu Yuni Anggraeni S.Si, Apt., selaku pembimbing II, kami haturkan terima kasih banyak atas bimbingan, bantuan, motivasi, dan arahannya.
ix
memberikan semangat terus tanpa henti baik moril, materil dan kasih sayang. Terima kasih atas pengorbanan Ayah Bunda kami, karena beliau kami tetap semangat dan tegar setiap menjalani hidup ini. Serta adikku Egi B. Rivai dan Rivkie S. Ramadhani atas segala dukungannya.
Kepada staff dan karyawan Farmasi UIN, Bapak Zamzani Kiran, Mbak Via, Mas Anang, Mas Taufik, dan Mas Toni terima kasih telah banyak membantu dalam proses penelitian.
Kepada staff laboran Ka Pritta, Ka Pipit, Ka Eris Risenti, dan Ka Nurul, terima kasih banyak telah membantu dalam proses penelitian ini hingga selesai.
Kepada teman-teman Farmasi angkatan 2006, junior maupun senior di FKIK UIN jakarta, khususnya di jurusan Farmasi, terima kasih atas dukungan, dan bantuannya selama ini.
Kepada teman-teman perumahan Bukit Asri Ciomas Bogor, meskipun mereka agak sedikit bandel Insyaallah mereka semua adalah orang-orang yang baik, terima kasih atas segala dukungan, canda, dan kebaikan kalian semua.
x
Akhirnya, semoga Allah membalas kita semua dengan kebaikan, meridhai kita dalam segala gerak langkah kehidupan kita, memenuhi hati kita dalam perasaan kaya, dan memenuhi kedua tangan kita dengan rizki yang baik penuh barakah, karena tawakkal dan ridha kita kepada-Nya. Semoga apa yang kita usahakan di dunia menjadi amal baik, bekal kita menghadap Allah SWT. Amin
Semoga dalam mengarungi kehidupan ini, kita menjadi seorang mukmin sebagaimana yang disabdakan oleh Rasulullah SAW:
"Sungguh menakjubkan urusan seorang mukmin. Semua urusannya mengandung kebaikan baginya dan hal ini tidak berlaku bagi seorangpun, kecuali seorang mukmin. Jika mendapat kenikmatan, Ia bersyukur, maka itu baik baginya. Dan jika tertimpa musibah Ia bersabar, maka itu pun baik baginya." (HR. Muslim)
Bogor, 27 September 2010 18 Syawal 1431
xi
BAB II. TINJAUAN PUSTAKA 2.1 Jinten Hitam (Nigella sativa L.)... 4
BAB IV. METODOLOGI PENELITIAN 4.1 Tempat dan Waktu Penelitian ... 23
4.2 Bahan dan Alat ... 23
4.3 Cara Kerja ... 24
BAB V. HASIL PENELITIAN DAN PEMBAHASAN 5.1 Hasil Penelitian ... 33
5.2 Pembahasan ... 38
BAB VI. KESIMPULAN DAN SARAN 6.1 Kesimpulan ... 43
6.2 Saran ... 43
DAFTAR PUSTAKA ... 44
xii
DAFTAR TABEL
Halaman
Tabel 1. Formula Gel Minyak Jinten Hitam... 29
Tabel 2. Hasil Penapisan Fitokimia Biji Jinten Hitam ... 33
Tabel 3. Hasil Penapisan Fitokimia Minyak Jinten Hitam... 34
Tabel 4. Hasil Pemeriksaan Minyak Jinten Hitam ... 34
Tabel 5. Hasil Pemeriksaan Organoleptis ... 35
Tabel 6. Hasil Pemeriksaan Homogenitas... 36
Tabel 7. Hasil Pemeriksaan pH ... 36
Tabel 8. Hasil Pemeriksaan Viskositas ... 37
Tabel 9. Hasil Pemeriksaan Stabilitas Fisik ... 37
xiii
Gambar 1. Penampang Kulit Graaff ... 15
Gambar 2. Struktur Karbomer 940 ... 19
Gambar 3. Struktur HPMC ... 20
Gambar 4. Struktur Na CMC... 20
Gambar 5. Tanaman Jinten Hitam (Nigella sativa L.) ... 48
Gambar 6. Biji Jinten Hitam (Nigella sativa L.) ... 48
Gambar 7. Kurva Serapan Minyak Jinten Hitam... 51
Gambar 8. Evaluasi Pemeriksaan Stabilitas Fisik ... 52
Gambar 9. Kurva Hasil Pemeriksaan Difusi ... 62
Gambar 10. pH meter ... 63
Gambar 11. Viskometer Brookfield... 63
Gambar 12. Refraktometer ... 63
Gambar 13. Spektrofotometer UV-Vis ... 63
xiv
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Tanaman dan Biji Jinten Hitam (Nigella sativa L.) ... 48
Lampiran 2. Perhitungan Bobot Jenis Minyak Jinten Hitam ... 49
Lampiran 3. Hasil Scanning λ Maksimum Minyak Jinten Hitam ... 50
Lampiran 4. Kurva Serapan Minyak Jinten Hitam ... 51
Lampiran 5. Evaluasi Pemeriksaan Stabilitas Fisik ... 52
Lampiran 6. Absorbansi Pemeriksaan Difusi ... 54
Lampiran 7. Perhitungan Pemeriksaan Difusi ... 60
Lampiran 8. Perhitungan Faktor Koreksi (FK) Pemeriksaan Difusi ... 61
Lampiran 9. Evaluasi Pemeriksaan Difusi ... 62
Lampiran 10. Gambar dan Alat Penelitian ... 63
1 BAB I PENDAHULUAN
1.1 Latar Belakang
2
Untuk mengatasi penyakit dan gangguan pada kulit, dibutuhkan suatu sediaan yang mempunyai daya penetrasi yang baik, waktu kontak yang cukup lama, dan dosis yang sesuai. Minyak biji jinten hitam (Nigella sativa L.) secara tradisional telah digunakan untuk mengatasi penyakit dan gangguan pada kulit, salah satunya berkhasiat sebagai antioksidan. Minyak biji jinten hitam dapat dibuat menjadi suatu sediaan farmasi, salah satunya adalah sediaan gel, dimana sediaan gel mempunyai kadar air yang tinggi, sehingga dapat menghidrasi stratum corneum dan juga mengurangi resiko timbulnya peradangan lebih lanjut akibat menumpuknya minyak pada pori-pori.
Bentuk sediaan semisolid merupakan bentuk yang sangat ideal karena penggunaannya lebih praktis. Sedian gel merupakan bentuk sediaan semisolid yang banyak digunakan dalam kosmetika karena lebih mudah dibuat, lebih cepat menyebar ke permukaan kulit, pelepasan obatnya baik, lebih enak dipakai karena pada pemakain di kulit setelah kering meninggalkan film tembus pandang elastis, daya lekat tinggi, dan mudah dicuci dengan air. Untuk menghasilkan gel yang baik diperlukan suatu formula gel yang mengandung bahan-bahan yang cocok dengan konsentrasi yang sesuai.
Pada penelitian ini akan dibuat enam macam formula gel minyak jinten hitam (Nigella sativa L.) dengan variasi jenis dan konsentrasi gelling agent. Variasi jenis dan konsentrasi gelling agent ini akan dilihat
1.1 Perumusan Masalah
1. Apakah minyak biji jinten hitam (Nigella sativa L.) dapat dibuat menjadi sediaan gel yang baik dan stabil?
2. Bagaimana pengaruh konsentrasi dan jenis gelling agent yang digunakan terhadap stabilitas fisik dan profil difusi sediaan gel minyak biji jinten hitam (Nigella sativa L.)?
1.2 Tujuan Penelitian
Menentukan jenis dan konsentrasi gelling agent yang dapat menghasilkan sediaan gel minyak biji jinten hitam (Nigella sativa L.) yang baik dan stabil.
1.3 Manfaat Penelitian
4 BAB II
TINJAUAN PUSTAKA
2.1
Jinten Hitam (Nigella sativa L.) (Depkes RI, 1979; Depkes RI, 1989) 2.1.1 KlasifikasiBerdasarkan ilmu taksonomi, klasifikasi tanaman jinten hitam adalah sebagai berikut :
Kingdom : Plantae Subkingdom : Traceabionta Divisi : Spermatophyta Subdivisi : Magnoliophyta
Kelas : Magnoliopsida dicotyledon Subkelas : Magnoliidae
Ordo : Ranunculales Famili : Ranunculaceae Genus : Nigella Linn. Spesies : Nigella sativa Linn.
Nama lain Nigella sativa L. diantaranya adalah : Kalonji (bahasa
Hindi), Kezah (Hebrew), Chamushka (Rusia), Habbatus Sauda’
2.1.1 Morfologi
Nigella sativa Linn atau Jintan Hitam Pahit ini merupakan jenis
tanaman bunga, terna setahun berbatang tegak. Tumbuh setinggi 20-50 cm, berkayu, dan berbentuk bulat menusuk. Batang biasanya berusuk dan berbulu kasar, rapat, atau jarang-jarang, dan disertai dengan adanya bulu-bulu yang berkelanjar. Bentuk daun lanset (bulat telur berujung lancip), berbentuk garis panjang 1,5 cm sampai 2 cm, ujung lancip terdapat tiga tulang daun yang berbulu, daunnya kadang-kadang tunggal, atau bisa juga majemuk dengan posisi tersebar atau berhadapan. Daun bagian bawah bertangkai dan bagian atas duduk. Daun pembalut bunga kecil. Di bagian permukaan daunnya terdapat bulu halus.
6
Buah bulat telur atau agak bulat. Buahnya keras seperti buah buni. Berbentuk besar, menggembung, berisi 3-7 unit folikel, masing-masing berisi banyak biji atau benih yang sering digunakan manusia sebagai rempah-rempah.
Biji hitam, jorong bersudut tiga tak beraturan, dan sedikit berbentuk kerucut, panjang 3 mm, berkelanjar. Bijinya berwarna hitam pekat.
2.1.2 Budidaya
Tanaman ini diperbanyak dengan biji. Di Indonesia tanaman ini belum dibudidayakan secara umum.
2.1.3 Ekologi dan penyebaran
Tumbuh dari daerah Levant ke arah timur Samudra Indonesia sebagai gulma semusim.
2.1.4 Bagian tanaman yang digunakan Biji
2.1.5 Kandungan kimia
Biji jinten hitam mengandung asam lemak (35,6-41,6%), meliputi asam arakidonat, asam linolenat, asam linoleat, asam oleat, asam palmitat, asam stearat, dan asam miristat. Minyak atsiri (0,5-1,6%), meliputi nigellone, thymoquinone, thymohydroquinone, dithymoquinone, thymol, carvacrol, α dan β-pinene, d-limonene, d-citronellote, dan p-cymene. Protein (22,7%), asam amino meliputi
prolin, serin, treonin, triptopan dan tirosin. Alkaloid meliputi nigellicine, nigellidine-N-oxide. Mineral (1,79-3,74%), meliputi Fe,
Na, Cu, Zn, P, dan Ca. Vitamin seperti asam askorbat, tiamin, niasin, piridoksin, dan asam folat, serta karbohidrat (33,9%), serat (5,5%), air (6%), jadi juga memiliki nilai gizi. Selain itu, terkandung senyawa flavonoid, saponin, dan tannin, asam organik. Bijinya juga mengandung lipase, fitosterol, dan β-sitosterol. (Hassan Gilani et al, 2004).
Pada bagian luar (kulit) biji terdapat sulfat (garam asam belerang), fosfor, fosfat, karotin, besi, dan salinium. Pada bagian dalam (isi), terdapat kandungan minyak, enzim, hormon, dan bahan-bahan karbohidrat dan protein. Pada bagian yang memisahkan kulit dan isi, yang berwarna cokelat mengandung tocopherol, bahan-bahan yang bersifat sulfat, dan tembaga, juga mengandung antibiotik serta hormon-hormon dan sebagainya. (Hasan M.M, 2007).
2.1.6 Khasiat dan Kegunaan (Hassan et al, 2004; Padhye et al, 2008)
8
penyinaran; memperkuat sistem kekebalan tubuh, memperlambat penuaan sel, menekan rasio sel-T sebagai indikator penyakit; antioksidan yang mampu membuang racun dari dalam tubuh (detoksifikasi); karena kandungan asam lemak tidak jenuh yang tinggi, minyak jinten hitam sangat rentan terhadap oksidasi. Pada penyumbatan (sembelit) dalam tubuh diperlukan perlindungan selanjutnya dari pengaruh buruk oksigen reaktif; memberikan asupan kandungan nutrisi yang tinggi meliputi monosakarida, silosa, dan arabinosa; meningkatkan produksi susu pada ibu menyusui. Hal ini disebabkan adanya kombinasi antara porsi lipid dan struktur hormon; menjaga stamina, memperkuat daya konsentrasi; mengatasi problema paru-paru; menyembuhkan radang pada persendian atau rematik; mengatasi impotensi.
2.2
Minyak LemakMinyak lemak (Olea pinguia) adalah suatu cairan jernih atau massa padat yang menjadi jernih di atas suhu leburnya, tidak berbau asing atau tengik, mudah larut dalam kloroform P, eter P, dan dalam eter minyak tanah P. (Depkes RI, 1979).
perbedaannya terletak pada baunya, stabilitas penyimpanannya, dan kapasitas emulsifikasi. Penggunaan topikal minyak relatif tidak menimbulkan efek samping. (Oen, 1986).
Minyak lemak adalah salah satu kelompok yang termasuk pada golongan lipid , yaitu senyawa organik yang terdapat di alam serta tidak larut dalam air, tetapi larut dalam pelarut organik non-polar,misalnya dietil eter (C2H5OC2H5), Kloroform(CHCl3), benzena dan hidrokarbon lainnya, lemak dan minyak dapat larut dalam pelarut yang disebutkan di atas karena lemak dan minyak mempunyai polaritas yang sama dengan pelarut tersebut.
Lemak dan minyak merupakan senyawaan trigliserida atau
triasgliserol, yang berarti “triester dari gliserol” . Jadi lemak dan minyak juga
merupakan senyawaan ester . Hasil hidrolisis lemak dan minyak adalah asam karboksilat dan gliserol . Asam karboksilat ini juga disebut asam lemak yang mempunyai rantai hidrokarbon yang panjang dan tidak bercabang. (Netti dkk, 2002).
2.3
Ekstraksi10
senyawa-senyawa tersebut terhadap pemanasan, udara, cahaya, logam berat, dan derajat keasaman. Dengan diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dan cara ekstraksi yang tepat. (DepKes RI, 2000)
Ragam ekstraksi yang tepat sudah tentu bergantung pada tekstur dan kandungan air bahan tumbuhan yang diekstraksi dan pada jenis senyawa yang diisolasi. (Harborne, 1987).
2.3.1 Proses pembuatan ekstrak (DepKes RI, 2000) a. Pembuatan serbuk simplisia dan klasifikasinya
Proses awal pembuatan ekstrak adalah tahapan pembuatan serbuk simplisia kering (penyerbukan). Dari simplisia dibuat serbuk simplisia dengan peralatan tertentu sampai derajat kehalusan tertentu. Proses ini dapat mempengaruhi mutu ekstrak. Makin halus serbuk simplisia, proses ekstraksi makin efektif-efisien, namun makin halus serbuk, maka makin rumit secara teknologi peralatan untuk tahapan filtrasi.
b. Cairan pelarut
12
c. Separasi dan pemurnian
Tujuan dari tahapan ini adalah menghilangkan (memisahkan) senyawa yang tidak dikehendaki semaksimal mungkin tanpa berpengaruh pada senyawa kandungan yang dikehendaki, sehingga diperoleh ekstrak yang lebih murni.
d. Pemekatan atau Penguapan
Pemekatan berarti peningkatan jumlah partial solute (senyawa terlarut) secara penguapan pelarut tanpa sampai menjadi kondisi kering, ekstrak hanya menjadi kental atau pekat.
e. Rendemen
Rendemen adalah perbandingan antara ekstrak yang diperoleh dengan simplisia awal.
2.3.2 Metode ekstraksi (DepKes RI, 2000) a. Ekstraksi dengan menggunakan pelarut
1. Cara dingin Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar). Secara teknologi termasuk ekstraksi dengan prinsip metode pencapaian konsentrasi pada keseimbangan.
Perkolasi
ruangan. Proses terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali bahan. 2. Cara panas
Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna.
Sokhlet
Sokhlet adalah ekstraksi menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur yang lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-50oC.
Infus
14
mendidih, temperatur terukur 96-98oC) selama waktu tertentu (15-20 menit).
Dekok
Dekok adalah infus pada waktu yang lebih lama (≥30 menit) dan temperatur sampai titik didih air.
b. Destilasi uap
2.4
KulitGambar 1. Penampang Kulit (Graaff dkk, 2001)
Pembagian kulit secara garis besar tersusun atas tiga lapisan utama yaitu : lapisan epidermis atau kutikel, lapisan dermis (korium, kutis vera, true skin), dan lapisan subkutis (hypodermis). Tidak ada garis tegas yang memisahkan dermis dan subkutis, subkutis ditandai dengan adanya jaringan ikat longgar dan adanya sel dan jaringan lemak. Tiga lapisan kulit utama, antara lain :
1. Lapisan epidermis yang terdiri atas:
a. Stratum korneum (lapisan tanduk) adalah lapisan kulit yang paling luar dan terdiri atas beberapa lapisan sel-sel gepeng yang mati, tidak berinti, dan protoplasmanya telah berubah menjadi keratin (zat tanduk).
16
c. Stratum granulosum (lapisan keratohialin/lapisan seperti butir) merupakan 2 atau 3 lapis sel gepeng dengan sitoplasma berbutir kasar dan terdapat inti diantaranya.
d. Stratum spinosum (stratum malphigi/lapisan sel duri) atau disebut pula prikle cell layer (lapisan akanta) terdiri atas beberapa lapis sel yang berbentuk poligonal yang besarnya berbeda-beda karena adanya proses mitosis.
e. Stratum germinativum (lapisan sel basal) terdiri atas sel-sel berbentuk kubus (kolumnar) yang tersusun vertikal pada perbatasan dermo-epidermal berbaris seperti pagar (palisade).
2. Lapisan dermis adalah lapisan di bawah epidermis yang jauh lebih tebal daripada epidermis. Lapisan ini terbentuk oleh lapisan elastik dan fibrosa padat dengan elemen selular, kelenjar, dan folikel rambut. Secara garis besar dibagi menjadi dua bagian :
a. Pars papilare, yaitu bagian yang menonjol ke epidermis, berisi ujung serabut saraf, dan pembuluh darah.
b. Pars retikulare, yaitu bagian bawah dermis yang berhubungan dengan subkutis, bagian ini terdiri dari serabut-serabut penunjang misalnya serabut kolagen, elastin, dan retikulin.
Derajat keasaman (pH) kulit manusia berkisar antara 4,2-6,5. Keadaan asam ini sebagian besar disebabkan oleh adanya zat bersifat asam seperti asam amino dan asam lemak bebas misalnya asam laktat, yang merupakan sekresi dari kelenjar sebaseus. Lapisan bersifat asam ini dikenal dengan istilah mantel asam kulit yang dapat melindungi tubuh dari serangan bakteri dan zat kimia yang dapat merusak jaringan (Anief, 1997; Wasitaatmadja, 1997).
Fungsi kulit antara lain : sebagai pelindung, absorpsi cairan mudah menguap, eksresi, pengindra (sensori), pengaturan suhu tubuh, pembentukan pigmen, sawar radiasi UV, dan sawar listrik (Anief, 1997; Wasitaatmadja, 1997).
Berbagai faktor dapat mempengaruhi absorpsi kulit terhadap kosmetika, yaitu faktor yang berasal dari lingkungan hidup (sinar UV, suhu, dan kelembaban udara), faktor dari lingkungan tubuh (tempat aplikasi kosmetik, luas aplikasi kosmetik, umur pemakai, kondisi kulit yang diaplikasikan kosmetik), dan faktor kosmetika yang dipakai (intensitas pemakaian, keasaman kosmetika, konsentrasi bahan aktif, jenis bahan dasar yang menjadi bahan pelarut pada kosmetika) (Wasitaatmadja, 1997).
18
dan mempunyai sifat yang bermacam-macam seperti hidrofil atau hidrofob. (Anief, 1993).
2.5
GelGel atau jelly adalahsistem semipadat terdiri dari suspensi yang dibuat dari partikel anorganik yang kecil atau molekul organik yang besar, terpenetrasi oleh suatu cairan. Jika massa gel terdiri dari jaringan partikel kecil yang terpisah, gel digolongkan sebagai sistem dua fase (misalnya gel aluminium hidroksida). Dalam sistem dua fase, jika ukuran partikel dari fase
terdispersi relatif besar, misalnya gel kadang-kadang dinyatakan sebagai magma (misalnya magma bentonit). Baik gel maupun magma dapat berupa tiksotropik, membentuk semipadat jika dibiarkan dan menjadi cair pada pengocokan. Sediaan harus dikocok dahulu sebelum digunakan untuk menjamin homogenitas dan hal ini tertera pada etiket (lihat suspensi). (DepKes RI 1995).
2.6
Stabilitas SediaanStabilitas sebuah gel adalah sifat gel untuk mempertahankan distribusi halus dan teratur dari fase terdispersi yang terjadi dalam jangka waktu yang panjang. Gel mempunyai kakakuan yang disebabkan oleh jaringan yang saling menganyam dari fase terdispersi yang mengurung dan memegang medium pendispersi. Perubahan dalam temperatur dapat menyebabkan gel tertentu mendapatkan kembali bentuk sol dan bentuk cairnya. Juga beberapa gel menjadi encer setelah pengocokan dan kembali menjadi setengah padat atau padat kembali setelah dibiarkan tidak terganggu untuk beberapa waktu tertentu, peristiwa ini disebut tiksotropi.(Ansel C Howard, 1989).
2.7
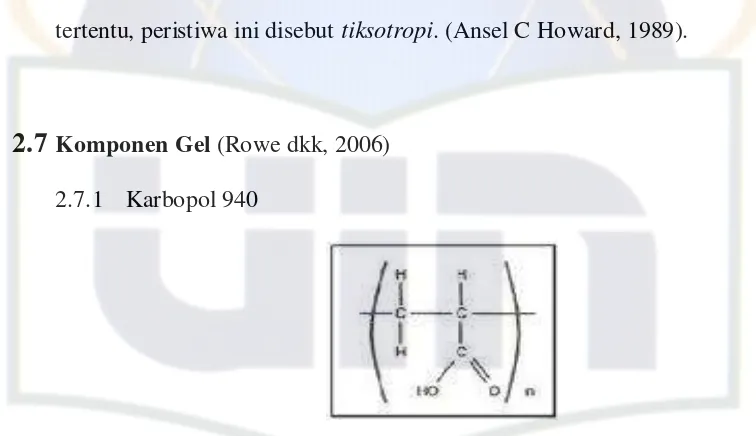
Komponen Gel (Rowe dkk, 2006) 2.7.1 Karbopol 940
Gambar 2. Struktur Karbopol 940
Karbopol merupakan kelompok acrylic polymer cross-linked dengan poly alkenyl ether. Nama lain karbopol adalah acitamer, acrylic acid polymer, carbomer, carboxyvinyl polymer. Karbopol
20
formulasi krim, gel, dan salep dan kemungkinan digunakan sebagai sediaan opthalmic, rectal, dan sediaan topikal lain.
2.7.2 HPMC (Hidroksi Propil Metil Selulosa)
Gambar 3. Struktur HPMC
Nama lain HPMC antara lain: hypromellose, methocel, hydroxy propyl methyl cellulose, metolose, dan pharmacoat. Rumus kimia
HPMC adalah CH3CH(OH)CH2. HPMC secara luas digunakan sebagai suatu eksipien di dalam formulasi pada sedian topikal dan oral. Dibandingkan dengan metilsellulosa, HPMC menghasilkan cairan lebih jernih. HPMC juga digunakan sebagai zat pengemulsi, agen pensuspensi dan agen penstabil di dalam sediaan salep dan gel. Pemeriannya adalah serbuk hablur putih, tidak berasa, tidak berbau, larut dalam air dingin, dan membentuk koloid yang merekat. Tidak larut dalam kloroform, etanol 95%, dan eter tetapi dapat larut dalam diklorometana. Fungsinya adalah suspending agent.
2.7.3 Na CMC (natrium karboksilmetilselulosa)
22 BAB III
KERANGKA KONSEP
Serbuk simplisia kering biji jinten hitam (Nigella sativa L.)
Evaluasi sediaan gel minyak jinten hitam (Nigella sativa L.) Pembuatan gel dengan menggunakan minyak jinten hitam (Nigella sativa L.)
Diperoleh minyak jinten hitam (Nigella sativa L.)
Ekstraksi
(maserasi dengan pelarut n-heksana)
Pemeriksaan minyak jinten hitam : 3. Pemeriksaan organoleptis 5. Uji Stabilitas Cycling test 6. Uji difusi
Jinten hitam (Nigella sativa L.) diketahui berkhasiat untuk
menyembuhkan berbagai penyakit dan masalah pada kulit.
Analisis data
23 BAB IV
METODOLOGI PENELITIAN
4.1 Tempat dan Waktu Penelitian 4.1.1 Tempat penelitian
Laboratorium Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta dan Pusat Laboratorium Terpadu UIN Syarif Hidayatullah Jakarta.
4.1.2 Waktu penelitian
Proses penelitian berlangsung selama 5 bulan, dari tanggal 7 maret 2010 hingga 7 agustus 2010.
4.2 Bahan dan Alat 4.2.1 Bahan
24
4.2.1 Alat
Alat-alat yang akan digunakan antara lain: peralatan gelas, lumpang, hot plate (Wiggen Hauser), piknometer, pH meter (Mettler-Toledo), refraktometer (Atago), viskometer Brookfield, timbangan analitik (Wiggen Hauser), kaca objek, mikroskop optik (Yamiza X52-107BN, erma objective micrometer), lemari pendingin, oven, alat-alat uji difusi (mini pump variable flow, membran difusi, termometer), spektrofotometer UV-Vis (Perkin Elmer).
4.3 Cara Kerja
4.3.1 Penapisan Fitokimia (Skrining) a. Identifikasi golongan alkaloid
Dragendroff atau endapan putih dengan pereaksi Mayer menunjukkan adanya senyawa alkaloid.
b. Identifikasi golongan flavonoid
Sebanyak 10 gram serbuk ditambahkan 100 ml air panas, lalu didihkan selama 5 menit kemudian disaring. Ambil 5 ml filtratnya (dalam tabung reaksi), ditambahkan serbuk Mg secukupnya dan 1 ml asam klorida pekat dan 2 ml amil alkohol, kocok kuat dan dibiarkan memisah. Terbentuknya warna merah, kuning, atau jingga pada lapisan amil alkohol menunjukkan adanya flavonoid. c. Identifikasi golongan saponin
Serbuk dimasukkan ke dalam tabung reaksi, ditambahkan 10 ml air panas. Setelah dingin dikocok kuat secara vertikal selama 10 detik. Terbentuknya busa yang stabil, menunjukkan adanya saponin, bila ditambahkan 1 tetes HCl 1% busa tetap stabil.
d. Identifikasi golongan steroid dan triterpenoid
Sebanyak 5 gram serbuk dimaserasi dalam 20 ml eter selama 2 jam kemudian disaring. Larutan diuapkan dalam cawan penguap sampai kering kemudian ditambahkan 2 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat ke dalam residu. Terbentuknya warna hijau atau merah menunjukkan adanya steroid/triterpenoid.
e. Identifikasi golongan tanin
26
terbentuknya warna biru, hijau, atau hitam menunjukkan adanya seyawa golongan tanin.
f. Identifikasi golongan kuinon
Sebanyak 1 gram serbuk dipanaskan dalam air selama 5 menit, disaring. Sebanyak 5 ml filtrat yang diperoleh ditambahkan 5 ml NaOH 1 N. Terbentuknya warna merah menunjukkan adanya kuinon.
g. Identifikasi golongan minyak atsiri
Sebanyak 2 gram serbuk dimasukkan ke dalam tabung reaksi (volume 20 ml) kemudian ditambahkan 10 ml pelarut petroleum eter. Pada mulut tabung dipasang corong yang diberi lapisan kapas yang telah dibasahi dengan air, kemudian disaring dengan kertas saring. Filtrat yang diperoleh diuapkan pada cawan penguap, selanjutnya residu dilarutkan dengan pelarut etanol 95% sebanyak 5 ml, kemudian disaring dengan kertas saring. Filtratnya diuapkan dengan cawan penguap. Residu yang berbau aromatik menunjukkan adanya senyawa golongan minyak atsiri.
h. Identifikasi golongan kumarin
dimasukkan ke dalam tabung reaksi, kemudian ditambahkan 0,5 ml amoniak 1% dan diamati dibawah sinar UV 366 nm. Flouresensi biru atau hijau menunjukkan adanya kumarin.
4.3.2 Ekstraksi Minyak Jinten Hitam
Biji jinten hitam dibersihkan dari benda-benda asing dan zat pengotor lainnya. Sebanyak 700 gram biji jinten hitam dihaluskan hingga menjadi serbuk kemudian ditimbang. Setelah itu dimaserasi dengan pelarut n-heksana selama satu minggu sampai pelarutnya agak jernih pada suhu kamar. Minyak yang diperoleh dikumpulkan dan dipekatkan dalam rotary evaporator.
4.3.3 Penapisan Fitokimia Minyak Jinten Hitam
Meliputi identifikasi alkaloid, flavonoid, tanin, saponin, steroid, triterpenoid, kuinon, minyak atsiri, dan kumarin.
4.3.4 Pemeriksaan Minyak Jinten Hitam
a. Pemeriksaan organoleptik : bentuk, warna, bau b. Pemeriksaan keasaman/pH
pH minyak jinten hitam diukur dengan pH meter yang telah dikalibrasi dengan dapar standar pH 4 dan pH 7.
c. Pemeriksaan indeks bias
Indeks bias diperiksa dengan menggunakan alat refraktometer. d. Pengukuran viskositas (Martin, 1993)
28
e. Pemeriksaan kelarutan
Minyak jinten hitam dilarutkan dalam etanol (95%) P. f. Pemeriksaan bobot jenis (DepKes RI, 1995)
Piknometer ditimbang dalam keadaan bersih dan kering sebagai berat kosong. Piknometer tersebut diisi dengan air sampai penuh dan temperatur diatur hingga 25oC, lalu ditimbang. Cara yang sama dilakukan terhadap minyak jinten hitam.
Perhitungan : Berat piknometer berisi air dan minyak jinten hitam masing-masing dikurangkan dengan berat piknometer kosong. Bobot jenis minyak jinten hitam adalah hasil bagi berat minyak jinten hitam dengan berat air, dalam piknometer kemudian dikalikan dengan berat jenis air.
g. Pengukuran panjang gelombang maksimum
Panjang gelombang ditentukan pada konsentrasi 1 ppm minyak jinten hitam (Nigella sativa L.) dalam larutan etanol 95%. Pengukuran dilakukan pada panjang gelombang UV yaitu 200 – 400 nm. Kemudian dibuat kurva hubungan antara panjang gelombang terhadap serapanya.
h. Penentuan kurva kalibrasi minyak biji jinten hitam
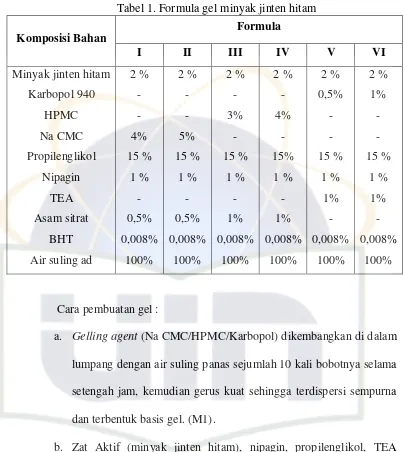
4.3.5 Pembuatan Formula gel
Tabel 1. Formula gel minyak jinten hitam Komposisi Bahan
a. Gelling agent (Na CMC/HPMC/Karbopol) dikembangkan di dalam
lumpang dengan air suling panas sejumlah 10 kali bobotnya selama setengah jam, kemudian gerus kuat sehingga terdispersi sempurna dan terbentuk basis gel. (M1).
30
dalam lumpang sampai terbentuk massa gel. Penggerusan dilakukan pada suhu kamar.
4.3.6 Evaluasi Gel
a. Pemeriksaan Organoleptik
Pemeriksaan meliputi penampilan sediaan, warna, bau, dan tekstur. b. Pemeriksaan pH
Gel dimasukkan ke dalam wadah, lalu diukur pHnya dengan pHmeter yang telah dikalibrasi dengan dapar standar pH 4 dan pH 7.
c. Pemeriksaan Homogenitas
Gel dioleskan diatas kaca objek, kemudian dikatupkan dengan kaca objek lain, lalu diamati kehomogenan gel tersebut.
d. Pemeriksaan viskositas
Sediaan gel disiapkan dalam becker glass 100 ml. Kemudian dipilih nomor spindel 7. Pemeriksaan ini menggunakan viskometer Brookfield.
e. Uji stabilitas fisik dengan metode cycling test
f. Uji difusi (Martin, 1993) Pembuatan membran difusi
Membran yang digunakan adalah kertas Whatman no 1 yang diimpregnasi pada cairan spangler. Komposisi cairan spangler :
Asam palmitat 10 g Asam oleat 15 g Asam stearat 5 g Minyak kelapa 15 g Parafin 10 g Kolesterol 5 g Lilin putih 15 g
Cara pembuatan : Semua bahan dilebur dalam cawan petri. Setelah itu kertas Whatman dicelupkan atau direndam dalam cairan spangler selama 15 menit. Kemudian diangkat dan dikeringkan dengan kertas tissue.
Bobot membran sebelum dan sesudah impregnasi ditimbang untuk mendapatkan kondisi yang sama pada setiap membran. Persentasi impregnasi membran dapat dihitung berdasarkan rumus:
Presentase impregnasi = X 100 %
32
Uji difusi
Alat difusi terdiri dari sel difusi (mini pump variable flow, membran difusi, termometer), pompa peristaltik, alat penghilang gelembung udara, dan gelas kimia sebagai wadah cairan penerima. Sebanyak enam formula uji ditimbang 1 gram kemudian diratakan di atas membran dengan diameter 1,5 cm. Suhu sistem 37±0,5oC dengan cairan sirkulasi hydroalcoholic (etanol:air 40:60) sebanyak 300 ml. Pompa peristaltik menghisap cairan reseptor dari gelas kimia kemudian dipompa ke sel difusi melewati penghilang gelembung sehingga aliran terjadi secara hidrodinamis. Kemudian cairan dialirkan kembali ke reseptor. Proses dilakukan selama 3 jam. (Alessandro et al, 2007).
Cuplikan diambil dari cairan reseptor dalam gelas kimia sebanyak 5 ml. Setiap pengambilan selalu diganti dengan cairan hydroalcoholic sebanyak 5 ml. Pengambilan cuplikan dilakukan
33 BAB V
HASIL PENELITIAN DAN PEMBAHASAN
5.1 Hasil Penelitian
5.1.1 Determinasi tanaman
Determinasi tanaman dilakukan di Herbarium Bogoriense, Pusat Penelitian Biologi LIPI, Bogor, Jawa Barat. Hasil determinasi menunjukkan bahwa tanaman ini adalah tanaman jinten hitam (Nigella sativa L.) famili Ranunculaceae.
5.1.2 Penapisan fitokimia serbuk biji jinten hitam
Berdasarkan hasil pemeriksaan penapisan fitokimia serbuk biji jinten hitam (Nigella sativa L.) terdapat beberapa golongan senyawa. Hasilnya dapat dilihat pada tabel dibawah ini.
Tabel 2. Hasil penapisan fitokimia biji jinten hitam Golongan senyawa Hasil penapisan
Alkaloid
5.1.3 Ekstraksi biji jinten hitam
34
5.1.1 Penapisan fitokimia minyak jinten hitam
Berdasarkan hasil pemeriksaan penapisan fitokimia minyak jinten hitam (Nigella sativa L.) terdapat beberapa golongan senyawa. Hasilnya dapat dilihat pada tabel dibawah ini.
Tabel 3. Hasil penapisan fitokimia minyak jinten hitam Golongan senyawa Hasil penapisan
Alkaloid
5.1.2 Pemeriksaan minyak jinten hitam
Data hasil pemeriksaan minyak jinten hitam terdapat pada tabel dibawah ini.
Tabel 4. Hasil pemeriksaan minyak jinten hitam Pemeriksaan Hasil Pemeriksaan
5.1.3 Evaluasi gel anti jerawat minyak jinten hitam (sesudah dan sebelum cycling test)
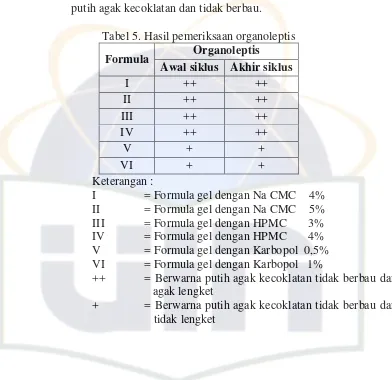
a. Pemeriksaan organoleptis (pada awal siklus dan akhir siklus) Hasil pengamatan organoleptis menunjukan gel berwarna putih agak kecoklatan dan tidak berbau.
Tabel 5. Hasil pemeriksaan organoleptis Formula Organoleptis
Awal siklus Akhir siklus
I ++ ++
II ++ ++
III ++ ++
IV ++ ++
V + +
VI + +
Keterangan :
I = Formula gel dengan Na CMC 4% II = Formula gel dengan Na CMC 5% III = Formula gel dengan HPMC 3% IV = Formula gel dengan HPMC 4% V = Formula gel dengan Karbopol 0,5% VI = Formula gel dengan Karbopol 1%
++ = Berwarna putih agak kecoklatan tidak berbau dan
a agak lengket
+ = Berwarna putih agak kecoklatan tidak berbau dan
36
b. Pemeriksaan homogenitas (pada awal siklus dan akhir siklus) Hasil menunjukan bahwa semua gel terlihat homogen.
Tabel 6. Hasil pemeriksaan homogenitas
Formula Homogenitas
Awal siklus Akhir siklus
I H H
c. Pemeriksaan pH (pada awal siklus dan akhir siklus)
Hasil pengukuran menunjukan bahwa pH sediaan memenuhi kriteria pH kulit, yaitu berada pada interval 4,5 - 6,5.
Tabel 7. Hasil pemeriksaan pH
Formula pH
Awal siklus Akhir siklus
d. Pemeriksaan viskositas (pada awal siklus dan akhir siklus) Tabel 8. Hasil pemeriksaan viskositas
Formula Viskositas (cP) Awal siklus Akhir siklus
I 50600 56000 e. Uji stabilitas fisik sediaan dengan metode cycling test
Ke-6 formula gel menunjukan hasil yang stabil pada pengamatan cycling test.
Tabel 9. Hasil pemeriksaan stabilitias fisik Formula Uji Stabilitas
Awal siklus Akhir siklus
38
f. Uji difusi
Tabel 10. Hasil pemeriksaan difusi Formula
Kadar (ppm) minyak jinten hitam Menit Ke
5.2.1 Ekstraksi Minyak Jinten Hitam (Nigella sativa L.)
Penelitian formulasi gel ini menggunakan minyak jinten hitam (Nigella sativa L.) yang diperoleh dengan cara maserasi menggunakan pelarut n-heksana, karena n-heksana merupakan pelarut non polar sehingga dapat menarik lipid atau minyak yang bersifat non polar dari biji jinten hitam.
masih berada dalam kisaran pH kulit yaitu pada interval 4,5-6,5. Hasil pemeriksaan indeks bias minyak jinten hitam yaitu 1,4719. Nilai tersebut cukup memenuhi syarat standar mutu minyak jinten hitam. Menurut beberapa literatur, syarat standar indeks bias minyak jinten hitam berkisar antara 1,470-1,475 (Goerlich Pharma Internasional, 2007). Pemeriksaan bobot jenis minyak jinten hitam diperoleh hasil 0,8964, umumnya bobot jenis minyak memang tidak melebihi 1,000. Penentuan bobot jenis adalah salah satu dari cara analisa yang dapat menggambarkan kemurnian minyak (Depkes RI, 1985).
5.2.2 Pembuatan Sediaan
40
5.2.3 Evaluasi Sediaan
Dari hasil evaluasi semua formula gel terlihat homogen serta tidak menunjukan perubahan warna dan bau. Untuk formula dengan basis Na CMC dan HPMC menunjukan gel memiliki tekstur yang agak lengket sedangkan pada formula dengan basis karbopol menunjukan gel memiliki tekstur yang tidak lengket. Dari hasil pengukuran pH terlihat sediaan memenuhi kriteria kulit yaitu berada dalam interval 4,5 – 6,5. Jika pH sediaan berada diluar interval pH kulit dikhawatirkan akan menyebabkan kulit bersisik. Perubahan pH dapat disebabkan oleh kondisi lingkungan penyimpanan seperti cahaya dan kelembaban udara.
Uji cycling test pada gel untuk menguji apakah terjadi sineresis pada gel. Sineresis adalah gejala pada saat gel mengerut secara alamiah dan sebagian dari cairanya terperas keluar. Hal ini terjadi karena struktur matriks serat gel yang terus mengeras dan akhirnya mengakibatkan terperasnya air ke luar. Hasil cycling test pada keenam sediaan menunjukan bahwa keenam sediaan menunjukan tidak terjadi sineresis.
Uji difusi bertujuan untuk mengetahui laju pelepasan suatu bahan aktif dari pembawanya dan juga untuk melihat seberapa besar kadar bahan aktif yang dapat berpenetrasi melalui membran, secara in-vitro.
Uji difusi pada gel ini dilakukan selama 3 jam, dengan pengambilan cuplikan sebanyak 5 ml setiap beberapa menit sekali, setelah itu diukur dalam spektrofotometer UV-Vis. Pengukuran dilakukan pada panjang gelombang 253 nm, diperoleh berdasarkan hasil scanning panjang gelombang maksimum minyak jinten hitam.
42
43 BAB VI
KESIMPULAN DAN SARAN
6.1 Kesimpulan
Dari hasil penelitian dapat disimpulkan bahwa minyak biji jinten hitam (Nigella sativa L.) dapat dibuat sediaan gel yang baik dan stabil dengan menggunakan basis Karbopol 940 pada konsentrasi 1% karena dari hasil evaluasi stabilitas fisik dan profil uji difusi menunjukan stabilitas fisik yang baik serta laju pelepasan bahan aktif yang paling tinggi.
6.2 Saran
Perlu dilakukan pengujian lebih lanjut untuk mengetahui efektifitas gel antioksidan minyak biji jinten hitam (Nigella sativa L.).
44
44
DAFTAR PUSTAKA
Alessandro DL, Francesco L, Chiara S, Marco Z, Rainer HM, Anna MF. 2007. SLN as Topical Delivery System for Artesimia arborescens Essential Oil : In vitro Antoviral Activity and Skin Permeation Study. International Journal of Nanomedicine, Volume 2, No 3, Italy. Hal 419-425
Anief, Moh. 1993. Farmasetika. Gadjah Mada University Press : Yogyakarta. Anief, Moh. 1997. Formulasi Obat Topikal dengan Dasar Penyakit Kulit.
Gadjah Mada University Press : Yogyakarta.
Ansel, Howard C. 1989. Pengantar Bentuk Sediaan Farmasi Edisi Keempat. Penerjemah Farida Ibrahim. UI Press : Jakarta.
Arici M, Sagdic O, Gecgel U. 2005. Antibacterial Effect of Turkish Black Cumin (Nigella sativa L.) Oils. Grasas y Aceites, Volume 56, Turkey. Hal 259-262.
Armenia, Suardi Muslim, Maryawati Anita. 2007. Formulasi Uji Klinik Gel Anti Jerawat Benziol Peroksida-HPMC. Journal Of Fakultas Farmasi F-MIPA UNAND.
Departemen Kesehatan RI. 1979. Farmakope Indonesia Edisi III. Direktorat Jendral Pengawasan Obat dan Makanan : Jakarta.
Departemen Kesehatan RI. 1979. Materia Medika Indonesia Jilid III. Direktorat Jendral Pengawasan Obat dan Makanan : Jakarta.
Departemen Kesehatan RI. 1979. Materia Medika Indonesia Jilid IV. Direktorat Jendral Pengawasan Obat dan Makanan : Jakarta.
Departemen Kesehatan RI. 1985. Cara Pembuatan Simplisia. Direktorat Jendral Pengawasan Obat dan Makanan : Jakarta. Hal 122-123. Departemen Kesehatan RI. 1985. Formularium Kosmetika Indonesia.
Direktorat Jendral Pengawasan Obat dan Makanan : Jakarta.
Departemen Kesehatan RI. 1989. Vademekum Bahan Obat Alam. Direktorat Jendral Pengawasan Obat dan Makanan : Jakarta.
Departemen Kesehatan RI. 1995. Farmakope Indonesia Edisi IV. Direktorat Jendral Pengawasan Obat dan Makanan : Jakarta. Hal 7-8, 1030. Departemen Kesehatan RI. 2000. Parameter Standar Umum Ekstrak
Tumbuhan Obat. Direktorat Pengawasan Obat Tradisional : Jakarta. Hal 1, 9-12.
Galuh Yulianhar Rosyad, Putri. 2009. FORMULASI GEL OBAT JERAWAT MINYAK ATSIRI DAUN JERUK NIPIS (Citrus aurantifolia, swingle) DAN UJI ANTIBAKTERI (Propionibacterium acne) SECARA IN VITRO. Skripsi : Fakultas Farmasi Universitas Muhammadiyah Surakarta, Surakarta.
Goerlich Pharma International. 2007. Spesification Egyptian Black Cumin Oil. Germany.
Harborne, J.B. 1987. Metode Fitokimia Penuntun Cara Modern Menganalisis Tumbuhan. Penerbit ITB : Bandung. Hal 6-7.
Hartati Sri. Yuliani. 2005. Formulasi Gel Repelan Minyak Atsiri Tanaman Akar Wangi (Vativera zizanioidesi. L. Nogh): Optimasi Komposisi Karbopol 3% b/v Propilenglikol. Jurnal Fakultas Farmasi Universitas Sanata Dharma.
Hasan Mahmud Muhammad, Mahir. 2007. Mukjizat Kedokteran Nabi Berobat dengan Rempah dan Buah-Buahan. Qultum Media : Jakarta. Hal 8, 104.
Hasnah Sirat, Basar Norazah, Fang Err. 2000. Analisis Biji Jinten Hitam (Nigella sativa, L). Malaysian Journal Of Analitycal Science, Vol. 7, No. 1.
46
Padhye, Subhash dkk. 2008. From Here to Eternity - The Secret of Pharaohs : Therapeutic Potential of Black Cumin Seeds and Beyond. Department of Pathology and Division of Internal Medicine, Barbara Ann Karmanos Cancer Institute, Wayne State University, School of Medicine, Detroit, MI- 48201, USA. Cancer Ther. 6(b): 495–510. Padmadisastra Yudi, Sidik, Azizah Sumi. 2003. Formulasi sediaan Cair Gel
Lidah Buaya (Aloe Vera. L) Sebagai Minuman Kesehatan. Simposium Nasional Kimia Bahan Alam III Fakultas Farmasi Universitas Padjadjaran.
Sakkara Essential Oil. Material Safety Data Sheet and Specification Egyptian Black Cumin Seed Oil. Egypt.
Salman MT, Khan RA, Shukla I. 2002. Antimicrobial Activity of Black Cumin Seeds (Nigella sativa) Against Multidrug Resistant Strains of Coagulase Negative Staphylococci. Departments of Pharmacology and Microbiology, Jawaharlal Nehru Medical College, Aligarh Muslim University, Aligarh India.
Toama MA, El-Alfy TS, El-Fatatry HM. 1974. Antimicrobial Activity of the Volatile Oil of Nigella sativa Linneaus Seeds. Antimicrobial Agents and Chemotherapy, Volume 6, No 2. Hal 225-226.
Underwood, JCE. 2004. General and Systematic Pathology Fourth Edition. Churcill Livingstone. Hal 697.
Voigt, Rudolf. 1995. Buku Pelajaran Teknologi Farmasi. Penerjemah Dr.rer.nat. Soendani Noerono Soewandhi, Apt. Dan Dr. Mathilda B. Widianto, Apt., Jurusan Farmasi FMIPA ITB, Penyunting Prof. Dr. Moch. Samhoedi Reksohadiprodjo, Apt., Fakultas Farmasi UGM. Gajah Mada University Press : Yogyakarta. Hal 351-353, 564.
Wade A, Waller PJ. 1994. Handbook of Pharmaceutical Excipients Second Edition. The Pharmaceutical Press : London. Hal 47, 204, 310, 494, 538.
Wade A, dkk. 1982. Martindale The Extra Pharmacopoeia Twenty-eight Edition. The Pharmaceutical Press : London. Hal 950, 955, 708, 1287, 1291-1292, 1290-1292.
Wasitaatmadja, Sjarif M. 1997. Penuntun Ilmu Kosmetik Medik. UI Press : Jakarta. Hal 3-6, 11-14, 23-24, 90, 186.
47
48
LAMPIRAN
Lampiran 1. Tanaman dan Biji Jinten Hitam (Nigella sativa L.).
Gambar 5. Tanaman Jinten Hitam (Nigella sativa L.)
Lampiran 2. Perhitungan Bobot Jenis Minyak Jinten Hitam (Nigella sativa L.).
Bobot jenis = �2−�0
�1−�0 X berat jenis air
m0 (berat piknometer kosong) = 13,2199
m1 (berat piknometer + air) = 23,4051
m2 (berat piknometer + minyak jinten hitam) = 22,35
Bobot jenis = �2−�0
�1−�0
= 22,35−13,2199
22,4051−13,2199 X 1
= 0,8964
50
Lampiran 3. Hasil Scanning λ Maksimum Minyak Jinten Hitam.
13 Juli 2010
Spectrum Name: C:\UVWINLAB\DATA\JINTEN.SP
Description: Panjang gelombang maksimum minyak jinten 1 ppm
Date Created: Wed Jan 01 05:24:33 2003
Data Interval: 1.0000 nm
200.0 220 240 260 280 300 320 340 360 380 400.0
Lampiran 4. Kurva serapan minyak jinten hitam.
Wavelength Program
__________________
Date: 7/8/2010 Time: 10:17:27 AM Method: Minyak jinten hitam Slit: UV/VIS: 1.00 nm
Analyst: Ardian S. Nurhakim
Sample ID Cyc Factor 253.00 nm
52
Lampiran 5. Evaluasi pemeriksaan stabilitas fisik (cycling test).
1. I
Awal Siklus Akhir siklus
2. II
Awal siklus Akhir siklus
3. III
Awal siklus Akhir siklus
4. IV
Awal siklus Akhir siklus
Lampiran 5. Evaluasi pemeriksaan stabilitas fisik (cycling test). ...(Lanjutan).
5. V
Awal siklus Akhir siklus
6. VI
Awal siklus Akhir siklus
Gambar 8. Evaluasi pemeriksaan stabilitas fisik (cycling test) ....(lanjutan) Keterangan :
54
Lampiran 6. Absorbansi pemeriksaan difusi.
Wavelength Program
__________________
Date: 9/22/2010 Time: 8:39:44 AM Method: Formula I Slit: UV/VIS: 1.00 nm
Analyst: Ardian S. Nurhakim
Sample ID Cyc Factor 253.00 nm
__________________________________________________________________ __________________________
1 1 1.0000 0.0983 Serapan zat aktif menit ke 5 2 1 1.0000 0.1937 Serapan zat aktif menit ke 15 3 1 1.0000 0.2941 Serapan zat aktif menit ke 25 4 1 1.0000 0.3915 Serapan zat aktif menit ke 35 5 1 1.0000 0.4977 Serapan zat aktif menit ke 45 6 1 1.0000 0.5777 Serapan zat aktif menit ke 60 7 1 1.0000 0.6391 Serapan zat aktif menit ke 80 8 1 1.0000 0.5840 Serapan zat aktif menit ke 100 9 1 1.0000 0.3571 Serapan zat aktif menit ke 160 10 1 1.0000 0.1995 Serapan zat aktif menit ke 180
Lampiran 6. Absorbansi pemeriksaan difusi. ...(lanjutan)
Wavelength Program
__________________
Date: 9/22/2010 Time: 8:49:13 AM Method: Formla II Slit: UV/VIS: 1.00 nm
Analyst: Ardian S. Nurhakim
Sample ID Cyc Factor 253.00 nm
__________________________________________________________________ __________________________
1 1 1.0000 0.0918 Serapan zat aktif menit ke 5 2 1 1.0000 0.1915 Serapan zat aktif menit ke 15 3 1 1.0000 0.2707 Serapan zat aktif menit ke 25 4 1 1.0000 0.3540 Serapan zat aktif menit ke 35 5 1 1.0000 0.4343 Serapan zat aktif menit ke 45 6 1 1.0000 0.5339 Serapan zat aktif menit ke 60 7 1 1.0000 0.6001 Serapan zat aktif menit ke 80 8 1 1.0000 0.5091 Serapan zat aktif menit ke 100 9 1 1.0000 0.4519 Serapan zat aktif menit ke 160 10 1 1.0000 0.2658 Serapan zat aktif menit ke 180
56
Lampiran 6. Absorbansi pemeriksaan difusi. ...(lanjutan)
Wavelength Program
__________________
Date: 9/22/2010 Time: 9:01:21 AM Method: Formula III Slit: UV/VIS: 1.00 nm
Analyst: Ardian S. Nurhakim
Sample ID Cyc Factor 253.00 nm
__________________________________________________________________ __________________________
1 1 1.0000 0.0868 Serapan zat aktif menit ke 5 2 1 1.0000 0.1977 Serapan zat aktif menit ke 15 3 1 1.0000 0.2564 Serapan zat aktif menit ke 25 4 1 1.0000 0.3529 Serapan zat aktif menit ke 35 5 1 1.0000 0.4471 Serapan zat aktif menit ke 45 6 1 1.0000 0.5132 Serapan zat aktif menit ke 60 7 1 1.0000 0.6020 Serapan zat aktif menit ke 80 8 1 1.0000 0.4550 Serapan zat aktif menit ke 100 9 1 1.0000 0.3010 Serapan zat aktif menit ke 160 10 1 1.0000 0.2406 Serapan zat aktif menit ke 180
Lampiran 6. Absorbansi pemeriksaan difusi. ...(lanjutan)
Wavelength Program
__________________
Date: 9/23/2010 Time: 8:29:07 AM Method: Formula IV Slit: UV/VIS: 1.00 nm
Analyst: Ardian S. Nurhakim
Sample ID Cyc Factor 253.00 nm
__________________________________________________________________ __________________________
1 1 1.0000 0.0882 Serapan zat aktif menit ke 5 2 1 1.0000 0.1974 Serapan zat aktif menit ke 15 3 1 1.0000 0.2545 Serapan zat aktif menit ke 25 4 1 1.0000 0.3454 Serapan zat aktif menit ke 35 5 1 1.0000 0.4339 Serapan zat aktif menit ke 45 6 1 1.0000 0.5312 Serapan zat aktif menit ke 60 7 1 1.0000 0.6115 Serapan zat aktif menit ke 80 8 1 1.0000 0.4109 Serapan zat aktif menit ke 100 9 1 1.0000 0.3220 Serapan zat aktif menit ke 160 10 1 1.0000 0.2993 Serapan zat aktif menit ke 180
58
Lampiran 6. Absorbansi pemeriksaan difusi. ...(lanjutan)
Wavelength Program
__________________
Date: 9/23/2010 Time: 8:48:20 AM Method: Formula V Slit: UV/VIS: 1.00 nm
Analyst: Ardian S. Nurhakim
Sample ID Cyc Factor 253.00 nm
__________________________________________________________________ __________________________
1 1 1.0000 0.0955 Serapan zat aktif menit ke 5 2 1 1.0000 0.1990 Serapan zat aktif menit ke 15 3 1 1.0000 0.2955 Serapan zat aktif menit ke 25 4 1 1.0000 0.3909 Serapan zat aktif menit ke 35 5 1 1.0000 0.4924 Serapan zat aktif menit ke 45 6 1 1.0000 0.5808 Serapan zat aktif menit ke 60 7 1 1.0000 0.6652 Serapan zat aktif menit ke 80 8 1 1.0000 0.6019 Serapan zat aktif menit ke 100 9 1 1.0000 0.5306 Serapan zat aktif menit ke 160 10 1 1.0000 0.4366 Serapan zat aktif menit ke 180
Lampiran 6. Absorbansi pemeriksaan difusi. ...(lanjutan)
Wavelength Program
__________________
Date: 9/23/2010 Time: 9:10:20 AM Method: Formula VI Slit: UV/VIS: 1.00 nm
Analyst: Ardian S. Nurhakim
Sample ID Cyc Factor 253.00 nm
__________________________________________________________________ __________________________
1 1 1.0000 0.0998 Serapan zat aktif menit ke 5 2 1 1.0000 0.2011 Serapan zat aktif menit ke 15 3 1 1.0000 0.2982 Serapan zat aktif menit ke 25 4 1 1.0000 0.3956 Serapan zat aktif menit ke 35 5 1 1.0000 0.4992 Serapan zat aktif menit ke 45 6 1 1.0000 0.5955 Serapan zat aktif menit ke 60 7 1 1.0000 0.6917 Serapan zat aktif menit ke 80 8 1 1.0000 0.6135 Serapan zat aktif menit ke 100 9 1 1.0000 0.5354 Serapan zat aktif menit ke 160 10 1 1.0000 0.4444 Serapan zat aktif menit ke 180
60
Lampiran 7. Perhitungan pemeriksaan difusi.
62
Lampiran 9. Evaluasi pemeriksaan difusi.
Tabel 11. Hasil pemeriksaan difusi gel minyak jinten hitam
Formula
Kadar (ppm) minyak jinten hitam
menit ke
Gambar 9. Kurva hasil pemeriksaan difusi gel minyak jinten hitam
Lampiran 10. Gambar Alat-alat Penelitian.
Gambar 10. pH meter Gambar 11. Viskometer Brookfield
Gambar 12. Refraktometer Gambar 13. Spektrofotometer UV-Vis
64