1
DEPURASI LOGAM BERAT TIMBAL (Pb) PADA IKAN NILA
(
Oreochromis niloticus
) DENGAN MENGGUNAKAN
SALINITAS BERBEDA
Diajukan sebagai salahsatu syarat uk meraih gelar Master Sains di Fakultas Perikanan dan Ilmtut Pertanian Bogor
LA ODE ASLIN
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
2
PERNYATAAN MENGENAI TESIS DAN SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa tesis : Depurasi Logam Berat Timbal (Pb) pada Ikan Nila (Oreochromis niloticus) dengan Menggunakan Salinitas Berbeda adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, November 2012
3
ABSTRACT.
LA ODE ASLIN. Depuration Heavy Metal Lead (Pb) in Tilapia Fish (Oreochromis niloticus) with Differen Salinity. Under supervision of KUKUH NIRMALA and ENANG HARRIS.
Heavy metal pollution in the water is one of the limiting factor that also determine the success of aquaculture operation. The purpose of this study was to analyze the influence of salinity with increasing depuration of heavy metals Pb, which accumulate in the flesh, measured the level of oxygen consumption, growth and survival of oreochromis and analyze changes in the kidney due to histopathology gills and exposure to heavy metals. This research was carried out in February-April 2011. This research was carried out in the laboratory of the Bogor agricultural University. Results of research depuration of heavy metals indicates that there are significant differences between all treatments. The best salinity is 20 ppt, where the lowest percentage of heavy metals Pb during the process of depuration 120 hours is 1.21%. One is the level of oxygen consumption charge indicators will fish tilapia low salinity obtained at 0 ppt (0.28 0.05 mgO2/gram of fish/hour) and the highest on the salinity of 8 ppt (0.64 0.02 mgO2/g of fish/day). Low oxygen consumption indicates that the amount of energy used to metabolize a little more so that the portion of energy for greater growth. On experiment depurasi of heavy metals Pb in fish flesh of oreochromis shows response inversely between fish oreochromis growth and changes in salinity, growth pressures oreochromis more decreases the increasing salinity of the medium. The greatest growth reduction is obtained at the treatment of 20 ppt salinity is 11.64± 1.15 gr. based on the observations, the degree of survival of oreochromis high salinity media achieved at 0 ppt, 5 ppt and 10 ppt to reach 100%. Whereas on 15 and 20 ppt salinity ppt respectively reached 86.45% and 83.3%. In addition, observations of the Chemical Physics of water media maintenance which include the temperature, DO, pH and alkalinity showed conditions still favor the growth of oreochromis fish.
4
RINGKASAN
La Ode Aslin. Depurasi Logam Berat Timbal (Pb) pada Ikan Nila (Oreochromis niloticus) dengan Menggunakan Salinitas yang Berbeda . Dibimbing oleh Kukuh Nirmala dan Enang Harris.
Meningkatnya kegiatan akuakultur yang dilakukan oleh masyarakat menyebabkan meningkatnya kebutuhan akan air sebagai media budidaya. Banyak sumber air yang dapat dimanfaatkan para pembudidaya ikan salah satunya adalah pemanfaatan kolong bekas galian tambang mineral yang memiliki sifat pH rendah dan mengandung logam berat sehingga dapat mengakibatkan terjadinya proses akumulasi pada tubuh ikan nila yang dimanfaatkan sebagai ikan konsumsi. Metode yang digunakan untuk mengurangi atau menghilangkan logam berat yang terakumulasi dalam tubuh ikan adalah metode depurasi yaitu menempatkan ikan pada air bersih yang tidak mengandung logam berat. Tujuan penelitian ini adalah menganalisis pengaruh salinitas dengan meningkatkan depurasi logam berat Pb yang terakumulasi dalam daging, mengukur tingkat konsumsi oksigen, kelangsungan hidup dan pertumbuhan ikan nila serta menganalisis perubahan histopathologi insang dan ginjal akibat pemaparan logam berat.
Penelitian ini dilaksanakan pada bulan Februari - April 2012. Pengukuran kandungan Pb pada air dan organ ikan dilakukan di Laboratorium Pengujian Departemen Teknologi Industri Pertanian. Analisa proksimat daging pada Laboratorium Nutrisi Ikan Departemen Budidaya Perairan. Pembuatan preparat histopathologi insang dan ginjal dilakukan di bagian patologi, Departemen Klinik, Reproduksi dan Patologi, Fakultas Kedokteran Hewan.
5 Pada percobaan depurasi logam berat Pb dalam daging ikan nila menunjukkan respon yang berbanding terbalik antara pertumbuhan ikan nila dan perubahan tekanan salinitas, pertumbuhan ikan nila semakin menurun seiring meningkatnya salinitas media. Penurunan pertumbuhan yang paling besar didapatkan pada perlakuan salinitas 20 ppt yaitu sebesar 11.64±1.15 gr. Berdasarkan hasil pengamatan, derajat kelangsungan hidup ikan nila tertinggi dicapai pada salinitas media 0 ppt, 5 ppt dan 10 ppt yang mencapai 100%. Sedangkan pada salinitas 15 ppt dan 20 ppt masing-masing mencapai 91.7% dan 83.3%. Selain itu, pengamatan fisika kimia air media pemeliharaan yang meliputi suhu, DO, pH dan alkalinitas menunjukkan kondisi yang masih mendukung pertumbuhan ikan nila.
6
© HAK CIPTA milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan,
penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan
7
DEPURASI LOGAM BERAT TIMBAL (Pb) PADA IKAN NILA
(
Oreochromis niloticus
) DENGAN MENGGUNAKAN
SALINITAS BERBEDA
Diajukan sebagai salahsatu syarat uk meraih gelar Master Sains di Fakultas Perikanan dan Ilmu K Institut Pertanian Bogor
LA ODE ASLIN
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains Pada Program Studi Ilmu Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
9
PRAKATA
Segala puji dan rasa syukur penulis haturkan kepada Alloh SWT, pemberi nikmat dan anugrah sehingga penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini dilakukan sebagai sebuah aplikasi ilmiah terhadap perkuliahan pasca sarjana yang telah ditempuh. Penelitian ini mengambil judul : Depurasi Logam Berat Timbal (Pb) pada Ikan Nila (Oreochromis niloticus) dengan Menggunakan Salinitas Berbeda
Penulis mengucapkan terima kasih kepada Bapak Dr. Ir. Kukuh Nirmala, M.Sc dan Bapak Prof. Dr. Ir. Enang Harris, MS selaku komisi pembimbing atas segala arahan, saran dan bimbingan serta pengajaran tentang ketajaman cara berpikir ilmiah sehingga tesis ini dapat terselesaikan dengan baik. Juga kepada Bapak Dr. Ir. Eddy Supriyono, M.Sc selaku dosen penguji luar komisi atas masukan, saran dan sumbangan keilmuannya untuk kebaikan tesis ini. Tidak lupa yang paling utama penulis mengucapkan terima kasih kepada kedua orang tua (Bapak La Ode Harisi dan Almarhumah Ibunda Wa Ode Daeno) atas segala perhatian yang diberikan kepada penulis. Penulis juga secara khusus mengucapkan terima kasih kepada saudara La Ode Kahar M., La Ode Hasida, S.Pd., Wa Ode Siti Amini., Abdul Sarifin, S.Pi., Abdul Rifai, SH., dan Abdul Johar atas segala dukungan, kesabaran, kerinduan dan doa yang diberikan. Terima kasih kepada semua pihak yang membantu penelitian ini (Robin, S.Pi., M. Si) dan juga rekan-rekan dosen FPIK Unhalu serta teman-teman akuakultur 2010 atas kebersamaannya.
Karya ilmiah ini semoga memberikan manfaat.
Bogor, November 2012
10
RIWAYAT HIDUP
Penulis dilahirkan di Watuputih, Kabupaten Muna, Provinsi Sulawesi Tenggara pada tanggal 5 April 1984 sebagai anak ketiga dari enam bersaudara dari ayah La Ode Harisi dan ibu almarhumah Wa Ode Daeno.
11
DAFTAR ISI
DAFTAR ISI ... xi
DAFTAR TABEL ... ... xiiiv
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN... xvvi
PENDAHULUAN Latar Belakang ... 1
Perumusan Masalah ... 4
Pendekatan masalah ... 4
Tujuan Penelitian ... 5
Manfaat Penelitian ... 5
Hipotesis ... 5
TINJAUAN PUSTAKA Ikan Nila Merah (O. niloticus) ... 7
Logam Berat Timbal (Pb) ... 7
Salinitas dan Osmoregulasi ... 10
Konsumsi Oksigen ... 15
Proses Aklimatisasi Ikan ... 17
Proses Akumulasi Logam Berat ... 17
Proses Depurasi Logam Berat ... 18
Pertumbuhan dan Kelangsungan Hidup Ikan... 19
Kadar Lemak Tubuh Ikan ... 20
Histopathologi Organ Ikan ... 21
METODOLOGI PENELITIAN Tempat dan Waktu ... 23
Hewan Uji ... 23
Metode Penelitian ... 23
Prosedur Penelitian ... 24
Parameter Pengamatan ... 26
Analisis Data ... 30
HASIL DAN PEMBAHASAN Akumulasi Logam Berat Timbal (Pb) ... 31
Depurasi Logam Berat Pb dengan Air Bersalinitas ... 33
Tingkat Konsumsi Oksigen ... 35
Perubahan Bobot Tubuh Ikan ... 36
Kadar Lemak pada Ikan Nila ... 38
Kelangsunga Hidup Ikan ... 39
Analisis Histopathologi ... 40
Kualitas Air ... 46
SIMPULAN DAN SARAN ... 55
SIMPULAN ... 55
12
DAFTAR TABEL
Tabel
Halaman
1. Kosentrasi logam berat pada air yang mematikan ikan
pada pemaparan 96 jam ... 8
2. Perbandingan tingkat konsumsi oksigen pada beberapa jenis tilapia. ... 16
3. Pengaruh pemberian Pb dalam air terhadap peningkatan kosentrasi Pb dalam daging dan beberapa peubah pertumbuhan ikan. ... 31
4. Rata-rata konsentrasi Pb dalam daging pada salinitas dan waktu pengamatan yang berbeda ... 33
5. Rata-rata tingkat konsumsi oksigen ikan nila pada salinitas yang berbeda .... 35
6. Rata-rata pertumbuhan harian (g) ikan nila yang dipelihara pada salinitas yang berbeda ... 36
7 Persentase (%) kadar lemak ikan nila (O. niloticus) yang dipelihara pada salinitas yang berbeda selam penelitian ... 38
8 Derajat kelangsungan hidup (%) ikan nila (O.niloticus) pada perlakuan salinitas yang berbeda ... 39
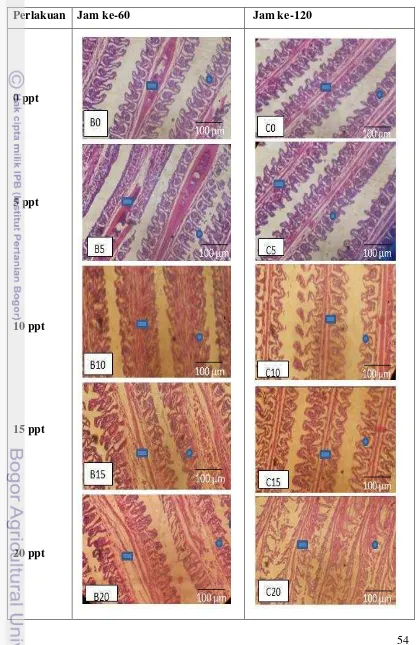
9 Perubahan histopathologi organ insang ikan nila pada salinitas yang berbeda pada jam ke-60 dan jam ke-120 ... 41
10. Histopathologi organ insang ikan nila pada salinitas yang berbeda pada ... 42
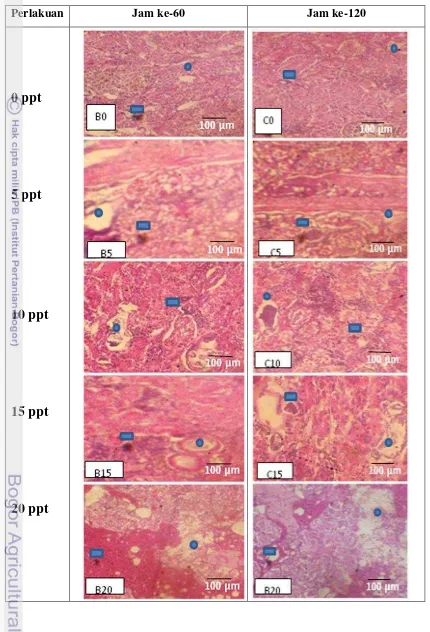
11. Perubahan histopathologi organ ginjal ikan nila pada salinitas yang berbeda pada jam ke-60 dan jam ke-120 ... 44
12 Histopathologi organ ginjal ikan nila pada salinitas yang berbeda ... 45
13 Kisaran parameter kualitas air selama proses akumulasi logam Pb ... 46
13
DAFTAR GAMBAR
Gambar
Halaman
1. Mekanisme osmoregulasi pada teleost air laut (a) dan teleost air tawar (b). ... 12 2. Grafik Jumlah Pb yang terkonsentrasi terkonsentrasi pada daging ikan
selama proses akumulasi pada media air yang mengandung logam berat. ... 31 3. Grafik rata-rata konsentrasi Pb dalam daging pada salinitas dan waktu
pengamatan yang berbeda. ... 33 4. Persentase (%) konsentrasi Pb yang tersisa did aging ikan dengan
salinitas yang berbeda pada akhir penelitian ... 34 5. Rata-rata tingkat konsumsi oksigen ikan nila pada salinitas yang berbeda .... 36 6. Rata-rata pertumbuhan harian (g) ikan nila yang dipelihara
pada salinitas yang berbeda ... 37 7 Persentase (%) kadar lemak ikan nila (O. niloticus) yang dipelihara
14
PENDAHULUAN
Latar Belakang
Masalah pencemaran lingkungan terutama masalah pencemaran air mendapat perhatian yang besar dari pemerintah, karena air merupakan salah satu unsur penting bagi makhluk hidup. Dengan meningkatnya kegiatan akuakultur yang dilakukan oleh masyarakat dan pembudidaya ikan menyebabkan meningkatnya kebutuhan akan air sebagai media budidaya. Banyak sumber air yang dapat dimanfaatkan para pembudidaya ikan salah satunya adalah pemanfaatan kolong bekas galian tambang mineral yang diketahui memiliki sifat pH rendah dan mengandung logam berat.
Kandungan logam berat dalam suatu perairan merupakan salah satu faktor pembatas yang juga menentukan keberhasilan usaha budidaya perairan. Konsentrasi logam berat yang berlebihan akan memberi tekanan terhadap pertumbuhan dan perkembangan suatu mahkluk hidup. Oleh sebab itu, konsentrasi logam berat pada perairan akan menentukan apakah perairan itu layak digunakan sebagai tempat melakukan kegiatan budidaya perairan atau tidak. Logam berat mempunyai bahaya langsung maupun tidak langsung terhadap mahkluk hidup, karena itu keberadaannya dalam perairan harus diketahui sehingga dapat mengantisipasi bahaya yang ditimbulkanya. Air yang tercemar logam berat sangat berbahaya bagi ikan budidaya dan memiliki potensi berbahaya bagi manusia. Logam berat yang terdapat pada media pemeliharaan ikan dapat menyebabkan gangguan dan kematian pada ikan. Pada konsentrasi logam yang masih dapat ditoleransi, logam berat akan terakumulasi dalam tubuh ikan (bioakumulasi) dan memiliki potensi berbahaya bila dikonsumsi oleh manusia.
15 potensi untuk menyesuaikan diri pada salinitas air laut (± 35 ppt) (Watanabe et al, 1989).
Ikan nila (O. niloticus) merupakan hewan yang banyak dikonsumsi masyarakat sehari-hari dan dibudidayakan pada air tawar seperti sungai, waduk dan danau. Namun belakangan ini pemeliharaan ikan nila sudah banyak dilakukan pada perairan kolong sebagai bekas galian tambang mineral yang mana diketahui memiliki pH yang rendah dan memiliki kandungan limbah berupa logam berat. Penelitian yang dilakukan oleh Henny dan Susanti (2009) menyatakan bahwa salah satu logam berat yang berpotensi di perairan kolong bekas galian tambang timah adalah logam berat timbal (Pb).
Timbal (Pb) merupakan unsur logam berat yang sama sekali tidk dibutuhkan oleh mahluk hidup termasuk ikan. Logam Pb yang bersifat toksik biasanya dalam bentuk Pb2+. Secara umum keberadaan Pb dalam perairan bersumber dari kegiatan pertambangan juga kegiatan industri. Keberadaan Pb pada air sebagai media budidaya akan sangat berdampak pada terjadinya proses akumulasi pada tubuh ikan. Ikan yang terakumulasi logam berat Pb apabila dikonsumsi manusia maka akan menghambat proses enzimatik (Widowati et al. 2008) merusak sistem saraf pusat, ginjal, liver, dan sistem reproduksi (Fu dan Wang 2011). Oleh karena itu, ikan yang dihasilkan dari kegiatan budidaya dan mengandung logam berat harus diberikan perlakuan (treatment) untuk menghilangkan logam beratnya sebelum dikonsumsi manusia.
Untuk mengantisipasi maslah ini diperlukan alternatif antara lain metode depurasi yaitu menempatkan ikan pada air bersih yang tidak mengandung logam berat (Suseno et al. 2010). Pada metode ini diharapkan logam berat (Pb) yang cenderung terikat di lemak pada jaringan daging bisa terlepas melalui proses metabolisme. Menurut Boyd et al. (1990) proses osmoregulasi pada ikan air tawar memanfaatkan kandungan lemak sebagai sumber energi utama dalam menyesuaikan perubahan kondisi lingkungan khususnya perubahan salinitas. Air akan masuk ke tubuh ikan karena kondisi tubuhnya hipertonik, sehingga ikan banyak mengeksresikan air dan menahan ion dari lingkunganya (Fujaya 2004).
16 Stickney (1969) dalam Affandi dan Tang (2002) menyatakan bahwa ikan yang dipelihara pada media yang tingkat salinitasnya mendekati konsentrasi ion darahnya, maka energi untuk proses osmoregulasi akan cukup kecil dan akan lebih banyak digunakan untuk pertumbuhan. Salinitas dapat mempengaruhi komposisi nutrisi/kimiawi tubuh organisme akuatik antara lain molekul-molekul yang terdiri dari asam lemak, asam amino, glukosa dan kandungan mineral tubuh lainya yang akan tercermin pada penampilan fisik (warna, tekstur) dan cita rasa organisme akuatik yang dihasilkan.
Budidaya ikan nila pada media bersalinitas memiliki kelebihan dan kekurangan. Kajian tentang salinitas penting dilakukan terkait dengan upaya untuk mendapatkan keuntungan baik secara kuantitas maupun kualitas dalam kegiatan budidaya ikan nila. Penelitian mengenai pemeliharaan ikan nila pada berbagai kisaran salinitas yang berkaitan dengan pertumbuhan dan kelangsungan hidup telah banyak dilakukan. Namun penelitian tersebut tidak mengkaji peranan salinitas yang berkaitan dengan kualitas daging terhadap cemaran logam berat pada ikan nila yang dihasilkan. Salami et al. (2006) melakukan penelitian tentang depurasi logam tembaga (Cu) pada ikan nila dengan air PDAM yang berkesadahan soft dan pH netral yang dilakukan selam 3 hari namun hasil menujukan bahwa proses depurasi tidak dapat menurunkan kadar logam Cu pada daging ikan secara efektif. Prihatiningsih et al. (2009) melaporkan bahwa salinitas pada air laut mempengaruhi pelepasan logam berat merkuri yang terakumulasi dalam tubuh ikan bandeng dimana kadar logam berat mengalami penurunan seiring dengan bertambahnya waktu.
Oleh sebab itu, air bersalinitas dapat digunakan secara tidak langsung sebagai metode yang efektif dalam proses depurasi pada ikan air tawar yang tercemar logam berat untuk mengeluarkan konsentrasi Pb yang terakumulasi dalam daging. Melihat keunggulan air bersalinitas sebagai media depurasi dalam proses pengurangan logam berat yang terkandung dalam daging ikan air tawar, maka teknologi ini memiliki peluang untuk dikembangkan menjadi salah satu teknik untuk keamanan pangan pada budidaya ikan sehingga perlu dilakukan suatu penelitian yang berkelanjutan.
17 Masalah utama pada budidaya ikan nila adalah media budidaya yang mengandung logam berat dalam konsentrasi tinggi menyebabkan terjadinya kematian ikan dan terakumulasinya logam berat kedalam tubuh ikan. Ikan yang mengandung logam berat Pb akan menyebabkan resiko dan ketidaklayakan dalam kegiatan budidaya ikan. Ketidaklayakan tersebut berupa daging ikan yang tidak layak digunakan sebagai bahan konsumsi. Selain itu, permasalahan yang timbul akan berdampak pada menurunnya produksi dan harga jual serta nilai ekspor yang rendah sehingga keuntungan yang diraih juga rendah. Salinitas merupakan salah satu faktor lingkungan yang diupayakan untuk menjadi solusi dalam mengatasi berbagai permasalahan akumulasi logam berat.
Pendekatan Masalah
Salinitas merupakan salah satu parameter fisika lingkungan yang digunakan untuk melihat produktifitas dan proses depurasi logam berat pada ikan. Salinitas sangat berhubungan erat dengan proses osmoregulasi pada organisme akuatik. Ikan nila merupakan jenis ikan yang mampu hidup pada kisaran toleransi salinitas yang luas (euryhaline).
Upaya ikan untuk menjaga keseimbangan salinitas media dengan konsentrasi ion tubuhnya dikenal dengan istilah osmoregulasi. Proses osmoregulasi membutuhkan energi yang besarnya tergantung pada tingkat osmotik. Pada saat ikan dipelihara pada kondisi perairan yang bersalinitas tinggi maka energi yang dibutuhkan untuk proses metabolisme semakin besar pula. Salah satu sumber energi yang dimanfaatkan adalah bersumber dari lemak yang terkandung dalam daging. Pada saat terjadi metabolisme lemak sebagai sumber energi mengakibatkan logam berat yang memiliki sifat kecenderungan terikat pada bagian lemak akan ikut terurai dan selanjutnya melalui transport aktif logam berat masuk dalam peredaraan darah yang kemudian diekskresikan bersama cairan tubuh melalui pembuangan urin.
18 konsentrasi optimal didapatkan dengan cara memberikan perlakuan konsentrasi yang berbeda pada percobaan.
Tujuan Penelitian
Penelitian ini bertujuan untuk menganalisis pengaruh salinitas dalam meningkatkan depurasi logam berat Pb pada daging ikan, mengukur tingkat kosumsi oksigen, kelangsungan hidup dan pertumbuhan ikan nila, menganalisis kadar lemak serta histopathologi organ insang dan ginjal yang telah terpapar logam berat Pb pada kegiatan akuakultur.
Manfaat Penelitian
Menghasilkan teknologi tepat guna pada system teknologi akuakultur pada kolong bekas tambang mineral sehingga diharapkan air bersalinitas dapat menjadi solusi yang efektif dan efisien dalam menghilangkan logam berat Pb yang terakumulasi pada daging ikan budidaya.
Hipotesis
19
TINJAUAN
PUSTAKA
Ikan Nila Merah (O. niloticus)
Ikan nila (O. niloticus) sebagai salah satu komoditas andalan di subsektor perikanan dan sangat diminati masyarakat luas karena rasa dgingnya yang khas. Ikan ini banyak dibudidayakan oleh para pembudidaya ikan baik pada skala pembenihan maupun pembesaran. Tingginya permintaan konsumen dan kisaran toleransinya yang tinggi sehingga sangat potensial untuk dikembangkan pada skala usaha budidaya baik secara teknis maupun kualitas produksi. Selain hal tersebut, ikan nila cukup pekah terhadap pencemaran logam berat terutama pada fase awal kehidupan (Rachmansyah 1998).
Ikan nila merah mempunyai ciri-ciri morfologi : bentuk bulat pipih, punggung lebih tinggi, pada badan dan sirip ekor (caundal fin) ditemukan garis lurus (vertikal). Sedangkan garis lurus memanjang ditemukan pada sirip punggung. Ikan nila merah dapat hidup diperairan tawar dan mereka menggunakan ekor untuk bergerak, sirip perut, sirip dada dan penutup insang yang keras untuk mendukung badannya. Ikan nila merah termasuk omnivora. Makanannya berupa hewan-hewan seperti protozoa dan zooplankton serta ganggang, algae yang tersedia di kolam. Persyaratan kualitas air budidaya ikan nila merah yaitu suhu 25-30 0C, DO ≥ 3 mg/l, pH 6-8,5, kecerahan 20-30 cm dan CO2 < 5 mg/l (Zonneveld et al. 1991).
Logam Berat Timbal (Pb)
20 logam berat dalam jumlah yang berlebihan dapat bersifat racun. Bahan cemaran ini akan mengalami tiga macam proses akumulasi yaitu proses fisik, kimia dan biologi.
Logam memiliki karakter bereaksi sebagai akseptor pasangan elektron (asam lewis) dan donor pasangan elektron (basa lewis) untuk membentuk beragam gugus kimia seperti suatu pasangan ion, kompleks logam, senyawa koordinasi dan kompleks donor-akseptor (Connel dan Miller 2006). Berdasarkan karakteristik inilah logam berat dapat diikat oleh bahan lain yang bisa menjadi pasangan atau senyawa koordinasi yang sering disebut dengan ligan.
Menurut Vouk (1986) dalam Tjakrawidjaja (2001) logam berat dapat dibagi dalam dua jenis yaitu logam berat esensial dimana keberadaannya dalam jumlah tertentu sangat dibutuhkan oleh organisme hidup namun dalam jumlah yang berlebihan dapat menimbulkan efek racun. Contoh logam berat ini adalah Zn, Cu, Fe, Co dan Mn. Sedangkan jenis kedua adalah logam berat tidak esensial atau beracun di mana keberadaannya dalam tubuh masih belum diketahui manfaatnya atau bahkan dapat bersifat racun seperti Pb.
Konsentrasi logam berat pada kulit ikan dapat menjadi lebih tinggi karena kandungan lipid/lemak pada kulit lebih banyak dari pada daging. Seperti yang telah diketahui bahwa logam berat mempunyai kecenderungan untuk terikat dengan lemak yang ada dalam tubuh. Semakin banyak lemak yang terdapat dalam tubuh maka semakin besar kemungkinan logam berat untuk dapat terakumulasi dalam tubuh (Chen dan Chen 2001).
Tabel 1 Konsentrasi logam berat pada air yang mematikan ikan pada pemaparan 96 jam
Jenis logam berat Konsentrasi mematikan pada ikan (mg/l) Cd
Cu Pb Zn Ni
22 - 25 2,5 - 3,5
21 Timbal atau dalam keseharian lebih dikenal dengan nama timah hitam, dalam bahasa ilmiahnya dinamakan plumbum dan logam ini disimbolkan dengan Pb. Logam ini termasuk ke dalam kelompok logam-logam golongan IV-A pada tabel periodik unsur kimia. Timbal (Pb) dan persenyawaannya dapat berada di badan perairan dalam bentuk terlarut dan tersuspensi, baik secara alamiah maupun sebagai dampak aktivitas manusia. Pb masuk ke perairan melalui limbah industri dan pertambangan. Logam berat timah hitam atau timbal (Pb) merupakan salah satu logam berat yang berbahaya bagi mahluk hidup. Logam berat ini merupakan elemen non esensial yang ditemukan pada konsentrasi yang tinggi di alam akibat kegiatan manusia, seperti : kegiatan pertambangan (Leston et al. 2010). Sifat berbahaya Pb pada mahluk hidup antara lain dapat menimbulkan penghambatan sintesis hemoglobin, disfungsi pada ginjal, sendi dan sistem reproduksi, sistem kardiovaskular, dan kerusakan akut dan kronis dari sistem saraf pusat (SSP) serta sistem saraf perifer (PNS). Efek lainnya termasuk kerusakan pada saluran pencernaan (GIT) dan saluran kemih, gangguan neurologis, serta kerusakan otak parah dan permanen (Khan et al. 2011).
22 dan sisik, insang, mata, hati, ginjal dan otot . Disamping itu ion Pb juga dapat masuk kedalam tubuh ikan bersama dengan makanan dan air yang akhirnya diserap di usus dan jaringan lainnya.
Beberapa pengaruh toksisitas logam pada ikan yang telah terpapar logam berat yaitu pada insang, alat pencernaan dan ginjal (Khan et al, 2011). Jumlah Pb yang terakumulasi pada tubuh ikan tergantung dari ukuran, umur dan kondisi ikan. Distribusi dan akumulasi logam berat sangat berbeda-beda untuk organisme air. Hal ini tergantung pada spesies, konsentrasi logam dalam air, pH, fase pertumbuhan dan kemampuan ikan (Darmono 1995). Toksisitas kronis Pb umumnya sama antara ikan dan mamalia terutama yang melibatkan disfungsi neurologis dan hematologi Pada ikan, efek sublethal Pb dapat menyebabkan efek orde tinggi, seperti berkurangnya kemampuan renang. Secara neurologis efek sublethal Pb berpotensi melibatkan gangguan respon koordinasi sensorik-motorik yang diperlukan untuk menangkap mangsa dan menghindari predator. Penelitian Olaifa et al. (2003) menemukan bahwa efek sublethal Pb pada ikan yaitu kehilangan keseimbangan, pemutihan kulit dan pelemahan ikan. Kerusakan jaringan oleh logam berat terhadap pada beberapa lokasi baik tempat masuknya logam (insang) maupun tempat penimbunanya (hati). Akibat yang ditimbulkan dari toksisitas logam berat timbal (Pb) dapat berupa kerusakan fisik (erosi, degenerasi, nekrosis) dan dapat berupa gangguan fisiologi (gangguan fungsi enzim dan gangguan metabolisme).
Salinitas dan Osmoregulasi
Salinitas adalah bobot garam-garam anorganik halogen yang terlarut (garam) dalam 1 kg air, apabila semua bromide dan iodida disetarakan dengan klorida dan semua karbonat disetarakan dengan oksidanya (Knedsen dalam
23 metabolisme ikan sehingga dalam kondisi tersebut sekresi mucus akan meningkat (Baldisserotto et al. 2007).
Salinitas berhubungan erat dengan tekanan osmotik dan tekanan ionik air, baik air sebagai media internal maupun eksternal. Sifat osmotik air bergantung pada seluruh ion yang terlarut dalam air tersebut, semakin besar jumlah ion yang terlarut dalam air maka tingkat salinitas dan kepekatan osmotik larut akan semakin tinggi, sehingga akan menyebabkan tekanan osmotik medium bertambah besar. Ion-ion yang dominan dalam menentukan tekanan osmotik (osmolaritas) air laut adalah Na+ dan Cl- dengan kandungan masing-masing sebesar 30,61% dan 55,04% dari total seluruh kandungan ion-ion yang terlarut dalam air (Harvey 1976).
Dengan respon osmotiknya, ikan-ikan air tawar mempunyai tekanan osmotik cairan internal (dalam tubuh) lebih besar dari tekanan osmotik eksternal (lingkungan) sehingga cairan cenderung keluar dalam tubuh sedangkan air dari lingkungan cenderung masuk kedalam tubuh. Oleh sebab itu dibutuhkan proses pengaturan tekanan osmotik untuk mengontrol keseimbangan osmotik antara cairan didalam tubuh dengan air sebagai media hidupnya. Pengaturan osmotik ini dilakukan dengan mekanisme osmoregulasi (Affandi dan Tang 2002)
Ikan teleost air tawar mempunyai konsentrasi osmotik dalam darahnya 300-400 mOsm per liter, yang mana lebih tinggi dari lingkungan air tawar atau berada pada keadaan yang hiperosmotik, secara kontinyu melakukan pelepasan sejumlah ion-ion natrium dan klorida ke lingkungan dengan cara difusi melintasi epithelial insang yang tipis. Sejumlah larutan secara kontinyu dilepaskan lewat urin maupun berdifusi secara pasif melintasi lapisan epithelial insang (Moyle and Cech 1988). Walaupun beberapa garam juga diperoleh melalui sumber makanan, sebagian besar ion-ion terutama ion natrium dan klorida diperlukan untuk keseimbangan ion-ion internal melalui mekanisme transport aktif dalam insang (Schmidt 1987).
24 perpindahan ion Na+ dan Cl- kedalam tubuh ikan lebih baik dibandingkan dengan ke luar. Mekansime pertukaran ion melayani beberapa fungsi selain untuk memelihara Na+ dan Cl- ke dalam ikan. Pertukaran Na+ dengan NH4+ terjadi dengan baik pada ikan yang merupakan bagian dari mekanisme produksi amonia. Pertukaran Na+ dengan H+ dan Cl- dengan HCO3- terjadi untuk mempertahankan keseimbanagan asam-basa. Menurut Moyle dan Cech (1986), kedua mekanisme pertukaran ion tersebut dilangsungkan untuk :
1. Memelihara (Na+) internal yang tepat 2. Memelihara internal (Cl-) yang tepat 3. Mendepurasi beberapa potensi racun
4. Mengeluarkan beberapa metabolik CO2 (HCO3-) 5. Mengatur kosentrasi H+ dan OH- internal
6. Keseimbangan elektris ion-ion
a b
Gambar 1. Mekanisme osmoregulasi pada teleost air laut (a) dan teleost air tawar (b). Keterangan : CC = sel klorida; N = Nucleus
25 Sebagaimana diketahui bahwa kondisi osmotik dari teleost air tawar pada umumnya menyerupai invertebrata air tawar. Konsentrasi osmotik dalam darah berkisar pada 300 mOsm per lieter, yang lebih tinggi dibandingkan dengan konsentrasi osmotik air tawar. Sehingga masalah utama pada ikan ini adalah bagaiamana memasukan air secara osmosis. Insang memainkan peranan penting sebab luas permukaan lebih besar dan relatif lebih permeabel, sedangkan permukaan kulit relatif kecil sehingga dapat disimpulkan bahwa pada ikan ini permukaan kulit kurang berperan dalam aktivitas absorbsi. Kelebihan air diekskresikan sebagai urin yang sangat encer dan dapat dihasilkan dalam jumlah sampai sepertiga dari berat badan per hari. Pada insang sedikit lebih permeabel terhadap ion dan kehilangan ion di sini harus ditutupi melalui pengambilan ion (Schmidt 1987). Di samping insang dan ginjal, epithelial usus juga berperan dalam pengaturan keseimbangan air dan mineral. Pada usus ikan yang diadaptasikan ke air tawar terdapat sedikit peran Na-K-ATPase untuk aktivitas transport natrium ke dalam darah dari lumen usus, tetapi aktivitas Na-K-ATPase lebih berperan pada ikan yang diadaptasikan di air laut.
26 Osmoregulasi adalah upaya hewan air untuk mengontrol keseimbangan air dan ion antara tubuh dan lingkungannya atau suatu proses pengaturan tekanan osmose (Fujaya 2004). Karena itu, pengetahuan tentang osmoregulasi sangat penting dalam mengelola kualitas air media pemeliharaan terutama bila adanya perbedaan salinitas. Ikan nila yang dipelihara di media buatan seringkali mengalami masalah karena osmolaritas media hidupnya belum tentu sesuai dengan osmolaritas cairan tubuhnya. Untuk mengatasi permasalahan osmotik tersebut maka ikan nila dapat menjaga keseimbangan osmotik dengan cara mempertahankan kemampuan osmolaritas cairan internal melalui mekanisme osmoregulasi. Beberapa organ tubuh ikan yang berperan dalam proses osmoregulasi ikan yaitu insang, ginjal dan usus. Organ-organ ini melakukan fungsi adaptasi di bawah kontrol hormon, terutama hormon-hormon yang disekresi oleh pituitari, ginjal dan urofisis (Smith 1982).
Menurut Fujaya (2004) menyatakan bahwa osmoregulasi dari beberapa golongan ikan terdapat ada tiga pola regulasi ion dan air yaitu :
1. Regulasi hipertonik atau hiperosmotik yaitu pengaturan secara aktif dimana konsentrasi cairan tubuh yang lebih tinggi dari konsentrasi media. Misalnya pada potadrom (ikan air tawar ).
2. Regulasi hipotonik atau hipoosmotik yaitu pengaturan secara aktif konsentrasi cairan tubuh yang lebih rendah dari konsentrasi media, misalnya pada oseandrom (ikan air laut).
3. Regulasi isotonik atau isoosmotik yaitu bila konsentrasi cairan tubuh sama dengan konsentrasi media, misalnya ikan – ikan yang hidup pada daerah estuari.
27 aktif. Selain itu, insang juga aktif mengambil garam-garam dari lingkungannya. Kedua hal ini membutuhkan energi metabolik dimana semakin jauh perbedaan tekanan osmose antara tubuh dan lingkungan maka semakin banyak energi metabolisme yang dibutuhkan untuk melakukan osmoregulasi (Smith 1982 ).
Konsumsi Oksigen
Tingkat konsumsi oksigen adalah banyaknya oksigen yang diambil atau dikonsumsi oleh organisme akuatik dalam waktu tertentu yang berhubungan linear dengan banyaknya oksigen terlarut diperairan tersebut (Vernberg 1972).
Oksigen terlarut (Dissolved oxygen = DO) dibutuhkan oleh semua jasad hidup untuk pernapasan, proses metabolisme atau pertukaran zat yang kemudian menghasilkan energi untuk pertumbuhan. Disamping itu, oksigen juga dibutuhkan untuk oksidasi bahan-bahan organik dan anorganik dalam proses aerobik. Keperluan organisme terhadap oksigen relatif bervariasi tergantung pada jenis, stadium dan aktivitasnya. Kebutuhan oksigen untuk ikan dalam keadaan diam relative lebih sedikit apalagi dibandingkan dengan ikan pada saat bergerak. Kandungan oksigen terlarut (DO) minimal adalah 2 ppm dalam keadaan normal dan tidak tercemar oleh senyawa beracun (Wardoyo 1987).
28 suhu yang merupakan aspek yang sangat penting yang berhubungan dengan metabolisme rutin dan konsumsi oksigen pada ikan, salinitas dan aktivitas berenang (Caulton 1977).
Dalam mekanisme transport aktif diperlukan energi dan yang sangat menarik untuk diketahui bahwa peningkatan keperluan energi dapat berubah-ubah pada ikan. Sebagai contoh apabila ikan berpindah dari medium yang lebih encer atau dari air tawar ke air payau dan air laut akan terjadi peningkatan kebutuhan energi yang ditandai dengan peningkatan dalam laju konsumsi oksigen yang cukup besar, bahkan dapat mencapai 50 persen. Hal ini dapat disimpulkan bahwa peningkatan ini merupakan pertanda peningkatan kerja transport aktif ion yang diperlukan untuk memelihara tingkat osmotik cairan tubuh ikan tersebut.
Konsumsi oksigen pada tilapia sangat beragam. Job (1969) melaporkan konsumsi oksigen yang sangat tinggi pada tilapia dalam kondisi yang isoosmotik. Sebaliknya Asem (1981) melaporkan bahwa konsumsi oksigen tilapia meningkat pada setiap kondisi salinitas. Perbedaan dapat diakibatkan oleh beberap faktor seperti suhu, salinitas dan aktivitas (Ross dan Mickinney 1988).
Tabel 2. Perbandingan tingkat konsumsi oksigen pada beberapa jenis tilapia.
29
Proses Aklimatisasi Ikan
Aklimatisasi mengambarkan respon kompenisasi dari suatu organisme terhadap perubahan beberapa faktor lingkungan, sedangkan jika dipengaruhi oleh satu faktor lingkungan disebut aklimasi (Affandi dan Tang 2002). Ikan nila merupakan jenis ikan yang mampu hidup pada salinitas yang tinggi. Kemampuan ikan nila untuk hidup pada salinitas tinggi harus melalui proses aklimatisasi. Menurut Boyed (1982) dalam Taqwa (2008), peningkatan salinitas yang dilakukan pada ikan nila berkisar antara 1 atau 2 ppt per jam. Penempatan ikan nila secara mendadak pada air laut yang salinitasnya lebih tinggi (hiperosmotik) akan menyebabkan kehilangan ion melalui permukaan tubuh dan urin. Hal ini akan menyebabkan kematian bila perubahan osmotik yang dialami sangat besar. Cara mengatasinya diperlukan sejumlah energi metabolik yang besar dan sebanding dengan laju kehilangan ion dari tubuh maupun urin (Lockwood 1967 dalam Taqwa 2008).
Proses Akumulasi Logam Berat
Pengambilan bahan pencemaran oleh makhluk hidup mengakibatkan peningkatan kepekatan yang dapat memiliki pengaruh yang negatif dalam tubuh organisme tersebut. Proses ini dapat terjadi oleh penyerapan langsung dari lingkungan sekeliling atau oleh penyerapan suatu pencemar dalam makhluk hidup bahan makan. Pencemar dalam makhluk hidup bahan makanan dapat timbul dari sumber yang sama. Jadi dalam suatu rantai makanan alamiah, pencemar dapat dipindahkan dari suatu tingkat trofik ke tingkat trofik lainya ( Connell dan Miller. 2006).
Sanusi (1980) dalam Darmono (2008) mengemukakan bahwa terjadinya proses akumulasi logam berat di dalam tubuh hewan air terjadi karena kecepatan pengambilan logam berat (uptake rate) oleh organisme air lebih cepat dibandingkan dengan proses pelepasan. logam berat akan terlibat dalam proses enzimatik, terikat dengan protein (ligan binding).
30 (gastrointestinal) melalui dinding-dindingnya akan menuju ke cairan sirkulatori. Bahan-bahan kimia setelah dari cairan sirkulatori ada yang di metabolisme dan ada yang bertemu dengan kebanyakan jaringan tubuh dan selanjutnya ditimbun dalam jaringan lemak. Bahan-bahan kimia (senyawa timbal) dalam cairan sirkulatori akan teroksidasi menjadi Pbdan akan terakumulasi dalam hati. Logam berat Pb dalam hati akan dimetabolisme dan akan diinaktifkan oleh enzim-enzim di dalam hati sehingga terjadi biotransformasi zat- zat berbahaya menjadi zat-zat yang tidak berbahaya yang kemudian diekskresikan oleh ginjal.
Proses Depurasi Logam Berat Pb
31
Pertumbuhan dan Kelangsungan Hidup Ikan
Hewan air dalam hubunganya dengan lingkungan tempat hidupnya dikelompokan atas dua kategori yaitu kelompok hewan yang toleran terhadap
kadar salinitas yang sangat luas yang disebut “eurihalin” dan kelompok yang hanya terbatas pada kondisi kadar salinitas yang sempit disebut “stenohalin”
(Schmidt 1987). Apabila hewan air menghadapi perubahan kadar salinitas, salah satu jalan yang ditempuh untuk menjaga kelangsungan hidupnya adalah menggunakan transport aktif terutama pompa Na-K-ATPase, karena ion-ion Na+, K+, merupakan ion-ion yang dominan dalam proses ini. Hal ini dilakukan untuk mempertahankan gradien osmotik antara cairan tubuh dengan cairan lingkungan eksternal agar proses fisiologis dalam tubuh berjalan normal (Foskett et al. 1983). Brett (1979) menyatakan bahwa respon terhadap kadar salinitas mempunyai hubungan tekanan osmotik cairan tubuh ikan tersebut. Hal ini dapat dilihat pada ikan salmon dan sidat yang walaupun mempunyai cara atau siklus hidup yang berbeda, perubahan dari lingkungan air tawar ke lingkungan air laut atau sebaliknya sangat memerlukan perubahan dalam proses osmoregulasi dan pada kondisi di air laut ikan menunjukan pertumbuhan yang lambat dibandingkan dengan pada air tawar karena energi pemelihraan di air laut lebih banyak dibandingkan dengan air tawar. Hal ini terlihat dari nilai osmotik pada salmon yang dipuasakan pada tiga kondisi lingkungan yang berbeda masing-masing air tawar, payau dan air laut dengan nilai osmotik berturut-turut; 300.9, 308.0 dan 358.2 mOsm/kg. peningkatan salinitas ini diketahui peningkatan kebutuhan energi yang ditunjukan peningkatan aktivitas Na-K-ATPase insang (Yamauchi et al. 1990). Walaupun demikian tidak semua ikan mempunyai kemampuan adaptasi yang sama terhadap kadar salinitas. Brett (1979) menyatakan bahwa ikan air tawar mempunyai kemampuan adaptasi terhadap kadar salinitas tertentu.
32 pada populasi, makanan, tingkatan trofik, energi matahari dan keadaan fisika-kimia lingkungan.
Effendi (1979) menerangkan bahwa Survival Rate atau SR adalah tingkat kelangsungan hidup. Nilai SR digunakan untuk menentukan peluang hidup ikan dalam waktu tertentu. Kelangsungan hidup adalah kemampuan organisme untuk bertahan hidup pada lingkungannya. Kelangsungan hidup organisme perairan ditentukan oleh kualitas perairannya. Ikan merupakan organisme yang mempunyai kisaran kualitas air tertentu dan toleransi yang berbeda-beda untuk melangsungkan aktivitas kehidupanya dengan baik. Salinitas adalah salah satu faktor lingkungan yang berpengaruh terhadap kelangsungan hidup ikan budidaya. Pada umumnya ikan dapat hidup dan beradaptasi pada berbagai salinitas atau pH serta berbagai faktor lingkungan lainya (Usman 1993).
Kadar Lemak Tubuh Ikan
Indikator kualitas ikan dapat dilihat dari komposisi kimiawi tubuh. Kualitas ikan yang dibudidayakan dipengaruhi oleh dua faktor utama yaitu lingkungan dan komposisi pakan (Goddard 1996). Diantara komponen nutrisi yang paling berperan terhadap kualitas rasa, aroma dan tekstur salah satunya adalah kadar lemak.
33
Histopathologi Organ Ikan
Pada organisme akuatik seperti ikan terdapat beberapa organ yang berperan dalam proses osmoregulasi yaitu insang, ginjal dan usus (Alvarellos et al. 2003). Sedangkan menurut Affandi dan Tang (2002), selain organ insang, ginjal dan usus organ kulit juga berperan dalam proses tersebut.
Insang berfungsi sebagai alat pernapasan tetapi dapat pula berfungsi sebagai alat ekskresi garam-garam, penyaring makanan, alat pertukaran ion dan osmoregulator. Pada hampir semua ikan, insang merupakan komponen penting dalam pertukaran gas. Insang terbentuk dari lengkungan tulang rawan yang mengeras, dengan beberapa filamen insang di dalamnya. Tiap-tiap filamen insang terdiri atas banyak lamella yang merupakan tempat pertukaran gas. Tugas ini ditunjang oleh struktur lamella yang tersusun atas sel-sel tiang sebagai penyangga pada bagian dalam. Pinggiran lamella yang tidak menempel pada lengkung insang sangat tipis, ditutupi oleh epithelium dan mengandung jaringan pembuluh darah kapiler. Jumlah dan ukuran lamella sangat besar variasinya tergantung tingkah laku ikan (Fujaya 2004).
Menurut Evans (1987), insang merupakan tempat utama dalam proses pertukaran gas (respirasi), pengaturan ionik (ion transport), pengaturan keseimbangan asam basa dan pengeluaran produk buangan seperti ammonia. Selain itu juga insang berperan sebagai tempat pengambilan, biotransformasi pada ekskresi bahan-bahan logam berat yang bersifat toksit.
Pada insang terdapat sel klorida yang melakukan transport aktif. Sumber utama energi untuk transport aktif disediakan oleh mitokondria yang berhubungan dengan Na+ - K+ ATP yang terletak disepanjang basolateral dan pada system mikrotubular sel klorid yang secara ekstensif dan aktif melakukan transport Na+ keluar sel untuk bertukar dengan K+ ke dalam sel (Moyle dan Cech 2004).
34 negatif terhadap pertumbuhan. Munculnya kelainan atau kerusakan pada insang secara makroskopis ataupun mikroskopis bisa digunakan sebagai tanda peringatan terhadap tingkat kesehatan ikan (Camargo et al. 2007).
Beberapa informasi tetang perubahan histopathologi telah banyak dilakukan dan salah satunya adalah kajian tetang perubahan histopathologi karena stress lingkungan. Menurut Bonga dan Lock (1992) perubahan struktur pada insang yang disebabkan karena stress lingkungan yaitu terangkatnya sel epitel (epithelium lifting), nekrosis pada sel penyangga dan sel klorida, epitel yang menggembung (epitehelial swelling) yang disebabkan karena meningkatnya jarak interseluler, luruhnya sel epitel (Epithelium rupture) dan lamella yang bergabung (lamella Fusion). Kerusakan ini biasanya disertai juga dengan adanya hyperplasia, hipertropi serta infiltrasi sel leukosit pada branchial epithelium.
Hal yang sama juga diungkapkan oleh Heat (1987), bahwa beberapa bahan toksit dapat mengakibatkan perubahan pada struktur insang termasuk bahan-bahan kimiawi yang bersifat stressor. Lesion yang biasa ditemukan diantaranya adalah nekrosis, hyperplasia, inflamasi, terangkatnya sel epitel (epithelial lifting), sel yang mengembang (cell swelling) dan hipersekresi mukus.
35
METODOLOGI
PENELITIAN
Tempat dan Waktu
Penelitian ini dilaksanakan selama 3 (tiga) bulan yaitu pada bulan Februari - April 2012. Penelitian ini dilakukan di Laboratorium Lingkungan BDP, Fakultas Perikanan dan Ilmu Kelautan, IPB. Pengukuran kandungan Pb pada air dan organ ikan dilakukan di Laboratorium Pengujian Departemen Teknologi Industri Pertanian, IPB. Analisa kadar lemak daging dilakukan di Laboratorium Nutrisi Ikan Departemen Budidaya Perairan Fakultas Kelautan dan Perikanan, IPB. Pembuatan preparat histopathologi insang dan ginjal dilakukan di Bagian Patologi, Departemen Klinik, Reproduksi dan patologi, Fakultas Kedokteran Hewan, IPB.
Ikan Uji
Ikan uji yang digunakan adalah ikan nila (O. niloticus) yang berumur 2 bulan (panjang : ± 20 cm, berat : ± 195.33 gram) yang bersumber dari kolam budidaya Fakultas Perikanan dan Ilmu Kelautan, IPB. Pada tahap proses akumulasi, padat penebaran ikan uji sebanyak 28 ekor pada setiap akuarium yang berukuran 70 x 60 x 50 cm3 sebanyak 3 unit. Sedangkan pada akuarium pengamatan uji depurasi sebanyak 4 ekor pada setiap akuarium yang berukuran 50 x 40 x 30 cm3. Pakan yang diberikan untuk ikan adalah pakan ikan komersil berbentuk pelet terapung yang biasa digunakan oleh para pembudidaya ikan. Pemberian dilakukan sebanyak 3 kali sehari secara at satiation.
Metode Penelitian
36 melihat tingkat pengurangan Pb selama selang waktu tersebut. Masing-masing perlakuan memiliki tiga ulangan. Formulasi rancangan percobaan yaitu :
Faktor Perlakuan
A. Ikan yang dipelihara pada salinitas 0 ppt B. Ikan yang dipelihara pada salinitas 5 ppt C. Ikan yang dipelihara pada salinitas 10 ppt D. Ikan yang dipelihara pada salinitas 15 ppt E. Ikan yang dipelihara pada salinitas 20 ppt Waktu Pengamatan
A. Ikan yang di pelihara selama 0 jam B. Ikan yang di pelihara selama 60 jam C. Ikan yang di pelihara selama 120 jam
Prosedur Penelitian
Penelitian ini terdiri dari 2 tahap, yaitu bagian pertama berupa perlakuan akumulasi logam berat Pb dalam ikan dan bagian kedua berupa perlakuan depurasi logam berat Pb dalam tubuh ikan dengan menggunakan salinitas yang berbeda serta pengaruhnya terhadap tingkat konsumsi oksigen, kadar lemak, pertumbuhan, kelangsungan hidup dan histopathologi insang dan ginjal.
Tahap 1 Perlakuan Akumulasi Logam Berat Pb
37 Setelah menjalani proses aklimatisasi, sebanyak 150 liter air pada media pemeliharaan, diberikan Pb(NO3)2 yang mengandung konsentrasi awal logam berat Pb didalam air sebesar 2.36 mg/l. Proses pemeliharaan dilakukan selama 28 hari dan selama pemeliharaan ikan nila diberi pakan secara at satiation dengan frekuensi pemberian 3 kali sehari.
Selama percobaan berlangsung pergantian air juga dilakukan sebanyak 100% setiap 3 hari dan untuk menjaga konsentrasi bahan uji tetap tersedia untuk penyerapan maka pada saat dilakukan pergantian air lalu dilakukan pemberian Pb(No3)2 dengan konsentrasi yang sama pada awal percobaan. Untuk pengukuran logam berat Pb pada air dan daging ikan serta pengukuran peubah pertumbuhan, pengambilan sampel dilakukan sebelum aplikasi dan setiap minggu setelah aplikasi selama empat minggu. Begitu pula pada pengukuran kualitas air dilakukan setiap minggu untuk menilai kelayakan media pemeliharaan terhadap pertumbuhan dan kelangsungan hidup serta melihat kemungkinan pengaruh logam berat Pb. Parameter kualitas air meliputi suhu, pH, salinitas, oksigen terlarut dan alkalinitas.
Tahap 2. Perlakuan Depurasi Logam Berat Pb pada Air Bersalinitas
38 ke-60 dan jam ke-120. Untuk mendapatkan sampel daging guna pengukuran kandungan logam berat Pb, lemak dan histopathologi yaitu diambil 3 ekor setiap perlakuan dengan cara memotong bagian organ yang dibutuhkan (daging, insang dan ginjal) dan selanjutnya sampel dimasukan kedalam botol sampel untuk dianalisis.
Pada percobaan ini dilakukan pengukuran tingkat konsumsi oksigen pada kondisi metabolisme aktif. Pada setiap kali pengambilan sampel dilakukan juga penimbangan bobot tubuh setiap ikan. Selama percobaan berlangsung ikan diberi pakan berupa pelet yang diberikan dua kali per hari sebanyak 3 persen dari bobot ikan (Yunus et al. 1990). Jumlah pakan yang diberikan disesuaikan setiap hari yang didasarkan atas data penimbangan biomasa ikan. Sisa pakan dan kotoran dibersikan dari tempat percobaan dengan cara menyipon setiap saat sebelum pemebrian pakan.
Parameter Pengamatan
Tingkat Konsumsi Oksigen (TKO)
Tingkat konsumsi oksigen diukur pada awal penelitian dengan menghitung rasio oksigen terlarut pada awal dan akhir pengamatan. Tingkat konsumsi oksigen dilakukan pada kondisi ikan setelah diberi makan (metabolisme aktif) dengan menggunakan sistem tertutup (air diam). Pengukuran konsumsi oksigen dilakukan dengan cara menempatkan ikan masing-masing 2 ekor ke dalam akuarium (volume 30 liter air) dan bobot ikan sebelumnya ditimbang terlebih dahulu. Sebelum ikan ditempatkan ke dalam wadah percobaan, air terlebih dahulu diaerasi dengan kuat (bubling) sehingga kandungan oksigennya bertambah dan mencapai titik jenuh oksigen, kemudian dilakukan pengukuran oksigen terlarut sebagai DO awal. Ikan ditimbang kemudian dimasukan kedalam media respirasi dan ditutup selama 1 jam untuk dihitung DO akhir, maka akan didapatkan tingkat konsumsi oksigen dengan menggunakan rumus :
TKO =
WxT DO DO
39 dengan : TKO = tingkat konsumsi oksigen (mg O2/g/jam)
V = volume air dalam wadah (L)
DOto = konsentrasi oksigen terlarut pada awal pengamatan (mg/L) DOtt = konsentrasi oksigen terlarut pada waktu t (mg/L)
W = bobot ikan uji (g)
T = periode pengamatan (jam)
Kandungan Logam Berat Pb di Air dan di Daging Ikan
Analisa Pb dilakukan dengan menggunakan spektrofotometrik serapan atom (Atomic Asdorbent Spectrofotometric, AAS) yaitu prosedur spectroanalytical untuk penentuan kualitatif dari unsur-unsur kimia menggunakan penyerapan radiasi optic (cahaya) oleh atom bebas dalam bentuk gas. Prinsip analisanya menggunakan prinsip berdasarkan Hukum Lambert-Beert yaitu banyaknya sinar yang diserap berbanding lurus dengan kadar zat. Persamaan garis antara konsentrasi logam berat dengan absorbansi adalah persamaan linier dengan koefisien arah positif yaitu Y = a + bX. Dengan memasukkan nilai absorbansi larutan contoh ke persamaan garis larutan standar maka kadar logam berat contoh dapat diketahui. Larutan contoh yang mengandung ion logam dilewatkan melalui nyala udara-asetilen bersuhu 2000 0C sehingga terjadi penguapan dan sebagian tereduksi menjadi atom. Lampu katoda yang sangat kuat mengeluarkan energi pada panjang gelombang tertentu dan akan diserap oleh atom-atom logam berat yang sedang di analisis. Jumlah energi cahaya yang diserap atom logam berat pada panjang gelombang tertentu ini sebanding dengan jumlah zat yang diuapkan pada saat dilewatkan melalui nyala api udara-asetilen. Setiap unsur logam berat membutuhkan lampu katoda yang berbeda. Keseluruhan prosedur ini sangat sensitif dan selektif karena setiap unsur membutuhkan panjang gelombang yang sangat pasti (Tinsley 1979).
Kadar Lemak Ikan
40 disambungkan dengan tabung soxhlet. Selongsong lemak dimasukkan ke dalam ruang ekstraktor tabung soxhlet dan disiram dengan pelarut lemak. Tabung ekstraksi dipasang pada alat destilasi soxhlet lalu dipanaskan pada suhu 40 °C dengan menggunakan pemanas listrik selama 6 jam. Pelarut lemak yang ada dalam labu lemak didestilasi hingga semua pelarut lemak menguap. Pada saat destilasi pelarut akan tertampung di ruang ekstraktor, pelarut dikeluarkan sehingga tidak kembali ke labu lemak, selanjutnya labu lemak dikeringkan dalam oven pada suhu 105 °C, setelah itu labu didinginkan dalam desikator sampai beratnya konstan (W3)(OAC-I 1999). Kadar lemak ditentukan dengan rumus :
% Kadar lemak = W3 −W2 W1 × 100%
Keterangan : W1 = Berat sampel (gram)
W2 = Berat labu lemak tanpa lemak (gram) W3 = Berat labu lemak dengan lemak (gram)
Kelangsungan Hidup
Kelangsungan hidup dihitung dengan mengamati jumlah ikan nila yang dipelihara pada awal pengamatan dan jumlah ikan nila yang dipelihara pada akhir pengamatan. Penghitungan kelangsungan hidup pada ikan menggunakan rumus Effendie (1979) :
Keterangan : SR = Survival Rate (%)
Nt = Jumlah ikan pada akhir pengamatan (ekor) N0 = Jumlah ikan pada awal pengamatan (ekor)
Laju Pertumbuhan
Laju pertumbuhan menggunakan data yang diperoleh dengan mengambil ikan nila pada awal dan akhir percobaan dan ditimbang bobotnya. Laju pertumbuhan dihitung dengan menggunakan rumus Zooneveld et al. (1991) :
41 Keterangan : Wt = Bobot rata-rata ikan pada hari ke-t (gram)
Wo = Bobot rata-rata ikan pada hari ke-0 (gram) t = Waktu (hari)
α = Laju pertumbuhan spesifik (% berat badan/hari)
Uji Histopathologi
Pengamatan histopathologi dilakukan pengamatan dengan menggunakan metode mikroteknik, yaitu dengan cara membuat preparat histopathologi. Preparat histopathologi yang dibuat adalah insang dan ginjal ikan. Prosedur dalam pembuatan preparat histologist adalah Ikan dibedah dan diambil bagian insang dan ginjalnya, Kemudian diawetkan dengan formalin 4% selama 24 jam dan difiksasi dengan alcohol 70% selama 24 jam. Setelah itu dimasukan ke dalam alcohol 80%, 95%, absolute i dan ii, larutan alcohol : xylol (1:1), xylol:paraffin (1:1), paraffin I dan II 1 jam. Kemudian sampel ditanam dalam cetakan dan dibiarkan mengeras membentuk blok yang kemudian ditempel pada blok kayu (holder), lalu sampel dipotong dengan microtome dengan ketebalan 6-10 mikron. Potongan ditempel pada gelas objek yang sebelumnya telah diolesi dengan
glycerin albumin. Sampel dikeringkan pada incubator 40oC selama 24 jam lalu diwarnai dengan HE.
42
Pengukuran Kualitas Air
Pengukuran kualitas air terdiri salinitas, suhu, pH, DO dan alkalinitas. Pengukuran salinitas dilakukan setia hari dan pengaturan salinitas untuk mencapai nilai salinitas perlakuan dilakukan setiap 8 jam. Pengukuran suhu, pH, DO dan alkalinitas dilakukan setiap hari pada waktu pagi dan sore selama penelitian. Pengukuran ini bertujuan untuk mengetahui kualitas air sebelum dan sesudah menggunakan salinitas serta mengetahui kualitas air selama proses budidaya ikan nila.
Analisis Data
Data pengukuran konsentrasi logam berat Pb di air dan ikan, tingkat konsumsi oksigen, pertumbuhan bobot tubuh, kadar lemak dan kelangsungan hidup dianalisis dengan sidik ragam (ANOVA). Histopathologi insang dan ginjal dianalisis secara deskriptif. Hasil yang disajikan merupakan nilai rata-rata (±) dan standar deviasi (SD). Selanjutnya jika hasil pengujian keragaman dari parameter-parameter tersebut menunjukan perbedaan yang nyata, pengujian akan dilanjutkan dengan uji tukey (BNJ) untuk menguji perbedaan terkecil dari nilai tengah antara perlakuan. Dari data hasil penelitian ini akan dilihat pula pola hubungan antara salinitas dengan setiap parameter uji.
43
HASIL DAN PEMBAHASAN
Hasil
Akumulasi Logam Berat Pb
Konsentrasi awal logam berat di air pada awal perlakuan yang terukur dengan menggunakan spektrofotometer serapan atom (AAS) yaitu sebesar 2.36 mg/l.
Tabel 3 Pengaruh pemberian Pb dalam air terhadap peningkatan konsentrasi Pb dalam daging dan beberapa peubah pertumbuhan ikan.
Pengamatan
Pengamatan Minggu Ke - Nilai
Awal 1 2 3 4
Rata-rata Konsentrasi Pb dalam daging(mg/kg)
<0.030 0.96±0.69 1,73 ± 0.74 2,98±0.63 4,54 ±0.27 Rata-rata Kelangsungan
Hidup (%)
100 100 100 100 95
Rata-rata pertumbuhan bobot tubuh ikan (gr)
195.33± 2.05
9.67±1.35 20.45±2.16 35.55±1.38 47.88±1.67 Laju pertumbuhan bobot
rerata harian (%)
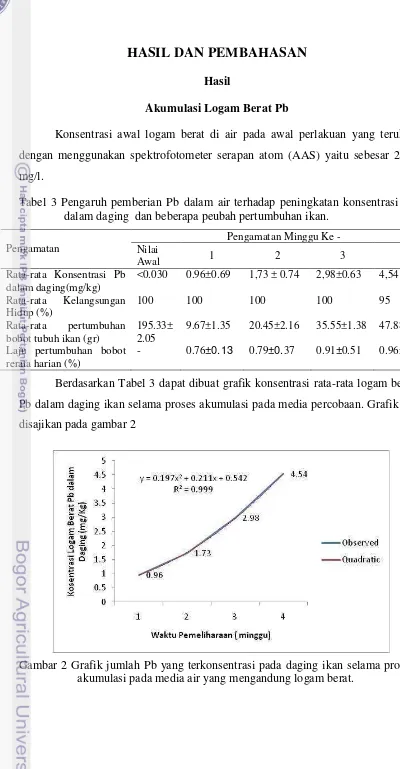
- 0.76±0.13 0.79±0.37 0.91±0.51 0.96±0.42 Berdasarkan Tabel 3 dapat dibuat grafik konsentrasi rata-rata logam berat Pb dalam daging ikan selama proses akumulasi pada media percobaan. Grafik ini disajikan pada gambar 2
[image:43.595.95.495.41.810.2]44 Dari Tabel 3 dan Gambar 2 terlihat adanya peningkatan terhadap konsentari Pb dalam daging ikan dengan semakin bertambahnya waktu pemeliharaan. Peningkatan yang diperoleh diakibatkan karena adanya pemberian logam berat Pb dalam air sebagai media pemeliharaan dan seiring bertambahnya waktu pemeliharaan. Dari hasil pengukuran kosentarsi Pb dalam daging bahwa laju akumulasi konsentrasi Pb dalam daging relatif cepat dan mengalami peningkatan setiap minggu selama empat minggu. pada minggu ke-1 konsentrasi Pb dalam daging ikan mencapai 0,96 mg/kg, pada minggu ke-2 yaitu 1,73 mg/kg, minggu ke-3 2,98 mg/kg sedangkan pada minggu ke-4 mencapai 4,54 mg/kg. Rata-rata tingkat akumulasi logam berat pada pengamatan memberikan respon kuadratik terhadap konsentrasi logam berat dalam air (gambar 2) dengan persamaan : Y= 0.197X2 + 0.211X + 0.524; R2 = 0.999
Selama tahap akumulasi bobot tubuh ikan mengalami peningkatan dari minggu pertama hingga minggu ke-empat. Pada minggu pertama kenaikan bobot tubuh ikan mencapai 9.67 gr dengan rata-rata pertumbuhan harian 0,76%. Sedangkan pada minggu ke-4 pertambahan bobot tubuh ikan hingga mencapai 47.88 gr dengan rata-rata pertumbuhan harian 0,96%. Adanya paparan timbal selama pemeliharaan tidak mempengaruhi tingkat pertumbuhan ikan nila terhadap penambahan berat bobot tubuh. Hal ini terjadi karena efesiensi ikan dalam pemanfaatan pakan tidak terganggu dan tidak menyebabkan terganggunya sistem metabolisme tubuh ikan nila merah, sehingga energi dari pakan dapat digunakan secara optimal untuk pertumbuhan.
45
Depurasi Logam Berat Pb dengan Air Bersalinitas
[image:45.595.103.498.88.806.2]Hasil konsentrasi Pb dalam daging ikan nila setelah proses depurasi secara umum mengalami penurunan yang disebabkan oleh perlakuan salinitas.
Tabel 4 Rata-rata konsentrasi Pb dalam daging ikan nila pada salinitas dan waktu pengamatan yang berebda.
Salinitas Media (ppt)
Konsentrasi Pb dalam daging ikan (mg/kg)
0 jam 60 jam 120 jam
0 4,54±0.12a 2,76±0.09a 1,84±0.06a 5 4,52±0.25a 2,64±0.64a 0,27±0.05b 10 4,53±0.25a 0,99±0.33b 0,14±0.13bc 15 4,50±0.24a 0,58±0.42bc 0,12±0.23bc 20 4,47±0.76a 0,46±0.55c 0.05±0.14c
Nilai ditunjukan sebagai rata-rata±standar deviasi dengan pengujian tiga kali ulangan. Huruf yang berbeda dalam satu baris menunjukan berbeda nyata (P> 0.05).
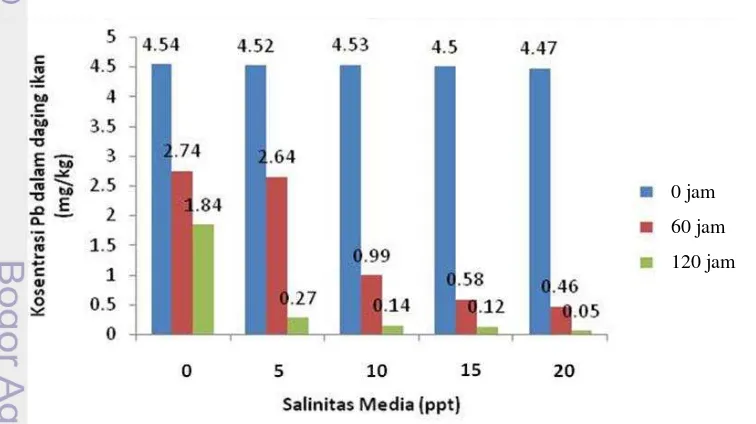
Berdasarkan Tabel 4 dapat dibuat grafik konsentrasi rata-rata logam berat Pb yang tersisa di daging oleh proses depurasi pada salinitas berbeda dan waktu pengamatan yang berebda. Grafik ini disajikan pada gambar 3
Gambar 3 Grafik konsentrasi rata-rata logam berat Pb dalam daging ikan nila pada salinitas dan waktu pengamatan yang berebda.
Pada Tabel 4 diketahui bahwa perlakuan salinitas untuk menurunkan logam berat Pb di daging ikan memiliki tingkat efektifitas yang tinggi. Perlakuan
0 jam
60 jam
[image:45.595.112.490.451.663.2]46 salinitas dapat mendepurasi logam berat pada daging dengan tingkat pengeluaran hingga mencapai ± 98%. Depurasi logam berat Pb oleh masing-masing perlakuan salinitas dan waktu pengamatan saling berbeda. Berdasarkan uji statistik pada didapatkan bahwa perlakuan salinitas dan waktu pengamatan berpengaruh terhadap depurasi logam berat Pb dalam daging ikan. Hal ini dapat terlihat pada perlakuan kontrol (0 ppt) berbeda nyata dengan perlakuan salinitas. perlakuan salinitas 20 ppt lebih baik dibandingkan dengan perlakuan salinitas 5 ppt, 10 ppt dan 15 ppt dalam mendepurasi logam berat Pb dalam daging. Depurasi pada perlakuan salinitas yang semakin tinggi seiring dengan lamanya waktu pemeliharaan. Semakin lama waktu pemeliharaan ada kecenderungan bahwa semakin banyak logam berat Pb yang keluar dari daging ikan. Pada setiap waktu depurasi dengan perlakuan salinitas menunjukan bahwa laju depurasi logam berat Pb dari tubuh ikan nila menunjukan bahwa terjadi penurunan konsentrasi yang semakin cepat dengan semakin tingginya salinitas.
Gambar 4 Persentase (%) konsentrasi Pb yang tersisa di daging ikan dengan salinitas yang berbeda pada akhir penelitian.
47 perlakuan salinitas 20 ppt yaitu 1.21%. Hal ini menunjukan bahwa dengan semakin meningkatnya salinitas maka proses depurasi logam berat pada tubuh ikan semakin meningkat.
Tingkat Konsumsi Oksigen (TKO)
Pengukuran konsumsi oksigen merupakan salah satu parameter fisiologi yang baik secara tidak langsung digunakan dalam menetukan laju metabolisme yaitu dengan menentukan oksgen yang digunakan dalam proses oksidasi dalam memperoleh energi yang akan digunakan untuk mempertahankan hidup (dalam hal ini termasuk osmoregulasi) dan pertumbuhan. Kebutuhan oksigen biologi didefenisikan sebagai banyaknya oksigen yang diperlukan oleh organisme pada saat pemecahan bahan organik, pada kondisi aerobik. Pemecahan bahan organik diartikan bahwa bahan organik ini digunakan oleh organisme sebagai bahan makanan dan energinya diperoleh dari proses oksidasi.
Tingkat konsumsi oksigen pada setiap perlakuan dan ulangan terdapat pada (tabel lampiran 8). Rata-rata tingkat konsumsi oksigen pada setiap perlakuan disajikan pada tabel 5 dan gambar 5
Tabel 5 Rata-rata tingkat konsumsi oksigen ikan nila pada salinitas yang berbeda
Salinitas (ppt) TKO (mgO2/g Ikan/jam) 0
5 10 15 20
0,28 + 0,05 0, 35 + 0,09
0,38 + 0,06 0,57 + 0,05 0,64 + 0,02
48 Gambar 5 Rata-rata tingkat konsumsi oksigen ikan nila pada salinitas yang
berbeda.
Tingkat konsumsi oksigen dapat dijadikan sebagai parameter untuk mengetahui laju metabolisme organisme air. Pada tabel 5 memperlihatkan bahwa tingkat konsumsi oksigen ikan nila terendah didapatkan pada salinitas 0 ppt (0,28 + 0,05 mgO2/g ikan/jam) dan tertinggi pada salinitas 20 ppt (0,64 + 0,02 mgO2/g ikan/jam). Rata-rata tingkat konsumsi oksigen pada perlakuan memberikan respon kuadratik terhadap peningkatan salinitas (gambar 5) dengan persamaan :
Y = 0.011X2 + 0.02X – 0.242: R2 = 0.958
[image:48.595.108.503.82.728.2]Perubahan Bobot Tubuh Ikan
Tabel 6 Rata-rata pertumbuhan harian (gr) ikan nila yang dipelihara pada salinitas yang berbeda.
Salinitas
(ppt) Bobot Awal
Perubahan Bobot Ikan (gr)
0 Jam 60 Jam 120 Jam
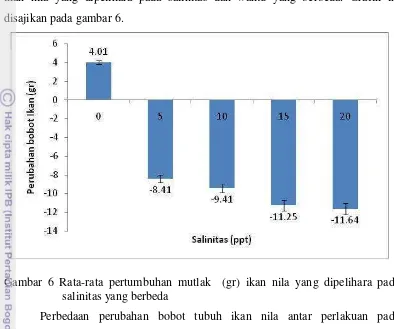
[image:48.595.113.476.83.329.2]49 Berdasarkan Tabel 6 dapat dibuat grafik rata-rata pertumbuhan mutlak (gr) ikan nila yang dipelihara pada salinitas dan waktu yang berbeda. Grafik ini disajikan pada gambar 6.
Gambar 6 Rata-rata pertumbuhan mutlak (gr) ikan nila yang dipelihara pada salinitas yang berbeda
Perbedaan perubahan bobot tubuh ikan nila antar perlakuan pada penelitian ini disebabkan oleh berbagai faktor. Salah satu faktor yang berhubungan dengan proses pertumbuhan ikan adalah penggunaan energi metabolisme. Payne et al. (1988) menyatakan bahwa beberapa faktor utama yang berhubungan dengan pengaruh salinitas terhadap perubahan bobot tubuh ikan salah satunya adalah energi metabolisme.
[image:49.595.110.504.115.444.2]50 media yang mempunyai salinitas yang tinggi maka kebutuhan energi untuk melakukan osmoregulasi semakin besar sehingga dapat mempengaruhi pertumbuhan.
Kadar Lemak Tubuh Ikan
[image:50.595.108.480.78.808.2]Komposisi kimiawi tubuh yang meliputi kadar lemak yang terkandung dalam tubuh ikan nila selama percobaan disajikan pada Tabel 7.
Tabel 7 Persentase (%) kadar lemak ikan nila (O. niloticus) yang dipelihara pada salinitas yang berbeda selama percobaan
Salinitas (ppt) Komposisi Lemak pada Daging Ikan (%) 0
5 10 15 20
12.53 8.88 7.97 7.90 7.36
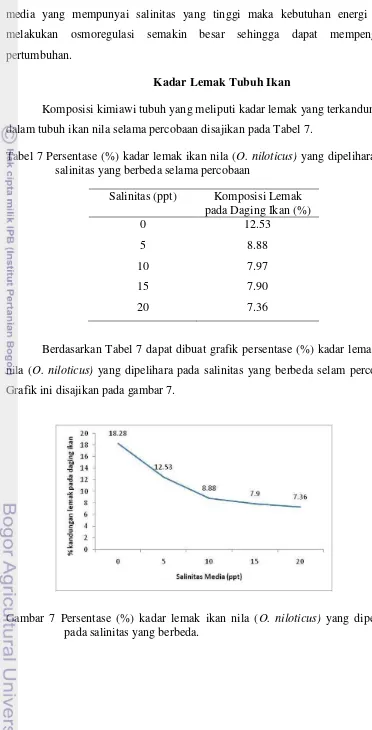
Berdasarkan Tabel 7 dapat dibuat grafik persentase (%) kadar lemak ikan nila (O. niloticus) yang dipelihara pada salinitas yang berbeda selam percobaan. Grafik ini disajikan pada gambar 7.
51 Tabel 7 di atas menunjukan bahwa kadar lemak pada tubuh ikan nila selama percobaan bervarisi. Kandungan lemak ikan kontrol lebih tinggi dibandingkan ikan perlakuan. Rendahnya kandungan lemak pada ikan perlakuan karena meningkatnya proses osmoregulasi. Mekanisme tersebut diduga melalui optimasi pemanfaatan lemak sebagai sumber energi untuk proses osmoregulasi. Selanjutnya, penurunan kadar lemak tubuh pada ikan perlakuan diduga berkaitan dengan aktivitas enzim lipase, sesuai yang dikemukakan oleh Irawati et al. (2012), bahwa kandungan lemak yang lebih rendah dibandingkan pada kontrol diduga meningkatnya proses katabolisme dalam tubuh untuk pemanfaatan energi terhadap perubahan kondisi lingkungan. Hal ini tersebut terlihat pertumbuhan pada perlakuan salinitas yang lebih rendah dibandingkan pada ikan pada kontrol.
Kadar lemak dalam tubuh ikan nila selama percobaan mengalami penurunan dengan semakin meningkatnya salinitas. Perubahan kandungan lemak dalam tubuh ikan akan mempengaruhi komposisi dan nilai asam lemak yang terkandung dalam tubuh ikan (Fitriani 2009).
Kelangsungan Hidup
Data kelangsungan hidup ikan nila yang diperoleh pada akhir penelitian, dapat dilihat pada tabel 8. Kelangsungan hidup tertinggi terjadi pada perlakuan 0 ppt, 5 ppt, dan 10 ppt yaitu 100% sedangkan nilai terendah terdapat pada perlakuan 20 ppt yaitu 83,3%. Kematian yang terjadi pada perlakuan 20 ppt diduga adanya kerusakan jaringan insang sehingga kemampuan insang menyerap oksigen berkurang dan ikan mengalami anemia dengan tingkat yang lebih akut. Tabel 8. Derajat kelangsungan hidup (%) ikan nila (O.niloticus) pada perlakuan
salinitas yang berbeda. Salinitas
(ppt)
SR (%)
0 Jam 60 jam 120
0 100 100 100
5 100 100 100
10 100 100 100
15 100 100 91.7
52 Berdasarkan data yang terdapat pada Tabel 8 di atas, terlihat bahwa derajat kelangsungan hidup ikan nila tertinggi dicapai pada salinitas media 0 ppt, 5 ppt dan 10 ppt yang mencapai 100%. Sedangkan pada salinitas 15 ppt dan 20 ppt masing-masing mencapai 91.7% dan 83.3%. Hal ini disebabkan karena ikan tidak mampu lagi megimbangi perubahan kondisi lingkungan dalam hal ini perubahan salinitas yang sangat tinggi dan juga karena pengaruh efek logam berat Pb pada saat proses akumulasi. Menurut Affandi dan Tang (2002) menyatakan bahwa ikan sebagai hewan yang hidup di air mempunyai kapasitas osmoregulasi baik melalui insang maupun kulit. Terganggunya proses osmoregulasi dapat disebabkan karena insang atau kulit menjadi lebih permeabel sehingga sulit dilalui air, akibatnya pengeluaran garam dari insang menjadi terhenti dan menyebabkan gagal ginjal dan akan menyebabkan ikan mati (Bonga 1992). Hal serupa dilaporkan oleh Holiday (1969) bahwa kemampuan ikan untuk bertahan pada media bersalinitas tergantung pada kemampuan untuk mengatur cairan tubuh sehingga mampu mempertahankan tingkat tekanan osmotik yang mendekati normal.
Analisis Histopathologi
Gambaran histopatologi organ ikan nila ini dapat dijadikan indikasi ada atau tidak adanya efek pemaparan logam berat pada saat uji akumulasi dan pemeliharaan pada media bersalinitas. Analisa histopathologi organ insang dan ginjal ikan akan dapat menunjukkan kerusakan jaringan yang beragam, sehingga dapat dijadikan indikasi terjadinya pemaparan logam berat maupun adanya perubahan salinitas yang menyebabkan struktur sel mengalami kerusakan.
Analisis Histopatologi Insang ikan Nila (O. niloticus)
53 insang ikan nila yakni mengalami degenerasi, deformasi, nekrosis dan hypertrophy seperti yang tercantum pada Tabel 9 dan Tabel 10 serta sebagai pembanding insang ikan normal dapat dilihat pada Gambar 8.
Tabel 9 Perubahan histopathologi insang ikan nila pada salinitas yang berbeda.
Salinitas (ppt)
Kerusakan Insang Keterangan
0 = Mineralisasi
= Deformasi sel-sel lamella
Degenerasi : lamella insang yang mengalami lisis atau hancur
Deformasi : susunan lamella yang tidak teratur
Nekrosis : kematian sel
Hypertrophi : pembesaran akibat suatu gangguan 5 = Mineralisasi
= Nekrosis 10
= Degenerasi sel-sel lamella = Deformasi sel-sel lamella 1