Lampiran 3. Perhitungan penetapan kadar betametason valerat Penetapan kadar betametason valerat menggunakan rumus:
Keterangan: As = Luas Area Larutan Standart Au = Luas area larutan uji
BWS = Bobot betametason valerat yang ditimbang (mg) KWS = Kadar betametason valerat (%)
Bu = Bobot sampel yang ditimbang (mg)
1/1000 = Kandungan betametason valerat krim betametason 50/5 x 100 = Faktor pengenceran larutan standart
100 = Faktor Pengenceran larutan uji
Diketahui :
Lampiran 3. (Lanjutan)
Lampiran 4. Alat yang digunakan
Alat Neraca analitik
DAFTAR PUSTAKA
Anief, M. (2000). Ilmu Meracik Obat. Yogyakarta: Gadjah Mada University Press. Hal. 72–73.
Direktorat Jendral Pengawasan Obat dan Makanan. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan R.I . Hal. 1009.
Direktorat Jendral Pengawasan Obat dan Makanan. (2014). Farmakope Indonesia. Edisi Kelima. Jakarta: Departemen Kesehatan R.I . Hal. 51, 240-241. Gandjar, I. B., dan Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta:
Pustaka Pelajar. Hal. 378-385.
Johnson, E.L., dan Stevenson, R. (1991). Dasar Kromatografi Cair. Penerjemah: Kosasih Padmawinata. Bandung: Penerbit ITB. Hal. 7-10.
Katzung, B. G. (2004). Farmakologi Dasar dan Klinik. Edisi Kedelapan. Penerjemah: Dripa Sjabana, dkk. Jakarta: Salemba Medika. Hal. 525. Neal, M. J. (2006). At a Glance Farmakologi Medis. Edisi Kelima. Jakarta:
Erlangga. Hal. 71, 72.
Putra, E. D. L. (2004). Kromatografi Cair Kinerja Tinggi dalam Bidang Farmasi. Medan : Fakultas FMIPA Universitas Sumatera Utara. Hal. 5-10. http://library.usu.ac.id/download/fmipa/farmasi-effendy2.pdf diakses pada tanggal 29 Maret 2016.
Rohman, A. (2009). Kromatografi untuk analisis obat. Yogyakarta: Graha Ilmu. Hal. 111-115.
Sartono. (1996). Apa Yang Sebaiknya Anda Ketahui Tentang Obat Wajib Apotek. Jakarta : Gramedia Pustaka Utama. Hal. 88-89, 94
Schunack, W., Mayer, K., Haake, M.(1990). Senyawa Obat. Penerjemah: Joke R. W. dan Sriewoelan S. Yogyakarta: UGM Press. Hal 521.
Suherman, A. K. dan Ascorbat, P. (2007). Farmakologi dan Terapi. Edisi kelima. Jakarta : Gaya Baru. Hal. 500, 506.
Tjay, T.H., dan Rahardja, K. (2007). Obat-Obat Penting. Edisi Keenam Cetakan Pertama. Jakarta: Penerbit PT Elex Media Komputindo Kelompok Gramedia. Hal. 730, 734.
BAB III
METODE PENGUJIAN
3.1 Waktu dan Tempat Pelaksanaan
Penetapan kadar ini dilakukan pada tanggal 15 Februari – 26 Februari 2016 di Ruang instrumen bagian Quality Control yang terdapat di PT. Kimia Farma (Persero) Tbk. Plant Medan yang beralamat di Jalan Sisingamangaraja XII Km. 9 No. 59, Medan.
3.2 Alat-alat
Alat–alat yang digunakan adalah batang pengaduk, beaker glass (Pyrex ukuran 25 mL, 1000 mL), bola karet, botol vial, corong, gelas ukur (Pyrex ukuran 5 mL, 50 mL, 1000mL), pipet volum (Pyrex ukuran 5 mL), labu tentukur (Pyrex ukuran 50 mL, 100 mL), membran filter (Phenex NY 0,45 μm), neraca analitik (Digital semi micro balance), pipet tetes, spuit (1 mL, 30 mL), ultrasonic bath, dan unit peralatan kromatografi cair kinerja tinggi (Waters) yang terdiri dari detektor Ultraviolet sinar tampak, kolom bondapack C18 (3,9 x 300 mm), penyuntik mikroliter, pompa, wadah fase gerak dan wadah buangan.
3.3 Bahan–bahan
3.4 Prosedur Pengujian 3.4.1 Pengambilan Sampel
Diambil 10 gram krim betametason 0,1% dalam bentuk produk ruahan (PT. Kimia Farma (Persero) Tbk. Plant Medan), ditimbang seksama lebih kurang 2 gram sebanyak dua kali.
3.4.2 Larutan fase gerak
Fase gerak: asetonitril–akuabides ( 3 : 2 ), yaitu dengan asetonitril 600 mL dan fase gerak 400 mL dimasukkan dalam gelas beaker lalu saring dan bebas gaskan dengan alat penyaring fase gerak.
3.4.3 Pembuatan pelarut
Dicampur larutan metanol 1000 mL dengan 1 mL asam asetat glacial kedalam botol pelarut.
3.4.4 Pembuatan Larutan Standart
Ditimbang seksama lebih kurang 20 mg betametason valerat, kemudian dimasukkan ke dalam labu tentukur 100 mL dan diencerkan dengan larutan asam asetat glacial - metanol (1 dalam 1000), sampai tanda. Dipipet 5 mL masukkan dalam labu 50 mL, ditambahkan ±30 mL larutan asam asetat glacial - metanol (1 dalam 1000), diletakkan di ultrasonic bath selama 15 menit lalu ditambahkan larutan asam asetat glacial - metanol sampai garis tanda, disaring dengan membran filter 0,45 µm dan masukkan ke dalam botol vial.
3.4.5 Pembuatan Larutan Sampel
asetat glacial - metanol, lalu dimasukkan ke dalam labu tentukur 100 mL, gelas beaker dibilas dengan ±10 mL asam asetat glacial - metanol dan dimasukkan ke dalam labu tentukur 100 mL tersebut, lalu dilarutkan di ultrasonic bath selama 15 menit lalu ditambahkan larutan asam asetat glacial - metanol sampai garis tanda, disaring dengan filter 0,45 µm dan masukkan ke dalam botol vial.
3.4.6 Pengukuran
Larutan standar dan larutan uji diukur dengan kromatografi cair kinerja tinggi dengan parameter yaitu fase gerak: asetonitril – akuabides (3 : 2), fase diam: kolom bondapack C18 ( 3,9 x 300 mm ), dengan panjang gelombang: 254 nm, laju alir: 1,5 mL/menit dan volume injeksi: 20 µL.
3.4.7 Cara Kerja Penetapan Kadar
Tahapan kerja penetapan kadar yang dilakukan adalah sebagai berikut : 1. Dihidupkan komputer
2. Dihidupkan power detector 2489 dan Pompa 1525
3. Di detektor sampai muncul tampilan panjang gelombang 254 nm
4. Dibuka kran pada pump 1525 ke arah kanan, kemudian lakukan purging,
set laju alir 5 mL/menit. Lakukan purging selama 5 menit. Setelah selesai tutup krannya.
5. Diatur laju alir 1,5 mL/menit dan komposisi fase gerak yaitu asetonitril-akuabides (3 : 2).
6. Kemudian dilakukan conditioning selama 20 menit.
8. Dipilih inject only selected lines untuk inject run time, dan tampilkan kromatogram mentah.
9. Diinjeksikan larutan standart, setelah peak muncul kemudian diatur setting run time misalkan 7 menit
10.Kemudian set run time produk
11.Ditunggu sampai pada layar monitor tertulis waiting for injection maka sampel/standar siap diinjeksikan.
12.Dilakukan injeksi larutan standart sebanyak 6 kali. 13.Kemudian injeksikan larutan uji sebanyak 2 kali
14.Kadar betametason valerat dalam krim betametason dapat dihitung dengan menggunakan rumus di bawah ini:
Ket : As = Luas area larutan standar Au = Luas area larutan uji
BWS = Bobot betametason valerat yang ditimbang (mg) KWS = Kadar betametason valerat (%)
Bu = Bobot sampel yang ditimbang (mg)
1/1000 = Kandungan betametason valerat pada krim 50/5 x 100 = Faktor pengenceran larutan standar
100 = Faktor pengenceran larutan uji
Perhitungan kadar betametason valerat dapat dilihat pada Lampiran 3 halaman 24-25.
3.5 Persyaratan
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil
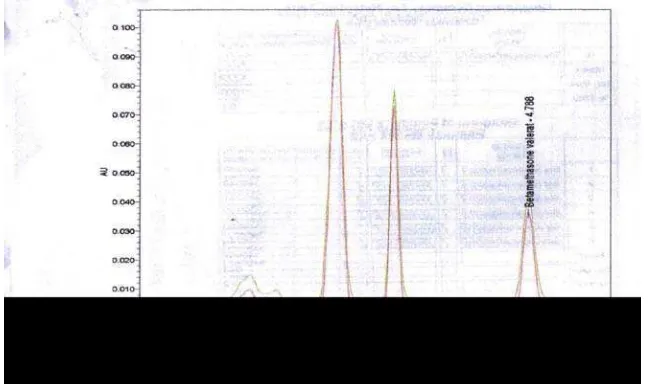
Kromatogram sampel uji betametason valerat dapat dilihat pada Gambar 4.1 dan data hasil penetapan kadar betametason valerat pada produk ruahan krim betametason 0,1% dapat dilihat pada Tabel 4.1. Kromatogram standart betametason valerat dan kromatogram sampel uji betametason valerat masing-masing dapat dilihat pada Lampiran 1 dan Lampiran 2.
Gambar 4.1 Kromatogram sampel uji betametason valerat
Tabel 4.1 Data hasil penetapan kadar betametason valerat pada produk ruahan krim betametason 0,1%
Keterangan : Au = Area uji, As = Area standart
No. Batch Au As Kadar (%) Persyaratan (%) M51367T (a) 373898 345967 107,55 90,00 - 110,00 M51367T (b) 373994 345967 107,58 90,00 - 110,00
4.2 Pembahasan
Hasil dari pengujian kadar betametason valerat pada produk ruahan krim betametason 0,1% dengan nomor batch M15367T yang dilakukan secara kromatografi cair kinerja tinggi dengan fase gerak asetonitril-akuabides (3:2), fase diam kolom bondapack C18 (3,9 mm x 300 mm), panjang gelombang 254 nm, laju alir 1,50 mL/menit dan volume injeksi 20 µL. Area uji betametason valerat (a) dan area uji betametason valerat (b) masing-masing diperoleh 373898 dan 373994 serta area standar betametason valerat 345967 yang merupakan rata-rata dari area standart betametason valerat. Hasil kadar betametason valerat (a) dan betametason valerat (b) masing-masing sebesar 107,55 % dan 107,58 %.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Penetapan kadar betametason valerat pada produk ruahan krim betametason 0,1% yang diproduksi PT Kimia Farma (Persero) Tbk. Plant Medan yaitu 107,56%. Hasil yang didapatkan memenuhi persyaratan yang tertera pada Farmakope Indonesia Edisi ke-V, yaitu tidak kurang dari 90,00% dan tidak lebih dari 110,00% dari jumlah yang tertera pada etiket.
5.2 Saran
BAB II
TINJAUAN PUSTAKA 2.1 Betametason
Menurut Neal (2006), Betametason berada di dalam tubuh manusia, dimana korteks adrenal melepaskan beberapa hormon steroid ke dalam sirkulasi. Hormon tersebut dibagi berdasarkan kerjanya menjadi dua kelas yaitu:
a) Mineralokortikoid, terutama aldosteron pada manusia, mempunyai aktivitas menahan garam dan disintesis dalam sel-sel zona glomerulosa. Termasuk hormon dari mineralokortikoid adalah aldosteron dan fludrokortison.
b) Glukokortikoid, terutama kortisol (hidrokotison) pada manusia, mempengaruhi metabolisme karbohidrat dan protein, tetapi juga mempunyai aktivitas mineralokortikoid yang bermakna. Hormon ini disintesis dalam sel-sel zona fasikulata dan zona retikularis. Termasuk hormon pada glukokortikoid adalah hidrokortison (kortisol) sedangkan hormon yang disintesis yaitu prednisolon, betametason, dan deksametason. Secara topikal betametason tidak terlalu aktif, tetapi dengan mengikat 5 rantai atom karbon valerat pada posisi hidroksil-17 menghasilkan suatu senyawa yang 300 kali lebih aktif dibandingkan dengan hidrokortison untuk pemakaian topikal (Katzung, 2004).
(prugio). Tidak jarang gangguan ekzem segera kambuh lagi, terutama bila digunakan fluorkortikoida dengan khasiat kuat (Tjay dan Rahadja, 2007).
2.1.1 Sifat Fisika dan Kimia
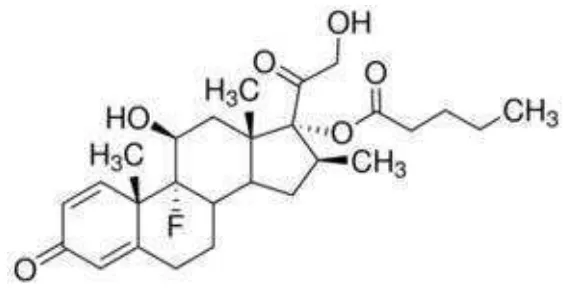
Betametason adalah stereoisomer dari deksametason, dimana gugus-metil pada C16 berada pada posisi-beta. Struktur betametason valerat dapat dilihat pada gambar dibawah ini:
Gambar 2.1 Struktur betametason valerat
Rumus Molekul : C22H37FO6 Berat Molekul : 476,58
Nama Kimia : 9-Fluoro-11β,17,21-trihidroksi-16β-metilpregna-1,4 diena- 3,20-dion 17-valerat.
Pemerian : Serbuk, putih sampai praktis putih, tidak berbau. Melebur pada suhu lebih kurang 190o disertai penguraian.
2.1.2 Farmakologi Betametason Mekanisme kerja :
Kortikosteroid bekerja dengan mempengaruhi kecepatan sintesis protein. Molekul hormon memasuki sel melewati membran plasma secara difusi pasif. Reseptor protein yang spesifik dalam sitoplasma sel hanya bereaksi di jaringan target hormon ini dan membentuk kompleks reseptor-steroid. Kompleks ini mengalami perubahan konformasi, lalu bergerak menuju nukleus dan berikatan dengan kromatin. Ikatan ini menstimulasi transkripsi asam ribonukleat (ribonucleic acid, RNA) dan sintesis protein spesifik. Induksi sintesis protein ini yang menghasilkan efek fisiologi steroid (Suherman dan Ascobat, 2007).
Farmakokinetik : Betametason secara topikal dapat diabsorpsi melalui kulit. Penggunaan jangka panjang atau pada daerah kulit yang luas dapat menyebabkan efek sistemik, antara lain mempunyai kemampuan untuk supresi (menekan) korteks adrenal (Suherman dan Ascobat, 2007).
Indikasi : alergi dan peradangan lokal
Kontraindikasi : Infeksi bakteri, fungi, dan penyakit kulit yang disebabkan oleh virus. Selain itu, penderita acne rosacea, dan perioral dermatitis (Sartono, 1996)
Efek samping : Atropi lokal, gatal-gatal, hipopigmentasi, perioral dan alergi dermatitis, serta infeksi sekunder (Sartono, 1996). 2.2 Krim
secara tradisisonal telah digunakan untuk sediaan setengah padat yang mempunyai konsistensi relatif cair diformulasi sebagai emulsi air dalam minyak atau minyak dalam air. Sekarang ini batas tersebut lebih diarahkan untuk produk yang terdiri dari emulsi minyak dalam air atau dispersi mikrokristal asam-asam lemak atau alkohol berantai panjang dalam air, yang dapat dicuci dengan air dan lebih ditujukan untuk penggunaan kosmetika dan estetika. Krim dapat digunakan untuk pemberian obat melalui vaginal (Ditjen POM, 2014).
Sebagai obat luar, krim harus memenuhi beberapa persyaratan berikut: a) Stabil selama masih dipakai untuk pengobatan, krim harus bebas dari
inkompatibilitas, stabil pada suhu kamar, dan kelembaban yang ada di dalam suhu kamar.
b) Lunak, semua zat dalam keadaan halus dan seluruh produk menjadi lunak serta homogen.
c) Mudah dipakai, krim tipe emulsi adalah yang paling mudah dipakai dan dihilangkan dari kulit.
d) Terdistribusi secara merata, obat harus terdispersi merata melalui dasar krim padat atau cair pada penggunaan (Widodo, 2013).
2.2.1 Penggolongan Krim
Untuk penstabilan krim ditambah zat antioksidan dan zat pengawet. Zat pengawet yang sering digunakan ialah nipagin 0,12% - 0,18%, nipasol 0,02% - 0,05% (Anief, 2000).
2.3 Uji Kualitatif dan Kuantitatif Betametason 2.3.1 Uji Kualitatif Betametason
a) Identifikasi dengan Kromatografi Lapis Tipis
Menurut Farmakope Indonesia edisi V (2010), uji kualitatif betametason menggunakan metode kromatografi lapis tipis dilakukan dengan ditotolkan masing-masing 10 µL larutan etanol mutlak yang mengandung (1) zat uji 0,5 mg per mL dan (2) Betametason BPFI 0,5 mg per mL pada jarak yang sama, 2,5 cm dari tepi lempeng kromatografi silika gel setebal 0,25 mm. masukkan lempeng ke dalam bejana kromatografi yang telah dijenuhkan dengan fase gerak campuran kloroform-dietilamina (2:1) dan dibiarkan fase gerak merambat hingga lebih kurang tiga per empat tinggi lempeng. Angkat lempeng, biarkan fase gerak menguap, semprot lempeng dengan larutan asam sulfat (1 dalam 2) dan panaskan di atas lempeng pemanas atau di bawah lampu hingga bercak tampak.
b) Identifikasi dengan reaksi Porter-Silber
2.3.2 Uji Kuantitatif Betametason
Uji kuantitatif betametason dapat dilakukan dengan menggunakan metode Kromatografi Cair Kinerja Tinggi (KCKT). Pemeriksaan betametason valerat secara kromatografi cair kinerja tinggi dilengkapi dengan detektor 254 nm, menggunakan fase diam: kolom 4 mm x 30 cm bahan pengisi L1, fase gerak: asetonitril - air (3:2), dan pelarut: asam asetat glacial - metanol (1:1000) (Ditjen POM, 1995).
2.4 Kromatografi Cair Kinerja Tinggi
Kemajuan dalam teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sensitif telah menyebabkan perubahan kromatografi kolom cair menjadi suatu sistem pemisahan dengan kecepatan dan efisiensi yang tinggi. Metode ini dikenal sebagai kromatografi cair kinerja tinggi (Ditjen POM, 1995).
Kromatografi merupakan suatu proses pemisahan yang mana analit-analit dalam sampel terdistribusi antara dua fase, yaitu fase diam dan fase gerak. Fase diam dapat berupa bahan padat atau porus dalam bentuk molekul kecil, atau dalam bentuk cairan yang dilapiskan pada pendukung padat atau dilapiskan pada dinding kolom. Fase gerak dapat berupa gas atau cairan (Rohman, 2009).
senyawa organik makromolekul. Untuk analisis dan pemisahan obat / bahan obat campuran rasemis optis aktif dikembangkan suatu fase pemisahan kiral (chirale Trenphasen) yang mampu menentukan rasemis dan isomer aktif (Putra, 2004).
Kromatografi cair kinerja tinggi (High Performance Liquid Chromatography, HPLC) dikembangkan pada akhir tahun 1960-an dan awal tahun 1970-an. Saat ini, kromatografi cair kinerja tinggi merupakan teknik pemisahan yang diterima secara luas untuk analisis bahan obat, baik dalam produk ruahan atau dalam sediaan farmasetik, serta obat dalam cairan biologis (Rohman, 2009).
2.4.1 Keuntungan Kromatografi Cair Kinerja Tinggi
Kromatografi cair kinerja tinggi mempunyai banyak keuntungan jika dibandingan dengan kromatografi cair (KC) tradisional yaitu: cepat, daya pisahnya baik, peka, detektor unik, kolom dapat dipakai kembali, ideal untuk molekul besar dan ion dan mudah memperoleh kembali cuplikan (Johnson dan Robert, 1991).
2.4.2 Kerugian Kromatografi Cair Kinerja Tinggi
Kerugian dari kromatografi cair kinerja tinggi adalah mahal, sampel yang digunakan hanya sedikit dan perlu tenaga ahli untuk mengoperasikannya.
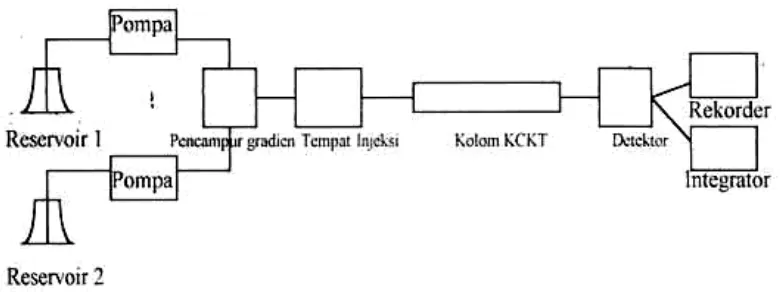
2.4.3 Instrumentasi Kromatografi Cair Kinerja Tinggi
Gambar 2.2 Komponen kromatografi cair kinerja tinggi 1. Wadah Fase Gerak pada Kromatografi Cair Kinerja Tinggi
Wadah fase gerak harus bersih dan lembam (inert). Wadah pelarut kosong ataupun labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini biasanya dapat menampung fase gerak antara 1 sampai 2 liter pelarut. Fase gerak sebelum digunakan harus dilakukan penghilangan gas (degassing) yang ada pada fase gerak, sebab adanya gas akan berkumpul dengan komponen lain terutama dipompa dan detektor sehingga akan mengacaukan analisis (Rohman, 2009). 2. Fase Gerak
3. Pompa
Pompa yang digunakan sebaiknya mampu memberikan tekanan sampai 5000 Psi dan mampu mengalirkan fase gerak dengan kecepatan alir 3 mL/menit. Tujuan penggunaan pompa atau sistem penghantaran fase gerak adalah untuk menjamin proses penghantaran fase gerak berlangsung secara tepat, reproduksibel, konstan, dan bebas dari gangguan (Gandjar dan Rohman, 2007). 4. Injektor
Sampel-sampel cair dan larutan disuntikkan secara langsung ke dalam fase gerak yang mengalir di bawah tekanan menuju kolom menggunakan alat penyuntik yang terbuat dari tembaga tahan karat dan katup teflon yang dilengkapi dengan keluk sampel (sample loop) internal atau eksternal (Gandjar dan Rohman, 2007).
5. Kolom
Kolom merupakan bagian kromatografi cair kinerja tinggi yang mana terdapat fase diam untuk berlangsungnya proses pemisahan solute / analit. Ada dua jenis kolom pada kromatografi cair kinerja tinggi yaitu kolom konvensional dan kolom mikrobor. Kolom mikrobor mempunyai tiga keuntungan yang utama dibandingkan dengan kolom konvensional.
a) Konsumsi fase gerak kolom mikrobor hanya 80% atau lebih kecil dibanding dengan kolom konvensional karena pada kolom mikrobor kecepatan alir fase gerak lebih lambat (10-100 µL/menit).
c) Sensitivitas kolom mikrobor ditingkatkan karena solute lebih peka, karenanya jenis kolom ini sangat bermanfaat jika jumlah sampel terbatas misal sampel klinis ( Gandjar dan Rohman, 2007).
6. Fase diam
Kebanyakan fase diam pada kromatografi cair kinerja tinggi berupa silica yang dimodifikasi secara kimiawi, silika yang tidak dimodifikasi, atau polimer-polimer stiren dan divinil benzene. Permukaan silika adalah polar dan sedikit asam karena adanya residu gugus silanol (Si-OH) (Gandjar dan Rohman, 2007).
Oktadesil silika (C18) merupakan fase diam yang paling banyak digunakan karena mampu memisahkan senyawa-senyawa dengan kepolaran yang rendah, sedang, maupun tinggi. Oktil atau rantai alkil yang lebih pendek lagi lebih sesuai untuk solute yang polar. Silika-silika aminopropil dan sianopropil (nitril) lebih cocok sebagai pengganti silika yang tidak dimodifikasi (Rohman, 2009).
7. Detektor
Detektor diperlukan untuk mengindera adanya komponen cuplikan di dalam efluen kolom dan mengukur jumlahnya. Detektor yang baik sangat peka, tidak banyak berderau, rentang tanggapan liniernya lebar, dan menanggapi semua jenis senyawa (Johnson dan Robert, 1991).
BAB I PENDAHULUAN 1.1 Latar Belakang
PT. Kimia Farma (Persero) Tbk. Plant Medan, Sumatera Utara, dikhususkan untuk memasok kebutuhan obat di wilayah Sumatera serta memproduksi beberapa obat. Produk yang diproduksi oleh pabrik yang telah memperoleh sertifikat Cara Pembuatan Obat yang Baik (CPOB) ini meliputi sediaan tablet, krim dan kapsul dengan menerapkan sistem manajemen mutu ISO-9001:2008.
Salah satu dari obat yang diproduksi oleh PT. Kimia Farma (Persero) Tbk. Plant Medan adalah Krim Betametason 0,1%. Dalam proses produksi krim betametason 0,1% dilakukan pengawasan mutu dari bahan baku sampai obat jadi. Dari beberapa proses tersebut salah satunya adalah pengawasan selama proses produksi. Pengawasan ini untuk memantau hasil dari proses produksi yang mungkin menjadi penyebab variasi karakteristik produk selama proses berjalan. Pada pembuatan krim betametason 0,1% dilakukan pengawasan selama proses produksi dalam produk ruahan untuk menjamin mutu obat. Salah satunya dengan parameter penetapan kadar zat aktif dari krim betametason 0,1% tersebut.
Ruahan Krim Betametason 0,1% menggunakan Metode Kromatografi Cair Kinerja Tinggi”.
1.2 Tujuan dan Manfaat 1.2.1 Tujuan
Untuk mengetahui kadar betametason valerat pada produk ruahan krim betametason 0,1% yang diproduksi oleh PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi syarat atau tidak.
1.2.2 Manfaat
PENETAPAN KADAR ZAT AKTIF BETAMETASON VALERAT PADA PRODUK RUAHAN KRIM BETAMETASON 0,1% MENGGUNAKAN
METODE KROMATOGRAFI CAIR KINERJA TINGGI ABSTRAK
Dalam produksi obat dilakukan pengawasan selama produksi (in process control). Pada pembuatan krim betametason 0,1% dilakukan pengawasan selama produksi dalam produk ruahan untuk menjamin mutu obat. Salah satunya dengan parameter penetapan kadar zat aktif dari krim betametason 0,1% tersebut. Tujuan dari penetapan kadar zat aktif pada produk ruahan krim betametason 0,1% adalah untuk mengetahui apakah kadar zat aktif obat telah memenuhi persyaratan yang tertera pada monografi Farmakope Indonesi Edisi V 2014.
Dalam penulisan tugas akhir ini, penetapan kadar betametason valerat pada produk ruahan krim betametason 0,1% dengan menggunakan metode kromatografi yaitu kromatografi cair kinerja tinggi. Dilakukan pada detector ultraviolet sinar tampak dengan panjang gelombang 254 nm, fase gerak yang digunakan adalah asetonitril–akuabides ( 3 : 2 ),fase diam yang digunakan adalah kolom bondapack C18 (3,9 × 300 mm) dan laju alir (flow rate) 1,50 mL/menit serta volume penyuntikan 20 µL.
Hasil yang diperoleh dari penetapan kadar betametason valerat pada produk ruahan krim betametason 0,1% menggunakan metode kromatografi cair kinerja tinggi yaitu 107,56% pada No. Batch M51367T, kadar tersebut memenuhi persyaratan Farmakope Indonesia Edisi V 2014 yaitu betametason valerat, C27H37FO6, tidak kurang dari 90,00% dan tidak lebih dari 110,00% dari jumlah yang tertera pada etiket.
PENETAPAN KADAR ZAT AKTIF BETAMETASON
VALERAT PADA PRODUK RUAHAN KRIM
BETAMETASON 0,1% MENGGUNAKAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI
TUGAS AKHIR
OLEH:
NURUL INDAH ASTUTI NIM 132410052
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR Bismillahirrahmannirrahim
Dengan mengucapkan Puji Syukur kehadirat Allah SWT atas segala limpahan rahmat dan karunia-Nya yang telah memberikan pengetahuan, kesehatan serta kesempatan kepada penulis sehingga penulis dapat menyelesaikan tugas akhir yang berjudul “Penetapan Kadar Zat Aktif Betametason Valerat pada Produk Ruahan Krim Betametason 0,1% menggunakan Metode Kromatografi Cair Kinerja Tinggi”. Tugas Akhir ini disusun untuk memenuhi salah satu syarat untuk menyelesaikan Program Studi Diploma III Analis Farmasi dan Makanan di Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak, penulis tidak akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya. Untuk itu penulis mengucapkan terima kasih sebesar-besarnya kepada:
1. Ibu Dr. Masfria, M.S., Apt., sebagai Dekan Fakultas Farmasi Universitas Sumatera Utara.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., sebagai Ketua Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara.
3. Bapak Drs. Nahitma Ginting M.Si., Apt., sebagai Dosen Pembimbing yang telah membimbing dan mengarahkan penulis dalam pembuatan tugas akhir ini.
5. Bapak Drs. Beben Budiman, Apt., sebagai Plant Manager PT. Kimia Farma (Persero) Tbk. Plant Medan.
6. Bapak Drs. Zulfadli, Apt., sebagai Asisten Manager PT. Kimia Farma (Persero) Tbk. Plant Medan yang telah memberikan bimbingan dan pengarahan kepada penulis selama melaksanakan praktek lapangan kerja. 7. Bapak Rahmat Rasyidi, S.Farm., Apt., sebagai Koordinator pembimbing
praktik kerja lapangan yang telah memberikan bimbingan dan pengarahan kepada penulis selama melaksanakan praktek lapangan kerja.
8. Bapak dan Ibu dosen staf pengajar Fakultas Farmasi Universitas Sumatera Utara atas semua ilmu, didikan dan bimbingan kepada penulis selama di perguruan tinggi ini.
9. Staf administrasi Fakultas Farmasi yang telah membantu kemudahan administrasi selama ini.
Penulis menyadari bahwa tugas akhir ini masih terdapat banyak kekurangan, baik dalam penulisan maupun penyajian tulisan ini masih jauh dari kesempurnaan. Oleh karena itu dengan segala kerendahan hati penulis menerima serta sangat mengharapkan saran dan kritik yang sifatnya membangun demi kesempurnaan tugas akhir ini. Akhir kata semoga Allah SWT melimpahkan rahmat dan karunia–Nya kepada kita semua dan harapan penulis semoga tugas akhir ini dapat memberikan manfaat bagi kita semua. Amin.
Medan, Nopember 2016 Penulis,
SURAT PERNYATAAN TIDAK PLAGIAT Saya yang bertandatangan di bawah ini,
Nama : Nurul Indah Astuti Nomor Induk Mahasiswa : 132410052
Program Studi : Analis Farmasi dan Makanan
Judul tugas akhir : Penetapan Kadar Zat Aktif Betametason Valerat pada Produk Ruahan Krim Betametason 0,1% menggunakan Metode Kromatografi Cair Kinerja Tinggi
Dengan ini menyatakan bahwa tugas akhir ini ditulis berdasarkan data dari hasil pekerjaan yang saya lakukan sendiri untuk memperoleh gelar Ahli Madya di perguruan tinggi negeri universitas sumatera utara, dan bukan plagiat karena kutipan yang ditulis telah disebutkan sumbernya di dalam daftar pustaka.
Demikian surat pernyataan ini saya perbuat dengan sebenarnya untuk dapat digunakan jika diperlukan sebagaimana mestinya.
Medan, Nopember 2016 Yang membuat pernyataan
PENETAPAN KADAR ZAT AKTIF BETAMETASON VALERAT PADA PRODUK RUAHAN KRIM BETAMETASON 0,1% MENGGUNAKAN
METODE KROMATOGRAFI CAIR KINERJA TINGGI ABSTRAK
Dalam produksi obat dilakukan pengawasan selama produksi (in process control). Pada pembuatan krim betametason 0,1% dilakukan pengawasan selama produksi dalam produk ruahan untuk menjamin mutu obat. Salah satunya dengan parameter penetapan kadar zat aktif dari krim betametason 0,1% tersebut. Tujuan dari penetapan kadar zat aktif pada produk ruahan krim betametason 0,1% adalah untuk mengetahui apakah kadar zat aktif obat telah memenuhi persyaratan yang tertera pada monografi Farmakope Indonesi Edisi V 2014.
Dalam penulisan tugas akhir ini, penetapan kadar betametason valerat pada produk ruahan krim betametason 0,1% dengan menggunakan metode kromatografi yaitu kromatografi cair kinerja tinggi. Dilakukan pada detector ultraviolet sinar tampak dengan panjang gelombang 254 nm, fase gerak yang digunakan adalah asetonitril–akuabides ( 3 : 2 ),fase diam yang digunakan adalah kolom bondapack C18 (3,9 × 300 mm) dan laju alir (flow rate) 1,50 mL/menit serta volume penyuntikan 20 µL.
Hasil yang diperoleh dari penetapan kadar betametason valerat pada produk ruahan krim betametason 0,1% menggunakan metode kromatografi cair kinerja tinggi yaitu 107,56% pada No. Batch M51367T, kadar tersebut memenuhi persyaratan Farmakope Indonesia Edisi V 2014 yaitu betametason valerat, C27H37FO6, tidak kurang dari 90,00% dan tidak lebih dari 110,00% dari jumlah yang tertera pada etiket.
2.3.1 Uji Kualitatif Betametason ... 7
2.3.2 Uji Kuantitatif Betametason ... 8
2.4 Kromatografi Cair Kinerja Tinggi ... 8
2.4.1 Keuntungan Kromatografi Cair Kinerja Tinggi .... 9
2.4.2 Kerugian Kromatografi Cair Kinerja Tinggi ... 9
2.4.3 Instrumentasi Kromatografi Cair Kinerja Tinggi .. 9
BAB III METODE PENGUJIAN ... 14
3.4.5 Pembuatan Larutan Sampel ... 15
DAFTAR GAMBAR
Gambar Halaman
DAFTAR TABEL
Tabel Halaman
1 Data hasil penetapan kadar betametason valerat pada produk
DAFTAR LAMPIRAN
Lampiran Halaman
1 Kromatogram standar betametason valerat ... 22
2 Kromatogram sampel uji betametason valerat ... 23
3 Perhitungan penetapan kadar betametason valerat ... 24